-
Medical journals
- Career
Léčba striktury uretry: dorzální lalok z bukální sliznice – zlatý standard
: A. Čermák; D. Pacík
: Urologická klinika FN Brno
: Urol List 2011; 9(1): 11-19
Pro rekonstrukci striktury bulbární uretry byla a je používána řada technik a metod. Použití kožních volných štěpů nebo přenesných kožních laloků penilní kůže byla dlouhou dobu s oblibou využívána jako nejvhodnější tkáň pro substituční uretroplastiku při řešení striktury uretry. Komplikace s přihojením, či spíše rejekcí štěpu, tvorba divertiklů, nebo naopak jizvení limitovalo jejich úspěšné využití. Určujícím faktorem pro úspěšný výsledek štěpu je jeho mechanická podpora. Historicky původně oblíbené ventrální umístění štěpu bylo hojně používáno pro snadný operační přístup příznivé vlastnosti lůžka štěpu, které zajišťovala spongiózní tkáň. Ve srovnání s povrchem corpora cavernosa, které nabízí velmi dobrou mechanickou podporu štěpu, je však lůžko tvořené spongiozní tkání ve ventrální pozici suboptimální. Využítí dorzálního umístění štěpu umožňuje dobré rozprostření štěpu na tunica albuginea corpora cavernosa po celé délce překlenutí striktury uretry. Fixace graftu zamezí svraštění a retrakci štěpu a přilnutí plochy zajistí dobrou revaskularizaci. V současné době jsou již i dlouhodobá data sledování velmi slibná ve srovnání s předchozími metodami.
Klíčová slova:
striktura uretry, bukální sliznice, graft, uretroplastika, rekonstrukce uretryÚvod
Striktura močové trubice představuje u mužů závažné onemocnění. V případě striktury je narušena normální schopnost správného a kompletního vyprázdnění močového měchýře. Dochází ke stáze moči nad překážkou, a tím se vytvářejí příhodné podmínky k rozvoji močové infekce. Závažnost problematiky spočívá v tom, že nemocných se zúžením močové trubice v posledním desetiletí přibývá. Neustálým rozšiřováním endoskopických metod v diagnostice a léčbě urologických onemocnění včetně mnohočetných manipulací v horních cestách močových se významně zvyšuje výskyt iatrogenních striktur. Záněty, traumata a rozvoj intenzivní medicíny, u které je nezbytné sledování nemocných včetně přesného monitorování diurézy pomocí zavedeného permanentního katétru, jsou příčinou vzniku striktury, která se může projevit až po několika letech. Etiologicky hraje u vzniku striktury hlavní roli parciální ztráta výstelky močové trubice. Vzniklé defekty mají tendenci se rychle hojit kontrakcí deepitelizovaných částí k sobě s následným překrytím sliznicí. Při mikci navíc dochází k rupturám vzniklé jizevnaté tkáně, dochází k průniku moči do subepiteliálních prostor, zánětlivé reakci a následné spongiofibróze. To vede ke zúžení lumen močové trubice. Infekce močových cest celý tento proces výrazně zhoršuje. Hlavními etiopatogenetickými faktory vedoucími ke tvorbě striktury jsou poranění a infekce močové trubice. Nejčastěji dochází k iatrogennímu poškození uretry mechanicky při nešetrném zavádění uretrálního katétru do nedostatečně lubrikované uretry, použitím nepřiměřeně velkého průměru katétru s následnou ischemickou nekrózou stěny, blokádou uretrálních žlázek s následným zánětem a zejména instrumentálními výkony v uropoetickém systému.
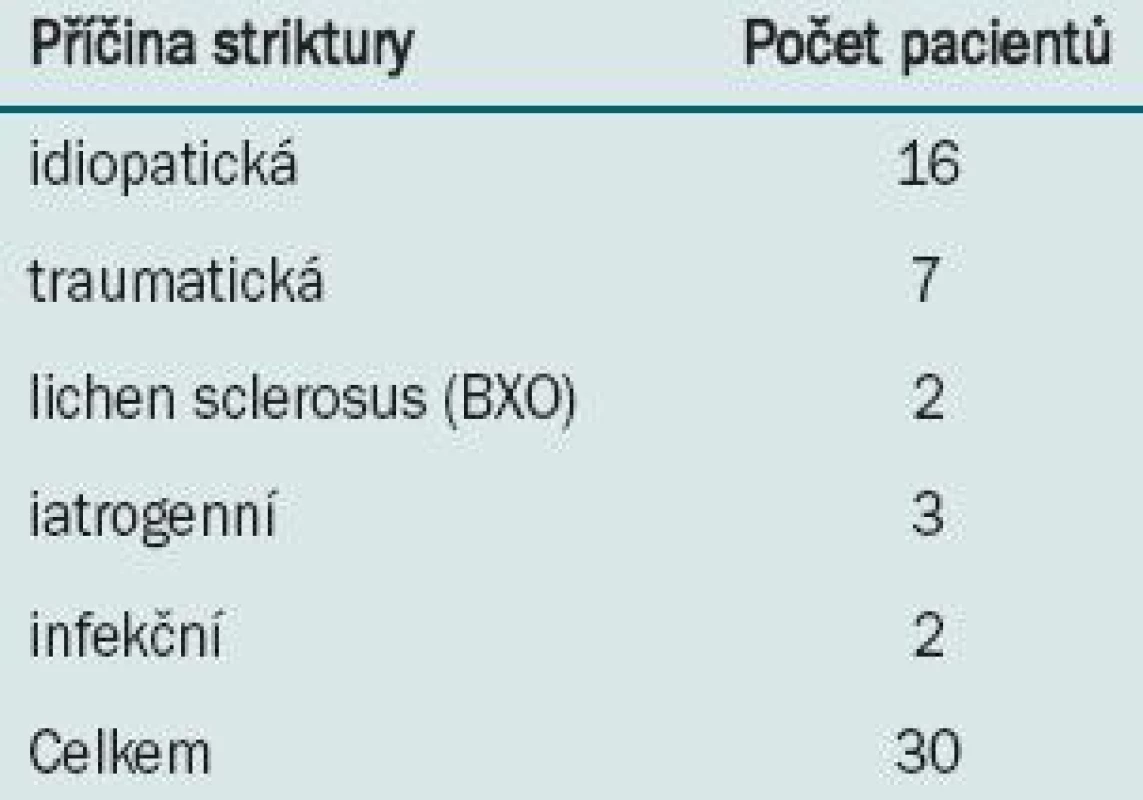
Příčina striktury uretry
Etilogicky lze rozdělit příčiny zúženiny močové trubice na:
- idiopatické
- vrozené
- traumatické
- pozánětlivé
- lichen sclerosus
Volba metody léčby striktury uretry závisí na lokalizaci, délce striktury, rozsahu poškození jizevnaté tkáně, spongiofibróze. Spongiofibróza se téměř vždy nachází na distálním i proximálním konci striktury. Důležitá je tedy její celková délka i tloušťka. Snaha o rekonstrukci striktury uretry musí vycházet nikoli z délky striktury, ale z délky spongiofibrózy, protože ta je nositelem strikturogenního potenciálu. Nejčastější příčinou restenózy, a tudíž selhání léčebného postupu, je v nedostatečném rozsahu excize postižené tkáně. Při volbě metody je důležité zhodnocení radiologického nálezu na uretrografii. Toto vyšetření samotné ale nestačí ke správnému zhodnocení a často vede k podhodnocení nálezu, protože radiologicky se jeví striktura krátká, ale ve skutečnosti může být rozsah spongiofibrózy delší. Excize nebo incize pouze radiologicky zúžené části trubice může vést k ponechání spongiofibrózy a časné restenóze. Pro určení rozsahu striktury je potřebné zhodnocení tzv. „grey“ šedé uretry (postižená část) a určení hranice „pink“ růžové uretry, která je normální, kde je sliznicí patrné normálně prokrvené spongiózní těleso.
Diagnostika
Pro určení rozsahu a naplánování adekvátní léčby je nutné pečlivé vyšetření močové trubice. K zobrazení lokalizace a délky striktury je standardním vyšetřením retrográdní uretrocystografie (UCG) a mikční cystouretrografie (MCUG).
Ultrasonografie uretry doplňuje uretrocystografii informací o stupni a rozsahu spongiofibrózy, která je důležitá pro volbu léčebného postupu. Dobře se zobrazují striktury penilní uretry, kde je až stoprocentní výtěžnost. Hůře lze hodnotit striktury bulbární uretry, kde je výtěžnost menší. Spongiofibróza uretry zahrnuje nálezy od prostého zesílení stěny až po hyper - echogenní jizvu. Striktury přední uretry se podle stupně zjištěné spongiofibrózy dělí do šesti skupin (Jordanova klasifikace z roku 1987). Objektivním průkazem ztížené mikce je uroflowmetrické vyšetření, které je velmi jednoduché a neinvazivní. Pro strikturu uretry je typický „obdélníkový“ tvar křivky s prodlouženou dobou močení a nízkým maximálním i průměrným průtokem. Experimentálně se zkouší měření rychlosti proudění kontrastní látky v oblasti striktury pomocí dopplerovské ultrasonografie. Tím lze hodnotit dynamickou závažnost zúženiny. Endoskopickým vyšetřením močové trubice se pátrá zejména po tzv. šedé („grey“) sliznici, která ukazuje na přítomnost spongiofibrózy. Při endoskopii lze lokalizovat zevně a určit délku striktury palpací konce ureteroskopu a prosvícením stěny.
Rekonstrukce uretry je i v současné době moderní urologie záležitost velmi jemná, delikátní, vyžadující často dlouhodobé zkušenosti a osvojení a zvládnutí řady technik, které je třeba někdy volit až podle aktuálního operačního nálezu. Stanovení rozsahu spongiofibrózy předoperačně může být nesnadné, protože je palpačně hmatná až při velkém rozsahu. Méně rozsáhlá, avšak chirurgicky významná spongiofibróza je patrná až po incizi uretry. Fibróza má vyhlazený šedý epitel, spongiozní těleso je na řezu fibrotické až sklerotické a nekrvácí. Délku spongiofibrózy lze určit až po prodloužení incize do růžové, měkké uretry a hojně krvácivého spongiouního tělesa.
Vnitřní optická uretrotomie (OUTi) je metoda jednoduchá a účinná u krátkých měkkých cirkulárních striktur. Optická uretrotomie byla zavedena do urologické praxe Sachsem v roce 1974. Podstatou je protětí striktury uretry až do zdravé tkáně. Tím se odstraní kontraktura jizvy. Poté probíhá hojení epitelizací incize z okrajů rány. Metoda je zatížena vysokou četností recidiv [1]. Pansadoro a Emiliozzi zjistili, že vnitřní optická uretrotomie byla dlouhodobě úspěšná jenom u striktur < 15 mm. V žádném případě se nezdařilo recidivu striktury úspěšně vyřešit druhou optickou uretrotomií, naopak často po ní došlo k prodloužení striktury. Celková úspěšnost léčby metodou OUTi se udává kolem 30 % [17]. Naději na trvalý úspěch mají jen krátké a blanité striktury nezánětlivého původu. V současné době se indikuje optická uretrotomie pouze u krátkých irisových striktur bez prokázané spongiofibrózy.
Rekonstrukce uretry s excizí spongiofibrózy a anastomózou end-to-end může dosahovat úspěšnosti až v 95 % případů. Metodu však lze použít u krátkých striktur tak, aby byla výsledná anastomóza zcela bez napětí. Hodí se tedy k řešení striktury délky max. 15–20 mm. Kromě samotného překlenutí defektu je třeba ještě počítat s 20 mm podélné incize spatřovaných okrajů uretry. Celkový posun je tedy 40 mm a i při dostatečné mobilizaci proximálního i distálního okraje je to maximální délka, aby anastomóza zůstala bez napětí a snížilo se riziko ischemie [2].
K náhradě postižené části uretry se již delší dobu využívá přenesených kožních laloků z oblasti genitálií, nebo štěpů získaných z genitální či extragenitální oblasti. Kožní laloky s sebou nesou komplikace v podobě nutnosti rozsáhlé excize na penisu či šourku, potřebě velké mobilizace laloku k přenosu hluboko do perinea. Laloky vykazují vyšší četnost jizvení z důvodu torze vyživující stopky. Při použití skrotálního laloku vyrůstá z ponechaných folikulů ochlupení, na kterém může vznikat litiáza [3,4]. Extragenitální kožní laloky také vykazují vysokou tendenci k jizvení [5]. Webster et al porovnávali výsledky štěpů získaných z kůže penisu a z extragenitálních oblastí (vnitřní strana paže) a zjistili, že extragenitální štěpy vykazují velmi vysokou četnost komplikací a neúspěchu. První, kdo popsal použití sliznice močového měchýře pro substituční uretroplastiku, byl Mammelar [6]. Výsledky nebyly příliš povzbudivé jednak pro komplikace při odběru tkáně, velkou tloušťku a nepravidelný povrch uretry v místě štěpu, hojnou sekreci a tendenci k tvorbě divertiklů.
Využití štěpu z bukální sliznice získalo v poslední době velkou popularitu. Bukální sliznici lze použít pro rekonstrukci při řešení jak striktury uretry, tak i komplexu hypospadie. Použití bukální sliznice není však úplně nové. Humby popsal použití bukální sliznice již v roce 1941 [7], ale největšího rozmachu dosáhla až po roce 1990. V roce 1998 referoval Barbagli sestavu 37 pacientů, u kterých byla použita předkožka, ale v 6 případech z důvodu nedostatku tkáně byla striktura bulbární uretry řešena jednodobou plastikou s dorzálním, netubularizovaným „onlay“ štěpem z bukální sliznice [8].
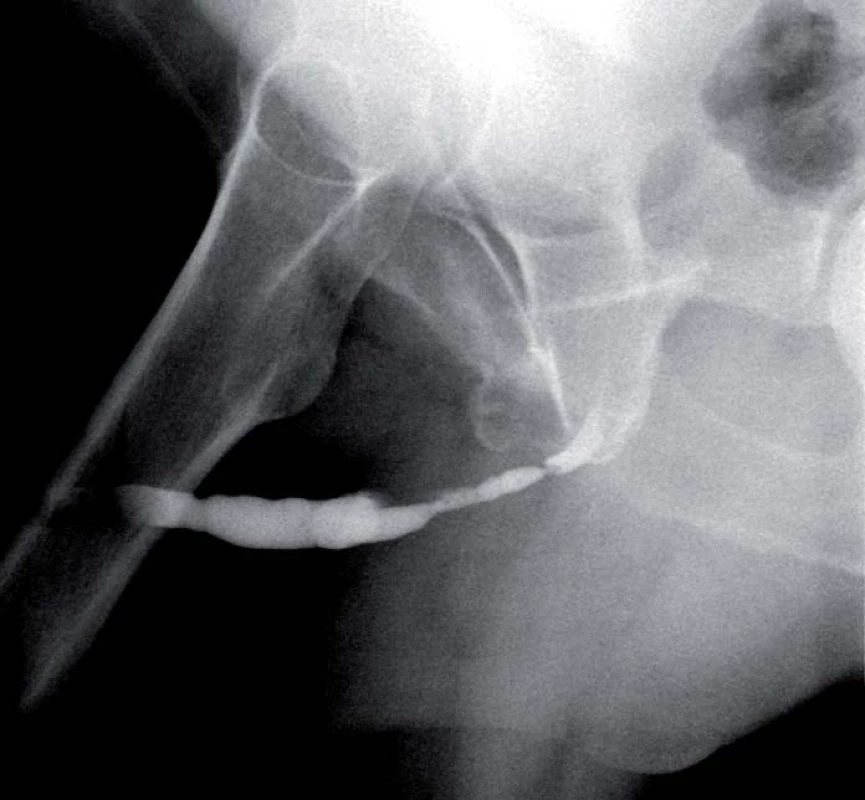
1. Striktura uretry – ureterografie. 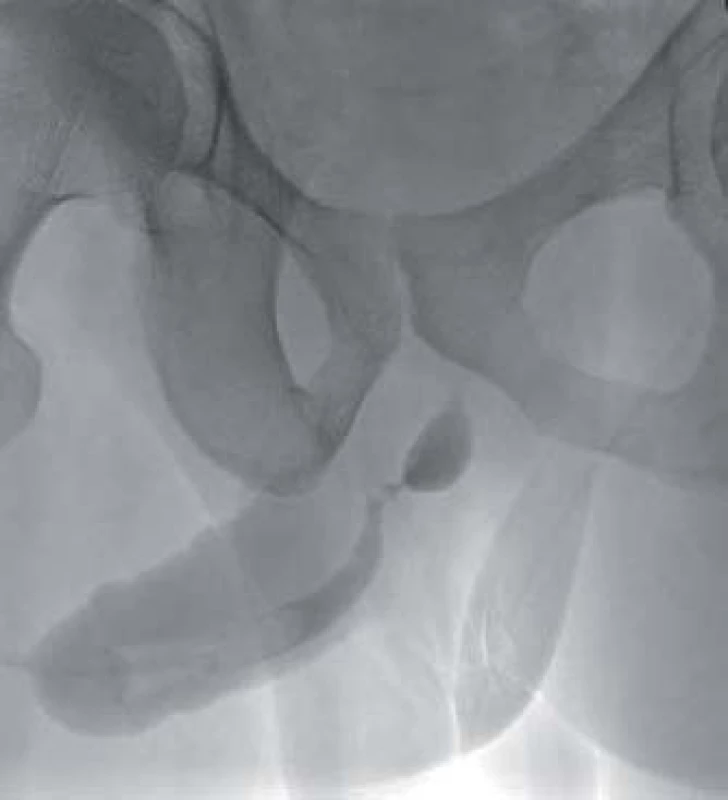
2. Striktura uretry – peroperační nález. 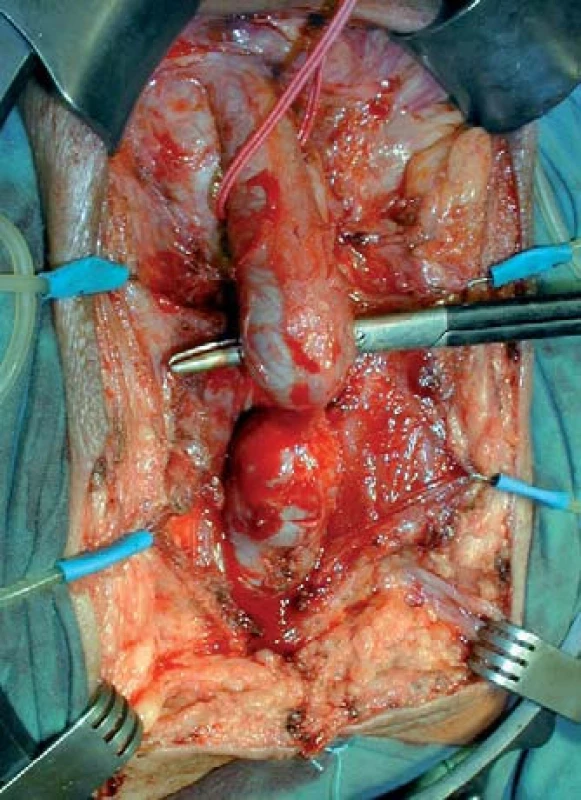
V současné době máme k dispozici následující materiál pro uretroplastiku:
- genitální nebo extragenitální kůže
- sliznici močového měchýře
- orální sliznici/štěp z bukální sliznice, rtu, jazyka
- střevní sliznice
- jiný materiál – matrix
- tkáňové inženýrství
Technika použití bukálního štěpu
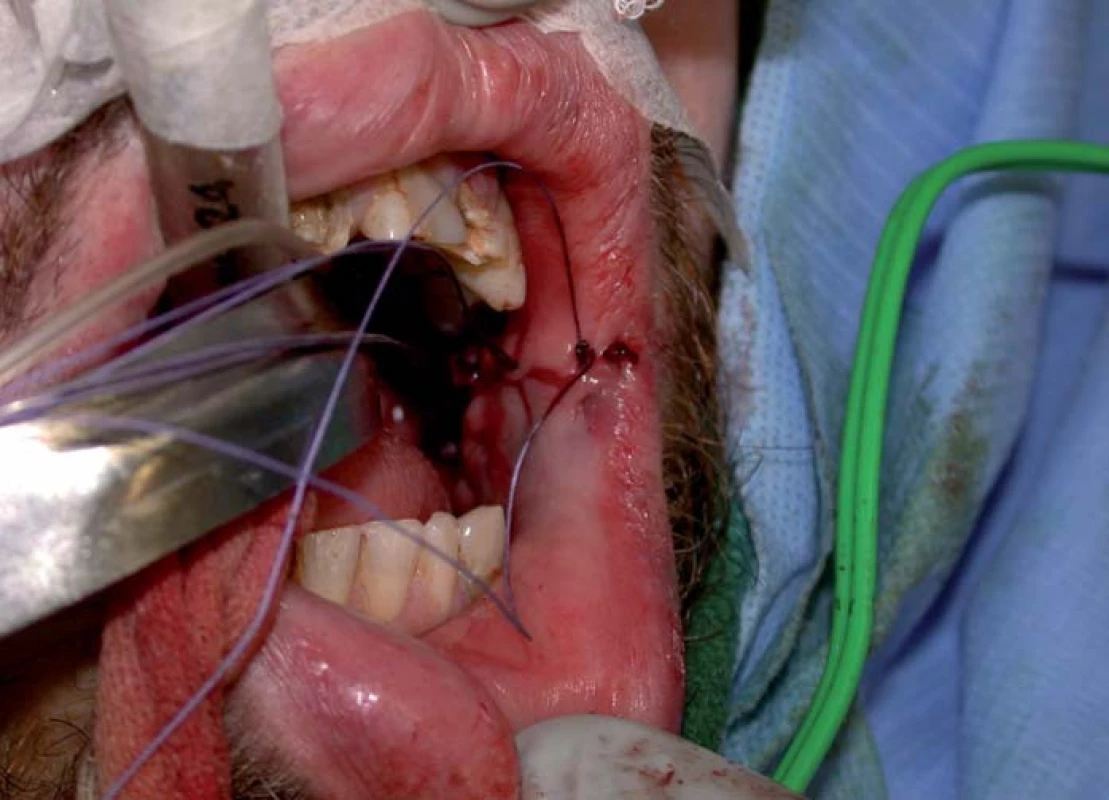
Operační výkon se provádí v celkové anestezii s nasotracheální intubací. Pacient je polohován do vysoké litotomické polohy. Operaci provádí dva operační týmy s vlastním instrumentáriem. Jedna skupina provádí samotnou plastickou operaci na uretře, druhá skupina (v našem případě využíváme služeb plastického chirurga) odebírá potřebný stěp z bukální nebo lingvální sliznice. Tkáň je odebírána nejčastěji z vnitřní strany tváře pod Stensenovým vývodem, který nesmí být poraněn. Touto technikou lze obvykle získat až 6 cm dlouhý štěp. Pokud je třeba získat delší úsek, je možné řez prodloužit pod dolní ret směrem ke střední linii. Tímto způsobem lze získat až 10–12 cm tkáně. Je možné provést i odběr z druhé strany tváře a štěpy spojit. Před odběrem je vhodné injikovat podkožně Lidocain 2 % s adrenalinem 1 : 100 000 pro lepší hemostázu. Podkožní injekce roztoku vypne tkáň, a usnadní tak odběr štěpu. Barvivem označený štěp je vyříznut a vyjmut. Rána je zkontrolována a provedena pečlivá hemostáza. Ránu šijeme obvykle jednotlivými Vicryl Rapid 3-0 stehy. Pokud je odběr elipsoidního tvaru, okraje lze dobře přiblížit a ránu sešíváme jednotlivými stehy tak, aby tkáň byla bez napětí (obr. 3,4). Pokud je odběr obdélníkového tvaru, je vhodnější ponechat místo odběru bez sutury k volnému hojení granulací a epitelizací. Po odběru upravujeme graft do potřebného tvaru (obr. 5). Před vložením štěpu provedeme jeho pečlivé očištění od zbytků podkožního tuku.
4. Steh lůžka po odběru štěpu z bukání sliznice. 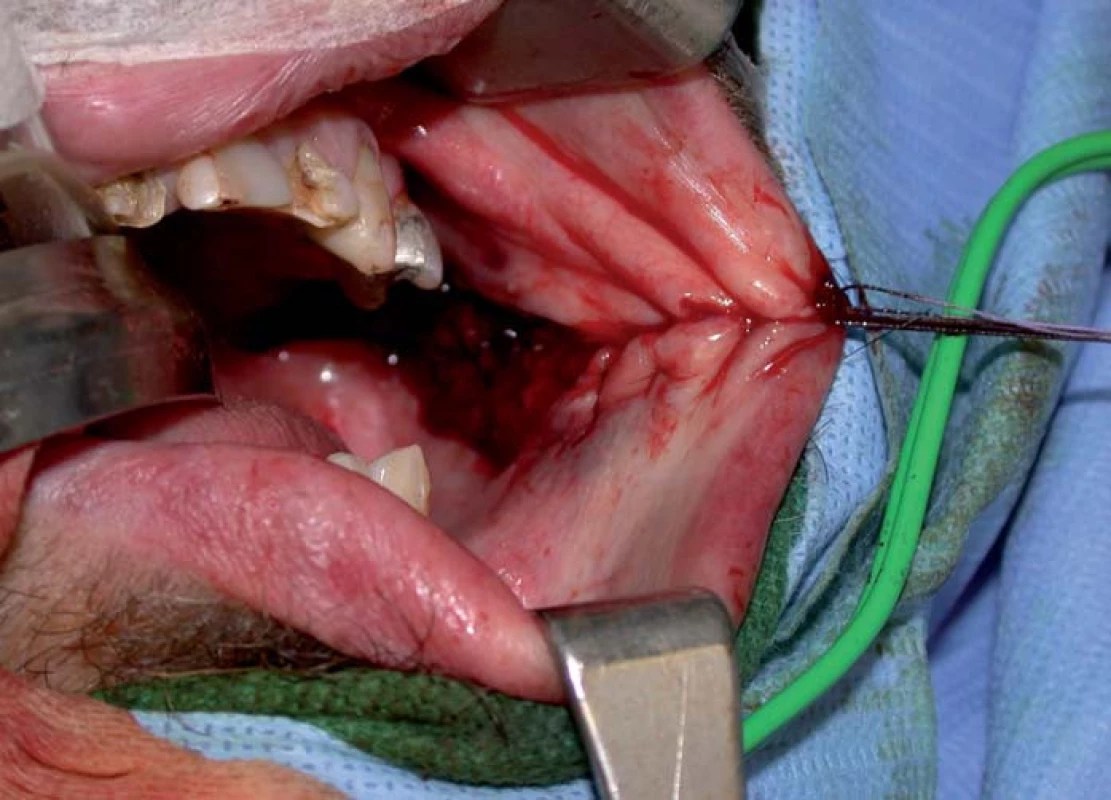
5. Upravené štěpy bukání sliznice. 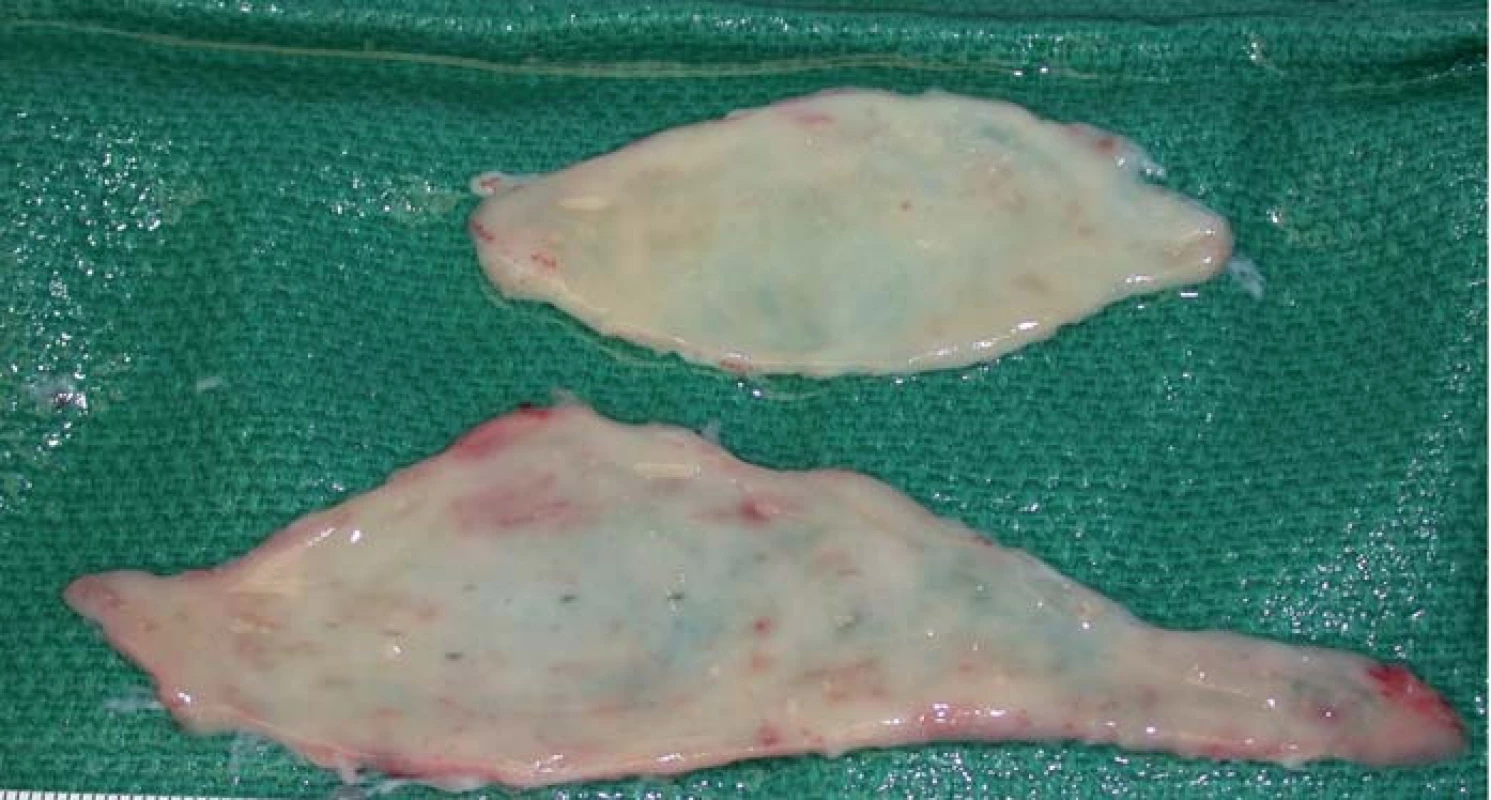
Výhody použití orální sliznice:
- relativně snadné získání, v případě potřeby lze získat dva štěpy
- relativně pevná, ale pružná
- obvykle je k dispozici dostatek tkáně
- dává dobré šance na přihojení
- tkáň je dobře vaskularizovaná, epitelová část je dostatečně silná a podkožní je relativně tenká
- malá četnost komplikací v místě odběru
- pro tkáň je přirozené vlhké prostředí
- odolnost vůči kožním nemocem
- odolnost vůči infekcím, má výborné imunologické vlastnosti
- místo odběru zůstává skryté
Odběr tkáně však musí být proveden zkušeným chirurgem v orofaciální oblasti, aby nedošlo ke komplikacím. Možné komplikace při odběru bukální sliznice:
- parestezie (nejčastější komplikace)
- peroperační krvácení
- pooperační infekce
- bolest a otok
- poranění vývodu slinné žlázy
- obtížný odběr při omezené hybnosti čelisti
- ztráta, nebo porucha citlivosti tváře nebo dolního rtu při poškození nervu
Velikost štěpu musí být velká podle fyziognomie ústní dutiny pacienta, aby nedošlo k potížím při otevírání úst. Standardní potřebná velikost graftu je 4 cm délky a 2,5 cm šířky. Tato velikost bývá bezproblémová při odběru i pooperačně při otevírání úst. Pokud je potřeba větší štěp, preferujeme odběr dalšího štěpu z druhé strany před rozsáhlým odběrem právě z důvodu vyhnutí se popsaným komplikacím.
Odběr tkáně ze rtu
Odběr tkáně ze rtu je rychlá a snadná metoda. Podél zevní hrany dolního rtu jsou naloženy 3 situační stehy, aby bukální slizince zůstala natažená. Stejným způsobem jako u bukální sliznice se používá injekce 1–2% Lidokainu s adrenalinem 1 : 100 000. Graft je odejmut v potřebné délce. Je provedena pečlivá hemostáza. Místo odběru se ponechává k sekundárnímu hojení bez sutury. Ihned po odběru se na ránu přikládá led k zamezení vzniku otoku a hematomu. Metoda je velmi jednoduchá a rychlá, ale někteří pacienti si stěžují na kosmetický výsledek. Po zhojení může být hranice rtu vtažená nebo naopak evertovaná. Z těchto estetických důvodů není vhodné odebírat štěp větší než 4 cm délky a 1,5 cm šířky.
Výhody odběru štěpu ze rtu:
- odběr je možné provést u všech pacientů
- odběr je rychlý a snadný, nevyžaduje nosní intubaci a speciální ústní retraktor
- štěp je ideální pro všechny typy uretroplastik vyžadujících menší a tenký typ graftu
Graft je vhodný v dětské urologii (hypospadie) pro „one-stage“ dorzální penilní a bulbární uretroplastiky.
Odběr tkáně z jazyka
Odběr z jazyka by měl provádět ústní chirurg. Je použit standardní ústní rozvěrač, špička jazyka je vytažena na stehu z dutiny ústní. Není potřeba instilace Lidokainu ani adrenalinu. Po identifikaci Whartonova vývodu je pečlivě zkontrolován průběh lingválního nervu. Okraje štěpu jsou naříznuty skalpelem a celý štěp je získán uvolněním nůžkami od spodiny. Lůžko je pečlivě zkontrolováno a stavěno krvácení. Rána je zašita jednotlivými 4-0 stehy. Štěp je upraven odstraněním spodní fibrovaskulární tkáně. Obvyklá velikost získaného štěpu je 4 cm délky a 2,5 cm šířky. V případě potřeby je možné odebrat tkáň z druhé strany jazyka. Na závěr výkonu je vhodné pokapat dorzální povrch jazyka několika kapkami citronového džusu ke stimulaci slinných žláz. Pooperačně má být pacient kontrolován ústním chirurgem nejméně dvakrát denně.
Výhody odběru štěpu z jazyka:
- odběr je možné provést u všech pacientů
- možnost získání dvou štěpů
- jizva po odběru je skrytá
- odběr je rychlý a snadný
- štěp je vhodný pro jakoukoli uretroplastiku, kde je použit menší a tenký štěp. Je dobrou alternativou odběru tkáně ze rtu.
Pooperační péče
Po odběru tkáně z oblasti dutiny ústní je potřeba kontrola chirurgem alespoň dvakrát denně. První den může pacient přijímat tekutiny a zmrzlinu, následně tekutou stravu a třetí den může přijímat běžnou dietu.
3. Zlepšení Q-max a IPSS symptom skóre po operaci. 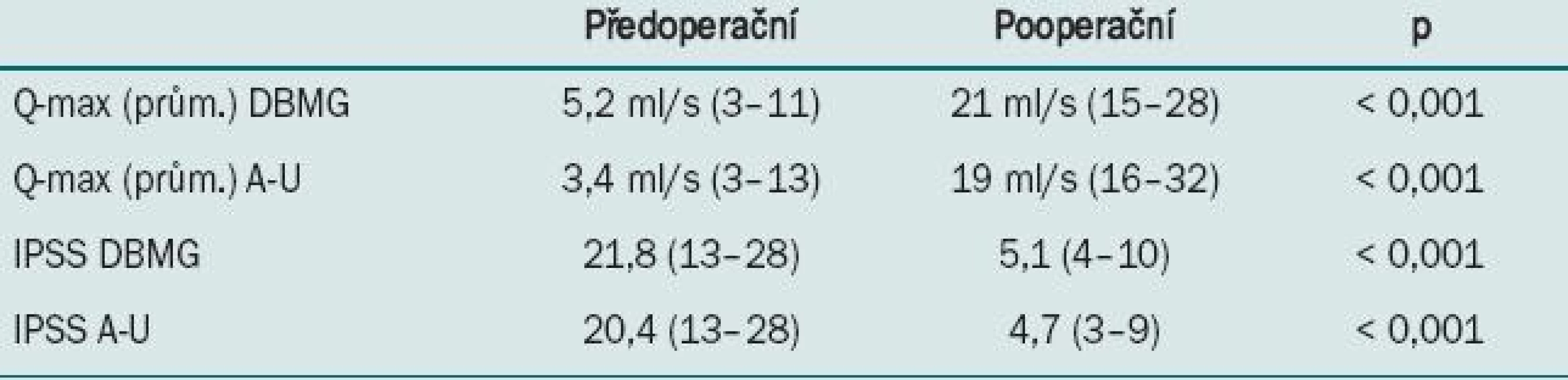
DBMG: dorsal buccal mucosa graft, A-U: resekční ureteroplastika – (anastomotic urethroplasty) 4. Tab. 4. Restenóza podle typu uretroplastiky. 
DBMG: dorsal buccal mucosa graft, A-U: resekční ureteroplastika – (anastomotic urethroplasty) Příprava uretry
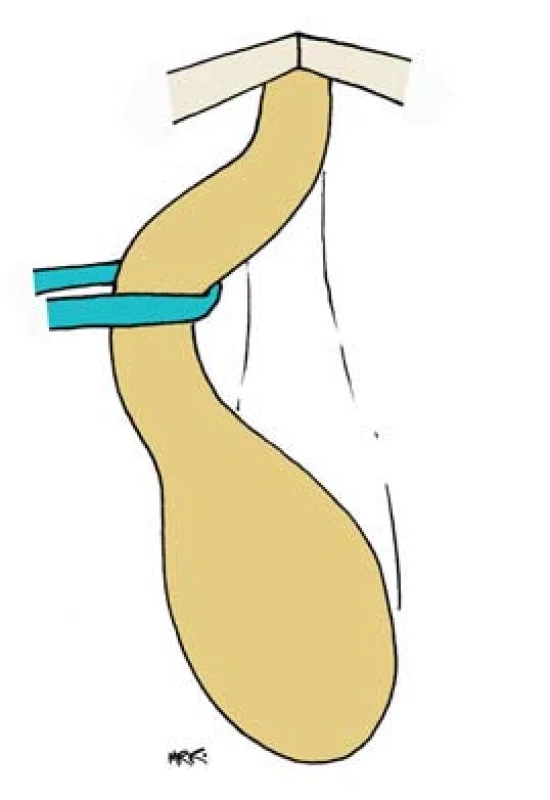
Obvykle začínáme operovat nejprve uretru, abychom zhodnotili rozsah defektu a mohli určit potřebný rozsah odebíraného štěpu. Přístup k bulbární uretře volíme standardně ze sagitálního řezu v perineální oblasti. Provedeme rozdělení musculus bulbocavernosus. Poškození bulbospongiózních svalů a perineálních nervů může vést k nedostatečným uretrálním kontrakcím s výslednou poruchou evakuace semene a zbytkové moči z uretry. Tyto poruchy mohou vyústit v oslabení proudu ejakulace, ve ztrátu ejakulace, neschopnost ejakuace semene, infertilitu, zadržení zbytkové moči v uretře či postevakuační odkapávání moči. Všechny tyto komplikace se mohou podílet na vzniku dočasné nebo trvalé sexuální dysfunkce. V některých případech proto provádíme techniku „muscle and nerve sparing“ bulbární uretroplastiku s šetřením perineálního nervu a ozřejměním dorzálního obvodu uretry bez protětí svalů. Tuto metodu však nelze dobře využít v případě proximální striktury zasahující až k membranózní uretře. Tam vede šetření svalu k omezení manipulačního prostoru, který je nutný pro dostatečnou expozici dorzální strany uretry a bezpečné založení anastomózy mezi incidovanou uretrou a štěpem. Uretra je kompletně mobilizována (obr. 6), otočena o 180°, a tak je ozřejměna její dorzální strana (obr. 7). Ta je podélně incidovaná v místě striktury a řez je prodloužen proximálním i distálním směrem 1 cm do zdravé tkáně a normálního lumen. Proximální i distální uretra je kalibrována.
7. Otočení mobilizované uretry o 180° a podélná incize. 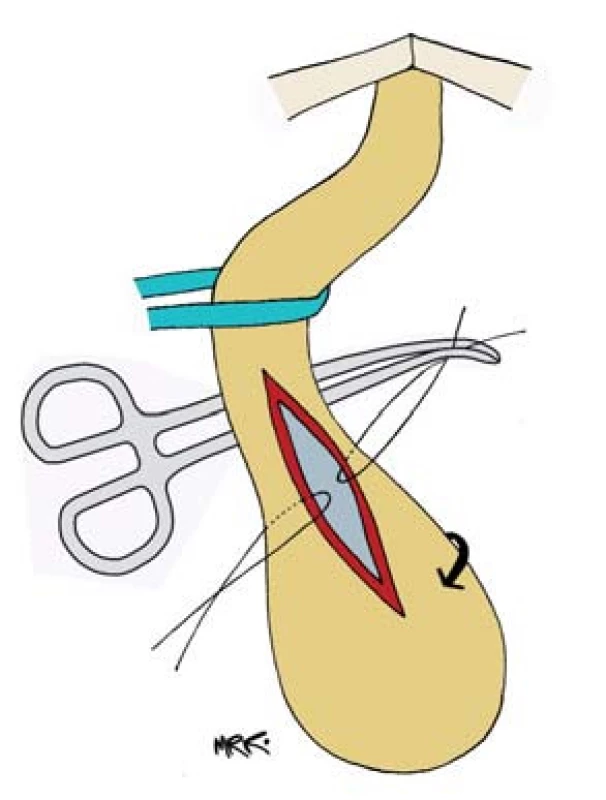
Připravený graft pečlivě rozprostřeme a fixujeme na corpora cavernosa situačními stehy Vicryl 5-0 (obr. 8). Štěp fixujeme i v centrální části, abychom zamezili vzniku „mrtvého“ prostoru. S výhodou lze použít tkáňového lepidla. Podle současných zkušeností je použití tkáňového lepidla preferováno z důvodu lepší adheze po celé ploše vloženého štěpu a možnosti vyhnout se použití množství fixačních stehů. Poté provedeme anastomózu okraje sliznice uretry se štěpem pokračujícím stehem 5-0 (obr. 9). Zavedeme silikonový katétr F 18 a rotujeme uretru zpět do původní polohy. Dokončíme suturu druhé stěny incize uretry ke graftu (obr. 10).
8. Vložení štěpu a jeho fixace na corpora cavernosa. 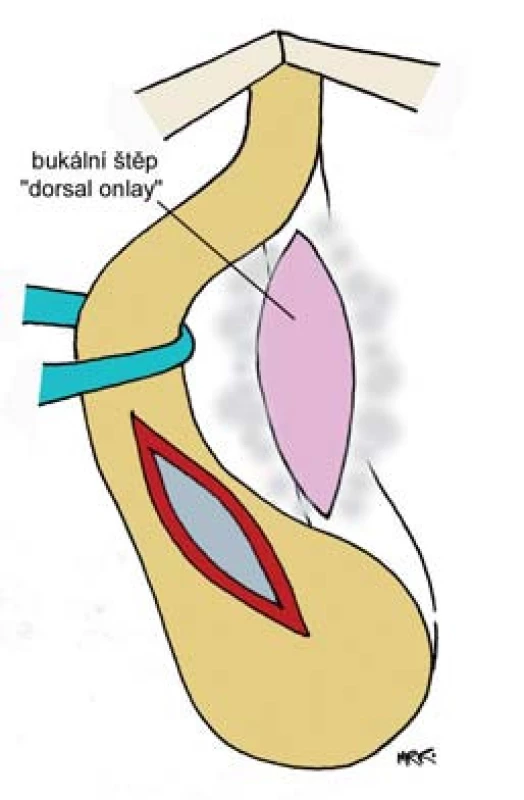
9. Proximální a distální apex, otevřené uretry jsou našity na hroty štěpu. 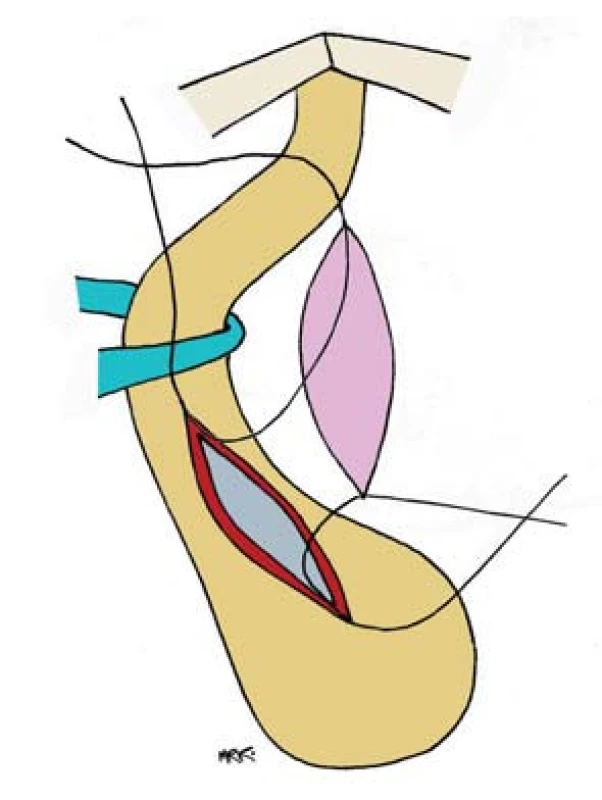
10. Uretra je rotována do původní pozice. 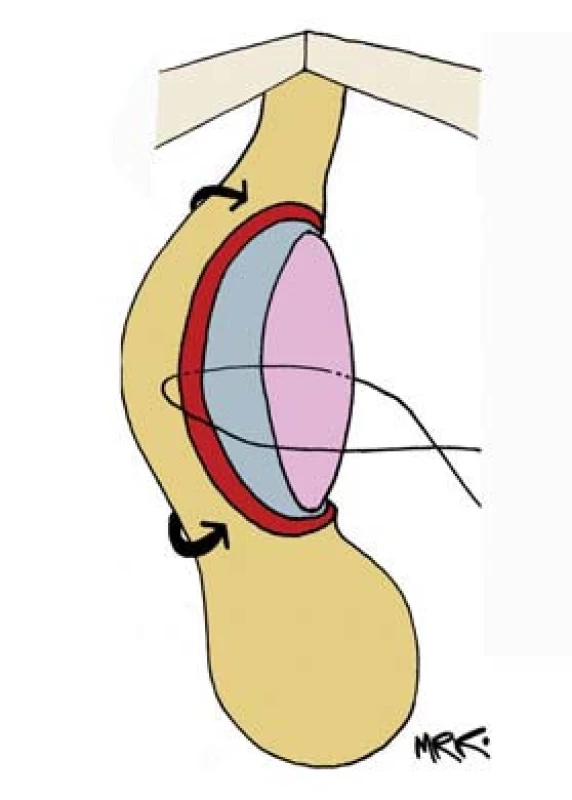
Za 3 týdny po operaci provádíme RTG kontrastní vyšetření uretrografií. Za 3 měsíce po operaci provádíme uroflowmetrii. Po uretroplastice rutinně zavádíme epicystostomii. Stále se vedou diskuze o nutnosti epicystostomie a názor není jednotný. Zastánci epicystostomie vyzdvihují větší bezpečnost při hojení operační plastiky. Vychází z předpokladu, že při epicystostomii se dokonaleji vyprazdňuje močový měchýř a nedochází k průniku moči kolem katétru do operované oblasti. Odpůrci epicystostomie poukazují na možný výskyt krvácivých komplikací po zavedení epicystostomie a nutnost operační revize s evakuací hematomu.
Výsledky našeho souboru
V roce 2001–2011 bylo ošetřeno 87 pacientů se strikturou uretry, u kterých bylo provedeno 213 endoskopických uretrotomií OUTi (průměr 2,44 na pacienta). Výkon bylo nutno opakovat u 55 pacientů (63,2 %). U nich bylo provedeno 181 reoperací, nejméně jedna a maximálně pět. Tři a více výkonů bylo provedeno u 16 (20 %) z celkového počtu pacientů.
Neúspěchy s OUTi vedly ke změně strategie v péči o nemocné se strikturou uretry. Pouze u pacientů se strikturou v bulbární části, která má irisový charakter, indikujeme optickou uretrotomii jako metodu volby s vědomím rizika recidivy. Pro provádění OUTi indikujeme jednoduché, bulbární, „měkké“ striktury kratší než 2 cm, dříve neléčené, dále jako metodu léčby striktury vzniklé jako komplikace léčeného karcinomu prostaty a u mužů s komorbiditami, které vylučují provedení uretroplastiky. U pacientů s již provedenou uretrotomií a irisovou strikturou indikujeme otevřenou rekonstrukci a endoskopickou uretrotomii v případě časné recidivy neopakujeme. Tubulární striktury primárně indikujeme k otevřené uretroplastice.
12. Dorzální „onlay“ bukání štěp. 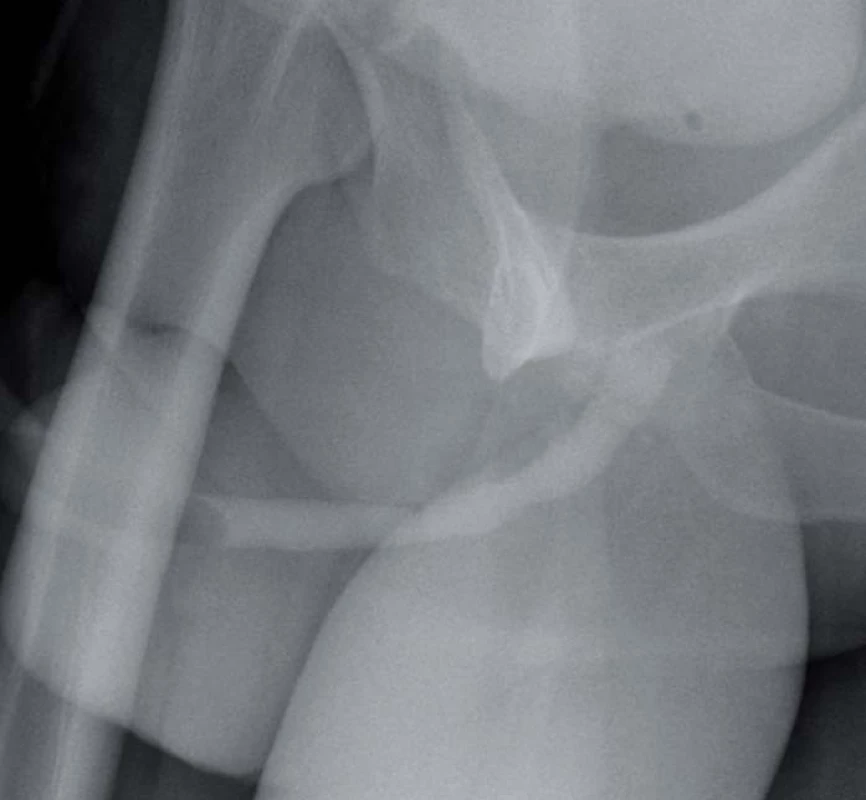
13. Distrakční ruptura uretry. 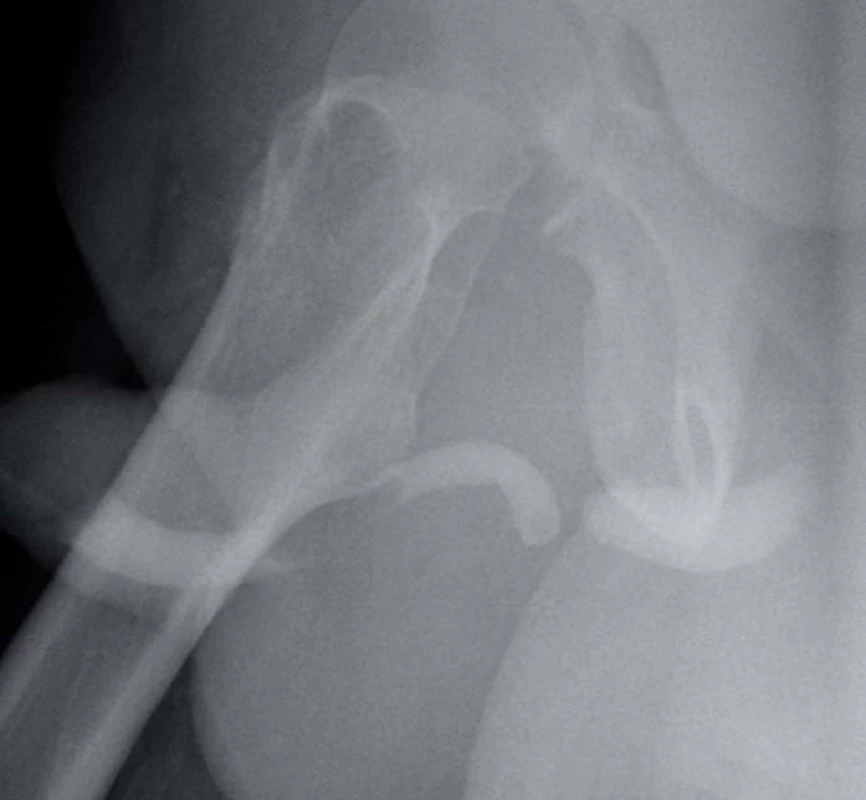
14. Resekční anastomóza end-to-end. 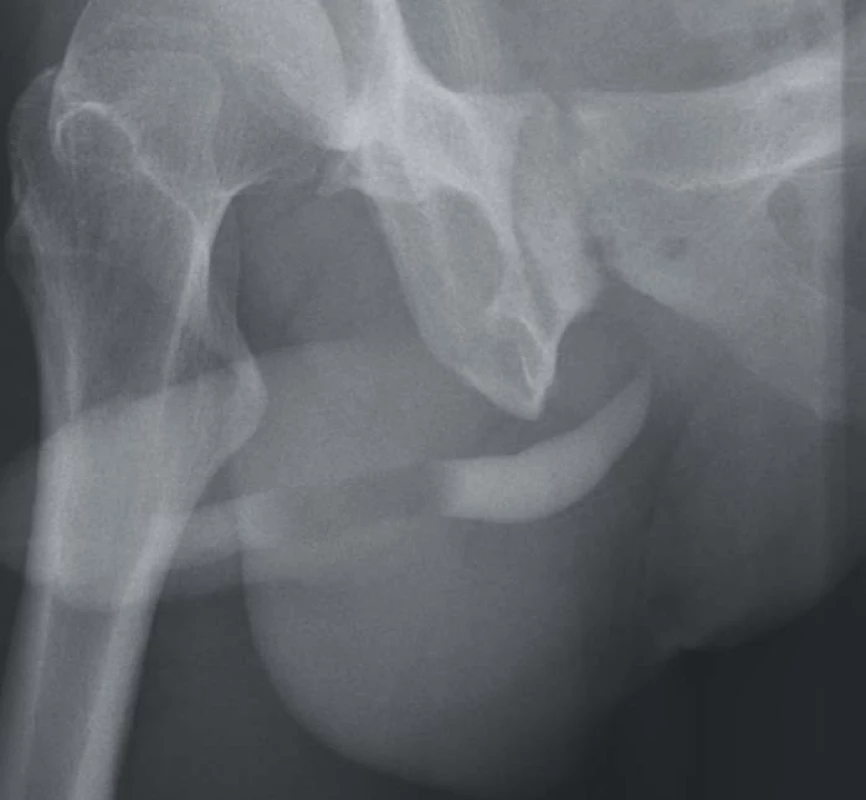
V roce 2008–2010 bylo ošetřeno 18 pacientů (27–62 let, průměrný věk 32 let) metodou dorzální bukání štěp a 12 pacientů resekční plastikou. Průměrná doba sledování byla 26 měsíců (4–39 měsíců).
Žádný z pacientů nevyžadoval krevní převod. U dvou pacientů (dorzální bukání štěp) byl při kontrolní uretrografii (3 týdny po operaci) zjištěn únik malého množství kontrastní látky v místě anastomózy. V jednom případě v proximální části, v druhém případě distálně. V obou případech došlo k úspěšnému zhojení po dvoutýdenním zavedení katétru.
U dvou (11,1 %) uretroplastik dorzálním bukáním štěpem a v jednom případě resekční anastomózy (8,3 %) došlo k restenóze po 31, resp. 34 měsících, resp. 12 měsících. U dvou pacientů se vyvinula infekce v ráně, která byla úspěšně léčena změnou antibiotika. V jednom případě po resekční plastice došlo k infekci a rozestupu rány na perineu a stav si vyžádal resuturu.
U žádného pacienta nevznikl divertikl nebo píštěl. Mikční průtok Q-max se zlepšil z 5,2 ml/s (DBMG), resp. 3,4ml/s (A-U) na 21 ml/s (DBMG) 19 ml/s (A-U). IPSS symptomové skóre se snížilo signifikantně u DMBG i A-U.
Komplikace v místě odběru tkáně (DBMG):
- 90 % pacientů nemělo bolesti
- 75 % mělo lehký nebo střední otok, který vymizel do 5 dnů
- 0 % podkožní hematom či krvácení
- 94 % mělo sníženou citlivost nejméně týden po operaci; porucha cítivosti přetrvávala 3 měsíce po operaci u 6 % pacientů
- 0 % ED – erektilní dysfunkce
- 6 % (jeden pacient) měl poruchu ejakulace
- 11,1 % mělo ukapávání moči po vymočení, zvláště při sedání do auta a vstávání
Naše čísla jsou na malých souborech a sledování zatím není dlouhodobé. Proto je statistické hodnocení obtížné a lze předpokládat, že výsledky se budou ještě měnit. Obvyklá četnost je udávána na velkých souborech [16].
Diskuze
Jednodobá nebo vícedobá plastika
Výsledky dlouhodobých sledování ukazují, že většina jednodobých plastik dosahuje vyšší účinnosti. Štěpem z bukální sliznice je dosahováno lepších výsledků u léčby defektů přední uretry spojených s hypospadií/epispadií (84 %, 75 %) stejně tak jako u léčby bulbární striktury (96 %) [9]. Při použití bukálního štěpu bylo dosaženo nejlepších výsledků ve srovnání s ostatními volnými štěpy i přenesenými živenými laloky. Vícedobá plastika je doporučována pro komplexní striktury vyžadující přenos většího množství tkáně nebo u přidružených lokálních komplikací, jako jsou extenzivní jizvení, píštěle či infekce [10].
Umístění štěpu
Krátkodobé sledování výsledků hodnotilo úspěšnost dorzálních graftů 96 % a 85 % ventrálních. Při dlouhodobém sledování neshledává podstatných rozdílů mezi použitím dorzálního a ventrálního graftu [11,12]. Barbagli popsal tři varianty umístění bukálního štěpu: dorzální, ventrální a laterální [14]. Barbagli et al jsou průkopníky metody dorzálního bukálního štěpu. Původní reference byly 100% úspěšnost této metody a 90% úspěšnost dorzálního laloku kůže předkožky [8]. Nicméně další dlouhodobá sledování poukázala na nižší úspěšnost 84 % u dorzálního bukálního štěpu [13] a 73 % při použití kůže předkožky [14].
Excize stenózy vs jednoduchá augmentace striktury
Delvecchio et al v roce 2004 poukazovali na vhodnost provedení excize stenotické části uretry a doporučovali tento postup provádět vždy [15]. Předpokládali, že pouhé vložení „onlay“ laloku je nevhodné z důvodu přenosu již primárně méněcenné tkáně štěpu, který je vystaven působení moči. Následné studie neprokázaly signifikantní rozdíl mezi úspěšností plastiky s agumentací štěpu a mezi resekční plastikou s náhradou štěpem. Uretroplastiky s resekcí by měly být prováděny pouze u traumatických striktur.
Lokální komplikace
Lokální komplikace se obecně vyskytují do tří let po operaci. Místní komplikace, jako jsou tvorba píštěle, tvorba divertiklu, stenóza meatu uretry a kontraktura štěpu se obvykle projeví do jednoho roku po operaci, ale mohou se vyskytnout i v pozdějším období. Odkapávání po vymočení se obvykle vyskytuje 2–3 roky po operaci.
Současná doporučení léčby striktury uretry
Vnitřní uretrotomie (OUTi) je metoda s velmi vysokou pravděpodobností neúspěchu. Při hodnocení otázky, zda se stále mají provádět OUTi, nebo již neprovádět, je odpověď „ano“ i „ne“.
Pro provádění OUTi jsou vhodné jednoduché bulbární striktury kratší než 2 cm, dříve neléčené, jestliže očekáváme úspěšnost > 40 % a pokud recidivu lze očekávat nejdříve po 6 měsících po první proceduře. Metoda by měla být používaná u striktury vzniklé jako komplikace léčeného karcinomu prostaty a u mužů s komorbiditami, které vylučují provedení uretroplastiky nebo s krátkou předpokládanou dobou života. Dále je OUTi možné indikovat u mužů, kteří primárně odmítají provedení uretroplastiky. Je nutné pacienta na horší výsledky a vysokou pravděpodobnost recidivy upozornit. OUTi by neměla být prováděna u delších striktur (> 2 cm) s extenzivní spongiofibrózou, u časné recidivy (méně než 3 měsíce) po OUTi nebo dilataci uretry. Není vhodná jako metoda léčby u stenózy membranózní uretry po pánevní fraktuře.
Substituční uretroplastika je zatížena výskytem komplikací a selhání. Kde to lze, má být použita resekční plastika s anastomózou „end to end“.
V případě, že nelze provést anastomózu, má být provedena substituční uretroplastika. Metoda „onlay“ graft je účinnější než přenesené laloky. Jako nejúčinnější se dnes jeví uretroplastika s použitím přenosu bukálního štěpu.
Bulbární uretroplastika by měla být prováděna se šetřením m. bulbospongiosus a perineálních nervů. Protětí bulbární uretry je doporučeno pouze u traumatických striktur. U netraumatických striktur je metoda první volby s použitím „onlay“ graftu. Umístění štěpu by mělo být dorzální u celé přední uretry, pouze u proximální části bulbární uretry je vhodné provést ventrální umístění laloku. Pro fixaci štěpu je výhodné použití tkáňového fibrinového lepidla. Orální sliznice vykazuje nejlepší biologické vlastnosti ze současných známých substitučních materiálů.
Pro správné hodnocení výsledků je nutné provádět pooperační sledování s RTG kontrastním vyšetřením uetrografie a sledování uroflowmetických parametrů průtoku moči. Výsledky je nutné hodnotit porovnáním předoperačních a pooperačních dotazníků.
Závěr
Je důležité si uvědomovat, že operační plastiky uretry přinášejí i přes propracované techniky poměrně značné procento selhání a že náhrada jakýmkoli materiálem je v průběhu času stále ohrožena vznikem komplikací. Žádná ze současných metod nenabízí 100% úspěšnost léčby, proto je potřeba další zkoumání a hledání účinnějších metod léčby striktury uretry.
prim. MUDr. Aleš Čermák
Urologická klinika FN Brno
Jihlavská 20
acermak@fnbrno.cz
Sources
1. Heyns CF, Steenkamp JW, De Kock ML et al. Treatment of male urethral strictures: is repeated dilation or internal urethrotomy useful? J Urol 1998; 160(2): 356–358.
2. Fiala R, Záťura F, Reif R. Striktura a trauma mužské uretry. Praha: StudiaGeo 1999, edice UROLOG: 74–77.
3. Morey AF, McAninch JW. When and how to use buccal mucosal grafts in adult bulbar urethroplasty. Urology 1996; 48(2): 194–198.
4. Greenwell TJ, Venn SN, Mundy AR. Changing practice in anterior urethroplasty. BJU Int. 1999; 83(6): 631–635.
5. Webster GD, Brown MW, Koefoot RB Jr. et al. Suboptimal results in full thickness skin graft urethroplasty using an extrapenile skin donor site. J Urol 1984; 131(6): 1082–1083.
6. Memmelar J. Use of bladder mucosa in a one-stage repair of hypospadias. J Urol 1947; 58(1): 68–73.
7. Humby GA. A one-stage operation for hypospadias. Br J Surg 1941; 29 : 84–92.
8. Barbagli G, Palminteri E, Rizzo M. Dorsal onlay graft urethroplasty using penile skin or buccal mucosa in adult bulbourethral strictures. J Urol 1998; 160(4): 1307–1309.
9. Wessells H and McAninch JW. Current controversies in anterior urethral stricture repair: free-graft versus pedicled skin-flap reconstruction. World J Urol 1998; 16(3): 175–180.
10. Palminteri E, Lazzeri M, Guazzoni G, Turini D and Barbagli G: New 2-stage buccal mucosal graft urethroplasty. J Urol 2002; 167(1): 130–132.
11. Pansadoro V, Emiliozzi P, Gaffi M et al. Buccal mucosa urethroplasty in the treatment of bulbar urethral strictures. Urology 2003; 61(5): 1008–1010.
12. Pansadoro V, Emiliozzi P, Gaffi M et al.
Buccal mucosa urethroplasty for the treatment of
bulbar urethral strictures. J Urol 1999; 161(5): 1501–1503.
13. Barbagli G, Palminteri E, Guazzoni G et al. Bulbar urethroplasty using buccal mucosa grafts placed on the ventral, dorsal or lateral surface of the urethra: are results affected by the surgical technique? J Urol 2005; 174(3): 955–997.
14. Barbagli G, Palminteri E, Lazzeri M et al. Interim outcomes of dorsal skin graft bulbar urethroplasty.
J Urol 2004; 172 (4 Pt 1): 1365–1367.
15. Delvecchio FC, Anger JT, Webster GD. A proposal that whenever possible stricture excision be a part of all bulbar urethroplasties: A progressive approach to patient selection. J Urol 2004; 171 : 17.
16. Andrich DE, Dunglison N, Greenwell TJ et al. The long-term results of urethroplasty, J Urol. 2003; 170(1): 90–92.
17. Hyršl l, Kawaciuk I. Současný pohled na dg. a léčbu striktur močové trubice, Zdravotnické noviny, Lékařské listy 22/2000.
Labels
Paediatric urologist Urology
Article was published inUrological Journal

2011 Issue 1-
All articles in this issue
- Technique of harvesting oral mucosa for urethral reconstruction. Evaluation of postoperative complications and patient satisfaction
- Management of urethral stricture: dorsal flap from buccal mucosa – the gold standard
- Urinary tract and genital trauma
- Neuro-urological assessment and treatment
- Stress urinary incontinence in women: diagnostics and treatment based on AUA guidelines review
- Percutaneous nephrolithotomy (PNL): a review of current procedural techniques and developments
- Hormone therapy in the management of prostate cancer: treating the cancer without hurting the patient
- Cancer treatment induced bone loss (CTIBL): burning issue in prostate cancer patients – our experience
- EAU Guidelines on Urethral Trauma
- Urological Journal
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Management of urethral stricture: dorsal flap from buccal mucosa – the gold standard
- Hormone therapy in the management of prostate cancer: treating the cancer without hurting the patient
- Urinary tract and genital trauma
- Technique of harvesting oral mucosa for urethral reconstruction. Evaluation of postoperative complications and patient satisfaction
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career