-
Medical journals
- Career
Technické aspekty provedení transperitoneální laparoskopické nefrektomie
Authors: M. Hora 1; V. Eret 1; P. Stránský 1; T. Ürge 1; J. Klečka 1; O. Hes 2; J. Ferda 3; Z. Chudáček 4
Authors‘ workplace: LF UK a FN Plzeň ; Urologická klinika 1; Šiklův patologicko-anatomický ústav 2; Radiodiagnostická klinika 3; Radiodiagnostické oddělení 4
Published in: Urol List 2010; 8(1): 33-38
Overview
Laparoskopická transperitonální nefrektomie (TLNE) je dnes nejrozšířenějším způsobem odstranění ledviny jak pro benigní, tak zejména pro maligní onemocnění u parenchymových nádorů ledvin, zde je již standardem pro nádory kategorie T1-2 nevhodných k záchovným výkonům. V článku je probrán standardní postup TLNE jednoho pracoviště se zkušeností s téměř 400 výkony.
Klíčová slova:
nefrektomie, laparoskopie, nádor ledvinyUrologové se v posledních dvou desetiletích poměrně úspěšně snaží o snížení invazivity nefrektomie a jiných operací ledvin. Metod provedení mininvazivní nefrektomie je celá řada. Od trochu exotické nefrektomie z minilaparotomie [1] k poměrně standardizované a rutinně užívané laparoskopické nefrektomii až k dnešnímu dni zaváděné nefrektomii jedním portem (LESS – laparoscopic endoscopic single-site surgery) [2] či nefrektomie bez řezu (NOTES – natural orifice translumenal endoscopic surgery), kdy jsou využívány přirozené vstupy do dutiny břišní, v urologii zatím používaný přístup transvaginální [3–4]. V článku se budeme věnovat každodenní rutinní praxi – transperitoneální laparoskopické nefrektomii (TLNE). Jedná se o nejrozšířenější metodiku jak na většině pracovišť ve světě, tak na naší klinice. Od ledna 2003 do října 2009 jsme provedli 379 laparoskopických nefrektomií, z toho u 304 případů z onkologické indikace, u zbytku u benigních afekcí. Z toho jen 18 (4,7 %) přístupem retroperitoneoskopickým. Rukou asistovanou nefrektomii neprovádíme. U nádorů ledviny je laparoskopická nefrektomie považována již za standard u nádorů kategorie T1-2, nejsou-li samozřejmě vhodné k záchovnému výkonu [5]. Cílem článku je probrat metodiku TLNE krok za krokem s upozorněním na možné varianty provedení, možné komplikace a jejich řešení jak z pohledu literárních údajů, tak zejména dle poznatků z naší klinické praxe. Metodiku včetně našich výsledků jsme opakovaně publikovali [6–8]. TLNE je již na našem pracovišti standardizovaná, s minimem komplikací i konverzí, operační časy se v rukách zkušených laparoskopických chirurgů pohybují u naprosté většiny případů mezi 60–90 min. Mladší urologové začínající s laparoskopií mají většinu operačních časů mezi 100–120 min. Stejný transperitoneální laparoskopický pří stup používáme i u nefroureterektomií, resekcí ledvin, adrenalektomií, pyeloplastik.
NÁŠ STANDARDNÍ POSTUP TLNE
Pacient je po úvodu do anestezie zacévkován a přetočen na bok resp. do lumbotomické polohy. Pacient je však jen lehce rozevřen, pouze v případě konverze jej rozevíráme více. Zejména u začínajících operatérů a u nálezů s vyšším rizikem konverze doporučujeme si v klidu před zahájením operace sterilním fixem označit polohu žeber a linii eventuálního řezu pro konverzi. Veressovu jehlu zavádíme do mesogastria lehce laterálně od přechodu m. rectus abdominis v m. obliquus abdominis externus. Otevřenou Hassonovu techniku (krátkou incizí se za kontroly zraku bezpečně zavede port) jsme nikdy nepoužili. Po vytvoření kapnoperitonea tlakem 12 mm Hg zavádíme první port 10 mm pararektálně v úrovni pupku či lehce kraniálně. Pupkem zavádíme videoport zcela výjimečně, spíše z kosmetických důvodů u štíhlých mladších žen. Při zavedení videoportu do pupku bývá kamera od ledviny zbytečně dále a často je pohled na ledvinu zhoršen (je patrná za tlustým střevem jako „za horami“). Za kontroly zraku zavádíme do podžebří port 5 mm, v případě, že chceme zavádět tímto portem Ligasure® Atlas® či Hem-o-lok klipy velikosti L, je nutno zde zavést port 10 mm. Do podbřišku je zaveden port 12 mm, jím je možno zavést stapler. Pod konec 12. žebra je zaveden port 5 mm pro asistenci. Na pravé straně zavádíme ještě 5mm port 2 cm pod mečík (obr. 1). Jím zavedený grasper 5 mm je podvlečen pod játry, játra se jím nadzvednou a grasper se přichytí na bránici a játra jsou celou dobu operace bezpečně elevována (obr. 2).
Image 1. Břicho u obézního muže, třetí pooperační den po pravostranné radikální nefrektomii. Je zde ukázáno typické rozmístění portů. Čísla značí velikost portů. 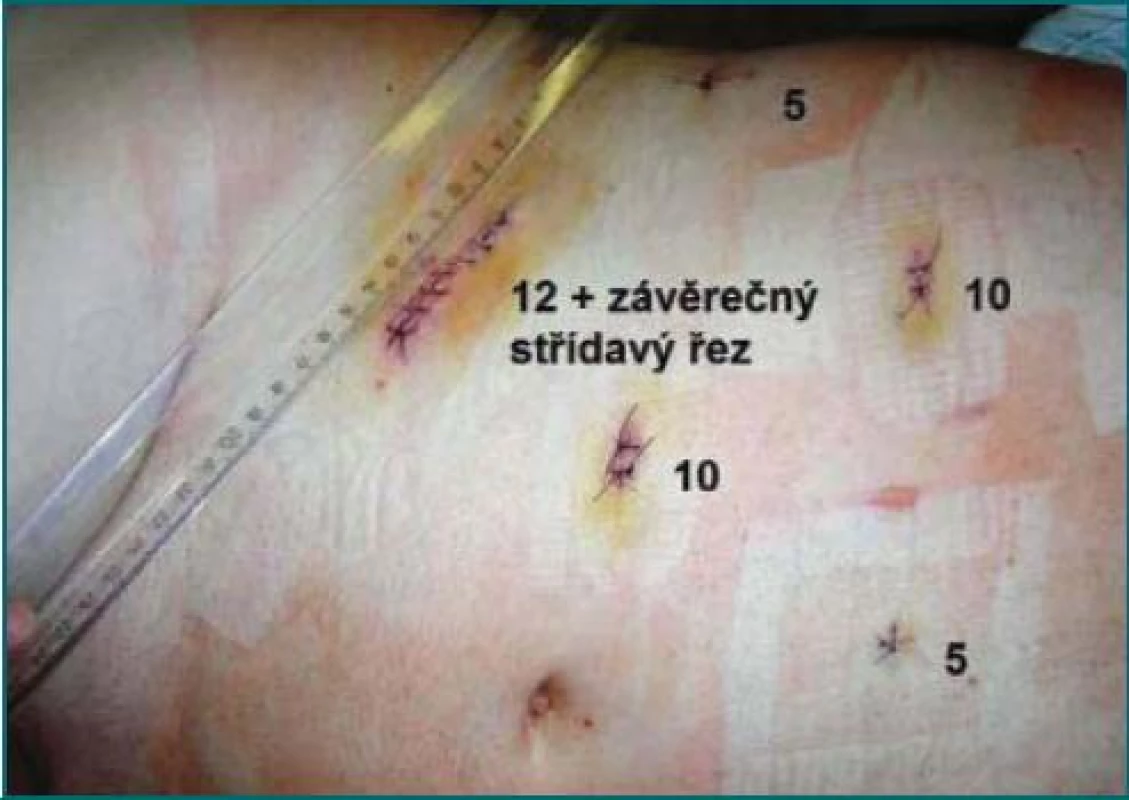
Image 2. Pomocí grasperu zavedeného portem pod mečíkem jsou elevována játra, grasper je uchycen k bránici. 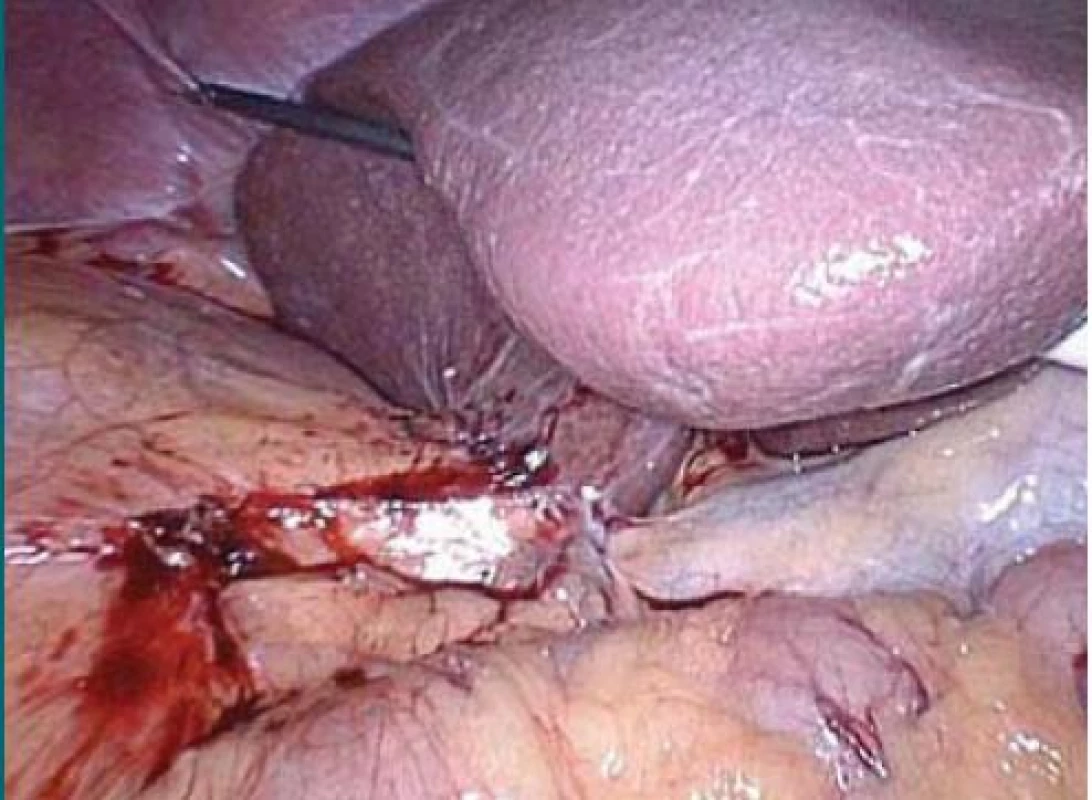
Často je nutno rozrušit drobnější srůsty pod játry. Dále pokračuje operace na obou stranách podobně. Operatér drží v jedné ruce bipolární grasper (jím elevuje tkáň a v případě potřeby se jím i bezpečně koaguluje) (obr. 3). Pomocí nůžek (v druhé ruce) či lépe harmonického skalpelu či Ligasure (nástroj Atlas® či Advance®) se laterokolicky otevře zadní peritoneum a podélně Gerotova fascie. Grasperem a nejlépe uzavřeným nástrojem Atlas® se natupo vypreparuje dolní pól ledviny s ponechaným tukovým pouzdrem. Je nalezen ureter a pomocí Atlas® přerušen. Tuková tkáň mezi ledvinou a velkými cévami se preparuje opět tupě. V případě potřeby se tkáň může přerušit s Atlas®. Vlevo jdeme většinou laterálně od gonadálních cév, tzn. že renální žílu později přerušujeme periferně od odstupu gonadální a nadledvinové žíly. Pouze u rozsáhlejších tumorů, indikujeme-li adrenalektomii či lymfadenektomii, či u anatomicky nepříznivých poměrů resekujeme i gonadální žílu. Tu přerušujeme většinou pomocí Ligasure®. Užíváme-li klipy, poté dostatečně daleko od renální žíly, ne jak je kresleno v některých operačních atlasech těsně u renální žíly. Tyto klipy by nám totiž v případě potřeby znemožnily aplikaci stapleru. Když poté preparujeme blíže hilovým cévám, postupujeme již opatrněji. Na tupou preparaci s výhodou užíváme i savku, která má oblý konec. Přímo kolem cév preparujeme tkáň pomocí háčku s koagulačním proudem. Háčkem se tkáň nabere a za postupného mírného tahu a popojížděním háčku po tkáni se tkáň bezpečně přeruší. Tímto vypreparujeme ventrálně uloženou renální žílu.
Image 3. Bipolární grasper užívaný k uchopení tkáně a v případě potřeby hned zároveň ke koagulaci. Operatérem držen většinou v nedominantní ruce. 
Poté se snažíme nalézt dorzálně uloženou renální arterii. O přesném počtu a jejich topografické anatomii hilových cév nám dává excelentní informaci dvoufázová CT angiografie [9–11]. Tu lze provést dnes na většině modernějších CT přístrojů a doporučujeme dvoufázovou CT angiografii žádat od radiologů jako rutinní součást vyšetření ledviny postižené nádorem či u ledvin indikovaných k LNE (obr. 4 a, b).
Image 4. a, b. Dvoufázová CT angiografie ukazující cévní zásobení levé ledviny. 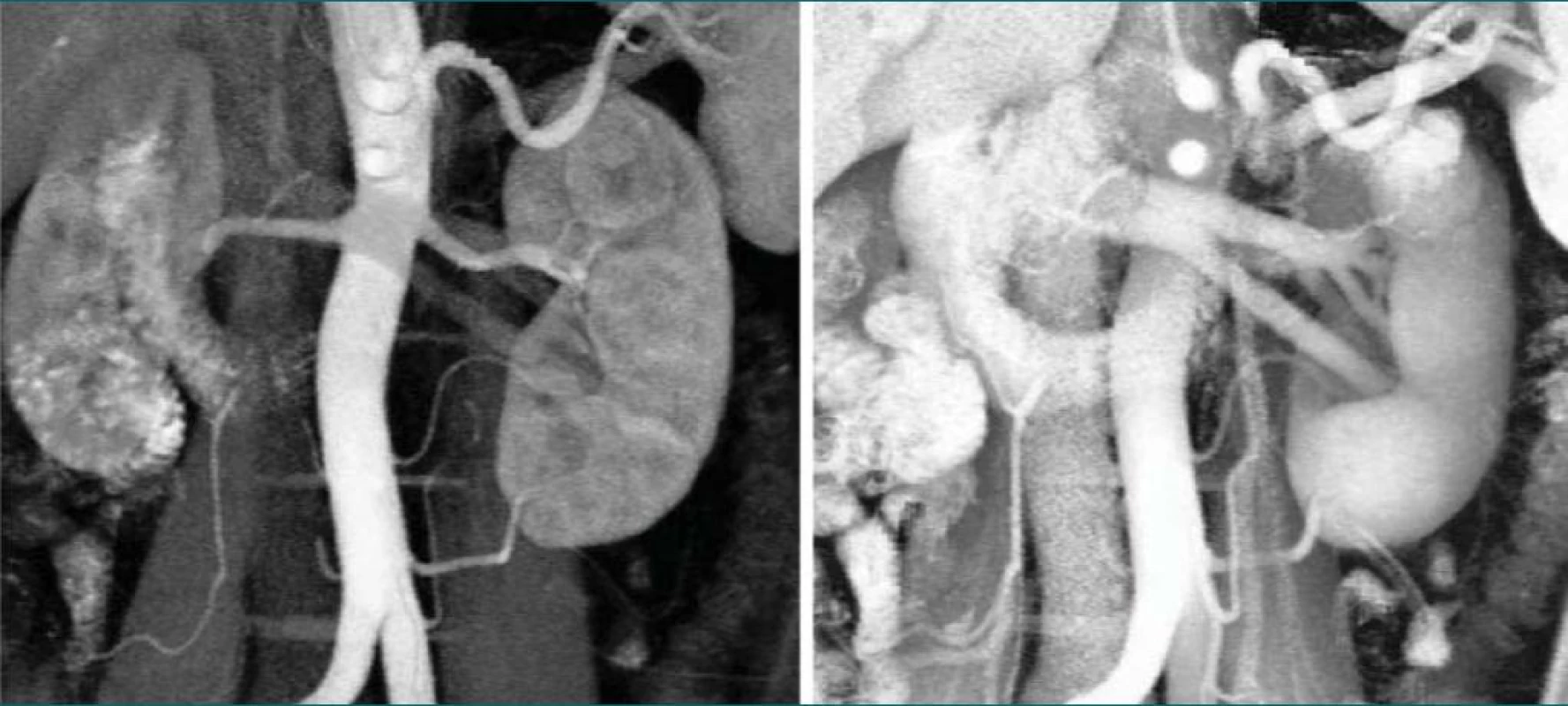
Dvoufázová CT angiografie může být samozřejmě i součástí komplexnějšího vyšetření PET/CT [12]. Nalezneme-li arterii, snažíme se ji uchopit nejlépe s Babcockovým grasperem (obr. 5).
Image 5. Babcock sloužící k atraumatickému uchopení cév. 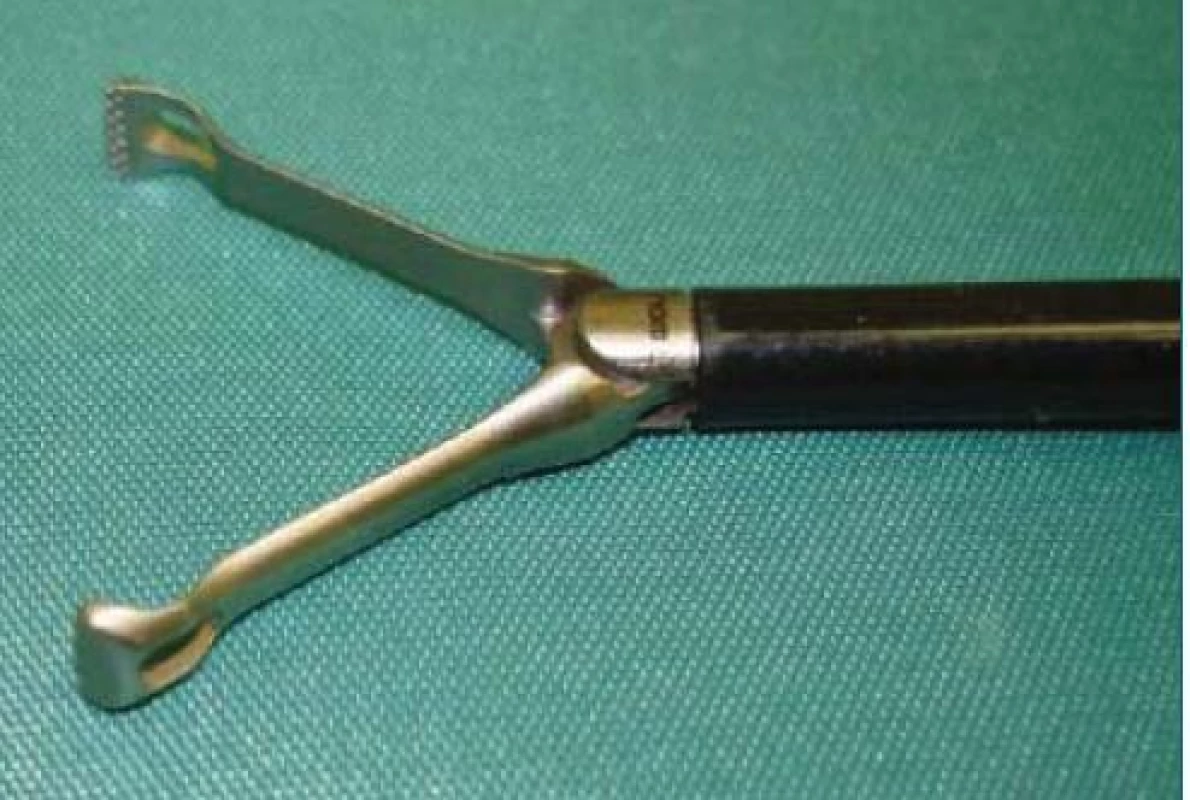
Tento nástroj umožňuje bezpečně zachytit cévu, aniž by ji traumatizoval. V pozdější fází dokáže mj. i zúžit žílu při nasazování klipů. Arterii přerušujeme pomocí Hem-o-lok® klipů (Weck) velikosti většinou L [13–15] (obr. 6). Dva klipy centrálně, jeden periferně k zabránění zpětného toku krve event. krvácení z provázejících drobných cév. Centrálně uložené klipy je nutno dát kus od sebe, aby nemohlo dojít k jejich sklouznutí, zejména u mladších jedinců se zachovalou elasticitou stěny a vysokou schopností kontrakce.
Image 6. Aplikátor s uzamykatelným umělohmotným nevstřebatelným klipem Hem-o-lok® Weck velikosti L. 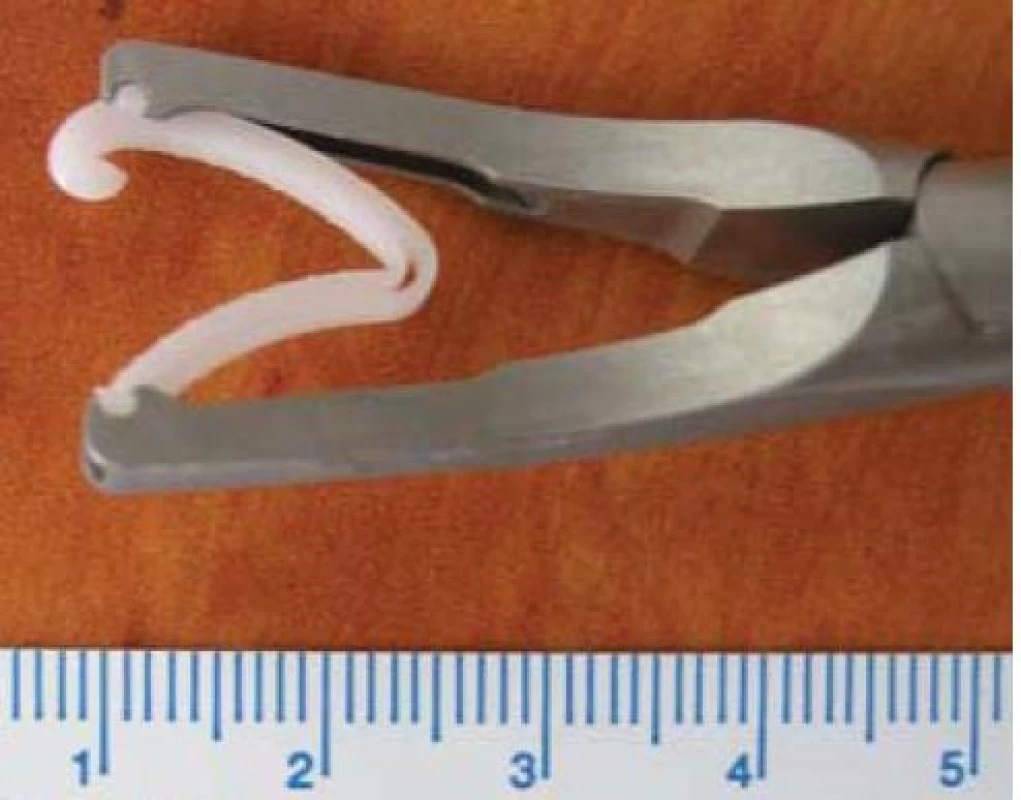
Arterii samozřejmě lze přerušit i staplerem. Sami to užíváme výjimečně, většinou když odstraňujeme i lipolymfatickou tkáň kolem aorty a renální arterii přerušujeme těsně u aorty. Následně uvolňujeme od okolí renální žílu, nejlépe pomocí velkého 10mm disektoru (obr. 7).
Image 7. Disektor 10 mm sloužící k obejití hilových cév před nasazením stapleru. 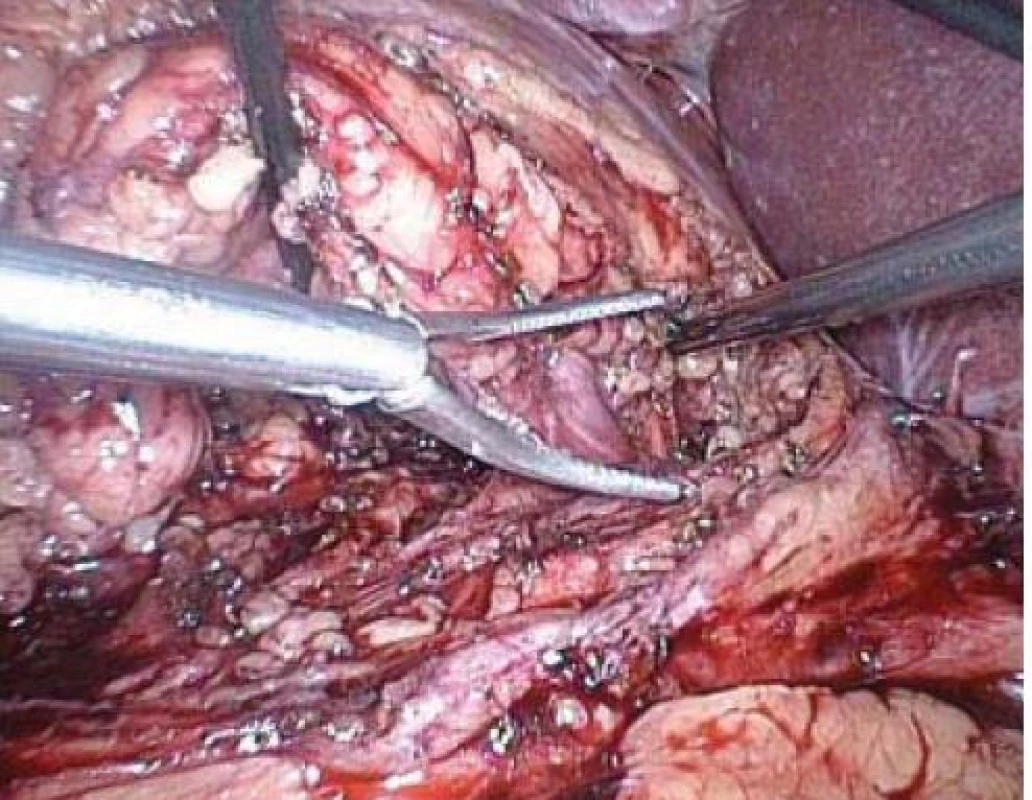
Renální žílu přerušujeme pomocí Hem-o-lok® klipů velikosti XL. Je třeba mít na mysli, že renální žíla je tenkostěnná, téměř neobsahuje svalovinu, takže může dojít snadno k jejímu poškození a významnému krvácení. Širokou žílu lze přerušit místo XL klipů pouze L klipy, když žílu stáhneme zmíněným Babcock grasperem či stehem (steh ale sami rutinně neužíváme). Samozřejmě lze žílu přerušit též staplerem. Pro případ léze hilu je vhodné mít připraveny extrakorporálně zaváděné cévní svorky (obr. 8).
Image 8. Extrakorporální cévní svorky používané zejména při laparoskopických resekcích ke klampování renálního hilu en bloc, lze jich s výhodou užít k ošetření případného cévního poranění při laparoskopické nefrektomii. 
Dovolí nám uzavřít celý hilus, odsát krev, zjistit rozsah léze cév a rozhodnout se o řešení léze, jímž je často nasazení stapleru en bloc. U hilu, kde je rozpreparování cév příliš komplikované, což je zejména pro operatéra s menší erudicí, lze přerušit hilus en bloc endovaskulárním staplerem (obr. 9).
Image 9. Naložení stapleru na hilus vpravo en bloc. 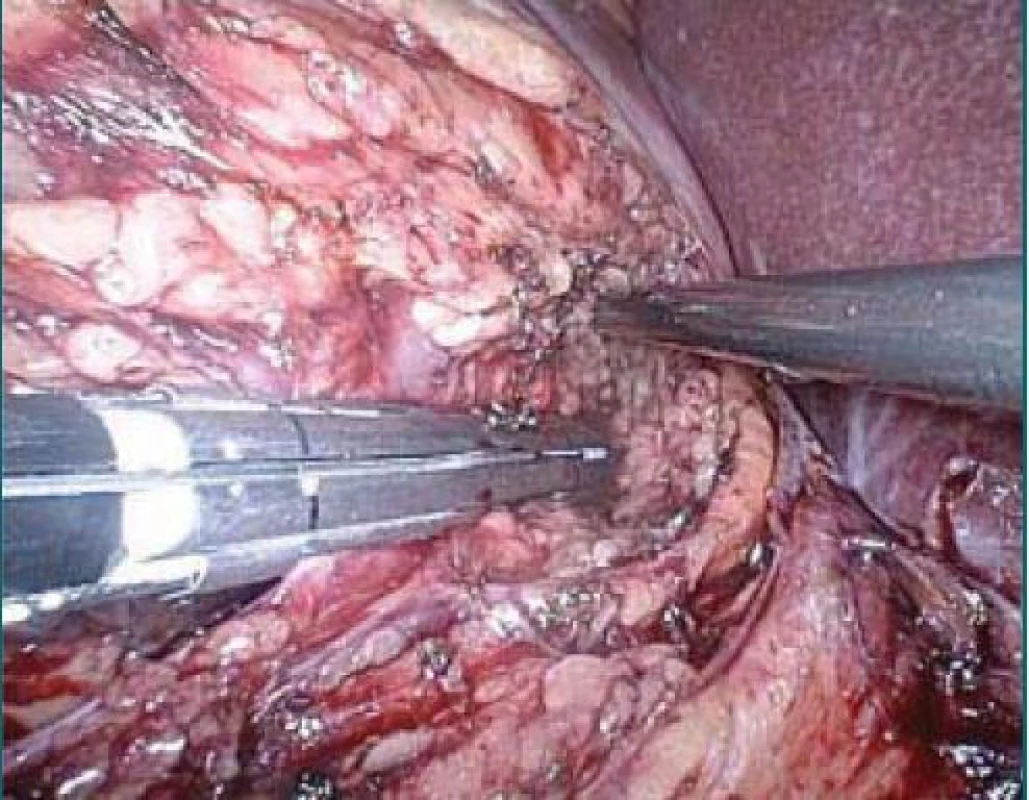
V literatuře bylo publikováno několik prací jasně ukazujících bezpečnost této metodiky [8,16–19]. Užíváme stapler většinou 45 mm dlouhý se 2 × 3 řadami titanových svorek výšky 2,5 mm. Je vhodné, abychom viděli konec stapleru. Linie řezu stapleru (označena na stapleru kolmou čárou k podélné ose) by měla být vždy minimálně 5 mm za koncem hilu. Při aktivaci stapleru se totiž tkáň nejdříve stiskne a prošívá (až později řeže) a přitom se tkáň hilu vytlačuje směrem ze stapleru. Poté je nebezpečí, že se hilové cévy nepřeruší celé. Zejména na pravé straně je při snaze vyhnout se traumatu dolní duté žíly někdy snaha operatérů nasadit stapler hodně laterálně, tedy v místě, kde se již hilové cévy větví, hilus je širší, a nemusí být tedy přerušen kompletně (obr. 10).
Image 10. Schematický obrázek znázorňuje přerušení renálního hilu en bloc vpravo. Linie „good“ označuje správné nasazení, linie „wrong“ špatné nasazení mající za následek nedopřerušený hilus. Zkratky: U – ureter, VCI – dolní dutá žíla, RV – renální žíla. 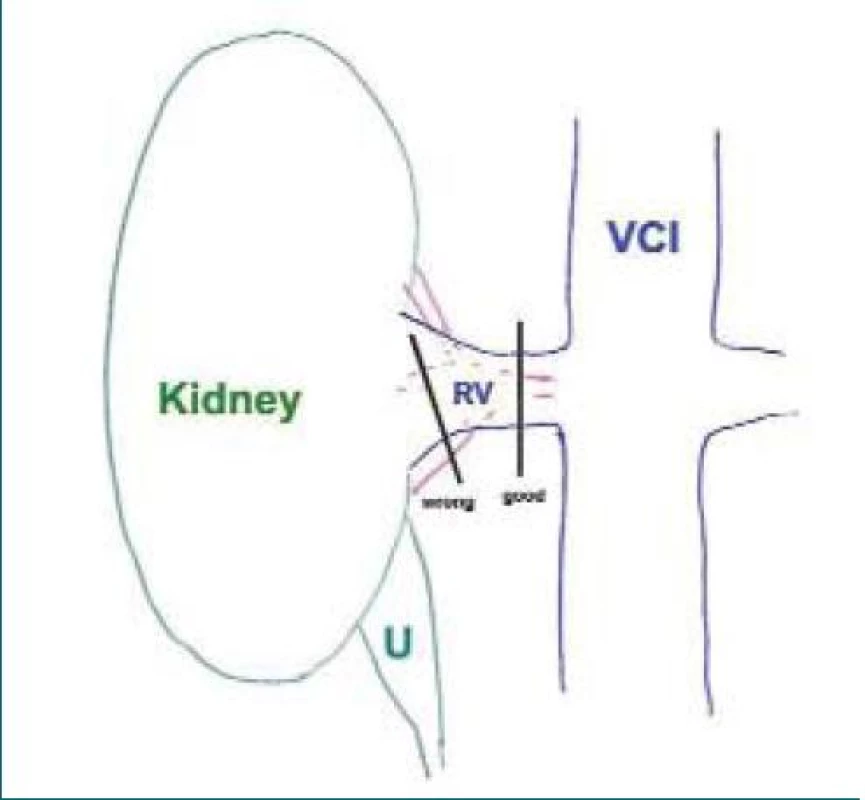
Zde je poté nutno nasadit na nepřerušenou tkáň Hem-o-lok® klip, a teprve poté zbytek hilu přerušit nůžkami. V žádném případě zde nelze užít Ligasure, neboť jsou ve tkáni kovové svorky. Ligasure® není též vhodné používat v blízkosti umělohmotných Hem-o-lok® klipů. Zde je nutno zmínit, že dříve používané titanové klipy již v podstatě nepoužíváme. Oproti uzamykatelným velmi snadno sklouznou z cévy. Jejich užití je nutné pouze v případech, kdy přerušujeme tkáň, kterou nemůžeme obejít, a vytvořit si tak okno za tkání nutné pro uzavření zámečku Hem-o-lok® klipu. Přerušení hilových cév je kruciální část operace. Špatná operační technika či i technické selhání vedly již k opakovaným úmrtím pacientů při laparoskopické nefrektomii [20]. Po přerušení hilových cév uvolňujeme horní pól ledviny od nadledviny. Nejlépe pomocí Ligasure Atlas®. Nástroj je velmi rychlý, ošetří i eventuální drobnější cévy. Po uvolnění horního pólu začínáme s Atlasem® uvolňovat dolní pól a laterální část ledviny včetně přilehlého peritonea a celého tukového pouzdra (obr. 11). Jako nástroj do druhé ruky se nám osvědčil retraktor 10 mm (obr. 11). Je dostatečně pevný, takže jej při elevaci ledviny neničíme. Nemáme-li Atlas®, je možno uvolňovat tkáň harmonickým skalpelem, bipolární koagulací či háčkem. Je to ale pomalejší a je větší riziko krvácení ze spojek mezi ledvinou a zádovými svaly. Při uvolňování ledviny (a jednoui nadledviny u adrenalektomie) háčkem s incizním proudem došlo v našem souboru při přerušení tkáně k náhlému uvolnění háčku a nekontrolovanému dotyku bránice s následnou její perforací včetně pleury, což muselo být řešeno intrakorporální suturou.
Image 11. Uvolnění pravé ledviny s celým tukovým pouzdrem pomocí Ligasure® Atlas, ledvina je elevována pomocí retraktoru 10 mm. 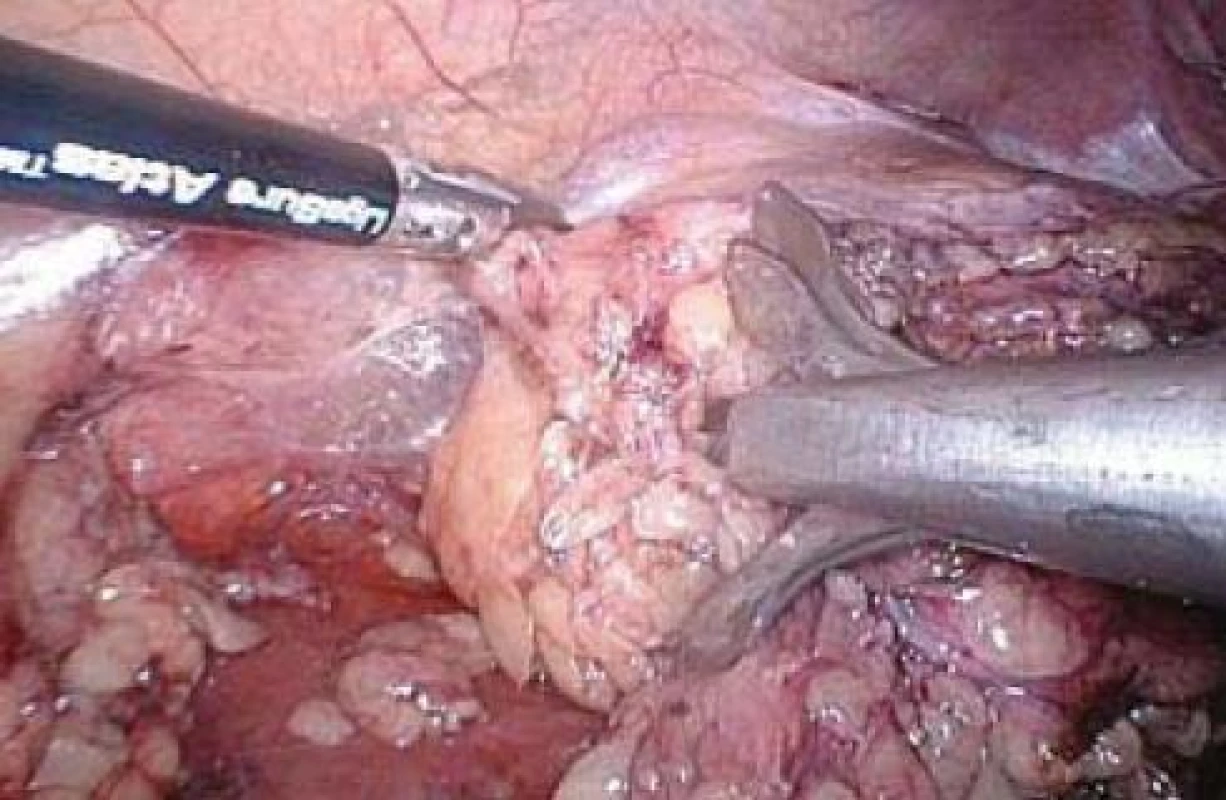
Následuje kontrola krvácení z lůžka. Obecně se doporučuje snížení tlaku na 5 mm Hg, ale sami většinou tak nečiníme, neboť při odsávání lůžka dochází samozřejmě k automatickému snížení tlaku v dutině břišní. Výplach lůžka provádíme relativně zřídka.
Po kontrole lůžka následuje extrakce preparátu. Rozhodně nedoporučujeme sáčky se zkolabovanými okraji. Je nutno minimálně dvěma nástroji držet okraje sáčku a zbývá jen jeden nástroj pro umístění preparátu. Lepší jsou sáčky se strunou v okraji, čímž se sáček otevře a uložení preparátu je jednodušší. Nicméně nejlepší jsou sáčky typu „podběráku na ryby“. Sáček v násadě se zavede do dutiny břišní, rozevře se pod preparátem, který je nadlehčován jedním grasperem (nejlépe přichyceným v oblasti hilu, za tukové pouzdro ledvinu nadzvednout nejde). Preparát se poté poměrně jednoduše uloží do sáčku (obr. 12). Sami užíváme sáček, jehož zavaděč je v průměru 15 mm, takže je teoreticky nutné mít port minimálně 15 mm. Zavádíme sáček portem v podbřišku po původním portu 12 mm. Buď je možno vyměnit port 12 mm za 15 mm (což jsme byli nuceni provést jen jednou u extrémně obézního pacienta) či extrahujeme port 12 mm, dilatujeme otvor po portu ve stěně břišní prstem a poté rovnou stěnou břišní zavedeme zavaděč sáčku. Před extrakcí preparátu ještě zavádíme drén. Portem v podžebří zavedeme grasper, který se protáhne směrem ven z dutiny břišní portem 5 mm pod 12. žebrem. Jím vtáhneme do dutiny břišní měkký kapilární (vrapovaný) drén. Redon drén většinou neužíváme. Poté následuje extrakce. Obecně máme dvě hlavní možnosti – rozšířit port (obr. 1) v podbřišku na střídavý řez či užít Pfannenstielův řez. Ten je dle literatury o něco výhodnější [21], nicméně my dáváme přednost extrakci střídavým řezem v podbřišku. Nemusí se zavírat port 12 mm, nepřibývá další incize, není nutné přetahovat vlákno od sáčku z portu 12 mm do incize v jiné incizi, je to rychlejší, velmi bezpečné. Pouze ve výjimečných případech užíváme jiné přístupy – většinou v kombinaci s korekcí hernie či využití jizvy po nějaké předchozí laparotomii. V každém případě doporučujeme užívat kvalitní firemní sáčky, které jsou pevné, neroztrhnou se a dovolí extrahovat preparát minimální incizí. Morcelaci jsme nikdy z řady důvodů neužívali. Zejména tím minimalizujeme riziko diseminace nádorů a samozřejmě se umožní přesné posouzení tumoru patologem. Střídavý řez v podbřišku uzavíráme Vicryl stehem po vrstvách. Uzávěr zbylých portů do 10 mm postačí podkoží a kůže, u portů větších je nutno provést i suturu svalů. Vzhledem k tomu, že port 12 mm užíváme k extrakci preparátu, tak jeho uzávěr samozřejmě není nutný.
Image 12. Uložení preparátu do sáčku EndoCatch®. 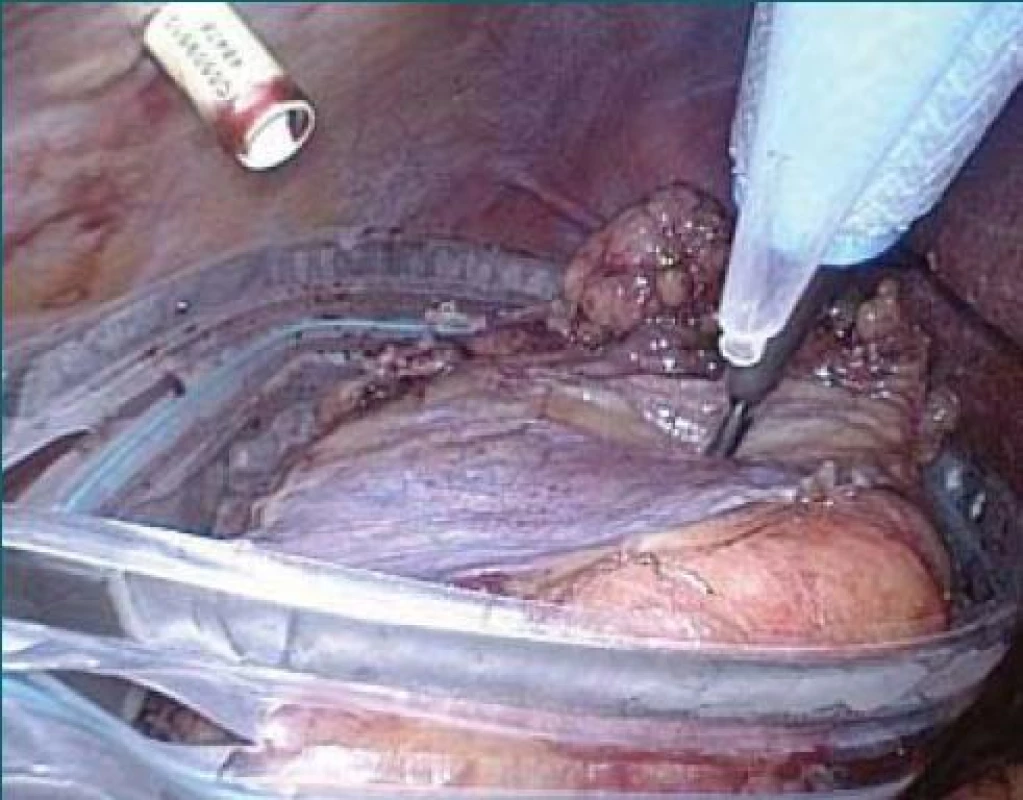
Lymfadenektomie jako součást radikální LNE si zaslouží poznámku. Lymfadenektomie u nádorů ledvin i u negativních uzlin je dle některých autorů laparoskopicky bezpečně proveditelná [22], nicméně význam lymfadenektomie je u nádorů ledvin obecně sporný, proto ji neindikujeme, a nemáme potřebu ji tedy provádět. U rozsáhlého uzlinového postižení indikujeme většinou otevřený výkon. Lymfadenektomii pro patologicky zvětšené uzliny menšího rozsahu jsme provedli pouze 5× [23], z toho 4× na levé straně, a to pouze laterálně a ventrálně od aorty. K přerušování lipolymfatické tkáně užíváme Ligasure Advance®.
TLNE je proveditelná u tumorů kategorie T3b, ale pouze u nádorových trombů omezených na renální žílu [24–25]. Sami jsme takto operovali osm pacientů (2,6 % radikálních LNE). Technika operace je obdobná, ale protože se jedná o pokročilejší tumory, bývá výkon obtížnější, zejména oddělování ledviny od velkých cév. Vlevo samozřejmě resekujeme gonadální žílu. Cévy přerušujeme separovaně, nejdříve arterii a poté žílu buď Hem-o-lok klipy či staplerem, trombus musí být vždy bezpečně odsunut periferně. Vždy je součástí výkonu adrenalektomie (AE). LNE u tumorů T3b lze doporučit jen u vybraných případů i s ohledem na erudici operatéra.
Adrenalektomie dle doporučených postupů [5] již není součástí radikální nefrektomie. Indikujeme ji pouze při postižení nadledviny dle CT, u nádorových trombů a u tumorů přímo naléhajících na nadledvinu či ji dokonce infiltrujících. Sami jsme AE jako součást TLNE provedli u 34 případů (11,2 %). Po přerušení hilu ledviny (vlevo přerušujeme renální žílu většinou mediálně od odstupu nadledvinové žíly) se oddělí nadledvina s ledvinou en bloc, přičemž postup oddělování nadledviny od okolí je stejný jako u adrenalektomií. K přerušení větších nadledvinových žil (vlevo vyjádřena vždy, vpravo jen u části pacientů) užíváme klipy, dříve titanové, nověji uzamykatelné, buď Hem-olok ® velikosti ML či vstřebatelné PDS klipy. K oddělení nadledviny užíváme většinou nástroj Ligasure® buď 5 mm (Advance®) či 10 mm (Atlas®).
U levostranné nefrektomie může samozřejmě dojít k traumatu sleziny. Sami jsme tuto situaci řešili dvakrát. Menší traumata je možno ošetřit koagulací (nejlépe argonovým koagulátorem) s následným přiložením tkané celulózy, event. je možno zvážit použití tkáňových lepidel [26]. U rozsáhlejších poranění je nutná splenektomie, buď laparoskopická nejlépe za účasti erudovaného chirurga či otevřená po konverzi.
Nyní bychom se chtěli zmínit, jak by měl probíhat co nejrychleji a nejefektivněji trénink urologa v technice laparoskopické nefrektomie. Trénink by měl probíhat dle našich zkušeností na pracovišti s dostatečným počtem prováděných laparoskopických výkonů. Na naší klinice je to přes 100 laparoskopických výkonů na ledvině (nefrektomie, resekce, nefroureterektomie) ročně. Laparoskopickou nefrektomii jsou schopni v současnosti samostatně provádět čtyři urologové. Po nezbytné teoretické přípravě je nutno nejdříve výkony asistovat, přičemž by školenec měl mít možnost si zkusit část operace – zavedení portů, otevření peritonea, uvolňování ledviny s již přerušeným hilem. Po přibližně 20 asistencích (závisí mj. na zručnosti školence, konkrétním pacientovi a také na míře trpělivosti vyučujícího urologa) lze nechat školence provádět výkon jako hlavní operatér, přičemž ale většinou zkušený asistent musí v dílčích krocích (zejména při přerušování hilu) pomoci. Po minimálně deseti takto samostatně provedených výkonech pod dozorem může školenec začít provádět výkony zcela samostatně, přičemž ale zkušenější kolega je pro první výkony v dosahu operačního sálu.
Pro začínající operatéry je nutno zmínit následující: Obecné pravidlo laparoskopie: Malé krvácení vede k horšímu přehledu, méně šetrné preparaci, a tedy často k výraznějšímu krvácení, což je cesta k dalším závažnějším komplikacím. Je třeba operovat opatrně, pro řešení komplikací máme při laparoskopii velmi omezené prostředky. Větší krvácení např. nelze tamponovat rouškou, jako při otevřené operaci, a než se provede urgentní konverze, může být krevní ztráta velmi významná. Při řešení komplikací je nutné rychlé rozhodování a i zkušený operatér se neustále v tomto směru učí. Vždy je nutno se nejdříve snažit alespoň omezit krvácení, poté s klidnou hlavou (jde-li to) odsát krev a odsavačkou odpreparovat okolní tkáň, přitom zjistit přesný rozsah poranění a poté se rozhodnout, jak to řešit. Zda konverzí, či ještě laparoskopicky. Chybou je většinou snaha na krvácení do nepřehledné tkáně nasadit kovové klipy. To nám mj. na hilu poté již znemožňuje nasadit stapler a oddělit hilus rychle a bezpečně en bloc. Pro event. konverzi je třeba se rozhodnout včas, abychom neúčelnou snahou řešit krvácení laparoskopicky nezvyšovali rozsah poranění a krevní ztrátu. Je nutno počítat s tím, že proniknutí do dutiny břišní při urgentní konverzi si vyžaduje určitý čas. A náhlý přechod výkonu laparoskopického v otevřený je trochu nepřirozený – mj. pro oči, důležitá je změna nástrojů, poloha a přístup jsou jiné než u primárně otevřeně prováděného výkonu atd. Je nutno zmínit obecnou chybu začínajících operatérů – „operování na místě“. Operatér se snaží preparovat stále na jednom místě, neví, kde má jaké okolní tkáně, terén je nepřehledný, neví, co a jak přerušit. Zde je nutné si tkáněmi různě pohybovat, popřípadě začít preparovat v jiném místě, a struktury začít přerušovat, až když je máme skutečně bezpečně zpřehledněné.
Práce byla podpořena výzkumným záměrem MSM 0021620819.
doc. MUDr. Milan Hora, Ph.D.1
MUDr. Viktor Eret1
MUDr. Petr Stránský1
MUDr. Tomáš Ürge, Ph.D.1
MUDr. Jiří Klečka jr., Ph.D.1
prof. MUDr. Ondřej Hes, Ph.D.2
MUDr. Josef Ferda, Ph.D.3
prim. MUDr. Zdeněk Chudáček, Ph.D.4
LF UK a FN Plzeň
1Urologická klinika
2Šiklův patologicko-anatomický ústav
3Radiodiagnostická klinika
4Radiodiagnostické odděleníUrologická klinika LF UK a FN
E. Beneše 13
305 99 Plzeň
horam@fnplzen.cz
Sources
1. Kato H, Kiyokawa H, Kobayashi S et al. Anatomical reconsideration to renal area: Lessons learned from radical nephrectomy or adrenalectomy through a minimal incision over the 12th rib. Int J Urol 2004; 11(9): 709–713.
2. Stolzenburg JU, Kallidonis P, Hellawell G et al. Technique of Laparoscopic-Endoscopic Single-Site Surgery Radical Nephrectomy. Eur Urol 2009; 56(4): 644–650.
3. Kaouk JH, White WM, Goel RK et al. NOTES Transvaginal Nephrectomy: First Human Experience. Urology 2009; 74(1): 5–8.
4. Sotelo R, Andrade R, Fernandez G et al. NOTES Hybrid Transvaginal Radical Nephrectomy for Tumor: Stepwise Progression Toward a First Successful Clinical Case. Eur Urol 2009; in print, doi:10.1016/ j.eururo.2009.04.031
5. Ljungberg B, Hanbury DC, Kuczyk MA et. Guidelines on Renal Cell Carcinoma, 2009, http://www.uroweb.org/fileadmin/tx_eauguidelines/2009/Full/RCC.pdf: 28
6. Hora M, Klečka J jr, Hes O et al. Miniinvazivní laparoskopická či retroperitoneoskopická radikální nefrektomie pro parenchymový tumor. Rozhledy v Chirurgii 2005; 84(5): 246–252.
7. Hora M, Klečka J. Možnosti laparoskopie a retroperitoneoskopie v léčbě parenchymových nádorů ledvin, část I – nefrektomie. Urol Listy 2005; 3(3): 29–34.
8. Eret V, Hora M, Klečka J et al. Laparoskopická radikální nefrektomie pro parenchymový tumor ledviny – soubor 150 pacientů. Čas lék čes 2007; 147(10): 758–762.
9. Hora M, Ferda J, Kreuzberg B et al. Využití dvoufázové CT-angiografie při chirurgické léčbě nádorů ledvin. Čes Urol 2005; 9(1): 14–19.
10. Ferda J, Hora M, Hes O et al. Dvoufázová multidetektorová CT-angiografie nádorů ledvin. Urol Listy 2006; 4(2): 32–35.
11. Ferda J, Kreuzberg B, Hes O et al. Dvoufázová multidetektorová CT-angiografie renálního renálního karcinomu. Čes Radiol 2007; 61(1): 11–19.
12. Ferda J, Ferdová E, Záhlava J et al. Možnosti zobrazení nádorů urogenitálního traktu pomocí 18FDG-PET/CT. Urol Listy, 2006, 4(2): 36–40.
13. Baumert H, Ballaro A, Arroyo C et al. The Use of Polymer (Hem-o-lok) clips for management of the renal hilum during laparascopic nephrectomy. Eur Urol May 2006; 49(5): 816–419.
14. Hora M, Klečka J, Eret V et al. Přerušení hilových cév při laparoskopické nefrektomii pomocí uzamykatelných klipů (Hilar vascular occlusion during laparoscopic nephrectomy by means of locking clips). Čes Urol 2007; 11(2): 89–92.
15. Ponsky L, Cherullo E, Moinzadeh A et al. The Hem-o-Lok clip is safe for laparoscopic nephrectomy: A multi-institutional review. Urology 2008; 71(4): 593–596.
16. Buse S, Gilfrich C, Pfitzenmaier J et al. En bloc stapler ligation of the renal vascular pedicle duringlaparoscopic nephrectomy. BJU Int 2007; 101(7): 878–882.
17. Kouba E, Smith AM, Derksen JE et al. Efficacy and Safety of En Bloc Ligation of Renal Hilum During Laparoscopic Nephrectomy. Urology 2007; 69(2): 226–229.
18. Conradie MC, Urry RJ, Naidoo D et al. Advantages of En Bloc Hilar Ligation During Laparoscopic Extirpative Renal Surgery. J Endourol 2009; 23(9): 1503–1507.
19. Schatloff O, Ramon O, Lindner U et al. Is postoperative arteriovenous fistula still a koncern after en bloc stapling of the renal hilum during laparoscopic nephrectomy. J Endourol Apr 2009; 23(4): 639–643.
20. Hsi RS, Saint-Elie DT, Zimmermann GJ et al. Mechanisms of Hemostatic Failure During Laparoscopic Nephrectomy: Review of Food and Drug Administration database. Urology 2009; 70(5): 888–892.
21. Tisdale BE, Kapoor A, Hussain A et al. Intact Specimen Extraction in Laparoscopic Nephrectomy Procedures: Pfannenstiel Versus Expanded Port Site Incisions. Urology 2007; 69(2): 241–244.
22. Chapman TN, Sharma S, Zhang S et al. Laparoscopic Lymph Node Dissection in Clinically Node-Negative Patients Undergoing Laparoscopic Nephrectomy for Renal Carcinoma. Urology 2008; 71(2): 287–291.
23. Eret V, Hora M, Hes O et al. Lymfadenektomie u laparoskopicky řešených pokročilých nádorů ledvin. Čes Urol 2009; 13(4): 319.
24. Hora M, Klečka J, Ferda J et al. Laparoskopická radikální nefrektomie u tumoru s žilním nádorovým trombem (T3b). Čes Urol 2005; 9(3): 52–55.
25. Guzzo TJ, Schaeffer EM, McNeil BK et al. Laparoscopic Radical Nephrectomy for Patients with Pathologic T3b Renal-Cell Carcinoma: The Johns Hopkins Experience. J Endourol 2009; 23(1): 63–67.
26. Hora M, Eret V, Ürge T et al. Možnosti využití tkáňových lepidel při ledvinu šetřících výkonech u tumorů ledvin. Čes Urol 2007; 11(3): 147–153.
Labels
Paediatric urologist Urology
Article was published inUrological Journal

2010 Issue 1-
All articles in this issue
- Diagnostika karcinomu prostaty a role PCA3
- Současné klinické a patologické proměnné biopsie prostaty, které predikují významné změny grade
- Laparoskopická adrenalektomie: operační technika
- Technické aspekty provedení transperitoneální laparoskopické nefrektomie
- Laparoskopická resekce ledviny
- Rekonstrukční laparoskopie v dětské urologii
- Laparoskopické rekonstrukční operace na horních močových cestách u dětí – technické aspekty
- Retroperitoneoskopie
- Laparoskopická operace vedoucí k odstranění konkrementů
- Komplikace při řešení nádorů ledvin laparoskopicky
- Psychologický mechanizmus při nádorovém onemocnění a základy komunikace v jednotlivých fázích
- Výzkum výsledků zdravotní péče v oblasti urologie
- Urological Journal
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Laparoskopická adrenalektomie: operační technika
- Laparoskopická resekce ledviny
- Laparoskopické rekonstrukční operace na horních močových cestách u dětí – technické aspekty
- Technické aspekty provedení transperitoneální laparoskopické nefrektomie
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

