-
Medical journals
- Career
Derivace moči po cystektomii
: L. Jarolím
: Urol List 2008; 6(2): 53-59
V současné době se u poloviny nemocných po cystektomii konstruuje ortotopická neovezika a u třetiny nemocných ureteroileostomie, zbylí nemocní mají kontinentní náhradu kontrolovanou análním sfinkterem a kontinentní heterotopickou neoveziku.
Nejlepší formou močové derivace je patrně ortotopická neovezika, pokud ovšem zůstane bez krátkodobých a dlouhodobých komplikací. U starších nemocných bývá tendence ke zhoršování kontinence zapříčiněná ochabováním muskulatury. Zkušenosti při sledování delším než 10 let ukazují příznivé dlouhodobé výsledky mikce s pomalým zhoršováním kontinence s přibývajícím věkem. Na riziko hyperkontinence je třeba myslet zejména u žen s ortotopickou neovezikou.
Ureteroileostomie je vhodná u polymorbidních nemocných pro technickou jednoduchost a u nemocných, u kterých je vysoké riziko lokální recidivy nebo se plánuje adjuvantní radioterapie.
Rekonvalescence a rehabilitace nemocných s náhradou kontrolovanou análním sfinkterem je velmi rychlá. Dlouhé intervaly evakuace pouche dovolují nemocným brzy po výkonu spát delší dobu, nebo dokonce bez buzení.
Výsledky heterotopické náhrady močového měchýře mohou být u starších nemocných ovlivněny mírou samoobslužnosti při autokatetrizaci. Složitější močové derivace využívající řady specifických prvků vedou k vyššímu riziku různých komplikací.
Pro nemocného musí být vybrána ta nejvhodnější konkrétní derivace, „na míru“. Funkční výsledky všech derivací jsou při správně zvoleném typu srovnatelné a závisí na správně provedené cystektomii a pečlivé rekonstrukci.Klíčová slova:
derivace moči, náhrady močového měchýřeÚVOD
Jednotlivé úseky vývodných cest močových na sebe morfologicky i funkčně navazují a končí zevním ústím uretry. Schází-li některý z anatomických úseků vývodných cest močových, je třeba jeho funkci zabezpečit náhradním způsobem, tj. zabezpečit odvádění moči jinou cestou než přirozenou. Tato náhradní funkce se označuje jako derivace moči. V užším slova smyslu se užívá termín derivace moči u stavů, kdy je vyřazena funkce močového měchýře a termín derivace pak označuje náhradu funkce močového měchýře.
Funkce močového měchýře spočívá ve sběru a kontrolované evakuaci moči. Náhradní systémy různých forem derivace mohou tyto funkce napodobovat v jednotlivostech nebo v celém komplexu. Znamená to současně různý stupeň dokonalosti derivace ve smyslu přiblížení se k optimálnímu, tedy fyziologickému stavu. Optimální formou derivace je stav, při kterém se nahradí obě základní funkce močového měchýře - střádací a evakuační. Takováto derivace je kontinentní. Není-li to možné, je třeba nahradit alespoň funkci evakuační, tj. zabezpečit volné odvádění moči. V tomto případě je taková derivace inkontinentní. Pro močovou derivaci se využívají některé části zažívacího traktu, nejčastěji střeva.
Historicky se začal střevní trakt používat k močové derivaci již před více než sto lety, přičemž moč byla svedena do terminální části střeva. Sir John Simon vytvořil v Londýně 5. července 1852 po několika pokusech na psech u 13letého chlapce píštěl mezi terminálními úseky ureterů ústících do exstrofického měchýře a rektem. Hedvábné stehy protáhl do rekta pomocí stříbrné trubičky zavedené do terminálního úseku ureteru pomocí jehly vyrobené z hodinového péra. Postupným dotahováním stehů vznikla píštěl. Pacient zemřel za 12 měsíců na kalkulózní pyelonefritidu [1]. Jednalo se o ureteroproktostomii, nikoli o ureterosigmoideostomii, jak se nesprávně uvádí prakticky ve všech publikacích, které Simona citují. Refluxní komplikace implantace ureterů do střeva vedly Karla Maydla v Praze v roce 1892 k implantaci využívající přirozený antirefluxní mechanizmus a implantoval terčík trigona do sigmatu [2,3]. Tato operace je nesmírně cenným přínosem v rekonstrukční urologii a náš Karel Maydl je právem citován ve všech publikacích týkajících se derivace moči.
Dalším přínosem Karla Maydla byla intususcepce na jejunostomii u nemocného s karcinomem žaludku, kterou v roce 1892 vytvořil ke krmení pacienta. Intususcepce bránila regurgitaci instilovaného obsahu [4]. Princip intususcepce se v 80. letech minulého století začal využívat při tvorbě antirefluxního mechanizmu u močových derivací.
První ortotopickou neoveziku zkonstruoval v roce 1889 Karel Pawlík u ženy a použil jako rezervoár pochvu [5]. V roce 1962 publikoval zprávu o ženských neovezikách z nedetubularizovaného střeva Eduard Hradec [6]. U nás zahájil v roce 1993 éru ženské neoveziky z detubularizovaného střeva Ladislav Jarolím [7-9].
Zpočátku se pro derivaci využívalo sigma, ale refluxní komplikace z vysokého intraluminárního tlaku vedly začátkem 50. let minulého století k rozšíření ureteroileostomie [10]. V 80. letech minulého století přišla nová éra nízkotlakých rezervoárů, která rozšířila spektrum močových derivací [11,12].
Výběr konkrétní močové derivace po cystektomii je třeba učinit před operací po důkladném seznámení pacienta s konkrétními možnostmi, jejich výhodách a nevýhodách a možných komplikacích. Je třeba zhodnotit věk pacienta, celkový zdravotní stav, stadium nádorového onemocnění a renální funkce.
Důležitým požadavkem na jakoukoli náhradu močového měchýře je zachování integrity horního močového traktu.
Koncem 80. let minulého století se ke tvorbě močových rezervoárů prakticky přestalo užívat střevo v tubulární podobě. Fyzikálními zákony bylo poukázáno na fakt, že sférický rezervoár vytvořený z určitého úseku střeva rekonfigurací má větší objem a nižší intrakavitární tlak než stejně dlouhý úsek střeva v původním tubulárním tvaru.
Detubulizace je podélné otevření střeva na antimezenteriální či antimezokolické straně. Při detubulizaci dochází k přerušení cirkulárních a spirálních svalových vláken, porušení normální peristaltiky a vznik interakce peristaltických a antiperistaltických vln. Z fyzikálního hlediska se jedná o uplatnění La Placeova zákona. Intrakavitární tlak (P) je výsledkem povrchového napětí (T) a velikosti (průměru, r) tělesa: P = T/r. Průměr je v uvedeném vzorci ve jmenovateli, proto spolu s růstem jeho hodnoty klesá intrakavitární tlak. Nízký intrakavitární tlak je jedním z hlavních požadovaných atributů sférických kontinentních močových rezervoárů, jejichž kompliance je vyšší než u rezervoárů tubulárních [13]. Detubulizací vznikne podlouhlý střevní štěp, z něhož lze vhodným uspořádáním vytvořit oválný nebo sférický rezervoár. Pruh střevní stěny se meandrovitě nebo spirálně složí. Meandrovité uspořádání může mít tvar písmene U, S, Z, M nebo W. Spirální uspořádání může obsahovat i dvě otočky. Rekonfigurace směřuje k získání maximálního objemu rezervoáru. Na druhé straně musí respektovat přítomnost mezenteria. Mezenterium má nepravidelný obsah tuku a nepravidelnou délku. Typ rekonfigurace proto nebývá rigidní a přizpůsobuje se aktuálním podmínkám a potřebám. Intrakavitární tlak klasické ureterosigmoideostomie dosahuje až 200 cm H20, tlak v ileální neovezice z detubulizovaného střevního segmentu jen 30 cm H20.
Typy derivace moče po cystektomii jsou následující:
- kontinentní náhrady močového měchýře, tzv. ortotopické substituce
- rezervoáry s kontinentním kutánním stomatem – heterotopické rezervoáry
- kontinentní derivace moči kontrolované análním sfinkterem
- inkontinentní ureteroileostomie
- paliativní derivace
1. KONTINENTNÍ NÁHRADY MOČOVÉHO MĚCHÝŘE, TZV. ORTOTOPICKÉ SUBSTITUCE
Ortotopická neovezika je uložena na místě měchýře a využívá originální sfinkter uretry. Je proveditelná nejen u muže (obr. 1), ale i u ženy (obr. 2) [9]. Vznik ortotopických derivací stimulovaly nepříznivé konsekvence inkontinentních konduitů v době, kdy nebyly k dispozici vhodné pomůcky pro sběr moči a primitivní urinály byly zcela nespolehlivé. Frekvence časných i pozdních komplikací ortotopických substitucí jsou obdobné jako u konduitů, které jsou obecně vnímány jako jednodušší a bezpečnější. Zkušenosti s ortotopickými náhradami ukazují, že motivovaní a správně indikovaní pacienti mají bezvadné výsledky. Život těchto pacientů je podobný jako u lidí s normálním dolním močovým traktem.
1. Ortotopická neovezika u muže – vylučovací urografie. 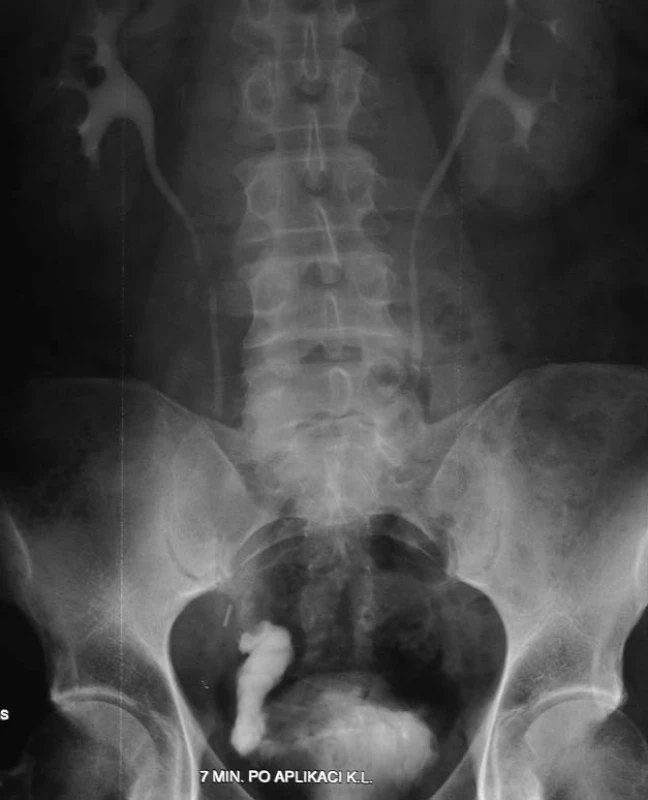
2. Ortotopická neovezika u muže – vylučovací urografie. 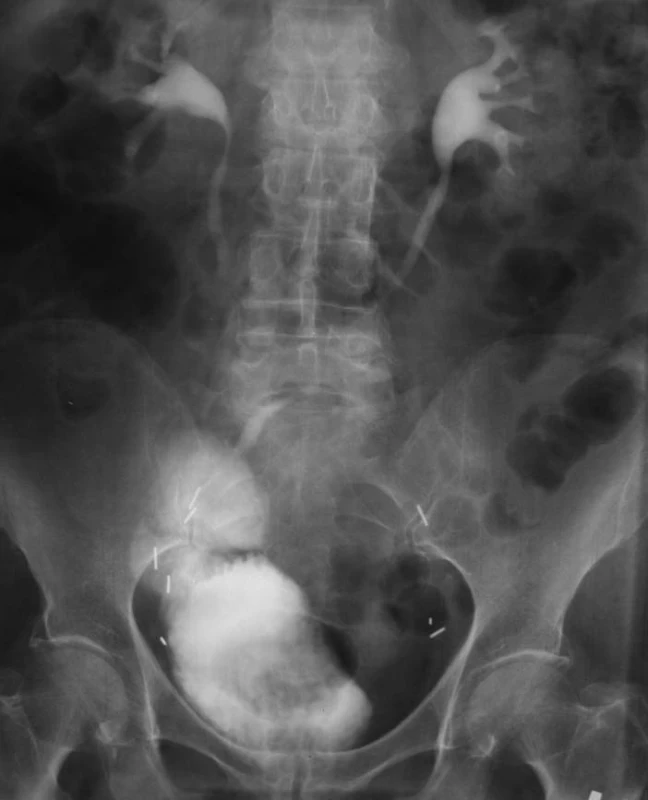
Nejčastěji se konstruují rezervoáry z ilea podle Hautmanna, Kocka a Studera. Varianta Richarda Hautmanna [14] je založena na rekonfiguraci detubulizovaného ilea ve tvaru písmene W a antirefluxní Le Ducově implantaci ureterů [15]. Nils Kock využil pro antirefluxní implantaci ureterů intususcepci přívodné kličky [16]. Urs Studer přinesl do spektra náhrad močového měchýře implantaci ureterů do dlouhé přívodné kličky bez antirefluxní implantace [17].
Indikace k ortotopické neovezice se zakládá v první řadě na přání nemocného. Absolutní kontraindikací kontinentní derivace je špatná renální funkce z dlouhodobé obstrukce nebo chronická renální insuficience s hladinou sérového kreatininu nad 150 až 200 µmol/l.
Kontinenci u ortotopické neoveziky zajišuje intaktní rabdosfinkter, jehož zachování nemůže být na úkor onkologické bezpečnosti výkonu. Předpokladem pro použití uretry je u muže negativní bioptický nález distální prostatické uretry a u ženy negativní bioptický nález hrdla močového měchýře [18].
Přesto, že ortotopická neovezika představuje ideální derivaci, není vhodná u polymorbidních a starých nemocných a stavů před nebo po radioterapii.
Implantace ureterů do neoveziky představuje jeden z jejích kritických prvků. Zvyšuje složitost chirurgického výkonu, a tím i četnost komplikací, konkrétně riziko striktury ureteroenterické anastomózy s následným ohrožením funkce ledviny.
Dlouhá přívodná klička u Studerovy neoveziky nebrání refluxu, za běžných podmínek bez přeplnění rezervoáru však funguje jako dynamický antirefluxní systém a reflux je minimální [19]. Antirefluxní implantace ureterů není potřebná, nebo během mikce produkuje břišní lis stejný nárůst tlaku na pouch, přívodnou kličku, uretery a pánvičku a k refluxu nedochází. Skutečný reflux lze vyvolat například jen při artificiálním plnění systému kontrastní látkou nad funkční kapacitu rezervoáru. Po návratu kontrastní látky do rezervoáru je při peristaltice ureterů a izoperistaltické aktivitě přívodné kličky během mikce absence refluxu.
Výhodou použití tubulární přívodné kličky u Studerovy ureteroileální implantace je z onkologického hlediska resekce ureterů s periureterálními lymfatickými cévami nad aa. iliaceae communes, tedy daleko od primárního tumoru. Kratší ponechané uretery mají menší riziko ischemie distálních partií s případnou následnou fibrózou vedoucí k jejich stenotizaci. Jednoduchá implantace ureterů do přívodné kličky nízkotlakého rezervoáru v kombinaci s jeho pravidelnou evakuací a pravidelným sledováním je výkon s nejnižším počtem komplikací. Na druhé straně představuje implantace bez antirefluxní úpravy vyšší riziko pyelonefritidy.
U antirefluxních ureteroenterických anastomóz je dilatace horních močových cest signifikantně častější. Dlouhodobá bezpečnost horních močových cest je podstatným požadavkem na úspěšnou derivaci. Obstrukce je s výjimkou renální insuficience pro renální funkci daleko nebezpečnější nežli reflux. Vyšší četnost komplikací a reoperací Le Ducovy antirefluxní implantace převyšuje její potenciální přínos. Nejčastější příčinou striktury ureteroenterické anastomózy je ischemie terminálního ureteru. Riziko striktury může snížit šetrná mobilizace ureteru se zachováním periuretrální tkáně s výživnými cévami. Levý ureter bývá ohrožen při složité transpozici na pravou stranu angulací.
Denní kontinence bez potřeby vložek nebo s potřebou jedné vložky dosahuje 85–90 % nemocných [20]. Noční kontinence dosahuje až 67 % nemocných, většinou se pohybuje noční inkontinence mezi 20–30 % [21]. Enurézu lze až u 25 % nemocných ovlivnit imipraminem v dávce 25 mg před spaním [22].
Stinnou stránkou ortotopické neoveziky je riziko chronické retence vyžadující autokatetrizaci. Pacienti se při nácviku mikce musí naučit vědomě zvýšit intraabdominální tlak Valsalvovým manévrem či Crédeho hmatem a simultánně relaxovat pánevní dno. Dysfunkce vyžadující intermitentní katetrizaci postihuje až 33 % mužů [23] a až 53 % žen s ortotopickou neovezikou [24]. Primární příčinou hyperkontinence u žen s ortotopickou neovezikou je patrně „pouchocele“ ze ztráty dorzální opory neoveziky, vedoucí k angulaci neovezikouretrální junkce. Oporu lze obnovit elevací rekonstruované pochvy nebo interpozicí omenta. Další možnou příčinou je poškození autonomní inervace dolní hypogastrické pleteně [25-30].
Onkologická bezpečnost ortotopické derivace je ohrožena při pozitivních okrajích preparátu cystektomie [31-33].
Ortotopická neovezika je vhodná pro pacienty s minimálním rizikem lokální recidivy nádoru bez potřeby adjuvantní radioterapie. V případě zdařilé ortotopické derivace je tato forma nejbližší normálnímu stavu a přináší pacientům dobrou kvalitu života.
2. REZERVOÁRY S KONTINENTNÍM KUTÁNNÍM STOMATEM – HETEROTOPICKÉ REZERVOÁRY
Kontinenci u heterotopických náhrad močového měchýře (Indiana pouch, Mainz pouch I) vytvořených ze segmentů střeva a výjimečně i ze žaludku zajišuje artificiální chlopeň [34]. Je konstruovaná intususcepcí či podélným zúžením dalšího střevního segmentu, což je komplikovaný mechanizmus zatížený vysokým rizikem insuficience kontinenčního mechanizmu a problémů s katetrizací. U nemocných, kteří dříve nepodstoupili apendektomii, je možné využít apendix pro kontinentní apendikostomii [35,36].
Heterotopické náhrady močového měchýře je možné konstruovat u nemocných, kteří si přejí být kontinentní, a není u nich možno využít k zabezpečení kontinence uretru ani anální sfinkter. Z onkologického hlediska je lze indikovat po radioterapii nebo při plánování adjuvantní radioterapie.
3. KONTINENTNÍ DERIVACE MOČI KONTROLOVANÉ ANÁLNÍM SFINKTEREM
Ureterosigmoideostomie je variace nejstarší popsané formy kontinentní močové derivace [1] a získala si v první polovině minulého století velkou popularitu. Počáteční nadšení však v 50. letech vystřídalo zklamání způsobené řadou komplikací, zvláště poruchami elektrolytové a acidobazické rovnováhy, recidivujícími pyelonefritidami a poškozením renálních funkcí. Dokonalejší technika ureteroenterální anastomózy [37], moderní šicí materiály a nová antibiotika snížila riziko komplikací, což spolu s důrazem kladeným na kvalitu života vedlo k obnovení zájmu o tento typ derivace. Snaha o dosažení úplné kontinence a zkušenosti s detubulizací střevních segmentů u ortotopických i heterotopických neovezik přinesly myšlenku úpravy klasické metody ureterosigmoideostomie a použití stejného principu k vytvoření nízkotlakého rektosigmoidálního rezervoáru. K renesanci ureterosigmoideostomie přispěl Rudolf Hohenfellner z Mainzu [38-40]. Výsledkem je poměrně jednoduchá operační metoda, která při precizním provedení a dokonalé pooperační péči ohrožuje nemocného jen malým množstvím komplikací [41-47]. Nejzávažnější pozdní komplikací je stenotizace uretereoenterické anastomózy. Příčinou může být nedokonalá operační technika nebo ischemie terminální části ureteru. Procento metabolických komplikací, zejména metabolické acidózy, je u sigma-rectum pouche vyšší než u jiných forem kontinentních derivací, což je zřejmě způsobeno refluxem moči do orálnějších úseků tračníku.
Ureterosigmoideostomie v moderním podání s využitím detubulizace se označuje jako sigma-rectum pouch (Mainz pouch II, Motol pouch). Sigma-rectum pouch v motolské variaci (obr. 3) odděluje více než Mainz pouch močový trakt a střevní pasáž přerušením střeva a anastomózou descendens k rektu pod rezervoárem [48-49]. Rekonvalescence a rehabilitace nemocných po operaci je velmi rychlá. Dlouhé intervaly evakuace pouche dovolují nemocným brzy po výkonu spát delší dobu, nebo dokonce bez buzení. Při konstrukci rektosigmoideálního rezervoáru Motol pouch se střevo přeruší v místě přechodu descendens v sigma a descendens se anastomózuje end-to-side s rektem. Sigma s proximální částí rekta se detubulizuje a rekonfiguruje do sférické podoby. Do rezervoáru se antirefluxní Goodwinovou technikou [37] implantují uretery. Podobnou techniku popsal v r. 1907 Descoms [50], použil však nedetubularizované střevo a přímou implantaci ureterů. Anastomóza descendens s rektem end-to-side umožňuje více oddělit pasáž stolice od močového rezervoáru.
3. Motol pouch – vylučovací urografie. 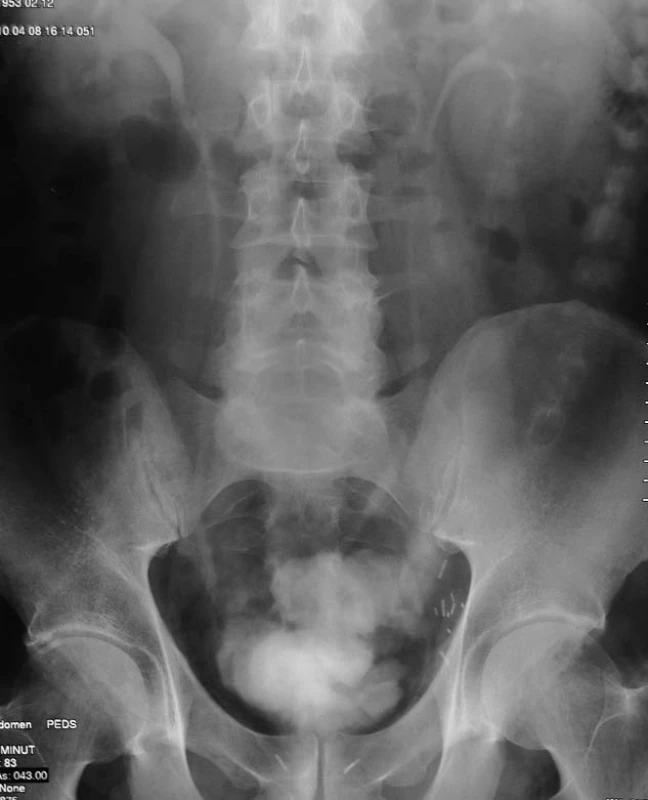
Rezervoár kontrolovaný análním sfinkterem lze indikovat u nemocných s normální funkcí sfinkteru, potvrzenou schopností udržet v rektu po dobu 1 hodiny obsah 400 až 500 ml. Nemocní s neurogenní poruchou měchýře mohou mít současně sfinkterickou dysfunkci, a proto u nich není sigma-rectum pouch vhodný. Není vhodný také u stavů po radiaci a před radioterapií.
4. INKONTINENTNÍ URETEROILEOSTOMIE
Inkontinentní konduit, ureteroileostomie či Brickerova operace, má ve srovnání s kontinentními formami derivace méně močových symptomů, vyžaduje však speciální jímače, urinály. Je vhodná u polymorbidních nemocných pro technickou jednoduchost a u nemocných, u kterých je vysoké riziko lokální recidivy nebo se plánuje adjuvantní radioterapie.
Indikací k inkontinentní ureteroileostomii je zejména stav po ozáření pánve, choroby střeva a neurogenní poruchy. Pro některé starší pacienty, kteří preferují návrat do původního usedlého způsobu života nebo žijí v sociální izolaci bez potřeby péče o tělesný vzhled, je ureteroileostomie optimálním řešením [51]. Ureteroileostomie si vyžádala zdokonalení stomických pomůcek (urinálů) až na dnešní moderní úroveň. Urinály jsou samolepicí, nedráždí pokožku, jsou opatřeny chlopněmi a ventily a jsou nákladné. Místo stomie je třeba vybrat již před výkonem: nemůže být v kožní rýze, která vzniká při předklonu nebo vsedě. Její okolí musí být hladké, bez jizev, aby na něj bylo možno aplikovat planžetu urinálu. Metoda byla nejrozšířenější derivací až do 80. let a stále je pro vybrané pacienty nejvhodnějším způsobem derivace. Při dlouhodobém sledování je ureteroileostomie zatížena komplikacemi, jako je parastomální hernie, stenóza stomie a zhoršení stavu horních močových cest. Incidence těchto komplikací roste s délkou sledování. Parastomální hernie se vyskytuje u 10–15 % nemocných.
5. PALIATIVNÍ DERIVACE
Paliativní derivace je indikovaná u nemocných v uremii, s hematurií nebo s bolestmi, u kterých nelze provést cystektomii pro pokročilý rozsah nádoru či špatný celkový stav a krátkou prognózu. V takových případech je vhodnou formou paliativní derivace perkutánní punkční nefrostomie. Další formou paliativní derivace je kožní ureterostomie, která je indikována u stavů, při nichž nemůže být použito střevo pro těžké srůsty nebo jeho onemocnění.
Pro kožní ureteroileostomii se oba uretry podélně discidují v délce 7 cm a podélně se spolu sešijí v délce 4,5 cm. Nesešité konce ureterů se pomocí Z-plastiky vyšijí do kožní incize [52]. Riziko u stenózy takové stomie je 8,3 %. Ureterostomii lze provést i laparoskopicky [53].
INTERAKCE STŘEVA S MOČOVÝM TRAKTEM, KOMPLIKACE
Funkcí střeva je selektivní vstřebávání a sekrece. Uplatňuje se délka střeva, velikost povrchu, doba přítomnosti moči, její koncentrace, pH, renální funkce a osmolarita moči. Trvalý přívod moči jako objemného roztoku do střeva ovlivňuje elektrolytové hospodářství a hepatální metabolizmus. Vzniká metabolická acidóza, poruchy tvorby a vstřebávání vitaminů, vstřebávání žlučových kyselin. Z poruchy metabolizmu minerálů vzniká osteomalacie [54]. Míra negativních vlivů je úměrná rozsahu expozice, době působení moči ve střevě a stavu renálních funkcí.
Hyperchloremická acidóza
Segment střeva použitý pro derivaci secernuje při expozici moči natriové a bikarbonátové ionty. Reabsorbuje ionty amoniové, vodíkové a chloridové. V ileu je absorpce kalia větší než v tlustém střevě. Zásadní roli ve vlivu na pH vnitřního prostředí hraje transport natriových a vodíkových iontů výměnou za ionty amoniové (NH3 a NH4), které jsou reabsorbovány. Amoniový iont tak působí jako kompetitivní inhibitor absorpce natria. Amoniové ionty se vážou na chlór, a tím vzniká hyperchloremická acidóza.
Použití tračníku může vést k hyperosmolaritě séra s následným poklesem hladiny aldosteronu, vyvolávajícím zvýšenou sekreci adiuretinu. Tyto metabolické poruchy působí vysokou koncentraci moči, ze které sliznice tračníku absorbuje více natria a chloridových iontů [55].
Riziko vstřebávání chlóru poklesá s dobou od vytvoření intestinální derivace. Schopnost kompenzovat metabolickou acidózu je u dětí a u pacientů s renální insuficiencí nižší. Je u nich proto výhodné užít pro derivaci žaludeční segment. Žaludek je primárně sekreční orgán s významnou sekrecí vodíkových a chloridových iontů, a acidóza proto při jeho užití pro močovou derivaci nehrozí. Korekce metabolické hyperchloremické acidózy spočívá v podávání alkalizujících prostředků, jako je natrium bikarbonát.
Dlouhodobá expozice střevní sliznice moči může vést ke vzniku adenokarcinomu ureteroenterické anastomózy [56].
Porucha vstřebávání vitaminu B12
Vitamin B12 se primárně absorbuje v terminálním ileu. Po resekci terminálního ilea roste riziko nedostatku tohoto vitaminu, což se projeví až po vyčerpání zásob, to je po 3 až 5 letech. Nedostatek vitaminu B12 může vést k ireverzibilním neurologickým a hematologickým komplikacím.
Poruchy kostního metabolizmu
Chronická acidóza ovlivňuje kostní metabolizmus aktivací osteoklastů s následkem kostní resorpce [57] a zhoršuje α-hydroxylaci 25-hydroxycholelalciferolu v ledvinách, vedoucí k deficitu vitaminu D, jehož absorpce je zhoršena i resekcí ilea. Nedostatek vitaminu D působí poruchu kostní mineralizace [58]. Kostní minerály – kalcium, karbonát a natrium se při acidóze spotřebovávají směnou za vodíkové ionty [59,60].
Sekrece hlenu
Denní sekrece hlenu u kontinentních náhrad močového měchýře představuje asi 35 g [61]. Močí-li nemocný volně a bez rezidua, nečiní produkce hlenu obtíže. U nemocných s retencí hlenu je možno rezervoár vyplachovat cévkou. K mukolýze lze užít ureu N-acetylcystein. Nejjednodušší prostředek usnadňující evakuaci hlenu je však dostatečný přívod tekutin.
ZÁVĚR
Současný stav distribuce jednotlivých typů derivací moči po cystektomii pro nádory měchýře shrnul Rudolf Hautman se spolupracovníky ve zprávě pro WHO. U více než 7 000 pacientů byla ve 47 % vytvořena ortotopická náhrada, ve 33 % ureteroileostomie, v 10 % kontinentní náhrada kontrolovaná análním sfinkterem, v 8 % kontinentní heterotopická neovezika a ve 2 % paliativní derivace [62].
Složitější močové derivace využívající řady specifických prvků vedou k vyššímu riziku různých komplikací. Nejlepší formou močové derivace je patrně ortotopická neovezika, pokud ovšem zůstane bez krátkodobých a dlouhodobých komplikací. U starších nemocných bývá tendence ke zhoršování kontinence, které je zapříčiněno ochabováním muskulatury. Zkušenosti při sledování delším než 10 let ukazují příznivé dlouhodobé výsledky mikce s pomalým zhoršováním kontinence s přibývajícím věkem [63]. Na riziko hyperkontinence je třeba myslet zejména u žen s ortotopickou neovezikou [28]. Výsledky heterotopické náhrady močového měchýře mohou být u starších nemocných ovlivněny mírou samoobslužnosti při autokatetrizaci. Pro nemocného musí být proto vybrána ta nejvhodnější konkrétní derivace, „na míru“.
Výběr vhodné derivace závisí na celkovém a onkologickém stavu pacienta, na jeho přáních a očekávání a v neposlední řadě na osobních zkušenostech operatéra. Funkční výsledky všech derivací jsou při správně zvoleném typu srovnatelné a závisí na správně provedené cystektomii a pečlivé rekonstrukci.
doc. MUDr. Ladislav Jarolím, CSc.
Urologická klinika UK, 2. LF a FN Motol, Praha
ladislav.jarolim@lfmotol.cuni.cz
Sources
1. Simon J. Ectopia vesicae (absence of the anterior walls of the bladder and pubis abdominal parieties); operation for directing the orifices of the ureters into the rectum; temporary success; subsequent death; autopsy. Lancet 1852; 2 : 568–570.
2. Maydl K. Prvé případy radikálního léčení rozštěpeného měchýře. čas Lék čes 1894; 33 : 337–343.
3. Maydl K. Neue Beobachtungen von Ureterenimplantaionen in die Flexura romana bei Ectopia vesicae. Wien med Wschr 1896; 46 : 1241, 1333–1373.
4. Maydl K. Über eine neue Methode zur Ausführung der Jejunostomie und Gastroenterostomie. Wien med Wschr 1892; 42 : 697–741.
5. Pawlík K. Exstirpace močového měchýře. čas Lék čes 1890; 29 : 705–706.
6. Hradec E. Chirurgische Behandlung der Strahlenschäden an der weiblichen Harnblase. Urol Int 1962; 14 : 89–110.
7. Jarolím L, Babjuk M, Hanuš T, Janský M, Skřivanová V. Ortotopická náhrada močového měchýře u ženy po cystektomii se zachováním funkční uretry. Rozhl Chir 1996; 75 : 222–226.
8. L Jarolím L, Babjuk M, Hanuš T, Janský M. 20 orthotopic neobladders in females. Eur Urol 1996; 30(suppl2): 264.
9. Jarolím L, Babjuk M, Hanuš T, Janský M, Skřivanová V. Female urethra sparing cystectomy and orthotopic bladder replacement. Eur Urol 1997; 31(2): 173–177.
10. Bricker EM. Bladder substitution after pelvic evisceration. Surg Clin North Am 1950; 30 : 1511–1521.
11. Thüroff JW, Alken P, Riedmiller H, Jacobi GH, Hohenfellner R. 100 cases of mainz-pouch (mixed augmentation ileum 'n zecum) for bladder augmentation and continent urinary diversion. World J Urol 1985; 3(3): 179–184.
12. Jarolím L. Kontinentní ileocékální měchýř (Mainz pouch). Rozhl chir 1988; 67 : 625–632.
13. Hinman F jr. Pascal, Laplace and a length of bowel. J Urol (Paris) 1989; 95 : 11–14.
14. Hautmann RE. The ileal neobladder to the female urethra. Urol Clin North Am 1997; 24 : 827–835.
15. Jarolím L. Le Ducova implantace ureterů do neoveziky. Rozhl Chir 1989; 68 : 714–717.
16. Skinner DG, Boyd SD, Lieskovsky G, Bennett C, Hopwood B. Lower urinary tract reconstruction following cystectomy: experience and results in 126 patients using the Kock ileal reservoir with bilateral ureteroileal urethrostomy. J Urol 1991; 146(3): 756–760.
17. Studer UE, Danuser H, Merz VW, Springer JP, Zingg EJ. Experience in 100 patients with an ileal low pressure bladder substitute combined with an afferent tubular isoperistaltic segment. J Urol 1995; 154(1): 49–56.
18. Jarolím L, Babjuk M. Biopsie prostatické uretry před radikální cystoprostatektomií a biopsie hrdla močového měchýře před radikální cystektomií. Endoskopie 1996; 5 : 24–26.
19. Studer UE, Danuser H, Thalmann GN, Springer JP, Turner WH. Antireflux nipples or afferent tubular segments in 70 patients with ileal low pressure bladder substitutes: long-term results of a prospective randomized trial. J Urol 1996; 156(6): 1913–1917.
20. Studer UE, Danuser H, Hochreiter W, Springer JP, Turner WH, Zingg EJ. Summary of 10 years' experience with an ileal low-pressure bladder substitute combined with an afferent tubular isoperistaltic segment. World J Urol 1996; 14(1): 29–39.
21. Elmajian DA, Stein JP, Esrig D, Frieman JA, Skinner EC, Boyd SD, Lieskovsky G, Skinner DG. The Kock ileal neobladder: updated experience in 295 male patients. J Urol 1996; 156(3): 920–925.
22. Ghoneim MA, Shaaban AA, Mahran MR, Kock NG. Further experience with the urethral Kock pouch. J Urol 1992; 147(2): 361–365.
23. Smith E, Yoon J, Theodorescu D. Evaluation of urinary continence and voiding function: early results in men with neo-urethral modification of the Hautmann orthotopic neobladder. J Urol 2001; 166 : 1346 – 1349.
24. Ghoneim MA. Orthotopic bladder substitution in women following cystectomy for bladder cancer. Urol Clin North Am 1997; 24(1): 225–239.
25. Jarolím L, Babjuk M, Hanuš T, Janský M. Maturition of the bladder replacement in the female. Brit J Urol 1997; 80 : 343.
26. Jarolím L, Babjuk M, Hanuš T, Janský M, Grim M, Naňka O, Povýšil C. Treatment of urinary retention in females with the orthotopic bladder replacement. Eur Urol 1999; 35 : 106.
27. Jarolím L, Babjuk M, Hanuš T, Janský M, Grim M, Naňka O, Povýšil C. Functional evaluation of orthotopic bladder replacement in females. Eur Urol 2000; 37(suppl2): 455.
28. Jarolím L, Babjuk M, Pecher M, Grim M, Naňka O, Tichý M, Hanuš T, Janský M. Causes and treatment of residual urine volume after orthotopic bladder replacement in women. Eur Urol 2000; 38(6): 748–752.
29. Jarolim L, Stenzl A, Coloby P, Golia S, Babjuk M, Bartsch G, Kakizoe T, Robertson Ch. Functional and urodynamic outcomes in orthotopic urinary diversion in women - multiinstitutional study. Eur Urol 2001; 39(5): 72.
30. Jarolim L, Babjuk M, Stenzl A, Bartsch G, Coloby P, Golia S, Kakizoe T, Robertson Ch. Multicentric study on functional and urodynamic outcomes in orthotopic urinary diversion in females with pelvic malignancy. J Urol 2001; 165(87): 353.
31. Stenzl A, Jarolim L, Coloby P, Golia S, Bartsch G, Babjuk M, Robertson Ch. Urethra-sparing cystectomy and orthotopic urinary diversion in women with malignant pelvic tumors. Cancer 2001; 92 : 1865–1871.
32. Stenzl A, Jarolim L, Coloby P, Golia S, Bartsch G, Babjuk M, Robertson Ch. European experience with urethra-sparing cystectomy and orthotopic urinary diversion in women: oncological outcome. Eur Urol 2001; 39(5): 145.
33. Stenzl A, Bartsch G, Jarolím L, Babjuk M, Coloby P, Golia S, Robertson Ch. Kakizoe T. Oncological outcome in women with an orthotopic neobladder to the urethra. J Urol 2001; 165(87): 356
34. Jarolím L, Babjuk M, Hanuš T, Janský M, Skřivanová V. Kontinentní močová derivace s použitím detubulizovaného rektosigmatu (sigma-rectum pouch). čas Lék čes 1996; 135 : 664–667.
35. Mitrofanoff P. Cystostomie continent transappendiculaire dans le traitement des vessies neurologiques. Chir Pediatr 1980; 21 : 297–305.
36. Monti PR, Lara RC, Dutra MA, de Carvalho JR. New techniques for construction of efferent conduits based on the Mitrofanoff principle. Urology 1997; 49 : 112–114.
37. Goodwin WE, Harris AP, Kaufman JJ, Beal JM. Open, transcolonic ureterointestinal anastomosis; new approach. Surg Gynekol Obstet 1953; 97 : 295–300.
38. Hohenfellner R. Ureterosigmoidostomy - Revisite. Akt Urol 1990; 21 : 63–66.
39. Fisch M, Hohenfellner R. Der Sigma-Rektum Pouch: eine Modifikation der Harnleiterdarmimplantation. Akt Urol 1991; 22 : 1–9.
40. Fisch M, Wammack R, Mueller SC, Hohenfellner R. The MAINZ pouch II (Sigma-rectum pouch) J Urol 1993; 149(2): 258–263.
41. Jarolím L, Babjuk M, Hanuš T, Janský M, Skřivanová V. Kontinentní močová derivace s použitím detubulizovaného rektosigmatu (sigma-rectum pouch) čas Lék čes 1996; 135 : 664–667.
42. Jarolím L, Babjuk M, Hanuš T, Janský M. One layer suture in Mainz pouch II - 50 cases. Eur Urol 1996, 30 : 755.
43. Gumus E, Miroglu C, Saporta L, Basaran G, Horasanli K, Tanriverdi O, Karadag H. Rectodynamic and radiological assessment in modified mainz pouch II cases. Eur Urol 2000; 38(3): 316–322.
44. Pajor L, Kelemen Z. Our experience with the Mainz pouch II: 40 patients; follow-up and complications. Ann Urol (Paris) 1995; 29(4): 246–9.
45. Fisch M, Wammack R, Hohenfellner R. The sigma - rectum pouch (Mainz pouch II). World J Urol 1996; 14 : 68–72.
46. Öbek C, Kural AR, Ataus S, Coskuner E, Demirkesen O, Çitçi A, Önder AU, Solok V: Complications of the Mainz Pouch II (Sigma-Rectum Pouch). E Urol 2001; 39(2): 204–211.
47. Hadzi-Djokic JB, Basic DT. A modified sigma-rectum pouch (Mainz pouch II) technique: analysis of outcomes and complications on 220 patients. BJU International 2006; 97(3): 587–591.
48. Kawaciuk I, Jarolím L. Motolský „sigma - rectum pouch“. In: Abrahámová J. Vybrané otázky onkologie VI. Praha: Galén 2002 : 40.
49. Jarolím L, Schmidt M, Hyršl L, Hanek P, Dušek P, Rejchrt M, Kaliská V, Chocholatý M, Kawaciuk I. Rekonvalescence pacientů po derivaci Motol-pouch. In: Abrahámová J. Vybrané otázky onkologie X. Praha: Galén 2006 : 21–23.
50. Hinman F, Weyrauch HM. A critical study of the different principles of surgery which have been used in ureterointestinal implantation. Trans Am Assoc Genitourin Surg 1936; 29 : 15–156.
51. Montie JE. Ileal conduit diversion after radical cystectomy: pro. Urology 1997; 49 : 659–662.
52. Hirokawa M, Iwasaki A, Yamazaki A, Asakura S, Nozaki A, Yamagishi T. Improved technique of tubeless cutaneous ureterostomy and results of permanent urinary diversion. Eur Urol 1989; 16(2): 125–132.
53. Puppo P, Perachino M, Ricciotti G, Bozzo V. Laparoscopic bilateral cutaneous ureterostomy for palliation of ureteral obstruction caused by advanced pelvic cancer. J Endourol 1994; 8 : 425–428.
54. Jarolím L, Babjuk M, Hanuš T, Novák K. Komplikace močové derivace po cystektomii pro karcinom měchýře. Rozhl Chir 1997; 76 : 425–428.
55. Stampfer DS, McDougal WS. Inhibition of the sodium/hydrogen antiport by ammonium ion. J Urol 1997; 157(1): 362–365.
56. Jarolím L, Horák L, Marek J. Adenokarcinom ureteroenetrické anastomózy a úloha endoskopie v mezioborové spolupráci. Endoskopie 1992; 1 : 11–12.
57. Arnett TR, Dempster DW. Effect of pH on bone resorption by rat osteoclasts in vitro. Endocrinology 1986; 119 : 119–124.
58. Lee SW, Russell J, Avioli LV. 25-Hydroxycholecalciferol to 1,25-dihydroxycholecalciferol: conversion impaired by systemic metabolic acidosis. Science 1977; 195(4282): 994–996.
59. Bettice JA, Gamble JL. Skeletal buffering of acute metabolic acidosis. Am J Physiol 1975; 229(6): 1618–1624.
60. McDougal WS, Koch MO, Shands C. Bony demineralization following urinary intestinal diversion. J Urol 1988; 140(4): 853–855.
61. Bushman W, Howards SS. The use of urea for dissolution of urinary mucus in urinary tract reconstruction. J Urol 1994; 151(4): 1036–1037.
62. Hautman RE, Abol-Enein H, Hafez K, Haro I, Mansson W, Mills RD, Montie JD, Sagalowski IA, Stein JP, Stenzl A, Studer UE, Volkmer BG. Urinary diversion. Urology 2007; 69(suppl1): 17–49.
63. Madersbacher S, Studer UE. Contemporary cystectomy and urinary diversion. World J Urol 2002; 20(3): 151–157.
Labels
Paediatric urologist Urology
Article was published inUrological Journal

2008 Issue 2-
All articles in this issue
- Current practice in the management of superficial bladder cancer in the Netherlands and Belgian Flanders: a survey
- Non-invasive blader cancer carcinoma – when should we start adjuvant intravesical instillation therapy and what to do in case of failure?
- Management of BCG failures in superficial bladder cancer
- The role and the extent of lymphadenectomy in patients with bladder cancer
- Sexual function sparing radical cystectomy
- Complications of cystectomy and urinary diversion
- Urinary diversion after cystectomy
- The indiana pouch, past and present
-
TVT – nová epocha urogynekologické operativy
Současná urogynekologická operativa II
- Urological Journal
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Non-invasive blader cancer carcinoma – when should we start adjuvant intravesical instillation therapy and what to do in case of failure?
- Urinary diversion after cystectomy
- Complications of cystectomy and urinary diversion
- Sexual function sparing radical cystectomy
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

