-
Medical journals
- Career
Zhodnocení výsledků embolizace sleziny u pacientů s polytraumatem – 4leté zkušenosti
Authors: Jan Kovařík 1; Martin Kocher 2; Igor Čižmář 1; Ján Palčák 1
Authors‘ workplace: Oddělení traumatologie, Fakultní nemocnice Olomouc 1; Radiologická klinika, Fakultní nemocnice Olomouc 2
Published in: Úraz chir. 21., 2013, č.1
Overview
ÚVOD:
Konzervativní terapie je nyní standardním přístupem u hemodynamicky stabilních pacientů po tupém poranění sleziny. Rozšiřující se využití angioembolizačních metod, jako doplňkové metody, zvyšuje pravděpodobnost úspěšné konzervativní terapie.CÍL:
Cílem práce je prezentovat výsledky souboru pacientů po embolizaci pro krvácení ze sleziny po tupém poranění břicha.METODIKA:
Zhodnocení souboru pacientů ošetřených angioembolizací pro krvácení po tupém poranění sleziny v Traumacentru FN Olomouc v časovém období 01/08 – 01/12. Předmětem hodnocení byla demografická data, typ embolizační techniky, stupeň poranění sleziny a četnost a tíže výskytu komplikací.VÝSLEDKY:
Do souboru bylo zařazeno 9 pacientů s průměrným věkem 37,3 let. Průměrný stupeň poranění sleziny byl dle AAST klasifikace 2.8. Všichni pacienti byli indikováni k angioembolizaci na základě průkazu aktivního krvácení na CT vyšetření. U všech byla provedena metoda distální embolizace. U žádného pacienta nebyla nutná konverze k otevřené revizi dutiny břišní. Zaznamenali jsme 1 velkou a 5 malých komplikací. Z velkých komplikací došlo 1x k postkontrastní nefropatii s nutností překlenovací dialýzy. Z malých komplikací byl zaznamenán 2x nález fluidothoraxu (1x s nutností punkce), 2x přítomnost febrilií bez zjištěného infekčního zdroje a 1x disekce kmene lineální arterie mikrospirálou (s dalším průběhem bez následků). Celkový výskyt komplikací byl 66.6 %. Žádná z komplikací nevedla k trvalým následkům, u žádného pacienta nebyla nutná konverze na otevřený výkon.ZÁVĚR:
Embolizace je účinná a bezpečná technika zlepšující výsledky konzervativní terapie po tupém poranění sleziny a nahrazuje tak dříve široce indikovanou splenektomii.Klíčová slova:
embolizace, poranění sleziny, komplikace.ÚVOD
Poranění sleziny je nejčastější příčinou hemoperitonea po tupém poranění dutiny břišní. Jako nejčastější mechanizmus jsou uváděny vysokoenergetické úrazy, mezi nimiž dominují autonehody, pády z výšek či napadení. Druhým typickým mechanizmem jsou pády a nárazy na prominující předměty s energií koncentrovanou na oblast levého hypochondria. Otevřená poranění jsou méně častá a vznikají většinou jako následek střelných poranění. Poranění sleziny může být solitárním nálezem, či jako součást polytraumatu [17].
Dříve standardní revize dutiny břišní pro nález hemoperitonea s následnou splenektomií byla preferovanou metodou ošetření poraněné sleziny. Tento postup obhajovaný obavami z recidivy možného fatálního krvácení doznal změny po představení úspěšné konzervativní léčby u pediatrických pacientů [24]. Důvodem hledání nových terapeutických směrů byl výskyt těžkých postsplenektomických sepsí (OPSI - Overhelming Post Splenectomy Infection) u dětských pacientů. Postiženy byly převážně děti do 2 let, protože protilátková odpověď proti opouzdřeným patogenům se tvoří až v pozdějším věku [2]. Riziko vzniku infektu je obdobné pro dospělé i dětské pacienty a pohybuje se kolem 3.2 %. Avšak incidence následného úmrtí pro vzniklý septický stav je větší o 0.4 % u dětí (1.7 versus 1.3 %) [1]. Riziko vzniku OPSI je větší u pacientů po splenektomii z hematologické indikace, nežli u úrazové splenektomie [14]. Jako alternativu mezi radikální splenektomií a konzervativní léčbou lze nalézt v literatuře řadu zdokumentovaných více či méně úspěšných alternativ – parciální splenektomie, splenografie, autotransplantace slezinné tkáně, tkáňová lepidla [24].
Po představení uspokojivých výsledků konzervativní terapie poraněné sleziny u dětí došlo přibližně před 25 lety k postupné implementaci neoperačního postupu i do algoritmů léčby poraněné sleziny u dospělých pa-cientů [17, 24].
MATERIÁL
Retrospektivně jsme zhodnotili soubor 9 pacientů ošetřených v Traumacentru FN Olomouc pro tupé poranění dutiny břišní s následnou angioembolizací a. lienalis v období 01/2008 – 01/2012. Z toho 6 mužů a 3 ženy. Průměrný věk byl 37.3 let (rozmezí 7-64 let). Průměrné ISS skóre bylo 20.1 (16-41).
METODIKA
Z počítačového nemocničního systému byly získány tyto informace: věk, pohlaví, vstupní ISS, mechanizmus úrazu, významná přidružená onemocnění, vstupní hodnota HGB délka pobytu ve FN Olomouc a komplikace spjaté s výkonem embolizace.
Byly zhodnoceny a klasifikovány výsledky CT vyšetření. Stupeň poranění byl hodnocen dle AAST klasifikace [23].
Table 1. Klasifikace poranění sleziny dle AAST 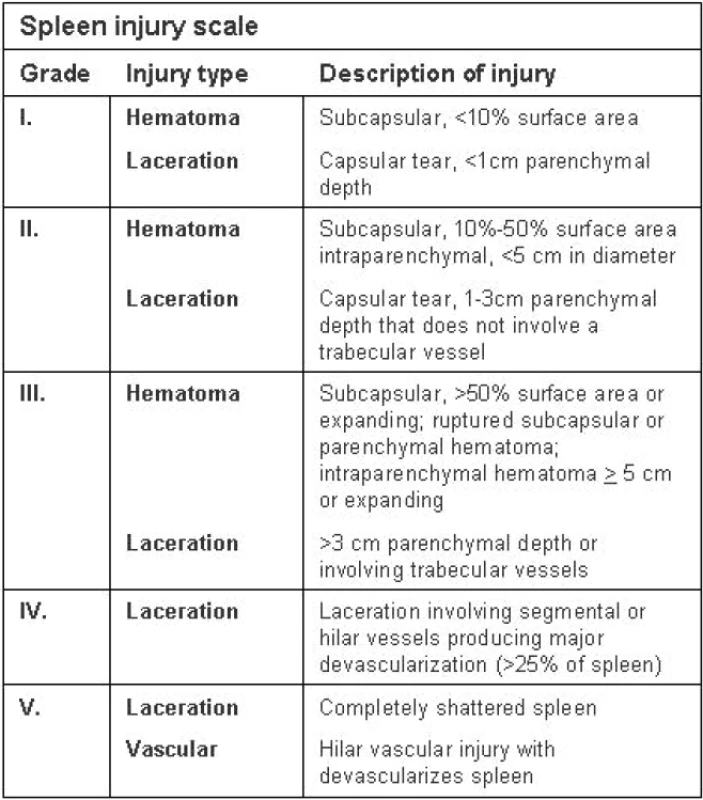
Obr. 1a: Muž 32 let - poranění sleziny s aktivním krvácením – IV. stupeň dle AAST 
Obr. 1b: Žena 40 let - poranění sleziny s aktivním krvácením – III. st. dle AAST 
Na CT byla hodnocena i velikost hemoperitonea, vycházející z pracovní klasifikace Peitzmanovy práce [15]. Nález perisplenického hematomu byl hodnocen jako malé hemoperitoneum. U středního hemoperitonea byla popsána perikolická kolekce krve a přítomnost volné krve v oblasti pánve byla hodnocena jako velké hemoperitoneum [15]. K hodnocení hemodynamické stability bylo použito skórování z Peitzmanovy práce, ve které byli pacienti rozděleni na stabilní (TK> 90 mmHg a P <112/min), s odpovědí na parenterální příjem většího množství tekutin (1-2 epizody TK <90mmHg nebo P>112/min) a na nestabilní (TK<90mm Hg nebo P>112/min) [15]. Nutnost revize dutiny břišní pro pokračující krvácení ze slezinné arterie byla hodnocena jako selhání konzervativní terapie.
Ve sledovaném období neexistoval protokol pro jednotlivé kroky konzervativní terapie poraněné sleziny včetně indikačních kritérií pro angioembolizační výkon. Intervenční výkon byl indikován dle rozhodnutí vedoucího traumatologa na podkladě hemodynamické stability a nálezu na CT. Samotný výkon byl proveden intervenčním radiologem na angiografickém či posléze hybridním sále. K embolizaci byly nejčastěji použity mikrospirálky Tornado®. Proximální embolizace byla definována jako uzavření hlavní slezinné tepny. Distální embolizace byla definována jako uzavření jednoho a více větví hlavního kmene slezinné arterie. Profylaktické podání ATB bylo indikováno dle přidružených poranění.
Komplikace byly rozděleny na malé a velké. Mezi velké komplikace byly zařazeny následky embolizace, které by mohly výrazně zhoršit stav pacient či vést k jeho smrti. Jako malé komplikace byly definovány stavy po embolizaci neohrožující život pacienta [3].
VÝSLEDKY
Během pětiletého sledovaného období bylo embolizací slezinné tepny ošetřeno 10 pacientů. Ze sledovaného souboru byl vyloučen jeden pacient, u kterého byla embolizace použita jako následné řešení recidivujícího krvácení z pahýlu a. lienalis po akutní splenektomii. Nejčastější příčinou úrazu byl pád z kola, dále pak pád na předmět (roh branky, květináč).
Osm pacientů bylo bez významných přidružených onemocnění, pouze jeden pacient byl dlouhodobě sledován s polycythaemia vera se sekundární splenomegalii. Průměrný stupeň poranění dle AAST byl 2.8 (4 pacienti II. stupeň, 3 pacienti III. stupeň, 2 pacienti IV. stupeň) . U tří pacientů byl nález velkého hemoperitonea, u čtyř byla velikost hemoperitonea hodnocena jako střední a u dvou jako malé hemoperitoneum.
Všichni pacienti splňovali kritéria hemodynamické stability, v našem souboru jsme nezaznamenali nestabilní či dočasně nestabilní pacienty. U všech pacientů byl na CT nález aktivního krvácení v místě poraněné sleziny. Nebyly nalezeny další patologie ve smyslu AV fistuly či pseudoaneurysmatu. Průměrná hodnota vstupního hemoglobinu byla 121 g/l (99-149g/l).
U všech pacientů byla provedena distální selektivní embolizace.
Obr. 2a, b: Příklad distální selektivní embolizace střední třetiny a distálního pólu sleziny 
Žádný pacient nepodstoupil proximální embolizaci. Průměrný čas od převzetí pacienta na urgentním příjmu po provedení akutní angiografie byl 2.5 hodiny. Z hodnocení tohoto parametru byl vyloučen jeden pacient, u něhož byla provedena odložená embolizace s odstupem 4 dní pro recidivu krvácení ze sleziny primárně léčenou konzervativně bez intervenčních metod. Průměrná délka hospitalizace byla 16.8 dne (4-45 dní).
Z velkých komplikací došlo 1x k ledvinnému selhání po podání kontrastní látky s nutností překlenující dialýzy. Z malých komplikací byl zaznamenán 2x nález fluidotoraxu (1x s nutností punkce), 2x přítomnost febrilií bez zjištěného infekčního zdroje, 1x disekce kmene lineální arterie mikrospirálou (s dalším průběhem bez následků). Výskyt malých komplikací byl 55 %, Celkový výskyt komplikací byl 66,6 %.
U žádného pacienta nedošlo k selhání konzervativní terapie ve smyslu nutnosti terapeutické laparotomie.
DISKUZE
Terapeutický protokol ošetření sleziny po tupém poranění, respektující nejnovější vědecké poznatky, významně usnadňuje a zrychluje rozhodnutí při péči o poraněné pacienty [5]. Vstupním vyšetřením u pacientů po vysokoenergetickém úrazu je ultrazvukové vyšetření (FAST – Focused Assessment Sonography in Trauma), které umožní rychlé rozpoznání přítomnosti volné tekutiny v dutině břišní. Alternativou, užívanou mimo ČR a nyní spíše opouštěnou pro svou invazivitu a možné komplikace, je diagnostická peritoneální laváž [25]. Poranění sleziny u hemodynamicky nestabilního pacienta je indikací k akutní revizi dutiny břišní [21]. Další indikací k urgentní laparotomii u pacientů s poraněnou slezinou jsou klinické známky peritonitidy s podezřením na poranění trávicího traktu a přítomnost jiného intraperitoneálního či retroperitoneálního poranění vyžadujícího akutní intervenci [7]. U hemodynamicky stabilního pacienta stanovíme rozsah slezinného poranění prostřednictvím CT vyšetření [6, 12, 16, 20, 25]. Provedení angiografie s event. embolizací je doporučeno jako součást konzervativní terapie u stabilních pacientů s poraněním sleziny III.-V. stupně dle AAST, v případě aktivního krvácení, u pseudoaneurysmatu slezinné tepny a u středně velkého hemoperitonea [20]. Slezinnou tepnu lze embolizovat dočasně prostřednictvím pěny (Gelfoam) či trvale pomocí mikrospirálek (coiling) [10, 11]. Krevní zásobení sleziny s dostatečnou sítí kolaterálních cév umožňuje embolizovat buď hlavní slezinnou tepnu – proximální embolizace, nebo selektivně jednotlivé krvácející větve – distální embolizace [10, 11]. Jedna z prvních terapeutických embolizací lienální arterie byla popsána Sclafanim v roce 1980 [18]. V české literatuře je popsána první zmínka o terapeutických embolizacích úrazových krvácení po tupých poraněních dutiny břišní a retroperitonea z roku 2012 [10].
Další terapie pacienta předpokládá intenzivní klinické sledování, s pravidelnými ultrazvukovými kontrolami lokálního nálezu, a dále s kontrolami krevního tlaku (TK) a krevního obrazu [7, 20]. Některé práce doporučují provedení kontrolního CT za 24-48 hodin po výkonu u pacientů s III. a vyšším stupněm poranění k odhalení vzniku pozdních aneuryzmat, která bývají zdrojem recidiv krvácení [27]. První sporadické výzkumy kvality humorální a buněčné imunity u pacientů po embolizaci nenacházejí rozdíly v měřitelných parametrech vůči zdravé populaci [26].
V našem velmi malém a poměrně heterogenním souboru pacientů paradoxně nedominovala vysokoenergetická traumata, jak uvádějí ostatní autoři, ale spíše úrazy s menší energií, což je možné přičíst i postupnému zavádění této metody do praxe s výběrem méně komplikovaných pacientů.
Terapeutický algoritmus jednotlivých pacientů ve studii, kromě indikace k provedení embolizace u aktivního tepenného krvácení, postrádal jednotný protokol. Fata ve své práci z roku 2004 postuluje nutnost jednotného protokolu v terapii poranění dutiny břišní jako prevenci zbytečných splenektomií či jako jednoduchý návod k indikaci intervenčního výkonu [5]. Chybějící protokol vede až k 12% riziku indikace splenektomie u pacientů, které je možné léčit angioembolizací [19].
Nález tepenného krvácení v oblasti sleziny byl dominantním faktorem indikujícím pacienty k provedení angiografie s následnou embolizací, což splňuje jedno z hlavních indikačních doporučení vzešlých z meta-analýzy vytvořené Stassenem v roce 2012. Tato metaanalýza reviduje quidelines vytvořená EAST (Eastern Association for the Surgery of Trauma practice) z roku 2003 a na podkladě nových 124 od té doby publikovaných prací upřesňuje doporučení [20]. V našem souboru jsme neměli pacienta, u kterého by byla provedena pouze angiografie bez následné terapeutické embolizace. Jedním z důvodů je již zmiňovaný malý soubor pacientů a také selekce pacientů s jednoznačným krvácením na CT. Haanova práce potvrzuje, že nadužívání angiografie bez nutnosti embolizace i u pacientů s I. či II. stupněm poranění nezlepšuje terapeutický výsledek, ale významně se podílí na zvyšování nákladů za péči o pacienta [7].
Rozhodnutí o lokalizaci provedené embolizace je závislé na angiografickém nálezu a na zručnosti intervenčního radiologa. Provedení proximální embolizace neboli „endovaskulární podvaz“ je vnímáno jako alternativa chirurgické intervence zachovávající slezinu u pacientů s těžkou lacerací sleziny, krvácení z více tepen a difuzního krvácení. Distální selektivní embolizace při poranění malého množství periferních větví lineální arterie vede k zachování většího množství funkčního parenchymu sleziny a minimalizuje rizika vzniklá příliš proximální embolizací vedoucí k nekrózám pankreatu či stěny žaludku. Hlavní nevýhodou je časová náročnost prováděného výkonu u polytraumatizovaného pacienta [9, 10, 11].
První práce popisující imunologické důsledky angioembloizace nenachází signifikantní rozdíl proti zdravé populaci. Nedostatkem je zatím malé množství studií, retrospektivní hodnocení, malé a heterogenní soubory hodnocených pacientů s distální nebo proximální embolizací a polymorfnost imunitního systému a tudíž jeho obtížná měřitelnost.
Průměrná doba hospitalizace se odvíjela od tíže přidružených poranění. Rozhodujícími kritérii pro vertikalizaci, realimentaci a propuštění pacienta byly výsledky kontrolních zobrazovacích a laboratorních vyšetření. Dózování zátěže, indikování kontrolních vyše-tření a zobrazovacích metod bylo vždy v rukou ošetřujícího lékaře na ambulanci. V dostupné literatuře jsme nenalezli protokol pooperační péče pro dospělé pa - cienty, týkající se dávkování zátěže a návratu ke sportu. Pranikoff sledoval 25 dětí s různým stupněm poranění sleziny po konzervativní terapii. Dle CT s odstupem 6 týdnů bylo 77 % slezin lehkého (I.a II. stupeň), ale jen 8 % těžkého stupně (III.-V.) plně zhojeno. Tento výsledek, ale nezměnil postup v podobě 3měsíčního klidu s následným návratem k plné aktivitě [16].
Komplikace vzniklé při konzervativní terapii jsou specifické pro jednotlivé kroky terapeutického algoritmu. Je popisováno přibližně 0,3% riziko poranění dutých orgánů při tupém poranění břicha [4]. U pacientů s poraněním parenchymatózního orgánu a Abbreviated Injury Score (AIS) více jak 2 je riziko 9.6 % současného poranění i dutých orgánů dutiny břišní [13]. Komplikace vázané na samotné provedení angioembolizačního výkonu lze rozdělit na velké a malé. Mezi velké patří recidiva krvácení, slezinný absces, postkontrastní nefropatie, akutní pankreatitida a infarkt sleziny. Mezi malé komplikace řadíme horečky, pleurální výpot-ky či migraci embolizačních spirál [6, 9, 11, 17, 20].
Hahn a kol. ve své multicentrické studii popsal 20 % riziko vzniku velkých komplikací a 23 % riziko vzniku malých komplikací. Jako nejčastější komplikace byly popsány slezinné abscesy a recidiva krvácení [8]. V našem souboru hodnotíme jako velkou komplikaci vznik postkontrastní nefropatie vzniklé s odstupem 2 dní s nutností akutní dialýzy s následnou úpravou stavu a renálních funkcí. Lze jen špatně posoudit jaký vliv měla na tuto komplikaci opakovaná kontrastní CT vyšetření indikovaná pro poranění mozku. Nižší vznik postkontrastních nefropatií po angiografických výkonech je připisován užívání nízkoosmolárnímch kontrastních látek [22]. K malým komplikacím jsme po vzoru Ekehovy práce zařadili výskyt teplot, vedoucí k nutnosti dalšího diagnostického došetřování a prodloužení hospitalizace [3]. Teploty u všech pacientů v našem souboru spontánně odezněly bez nutnosti dalších intervencí. Další z malých komplikací byl 2x nález fluidothoraxu, jedenkrát s jednorázovou nutností punkce u sedmiletého pacienta.
Angioembolizace se postupně stává jednou z arzenálu zbraní použitelných v boji s tupým poraněním dutiny břišní. S postupným zařazováním této metody do klinické praxe se objevuje množství nově vzniklých otázek týkajících se dalšího sledování pacienta po výkonu, vlivu výkonu na imunitu a nutnosti vakcinace. Souhrn těchto vědeckých cílů je shrnut v práci Stassena a kolektivu [20].
Hlavní nedostatky studie představuje retrospektivita, heterogenita, malý soubor a chybějící srovnávací soubor pacientů.
ZÁVĚR
Zhodnocení výsledků na našem malém souboru pacientů potvrzuje, že embolizace je účinná a bezpečná metoda konzervativní terapie tupého poranění sleziny, nahrazující tak u hemodynamicky stabilních pacientů dříve široce prováděnou splenektomii.
MUDr. Jan Kovařík
jan.kovarik@email.cz
Sources
1. BISHARAT, N. et al. Risk of infection and death among post-splenectomy patients. The Journal of infection. 2001-10, 43, 182–186. PMID: 11798256. DOI: 10.1053/jinf.2001.0904.
2. DI CATALDO, A. et al. Splenic trauma and overwhelming postsplenectomy infection. The British journal of surgery. 1987, 74, 343–345. PMID: 3297232.
3. EKEH, A. P. et al. Complications arising from splenic embolization after blunt splenic trauma. American journal of surgery. 2005, 189, 335–339. PMID: 15792763. DOI: 10.1016/j.amjsurg.2004.11.033.
4. FAKHRY, S. M., WATTS, D. D., LUCHETTE, F. A. Current diagnostic approaches lack sensitivity in the diagnosis of perforated blunt small bowel injury: analysis from 275,557 trauma admissions from the EAST multi-institutional HVI trial. The Journal of Trauma and Acute Care Surgery. 2003, 54, 295–306.
5. FATA, P., ROBINSON, L., FAKHRY, S. M. A survey of EAST member practices in blunt splenic injury: a description of current trends and opportunities for improvement. The Journal of Trauma and Acute Care Surgery. 2005, 59, 836–842.
6. GALVAN, D. A., PEITZMAN, A. B., Failure of nonoperative management of abdominal solid organ injuries. Current Opinion in Critical Care. 2006, 12, 590–594. DOI: 10.1097/MCC.0b013e328010d4ad.
7. HAAN, J. M. et al. Nonoperative management of blunt splenic injury: a 5-year experience. The Journal of trauma. 2005, 58, 492–498. PMID: 15761342.
8. HAAN, J. M. et al. Splenic embolization revisited: a multicenter review. The Journal of trauma. 2004, 56, 542–547. PMID: 15128125.
9. HAMERS, R. L., VAN DEN BERG, F. G., GROENEVELD, A. B. J. Acute necrotizing pancreatitis following inadvertent extensive splenic artery embolisation for trauma. British Journal of Radiology. 2009, 82, e11–e14. DOI: 10.1259/bjr/92246530.
10. KOCHER M. et al. Akutní endovaskulární výkony u poranění parenchymových orgánů dutiny břišní, retroperitonea a pánve. Ces Radiol. 2012, 66, 153–158.
11. LOPERA, J. E. Embolization in Trauma: Principles and Techniques. Seminars in Interventional Radiology. 2010, 27, 14–28. PMID: 21359011PMCID: PMC3036510. DOI: 10.1055/s-0030-1247885.
12. MAYGLOTHLING, J. A., HAAN, J. M., SCALEA, T. M. Blunt Splenic Injuries in the Adolescent Trauma Population: The Role of Angiography and Embolization. The Journal of Emergency Medicine. 2011, 41, 21–28. DOI: 10.1016/j.jemermed.2008.10.012.
13. NANCE, M. L. et al. Solid viscus injury predicts major hollow viscus injury in blunt abdominal trauma. The Journal of trauma. 1997, 43, 618–622; discussion 622–623. PMID: 9356057.
14. OKABAYASHI, T., HANAZAKI, K. Overwhelming postsplenectomy infection syndrome in adults - A clinically preventable disease. World Journal of Gastroenterology: WJG. 2008, 14, 176–179. PMID: 18186551PMCID: PMC2675110. DOI: 10.3748/wjg.14.176.
15. PEITZMAN, A. B. et al. Failure of observation of blunt splenic injury in adults: variability in practice and adverse consequences. Journal of the American College of Surgeons. 2005, 201, 179–187. PMID: 16038813. DOI: 10.1016/j.jamcollsurg.2005.03.037.
16. PRANIKOFF, T. et al. Resolution of splenic injury after nonoperative management. Journal of pediatric surgery. 1994, 29, 1366–1369. PMID: 7807327.
17. RICHARDSON, J. D. Changes in the Management of Injuries to the Liver and Spleen. Journal of the American College of Surgeons. 2005, 200, 648–669. DOI: 10.1016/j.jamcollsurg.2004.11.005.
18. SCLAFANI, S. J. The role of angiographic hemostasis in salvage of the injured spleen. Radiology. 1981, 141, 645.
19. SHANMUGANATHAN, K. et al. Nonsurgical Management of Blunt Splenic Injury: Use of CT Criteria to Select Patients for Splenic Arteriography and Potential Endovascular Therapy1. Radiology. 2000, 217, 75–82.
20. STASSEN, N. A. et al. Selective nonoperative management of blunt splenic injury: an Eastern Association for the Surgery of Trauma practice management guideline. The journal of trauma and acute care surgery. 2012, 73, Suppl 4, S294–300. PMID: 23114484. DOI: 10.1097/TA.0b013e3182702afc.
21. STEIN, D. M., SCALEA, T. M. Nonoperative management of spleen and liver injuries. Journal of intensive care medicine. 2006, 21, 296–304. PMID: 16946445. DOI: 10.1177/0885066606290854.
22. STERNER, G., NYMAN, U. VALDES, T. Low risk of contrastmedium-induced nephropathy with modern angiographic technique. Journal of Internal Medicine. 2001, 250, 429–434. DOI: 10.1046/j.1365-2796.2001.00903.x.
23. TINKOFF, G. et al. American Association for the Surgery of Trauma Organ Injury Scale I: Spleen, Liver, and Kidney, Validation Based on the National Trauma Data Bank. Journal of the American College of Surgeons. 2008, 207, 646–655. DOI: 10.1016/j.jamcollsurg.2008.06.342.
24. UPADHYAYA, P. Conservative management of splenic trauma: history and current trends. Pediatric Surgery International. 2003, 19, 617–627. DOI: 10.1007/s00383-003-0972-y.
25. VYHNÁNEK, F. Postup při poranění břicha. Rozhledy v chirurgii. 2012, 91, 632–638.
26. WALUSIMBI, M. S. et al. Circulating cellular and humoral elements of immune function following splenic arterial embolisation or splenectomy in trauma patients. Injury. 2012, 43, 180–183. PMID: 21696725. DOI: 10.1016/j.
27. WEINBERG, J. A. et al. The utility of serial computed tomography imaging of blunt splenic injury: still worth a second look? The Journal of trauma. 2007, 62, 1143–1147; discussion 1147–1148. PMID: 17495714. DOI: 10.1097/TA.0b013e318047b7c2.
Labels
Surgery Traumatology Trauma surgery
Article was published inTrauma Surgery

2013 Issue 1-
All articles in this issue
- Intenzita a délka tkáňové ischemie těžce polytraumatizovaných pacientů v závislosti na délce přednemocniční péče, péče na urgentním příjmu a operačním čase registrované mikrodialýzou svalové tkáně
- Experimentální léčba diafyzárního kostního defektu využitím biodegradabilních materiálů a spongioplastiky a jejich srovnání
- Zhodnocení výsledků embolizace sleziny u pacientů s polytraumatem – 4leté zkušenosti
- Je přesné umístění zevního fixátoru loketního kloubu v ose rotace podstatné? Studie na kadaverech
- Trauma Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Experimentální léčba diafyzárního kostního defektu využitím biodegradabilních materiálů a spongioplastiky a jejich srovnání
- Zhodnocení výsledků embolizace sleziny u pacientů s polytraumatem – 4leté zkušenosti
- Je přesné umístění zevního fixátoru loketního kloubu v ose rotace podstatné? Studie na kadaverech
- Intenzita a délka tkáňové ischemie těžce polytraumatizovaných pacientů v závislosti na délce přednemocniční péče, péče na urgentním příjmu a operačním čase registrované mikrodialýzou svalové tkáně
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career


