-
Medical journals
- Career
Hyperbarická oxygenoterapie v léčbě těžkých traumat a drtivých poranění
Authors: Michal Hájek; Pavel Zonča *
Authors‘ workplace: Centre of Hyperbaric Medicine, Department of Anesthesiology and Resuscitation, City Hospital of Ostrava ; Chirurgické oddělení , Městská nemocnice Ostrava *; Department of Surgery, City Hospital of Ostrava Centrum hyperbarické oxygenoterapie, Anesteziologicko-resuscitační oddělení, Městská nemocnice Ostrava *
Published in: Úraz chir. 15., 2007, č.4
Overview
Úvod:
Principem hyperbarické oxygenoterapie je dýchání kyslíku za podmínek vyššího tlaku, než je tlak atmosférický. Metoda se užívá v léčbě více než dvou desítek onemocnění a patofyziologických stavů.Materiál a metodika:
Cílem práce je zhodnocení významu hyperbarické oxygenoterapie pro pacienty s akutní traumatickou ischémií a drtivým poraněním. Jedná se o retrospektivní observační studii výsledků léčby u všech pacientů s výše uvedeným postižením léčených v našem centru v roce 2005. V našem centru hyperbarické oxygenoterapie bylo od roku 1965 dosud léčeno přes 14 000 pacientů o celkovém množství 168 000 léčebných expozic. Dosud jsme léčili přes 2300 pacientů s těžkými úrazy. V roce 2005 bylo přijato k léčbě 40 pacientů, z toho 12 žen a 28 mužů o průměrném věku 47 let.Výsledky:
Léčba byla hodnocena úspěšně u 30 pacientů (76 %), u 5 pacientů (12 %) léčba k úspěchu nevedla, u 5 pacientů (12%) nebyla z různých důvodů dokončena dle plánu.Závěr:
Hyperbarickou oxygenoterapii považujeme za účinnou adjuvantní léčebnou metodu v rámci komplexního přístupu k traumatologickým pacientům. Metoda by měla být postupně rozšiřována a v indikovaných případech dostupná do 24 hodin od těžkého úrazu zejména v traumatologických centrech fakultních nemocnic.Klíčová slova:
hyperbarická oxygenace, ischémie, drtivé poranění.Úvod
Hyperbarická oxygenoterapie (dále HBO) je kauzální metoda v léčbě některých patologických stavů s rozhodujícím a významným ovlivněním průběhu onemocnění, komplikací, léčebného výsledku, mortality a kvality života. K těmto stavům patří otrava oxidem uhelnatým a kouřovými plyny, dysbarické poranění spojené s dekompresí, plynová embolie a klostridiová myonekróza.
U dalších dvou desítek stavů se jedná o léčebnou metodu, doplňující konzervativní nebo chirurgický léčebný postup. Význam HBO u těžkých úrazů končetin spojených s traumatickou ischémií, drtivým poraněním a kompartment syndromem je dostatečně známý a opakovaně prokázaný.
V mnoha experimentálních i klinických studiích bylo prokázáno, že úraz i rozsáhlý chirurgický výkon vedou k výraznému ovlivnění imunitního systému. Každé větší trauma je následováno významnou odezvou endokrinního systému, někdy doslova endokrinní „bouří“, která má za cíl, spolu s dalšími mechanismy, udržet homeostázu postiženého organismu při zajištění určitých priorit. Mezi endokrinním a imunitním systémem existuje významný dialog - různé buňky imunitního systému mohou nejen reagovat na některé hormony, cytokiny, ale mohou i řadu těchto látek „vyrábět“. Rozsáhlé polytrauma, podobně jako závažné popálení, představuje největší možnou stresovou odezvu (odezvu akutní fáze neboli systémovou zánětlivou odpověď), která má zajistit pro přežití postiženého:
- dostatečnou dodávku energie,
- dostatečnou dodávku aminokyselin pro nezbytné reparativní procesy,
- udržet vodní a elektrolytové hospodářství,
- udržet teplotní homeostázu,
- zajistit rychle reagující imunitní odezvu,
- tlumit, pokud je to možné, vnímání bolesti [3].
V časné fázi úrazu dochází k vystupňované zánětlivé odpovědi, charakterizované uvolněním tumor necrosis faktoru alfa (dále TNFa), cytokinů typu interleukin 1 a 6 (IL-1 a IL-6). Jsou aktivovány neutrofily, které ve zvýšené míře nasedají na endotel kapilár, současně dochází k nadměrnému „oxidativnímu burstu“ polymorfonuklárů (PMN) a makrofágů. Jedná se o prudké a nekontrolované zvýšení spotřeby kyslíku a tvorbu kyslíkových reaktivních substancí. Souběžně s výše uvedenými procesy jsou aktivovány a uvolňovány protizánětlivé mediátory, jako prostaglandiny E2 (PGE2) a IL-10. Toto vede k imunosupresi, projevující se deaktivací monocytů. Nerovnováha mezi pro a protizánětlivými cytokiny a imunokompetentními buňkami určuje průběh onemocnění a v budoucnu by detailní znalost imunitního stavu měla lékařům pomoci sestavit léčebnou strategii [6].
Na patofyziologii systémové odpovědi organismu na tkáňové poškození se kromě výše uvedených cytokinů a prostaglandinů podílí taktéž oxid dusnatý (NO). Bylo prokázáno, že HBO způsobuje utlumení tvorby cytokinů, TNF, endothelinu, snižuje hladinu transkripčních faktorů pro PGE2 a cyklooxygenázu 2 (COX-2). HBO naopak zvyšuje množství vaskulárního endoteliálního růstového faktoru (VEGF). Efekt HBO na tvorbu NO ještě nebyl zcela přesně objasněn a bude nutné provést další studie [1].
Kompartment syndrom
Je definován jako „stav, při kterém zvýšený tlak v omezeném myofasciálním prostoru zhoršuje cirkulaci a funkci tkání umístěných v daném prostoru“. Je důsledkem zvýšeného úniku tekutin do intersticia z extrémně oteklého skeletálního svalstva se vzestupem intersticiálního tlaku nad hodnotu kapilárního perfuzního tlaku. Ke vzniku kompartment syndromu mohou vést tři faktory, seřazené podle jejich frekvence:
- zvýšení obsahu kompartmentu,
- tlak zvenčí,
- zmenšený objem kompartmentu.
Obvykle se vyskytuje u úrazů končetin (asi 70 %), po revaskularizačních výkonech na periferních tepnách v důsledku ischemicko-reperfuzního syndromu, u popálenin, po kostních operacích, při intenzivní svalové činnosti u netrénovaných jedinců (v poslední době velmi často po jízdě na spinningovém kole), naložením příliš těsné sádry či obvazu apod.
Tlak intersticiálního prostoru u svalů v klidu je kolem 4–8 mmHg. Pokud je tlak zvýšen nad hodnotu 25–30 mmHg, dojde ke kolapsu kapilár a přerušení krevního toku s následující ischémií. Tkáně odumírají za 4–6 hodin a jsou nahrazeny jizevnatou tkání. Příznaky a diagnostika:
- akutně nastupující bolest, zhoršuje se při elevaci postižené končetiny,
- poruchy citlivosti v inervační oblasti nervů, které procházejí kompartmentem - objevují se již za 30 minut ischemie,
- porucha motorické funkce, obvykle po 2–4 hodinách ischemie,
- výrazná bolestivost při pasivním napínání svalů postiženého kompartmentu,
- napětí a výrazná tuhost obalu příslušného kompartmentu.
Nutno zdůraznit, že puls distálně od kompartmentu může být zachován a arteriografie může být zcela normální[5]! Současně platí, že nepřítomnost pulsu na periferii je již příznak pozdní a ischemické a metabolické změny jsou pak již ve většině případů nevratné!
Léčba je zaměřena v časné fázi na vyvolávající příčinu, tedy na stabilizaci zlomenin, kontrolu krvácení, odstranění tísnící obvazu či sádry apod. Pokud tlak v kompartmentu překročí perfuzní kapilární tlak nebo se objeví neuropatie, je nutno provést co nejrychleji dermatofasciotomii. U rozsáhlých traumat s předpokladem vývoje tohoto syndromu lze provést i preventivní dermatofasciotomii během primárního chirurgického ošetření. V této fázi není vhodné provádět debridment svalů či primární suturu kůže, ale s odstupem 3–5 dnů provést prohlídku rány a excisi zřetelně nekrotických tkání. Kožní defekt se pak uzavře suturou nebo se kryje dermoepidermálním štěpem.
Crush syndrom
Je stav charakterizovaný myoglobinurií a poruchou ledvinné funkce v důsledku svalové ischemie způsobené déletrvající zevní kompresí. Vyskytuje se ve velkém počtu v epicentrech válečných či přírodních katastrof u postižených v důsledku zasypání sutinami domů. Hlavním mechanismem je několik hodin trvající komprese svalů, vedoucí k ischemickému postižení. Z nekrotické svalové tkáně je do krve vyplavován myoglobin, který posléze precipituje v kyselém prostředí moče a obturuje ledvinné tubuly. Současně dochází k hemokoncentraci, hypotenzi, rozvoji hypovolemického šoku a akutnímu selhání ledvin. Léčba spočívá v masivních tekutinových náhradách zejména krystaloidy, vysokém obratu tekutin, forsírování diurézy, alkalizaci moči, eventuálně nasazení eliminačních metod na základě sledování laboratorních hodnot. Mezi kompartment syndromem a crush syndromem není možno položit dělící čáru, pro oba stavy je společným jmenovatelem svalová ischemie. U kompartment syndromu převažují spíše lokální projevy, u crush syndromu spíše příznaky systémové - šok, rozvrat vnitřního prostředí a selhání ledvin [5].
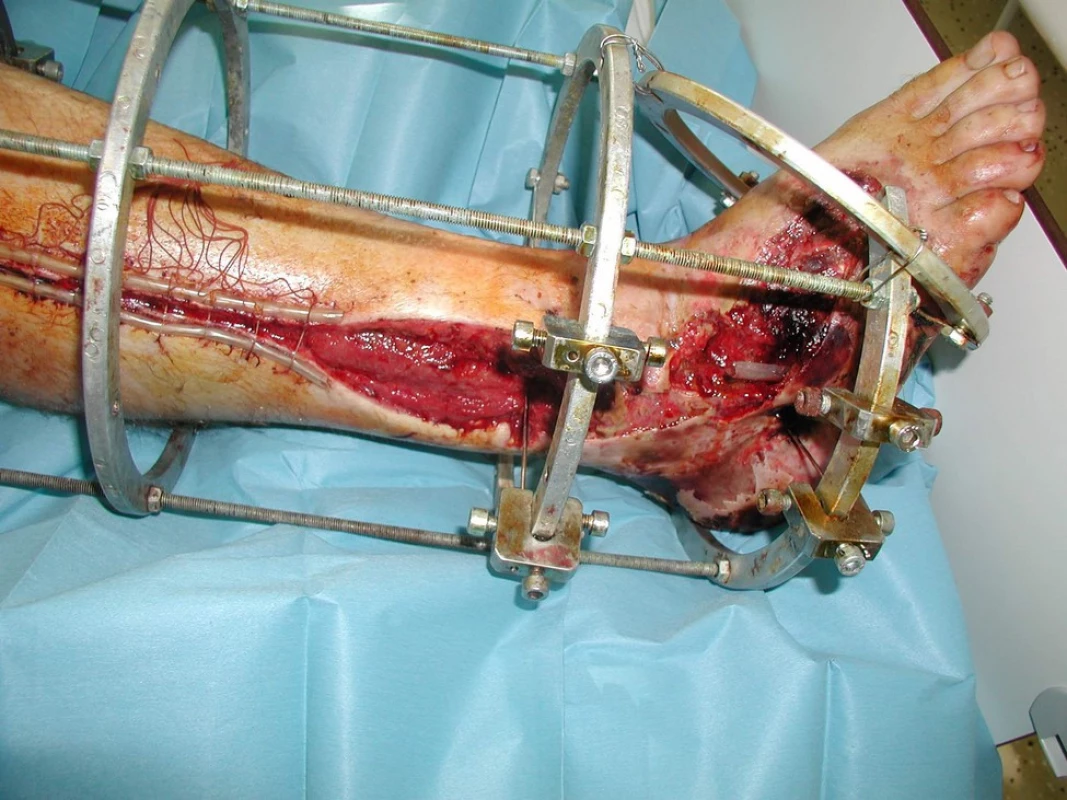
Drtivé poranění (crush injury)
Hovoříme o něm obvykle v souvislosti s vystavením některé části těla vysokoenergetickému úrazu. Obvykle se jedná o úder těžkým předmětem nebo přimáčknutí mezi dva předměty.
Čím větší je energie, tím horší jsou následky.
Definice
- postižení minimálně dvou tkání (kosti, svaly, nervy),
- tak rozsáhlé poranění, že přežití tkání je sporné,
- existuje „šedá“ zóna mezi živou a mrtvou tkání, jejíž záchrana je prioritou léčby.
Společným jmenovatelem těžkých úrazů je kombinace poranění kostí, cév, nervové tkáně a měkkých tkání. Zhoršení cirkulace může být způsobeno poškozením velkých artérií kostními úlomky při otevřených frakturách kostí nebo poškozenou mikrocirkulací vývojem výrazného otoku. Difúzní vzdálenost od kapiláry k buňce je zvýšená, zhoršuje se dostupnost kyslíku pro buňky, které současně mají zvýšené požadavky na kyslík. Otok měkkých tkání způsobuje kolaps kapilár zvyšujícím se tlakem intersticiální tekutiny. Drtivá poranění jsou charakterizována bludným kruhem ischemie, hypoxie, otoku a zhoršené mikrocirkulace. Důsledkem je neschopnost zajistit adekvátní dodávku kyslíku do tkání ke splnění jejich metabolických požadavků, dochází k buněčné dysfunkci a buněčné smrti. Rozsáhlá drtivá poranění proto mají vysokou míru komplikací. Patří k nim rozvoj infekce kostí i měkkých tkání včetně anaerobní klostridiové myonekrózy, zejména při poranění velkých cév. Odpověď organismu na infekci a ischémii je snížena zejména tehdy, pokud klesá parciální tlak kyslíku ve tkáních pod 30 mmHg. Zhoršuje se funkce bílých krevních elementů. Zejména „zabíječská“ funkce PMN se stává neefektivní, stejně jako se zastavuje produkce kolagenu fibroblasty [7]. Bez přítomnosti kolagenu v ráně nedochází k neovaskularizaci ani k hojení ran. Rozvoj infekce a nezhojení kostí se vznikem pakloubů jsou komplikací těžkých drtivých poranění až v 50–60 % případů s vysokým rizikem amputace.
Klasifikace
Nejčastěji užívanou klasifikací je Gustilova klasifikace otevřených zlomenin. V roce 1996 bylo na 3. Konsensuální konferencí ECHM v Miláně doporučeno užívat kombinaci Gustilovy klasifikace s hodnocením stavu obranyschopnosti pacienta k posouzení vhodnosti doplnění HBO k léčbě drtivého poranění (tab. 1). Typ I není jasně indikován k HBO, naopak všichni pacienti s typem III B a III C by měli být léčení metodou HBO. Pokud se týká typu II a III A, léčba je vyhrazena pouze pro tzv. kompromi-tované pacienty. Řadíme mezi ně pacienty s cukrovkou, ischémickou chorobou dolních končetin, systémovým imunitním onemocněním (kolagenóza, vaskulitida) apod.
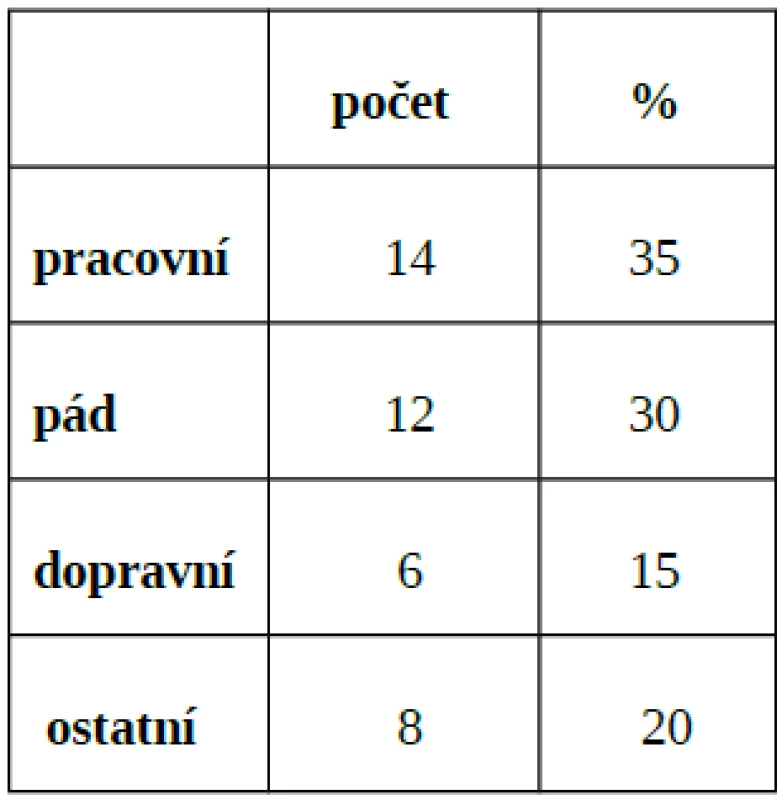
Table 1. Klasifikace dle Gustila a indikace HBO u jednotlivých typů poranění (volně dle Gustila ) 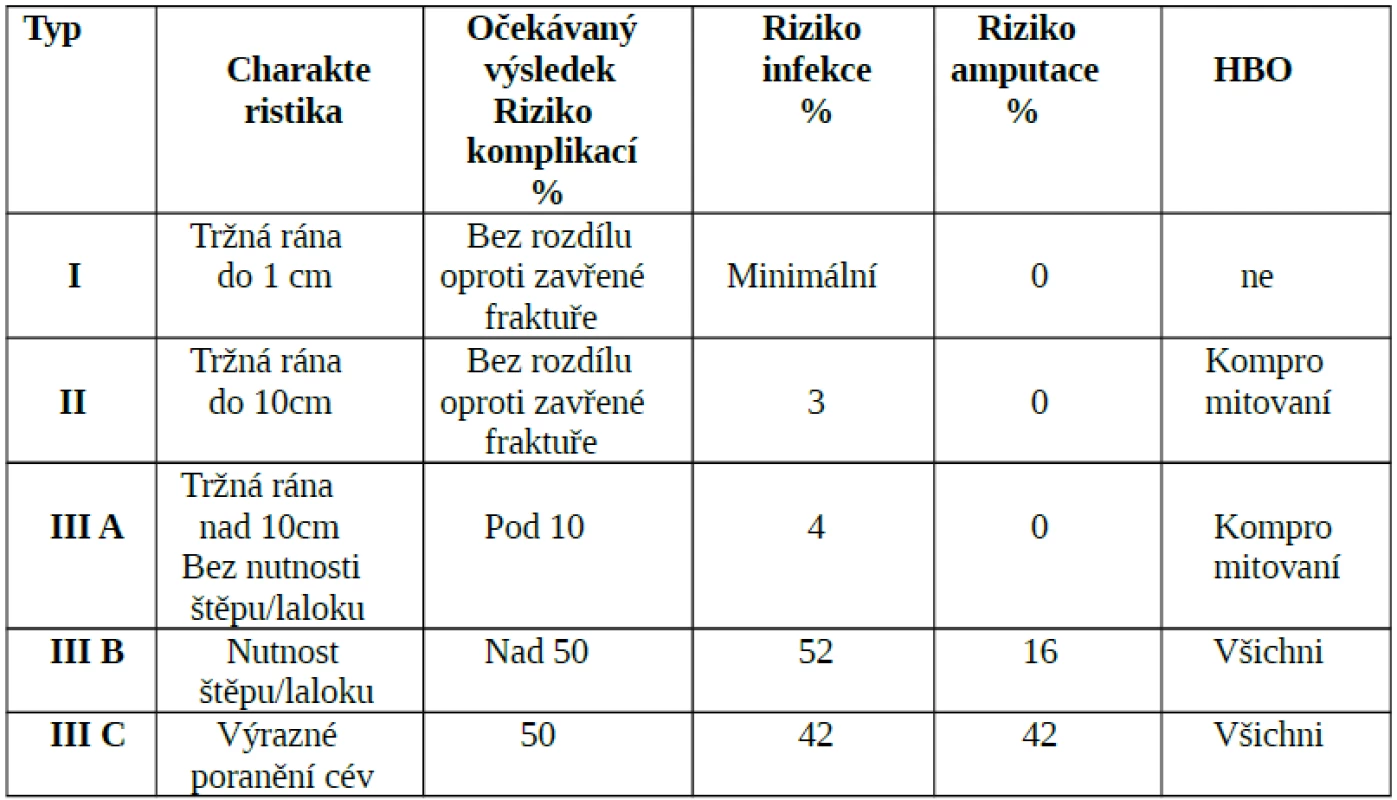
Požadovaným cílem léčby traumatické ischémie je:
- omezení tkáňových ztrát,
- omezení počtu komplikací (funkční omezení, jizvy, infekce, paklouby, chronická bolest),
- urychlení rehabilitace,
- snížení počtu operací,
- snížení délky pobytu v nemocnici a nákladů na léčbu [4].
Účinky a patofyziologické principy HBO v léčbě drtivého poranění jsou shrnuty v tab. 2.
Table 2. Účinky a patofyziologické principy HBO v léčbě drtivého poranění a akutní traumatické ischémie 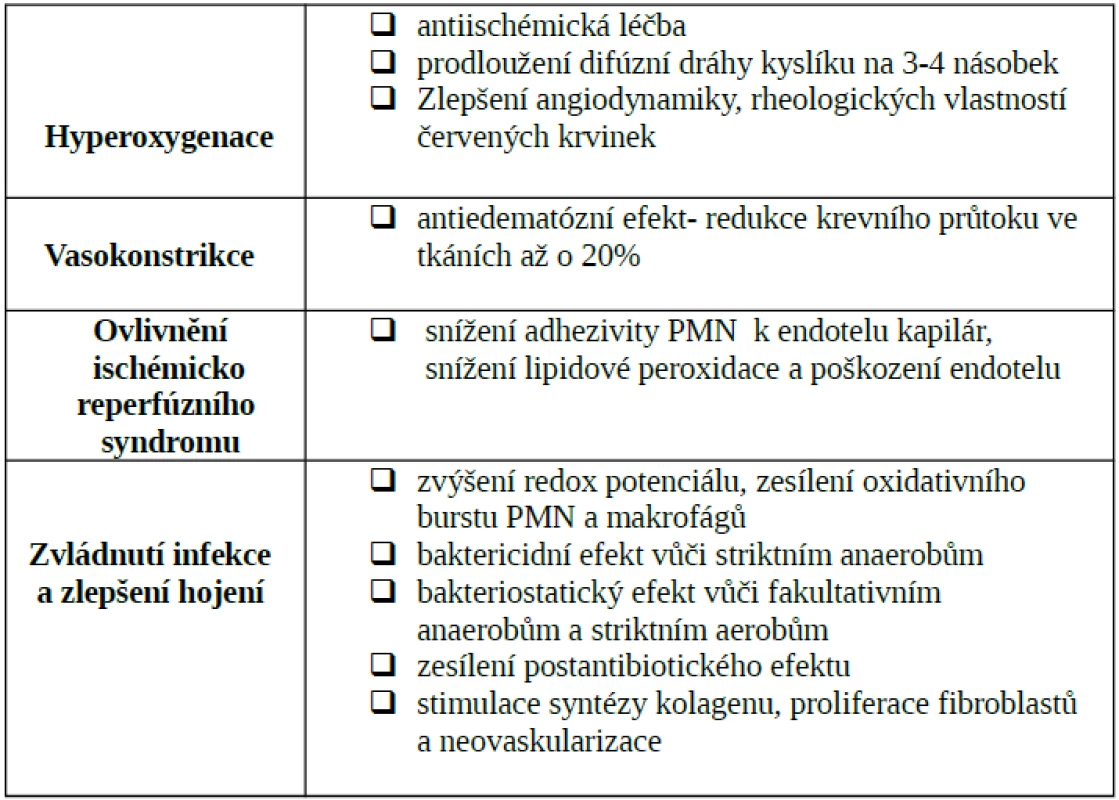
Léčba
Musí být zahájena okamžitě a agresivně. Primární je stabilizace hemodynamiky, korekce krevních ztrát, hypovolémie a vnitřního prostředí. Včasná chirurgická léčba spočívá ve vyčištění ran, odstranění cizího materiálu, debridementu nekrotických tkání, stabilizaci zlomenin - nejčastěji s využitím zevních fixátorů. Vnitřní osteosyntézy (dále OS), např. šroubování nebo nitrodřeňové hřebování, jsou zpravidla prováděny odloženě. Podání širokospektrých antibiotik je samozřejmostí. Ke krytí velkých kožních defektů je využíváno dočasné fyziologické krytí allogenními štěpy (umělá kůže). V pravidelných intervalech jsou prováděny převazy, čištění tkání s odstraněním nekrotických tkání. Doporučený léčebný režim HBO je 0,24–0,25 MPa (14–15 metrů vodního sloupce) po dobu 90 minut. Je doporučeno zahájit HBO nejpozději do 24 hodin od úrazu (v optimálním případě do 6 hodin) a aplikovat 3 léčebná sezení během tohoto intervalu. V dalších 3 dnech pak 2x denně a dále dle stavu a vývoje 1x denně.
Metodika
Na našem pracovišti hyperbarické oxygenoterapie jsme ve vícemístné hyperbarické komoře od roku 1965 dosud léčili více než 14 000 pacientů s celkovým počtem přes 168 000 léčebných expozic. Máme zkušenosti s léčbou pacientů pro chronická onemocnění, ale i pacientů v kritickém stavu, bezvědomí, na řízené či podpůrné plicní ventilaci. Použitý léčebný tlak, délka expozice i celkový počet expozic jsou individuální a závisí na indikaci, celkovém i místním stavu, vývoji onemocnění, toleranci léčebné metody, vývoji komplikací a na mnoha dalších faktorech. Primárním cílem naší observační retrospektivní studie bylo zjistit výsledný efekt léčby u pacientů léčených v našem centru pro drtivá poranění a akutní traumatickou ischémii v roce 2005. Sekundárním cílem bylo zjistit incidenci komplikací - riziko těžkých infekcí, reoperací, amputací. Do studie byli zařazeni všichni pacienti, kteří ve sledovaném období od 1. do 31. 2005 absolvovali léčbu HBO pro akutní traumatickou ischémii. Prostudováním rutinně zpracovávaných ročních statistik léčby a kontrolou lékařských záznamů byl zjištěn celkový počet pacientů, léčebných sezení, užitého léčebného tlaku. Byla zpracována epidemiologická data (věk, pohlaví, okolnosti úrazu, charakter poranění), dále způsob chirurgického ošetření, komplikující interní onemocnění, začátek léčby HBO od úrazu, komplikace (infekce, kompartment syndrom, amputace, fasciotomie a jiné reoperace), antibioterapie, diagnostické a terapeutické intervence. Výsledky léčby byly hodnoceny indikujícím specialistou (traumatologem, chirurgem, ortopédem) z klinického, rentgenologického a funkčního hlediska.
Výsledky
Celkově bylo ve sledovaném období zařazeno k léčbě HBO 40 pacientů, z toho 28 mužů (70 %) a 12 žen (30 %), průměrný věk 47 let (rozmezí 17–79 let). V Městské nemocnici bylo primárně léčeno 26 pacientů (65 %), 14 pacientů (35 %) bylo k léčbě převáženo z jiných zařízení, z toho 7 (17,5 %) z Traumacentra FN Ostrava. O poranění dolních končetin se jednalo v 31 případech (77,5 %), horních končetin v 9 případech (22,5 %). Rozdělení pacientů z hlediska mechanismu úrazu - viz tab. 3. V 5 případech (12,5 %) se jednalo o těžká zhmoždění měkkých tkání s tržnými ranami nad 15 cm, u 8 pacientů (20 %) o zavřené fraktury kostí po provedené osteosyntéze - tito pacienti indikováni k léčbě HBO pro hraničně prokrvený či nekrotický kožní kryt. U 27 pacientů (67,5 %) se jednalo o otevřené fraktury kostí s různým stupněm zhmoždění měkkých tkání. Rozdělení pacientů dle Gustilovy klasifikace v tabulce 4. Z výsledků vyplývá, že u celkově 26 pacientů (65 %) se jednalo o těžké poranění podle Gustilovy klasifikace II a více. Pacienti byli umístěni v 25 případech na standardním oddělení (62,5 %), 14x na JIP (35 %), 1x na ARO (2,5 %). Po nezbytné přípravě a hemodynamické stabilizaci byla prove-dena primární chirurgická intervence. Z toho 31x osteosyntéza (77,5 %), 1x byla současně provedena časná fasciotomie (2,5 %), 7x sutura kůže a podkožních struktur (17,5 %), 2x okamžitá amputace (5 %). Antibiotika byla podána u 38 pacientů (95 %). Analgetizace byla prováděna intravenózně nebo perorálně preparáty typu NSA a opioidy, v 6 případech byla zavedena kontinuální epidurální analgézie. V jednom případě byl pacient během HBO napojen na umělou plicní ventilaci.
Table 4. Rozdělení úrazů v roce 2005 dle Gustilovy klasifikace 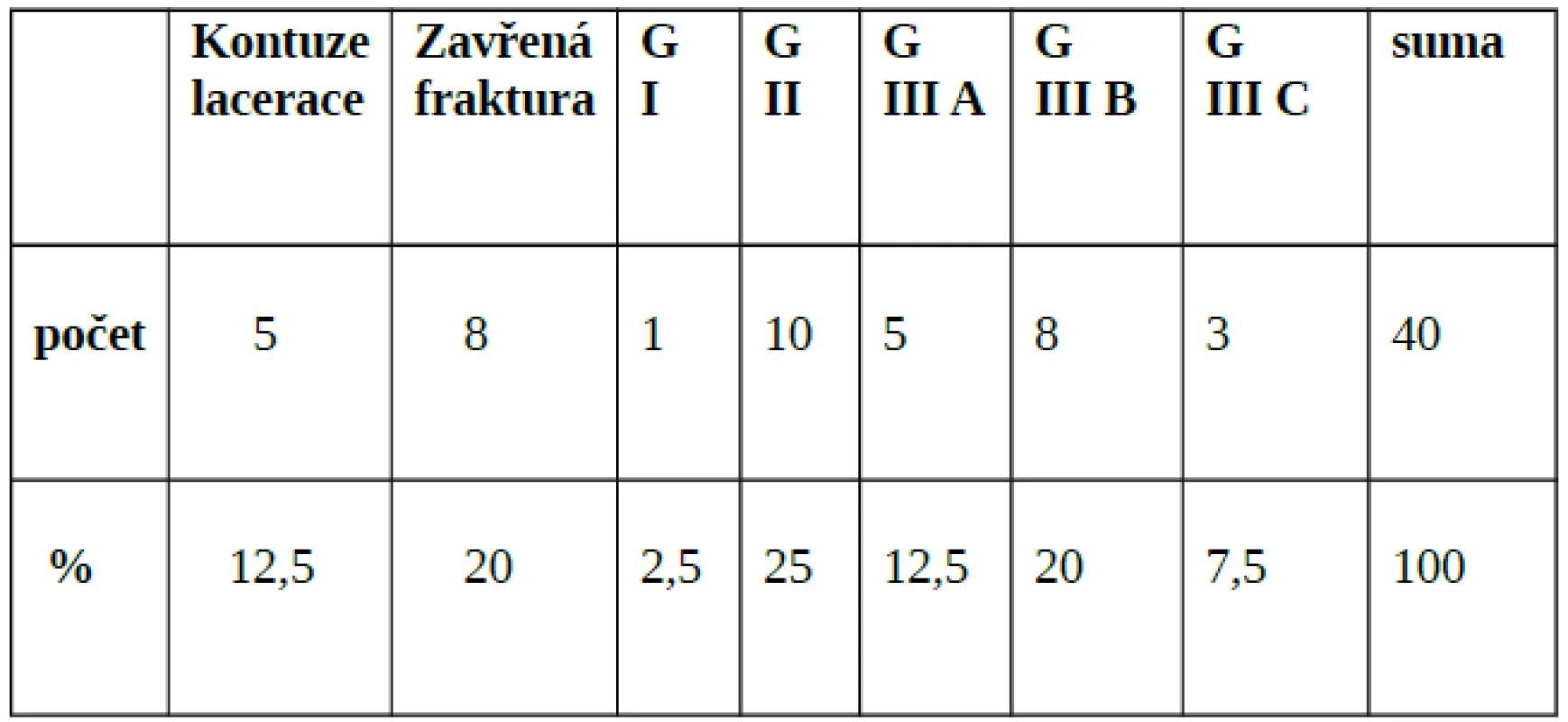
Table 5. Vztah mezi mírou amputací, infekcí a tíží poranění dle Gustilovy klasifikace 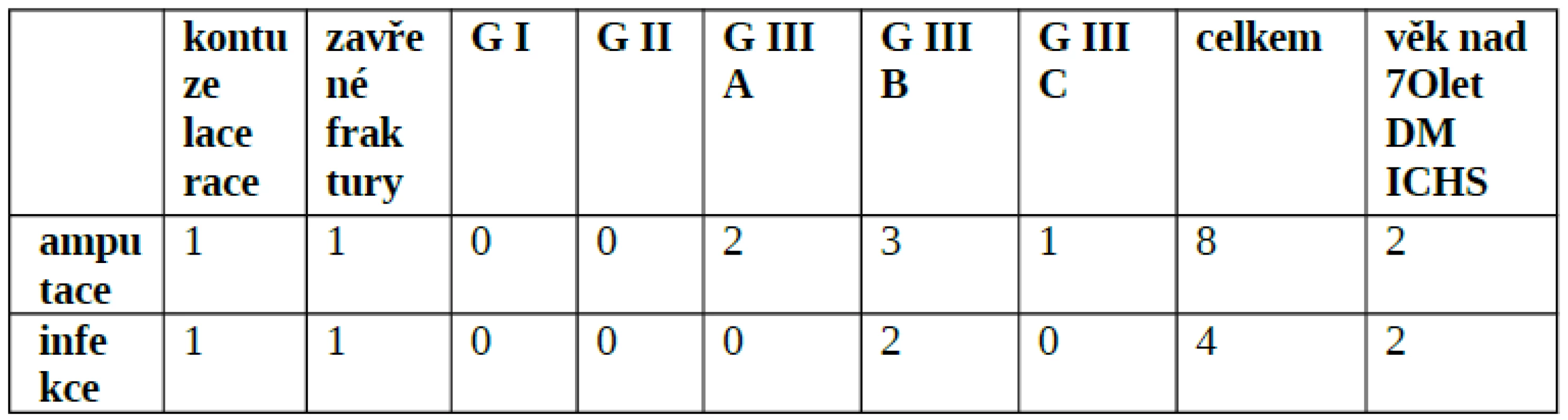
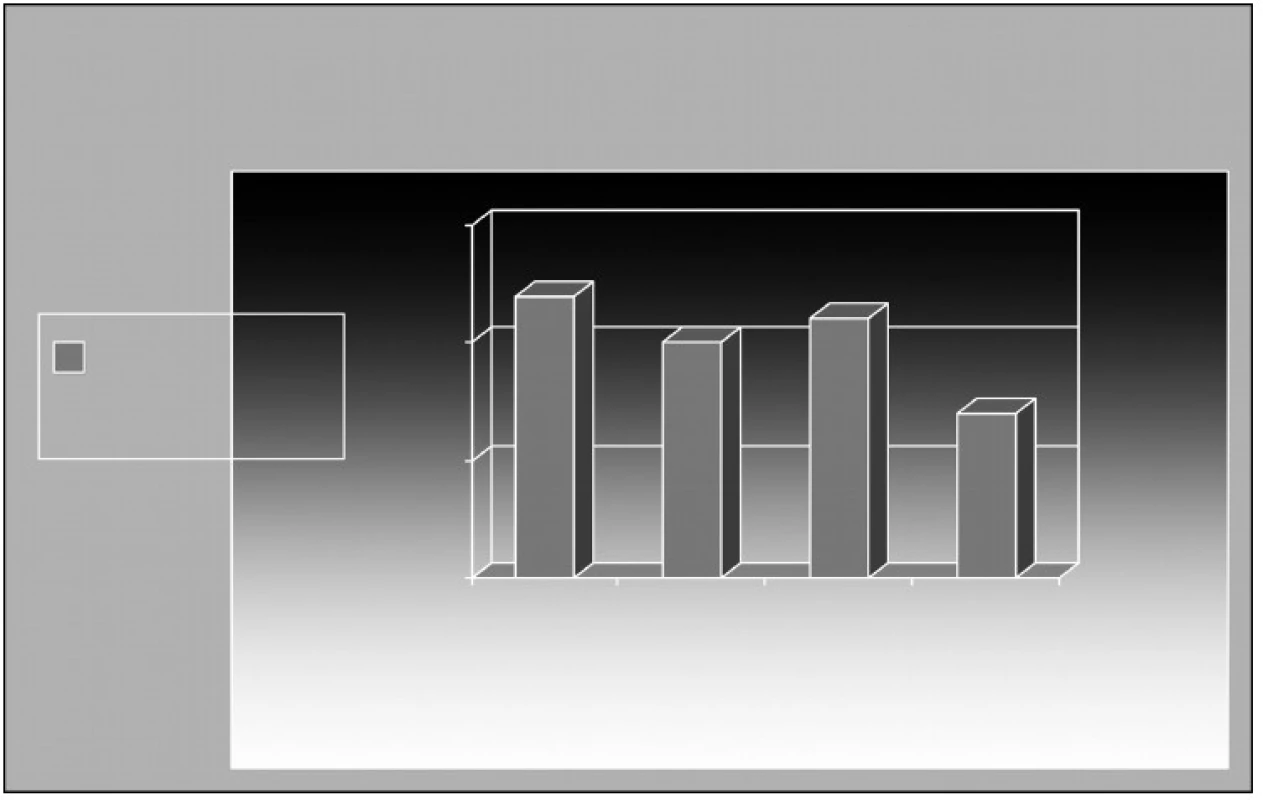
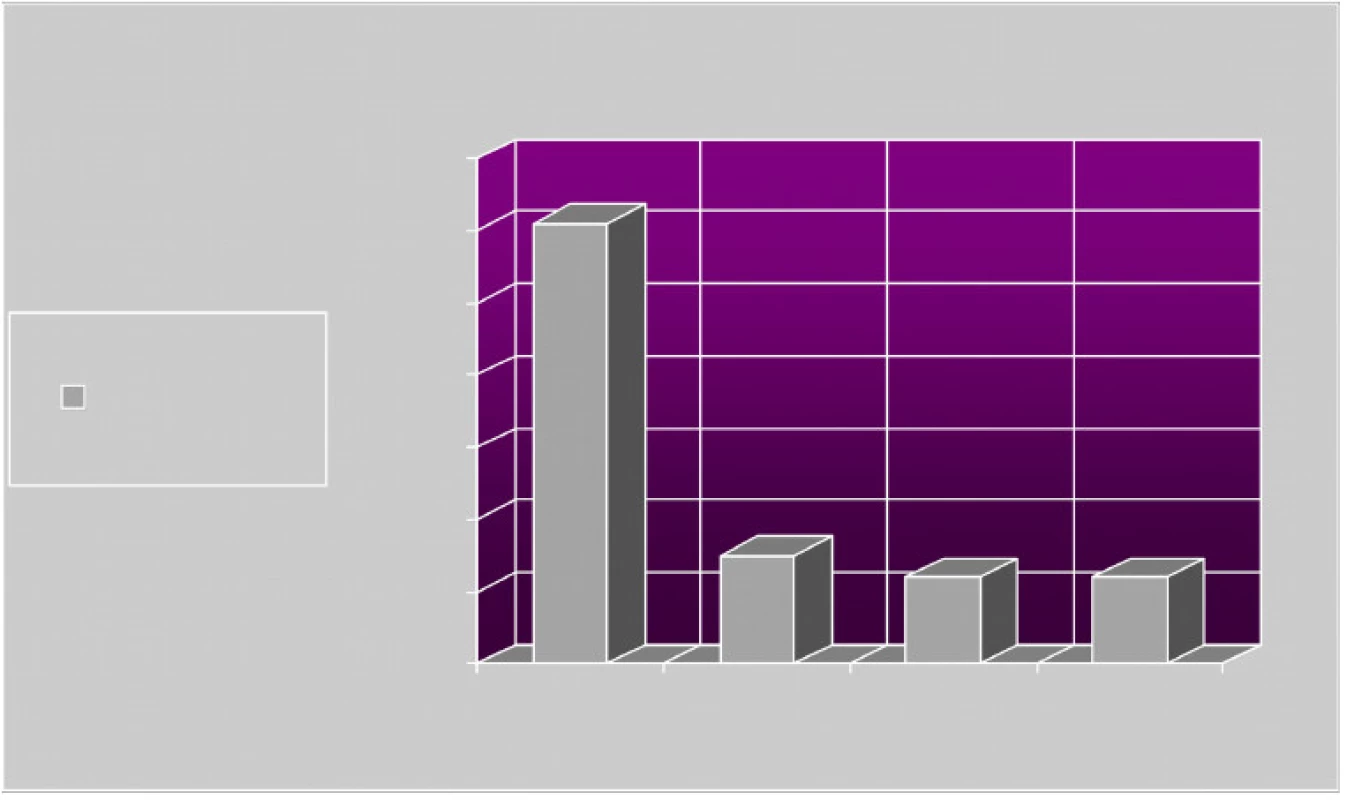
HBO byla zahájena v průměru 4. den po úraze (obr. 1). Z grafu vyplývá, že doporučované zahájení HBO do 24 h od úrazu se podařilo dodržet pouze ve 12 případech (30 %). Výsledný efekt léčby je znázorněn na obrázku 2. Pozitivní efekt (výrazný + mírný) léčby se dostavil celkově u 30 pacientů (76 %), u 5 pacientů (12 %) nebyla léčba úspěšná a rovněž u 5 pacientů (12 %) nebyla dokončena dle plánu a tudíž nebylo možno efekt zhodnotit. Jednalo se o následující důvody: 1x nesouhlas pacienta s pokračováním HBO, 1x neschopnost vyrovnat tlak mezi dutinou středoušní a okolním prostředím při zánětu středního ucha, 1x zánět tlustého střeva s úpornými průjmy, 2x pro provedení amputace.
Komplikace léčby:
Celkově u 18 pacientů (45 %) byla provedena reoperace po předchozím primárním chirurgickém ošetření. Jednalo se ve 4 případech (10 %) o revizi velké tepny pro poranění či trombózu. Amputace byla provedena u 6 pacientů (15 %), z toho 2x pro rozvoj anaerobní klostridiové infekce (10 %), 1x pro poranění velké artérie, 3x pro progresi ischémie a nekrózy. U 8 pacientů (20 %) došlo k vývoji kompartment syndromu s nutností provedení fasciotomie.
Jak bylo zmíněno, primární amputace byla provedena u dvou pacientů, celkově tedy v našem souboru byla provedena amputace u osmi pacientů. Vztah mezi příčinou amputace, rozvojem infekce v závislosti na stupni poranění a komplikujících faktorech uvádí tabulka 5. Celkově 6x se jednalo o pacienty s poraněním typu Gustilo III (2x III A, 3x III B, 1x III C), 1x o zavřenou frakturu s vnitřní OS s roz-vojem klostridiové myonekrózy, 1x o poranění s nepoznaným cizím tělesem a rozvojem klostridiové myonekrózy. Míra amputací u nejtěžších úrazů s klasifikací Gustilo III činila 37,5 % (6 pacientů ze 16), z toho u G III A 40 % (2 z 5), u G III B 37,5 % (3 z 8) a G III C 33,3 % (1 ze 3). Pneumotorax s následnou drenáží dutiny pohrudniční se vyskytl u jednoho pacienta, těžké drtivé poranění s vysokou hodnotou myoglobinémie a selháním ledvin s následnou nutností zavedení kontinuální eliminační metody se vyskytlo taktéž u jednoho pacienta. Komplikace spojené s barotraumatem ucha a střevním infektem již byly zmíněny.
Diskuse
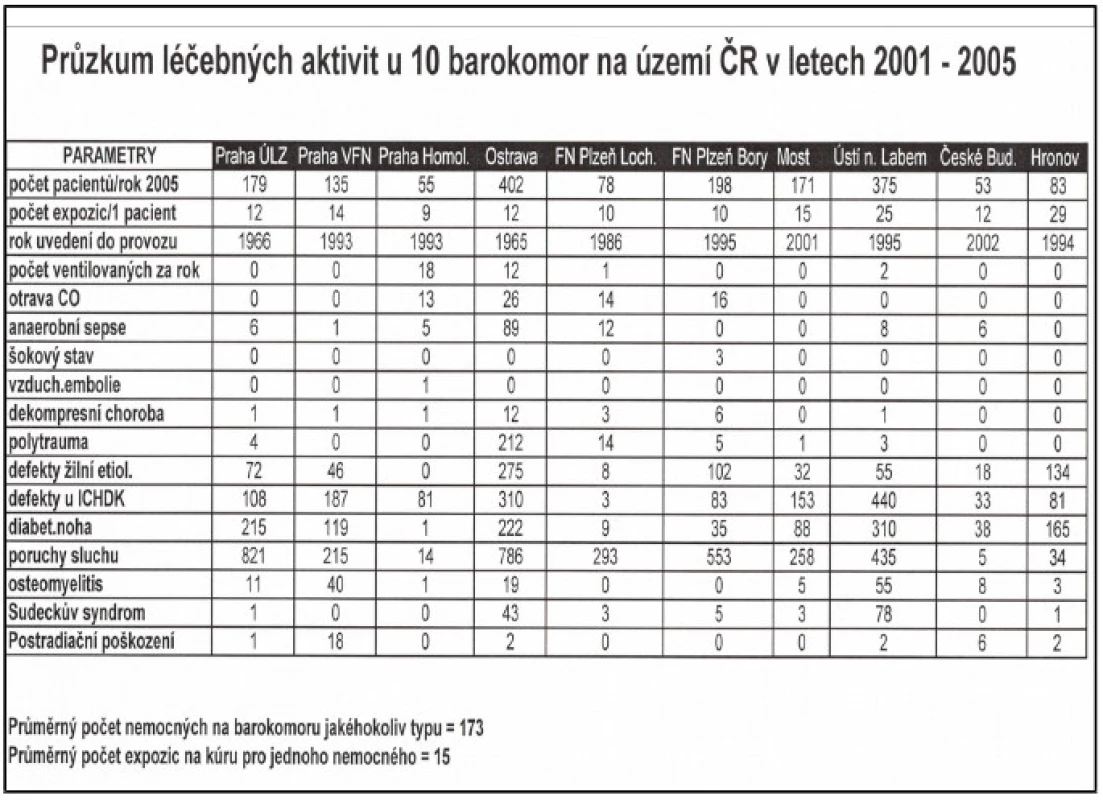
V dostupné literatuře existuje rozsáhlé množství prací, zejména retrospektivních, observačních studií, kasuistik, metaanalýz a expertních sdělení. Většina z nich poukazuje na příznivý adjuvantní efekt HBO v léčbě traumatické ischémie a drtivého poranění. Existuje však pouze minimum důkazů nejvyšší významnosti, tedy randomizovaných kontrolovaných studií. Mezi nejkvalitnější patří studie G. Bouachoura z roku 1996, která prokázala v souboru 18 pacientů léčených HBO (celkově 12 sezení 0,25 MPa během 6 dnů) statisticky významný pozitivní efekt na množství zcela zhojených pacientů, snížení počtu reoperací/amputací a zlepšení hojení ran u těžkých forem drtivého poranění ve srovnání s kontrolní skupinou [2] - tab. 6. V současné době probíhá mezinárodní prospektivní multicentrická studie HOLLT Study (Hyperbaric Oxygen in Lower Limb Trauma). Primárním cílem je prokázat snížení míry nekrózy měkkých tkání, rozvoje infekce a rozvoje kompartment syndromu u pacientů s frakturou bérce a poraněním měkkých tkání Gustilo 3 a více. Předpokládá se randomizace a zařazení 250–300 pacientů. Naše práce se řadí k mnoha retrospektivním observačním studiím, které popisují zkušenosti, výsledky a komplikace spojené s léčbou akutní traumatické ischémie a drtivého poranění. Je pravda, že „indikační práh“ na našem pracovišti je nižší než je obvyklé na jiných pracovištích. Dle našeho názoru je to způsobeno zvyklostmi a dobrou zkušeností chirurgů a traumatologů s touto metodou. U pacientů s vyšším věkem, komorbiditou a předpokladem vyššího výskytu infekčních komplikací jsou jimi indiko-váni k HBO i pacienti s nižším stupněm postižení, než je všeobecně doporučováno. Co se týče našich výsledků léčby, efektivita HBO je vysoká a míra komplikací se neliší od zkušeností zahraničních kolegů, např. Traumacentra v Murnau, které je německým referenčním hyperbarickým centrem pro léčbu traumatizovaných pacientů(Obr.3,4). V České republice kromě našeho pracoviště neexistuje jediné traumatologické pracoviště, které by HBO u těžkých traumat rutinně aplikovalo. Zejména je tato skutečnost zarážející v případech fakultních nemocnic, které mají funkční hyperbarickou komoru dostupnou. Jedinou výjimkou je Traumacentrum FN Ostrava, se kterým úzce spolupracujeme po mnoho let. Svědčí o tom průzkum léčebných aktivit v hyperbarických centrech České republiky za posledních pět let (tab. 7).
Table 6. Efekt HBO ve srovnání s kontrolní skupinou - signifikantní rozdíl v počtu zhojených, redukci operací a zlepšeném hojení ran u pacientů nad 40 let věku (volně dle Bouachoura) 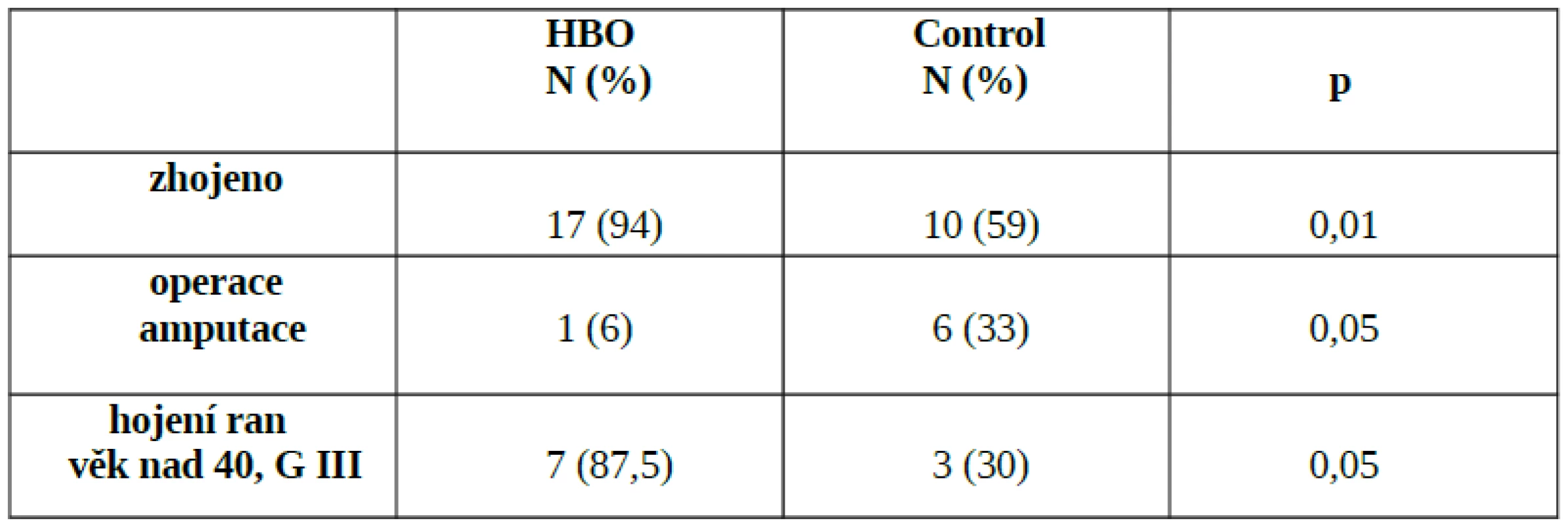
Shrnutí a závěr
HBO je vysoce efektivní metoda v léčbě těžkých úrazů spojených s drtivým poraněním a traumatickou ischémií. Pacientům přináší efekt, spočívající v lepších funkčních výsledcích, vyšší míře úplného zhojení, nižší míře infekčních komplikací, amputací a reoperací. Efekt HBO byl prokázán nejen v četných retrospektivních observačních studiích, jako je tato, ale taktéž v minimálně dvou prospektivních randomizovaných studiích. Rozšíření této metody léčby a její dostupnost do 24 hodin od úrazu by mělo být společným cílem jak odborné společnosti ČSHM (Česká společnost hyperbarické medicíny), tak společnosti úrazové chirurgie a chirurgické.
MUDr. Michal Hájek
Centrum hyperbarické oxygenoterapie, Anesteziologicko-resuscitační oddělení,
Městská nemocnice Ostrava,
michal.hajek@mnof.cz
Sources
1. Al-Waili, N., S., Butler, G., J. Effects of hyper-baric oxygen on inflammatory response to wound and trauma: possible mechanism of action. Scientific World Journal. 2006, 3, s. 425–441.
2. Bouachour, G., et al. Hyperbaric oxygen therapy in the management of crush injuries: a randomized double-blind placebo-controlled clinical trial. J Trauma. 1996, 41, s. 333–339.
3. Doleček, R., Pleva, L. Endokrinologie traumatu. Úraz. chir. 2006, 14, Suppl., s. 1–52.
4. Kemmer, A. Crush Injury and Other Acute Traumatic Ischemia. In: Mathieu, D.: Handbook on Hyperbaric Medicine. Dordrecht, Springer, 2006, s. 305–327(812).
5. Maňák, P. Kompartment syndrom a crush syndrom - přehled literárních poznatků. Zp. úraz. chir. 1995, 3, s. 15–22.
6. Menger, M., D., Volmar, B. Surgical trauma: hyperinflammation versus immuno suppression? Langenbecks. Arch Surg. 2004, 389, s. 475–484.
7. Niinikowski, J., Hunt, T., K., Zederfeldt, B., H. Oxygen supply in healing tissue. Am J Surg. 1972, 123, s. 247–252.
Labels
Surgery Traumatology Trauma surgery
Article was published inTrauma Surgery

2007 Issue 4
Most read in this issue- Súčasné možnosti liečby komplexných intraartikulárnych zlomenín distálneho rádia
- Hyperbarická oxygenoterapie v léčbě těžkých traumat a drtivých poranění
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career