-
Medical journals
- Career
Možnosti fyzioterapie u pacientů s onemocněním ledvin, dialyzovaných a transplantovaných – přehled od minulosti po současnost
Authors: A. Mahrová; L. Hellebrandová; K. Švagrová
Authors‘ workplace: Laboratoř sportovní motoriky, Fakulta tělesné výchovy a sportu Univerzity Karlovy v Praze, vedoucí pracoviště doc. Ing. F. Zahálka, Ph. D.
Published in: Rehabil. fyz. Lék., 23, 2016, No. 2, pp. 80-95.
Category: Original Papers
Overview
Tento článek volně navazuje na studie fyzioterapeutek Jurové a spol. (53, 54) a Mahrové a spol. (83), které byly publikovány v roce 2009. Poskytuje fyzioterapeutické veřejnosti ucelený přehled o stadiích chronického selhání ledvin a možnostech léčby, především přístrojové a nefarmakologické. Předkládá čtenářům přehled doposud popsaných poruch pohybového systému a příčiny omezené funkční fyzické a psychické zdatnosti dialyzovaných a transplantovaných pacientů a v rámci oboru fyzioterapie rozebírá možnosti jejich nefarmakologické léčby především pohybovými formami. Pro názornost doplňujeme teoretický přehled o kazuistiku pacienta po transplantaci ledviny s návrhy fyzioterapeutické intervence.
Cílem práce je navázat na studie věnované začlenění pohybové terapie v rámci oboru fyzioterapie, jako nedílné součásti komplexní léčby u pacientů s konečným stadiem chronického selhání ledvin léčených dialýzou a transplantací ledviny.Klíčová slova:
chronické selhání ledvin, dialýza, transplantace ledviny, fyzická aktivita, muskuloskeletální poruchy, fyzioterapie, kvalita životaÚVOD
Léčbě dialýzou předchází období tzv. predialýzy, kdy funkce ledvin postupně selhává (stadia 1-3 chronické renální insuficience – CHRI), ale pacient je zatím léčen konzervativně, tj. farmakologickými a dietními opatřeními. Jakmile selže funkce ledvin pod určitou hranici glomerulární filtrace, nahrazuje funkci ledvin tzv. umělá ledvina – dialýza, která je velkým pokrokem při léčbě chronického selhání ledvin (CHSL). Avšak náhrada zaniklé funkce ledvin umělou nebo transplantovanou ledvinou není vždy a po všech stránkách rovnocenná s původním stavem (130, 132). Se zdokonalováním dialyzační techniky a léčebných postupů se život pacientů prodlužuje a jejich nároky na kvalitní prožívání života se zvyšují. Jednou z možností léčby CHSL je transplantace (Tx) ledviny. Následně se mění pacientova léčba, celkový zdravotní stav, fyzická a psychická kondice a sociálně-ekonomické možnosti. Cílem orgánové transplantace není pouze zajistit prodloužení života příjemci, ale především mu umožnit návrat do takového funkčního a psychického stavu, který dosahoval před onemocněním (15). Jedná se o prostředek, který významnou měrou přispívá k úpravě a zvýšení pacientovy kvality života s důrazem na zajištění jeho soběstačnosti a práceschopnosti.
Pokud je věnována pozornost pacientově pohybovému aparátu již během predialýzy, popř. v období dialyzační léčby, je zde předpoklad, že po transplantaci ledviny bude mít menší výskyt funkčních poruch pohybového systému, často spojených s bolestí, která jej může dočasně zneschopnit. Udržení dobré fyzické zdatnosti pacientů s chronickým ledvinovým selháváním a po Tx ledviny s možností volby druhu pravidelné fyzické aktivity či fyzioterapeutických technik je nezbytné pro zachování či úpravu jejich celkového funkčního a psychického stavu, potažmo jejich soběstačnosti a lepší úrovně kvality života.
Fyzioterapeutická péče v predialýze, během dialýzy a po transplantaci ledviny není stále v českých dialyzačních střediscích pro pacienty běžně dostupná, ačkoli se jak v tuzemských, tak zahraničních realizovaných projektech ukázalo, že pacienti s CHRI a CHSL dobře tolerovali fyzickou zátěž s následnými pozitivními změnami v oblasti jejich kvality života (11, 22, 26, 27, 30, 31, 43, 51, 58, 61, 63 - 65, 81 - 83, 87, 95, 98, 103, 110 - 113, 121, 124, 127, 130, 132 - 136, 140, 143).
Nalézáme však méně studií s tématikou významu pravidelné fyzické aktivity na funkční a psychický stav, potažmo kvalitu života u jedinců po transplantaci ledviny (55, 56, 60, 80, 100, 101, 106). Vše, co se vztahuje k pohybu a k pohybovým aktivitám s cílem zlepšit funkční fyzický a psychický stav pacientů s CHSL a po Tx ledviny, považujeme za součást fyzioterapeutické aktivity.
Vzhledem k tomu, že pacienta často k vykonávání fyzické činnosti zneschopňuje bolest, která při onemocnění CHSL většinou vzniká v oblasti pohybového systému, věnujeme se částečnému rozboru poruch pohybového aparátu souvisejících s CHSL a jeho léčbou. Následně předkládáme rešeršní přehled studií, převážně zahraničních, které se ve své náplni zabývají vlivem pravidelné fyzické zátěže na funkční a psychický stav pacientů s CHSL. Tyto studie popisují různé formy pohybové intervence jako součásti léčby těchto pacientů a mohou být inspirativní pro realizaci pravidelných pohybových programů v našem prostředí. Zároveň předkládáme případovou studii pacienta po transplantaci ledviny s návrhy fyzioterapeutické intervence.
Vstup do problematiky
Statistická ročenka dialyzační léčby za rok 2013 uvádí 601 pacientů/milion obyvatel ČR léčených pro nezvratné selhání funkce ledvin (123). Tento počet se každý rok zvyšuje. S rozvojem a zdokonalováním technologie dialyzační léčby a lékařské péče se život pacientů prodlužuje. Zatímco v roce 1995 bylo 51 % HD pacientů starších 60 let (73), v roce 2004 již 63 % (74) a v roce 2013 se toto procento zvedlo na 70 % a z toho bylo 40 % diabetiků (123).
V roce 2013 byla v ČR pro nezvratné selhání funkce ledvin úspěšně provedena transplantace kadaverózní ledviny u 330 osob (123).
V současné době mají dialyzovaní jedinci delší předpokládanou dobu dožití a s ní narůstá výskyt muskuloskeletálních komplikací (117), v populaci dialyzovaných již tak početný (112, 113). Spolu s ostatními zdravotními komplikacemi přispívají poruchy pohybového systému ke zhoršení funkční schopnosti, která snižuje úroveň kvality života dialyzovaných jedinců v oblasti soběstačnosti.
Jak u nás tak převážně v zahraničí byla publikována řada výzkumů zaměřených na poruchy pohybového systému dialyzovaných (30, 52, 53, 54, 72, 82, 112, 117). Mezi symptomy těchto poruch patří bolest, omezená hybnost, snížená svalová síla, rychle nastupující únava, snížená citlivost a další projevy, jejichž příčiny se navzájem často prolínají. Většina poruch pohybového systému je způsobena převážně strukturálními změnami vyplývajícími z uremického stavu, ale jsou popsány také obtíže způsobené poruchami funkce ovlivněné sedavým způsobem života a dalšími omezeními vázanými na pravidelnou dialyzační léčbu.
V zahraniční literatuře nalézáme také studie zabývající se využitím individuální fyzioterapeutické intervence v souvislosti s poruchami pohybového systému vázanými na dialyzační léčbu a po transplantaci ledvin (11, 24, 55, 60, 80, 112). Tyto studie potvrzují, že role fyzioterapeuta je v multidisciplinárním týmu pracujícím s dialyzovanými a transplantovanými pacienty nezastupitelná. Cílem fyzioterapie u těchto jedinců je optimalizace funkční schopnosti, která může pomoci k co nejbezpečnější a nejdéle trvající mobilitě a soběstačnosti, s minimalizací závislosti na pomoci druhých (112). Individuální fyzioterapeutická intervence může předcházet intervenci skupinové, která již vyžaduje větší míru a kvalitu pohybových dovedností a funkčních schopností.
Yurdalan (145) zdůrazňuje, že pro udržení či zlepšení pacientovy kvality života v období léčby dialýzou a před následnou transplantací ledviny je důležité zahrnout pravidelný cvičební program do léčebného plánu. Klíčovou roli v sestavení a vedení cvičebního programu by měl mít, v rámci multidisciplinárního léčebného přístupu, fyzioterapeut.
Pohybový aparát u pacientů s chronickým onemocněním ledvin
Chronické onemocnění ledvin má několik stadií (CHRI 1-5), z nichž to poslední je označováno jako konečné stadium chronického selhání ledvin - CHSL a funkce ledvin musí být nahrazena přístrojovou dialyzační léčbou – hemodialýzou (HD) nebo peritoneální dialýzou (PD). V technikách očišťování ledvin u nás převažuje léčba hemodialýzou. Velkou nadějí každého pacienta s CHSL je transplantace ledviny.
U pacientů s chronickým onemocněním ledvin nacházíme funkční změny pohybového aparátu. Stejně jako u jiných interních onemocnění nacházíme i při onemocnění ledvin typický viscerální vzorec (onemocnění vnitřních orgánů), který se projevuje reflexními změnami specificky uspořádanými do viscerálního vzorce. Změny pohybového systému mají svá pravidla; při chronifikaci dochází k řetězení – vzorec se mírně ztrácí nebo utvrzuje, nemají-li poruchy tendenci k řetězení (78). Při chorobách ledvin nacházíme viscerální vzorec lokalizovaný většinou v thorakolumbálním přechodu (ThLp), zhruba od Th10 po L1. Mezi nejčastější prvky vzorce patří blokáda intervertebrálních kloubů, blokády jsou též v sakroiliakálním skloubení, a to se stranovou lokalizací shodnou s incuficientní ledvinou. Dochází k omezené hybnosti posledních dvou žeber. Dále jako součást viscerálního vzorce ledvin nacházíme spasmus m. psoas major, m. quadratus lumborum, vzpřimovačů trupu v ThL oblasti a zhoršená je i funkce bránice. Další svaly, které se mohou do vzorce řadit, jsou m. piriformis a adduktory stehna. Hyperalgické zóny jsou bilaterálně v oblasti ThL přechodu. Při onemocnění ledvin dochází k iritaci bolesti podéln dolních žeber většinou dozadu, směrem k ThL přechodu. Velmi často vyzařují do dolních končetin, čímž mohou imitovat kořenové dráždění (78).
Tyto komplikace jsou jednou z příčin snížené pohybové aktivity a jsou charakterizovány funkčními poruchami pohybového systému (bolesti v zádech, blokády páteře, bolesti kloubů) a s nimi souvisejícím omezeným rozsahem kloubní pohyblivosti, svalovými zkráceními, zmenšením svalové síly a zhoršením svalové vytrvalosti, poruchami stability, změnami stereotypu chůze a poruchami pohybové koordinace (87, 113).
Bolestivé problémy pohybového ústrojí omezují a zneschopňují i zdravé jedince. V kombinaci s vícečetnými zdravotními problémy, které se vyskytují u těchto pacientů, může přítomnost bolesti rychle vést k dekondici a snížení funkčních schopností (112). Propojení mezi vnitřními orgány, jejich vazy, fasciemi a pohybovým aparátem je naprosto konkrétní. Pro fyziologickou funkci orgánů je důležitá jejich „hybnost“. Barral (5) rozlišuje u vnitřních orgánů „mobilitu“ a „motilitu“. „Mobilita“ je pohyb orgánů a okolních struktur vůči sobě navzájem a je z velké části vyvolána bráničním dýcháním a znamená, že se každý vnitřní orgán pohybuje podle jasně definované fyziologické osy. „Motilita“ je inherentní pohyb – jeho směr a dynamika se pravděpodobně odvozuje z embryologického vývoje (5). Při poškození vnitřního orgánu zánětem, úrazem, operací nebo jinak, dochází k ovlivnění okolních struktur. V místě léze dochází ke ztrátě elasticity, což ovlivňuje směr pohybu okolních orgánů a může docházet k řetězení těchto funkčních poruch, které se po nějaké době projeví jako zdravotní problém na první pohled nesouvisející s vnitřním orgánem (68).
Motorem pohybu ledvin je bránice. Ledvina se během dechových pohybů (20000/den) pohybuje 3 – 4 cm kaudálně. Horní pól je stlačován během inspiria. Navíc se ledviny pohybují kaudolaterálním směrem a zevně. Během nádechu cítíme pohyb z mediokraniálního směru do laterokaudálního směru ve spojení se zevní rotací. Během výdechu se ledviny pohybují opačným směrem (42).
Ledviny jsou také ovlivňovány okolními orgány. Pravá ledvina je ovlivňována orgány gastrointestinálního traktu. Játra a vzestupný tračník jsou hlavními faktory mající vliv na pravou ledvinu. Levá ledvina je ovlivňována orgány genitálu prostřednictvím vyústění levostranné testikulár-ní/ovariální vény do renální žíly.
Poruchy funkce mobility či motility z jakéhokoli výše zmíněných důvodů se mohou projevovat jako následující symptomy (42): polyurie a žízeň; diskomfort v oblasti břišní dutiny s dušností; bolest v oblasti bránice nebo v pánevním dnu; bolest v oblasti lumbosakrální páteře objevující se krátce po vstání; bolest v oblasti lumbosakrální páteře související se zvýšením nitrobřišního tlaku, dlouhým sezením nebo stáním. Tyto symptomy, které se zhoršují při těchto funkčních poruchách ledvin, mohou být vysvětleny drážděním 3 nervů, které jsou uloženy vzadu za ledvinou na m. psoas major – jsou to subkostální, illiohypogastrický a ilioinguinální nerv. Bolest charakteristická pro ledvinovou koliku může být interpretovaná jako iritace ledviny těmito nervy. Když dojde k poruše mobility nebo motility ledviny v důsledku interního onemocnění, který má vliv na funkci ledvin, dochází k iritaci těchto 3 nervů, což způsobuje bolest kyčle nebo oblasti laterálního trochanteru. Je snadné si pak tuto dysfunkci splést s coxartrozou nebo burzitidou. Zde je důležité upozornit na to, že nemusí jít o poruchu samotné funkce ledviny (42).
Poruchy pohybového systému jedinců s CHSL jsou multifaktoriální etiologie. Jejich přehled, popis a návrhy fyzioterapeutické intervence jsou podrobně uvedeny v článku Jurové a kol. (53). Pro představu je ve zkratce uvádíme v tabulce 1.
Table 1. Přehled poruch pohybového systému u dialyzovaných jedinců (53). 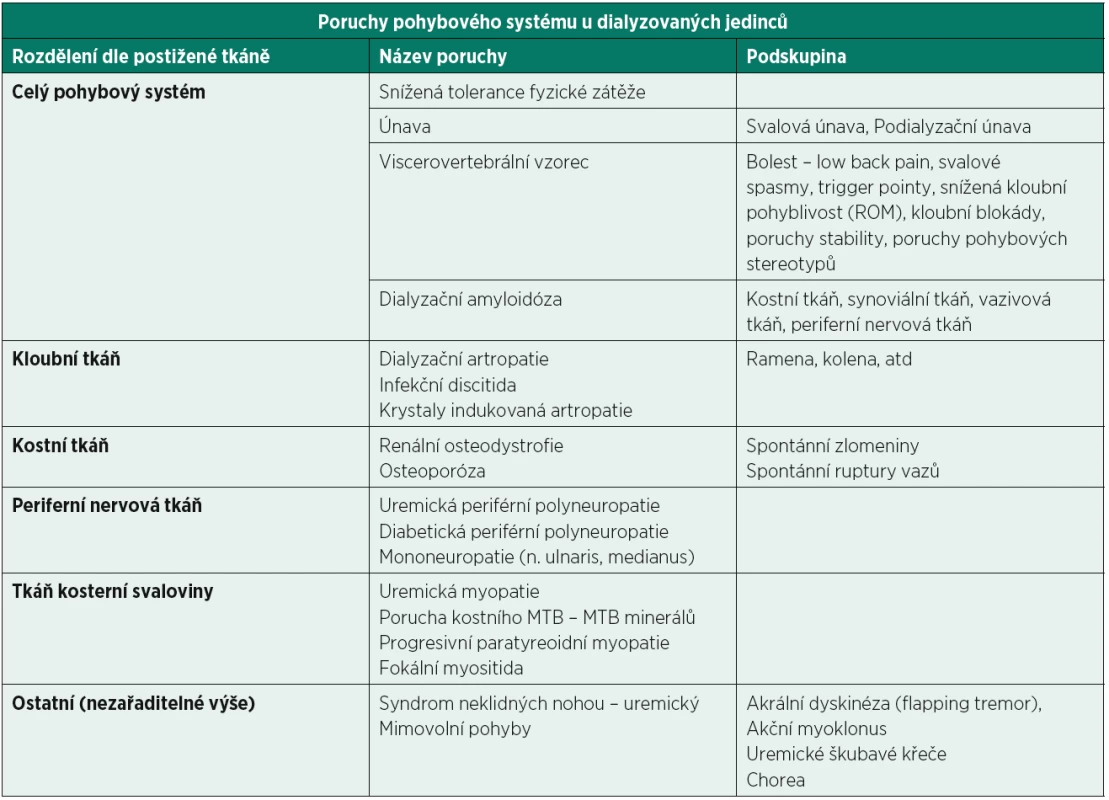
Přehled studií, které využívají u pacientů v pravidelné dialyzační léčbě a po transplantaci ledviny techniky fyzioterapie
Příznivý vliv pravidelné pohybové aktivity na celkový stav pacientů s CHRI a CHSL je za posledních 40 let popisován v řadě tuzemských a zahraničních studií. První zmínky o významu fyzioterapie a fyzikální terapie u pacientů s CHSL nalézáme v 70. létech 20. století (10). Tento článek popisuje postupy fyzioterapie v případě akutního (ASL) a chronického selhání ledvin (CHSL), při hemodialýze a peritoneální dialýze. Zdůrazňuje především techniky respirační fyzioterapie (při ASL a peritoneální dialýze), cvičení pro udržení či obnovení kloubního rozsahu, pro prevenci svalových atrofií a pro udržení či zvýšení svalové síly. Význam pravidelné fyzioterapie se u CHSL přikládá v terapii uremické polyneuropatii. Doporučenými postupy jsou jak individuální, tak skupinové formy cvičení. Ze cvičebních pomůcek je zmíněn bicyklový ergometr.
U pacientů s CHSL léčených hemodialýzou byla počáteční pozornost, týkající se pohybové aktivity, věnována především testování fyzické zdatnosti (48, 79, 120, 138). Následně, o několik let později, můžeme zaznamenat první zmínky o aplikaci pohybové aktivity jako prostředku pro zlepšení funkčního a psychického stavu těchto pacientů a zmírnění příznaků některých onemocnění přidružených k CHSL - arteriální hypertenze, anémie, hyperlipidémie, psychické poruchy (16, 17, 34, 40, 41, 66, 99, 147).
Ve většině výše uvedených studií jsme se setkali s aplikací pohybové aktivity aerobního charakteru během HD s využitím speciálně upraveného bicyklového ergometru, tzv. bed - side bicycle ergometer. Vzhledem k množství realizovaných studií vybíráme jen některé, zejména ty, na které jsme našli odkazy i v jiných odborných studiích a jsou ve full textu dostupné v knihovnách či elektronicky (6, 34, 41, 45, 58, 62, 67, 79, 85, 89, 95, 102, 110, 116, 118, 122, 128).
Délka pohybového programu se pohybovala od 4 týdnů do 14 měsíců, s frekvencí 2-3krát týdně 15-90 minut a s intenzitou zatížení 50-80% VO2max. Studie popisují především pozitivní výsledky ve smyslu zlepšení kardiorespirační výkonnosti a u některých hypertoniků i snížení hodnot krevního tlaku (12, 41, 88, 102). Od 90. let se začínají objevovat studie, které v rámci náplně pohybového programu během HD procedury využívají cvičební prvky rozvíjející kloubní pohyblivost, svalovou sílu a vytrvalost, udržující svalovou rovnováhu, rozvíjející pohybovou koordinaci, kladoucí důraz na koordinaci pohybu s dýcháním a nácvik relaxačních technik (20, 21, 25, 31, 43, 47, 69, 90, 95, 103, 124, 134).
V oblasti rehabilitace dialyzovaných pacientů a pacientů v predialýze se začíná používat termín “Renal Rehabilitation” (47), který byl vytvořen v roce 1996, kdy v USA publikovala pracovní skupina Life Options Rehabilitation Advisory Council materiál nazvaný „Renal Rehabilitation – Bridging the Barriers“ pro vytvoření rehabilitačního plánu pro dialyzované pacienty (133). Jedná se o „Koordinovaný program léčby, vzdělávání, poradenství, nutriční a pohybové intervence za účelem maximálního využití pracovního potenciálu, funkčního stavu a kvality života dialyzovaných pacientů“. Je zde zdůrazňována podpora soběstačnosti a zachování sebeobsluhy s minimalizací závislosti na pomoci druhých, pravě za integrace oboru fyzioterapie do multidisciplinárního léčebného postupu o pacienty s CHSL.
V tomto materiálu bylo definováno pět hlavních cílů rehabilitačního programu a oblasti, ve kterých by měla být zejména zlepšená všeobecná informovanost (oblasti medicínská, psychosociální, kondičně-rehabilitační, pracovně-rehabilitační a kvalita života). K těmto cílům vedou určité mosty, které byly pro snazší zapamatování označeny 5 E: Education (vzdělání); Encouragement (odhodlání, motivace); Exercise (cvičení); Employment (vzdělání); Evaluation (hodnocení, zpětná vazba).
Konkrétně složka „cvičení“ je charakterizována jako jedna z možností jak své životní šance využít, žít déle a lépe v plné kvalitě života, změnit životní styl. Schopnost vést aktivní život je u dialyzovaných a transplantovaných pacientů podceňována (133). Konkrétně složka „hodnocení, zpětná vazba“ je velice důležitá z hlediska motivace k jakékoli pohybové činnosti, a to nejen z hlediska pacienta, ale také realizačního týmu. Úspěch rehabilitace je měřitelný jen při vhodně zvolených kritériích. Tato kritéria zahrnují sledování tělesné funkční kapacity, psychosociální adaptaci, zaměstnanost, obecně či specificky kvalitu života nebo celospolečenské ekonomické efekty, jako např. náklady na hospitalizační péči, na sociální zajištění, úspory v léčbě a podobně. Bez průkazného efektu pohybové intervence u takto nemocných jedinců není šance získat finanční podporu programu rehabilitace. A protože v zahraničních studiích a v zahraničí byl efekt prokázán, přesunul se program pohybové intervence u dialyzovaných a transplantovaných v některých státech, např. Německo, Švédsko, Kanada, z kategorie charitativně či grantově podporovaných projektů do kategorie léčebné péče, systematicky podporované a hrazené z prostředků zdravotního pojištění.
Ve stejném roce byla založena společnost European Association of Rehabilitation in Chronic Kidney Disease (EURORECKD). Tato asociace sdružuje odborníky z oblasti nefrologie, fyziologie tělesné zátěže, rehabilitace a fyzioterapie, metabolismu a nutrice. Česká republika je zastoupena MUDr. Lukášem Svobodou, primářem dialyzačního oddělení Nemocnice Na Homolce v Praze.
Později se stále častěji setkáváme s pohybovým programem, který kombinuje posilovací (odporová) cvičení - cvičebními pomůckami jsou většinou elastické gumové pásy a činky; posilovací stroje “leg press” a aerobní trénink – využití bicyklového ergometru, chodeckého trenažéru (6, 12, 13, 14, 23, 96, 97, 119, 125, 126). Rocha a spol. (121) se zabývali efektem dvouměsíční fyzikální terapie, technik PNF, brániční dechové gymnastiky a efektem posilovacích cvičení dolních končetin na funkci dýchacích svalů, na sílu stisku ruky a kvalitu života u dialyzovaných jedinců.
Autorky Johansen a Painter (49) se dlouhodobě věnující fyziologii a patofyziologii tělesné zátěže a fyzické aktivity u pacientů s CHSL a v dialyzační léčbě a publikovaly přehledovou studii o vlivu fyzické zátěže na fyzické funkce a fyzickou zdatnost u takto nemocných jedinců v predialyzačním období. Potvrzují jednoznačný pozitivní efekt pravidelné fyzické aktivity u dialyzovaných jedinců. Níže uvádíme výsledky jednotlivých randomizovaných a experimentálních studií, které toto tvrzení podporují.
Po absolvování fyzické aktivity v rámci intervenčního pohybového programu nastalo zlepšení v hodnotách VO2max s průměrnými změnami o 17-23 %, dále v testech hodnotících fyzickou zdatnost (test rychlosti chůze – Up-Go test, 6 minut walk test, test Sed-stoj) a v oblasti kvality života, konkrétně v doménách hodnotících fyzickou oblast (47, 50, 108, 109).
Objevují se studie využívající jógová cvičení - Hatha jógu - v prevenci a léčbě oxidativního stresu, který způsobuje endoteliální dysfunkci a podporuje vznik aterosklerózy; u pacientů s CHSL léčených HD (38) pak vede k ovlivnění lipidového metabolis-mu (37). Yurtkuran a spol. (146) aplikovali tříměsíční cvičební program modifikovaných jógových cvičení na skupinu hemodialyzovaných pacientů se sledováním vlivu na míru bolesti, únavy, kvality spánku a krevních parametrů. Výsledky ukázaly významná zlepšení všech sledovaných proměnných ve srovnání se skupinou kontrolní.
Dobšák a spol. (28) porovnávali vliv aerobního tréninku na bicyklovém ergometru a elektrostimulaci (EMS) extenzorů dolních končetin pacientů s CHSL. Cvičení a elektrostimulace probíhaly mezi 2.-3. hodinou hemodialýzy, 2-3krát týdně, celkem 20 týdnů. Signifikantní pozitivní vliv na zlepšení fyzické zdatnosti a kvality života byl prokázán u obou intervenovaných skupin. EMS metoda může být do budoucna jednou z významných terapeutických součástí rehabilitace pacientů při hemodialýze.
Daleko menší přehled existuje pro hodnocení vlivu pravidelné fyzické zátěže u pacientů s onemocněním ledvin v predialyzačním stadiu, tj. ve stadiu chronického ledvinného onemocnění 1-3. V pohybovém programu byly aplikovány aerobní a posilovací pohybové aktivity, a to buď zvlášť anebo jejich kombinace. Z aerobních aktivit byly popsány chůze – na běhacím trenažéru (9, 92, 139), jízda na bicyklovém trenažéru (9, 29, 92, 139), aerobní kondiční cvičení v domácím prostředí (75) a plavání (111). Posilovací aktivity zahrnovaly posilování převážně velkých svalových skupin dolních končetin – extenzory a flexory kolenního kloubu, flexory a extenzory kyčelního kloubu, s využitím posilovacích pomůcek – posilovací gumy (39) a posilovací stroje – intenzita zátěže 60% (44) - 80% 1RM (4, 18, 19).
Délka trvání pohybového programu se pohybovala od 12 týdnů do 20 měsíců, většinou 3 – 12 měsíců, s frekvencí 2-3x týdně a délkou cvičební jednotky 30-60 minut. Intenzita fyzické zátěže se pohybovala v rozmezí 45-85% VO2max, většinou 60-70 % VO2max. Všechny studie zmíněné v období predialýzy byly odborně vedené, z toho dvě byly navíc, kromě ambulantního zařízení, aplikovány také individuálně v domácím prostředí (75, 92).
V odborných studiích věnujících se problematice pohybové aktivity u pacientů s CHRI v predialyzačním období a během dialýzy pozorujeme, že ke změnám ve sledovaných ukazatelích fyzické a psychické výkonnosti dochází většinou až po 12 týdnech (6, 14, 27, 31, 35, 47, 58, 95, 110 , 116, 119, 125, 126).
Setkáváme se také s výjimkami, které uvádějí změny ve sledovaných ukazatelích již po 6 - 8 týdnech pohybové intervence, jejíž náplň převážně tvoří pohybová aktivita aerobního charakteru provozována na bicyklovém ergometru nebo běhátku (76, 89, 97, 121, 147). Podstatnou roli v délce pohybové intervence, která má vliv na změny ve smyslu zlepšení sledovaných ukazatelů, jistě hraje intenzita zatížení ve CJ, délka CJ a její frekvence během HD procedury (58, 64, 65).
Cíle pohybové intervence pro jedince s chronickým selháním ledvin
Prioritním cílem pohybových programů (PP) je udržení nebo zlepšení fyzické kondice, a tím následně zachování celkové soběstačnosti a nezávislosti na druhých lidech, návrat do společnosti, u jedinců produktivního věku znovu začlenění do pracovního procesu, možnost žít na stejné úrovni jako zdravý člověk. Individuální či skupinové PP musí respektovat individualitu každého pacienta, jeho předchozí pohybovou zkušenost, aktuální úroveň fyzické zdatnosti, doporučení ošetřujícího lékaře. Nesmí ohrozit zdravotní stav jedince.
Hlavní náplní PP by měly být činnosti vedoucí k udržení či rozvoji kloubní pohyblivosti, svalové síly, ke kompenzaci svalových dysbalancí, k obnovení dynamických stereotypů nutných k sebeobsluze, ke korekci poruch pohybové koordinace a ke zlepšení kardiorespirační zdatnosti. Doprovodnými efekty fyzické zátěže jsou benefity v psychosociální oblasti, tj. zvýšení psychické odolnosti (sebedůvěry, sebehodnocení, zvládání stre-sových situací); přispění k celkové soběstačnosti a nezávislosti na jiné osobě; přispění ke snížení komplikací vlastního onemocnění a léčby (podpoření zkrácení hospitalizace, morbidity a mortality); podpora průběhu pracovních a volnočasových aktivit; podpora zvládání sociálních rolí v rodině, v zaměstnání a ve společnosti (26, 27, 31). Zajištění těchto požadavků, vyplývajících z pohybové léčby, je důležité hlavně u starších pacientů, kterých je v PDL převaha.
Možnosti rozdělení pohybových aktivit z hlediska zaměření
Pohybové programy pro jedince s CHSL můžeme rozdělit na individuální a skupinové. Dále potom podle časového průběhu v rámci komplexní HD léčby na PP během HD procedury a mimo HD proceduru. Každý pohybový program má v závislosti na průběhu komplexní HD léčby a vlastním onemocnění CHSL svá specifika. Podle zaměření na určitou oblast pohybových schopností a dovedností můžeme PP u HD jedinců rozdělit následovně; při dělení vycházíme z poznatků německého nefrologa Daula a spol. (26):
Kondiční: cílem je udržet či zlepšit celkovou kondici se zaměřením na rozvoj základních motorických schopností. Patří sem cviky na rozvoj kloubní pohyblivosti, svalové síly a vytrvalosti, pohybové koordinace a fyzické kondice.
Kondičně – vytrvalostní: cílem je upravit či zlepšit kardiorespirační fyzickou zdatnost a ovlivnit komplikace související s CHSL a HD léčbou (snížení TK, optimalizace MTB sacharidů a lipidů apod.). Zařazujeme sem vytrvalostní aktivity cyklického charakteru (chůze, běh, jízda na kole, jízda na bicyklovém ergometru apod.) a řídíme se doporučenými individuálními intenzitami zátěže pro HD jedince.
Silové: cílem je ovlivnit jak lokální tak celkovou svalovou sílu, zvětšit svalový objem, zabránit atrofizaci svalových vláken, podpořit mineralizaci kostní tkáně, korigovat svalové dysbalance jako prevenci funkčních poruch pohybového systému a podobně. Zařazujeme sem cvičení proti odporu i s využitím náčiní (činky, gumy – thera-bands, pytlíky s pískem atd.).
Koordinačně - balanční: cílem je korigovat koordinační poruchy a poruchy rovnováhy, které jsou spojené s periferními a centrálními poruchami nervového systému. Zařazujeme sem jak individuální tak skupinová herní cvičení, využíváme balanční pomůcky (overball, fyzioball, měkké žíněnky), gymnastické nářadí a náčiní (lavička, žebřiny, míče atd.).
Dechová cvičení jsou nezbytná pro nácvik správného stereotypu dýchání, který bývá u dlouhodobě nemocných jedinců porušen. Cílem dechových cvičení je naučit jedince všechny způsoby dýchání, zkoordinovat pohyb s dýcháním, pomocí dechu harmonizovat činnost vnitřních orgánů, uvolnit celkové tělesné napětí, optimalizovat psychické funkce (minimalizace stresu, úzkosti a strachu).
Relaxační cvičení jsou důležitou součástí PP pro HD jedince. Můžeme je zařadit na konci fyzické aktivity v rámci fáze zklidnění nebo úplně samostatně. Cílem relaxačních technik je zklidnit probíhající procesy v organismu, uvolnit svalové napětí v přetížených svalových skupinách, harmonizovat psychické funkce, redukovat riziko, které s sebou přinášejí stresové situace, kterým je většina HD jedinců vystavena, a načerpat energii pro další činnosti. V rámci relaxačních technik využíváme např. Schultzův autogenní trénink, Jacobsonovu progresivní relaxaci, hudební doprovod. Součástí relaxační fáze mohou být i cvičení, která se soustředí na uvědomění si vlastního těla (Feldenkreisova technika, prvky jógy) a podobně. Tabulka 2 předkládá příklady náplně PP u jedinců s CHSL.
Table 2. Příklad náplně pohybového programu u pacientů s konečným stadiem CHSL (105). 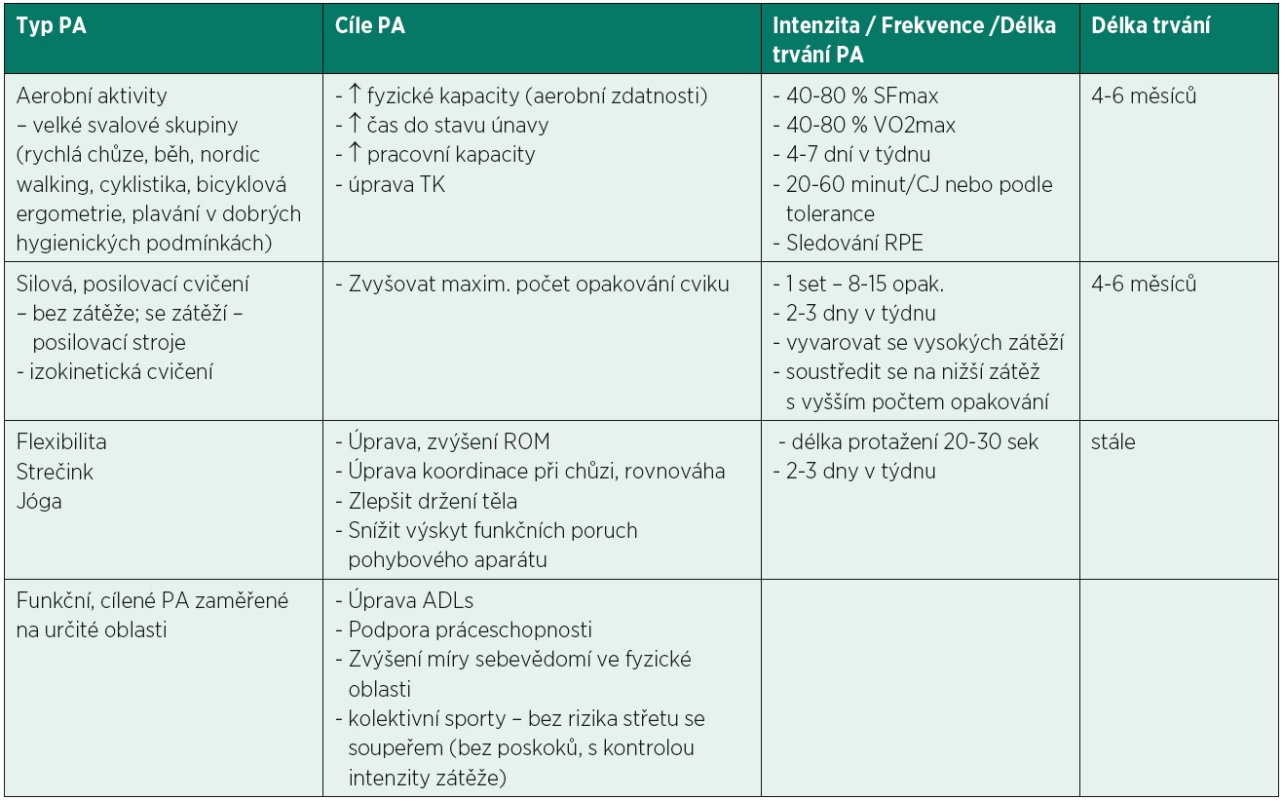
Pozn.: PA = pohybová(-é) aktivita(-y); SFmax = srdeční frekvence; TK = krevní tlak (v mm Hg); VO2max = maximální spotřeba kyslíku; ROM = range of motion, rozsah kloubní pohyblivosti; ADLs = activity of daily living, běžné denní činnosti; RPE = rating of perceived exertion, subjektivní intenzita vnímání zátěže. Shrnutí doporučení náplně pohybového programu pro jedince s chronickým selháním ledvin
Do současnosti nebylo definováno jednoznačné a optimální doporučení. Autorky Johansen a Painter (49) doporučují následovat postupy American Heart Association for older adults (94), které označují jako vhodné pro chronicky nemocné, byť mladší jedince než pro které jsou původně určeny, tzn. vhodné pro jedince s onemocněním CHSL. Kutner a spol. (70) doporučují odesílat pacienty s CHSL s diagnostikovanou srdeční vadou či onemocněním (výskyt u většiny pacientů) na rehabilitaci zaměřenou pro kardiaky. U těch, bez kardiovaskulárního onemocnění, doporučuje následující objem a intenzitu pohybových aktivit pro udržení fyzické a psychické kondice: mírná intenzita aerobní zátěže v pásmu SF 50-60 % SFmax., 30 minut denně, anebo vysoká intenzita aerobní zátěže v pásmu SF 70-80 % SFmax., 20 minut 3krát týdně. Zdůrazňuje individualitu každého pacienta a klade důraz na jeho aktuální zdravotní stav a fyzické možnosti s ohledem na volbu typu a intenzity fyzické zátěže.
Kutner a Jassal (71) vypracovali následující vstupní a pokračovací kritéria pro začlenění do komplexního integrovaného programu péče zahrnujícího dialýzu a aktivní krátkodobou a dlouhodobou rehabilitaci. Vstupní kritéria: vymezení krátkodobých rehabilitačních cílů podle potřeb pacienta a možností fyzioterapeuta; aktivní participace motivovaného pacienta v účasti na rehabilitačním programu (aktivní a dobrovolná spolupráce); výhledový potenciál možnosti úpravy či zlepšení aktuálního funkčního stavu jedince, ADL, sociální interakce a kognitivních funkcí. Pokračovací kritéria: spolupráce ošetřujících lékařů v úpravě léčby, spolupráce dialyzačních sester, multidisciplinární přístup; dlouhodobý zdravotní stav pacienta vykazující úpravu či změny funkčního stavu – pozitivní reakce organismu na působící podnět.
Zahraniční zdroje shrnující doporučení pro volbu a aplikaci fyzické aktivity pro jedince s CHSL jsou dostupné na webových stránkách společnosti Life Options website (86) ve formě “Exercise for the Dialysis Patient“, anebo na stránkáchNational Institutes for Health (93) ve formě “Exercise & Physical Activity.”
Souhrn doporučení při ordinaci pohybové aktivity pro pacienty s chronickým selháním ledvin
Pro pacienty v dialyzačním léčení a po transplantaci ledviny je pravidelná pohybová aktivita žádoucí a nezbytná z hlediska prevence či zmírnění příznaků tzv. křehkosti a k zachování co nejdéle trvající soběstačnosti a mobility, zejména u seniorských pacientů. Výše uvedené poznatky jsou odborným přehledem současných literárních poznatků. Přístup ke každému jedinci musí být vysoce individuální a opírat se o jeho zdravotní a pohybovou anamnézu. Kontraindikace pro aplikaci fyzické zátěže u pacientů s CHSL jsou následující (1, 2, 3, 26, 114):
Absolutní kontraindikace: maligní arteriální hypertenze (240/120 mm Hg); klidová nekompenzovaná hypertenze (200/100 mm Hg); nestabilní angina pectoris; srdeční nedostatečnost, srdeční selhávání; závažné poruchy srdečního rytmu bez medikamentózní terapie; akutní plicní embolizace a cévní příhody; pokročilá aortální stenóza; těžká plicní hypertenze; akutní onemocnění (akutní infarkt myokardu, zánětlivá onemocnění – myokarditida, tromboflebitida; horečnatý stav, tyreotoxikóza).
Relativní kontraindikace: hyperkalémie >6 mmol/l; hypokalémie <3,5 mmol/l; těžká renální osteopatie; těžká uremická polyneuropatie; nestabilní angina pectoris; méně závažné poruchy srdečního rytmu; některé vrozené nebo získané chlopenní vady; některé stavy po infarktu myokardu; dekompenzovaný diabetes mellitus; neochota pacienta ke spolupráci.
Níže uvádíme souhrnný přehled k doporučení pro praktickou aplikaci pohybového programu:
- Objem a intenzitu pohybové aktivity ordinovat individuálně na základě vyhodnocení pohybové anamnézy, výsledků motorických a zátěžových testů; vše konzultovat s ošetřujícím lékařem;
- Průběh pohybového programu dokumentovat v připraveném protokolu;
- Před zahájením CJ doporučujeme konzultovat aktuální zdravotní stav vybraného pacienta s ošetřujícím personálem, změřit a zaznamenat hodnoty SF, DF, TK do protokolu; následně je sledovat po celou dobu cvičení a opakovaně změřit na konci CJ;
- Zvýšenou pozornost věnovat hypertonikům, v pravidelných intervalech měřit TK;
- U diabetických pacientů mít k dispozici glukometr s příslušenstvím;
- Před začátkem CJ seznámit pacienta s aktuální náplní CJ, s limitujícími indikátory k přerušení cvičení; zvláštní důraz klást na vyloučení pohybu horní končetiny (HK) s AV spojkou, která je napojena na dialyzační přístroj;
- Během průběhu CJ doporučujeme se řídit indikacemi a kontraindikacemi k přerušení nebo snížení intenzity zátěže (viz. výše);
- Doporučená délka pohybového programu během HD, po kterém můžeme pozorovat změny v motorické a fyzické výkonnosti, je minimálně 12 týdnů. Frekvence CJ v PDL je doporučena minimálně dvakrát týdně a doba trvání se mění podle fáze pohybového programu a individuálních možností pacienta;
- V souladu s literárními doporučeními (26, 27, 98) se nám osvědčilo zařazení CJ během HD procedury do 2.-3. hodiny. Pro pacienty stejné dialyzační směny doporučujeme z organizačních důvodů zařazení do CJ max. 3 jedinců ve stejné směně (tzn. cca 30-40 min. trvání CJ/pacienta);
- Při dělení CJ na jednotlivé části doporučujeme dodržovat běžně užívané schéma na úvodní část; hlavní část - vyrovnávací a rozvíjející fáze; a závěrečnou část (84);
- Doporučená intenzita zatížení během CJ je v pásmu submaximálních hodnot SF, tj. 60-70 % SFmax se současnou kontrolou subjektivního vnímání intenzity zatížení Borgovou škálou (8), jejíž hodnota by neměla překročit stupeň 12-13. U HD pacientů může při fyzické zátěži docházet k pomalejšímu vzestupu SF než u zdravých osob;
- Intenzitu zatížení volit vždy individuálně na základě výsledků vstupních a kontrolních testů;
- U HD jedinců bez předchozí pohybové zkušenosti nebo u těch, kteří se pohybové aktivitě nevěnují již delší dobu, doporučujeme začít cvičit intervalovou formou, tzn. úseky zátěže prokládat odpočinkovými úseky; začít s menším počtem cviků ve CJ. Zpočátku volit nízkou intenzitu zátěže, tzn. 30-50 % SFmax a stupeň Borgovy škály 7 – 9.
Postupně zvyšovat objem a intenzitu CJ, tzn. prodlužovat intervaly zátěže a zkracovat odpočinkové úseky, ve CJ přidávat počet cviků a jejich varianty, zvyšovat počet opakování cviku v sérii a podobně. Během zvyšování zátěže by měla být dodržována opatrnost a intenzitu snížit, nebo cvičení přerušit dojde-li k neobvyklé slabosti, nadměrné únavě, dušnosti, nevolnosti, bolesti nebo tlaku na hrudi, nadměrnému zpocení (studený pot), zarudnutí obličeje či naopak nápadné bledosti okolo nosu a úst. Je vhodné při takovéto příhodě změřit TK i SF a zjištěná data předat lékaři;
- U aplikovaného pohybového programu se během HD osvědčilo prokládání sérií silových cviků s protahovacím a dechovým cvičením;
- Při realizaci jednotlivých CJ je důležité se řídit záznamem v protokolech z předchozích CJ a postupně zvyšovat objem a intenzitu cvičení;
- AV spojka nesmí být zaškrcována (náramky, hodinky), nesmí být použita k měření TK nebo pro aplikaci injekcí; přes paži s AV spojkou nedávat popruhy a nic, co by ji mohlo zaškrtit;
- Doporučujeme průběžně informovat ošetřující personál o průběhu pohybového programu každého pacienta individuálně;
- Mimo dialyzační den je vhodné cvičit krátce před snídaní a dále ve druhé části dne (odpoledne nebo v podvečer);
- Při sportu je vhodné chránit cévní přístup návlekem nebo bandáží a kontrolovat pravidelně několikrát denně pohmatem funkci píštěle (hmatný vír);
- Pacienti s centrálními žilními katétry se nesmějí koupat ve veřejných bazénech. Mohou se koupat jen v moři a po poradě s lékařem. Místo vstupu katétru je nutno sterilně krýt;
- U pacientů s polycystózou ledvin může dojít při prudším pohybu k prasknutí cysty, což je spojené s bolestí a objevením krve v moči. Potřebný je klid a sonografická kontrola.
Význam fyzické aktivity pro přípravu na transplantaci ledviny
Pro dialyzované jedince, kteří jsou zařazeni v seznamu čekatelů na transplantaci (Tx) ledviny je určitý stupeň fyzické zdatnosti nezbytný nejen pro absolvování náročné operace, ale především pro kvalitnější život s transplantovanou ledvinou.
Navíc rizikovým faktorem pro komplikace po transplantaci je také nadváha, body mass index (BMI) nad 35 je možno považovat za kontraindikaci transplantace ledviny (142). Samotná transplantace ledviny je spojená s dalšími zdravotními specifiky (způsobenými hlavně imunosupresí), mezi něž patří zvýšená chuť k jídlu, nadměrné ukládání tukové tkáně a další, které vedou k nárůstu váhy. Dlouhodobá inaktivita před transplantací ledvin, zvláště během dialyzační periody, vede ke snížení fyzické kondice příjemců transplantované ledviny. K rychlému zlepšení pracovní kapacity a tolerance fyzické zátěže pak dochází hlavně v prvním roce po transplantaci, ale pouze za podmínky dodržení předepsané pravidelné pohybové intervence (32, 104, 115). Pro pacienta navyklého pohybovým aktivitám v dialyzačním období je snazší zapojit se do po-transplantační pohybové intervence. Vyšší míra pohybových aktivit v období před transplantací ledviny je prediktorem lepšího přežívání štěpu a prožívání života po transplantaci (100).
Význam fyzické aktivity po transplantaci ledviny
Nárůst fyzické zdatnosti a pracovní kapacity závisí na pravidelné pohybové aktivitě (PPA) zejména v prvním roce po Tx ledviny (100, 115). Jedinci po Tx ledvin jsou schopni pomocí PPA dosáhnout stejných nebo i lepších výsledků než zdraví lidé. Zlepšení ve výkonu pacientů pomocí pravidelné pohybové aktivity je odhadováno na 25-28 % (105). Běžná pohybová aktivita u transplantovaných je relevantním faktorem kvality života (91). Pravidelně pohybově aktivní pacienti po Tx ledviny mají významně lepší hodnocení HRQOL než bez PPA (101). Metody léčebné rehabilitace po transplantaci ledviny pomáhají obnovit pacientovu fyzickou a psychickou kondici a podpořit aktivní rodinný, sociální a profesní život (60). Zvýšení fyzické kondice a kvality života po Tx ledviny prostřednictvím PPA by mělo být začleněno do managementu strategií snižujících rizika kardiovaskulárních onemocnění (7, 77, 100, 106), která jsou nejčastější příčinou úmrtí po transplantaci ledviny (142). Pravidelný cvičební režim po transplantaci ledviny vede k redistribuci tuku ve svalu a snížení rizikových kardiovaskulárních faktorů (137). V tabulce 3 je uveden přehled doporučených pohybových aktivit a jejich dávkování po transplantaci ledviny.
Table 3. Přehled doporučených PP po Tx ledviny (105). 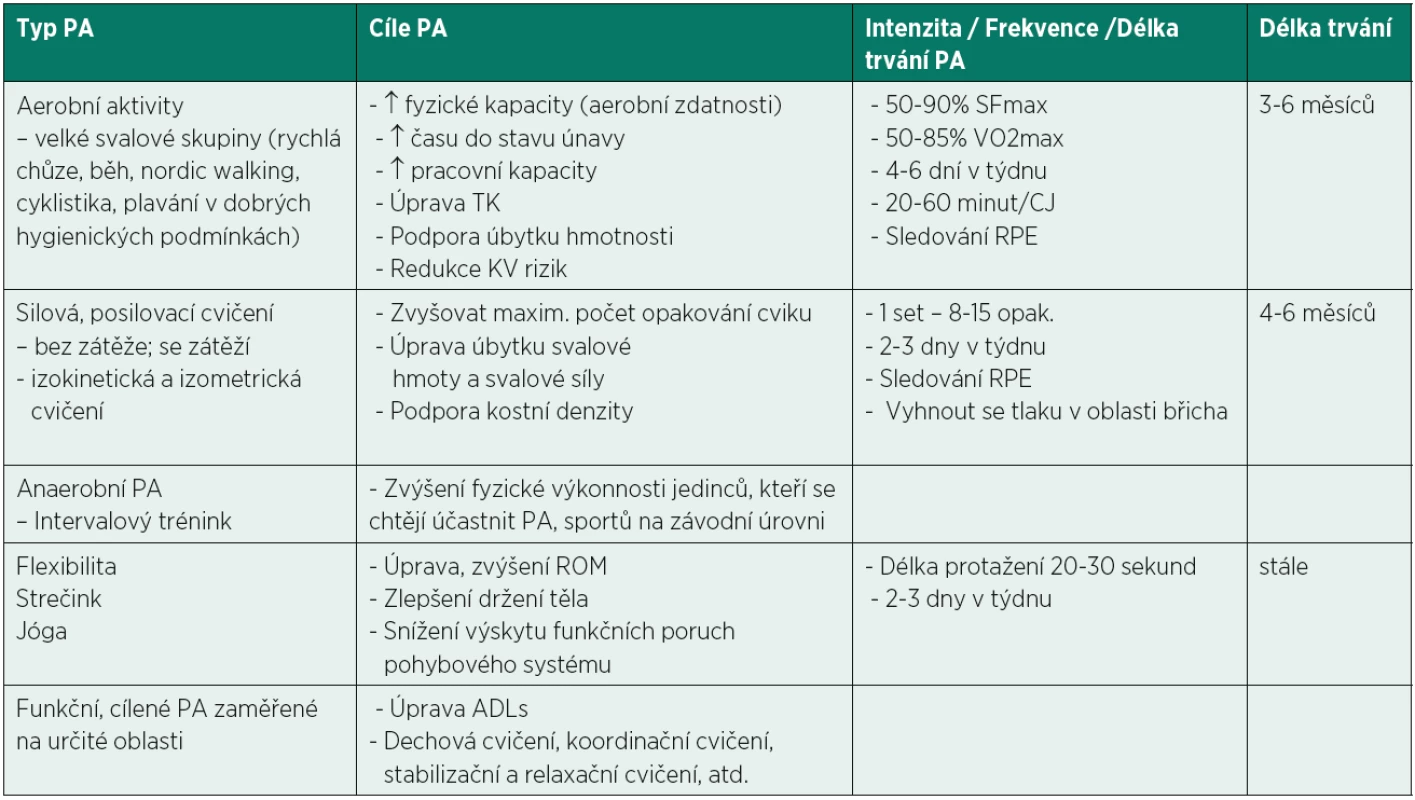
Pozn.: PA = pohybová(-é) aktivita(-y); SFmax = srdeční frekvence; TK = krevní tlak (v mm Hg); VO2max = maximální spotřeba kyslíku; ROM = range of motion, rozsah kloubní pohyblivosti; ADLs = activity of daily living, běžné denní činnosti; RPE = rating of perceived exertion, subjektivní intenzita vnímání zátěže; KV = kardiovaskulární; CJ = cvičební jednotka. Praktická doporučení při ordinaci pohybové aktivity po transplantaci ledviny
Při ordinaci pohybové aktivity a aplikaci zátěžových testů se řídíme stejnými pravidly jako u dialyzovaných jedinců, viz. výše. Níže uvádíme doporučení vztahující se pouze ke stavu po transplantaci ledviny:
- Čím dříve se začne s PA po operaci, tím lépe - vyšší motivace k zahájení kondičního cvičení (133);
- V časném období po Tx – ještě během hospitalizace – doporučujeme poučení a instruktáž k doporučené pohybové rehabilitaci, tzn. během prvních 14 dní po transplantaci;
- Žádoucí je třeba předem znát zdravotní stav pacienta po fyzické i psychické stránce a dodržovat individuální přístup;
- Pokud není první kontakt s pacientem již během po-transplantační hospitalizace, doporučujeme zjistit první ambulantní kontrolu na transplantačním pracovišti;
- Samotní pacienti uvádějí, že by informace ohledně doporučené pohybové aktivity a dietního režimu měli dostat ihned po transplantaci a v psané formě (131);
- Pokud je to jenom trochu možné, je vhodné pacienta kontaktovat předem telefonicky a domluvit si s ním setkání v konkrétní hodinu tak, aby to vyhovovalo jeho celodennímu plánu;
- Cílem prvního setkání je dostatečně a srozumitelně informovat pacienta o všech aspektech jeho účasti v pohybovém programu. Vzhledem k tomu, že pohybový program není součástí běžné po-transplantační péče, je nutné mít s účastí v programu písemné souhlasné stanovisko pacienta (tzv. informovaný souhlas);
- Dalším cílem prvního setkání je zjistit jak je na tom pacient s pohybovou aktivitou a případně s potížemi pohybového systému; pro stanovení úrovně aktivity pacienta jsou používány různé ankety a dotazníky, ale je možné potřebné informace získat i vedeným rozhovorem;
- V případě, že pacient s účastí v programu souhlasí a jeho stav účast umožňuje, následuje krátké úvodní sdělení obsahující základní instrukce o vhodných pohybových aktivitách, které může provádět pacient samostatně ještě před vstupním testováním. K tomu pacient obdrží podrobný instruktážní text popisující jak celý pohybový program, tak vhodné pohybové aktivity, jejich kontraindikace a situace, kdy cvičení není vhodné, a soubor kompenzačních cviků s popisem a nákresy;
- Samotní pacienti uvádějí, že by pohybový program měl začínat postupně mezi 1. týdnem až 1. měsícem po transplantaci (131);
- Pokud není již na první setkání domluvené zároveň i vstupní testování, pro udržení kontinuity je vstupní testování předběžně domluveno na další pacientovu návštěvu transplantačního centra;
- U pacientů po transplantaci ledviny by z důvodů náhlých změn způsobených chirurgickým zákrokem a umístěním ledvinného štěpu na místo k tomu nejvhodnějším, ale nefyziologické, by součástí pohybového programu měla být také dechová cvičení a cvičení zaměřená na stabilizační funkci posturálního systému. V případě výskytu určitých poruch pohybového systému by pacient měl být veden v počáteční fázi programu fyzioterepeutem, aby při nevhodném provádění cviků nedocházelo ke zhoršování dekompenzovaného stavu (133).
Soubor vyšetřených nemocných, metodika a léčebné postupy
Kazuistika
Muž, 52 let. Chronické selhání ledvin, na podkladě biopticky ověřené membranoproliferativní glomerulonefrity, léčen hemodialýzou, cca po 3 letech od začátku dialyzační léčby byla provedena kadaverózní transplantace ledviny .
Sport: 5x týdně-badminton, golf, tenis, volejbal (problémy se schuntem), squash, 2x týdně fitness, do 35ti let vrcholově fotbal.
Před transplantací musel sporty vyřazovat podle fyzické náročnosti.
Po transplantaci 3 měsíce hospitalizován pro esofagitidu a gastritidu.
Individuální fyzioterapie zahájena cca 10 měsíců po transplantaci.
Subjektivní obtíže s pohybovým aparátem: pozátěžová bolest v oblasti Lsp s iradiací do pravé kyčle, bolest pod pravou lopatkou, občas bolest v oblasti Cp – více vpravo.
Vyšetření pohybového aparátu: bolest pod pravou lopatkou a v obl. Cp., blokáda 1. a 2., žebra, 4., 5., 6. žebro., blok C2-3, Cthp, Th8-9, 10-11, ThLp; spasmus m. levator scapule, trp´s v m. trapezius pars ascendens, mm. rhomboidei, spasmus m. psoas major dx, m. quadratus lumborum, m. piriformis – vše vpravo; v pravém dolním kvadrantu klidná jizva po tranplantaci.
Použité medoty fyzioterapie: odstranění funkčních poruch (blokád a spasmů) technikami manuální medicíny (mobilizační techniky, techniky měkkých tkání, postizometrická relaxace, reciproční inhibice), uvolnění břišní stěny, facilitace fyzio-logického vzoru dechové a posturální funkce, potažmo i nitrobřišního tlaku zajišťující mobilitu a motilitu vnitřních orgánů pomocí metod na neurofyziologickém podkladě. Pacient byl také instruován o domácí autoterapii. Pacient docházel na individuální fyzioterapii 1x týdně po dobu 6 týdnů. Došlo k odstranění funkčních poruch, pacient byl zaučen do autoterapie pro případ lehčích recidiv subjektivních obtíží. Terapie byla ukončena po odstranění obtíží s pohybovým aparátem.
DISKUSE A ZÁVĚR
Výše zmíněné studie o vyšetření a doporučení týkající se pohybového systému a pohybových aktivit (PA) u pacientů s CHSL jasně ukazují, že by fyzioterapeutická péče, ať už individuální nebo skupinová, měla být standardně zahrnutá jako součást jejich multioborové léčebné péče. Podle Johansen a Painter (49) bychom si minimálně měli uvědomit, že ošetřující lékař-nefrolog nemá v rámci lékařské kontroly časovou kapacitu, přehled či náklonnost k vysvětlování přínosů a doporučení k pohybovým aktivitám (PA). V případě setkání se s dialyzovaným nebo transplantovaným jedincem v rámci fyzioterapeutické praxe je vhodné se vždy zeptat na typ a objem vykonávané běžné a volnočasové PA, pomoci při volbě PA, jako první volbu PA zvolit pokud možno chůzi (pokud pacient nemá nestabilní oběhové či metabolické potíže, potíže se stabilitou), doporučit edukační materiály, popř. odkázat na specialistu z oblasti fyzioterapie u CHSL („renal rehabilitation“) anebo rehabilitace pro kardiaky.
Cvičení během hemodialýzy a fyzioterapeutická péče není v českých dialyzačních střediscích pro pacienty běžně dostupná. Ukazuje se, že pacienti dobře tolerují fyzickou zátěž a v oblasti kvality života dochází k určitým funkčním a psychickým zlepšením. Pohybová aktivita v průběhu dialýzy, při dodržení doporučených zásad, neohrožuje pacienta v jeho zdravotním stavu. Dialyzované jedince lze označit jako zvláštní skupinu pacientů s vysokým výskytem určitých poruch pohybového systému (MSD – musculoskeletal disorders) a je vhodné zvážit zařazení fyzioterapeutické intervence do standardní péče o tyto jedince. Problematika poruch pohybového systému u dialyzovaných pacientů zatím není na půdě českého zdravotnictví dostatečně řešená.
V návaznosti na zahraniční studie citujeme (112): „Bolestivé problémy pohybového ústrojí omezují a zneschopňují i zdravé jedince. V kombinaci s vícečetnými zdravotními problémy, které se vyskytují u dialyzovaných pacientů, může přítomnost bolesti rychle vést k dekondici a snížení funkčních schopností. Fyzioterapeuti mohou pomoci dialyzovaným pacientům k co nejbezpečnější a nejdéle trvající mobilitě. Role fyzioterapeuta je v multidisciplinární péči o hemodialyzované pacienty nezastupitelná“.
Hlavním cílem péče o pohybový systém dialyzovaného pacienta je zajistit jeho co nejdéle trvající soběstačnost a sebeobsluhu, oddálit závislost na pomoci druhých a v sociálně-ekonomické sféře ušetřit náklady spojené s případnou péčí o tyto pacienty.
Ačkoliv je transplantace ledviny nejdokonalejším způsobem léčby chronického selhání ledvin, nezaručuje pacientům okamžitý a jednoznačný návrat do běžného života. Je třeba, aby pacienti věděli, že je péče o jejich pohybový systém a fyzickou kondici důležitou součástí jejich léčby (107). Pacienti po transplantaci ledviny mají lepší úroveň funkční fyzické kondice než pacienti dlouhodobě léčení dialýzou, ale stále tato úroveň nedosahuje normativních hodnot zdravé populace. Nejnižší úroveň byla prokázána v komponentě aerobní zdatnosti a nejvyšší úroveň v komponentě ohebnosti/flexibility (horních a dolních končetin).
Součástí zdravotní péče o tyto pacienty by měla být vhodná pohybová intervence zlepšující kondici pacientů a napomáhající tak návratu do běžného života. Vzhledem ke zdravotním a organizačním specifikům této populace není pohybová intervence běžně součástí jejich zdravotní péče.
Aby byla zajištěna „přiměřenost“ pohybové aktivity, měl by být pacient v pohybovém programu veden někým, kdo pacienta o pohybové aktivitě dostatečně informuje, průběžně kontroluje jeho stav a správnost provádění aktivity (charakter, intenzitu, atd.). Zátěžový fyziolog/tělovýchovný lékař/fyzioterapeut či rehabilitační pracovník však není v ČR, ani pokud je nám známo z evropských a světových dialyzačních středisek, běžně součástí nefrologického týmu. Běžně používané měření kapacity tělesné zátěže, jako je spiro-ergometrické vyšetření (zjištění maximální spotřeby kyslíku, maximální tepové frekvence atd.) není pro specifika této populace (riziko maximální zátěže atd.) pro tyto pacienty běžně a jednoduše dostupné. Jednoduché a srozumitelné hodnocení fyzické kondice může pacienty ujistit ve zlepšení jejich fyzické kondice a podpořit tak jejich motivaci k pohybovým aktivitám (36, 59).
V rámci individuální a skupinové fyzioterapie pacientů s poruchou ledvin je potřeba vycházet z výše zmíněných faktů. Pro zlepšení mobility a motility vnitřních orgánů, potažmo i ledvin samotných, které jsou pro jejich funkci nezbytné, je důležité odstranit funkční změny pohybového aparátu, jako jsou blokády kloubů páteře, sternokostálních a kostovertebrálních kloubů, stejně tak jako nastolit rovnováhu svalové funkce. Nemalou roli zde hraje uvolnění břišní stěny a vazivového aparátu viscerálních orgánů. Bránice je hlavním dechovým svalem, má významný podíl na stabilizační funkci bederní páteře (33, 46, 57) a prostřednictvím ovlivňování nitrobřišního tlaku také na kontinenci (129). Zde se nám jeví jako podstatná funkce bránice, která se značně podílí na výše zmíněné mobilitě vnitřních orgánů, kdy během inspirace dochází ke kaudálnímu pohybu vnitřních orgánů se současným zvýšením nitrobřišního tlaku (129, 144). Aby bránice mohla optimálně plnit všechny své funkce, včetně zajištění mobility vnitřních orgánů, je potřeba optimální koordinace svalové souhry s ostatními svaly břišní stěny. Během optimálního dechového stereotypu jsou břišní svaly synergisty bránice, bez nichž by její inspirační funkce byla mnohem méně efektivní. Mírná kontrakce břišních svalů zpevněním břišní stěny vytvoří oporu pro vnitřní orgány, a tím i pro další akci bránice. Optimální funkce břišního svalstva brání vyklenutí břišní stěny. Bez této funkce břišních svalů by orgány břišní dutiny byly stlačeny dolů a dopředu a neumožnily by tak dostatečnou stabilizaci bránice a současně by byla narušena jejich mobilita. Pokud je břišní stěna neaktivní, nádech jde pouze do břicha a do hrudníku již nepostupuje (141).
Poděkování
Tento článek byl zpracován za podpory grantového projektu GAČR P407/12/0166 s názvem„Determinanty fyzických a psychických funkcí jedinců s chronickým selháním ledvin a po transplantaci ledvin“ a výzkumného projektu PRVOUK P38 “Biologické aspekty zkoumání lidského pohybu”. Oba projekty jsou součástí výzkumné aktivity Fakulty tělesné výchovy a sportu Univerzity Karlovy v Praze.
Adresa pro korespondenci:
PhDr. Andrea Mahrová, Ph.D.
Laboratoř sportovní motoriky
Fakulta tělesné výchovy a sportu UK
J. Martího 31
162 52 Praha 6
e-mail: mahrova@centrum.cz
Sources
1. ACSM.: ACSM Position stand on Exercise and Physical activity for Older Adults. Medicine and Science in Sports and Exercise, roč. 30, 1998, č. 6, s. 992-1008.
2. ACSM.: Guidelines for exercise testing and prescription. Philadelphia, Lea&Febinger, 1991.
3. ACSM.: Physical Fitness Testing. In: ACSM´s Guidelines for Exercise Testing and Prescription. Philadelphia, Williams&Wilkins,1995.
4. Balakrishnan, V. S., Rao, M., Menon, V., Gordon, P. L., Pilichowska, M., Castaneda, F., Castaneda-Sceppa, C.: Resistance training increases muscle mitochondrial biogenesis in patients with chronic kidney disease. Clin. J. Am. Soc. Nephrol., roč. 5, 2010, č. 6, s. 996-1002.
5. BARRAL, J. P.: Visceral manipulation. Vista, California: Eastland Press, 2005.
6. Besnier, F., Laruelle, E., Genestier, S., Gié, S., Vigneau, C., Carré, F.: Effects of exercise training on ergocycle during hemodialysis in patients with end stage renal disease: Relevance of the anaerobic threshold intensity. Nephrol. Ther., roč. 8, 2012, č. 4, s. 231-237.
7. BETO, J. A., BANSAL, V. K.: Interventions for other risk factors: Tobacco use, physical inactivity, menopause, and homocysteine. Am. J. Kidney Dis., roč. 32, 1998, Suppl. 3, s. S172-S184.
8. Borg, G. A.: Psychophysical bases of perceived exertion. Med. Sci. Sports Exerc., roč. 14, 1982, č. 5, s. 377-387.
9. Boyce, M. L., Robergs, R. A., Avasthi, P. S., Roldan, C., Foster, A., Montner, P., Stark, D., Nelson, C.: Exercise training by individuals with predialysis renal failure: cardiorespiratory endurance, hypertension, and renal function. Am. J. Kidney Dis., roč. 30, 1997, č. 2, s. 180-192.
10. Bradford, E.: Physiotherapy and renal failure. Physiotherapy, roč. 59, 1973, č. 5, s. 146-148.
11. Brahee, D. D., Guebert, G. M., Virgin, B.: Dialysis-related spondyloarthropathy. J. Manipulative Physiol. Ther., roč. 24, 2001, č. 2, s. 127-130.
12. Brennan, B.: Combined resistance and aerobic training is more effective than aerobic training alone in people with coronary artery disease. J. Physiother., roč. 58, 2012, č. 2, s. 129.
13. Bulckaen, M., Capitanini, A., Lange, S., Caciula, A., Giuntoli, F., Cupisti, A.: Implementation of exercise training programs in a hemodialysis unit: effects on physical performance. J. Nephrol., roč. 24, 2011, č. 6, s. 790-797.
14. Bullani, R., El-Housseini, Y., Giordano, F., Larcinese. A., Ciutto, L., Bertrand, P. C., Wuerzner, G., Burnier, M., Teta, D.: Effect of intradialytic resistance band exercise on physical function in patients on maintenance hemodialysis: a pilot study. J. Ren. Nutr., roč. 21, 2011, č. 1, s. 61-65.
15. Burra, P., De Bona, M., Germani, G. et al.: The Concept of quality of life in organ transplantation. Transplantation Proceedings, roč. 39, 2007, č. 7, s. 2285-2287.
16. Carney, R. M., Mc Kevitt, P. M., Goldberg, A. P., Hagberg, J., Delmez, J. A., Harter, H. R.: Psychological effects of exercise training in hemodialysis patients. Nephron, roč. 33, 1983, č. 3, s. 179-181.
17. Carney, R. M., Templeton, B., Hong, B. A., Harter, H. R., Hagberg, J. M., Schechtman, K. B., Goldberg, A. P.: Exercise training reduces depression and increases the performance of pleasant activities in hemodialysis patients. Nephron, roč. 47, 1987, č. 3, s. 194-198.
18. Castaneda, C., Gordon, P. L., Parker, R.C., Uhlin, K. L., Roubenoff, R., Levey, A. S.: Resistance training to reduce the malnutrition-inflammation complex syndrome of chronic kidney disease. Am. J. Kidney Dis., roč. 43, 2004, č. 4, s. 607-616.
19. Castaneda, C., Gordon, P. L., Uhlin, K. L., Levey, A. S., Kehayias, J. J., Dwyer, J. T., Fielding, R. A., Roubenoff, R., Singh, M. F.: Resistance training to counteract the catabolism of a low-protein diet in patients with chronic renal insufficiency. A randomized control trial. Ann. Intern. Med., roč. 135, 2001, č. 11, s. 965-976.
20. Castaneda, C., Grossi, L., Dwyer, J.: Potential benefits of resistance exercise training on nutritional status in renal failure. J. Ren. Nutr, roč. 8, 1998, č. 1, s. 2-10.
21. Clyne, N., Ekholm, J., Jogestrand, T., Lins, L. E., Pehrsson, S. K.: Effects of exercise training in predialytic uremic patients. Nephron, roč. 59, 1991, č. 1, s. 84-89.
22. Colangelo, R. M., Stillman, M. J., Kessler-Fogil, D.: The role of exercise in rehabilitation for patients with end-stage renal disease. Rehabil. Nurs, roč. 22, 1997, č. 6, s. 288-292, 302.
23. Couto, C. I.: Exercise training improves cardiovascular fitness in people receiving haemodialysis for chronic renal disease. J. Physiother., roč. 58, 2012, č. 2, s. 130.
24. Cristofolini, T., Draibe, S., Sesso, R.: Evaluation of factors associated with chronic low back pain in hemodialysis patients. Nephron Clin. Pract., roč. 108, 2008, č. 4, s. c249-c255.
25. Curtin, R. B., Lowrie, E. G., DeOreo, P. B.: Self-reported functional status: an important predictor of health outcomes among end-stage renal disease patients. Adv. Ren. Replace Ther, roč. 6, 1999, č. 2, s. 133-140.
26. Daul, A. E. et al.: Sport - und Bewegungstherapie für chronisch Nierenkranke. Munchen, Dustri – Verlag, 1997.
27. Daul, A. E., Schäfers, R. F., Daul, K., Philipp, T.: Exercise during hemodialysis. Clin. Nephrol, roč. 61, 2004, Suppl 1, s. 26-30.
28. Dobsak, P., Homolka, P., Svojanovsky, J., Reichertova, A., Soucek, M., Novakova, M., Dusek, L., Vasku, J., Eicher, J.C., Siegelova, J.: Intra-dialytic electrostimulation of leg extensors may improve exercise tolerance and quality of life in hemodialyzed patients. Artif Organs, roč. 36, 2012, č. 1, s. 71-78.
29. Eidemark, I., Haaber, A. B., Feldt-Rasmussen, B., Kanstrup, I. L., Strandgaard, S.: Exercise training and the progression of chronic renal failure. Nephron, roč. 75, 1997, č. 1, s. 36-40.
30. FISCHEROVÁ, H., STABLOVÁ, A.: Kineziologický rozbor u chronicky dialyzovaných nemocných. Prakt. Lék., roč. 82, 2002, č. 10, s. 579-654.
31. Fuhrmann, I., Krause, R.: Principles of exercising in patients with chronic kidney disease, on dialysis and for kidney transplant recipients. Clin. Nephrol., roč. 61, 2004, Suppl 1, s. 14-25.
32. Gallagher-Lepak, S.: Functional capacity and activity level before and after renal transplantation. ANNA J., roč. 18, 1991, č. 4, s. 378-82; discussion 382, 406.
33. GANDEVIA, S. C., BUTLER, J., HODGES, P. W., TAYLOR, J.: Balancing acts: Respiratory sensations, motor control ad human posture. In Experimental Biology 2001 Symposium on Somatic Sensation During Movement and its Role in Autonomic Control. USA, 2001, s. 118-121.
34. Goldberg, A. P., Geltman, E. M., Hagberg, J. M., Gavin, J. R. 3rd, Delmez, J. A., Carney, R. M., Naumowicz, A., Oldfield, M. H., Harter, H. R.: Therapeutic benefits of exercise training for hemodialysis patients. Kidney Int, roč. 16, 1983, Suppl., s. 303-309.
35. Gołębiowski, T., Kusztal, M., Weyde, W., Dziubek, W., Woźniewski, M., Madziarska, K., Krajewska, M., Letachowicz, K., Strempska, B., Klinger, M.: A program of physical rehabilitation during hemodialysis sessions improves the fitness of dialysis patients. Kidney Blood Press Res., roč. 35, 2012, č. 4, s. 290-296.
36. Goodman, E. D., Ballou, M. B.: Perceived barriers and motivators to exercise in hemodialysis patients. Neph. Nurs J., roč. 31, 2004, č. 1, s. 23-29.
37. Gordon, L., Mc Growder, D. A., Pena, Y. T., Cabrera, E. and Lawrence-Wright, M. B.: Effect of exercise therapy on lipid parameters in patients with End-stage renal disease on hemodialysis. J. Lab. Physicians, roč. 4, 2012, č. 1, s. 17-23.
38. Gordon, L., Mc Growder, D. A., Pena, Y. T., Cabrera, E., Lawrence-Wright, M. B.: Effect of yoga exercise therapy on oxidative stress indicators with end-stage renal disease on hemodialysis. Int. J. Yoga, roč. 6, 2013, č. 1, s. 31-38.
39. Gregory, S. M., Headley, S. A., Germain, M., Flyvbjerg, A., Frystyk, J., Coughlin, M. A., Milch, C. M., Sullivan, S., Nindl, B. C.: Lack of circulating bioactive and immunoreactive IGF-1 changes despite improved fitness in chronic kidney disease patients following 48 weeks of physical training. Growth Horm IGF Res., roč. 21, 2011, č. 1, s. 51-56.
40. Gutman, R. A., Stead, W. W., Robinson, R. R.: Physical capacity and employment status in patients on maintenance dialysis. Engl. J. Med., roč. 304, 1981, č. 6, s. 309-313.
41. Hagberg, J. M., Goldberg, A. P., Ehsani, A. A., Heath, G. W., Delmez, J. A., Harter, H. R.: Exercise training improves hypertension in hemodialysis patients. Am. J. Nephrol., roč. 3, 1983, č. 4, s. 209-212.
42. HEBGEN, E.: Visceral manipulation in osteopathy. Georg Thieme Verlag KG, 2010.
43. Heiwe, S., Jacobson, S. H.: Exercise training in adults with CKD: a systematic review and meta-analysis. Am. J. Kidney Dis. , roč. 64, 2014, č. 3, s. 383-393.
44. Heiwe, S., Tollback, A., Clyne, N.: Twelve weeks of exercise training increases muscle function and walking capacity in elderly predialysis patients and healthy subjects. Nephron, roč. 88, 2001, č. 1, s. 48-56.
45. Heiwe, S., Tollin, H.: Patients‘ perspectives on the implementation of intra-dialytic cycling -a phenomenographic study. Implement Sci., roč. 25, 2012, č. 7, s. 68.
46. HODGES, P. W., GANDEVIA, S. C., RICHARDSON, C.: Contractions of specific abdominal muscles in postural tasks are affected by respiratory maneuvers. J. Appl. Physiol., roč. 83, 1997, č. 3, s. 753-760.
47. Cheema, B. S., Singh, M. A.: Exercise training in patients receiving maintenance hemodialysis: a systematic review of clinical trials. Am. J. Nephrol., roč. 25, 2005, č. 4, s. 352-364.
48. Jetté, M., Posen, G., Cardarelli, C.: Effects of an exercise programme in a patient undergoing hemodialysis treatment. J. Sports Med. Phys. Fitness, roč. 17, 1977, č. 2, s. 181-186.
49. Johansen, K. L, Painter, P.: Exercise in individuals with CKD. Am. J. Kidney Dis., roč. 59, 2012, č. 1, s. 126-134.
50. Johansen, K. L.: Exercise in the end-stage renal disease population. J. Am. Soc. Nephrol., roč. 18, 2007, č. 6, s. 1845-1854.
51. JOHANSEN, K. L.: Physical functioning and exercise capacity in patients on dialysis. Adv. Ren. Replace Ther., roč. 6, 1999, č. 2, s. 141-148.
52. Johansen, K. L.: Exercise and dialysis. Scholarly Review. Hemodyalisis Int. roč. 12, 2008, č. 3, s. 290-300.
53. JUROVÁ, K., MAHROVÁ, A., BUNC, V.: Poruchy pohybového systému dialyzovaných jedinců. Rehabilitácia, roč. 46, 2009a, č. 2, s. 76-86.
54. JUROVÁ, K., MAHROVÁ, A., BUNC, V. : Funkční vyšetření pohybového systému hemodialyzovaných jedinců. Rehabilitácia, roč. 46, 2009b, č. 3, s. 155-163.
55. Juskowa, J., Lewandowska, M., Bartłomiejczyk, I., Foroncewicz, B., Korabiewska, I., Niewczas, M., Sierdziński, J.: Physical rehabilitation and risk of atherosclerosis after successful kidney transplantation. Transpl. Proc., roč. 38, 2006, č. 1, s. 157-160.
56. Kjaer, M., Beyer, N., Secher, N. H.: Exercise and organ transplantation. Scand. J. Med. Sci. Sports, roč. 9, 1999, č. 1, s. 1-14.
57. KOLÁŘ, P.: Facilitation of agonist-antagonist co-activation by reflex stimulation methods. In Rehabilitation of the Spine - a Practitioners Manual 2. Craig Liebenson. Los Angeles Lippincott Williams&Wilkins, 2006.
58. Konstantinidou, E., Koukouvou, G., Kouidi, E., Deligiannis, A., Tourkantonis, A.: Exercise training in patients with end stage renal disease on hemodialysis:comparison of three rehabilitation programs. J. Rehabil. Med., roč. 34, 2002, č. 1, s. 40-45.
59. Kontos, P. C., Miller, K. L., Brooks, D., Jassal, S. V., Spanjevic, L., Devins, G. M., De Souza, M. J., Heck, C., Laprade, J., Naglie, G.: Factors influencing exercise participation by older adults requiring chronic hemodialysis: a qualitative study. Int. Urol. Nephrol., roč. 39, 2007, č. 4, s. 1303-1311.
60. Korabiewska, L., Lewandowska, M., Juskowa, J., Białoszewski, D.: Need for rehabilitation in renal replacement therapy involving alloveneic kidney transplantation. Transpl. Proc., roč. 39, 2007, č. 9, s. 2776-2777.
61. Kouidi, E., Albani, M., Natsis, K., Megalopoulos, A., Gigis, P., Guiba-Tziampiri, O., Tourkantonis, A., Deligiannis, A.: The effects of exercise training on muscle atrophy in hemodialysis patients. Nephrol. Dial. Transplant., roč. 13, 1998, č. 3, s. 685-699.
62. Kouidi, E., Grekas, D., Deligiannis, A., Tour-kantonis, A.: Outcomes of long-term exercise training in dialysis patients: comparison of two training programs. Clin. Nephrol., roč. 61, 2004, Suppl 1, s. 31-38.
63. Kouidi, E., Iacovides, A., Iordanidis, P., Vassiliou, S., Deligiannis, A., Ierodiakonou, C., Tourkantonis, A.: Exercise renal rehabilitation program: Psychosocial effects. Nephron, roč. 77, 1997, č. 2, s. 152-158.
64. Kouidi, E.: Central and peripheral adaptations to physical training in patiens with end-stage renal disease. Sports Med.., roč. 31, 2001, č. 9, s. 651-665.
65. Kouidi, E.: Exercise training in dialysis patients: Why, when and how? Artif. Organs., roč. 26, 2002, č. 12, s. 1009-1113.
66. Krause, R.: Körperliches Training während Hämodialyse. Nieren - und Hochdruckkr, roč. 18, 1989, s. 411.
67. KRAUSE, R.: Körperzusammensetzung und kardio-pulmonale Leistungsfähigkeit bei chronischen Dialysepatienten und bei Nierentransplantierten. In. FRANZ, I. W., MELLEROWICZ, H., NOACK, W.: Training und Sport zur Prävention und Rehabilitation in der technisiert Umwelt. Springer: Berlin, 1985, s. 579-583.
68. KUCHERA, M. L., KUCHERA, W. A.: Osteopathic considerations in systemic dysfunction. Columbus, OH: Greydon Press, 1994.
69. Kutner, N. G., Lin, L. S., Fielding, B., Brogan, D., Hall, W. D.: Continued survival of older hemodialysis patients: investigations of psychosocial predictors. Am. J. Kidney Dis., roč. 24, 1994, č. 1, s. 42-49.
70. Kutner, N. G.: Promoting functioning and well-being in older CKD patients: review of recent evidence. Int. Urol. Nephrol., roč. 40, 2008, č. 4, s. 1151-1158.
71. Kutner. N. G., Jasal, S. V.: Quality of life and rehabilitation of elderly dialysis patients. Seminars in Dialysis, roč. 15, 2002, č. 2, s. 107-112.
72. LACERDA, G., KRUMMEL, T., HIRSCH, E.: Neurologic presentations of renal diseases. Neurol. Clin., roč. 28, 2010, č. 1, s. 45-59.
73. Lachmanová, J.: Statistická ročenka dialyzační léčby v České republice pro rok 1999. Česká nefrologická společnost, Praha, 2000.
74. Lachmanová, J.: Statistická ročenka dialyzační léčby v České republice pro rok 2004. Česká nefrologická společnost, Praha, 2005.
75. Leehey, D. J., Moinuddin, I., Bast, J. P., Qureshi, S., Jelinek, C. S., Cooper, C., Edwards, L. C., Smith, B. M., Collins, E. G.: Aerobic exercise in obese diabetic patients with chronic kidney disease: a randomized and controlled pilot study. Cardiovasc. Diabetol., roč. 8, 2009, s. 62.
76. Lennon, D. L., Shrago, E., Madden, M., Nagle, F., Hanson, P., Zimmerman, S.: Carnitine status, plasma lipid profiles, and exercise capacity of dialysis patients: effect of a submaximal exercise program. Metabolism, roč. 35, 1986, č. 8, s. 728-735.
77. LEVEY, A. S., BETO, J. A., CORONADO, B. E. et al.: Cotrolling the epidemic of cardiovascular disease in chronic renal disease: What do we know? What do we need to learn? Where do we go from here? Am. J. Kidney Dis., roč. 32, 1998, č. 5, s. 853-906.
78. LEWIT, K.: Manipulační léčba v myoskeletální medicíně. Sdělovací technika, spol. s.r.o. ve spoluprácí s ČLS J. E. Purkyně, Praha 2003, 411 s.
79. Lisý, Z., TomáŠek, R.: Tříleté sledování změn krevního obrazu při submaximální zátěži u nemocných v pravidelném dialyzačním léčení. Sborník lékařský, roč. 78, 1976, č. 8, s. 230-240.
80. Macdonald, J. H., Kirkman, D., Jibani, M.: Kidney transplantation: a systematic review of interventional and observational studies of physical activity on intermediate outcomes. Adv. Chronic. Kidney Dis., roč. 16, 2009, č. 6, s. 482-500.
81. Mahrová, A., Bunc, V., Panáček, V., Prajsová, J.: Pohybová rehabilitace při hemodialýze – praktické zkušenosti. Aktuality v nefrologii, roč. 15, 2009, č. 1, s. 16-24.
82. Mahrová, A., Bunc, V., Fischerová, H.: Možnosti vyšetření funkčního stavu pohybového systému pacientů s chronickým selháním ledvin. Čas. Lék. Čes., roč. 145, 2006, č. 10, s. 782-787.
83. MAHROVÁ, A., JUROVÁ, K., PRAJSOVÁ, J., BUNC, V.: Význam fyzioterapie u jedinců s chronickým selháním ledvin. Rehabilitace a fyzikální lékařství, roč. 16, 2009, č. 4, s. 155-164.
84. Matoušová, M.: Zdravotní tělesná výchova I. Praha, Sport pro všechny, 1992.
85. MAUE, M.: Untersuchungen zur Leistungsfähigkeit von chronisch nierenkranken und niereninsuffizienten Patienten und ihre Beeinflussbarkeit durch Training. Medizin und Sport, 1983, 23, s. 155-157.
86. Medical Education Institut: Exercise for the Dialysis Patient. 1995. http://lifeoptions.org/catalog/pdfs/booklets/pro_prescguide.pdf.
87. Mercer, T. H., Koufaki, P., Naish, P. F.: Nutritional status, functional capacity and exercise rehabilitation in end-stage renal disease. Clin. Nephrol., roč. 61, 2004, Suppl 1, s. 54-59.
88. Miller, B. W., Cress, C. L., Johnson, M. E., Nichols, D. H., Schnitzler, M. A. Exercise during hemodialysis decreases the use of antihypertensive medications. Am. J. Kidney Dis., roč. 39, 2002, č. 4, s. 828-833.
89. Miller, T. D., Squires, R. W., Gau, G. T., Ilstrup, D. M., Frohnert, P. P., Sterioff, S.: Graded exercise testing and training after renal transplantation: a preliminary study. Mayo Clin. Proc., roč. 62, 1987, č. 9, s. 773-777.
90. Moinuddin, I., Leehey, D. J.: A comparison of aerobic exercise and resistance training in patients with and without chronic kidney disease. Adv. Chronic. Kidney Dis., roč. 15, 2008, č. 1, s. 83-96. Review.
91. Moons, P., Vanrenterghem, Y., Van Hooff, J. P., Squifflet, J. P., Margodt, D., Mullens, M., Thevissen, I., De Geest, S.: Health-related quality of life and symptom experience in tacrolimus-based regiment after renal transplantation: a multicentre study. Transpl. Int., roč. 16, 2003, č. 9, s. 653-664.
92. Mustata, S., Groeneveld, S., Davidson, W., Ford, G., Kiland, K., Manns, B.: Effects of exercise training on physical impairment, arterial stiffness and health-related quality of life in patients with chronic kidney disease: a pilot study. Int. Urol. Nephrol., roč. 43, 2011, č. 4, s. 1133-1141.
93. National Institutes for Health.: Exercise and Physical activity. 2011. http://www.nia.nih.gov/health/publication/exercise-physical-activity/introduction.
94. Nelson, M. E., Rejeski, W. J., Blair, S. N., Duncan, P. W., Judge, J. O., King, A. C., Macera, C. A., Castaneda-Sceppa, C.: American College of Sports Medicine; American heart association: physical activity and public health in older adults: recommendation from the American College of Sports Medicine and the American Heart Association. Circulation, roč. 116, 2007, č. 9, s. 1094-1105.
95. Oh-Park, M., Fast A, Gopal, S. Lynn, R., Frei, G., Drenth, R., Zohman, L.: Exercise for the dialyzed - Aerobic and strenght training during hemodialysis. Am. J. Phys. Med. Rehabil., roč. 81, 2002, č. 11, s. 814-821.
96. Oliveros, R. M. S., Avendaño, M., Bunout, D., Hirsch, S., De La Maza, M. P., Pedreros, C., Müller, H.: A pilot study on physical training of patients in hemodialysis. Rev. Med. Child, roč. 139, 2011, č. 8, s. 1046-1053.
97. Orcy, R. B., Dias, P. P., Seus, T. L., Barcellos, F. C., Bohlke, M.: Combined resistance and aerobic exercise is better than resistance training alone to improve functional performance of haemodialysis patients - Results of a randomized controlled trial. Physiother. Res., roč. 17, 2012, č. 4, s. 235-243.
98. Ouzouni, S., Kouidi, E., Sioulis, A., Grekas, D., Deligiannis, A.: Effects of intradialytic. Rehabil., roč. 23, 2009, č. 1, s. 53-63.
99. Painter P., Zimmermann S. W.: The role of exercise in the long therm rehabilitation of patients with end stage renal disease. AANNT J., roč. 10, 1983, č. 6, s. 41-46.
100. Painter, P. L., Hector, L., Ray, K., Lynes, L., Dibble, S., Paul, S. M., Tomlanovich, S. L., Ascher, N. L.: A randomized trial of exercise training following renal transplantation. Transplantation, roč. 74, 2002, č. 1, s. 42-48.
101. Painter, P. L., Luetkemeier, M. J., Moore, G. E., Dibble, S. L., Green, G. A., Myll, J. O., Carlson, L. L.: Health-related fitness and quality of life in organ transplant recipients. Clin. Transpl., roč. 64, 1997, č. 12, s. 1795-1800.
102. Painter, P. L., Nelson-Worel, J. N., Hill, M. M., Thornbery, D. R., Shelp, W. R., Harrington, A. R., Weinstein, A. B.: Effects of exercise training during hemodialysis. Nephron, roč. 43, 1986, č. 2, s. 87-92.
103. Painter, P., Carlson, L., Carey, S., Paul, S. M., Myll, J.: Physical functioning and health-related quality of life changes with exercise training in hemodialysis patients. Am. J. Kidney Dis., roč. 35, 2000, č. 3: s. 482-492.
104. Painter, P., Hanson, P., Messer-Rehak, D., Zimmerman, S. W., Glass, N. R.: Exercise tolerance changes following renal transplantation. Am. J. Kidney Dis., roč. 10, 1987, č. 6, s. 452-456.
105. Painter, P., Krasnoff, J. B.: End-Stage Renal Disease: Chronic kidney disease and liver failure. In. Durstine KL et al. (eds.): ACSM´s Exercise Management for Persons with Chronic Diseases and Disabilities. Champaign IL, Human Kinetics, 2009.
106. Painter, P., Taylor, J., Wolcott, S., Krasnoff, J., Adey, D., Tomlanovich, S., Stock, P., Topp, K.: Exercise capacity and muscle structure in kidney recipient and twin donor. Clin. Transplant., roč. 17, 2003, č. 3, s. 225-230.
107. Painter, P.: Implementing exercise: what do we know? Where do we go? Adv. Chronic Kidney Dis., roč. 16, 2009, č. 6, s. 536-544. Review.
108. Painter, P.: Physical functioning in end-stage renal disease patients: update 2005. Hemodial., roč. 9, 2005, č. 3, s. 218-235.
109. Parsons, T. L., King-Van vlack, C. E.: Exercise and end-stage kidney disease: functional exercise capacity and cardiovascular outcomes. Adv. Chronic. Kidney Dis., roč. 16, 2009, č. 6, s. 459-481.
110. Parsons, T. L., Toffelmire, E. B., King-VanVlack, C. E.: The effect of an exercise program during hemodialysis on dialysis efficacy, blood pressure and quality of life in end-stage renal disease (ESRD) patients. Clin. Nephrol., roč. 61, 2004, č. 4, s. 261-274.
111. Pechter, U., Ots, M., Mesikepp, S., Zilmer, K., Kullissaar, T., Vihalemm, T., Zilmer, M., Maaroos, J.: Beneficial effects of water-based exercise in patients with chronic kidney disease. Int. J. Rehabil. Res., roč. 26, 2003, č. 2, s. 153-156.
112. Perryman, B., Harwood, L.: The role of physiotherapy in a hemodialysis unit. Nephro. Nurs J., roč. 31, 2004, č. 2, s. 215-216.
113. PIANTA, T. F.: The role of physical therapy in improving physical functioning of renal patients. Adv. Ren. Replace Ther., roč. 6, 1999, č. 2, s. 149-158.
114. Placheta, Z., Dohnalová I.: Zátěžová funkční diagnostika a preskripce pohybové léčby ve vnitřním lékařství. Brno, Vydavatelství Masarykovy univerzity, 1995.
115. Poortmans, J. R., Niset, G., Godefroid, C., Lamotte, M.: Responses to exercise and limiting factors in hemodialysis and renal transplant patiens. In Rieu, M. (ed). Physical Work kapacity in Organ transplantation. Med. Sport Sci., Karger Basel, 1998.
116. Ragnarsdóttir, M., Malmberg, E., Strandberg, E., Indridason, O. S.: Increased physical fitness among patients following endurance training during haemodialysis. Scand. J. Urol. Nephrol., roč. 46, 2012, č. 1, s. 54-57.
117. Ramaswamy, D., Efthimiou, P., Gnanasekharan, I., Soni, A.: Management of musculoskeletal complications in endstage renal disease: an update. Clin. Rheumatol., roč. 25, 2006, č. 4, s. 440-442.
118. Reboredo, M. d. e M., Pinheiro, B. d. o. V., Neder, J. A., Ávila, M. P., Araujo, E., Ribeiro, M. L., de Mendonça, A. F., de Mello, M. V., Bainha, A. C., Dondici Filho, J., de Paula, R. B.: Effects of aerobic training during hemodialysis on heart rate variability and left ventricular function in end-stage renal disease patients. J. Bras. Nefrol., roč. 32, 2010, č. 4, s. 367-373.
119. Reboredo, M. M., Neder, J. A., Pinheiro, B. V., Henrique, D. M., Faria, R. S., Paula, R. B.: Constant work-rate test to assess the effects of intradialytic aerobic training in mildly impaired patients with end-stage renal disease: a randomized controlled trial. Arch. Phys. Med. Rehabil., roč. 92, 2011, č. 12, s. 2018-2024.
120. Rečková, R.: Fyzická výkonnost pacientů v pravidelném dialyzačním léčení. Čas. Lék. Čes., roč. 128, 1989, č. 10, s. 315-317.
121. Rocha, E. R., Magalhães, S. M., de Lima, V. P.: Repercussion of physiotherapy intradialytic protocol for respiratory muscle function, grip strength and quality of life of patients with chronic renal diseases. J. Bras. Nefrol., roč. 32, 2010, č. 4, s. 355 - 366.
122. Röseler, E., Aurisch, R., Precht, K., Strangfeld, D., Priem, F., Siewert, H., Lindenau, K., RÖSELER, E.: Haemodynamic and metabolic responses to physical training in chronic renal failure. Proc. Eur. Dial. Transpl. Assoc., 1980, č. 17, s. 702-706.
123. Rychlik, I., Lopot, F.: Statistická ročenka dialyzační léčby v České republice v roce 2013. Česká nefrologická společnost, 2013.
124. Samara, A. P., Kouidi, E., Ouzouni, S., Vasileiou, S., Sioulis, A., Deligiannis, A.: Relationship between exercise test recovery indices and psychological and quality-of-life status in hemodialysis patients: a pilot study. J. Nephrol., roč. 26, 2013, č. 3, s. 495-501.
125. Segura-Ortí, E., Kouidi, E., Lisón, J. F.: Effect of resistance exercise during hemodialysis on physical function and quality of life: randomized controlled trial. Clin. Nephrol., roč. 71, 2009, č. 5, s. 527-537.
126. Segura-Ortí, E., Rodilla-Alama, V., Lisón, J. F.: Physiotherapy during hemodialysis: results of a progressive resistance-training program. Nefrologia, roč. 28, 2008, č. 1, s. 67-72.
127. Shalom, R., Blumenthal, J. A., Williams, R. S., McMurray, R. G., Dennis, V. W.: Feasibility and benefits of exercise training in patients on maintenance dialysis. Kidney Int., roč. 25, 1984, č. 6, s. 958-963.
128. Shalom, R., Blumenthal, J. A., Williams, R. S., McMurray, R. G., Dennis, V. W.: Feasibility and benefits of exercise training in patients on maintenance dialysis. Kidney Int., roč. 25, 1984, č. 6, s. 958-963.
129. SMITH, M. D., RUSSEL, A., HODGES, P. W.: Disorders of breathing and continence have astronger association with back pain than obesity and physical activity. Australian Journal of Physiotherapy, roč. 52, 2006, č. 1, s. 11-16.
130. SOTORNÍK, I. a kol.: Kostní choroba při nezvratném selhání ledvin. Praha, Scientia Medica, 1994.
131. Stanfill, A., Bloodworth, R., Cashion, A.: Lessons learned: experiences of gaining weight by kidney transplant recipients. Prog. Transplant., roč. 22, 2012, č. 1, s. 71-78.
132. SulkovÁ, S. a kol.: Hemodialýza. Praha, Maxdorf, 2000.
133. SVOBODA, L., MAHROVÁ, A.: Pohyb jako součást léčby dialyzovaných a transplantovaných pacientů. 1. vyd., Praha, Triton, 2009. s. 271.
134. Svoboda, L.: Rehabilitace pacientů po transplantaci a při dialýze. ZdN 1998; č. 34, s. 8-9.
135. SVOBODA, L.: Cvičební soubor pro dialyzované a transplantované pacienty. 1. vyd., Praha, Triton, 2000, 40 s.
136. Tawney, K. W., Tawney, P. J., Hladik, G., Hogan, S. L., Falk, R. J., Weaver, C., Moore, D. T., Lee, M. Y.: The life readiness program: A physical rehabilitation program for patients on hemodialysis. Am. J. Kidney Dis., roč. 36, 2000, č.3, s. 581-591.
137. Teplan, V., Jírů, F., Hájek, M., Mahrová, A., Švagrová, K., Racek, J., Štollová, M., Látová, I., Adamcová, J.: Pravidelné cvičení ovlivňuje tuk ve svalu měřený MR spektroskopií a kardiovaskulární riziko po transplantaci ledviny. Aktuality v Nefrologii, roč. 18, 2012, č. 2, s. 61-71.
138. Tomásek, R., Lisý, Z., Válek, A., Pick, P., Straková, M.: Oběhové a metabolické změny při submaximální zátěži u pacientů s chronickým selháním ledvin léčených v rámci pravidelného dialyzačního programu. Sborník lékařský, roč. 77, 1975, č. 9, s. 278-288.
139. Toyama, K., Sugiyama, S., Oka, H., Sumida, H., Ogawa, H.: Exercise therapy correlates with improving renal function through modifying lipid metabolism in patients with cardiovascular disease and chronic kidney disease. J. Cardiol., roč. 56, 2010, č. 2, s. 142-146.
140. van Vilsteren M. C., de Greef, M. H., Huisman, R. M.: The effects of a low to moderate intensity preconditioning exercise programme linked with exercise counselling for sedentary haemodialysis patients in The Netherlands: results of a randomized clinical trial. Nephrol. Dial. Transplant., roč. 20, 2005, č. 1, s. 141-146.
141. VÉLE, F.: Kineziologie. Praha, Triton, 2006.
142. Viklický, O., Janoušek, L., Baláž, P. et al: Transplantace ledviny v klinické praxi. Praha, Grada Publishing, 2008.
143. Williams, A., Stephens, R., McKnight, T., Dodd, S.: Factors affecting adherence of end-stage renal disease patients to an exercise programme. Br. J. Sports Med., roč. 25, 1991, č. 2, s. 90-93.
144. XI, M., LIU, M. Z., LI, Q. Q., CAI, L., ZHANG, L., HU, Y. H., AI, Z.: Analysis of abdominal organ motion using four-dimensional CT. Chinese Journal of Cancer, roč. 28, 2009, č. 9, s. 989-993.
145. Yurdalan, S. U.: Physiotherapy in patients on hemodialysis. In: Suzuki, Hiromichi. Hemodialysis. 1. vyd., Rijeka, In TechOpen, 2013, kapitola č. 38, s. 845-868.
146. Yurtkuran, M., Alp, A., Yurtkuran, M., Dilek, K.: A modified yoga-based exercise program in hemodialysis patients: A randomized controlled study. Complement Ther. Med., roč. 15, 2007, č. 3, s. 164-171.
147. Zabetakis, P. M., Gleim, G. W., Pasternack, F. L., Saraniti, A., Nicholas, J. A., Michelis, M. F.: Long-duration submaximal exercise conditioning in hemodialysis patients. Clin. Nephrol., roč. 18, 1982, č. 1, s. 17-22.
Labels
Physiotherapist, university degree Rehabilitation Sports medicine
Article was published inRehabilitation & Physical Medicine

2016 Issue 2-
All articles in this issue
- Spektrum, trendy a postupy současné neurorehabilitace
- Sonografické posouzení stabilizačních svalů bederní páteře u vertebrogenních pacientů
- Posturální stabilita stoje u osob s kořenovým syndromem L5
- Možnosti fyzioterapie u pacientů s onemocněním ledvin, dialyzovaných a transplantovaných – přehled od minulosti po současnost
- Polohování dlouhodobě imobilních a terminálních pacientů
- Vliv odlehčující kolenní ortézy na chůzi u pacientů s gonartrózou – pilotní studie
-
Aplikace kolenní motodlahy po totální endoprotéze
Ovlivňuje rychlost dlahy terapeutický efekt? - Možnosti hipoterapie u dětských pacientů s dětskou mozkovou obrnou
- Sakralizácia stavca L5
- Rehabilitation & Physical Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Sakralizácia stavca L5
- Polohování dlouhodobě imobilních a terminálních pacientů
- Možnosti fyzioterapie u pacientů s onemocněním ledvin, dialyzovaných a transplantovaných – přehled od minulosti po současnost
- Spektrum, trendy a postupy současné neurorehabilitace
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

