-
Medical journals
- Career
Nádory appendixu a pseudomyxom peritonea: současná doporučení pro klinickou praxi
Authors: Dušan Klos 1; J. Riško 1; J. Hanuliak 1; M. Loveček 1; B. Mohelníková-Duchoňová 2; R. Lemstrová 2; L. Tučková 3; B. Melichar 2
Authors‘ workplace: I. chirurgická klinika Fakultní nemocnice a Lékařská fakulta Univerzity Palackého v Olomouci 1; Onkologická klinika Fakultní nemocnice a Lékařská fakulta Univerzity Palackého v Olomouci 2; Ústav klinické a molekulární patologie Fakultní nemocnice a Lékařská fakulta Univerzity Palackého v Olomouci 3
Published in: Rozhl. Chir., 2023, roč. 102, č. 1, s. 5-10.
Category: Review
doi: https://doi.org/10.33699/PIS.2023.102.1.5–10Overview
Nádory appendixu a pseudomyxom peritonea (PMP) jsou vzácné. Nejčastějším zdrojem PMP jsou perforované epiteliální nádory appendixu. Toto onemocnění je charakterizováno přítomností částečně na povrchy adherujícího mucinu různého stupně konzistence. Samotné apendikální mukokély jsou taktéž velmi vzácné a zpravidla jejich léčba zahrnuje pouze prostou apendektomii. Cílem této práce bylo vytvořit aktuální přehled doporučení pro diagnostiku a léčbu těchto malignit podle aktuálních doporučení skupiny PSOGI (The Peritoneal Surface Oncology Group International) a Modré knihy České onkologické společnosti ČLS JEP.
Klíčová slova:
hypertermická intraperitoneální chemoterapie – nádory appendixu – cytoredukce
ÚVOD
Nádory appendixu a pseudomyxom peritonea (PMP) jsou vzácné nádory. Nejčastějším zdrojem PMP jsou perforované epiteliální nádory appendixu. Jejich incidence je nízká. Celosvětově se uvádí incidence kolem tří případů na milion obyvatel ročně [1]. V České republice incidence všech typů nádorů v oblasti appendixu dosahuje 10,39 na milion obyvatel ročně [2]. Pseudomyxom peritonea je charakterizován progresivní produkcí mucinózního ascitu s dominantním postižením omenta v podobě tzv. „omental cake“ (Obr. 1). Klinická manifestace těchto tumorů je velmi nespecifická. Část pacientů se manifestuje příznaky obdobnými akutní apendicitidě (Obr. 2, 3). Podle dostupných údajů je 0,7−1,7 % epiteliálních nádorů appendixu náhod ně zjištěno v resekátech po apendektomii pro akutní apendicitidu [3]. Ostatní klinické příznaky jsou velmi nespecifické – břišní dyskomfort, bolest a nadýmání. Jindy se jedná o náhodné CT nálezy v rámci diferenciální diagnostiky jiných chorob nebo náhodné nálezy po gynekologických resekcích. U žen bývají tyto typy nádoru zjištěny časněji v rámci gynekologického screeningového vyšetření.
Image 1. Omental cake u pseudomyxomu peritonea
Fig. 1. Omental cake in pseudomyxoma peritonei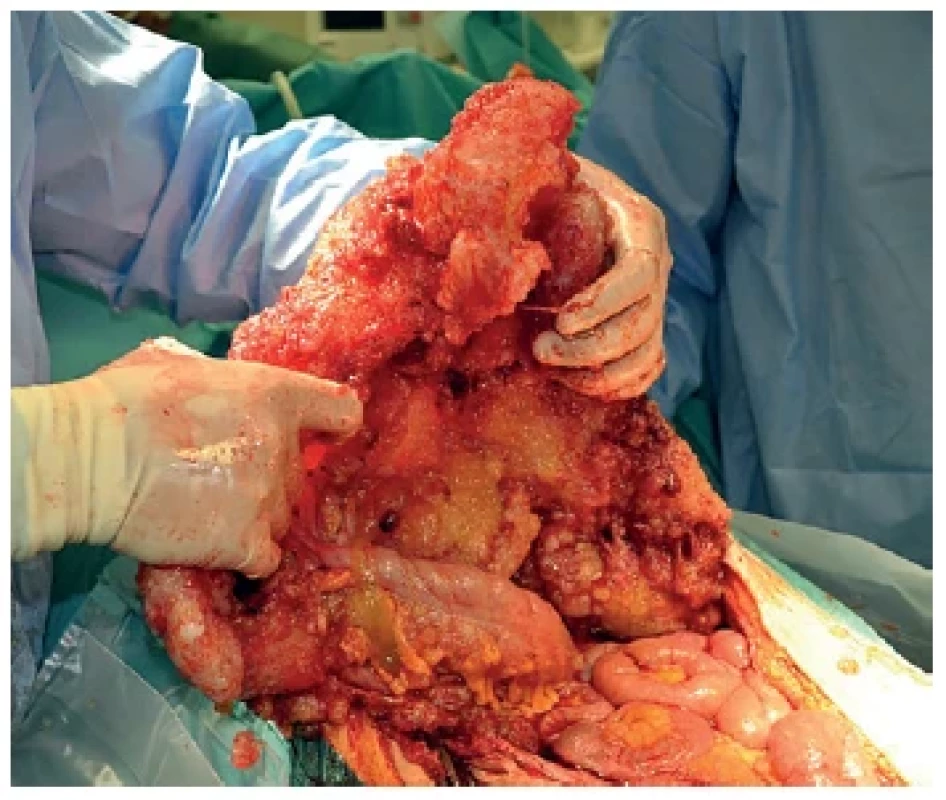
Image 2. Mukokéla appendixu – náhodný nález při apendektomii pro suspektní akutní apendicitidu
Fig. 2. Mucocoele of the appendix – an incidental finding during appendectomy for suspected acute appendicitis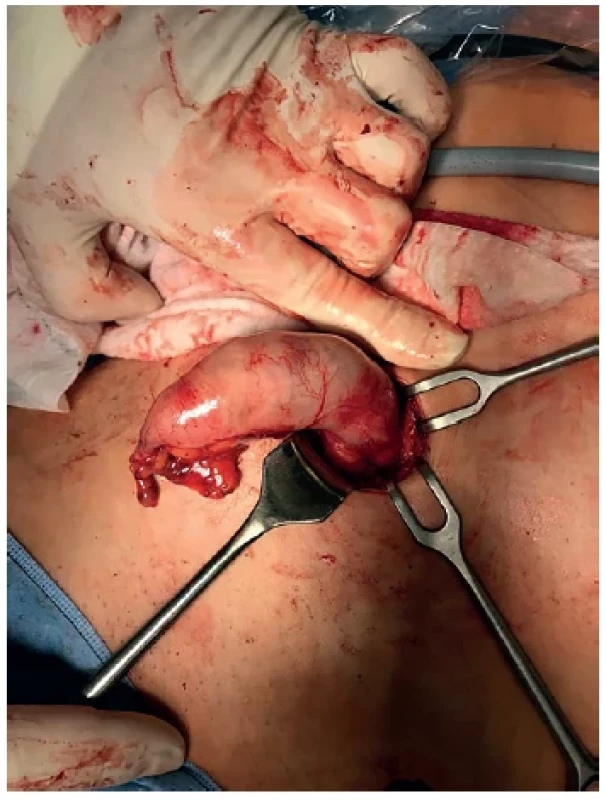
Image 3. Ileocekální resekát pro mukokélu appendixu – náhodný nález při apendektomii pro suspektní akutní apendicitidu
Fig. 3. Ileocecal resection for appendiceal mucocele – incidental finding during appendectomy for suspected acute appendicitis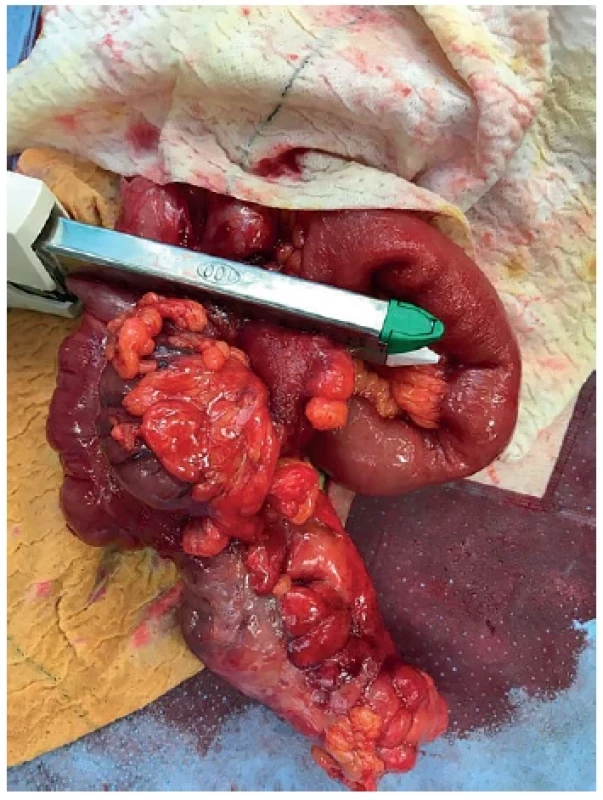
Od 80. let 20. století se rozvíjí koncept cytoredukční chirurgie (CRS) a hypertermické intraperitoneální chemoterapie (HIPEC) jako potenciální kurabilní metoda léčby [4]. Tato léčba se úspěšně rozvíjí na několika pracovištích i v České republice [5,6]. Díky malé četnosti tohoto onemocnění chybějí i důkazy o významu této léčby z velkých souborů randomizovaných studií. I když je tato metoda dnes dobře standardizována, v řadě částí se liší podle jednotlivých center a řada otázek stále zůstává nezodpovězena. Proto skupina PSOGI (The Peritoneal Surface Oncology Group International) zahrnující odborníky specializující se na léčbu malignit peritoneálního povrchu vydala v roce 2021 guidelines pro léčbu nádorů appendixu a PMP [7], které přinášíme v modifikaci a úpravě akceptující současná doporučení tzv. Modré knihy České onkologické společnosti a lokální podmínky a praxi v České republice.
METODY
Panel odborníků zahrnoval 80 expertů z celého světa, kteří participovali na odpovědích celkem 69 otázek. Tyto otázky odpovídaly tzv. GRADE systému (Grades of Recommendation, Assessment, Development, and Evaluation) využívající tzv. PICO-model (Patient, Intervention, Control, Outcome). Úroveň síly důkazů (dále jen „důkaz“) byla kategorizována do čtyř stupňů: A – vysoká (je nepravděpodobné, že by výsledky dalšího výzkumu změnily naše přesvědčení o očekávaném efektu), B – mírná (je pravděpodobné, že další výzkum bude mít významný vliv na naše přesvědčení a očekávaný efekt jej může změnit), C – nízká (další výzkum bude mít velmi pravděpodobně významný vliv na naše přesvědčení a očekávaný efekt jej pravděpodobně změní), D – velmi nízká (jakýkoliv očekávaný efekt je nejistý). Síla doporučení (dále jen „Doporučení“) potom byla rozdělena do čtyř možností: I – silně pozitivní – mělo by být provedeno vždy, II – slabě pozitivní – mělo by být zváženo, III – slabě negativní – nemělo by být uváženo, IV – silně negativní – nemá žádný význam a nemělo by být nikdy zvažováno.
Nejpodstatnější otázky a doporučení uvedené v práci Govaerts a spol. byly konfrontovány s doporučením uvedeným v části 4 a 38 (zhoubný novotvar kolorekta C18-20 a cytoredukční chirurgie a HIPEC v terapii peritoneální karcinomatózy) aktuálního vydání tzv. Modré knihy 2022 [8]. Síla doporučení poté byla modifikována podle praxe v ČR (dále jen „Doporučení ČR) zahrnující taktéž 4 úrovně dle síly důkazů a klinických postupů v ČR: I – silně pozitivní – mělo by být provedeno vždy, současná klinická praxe v ČR odpovídá doporučením PSOGI, II – slabě pozitivní – mělo by být zváženo, III – slabě negativní – nemělo by být zváženo, IV – silně negativní – nemá žádný význam a nemělo by být nikdy zvažováno, v ČR se neprovádí.
Table 1. Srovnání klasifikačních a nomenklutárních systémů pro kvalifikaci apendikálních tumorů
Tab. 1. Comparison of classification and nomenclature systems for appendiceal tumor qualification
VÝSLEDKY
I. Terminologie a patologická klasifikace
Pro klasifikaci nádorů appendixu a PMP se používá několik různých klasifikačních systémů. Globálně akceptovaná klasifikace nádorů appendixu podle PSOGI zahrnuje [9]:
Mucinózní epiteliální neoplazie
serátní polyp
low grade mucinous neoplasm – LAMN
high grade mucinous neoplasm – HAMN
mucinózní adenokarcinom (s nebo bez buněk tvaru pečetního prstenu)
Nemucinózní epiteliální neoplazie
adenom (typ kolorektální)
adenokarcinom
Epiteliální neoplazie s neuroendokrinními rysy
neuroendokrinní tumor
goblet cell karcinoid
Mezenchymální neoplazie
Následující mucinózní neoplazie appendixu mohou být spojeny s peritoneální diseminací (pseudomyxom peritonea): low grade appendiceal neoplasm (LAMN), high grade appendiceal neoplasm (HAMN), mucinózní adenokarcinom (s nebo bez buněk tvaru pečetního prstenu) a goblet cell carcinoids. Peritoneální rozsev všech ostatních nádorových entit appendixu označujeme jako peritoneální metastázy [10].
V podmínkách ČR se klasifikační systémy liší podle typu pracovišť, což činí obtíže při standardizaci péče a stanovení ideálního managementu a strategie léčby.
Doporučení 1
Použití terminologického konsenzu dle PSOGI 2016 k histopatologické klasifikaci PMP apendikálního původu.
Důkaz: A – vysoký
Doporučení: I – silně pozitivní
Doporučení ČR: I – silně pozitivníII. Předoperační vyšetření a hladina sérových tumormarkerů
Doporučení 2
Stanovení hladiny CEA v předoperačním stagingu nemocných s apendikálním PMP je povinné
Důkaz: B – mírný
Doporučení: I – silně pozitivní
Doporučení ČR: I – silně pozitivníDoporučení 3
Stanovení hladiny Ca 19.9 v předoperačním stagingu nemocných s apendikálním PMP je povinné
Důkaz: B – mírný
Doporučení: I – silně pozitivní
Doporučení ČR: I – silně pozitivníDoporučení 4
Stanovení hladiny Ca 125 v předoperačním stagingu nemocných s apendikálním PMP je povinné
Důkaz: B – mírný
Doporučení: II – slabě pozitivní
Doporučení ČR: I – silně pozitivníIII. Zobrazovací metody v diagnostice PMP
Doporučení 5
Předoperační CT hrudníku a břicha v diagnostice nemocných s apendikálním PMP by mělo být preferovanou metodou
Důkaz: B – mírný
Doporučení: II – slabě pozitivní
Doporučení ČR: I – silně pozitivníStandardní CT vyšetření hrudníku a břicha by mělo být podle našeho názoru preferovaným zobrazovacím vyšetřením v předoperačním stagingu apendikálních neoplazií a PMP. V ČR hojně využívané PETCT podle současných poznatků a důkazů má pouze slabý přínos v diagnostice mucinózních neoplazií. Význam má především pro vyloučení vzdálených metastáz [11].
IV. Kolonoskopie
Doporučení 6
U nemocných s apendikálním PMP vhodných k CRS a HIPEC by měla být provedena kolonoskopie k vyloučení jiných primárních nádorů tračníku.
Důkaz: B – mírný
Doporučení: I – silně pozitivní
Doporučení ČR: I – silně pozitivníKolonoskopie by měla být provedena vždy k vyloučení jiných neoplazií tračníku, byť benigních. A to zejména při plánovaných resekčních výkonech na tračníku.
V. Cytoredukční chirurgie
Doporučení 7
V případě neočekávaného nálezu PMP během plánované nitrobřišní operace pro nenádorové onemocnění (cholecystektomie, hernioplastika apod.) by chirurg měl přerušit prováděný výkon a provést pouhou biopsii, která by umožnila identifikovat histologickou diagnózu peritoneálního rozsevu; rozhodnutí o provedení pravostranné hemikolektomie by mělo vyčkat definitivního histologického nálezu.
Důkaz: B – mírný
Doporučení: I – silně pozitivní
Doporučení ČR: I – silně pozitivníDoporučení 8
Hlavní indikační kritéria pro provedení CRS a HIPEC v případě apendikálního PMP je schopnost pacienta podstoupit velký chirurgický výkon, nález je resekabilní a je proveden ve specializovaném centru.
Důkaz: B – mírný
Doporučení: I – silně pozitivní
Doporučení ČR: I – silně pozitivníV České republice se cytoredukční chirurgií a HIPEC zabývají tato centra: FN v Olomouci, VFN v Praze, MOÚ v Brně, dále FN Bulovka v Praze a Fakultní Thomayerova
nemocnice v Praze.Doporučení 9
Je indikována pravostranná hemikolektomie v uvedené histologické charakteristice primárního apendikálního nádoru s nebo bez peritoneálního rozsevu.
a. LAMN
Důkaz: B – mírný
Doporučení: IV – silně negativní
Doporučení ČR: IV – silně negativníb. HAMN
Důkaz: B – mírný
Doporučení: II – slabě pozitivní
Doporučení ČR: II – slabě pozitivníc. Mucinózní adenokarcinom G1–G3 (s nebo bezbb. tvaru pečetního prstenu)
Důkaz: B – mírný
Doporučení: I – silně pozitivní
Doporučení ČR: I – silně pozitivníd. Goblet cell karcinoid
Důkaz: B – mírnýDoporučení: I – silně pozitivní
Doporučení ČR: I – silně pozitivníVI. Význam neoadjuvantní chemoterapie
Doporučení 10
U nemocných s low grade PMP, kteří jsou schopni podstoupit CRS a HIPEC, nemá význam neoadjuvantní chemoterapie.
Důkaz: C – nízký
Doporučení: IV – silně negativní
Doporučení ČR: IV – silně negativníDoporučení 11
U pacientů s high grade PMP nebo high grade PMP s bb. tvaru pečetního prstenu, u kterých by bylo možné provést kompletní cytoredukci a HIPEC, by měla být zvážena neoadjuvantní chemoterapie.
Důkaz: C – nízký
Doporučení: II – slabě pozitivní
Doporučení ČR: I – silně pozitivníV České republice standardně používáme režimy FOLFOX (oxaliplatina, 5-fluorouracil, leukovorin) či XELOX (kapecitabin, oxaliplatina).
VII. Adjuvantní chemoterapie
Doporučení 12
U nemocných s low grade apendikální neoplazií a PMP, u kterých byla provedena kompletní CRS a HIPEC, není indikována adjuvantní chemoterapie.
Důkaz: C – nízký
Doporučení: IV – silně negativní
Doporučení ČR: IV – silně negativníDoporučení 13
U pacientů s high grade PMP s nebo bez bb. tvaru pečetního prstenu, u kterých byla provedena kompletní CRS a HIPEC, by měla být zvážena adjuvantní chemoterapie.
Důkaz: C – nízký
Doporučení: II – slabě pozitivní
Doporučení ČR: I – silně pozitivníDoporučení 14
V případě použití adjuvantní chemoterapie se doporučují kombinace fluropyrimidinu a alkylujících látek, např. oxaliplatina.
Doporučení 15
U nemocných s neresekabilním low i high grade PMP je indikována paliativní chemoterapie v režimu fluoropyrimidin a oxaliplatina.
Důkaz: B – mírný
Doporučení: II – slabě pozitivní
Doporučení ČR: I – silně pozitivníVIII. Pooperační sledování
Doporučení 16
V pooperačním průběhu po CRS a HIPEC pro apendikální PMP by pacient měl být dispenzarizován s klinickým vyšetřením, odběrem onkomarkerů a CT hrudníku a břicha první dva roky co 6 měsíců, následně co rok.
Doporučení: I – silně pozitivní
Doporučení ČR: I – silně pozitivníZÁVĚR
V diagnostice nádorů appendixu a PMP má zásadní význam především CT hrudníku a břicha, kolonoskopické vyšetření a také stanovení sérových hladin CEA, Ca 19.9 a Ca 125. V případě předoperačně zjištěné peritoneální karcinomatózy, kde není možné získat histologickou verifikaci, je na místě provedení diagnostické laparoskopie se stanovením rozsahu peritoneální karcinomatózy dle PCI (peritoneal cancer index) a odběrem validního histologického vzorku [7,12]. Všichni pacienti s neoplazií appendixu by měli být referováni do specializovaných center, která se specializují na diagnostiku a léčbu těchto nádorů. V případě low grade apendikální mucinózní neoplazie bez extraperitoneálního postižení v dobrém výkonnostním stavu by měla být zvážena cytoredukce a HIPEC. Provedení debulkingu bez HIPEC v daném případě nedoporučujeme. V případě nálezu neperforované mukokély appendixu, bez mucinu v dutině břišní, je považována při histologickém nálezu LAMN a čistých okrajích apendektomie za dostatečný výkon (Obr. 4). Doplnění pravostranné hemikolektomie není doporučeno. Následně by však mělo být doplněno CT hrudníku a břicha, kolonoskopie a stanovení hladiny CEA. V případě nálezu HAMN či PMP s buňkami tvaru pečetního prstence v definitivním nálezu by pacient měl být referován do centra k provedení CRS a HIPEC. Součástí tohoto výkonu by mělo být i dokončení pravostranné hemikolektomie. V případě nálezu perforované mukokély s nálezem acelulárního či celulárního mucinu v případě suspektní akutní apendicitidy je indikováno provedení apendektomie a odběru hlenu. Následně po dokončení stagingu (CT, kolonoskopie, CEA) reference do centra, a pokud je pacient výkonu schopen, je indikován k provedení CRS a HIPEC. V případě podezření na karcinom appendixu bez nebo s peritoneální karcinomatózou a provedení pravostranné hemikolektomie a peritonektomie na domovském pracovišti by měla následovat adjuvantní chemoterapie. Doplnění HIPEC v daném případě nemá větší význam. U nemocných po kompletní CRS a HIPEC pro LAMN a PMP není indikována adjuvantní (a ani neoadjuvantní) chemoterapie. U HAMN a PMP s buňkami tvaru pečetního prstence či adenokarcinomu appendixu s peritoneální karcinomatózou po CRS a HIPEC je indikována adjuvantní chemoterapie v režimu FOLFOX, FOLFIRI či XELOX. U nemocných s nekompletní resekcí nebo neschopných radikální CRS a HIPEC je ke zvážení paliativní chemoterapie v podobném režimu. Po CRS a HIPEC po apendikálním PMP by nemocný měl být dispenzarizován s kontrolou první dva roky co půl roku s odběrem CEA a CT hrudníku a břicha, jednou ročně kontrolní kolonoskopie, poté co rok CEA, CT hrudníku a břicha.
Image 4. Flow-chart léčebného postupu v případě nálezu neperforované mukokély apendixu
Fig. 4. Flow-chart for the management of a non-perforated appendiceal mucocele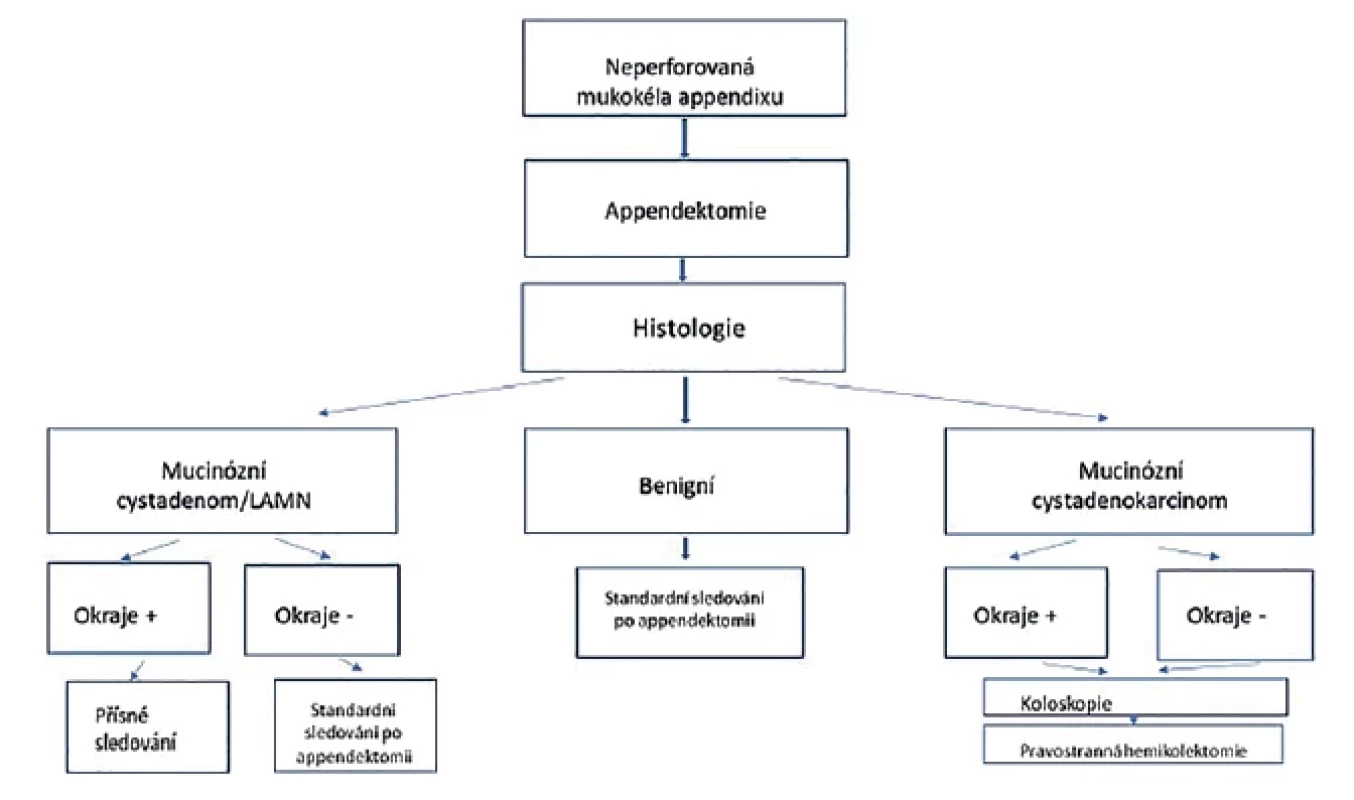
Nádory appendixu jsou vzácné, v případě jejich průkazu by nemocní měli být referováni do specializovaných center s aktuálním výsledkem CT hrudníku a břicha s kontrastem p.o. i i.v. k posouzení operability a indikace k cytoredukci a HIPEC. V případě podezření na tumor appendixu (byť náhodně nalezený) proveďte klasickou apendektomii, event. odstranění dalších zbytků tumoru v pericekální oblasti. Rozšiřovat výkon na pravostrannou hemikolektomii není v dané chvíli nutné, neboť extenzivní výkon může vést k rozvoji dalších srůstů nebo usnadnit peritoneální diseminaci a může také v případě pooperačních komplikací neadekvátně prodloužit čas k možnému definitivnímu řešení s kurativním potenciálem v podobě cytoredukce a HIPEC či neoadjuvantní chemoterapie, vždy však pečlivě odstraňte přebytečný mucin s odběrem k histologickému vyšetření a popište rozsah postižení peritoneální dutiny [1,5,12].
Podpořeno MZ ČR – RVO (FNOl, 00098892). Supported by Ministry of Health, Czech Republic – conceptual development of research organization (FNOl, 00098892).
Konflikt zájmů
Autoři článku prohlašují, že nejsou v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise, s výjimkou kongresových abstrakt a doporučených postupů.
doc. MUDr. JUDr. Dušan Klos, Ph.D., LL.M.
I. Chirurgická klinika
FN Olomouc
I. P. Pavlova 6, Olomouc
e-mail: dusan.klos@fnol.czORCID 0000-0002-3097-4418
Rozhl Chir. 2023;102 : 5–10
Sources
1. Rizvi SA, Syed W, Shergill R. Approach to pseduomyxoma peritonei. World J Gastrointest Surg Surg. 2018 Aug 27;10(5):49−56. doi:10.4240/wjgs.v10. i5.49.
2. Klos D, Riško J, Loveček M, et al. Trends in peritoneal surface malignancies: evidence from a Czech nationwide population - based study. World Journal of Surgical Oncology. 2019 Nov 6;17(1):182. doi:10.1186/s12957-019-1731-4.
3. Murphy EM, Farquaharson SM, Moran BJ. Management of an unexpected appendiceal neoplasm. Br J Surg. 2006 Jul;93(7):783−792. doi:10.1002/bjs.5385.
4. Smeenk RM, Verwaal V, Antonin N, et al. Survival analysis of pseduomyxoma peritonei patients treated by cytoreductive surgery and hypertermic intraperitoneal chemotherapy. Ann Surg. 2007 Jan;245(1):104−109. doi:10.1097/01.sla. 0000231705.40081.1a.
5. Bartoška P, Antoš F, Vítek P, et al. Pseudomyxom peritonea. Klinická onkologie 2019;32(5):329−332, doi:10.14735/ amko2019329.
6. Klos D, Riško J, Stašek M, et al. Současné postavení cytoredukční chirurgie (CRS) a intraperitoneální hypertermické chemoterapie (HIPEC) v multimodální léčbě nádorů peritoneálního povrchu. Čas Lék čes. 2018 Dec 17;157(8):419−428.
7. Govaerts K, Lurvink RJ, de Hingh IHJT, et al. Appendiceal tumours and pseudomyxoma peritonei: Literature review with PSOGI/EURACAN clinical practice guidelines for diagnosis and treatment. Eur J Surg Oncol 2021 Jan;47(1):11−35. doi:10.1016/j.ejso.2020.02.012.
8. ČOS (2022). Aktuální vydání Modré knihy. Availeble at: https://www.linkos.cz/ lekar-a-multidisciplinarni-tym/personalizovana - onkologie/modra-kniha-cos/ aktualni-vydani-modre-knihy/.
9. Carr NJ, Cecil TD, Faheez M, et al. A consensus for classification and pathological reporting of pseduomyxoma peritonei and associated appendiceal neoplasia: the results of the peritoneal surface oncology group international (PSOGI) modified Delphi process. Am j Surg Pathol. 2016 Jan;40(1):14−26. doi:10.1097/PAS.0000000000000535.
10. Valasek MA, Pai KR. An update on the diagnosis, grading and staging of appendiceal mucinous neoplasms. Adv Anat Pathol. 2018 Jan;25(1):38−60. doi:0.1097/ PAP.0000000000000178.
11. Dubreuil J, Giammarile F, Rousset P, et al. FDG-PET/ceCT is useful to predict recurrence of Pseudomyxoma peritonei. Eur J Nucl Med Mol Imag. 2016 Aug; 43(9):1630−1637. doi:10.1007/s00259 - 016-3347-z.
12. Kearsey CHC, Day N, Sutton PA. „It´s not just a mucocoele“ − pathology and treatment of appendix tumours. BJS 2022;209 : 566−569. doi:10.1093/bjs/ znac084.
13. Morano WF, Gleeson E, Bowne W, et al. Clinicopathological features and management of appendiceal mucoceles: A systematic review. Am Surg. 2018 Feb 1;84(2):273−281. doi:10.1177/000313481 80840023.7.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2023 Issue 1-
All articles in this issue
- Centralizace a praxe
- Appendiceal tumors and pseudomyxoma peritonei: current recommendations for clinical practice
- Native nephrectomy in patients with autosomal dominant polycystic kidney disease in the kidney transplant program – single-center retrospective results of 2000−2020
- Incidence of postoperative complications in patients with breast cancer depending on the type of drain
- Intrapulmonary sequestration with destructive pneumonia and life-threatening hemoptysis in an adult patient: a case report
- Incarcerated metastasis as the first manifestation of a rare sarcoma
- Case report Ileal diverticulitis with covered perforation complicated by pulmonary embolism – case report
- Retroperitoneal abscess after urgent resection of the stomach in a geriatric patient treated with a surgical extraperitoneal approach – case report
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Appendiceal tumors and pseudomyxoma peritonei: current recommendations for clinical practice
- Incidence of postoperative complications in patients with breast cancer depending on the type of drain
- Intrapulmonary sequestration with destructive pneumonia and life-threatening hemoptysis in an adult patient: a case report
- Case report Ileal diverticulitis with covered perforation complicated by pulmonary embolism – case report
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

