-
Medical journals
- Career
Uroteliální karcinomy horních močových cest – naše zkušenosti
Authors: R. Adwan
Authors‘ workplace: Urologické oddělení, Oblastní nemocnice Náchod
Published in: Rozhl. Chir., 2020, roč. 99, č. 5, s. 219-225.
Category: Original articles
doi: https://doi.org/10.33699/PIS.2020.99.5.219–225Overview
Úvod: Uroteliální karcinom je druhou nejčastější urologickou malignitou, 5–10 % nádorů je lokalizováno v horních močových cestách a většina, 90–95 %, karcinomů se vyskytuje v močovém měchýři.
Metody: Do souboru byli zařazeni pacienti našeho oddělení, u nichž byl v letech 2014–2018 diagnostikován uroteliální karcinom horních močových cest (UKHMC). Analyzována byla jeho četnost, zvolený terapeutický postup a hodnoceny léčebné výsledky.
Výsledky: Na náchodském urologickém oddělení bylo diagnostikováno a operováno v posledních pěti letech u 21 pacientů s diagnózou uroteliální karcinom horních močových cest. Hlavním typem operačního řešení byla nefroureterektomie. Celkem došlo k úmrtí ve 28,6 % případů v důsledku základního nádorového onemocnění. Uroteliální karcinom horních močových cest je mezi našimi pacienty častější u mužů než u žen.
Závěr: Uroteliální karcinomy horních močových cest jsou bohužel velmi často řešeny až při lokální pokročilosti nebo při uzlinových či vzdálených metastázách, což následně komplikuje i případné podání adjuvantní chemoterapie, která není dostatečně účinná. Proto pro více než polovinu pacientů zůstává zlatým standardem radikální nefroureterektomie. Celkové přežití nejvíce závisí na přítomnosti vzdálených metastáz. Pro vznik recidivy je hlavním ovlivňujícím parametrem pT kategorie.
Klíčová slova:
horní močové cesty – uroteliální karcinom – nefroureterektomie – segmentální resekce ureteru
ÚVOD
Uroteliální karcinomy horních močových cest zahrnují nádory vycházející z přechodního epitelu ledvinných kalichů, pánvičky a močovodu. Uroteliální karcinom je druhou nejčastější urologickou malignitou, 5–10 % nádorů je lokalizováno v horních močových cestách a většina, 90–95 %, karcinomů se vyskytuje v močovém měchýři. Nádory močovodu jsou vzácnější než nádory ledvinné pánvičky a tvoří zhruba 25 % nádorů horních močových cest s nejčastější lokalizací v distální části [1,2,3]. V České republice tvoří uroteliální karcinom horních močových cest (UKHMC) 0,3 % všech maligních tumorů [3,4], incidence byla v roce 2015 [5,6] u karcinomu ledvinné pánvičky 1,53 a u močovodu 0,34 na 100 000 obyvatel a mortalita 4,73 (pánvička) a 0,12 (močovod)/100 000 obyvatel.
Nádory horních močových cest se vzácně vyskytují před 40. rokem věku, maximum výskytu je v páté, šesté i sedmé dekádě [1], muži jsou postižení 3krát více než ženy [1,4]. V rodinách s balkánskou endemickou nefropatií je incidence 100 až 200krát vyšší, a navíc bývají mnohočetné nebo bilaterální [7]. Synchronní bilaterální výskyt UKHMC je udáván 1,5−2 %, u 6−8 % pacientů může dojít v průběhu sledování ke vzniku druhostranného nádoru [3,4]. V 8−13 % případů je synchronně diagnostikován nádor močového měchýře [3]. V pozdějším průběhu se recidivy v močovém měchýři objevují až v 51 % [2,8]. Přibližně u 30−75 % nádorů HMC je primárně nebo sekundárně přítomen nádor močového měchýře [1,9,10]. Naopak u nádoru močového měchýře může být nádor v horních močových cestách přítomen v 1−4 %, nicméně riziko může vzrůst až na 20 % [1,11,12].
METODY
Do souboru byli zařazeni pacienti našeho oddělení, u nichž byl v letech 2014–2018 diagnostikován uroteliální karcinom horních močových cest (UKHMC). Analyzována byla četnost UKHMC, zvolený terapeutický postup a hodnoceny léčebné výsledky.
VÝSLEDKY
Na náchodském urologickém oddělení bylo diagnostikováno a operováno v posledních pěti letech 21 pacientů s diagnózou uroteliální karcinom horních močových cest (Tab. 1–3; Graf 1).
Table 1. Výskyt nádorů podle lokalizací a podle pohlaví (Oblastní nemocnice Náchod, 2014−2018)
Tab. 1: Incidence of tumors by location and gender (Regional Hospital Nachod, 2014−2018)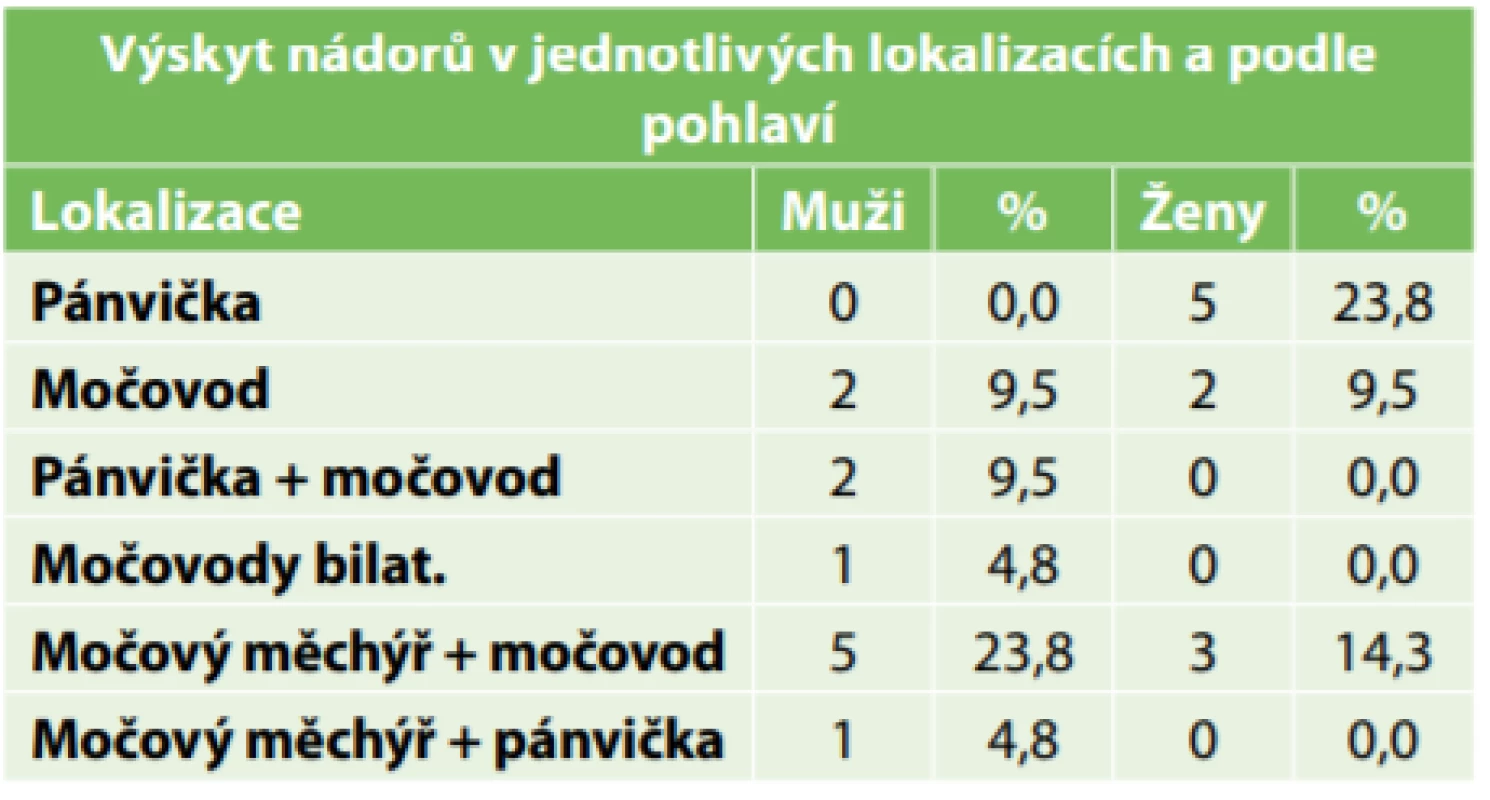
Table 2. Klasifikace TNM (soubor 21 pacientů Oblastní nemocnice Náchod, 2014−2018)
Tab. 2: TNM classification (21 patients in Regional Hospital Nachod, 2014−2018).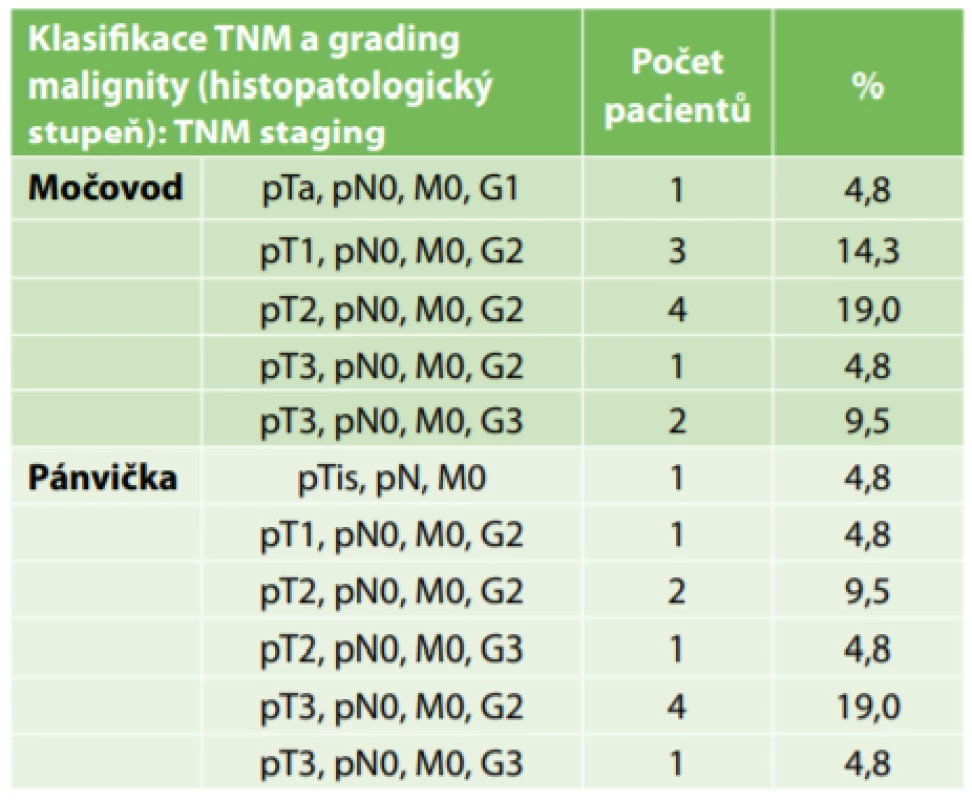
Table 3. Typy provedených operačních výkonů v Oblastní nemocnici Náchod 2014−2018
Tab. 3: Types of surgeries performed in Regional Hospital Nachod, 2014−2018
Graph 1. Typy provedených operačních výkonů v Oblastní nemocnici Náchod 2014−2018
Graph 1: Types of surgeries performed in Regional Hospital Nachod, 2014−2018
Karcinom močového měchýře mělo v anamnéze 52,4 % pacientů. Hlavním typem operačního řešení byla nefroureterektomie u uroteliálního karcinomu ledvinné pánvičky (66,6 % pacientů; z toho nefroureterektomie otevřená 57,1 % a nefroureterektomie laparoskopická 9,5 %). Při provedení nefroureterektomie byla nejčastěji použitou technikou transuretrální resekce intramurálního močovodu, která představuje kompletní odstranění ledviny s celým příslušným močovodem včetně terčíku ureterálního ústí a s lemem okolní části močového měchýře (en bloc). Resekce distální části močovodu i jeho reimplantace do močového měchýře byla provedena u ureteliálního karcinomu distálního močovodu (23,8 % našich operačních výkonů). Peroperačně byly histologicky potvrzeny negativní resekční okraje. V případě zvětšených lymfatických uzlin na zobrazovacím vyšetření nebo makroskopicky peroperačně byla provedena lymfadenektomie. U tří (14,3 %) pacientů z našeho souboru byly diagnosticky odstraněny pouze zvětšené regionální spádové uzliny, které byly detekovány při MDCTU a byly histologicky pozitivní. Celkem došlo k úmrtí 28,6 % případů v důsledku základního nádorového onemocnění. Celkové přežití bylo 90,5 % (jednoleté) a 71 % (tříleté). Uroteliální karcinom horních močových cest je mezi našimi pacienty častější u mužů než u žen, což odpovídá literatuře.
Adjuvantní léčba byla podána pro T3–T4 tumory, kde se předpokládá přítomnost mikrometastáz, standardně u našich pacientů byly podány gemcitabin a cisplatina, které mají obdobné odpovědi jako MVAC (metotrexát, vinblastin, adriamycin, cisplatina) s nižší toxicitou.
Důvodem sledování pacientů po chirurgické léčbě je odhalení lokální recidivy a vzdálených metastáz. Riziko lokální recidivy po nefroureterektomii je nízké a riziko vzniku vzdálených metastáz souvisí s hloubkou nádorové invaze a mírou histologické diferenciace primárního nádoru. Naše pacienty po radikální nefroureterektomii sledujeme minimálně po dobu pěti let. Podle doporučovaného schématu se pacientům po nefroureterektomii s nádory Ta a T1 provádějí kontrolní cystoskopie a cytologie tři měsíce po operaci, poté ročně, snímek plic a MDCTU jednou ročně, scintigrafie skeletu pouze při symptomech. U pacientů s nádory ≥ T2 (invazivní nádory) se provádějí kontrolní cystoskopie a cytologie tři měsíce po operaci, poté ročně, snímek plic a MDCTU à 6 měsíců po dobu 2 let, poté ročně, scintigrafie skeletu pouze při symptomech.
Po záchovných výkonech (konzervativním přístupem) cystoskopie s URS a výplachovou cytologií 3, 6 a 12 měsíců po operaci a dále každých šest měsíců po dobu dvou let, dále 1× ročně. MDCTU je vhodné provádět 3, 6 a 12 měsíců po operaci, dále 1× ročně, vše po dobu alespoň pěti let.
Příklad zobrazení uroteliálního karcinomu horních močových cest pacientů našeho pracoviště.
Operační řešení – resekce distální části pravého močovodu i jeho reimplantace do močového měchýře (psoas hitch., otevřený postup).
Histologicky uroteliální karcinom pravého močovodu – pTa, pN0 (12/0+), M0 (Obr. 1).
Image 1. Uroteliální karcinom distálního močovodu, vpravo – CT
Fig. 1: Urothelial carcinoma of the distal ureter, right – CT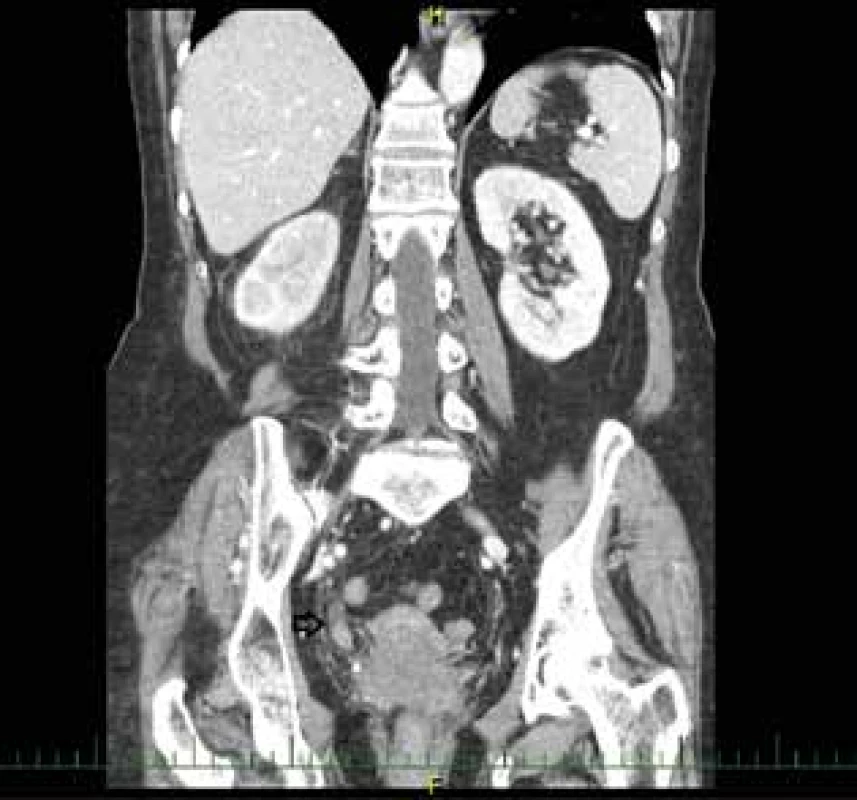
Zobrazení uroteliálního karcinomu pánvičky vlevo (dolní kalich) u pacientky třemi zobrazovacími metodami (Obr. 2–4).
Image 2. Uroteliální karcinom pánvičky levé ledviny – CT
Fig. 2: Urothelial carcinoma of the renal pelvis of the left kidney − Computed Tomography (CT)
Image 3. Uroteliální karcinom pánvičky – ascendentní pyelografie (defekt kontrastní náplně dolního kalichu)
Fig. 3: Urothelial carcinoma in the renal pelvis – ascendent pyelography (a contrast medium filling defect in the lower calyx)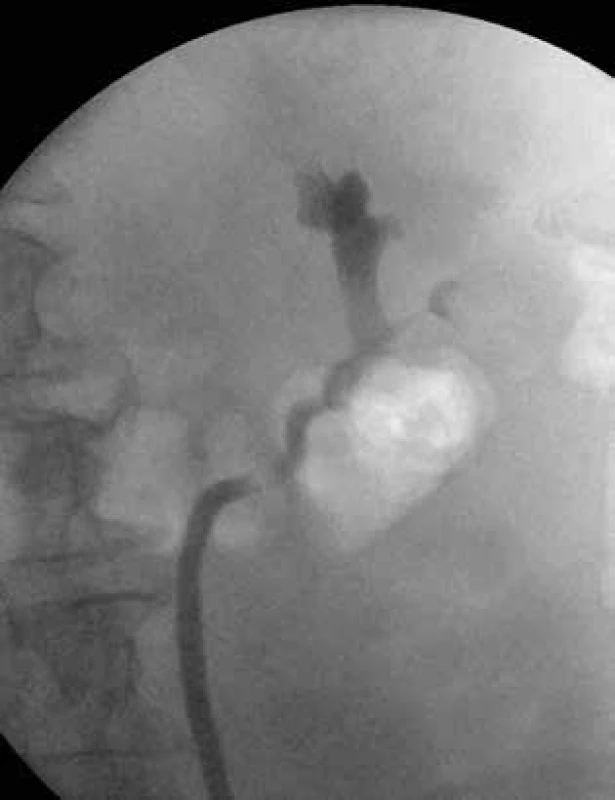
Image 4. Uroteliální karcinom pánvičky levé ledviny – sonografické vyšetření
Fig. 4: Urothelial carcinoma of the renal pelvis of the left kidney − ultrasonography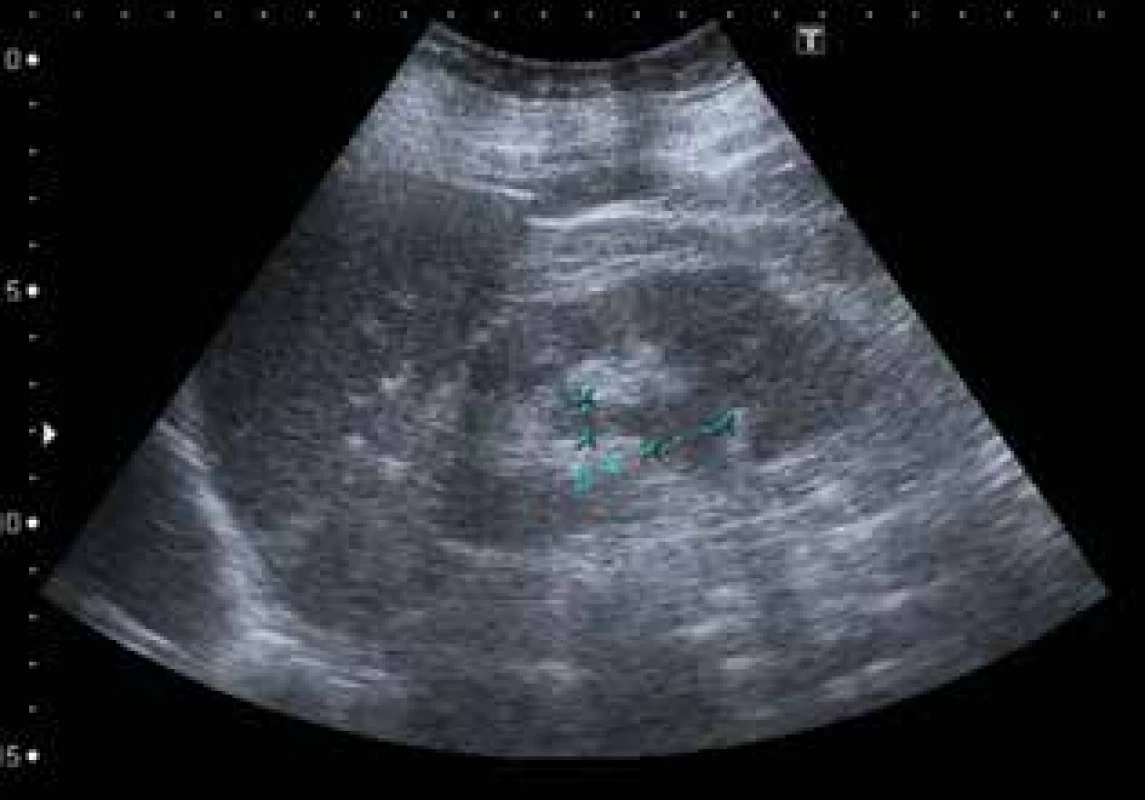
Operační řešení – nefroureterektomie, otevřený postup, adjuvantní chemoterapii pacientka odmítla.
Histologicky uroteliální karcinom ledvinné pánvičky – pT3, N0, M0, G2.
Zobrazení uroteliálního karcinomu pánvičky vpravo (horní kalich) u pacientky třemi zobrazovacími metodami (Obr. 5–7).
Image 5. Uroteliální karcinom pánvičky pravé ledviny – CT
Fig. 5: Urothelial carcinoma of the renal pelvis of the right kidney – CT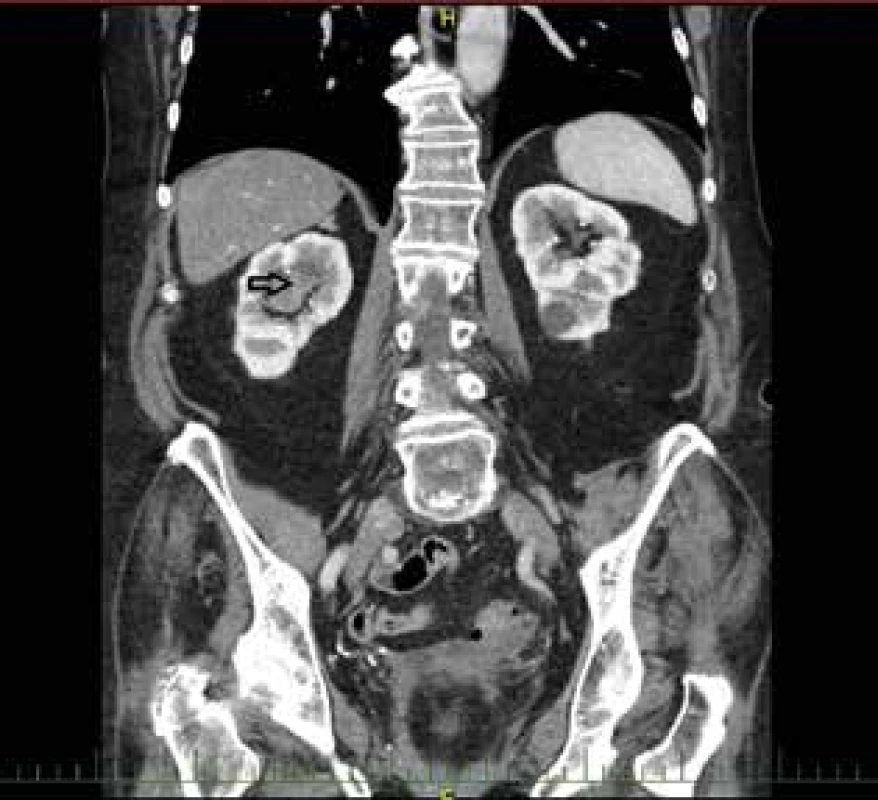
Image 6. Rekonstrukce CT – vylučovací urografie (chybí náplň kontrastní látkou v horním kalichu pravé ledviny)
Fig. 6: CT reconstruction – excretory urography (absent contrast agent filling in the upper calyx of the right kidney)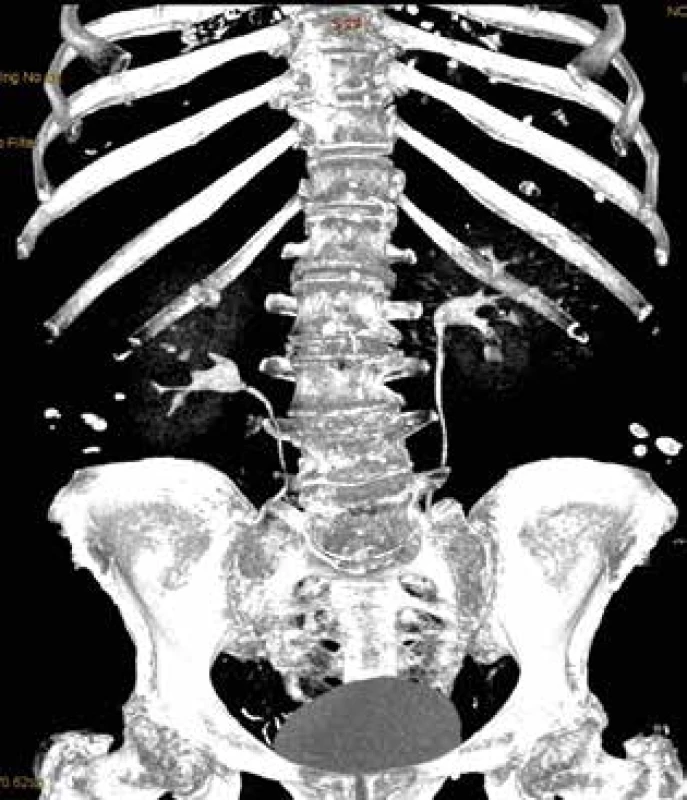
Image 7. Ascendentní pyelografie – chybí náplň kontrastní látkou v horním kalichu pravé ledviny
Fig. 7: Ascendent pyelography – absent contrast agent filling in the upper calyx of the right kidney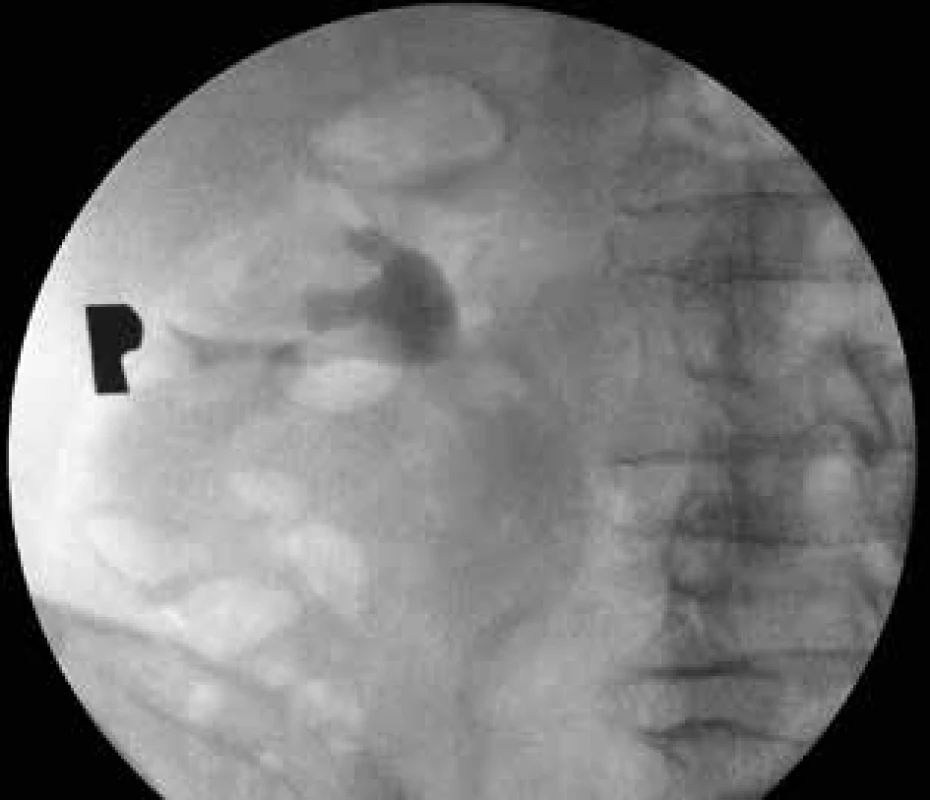
Operační řešení – nefroureterektomie, otevřený postup + adjuvantní chemoterapie.
Histologicky uroteliální karcinom ledvinné pánvičky: pT3, NX, MX.
Zobrazení uroteliálního karcinomu pánvičky vlevo (dolní kalich) u pacientky (Obr. 8–9).
Image 8. Pokročilý uroteliální karcinom pánvičky levé ledviny – CT
Fig. 8: Advanced urothelial carcinoma of the renal pelvis of the left kidney − CT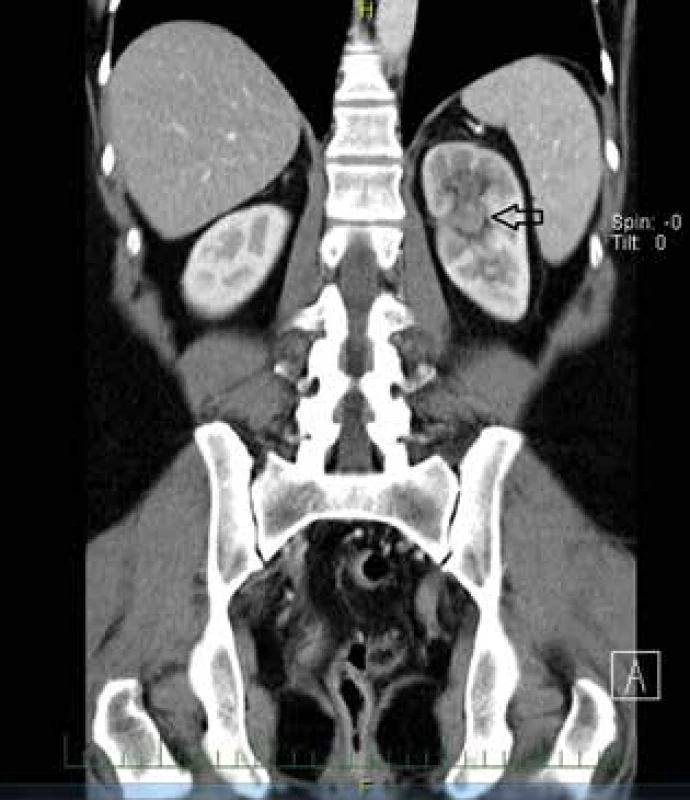
Image 9. Pokročilý uroteliální karcinom pánvičky levé ledviny s lymfadenopatií – PET CT (restaging)
Fig. 9: Advanced urothelial carcinoma of the renal pelvis of the left kidney with lymphadenopathy – PET CT ( restaging)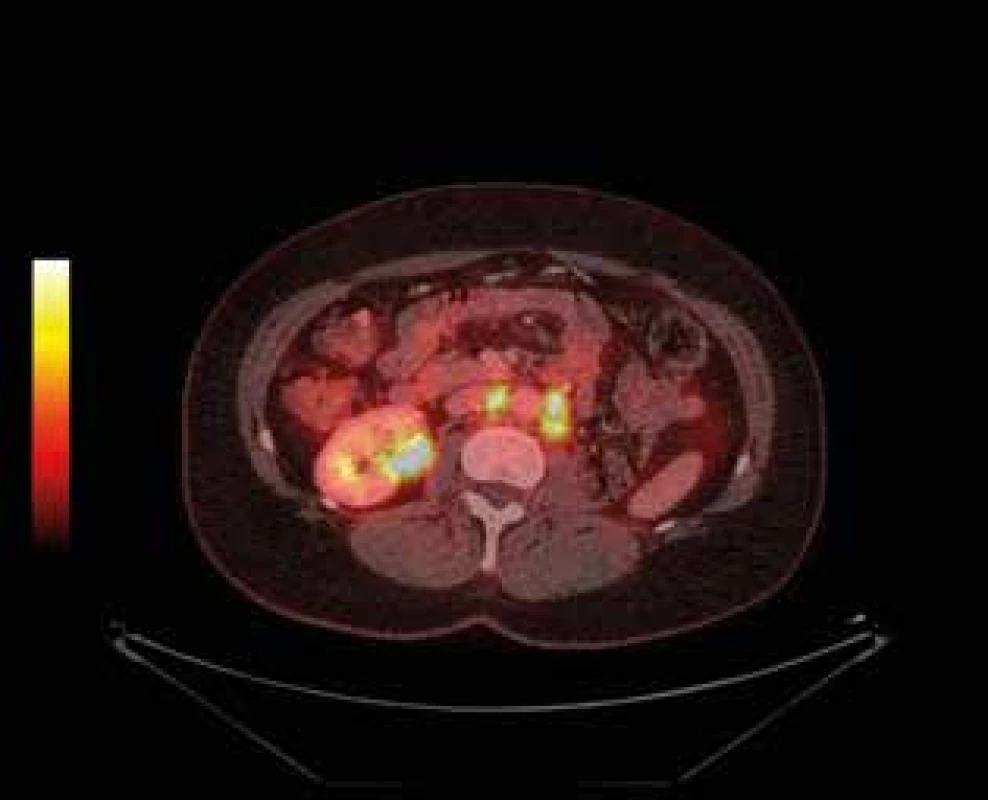
Operační řešení – nefroureterektomie, laparoskopický postup.
Histologicky uroteliální karcinom ledvinné pánvičky: pT2, N0, M0, G3.
Operační řešení – nefroureterektomie, otevřený postup (Obr. 10).
Image 10. Uroteliální karcinom pánvičky pravé ledviny – CT
Fig. 10: Urothelial carcinoma of the renal pelvis of the right kidney − CT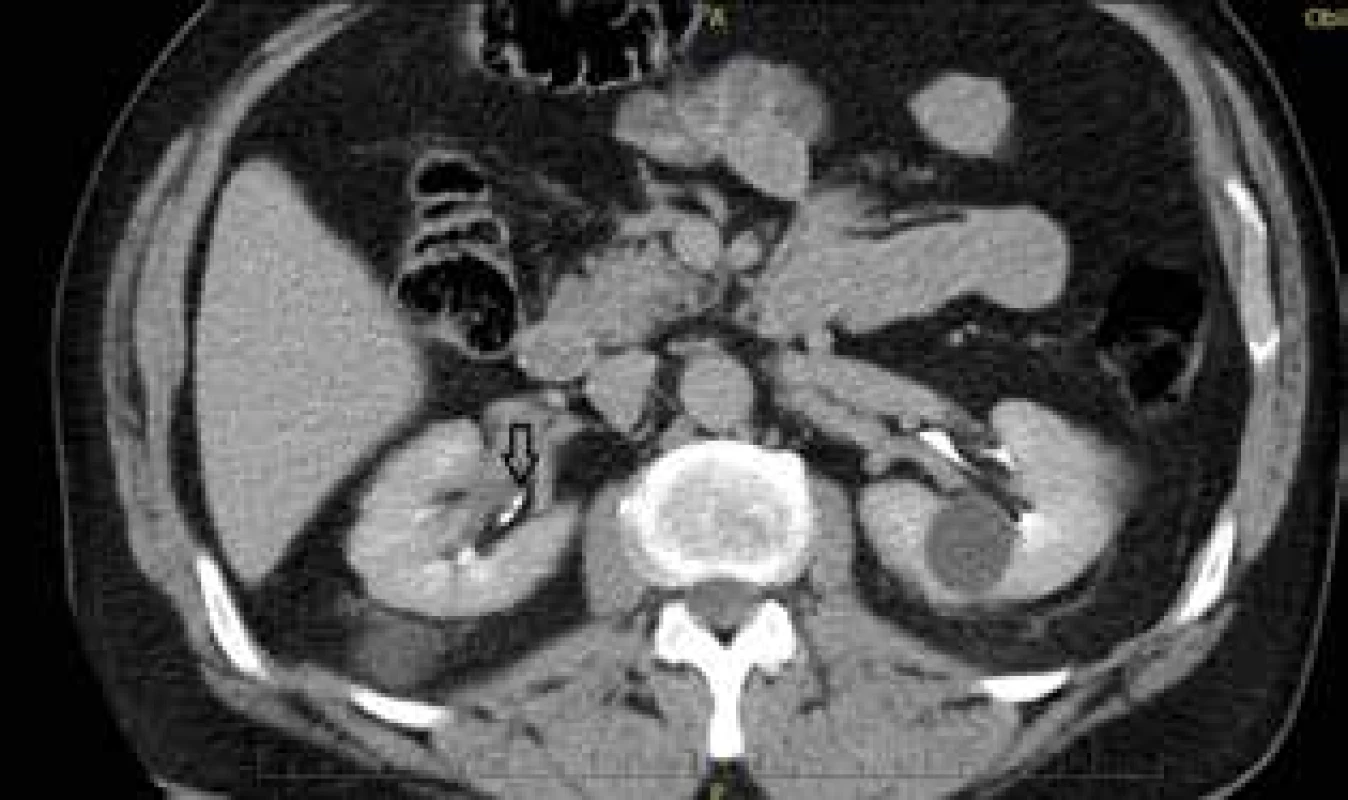
Histologicky uroteliální karcinom ledvinné pánvičky: pT2, N0, M0, G3.
DISKUZE
V literatuře uvádějí Köhler a Belej v r. 2012, že více než 60 % uroteliálních karcinomů horních močových cest je v době diagnózy invazivních, proto zůstává stále zlatým standardem léčby radikální nefroureterektomie [5]. Popsali i vývoj nových endoskopů a resekčně ablačních technik, zdokonalení diagnostiky primárních tumorů i jejich recidiv, a jak je v dnešní době možné významné části nemocných nabídnout ledvinu šetřící operaci. V roce 2011 Macek et al. [3] popsali biologické chování uroteliálních karcinomů horních močových cest. Hodnoceno bylo 121 pacientů za období leden 1996 až leden 2010 s výsledkem, že výrazná část pacientů (47,9 %) přichází s lokálně pokročilým nebo metastatickým onemocněním. I přes radikální léčbu nejsou výsledky příliš příznivé. Bylo zaznamenáno 27 recidiv a 1 progrese onemocnění, tříleté přežití bez recidivy bylo 63,2 %. Nádorově specifické tříleté přežití bylo 80,3 %, celkové tříleté přežití bylo 73,7 %. V roce 2012 Bagley et al. [13] publikovali význam a výhodu odběru biopsií z horních močových cest endoskopicky pomocí košíčku s plochými dráty nebo pomocí bioptických kleští k diagnostice nádorů. V roce 2013 Xylinas et al. [14] zmiňují a hodnotí prognostické faktory užívané u pacientů s UKHMC (včetně klinicko-patologických parametrů a molekulárních markerů) a v současné době dostupné prediktivní instrumenty.
V roce 2017 Liao et al. [15] hodnotili rozdíly v rozdělení patologických stadií pTNM u pacientů s vysoce rizikovým uroteliálním karcinomem horních močových cest (T3/T4 a G3). U těchto pacientů byla dle výsledku ureteronefroskopických biopsií podávána neoadjuvantní chemoterapie před radikální nefroureterektomií. U pacientů, kterým byla podána neoadjuvantní chemoterapie, bylo prokázáno nižší patologické stadium, než bylo u pacientů po radikální nefroureterektomii bez chemoterapie. Navíc u pacientů, kteří podstoupili neoadjuvantní chemoterapii, byla zjištěna úplná remise v 9,4 % případů.
V roce 2018 Liu et al. [16] publikovali srovnání účinnosti a bezpečnosti laparoskopické nefroureterektomie oproti otevřené nefroureterektomii u uroteliálního karcinomu horních cest močových. Laparoskopická nefroureterektomie byla spojena s delším časem operace, kratším pobytem v nemocnici a nižší ztrátou krve. Výskyt komplikací byl podobný u laparoskopické a otevřené operace. Nebyl zaznamenán žádný významný rozdíl v míře pětiletého přežití bez recidivy, v míře pětiletého nádorově specifického přežití a pětiletého celkového přežití.
První porovnávání otevřené a laparoskopické nefroureterektomie bylo vydáno v roce 1993. Prokázalo laparoskopickou alternativu jako možný postup. Invazivní nebo velké nádory byly nevhodné pro laparoskopický postup, ale vzhledem ke zlepšení technik a operačních zkušeností se kritéria pro laparoskopické postupy výrazně rozšířila. V mnoha studiích byl kontroverzně diskutován vliv laparoskopického postupu na vznik recidivy nádorů vlivem zvýšeného isuflačního tlaku a zakládáním portů.
V roce 2018 Samson et al. [17] popsali výhodu endoskopické ureteroskopické nebo perkutánní resekce uroteliálního nádoru horních močových cest u vybraných pacientů při zachování funkce ledviny za srovnatelných onkologických výsledků. Endoskopické výkony jsou výhodné nejen pro diagnózu, ale také jako léčebný postup u malých neinvazivních tumorů. Perkutánní resekce je upřednostňována před ureteroskopickou, a to v případě větších nádorů nebo nádorů nepříznivých pro retrográdní ureteroskopickou resekci (tj. dolní kalich). Navíc perkutánní přístup následně umožňuje antegrádní adjuvantní intrarenální instilaci Bacillus Calmette-Guérin (BCG) nebo mitomycin C (MMC). Výhodou je i možnost monitorování intrarenálního tlaku, který by neměl překročit 25 cmH2O.
Při progresi po chemoterapii na bázi platiny je pro pacienty s pokročilým nebo metastatickým uroteliálním karcinomem k dispozici jen málo účinných možností léčby. Na našem pracovišti se radikální nefroureterektomie (RNU) považovala za zlatý standard u 66,6 % pacientů. Představuje kompletní odstranění ledviny s celým příslušným močovodem včetně terčíku ureterálního ústí a s lemem okolní části močového měchýře (en bloc). V posledních letech je značná pozornost věnována imunoterapii. Léčba je založena na protilátkách inhibujících kontrolní body imunitní reakce. Blokádou inhibiční dráhy PD-1/PD-L1 (tj. dráhy programované buněčné smrti) dochází k utlumení inhibičního signálu, k obnovení účinnosti imunitních mechanismů a ke zvýšení protinádorové aktivity [18].
ZÁVĚR
V diagnostice a léčbě uroteliálních karcinomů horních močových cest došlo k výrazným endoskopickým pokrokům. I přesto pro více než polovinu těchto pacientů zůstává zlatým standardem radikální nefroureterektomie, stejné výsledky má i naše pracoviště. Přínosem endoskopických metod je nejen vizualizace horních močových cest, ale zejména možnost odběru biopsie z onkosuspektních ložisek i provedení záchovných výkonů u indikovaných pacientů, které zajišťují stejnou bezpečnost jako radikální výkony. Celkové přežití nejvíce závisí na přítomnosti vzdálených metastáz. Pro vznik recidivy je hlavním ovlivňujícím parametrem pT kategorie. Existuje celá řada klinických a patologických faktorů, které ovlivňují chování a vývoj uroteliálních karcinomů horních močových cest, zejména jaderný grade nádoru a lymfovaskulární invaze, postižení regionálních lymfatických uzlin, přítomnost nekrózy nádoru, vzhled tumoru (papilární nebo přisedlý) a přítomnost carcinoma in situ. Uroteliální karcinomy horních močových cest jsou bohužel velmi často řešeny až při lokální pokročilosti nebo při uzlinových či vzdálených metastázách, což následně komplikuje i případné podání adjuvantní chemoterapie, která není dostatečně účinná. Podání platiny je dále komplikováno nefrotoxicitou. Celková prognóza nemocných i přes vysoké procento odpovědí je špatná. Střední doba přežití se pohybuje kolem 12 měsíců. V úvahu při diagnostice UKHMC připadají pacienti s rizikovými faktory, například kouření cigaret je spojeno s 3krát vyšším rizikem vzniku nádoru [19]. Riziko vzniku nádoru je vyšší u ureterálního než u pelvického karcinomu a odpovídá celkovému počtu balíčko-roků. U dlouhodobých kuřáků (45 let a více) je riziko přibližně 7krát vyšší. Riziko vzniku nádoru se po zanechání kouření snižuje jen částečně. Bývalí kuřáci mají stále 2krát vyšší riziko oproti lidem, kteří nikdy nekouřili. Abusus analgetik (fenacetin) mělo v anamnéze kolem 20 % nemocných s nádorem pánvičky a 10 % s nádorem močovodu, UKHMC se objevují v odstupu přibližně 20−30 let [19]. Popsán je dobře také vliv pracovní zátěže aromatickými uhlovodíky v petrochemickém průmyslu, při zpracování barviv, gumy, dehtu nebo plastů [3,20]. Přítomnost konkrementů, chronická infekce, pití kávy a cyclophosphamid [1].
Expozice mutagenním metabolitům kyseliny aristolochové má velkou úlohu při vzniku nefropatie „z čínských bylin“ a s ní spojených uroteliálních nádorů horních močových cest (UKHMC) [3]. Podobný vliv je zvažován i při balkánské nefropatii [20]. Nádory při balkánské nefropatii jsou častější u žen, bilaterální, mnohočetné a proti minulým obdobím jsou také agresivnější [3,21,22]. Vysoký výskyt je na Tchaj-wanu [3,23]. Také je nověji uváděno 5% riziko výskytu UKHMC u nemocných s hereditárním nonpolypoidním kolorektálním karcinomem (Lynchův syndrom) [5,24].
Poděkování
Děkuji svému školiteli prim. MUDr. Petru Prošvicovi za podporu, důvěru a cenné zkušenosti.
Konflikt zájmů
Autor článku prohlašuje, že není v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise, s výjimkou kongresových abstrakt a doporučených postupů.
MUDr. Ramez Adwan
Urologické oddělení
Oblastní nemocnice Náchod
e-mail: adwan@email.cz
Sources
- Soukup V. Uroteliální karcinom močovodu. In: Hanuš T, Novák K, et al. Nemoci močovodu. Praha, Galén 2008 : 129−138.
- Colin, P, Koenig, P, Ouzzane A, et al. Environmental factors involved in carcinogenesis of urothelial cell carcinomas of the upper urinary tract. BJU Int. 2009;104(10):1436−1440. doi:10.1111/j.1464-410X.2009.08838.x.
- Macek P, Soukup V, Hanuš T, et al. Zhodnocení charakteru a vývoje onemocnění u nemocných s uroteliálními nádory horních močových cest. Endoskopie 2011;20(3−4):89.
- Prošvic P. Nádory horních močových cest: epidemiologie, etiologie a genetika. In: Dvořáček, J, Babjuk, M, et al. Onkourologie. Praha, Galén 2005 : 70−75.
- Köhler O, Belej K. Léčba uroteliálního karcinomu horních močových cest. Urol praxi 2012;13(5):204−207.
- Fritz GA, Schoellnast H, Deutschmann HA, et al. Multiphasic multidetector-row CT (MDCT) in detection and staging of transitional cell carcinomas of the upper urinary tract. Eur Radiol. 2006;16(6):1244−1252. doi:10.1007/s00330-005-0078-0.
- Petkovic SD. Epidemiology and treatment of renal pelvic and ureteral tumors. J Urol. 1975;114(6):858−865. doi:10.1016/s0022-5347(17)67160-x.
- Louda M, Hafuda A, Morávek P, et al. Koincidence uroteliálního karcinomu horních močových cest a močového měchýře. Ces Urol. 2003;7(1):8−10.
- Huben RP, Mounzer AM, Murphy GP. Tumour grade and stage as prognostic variables in upper urinary tract tumours. Cancer 1988;62(9):2016−2020. doi:10.1002/1097-0142(19881101) 62 : 9<2016:aid-cncr2820620924> 3.0.co;2-g.
- Kakizoe T, Fujita J, Murase M, et al. Transitional cell carcinoma of the bladder in patients with renal pelvic and ureteral cancer. J Urol. 1980;124(1):17−19. doi:10.1016/s0022-5347(17)55269-6.
- Oldbring J, Glifberg I, Mikulowsky PM, et al. Carcinoma of the renal pelvis and ureter following bladder carcinoma: frequency, risk factors and clinicopathological findings. J Urol. 1989;141(6):1311−1313. doi:10.1016/s0022-5347(17)41291-2.
- Hurle R, Losa A, Manzetti A, et al. Upper urinary tract tumors developing after treatment of superficial bladder cancer: 7-year follow-up of 591 consecutive patients. Urology 1999;53(6):1144−1148. doi:10.1016/s0090-4295(99)00002-3.
- Bagley DH, Healy KA, Kleinmann N, et al. Ureteroskopická biopsie tumorů horních cest močových: endoskopické a cytologické techniky. Urol List. 2012;10(2):26−30.
- Xylinas E, Klatte T, Matin S, et al. Prognostické faktory, molekulární markery a prediktivní instrumenty pro hodnocení uroteliálního karcinomu horních cest močových. Urol List. 2013;11(3):30−39.
- Liao RS, Gupta M, Schwen ZR, et al. Comparison of pathological stage in patients treated with and without neoadjuvant chemotherapy for high risk upper tract urothelial carcinoma. J Urol. 2018;200(1):68−73. doi:10.1016/j.juro.2017.12.054.
- Liu F, Guo W, Zhou X, et al. Laparoscopic versus open nephroureterectomy for upper urinary tract urothelial carcinoma: a systematic review and meta-analysis. Medicine (Baltimore) 2018;97(35):e11954. doi:10.1097/MD.0000000000011954.
- Samson P, Smith AD, Hoenig D, et al. Endoscopic management of upper urinary tract urothelial carcinoma. Journal of Endourology 2018;32(S1):S10−S16. doi: 10.1089/end.2018.0036.
- Zatloukalová P, Pjechová M, Babčanová S, et al. Úloha PD-1/PD-L1 signalizace v protinádorové imunitní odpovědi. Klin Onkol. 2016;29(suppl. 4):72−77.
- Kawaciuk I. Urologie. Praha, Galén 2009.
- Rouprêt M, Zigeuner R, Palou J, et al. European guidelines for the diagnosis and management of upper urinary tract urothelial cell carcinomas: 2011 update. Eur Urol. 2011;59(4):584–594. doi:10.1016/j.eururo.2010.12.042.
- Stefanovic V, Radovanovic Z. Balkan endemic nephropathy and associated urothelial cancer. Nat Clin Pract Urol. 2008;5(2):105−112. doi: 10.1038/ncpuro1019.
- Sostarić B, Vukelić M. Characteristics of urinary tract tumours in the area of Balkan endemicnephropathy in Croatia. IARC Sci Publ. 1991;(115):29−35.
- Yang MH, Chen KK, Yen CC, et al. Unusually high incidence of upper urinary tract urothelial carcinoma in Taiwan. Urology 2002;59(5):681−687. doi:10.1016/s0090-4295(02)01529-7.
- Rouprêt M, Yates DR, Comperat E, et al. Upper urinary tract urothelial cell carcinomas and other urological malignancies involved in the hereditary nonpolyposis colorectal cancer (Lynch syndrome) tumor spectrum. Eur Urol. 2008;54(6):1226−1236. doi: 10.1016/j.eururo.2008.08.008.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2020 Issue 5-
All articles in this issue
- Manažment liečby dehiscencie pažerákovej anastomózy po ezofagektómii pre karcinóm pažeráka
- Časné komplikace u operací pupečních a epigastrických kýl
- Chirurgická léčba zlomenin krční páteře v terénu ankylozující spondylitis: zadní stabilizace s užitím navigace založené na intraoperačním CT zobrazení
- Uroteliální karcinomy horních močových cest – naše zkušenosti
- “Maximálna” miniinvazívna tymektómia u pacientov s netymomatóznou myasténiou gravis – krátkodobé výsledky za obdobie 10 rokov – retrospektívna štúdia
- Nitrobřišní absces při salmonelóze − kazuistika
- Aorto-kavální píštěl – kazuistické sdělení
- Covidí příležitost
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Časné komplikace u operací pupečních a epigastrických kýl
- Uroteliální karcinomy horních močových cest – naše zkušenosti
- Manažment liečby dehiscencie pažerákovej anastomózy po ezofagektómii pre karcinóm pažeráka
- Nitrobřišní absces při salmonelóze − kazuistika
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

