-
Medical journals
- Career
Plicní kontuze
Authors: A. Stolz; J. Schützner; R. Lischke
Authors‘ workplace: 3. chirurgická klinika 1. LF Univerzity Karlovy a FN Motol, Praha přednosta: prof. MUDr. R. Lischke, Ph. D.
Published in: Rozhl. Chir., 2017, roč. 96, č. 12, s. 488-492.
Category: Review
Overview
Plicní kontuze je poranění plicního parenchymu na podkladě traumatu hrudníku. Nachází se asi u 23−35 % všech tupých poranění hrudníku. Následkem traumatu dochází k poškození alveolárních kapilár, což má za následek akumulaci krve a tekutin v plicním parenchymu. To má vliv na zhoršenou výměnu plynů, která vede k hypoxemii. Mezi následky plicní kontuze patří ventilačně/perfuzní nerovnováha, zvýšení AV zkratů a zhoršení compliance plicního parenchymu. Tyto fyziologické následky se manifestují obvykle během několika hodin po traumatu a k jejich vymizení dochází během týdne. Hlavním diagnostickým nástrojem je počítačová tomografie, která je velmi senzitivní při diagnostice plicní kontuze. Mezi klinické příznaky patří hypoxemie a hypekapnie, které se manifestují hlavně během 72 hodin po úraze. Terapie samotné plicní kontuze je ve většině případů konzervativní. K chirurgické intervenci může dojít pro hemothorax spojený s kontuzí plíce nebo progresi A-V shuntů při lokalizované plicní kontuzi.
Klíčová slova:
plicní kontuze − tupé poranění hrudníku − počítačová tomografieÚvod
V roce 1761 italský lékař Giovanni Battista Morgani jako první popsal poškození plic bez otevřeného poranění hrudníku. Tím, kdo zavedl termín plicní kontuze, byl francouzský vojenský chirurg Guillaume Dupuytren v 19. století. Do 20. století byla plicní kontuze (pulmonary contusion – PC) vcelku nepoznaným a málo probádaným patologickým stavem. Během 1. světové války bylo pozorováno signifikantní množství úmrtí vojáků bez zevních známek traumatu hrudníku. Při pitvě se pak zjistilo rozsáhlé poškození plic s intersticiálním krvácením [1,2]. Následné rozbory těchto případů identifikovaly plicní kontuzi jako signifikantní následek výbuchu a střel během této války. Tato pozorování se opakovala také během 2. světové války. Zjistilo se, že poraněná plíce produkuje více intersticiální a intraalveolární tekutiny než plíce u zdravých jedinců [1]. Dalším fenoménem byl fakt, že poraněná plíce měla zhoršenou schopnost se zbavovat přebytečné tekutiny. Na rozdíl od plicní kontuze jako následku vojenských akcí byla kontuze v civilním životě do 50. let minulého století vcelku zřídkavá. S rozvojem motorismu došlo k signifikantnímu nárůstu tupých poranění u civilistů jako obětí dopravních nehod. V současné době jsou v 70 % dopravní nehody příčinou tupých poranění hrudníku [2,3]. Vzhledem k rozvoji globalizace a cestovního ruchu lze předpokládat, že tato incidence dále poroste. Úmrtí jako následek tupých traumat hrudníku může být ve třech časových fázích [3]. Jednak na místě úrazu, a to jako následek například ruptury aorty či krčních poranění páteře. Část pacientů umírá v průběhu několika hodin nebo dní po úraze následkem těžkého krvácení, plicního selhání, kardiogenního šoku nebo rozsáhlého poranění mozku. Třetí skupina pacientů umírá v rozmezí dnů až týdnů. Většinou jde o následek infekce nebo multiorgánového selhání [3].
Etiopatogeneze
Plicní kontuze vzniká náhlou decelerací, kdy pohybující se hrudník narazí na fixovaný objekt. Objevuje se asi u 23–35 % všech tupých poranění hrudníku [1,2,4]. Tehdy může kontuze doprovázet jednoduchou nebo blokovou zlomeninu žeber, vyskytovat se může také bez poranění skeletu hrudníku. Poranění plicního parenchymu vede k patofyziologickým změnám a jejich závažnost závisí na rozsahu poranění (Obr. 1). Do nedávné doby byla kontuze plíce charakterizována jako intersticiální hemoragie a otok, bez lacerace. V současné době jsou práce, kdy se pod pojmem plicní kontuze rozumí také tupé poranění plíce zahrnující plicní laceraci s intraparenchymovým a intraalveolárním krvácením [4]. Při stlačení hrudníku může dojít k laceraci plíce, ale skelet hrudníku může zůstat intaktní. Během tupého poranění hrudníku s rozvojem plicní kontuze může docházet k akutní zánětlivé odpovědi, zvýšení alveolo-kapilární permeability a plicnímu edému. Přítomná je také ventilačně/perfuzní dysbalance, zvýšení A-V zkratů a také může docházet ke ztrátě compliance plicního parenchymu. Počáteční zánětlivá odpověď plicního parenchymu na přímý nebo nepřímý podnět obsahuje aktivaci leukocytů v krvi, tkáňových makrofágů a produkci série mediátorů jako cytokinů, chemokinů nebo metabolitů kyseliny arachidonové. Tato zánětlivá odpověď může postihnout i neporaněnou kontralaterální plíci s rozvojem edému a zesílení alveolárních sept. Těžká zánětlivá odpověď může vést k rozsáhlé poruše činnosti plicního parenchymu s následným ARDS (Acute Respiratory Distress Syndrome).
Image 1. Rozsáhlá plicní kontuze v levém dolním laloku se sdruženým poraněním hrudníku Fig. 1: Extensive pulmonary contusion in the left lower lobe with chest wall injury 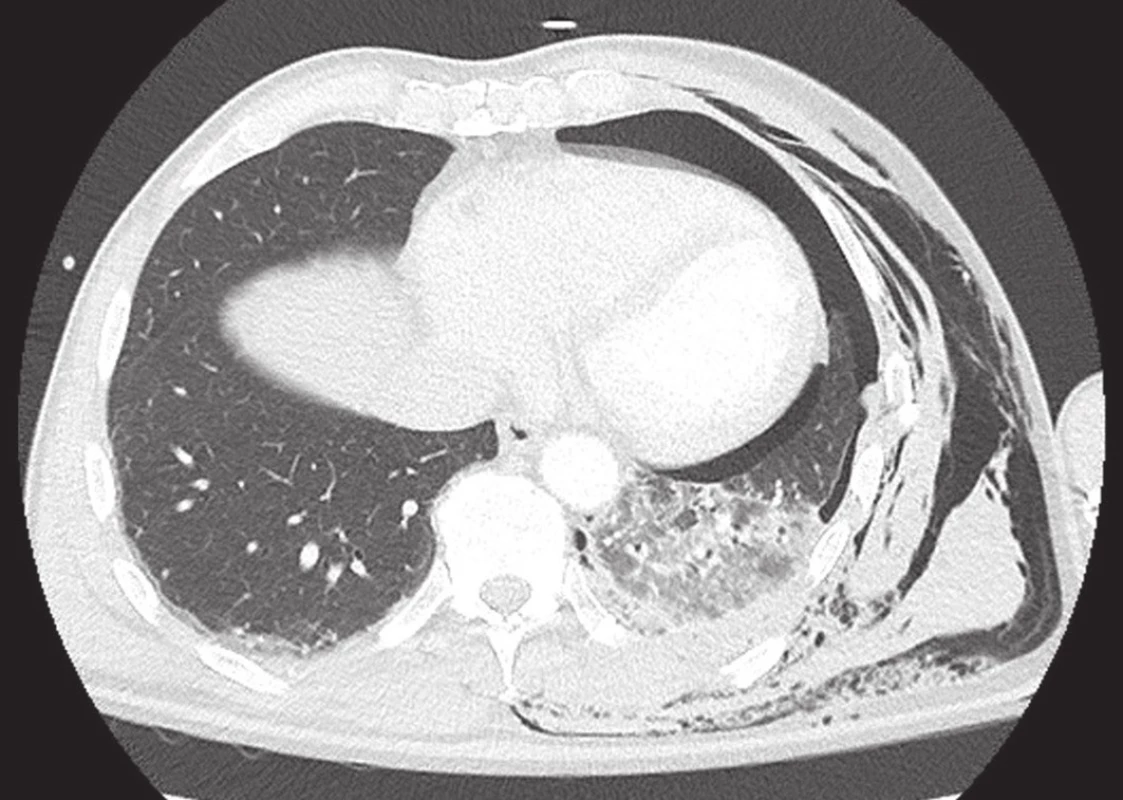
Během plicní kontuze může také docházet k abnormalitám v činnosti surfaktantu se zvýšením koncentrací alveolárních plazmatických proteinů. Poruchy funkce surfaktantu jsou nejčastější v prvních 24 hodinách po traumatu [2]. Právě porucha činnosti surfaktantů může vést ke zvýšení povrchového napětí. To následně může zapříčinit kolaps, atelektázu a konsolidaci plicního parenchymu. Během následujících 48–96 hodin se může hodnota surfaktantu vracet do normálu spolu se zlepšujícím se stavem plicního parenchymu. Atelektázu plicního parenchymu může způsobit také bronchiální obstrukce krevními koaguly [4].
Po tupém poranění hrudníku s rozvojem plicní kontuze dochází k poklesu v poměru ventilace/perfuze plicního parenchymu. Tento poměr je snížen u plicní kontuze. Tekutinou vyplněné alveoly se nenaplní vzduchem, nedochází k saturaci hemoglobinu kyslíkem. S poklesem tohoto poměru na podkladě vyřazení plicního parenchymu z ventilace dochází následně ke snížení saturace krve kyslíkem. Plicní zkrat je odpovědí plicního parenchymu, když alveoly jsou perfundované krví, ale ventilace těchto perfundovaných alveolů je nedostatečná. Dále dochází k hypoxemické vasokonstrikci.
Klinický obraz
Klinický obraz plicní kontuze závisí na stupni poškození plicního parenchymu a dalších přidružených poraněních, která často mohou doprovázet plicní kontuzi. Porucha výměny plynů v oblasti alveolů způsobí pokles saturace krve kyslíkem, cyanózu a tachypnoi. Klinicky nacházíme oslabené dýchání, může se vyskytnout hemoptoe, i když není zásadního významu. V případě pokračování stavu na podkladě plicní kontuze se může pacient dostat až do stavu ARDS. Tento stav se vyskytne asi v 17 % případů, kdy jde o izolovanou plicní kontuzi [2]. Když je plicní kontuze doprovázena poraněním jiných orgánů, ARDS se vyskytne skoro v 80 % případů. Mezi další komplikace plicní kontuze patří také pneumonie, která se může vyskytnout asi v 20 % všech pacientů s plicní kontuzí [1,4]. Krevní koagula v alveolech poskytují bakteriím živnou půdou s možností rozvoje následné infekce. Je otázka, zda podávat profylakticky antibiotika u pacientů s izolovanou plicní kontuzí. Žádná studie neprokázala přínos takto podávaných antibiotik [1,2]. Na druhé straně necílená aplikace antibiotik může vést k rozvoji rezistence na antibiotika. Zde je na místě prevence jako důsledná analgetická terapie a dechová rehabilitace s cílem zamezení bronchiální retence. Krvácení v oblasti kontuzního ložiska může progredovat směrem k viscerální pleuře s rozvojem hemothoraxu nebo pneumothoraxu [4]. Kontuzní ložisko s prokrvácením plicního parenchymu může progredovat a vyplnit celý plicní lalok. Za těchto okolností může být indikovaná plicní lobektomie. Vzduch z kontuzního ložiska může podél perivaskulárních prostor postoupit až k mediastinu se vznikem podkožního emfyzému. Ten se projeví na krku svým typickým nálezem nebo je jenom nálezem na CT vyšetření pacienta. V souvislosti s tupým poraněním hrudníku, které zapříčiní plicní kontuzi a zlomeninu žeber, se mohou vyskytovat také traumatické plicní pseudocysty (traumatic pulmonary pseudocysts − TPP). Vyskytují se pouze u 2−10 % tupých poranění a jsou diagnostikované pomocí CT vyšetření [5]. Průměrné ISS (Injury Severity Score) skóre, které se vyskytlo u pacientů s pseudocystou, bylo 33,2 [5]. Je to dáno tím, že pseudocysty se vyskytují při větším rozsahu poranění hrudníku a na jejich vytvoření je nutná větší síla (Obr. 2). I proto je jejich incidence u automobilových dopravních nehod vyšší než u nehod motocyklů nebo pádů. Na rozsah pseudocyst má také vliv ohebnost hrudního koše. Vyšší podíl TPP je u mladších pacientů (věk <15 let), na což může mít vliv vyšší elasticita a ohebnost hrudníku u této skupiny pacientů. Také u této skupiny pacientů byl nižší počet zlomených žeber než u vyšší věkové skupiny [5]. Wagner klasifikoval TPP do 4 skupin na podkladě rozsahu poranění, CT nálezu a mechanismu poranění. Při typu 1 a 2 je přítomnost cyst s hydroaerickým fenoménem uvnitř plicního parenchymu, což je to způsobeno náhlým stlačením hrudního koše [5]. Tyto typy se vyskytují u mladších pacientů, což souvisí s ohebností hrudního koše. Tento typ TPP se objevuje v případech, kdy poranění je vyššího ISS skóre s vyšší energií nárazu. U typu 3 a 4 jde o cysty v blízkosti zlomených žeber, někdy klasifikované jako subpleurální. U tupého poranění hrudníku dochází nejčastěji ke zlomenině 4.–10. žebra. Přítomnost pseudocysty 3. a 4. typu je nejčastěji u zlomeniny v oblasti 4.–5. žebra. Počet zlomených žeber nebyl signifikantní rizikový faktor k vytvoření pseudocysty. Komplikací pseudocyst může být masivní hemoptýza nebo jejich infikování. V těchto případech je nutné zvážit plicní resekci nebo perkutánní drenáž. Nutnost těchto intervencí je však nízká. Postupem času spíše dochází k vyplnění pseudocysty tekutinou a s odstupem několika týdnů k jejich úplné resorpci.
Image 2. Traumatická plicní pseudocysta v pravém dolním laloku Fig. 2: Traumatic pulmonary pseudocyst in the right lower lobe 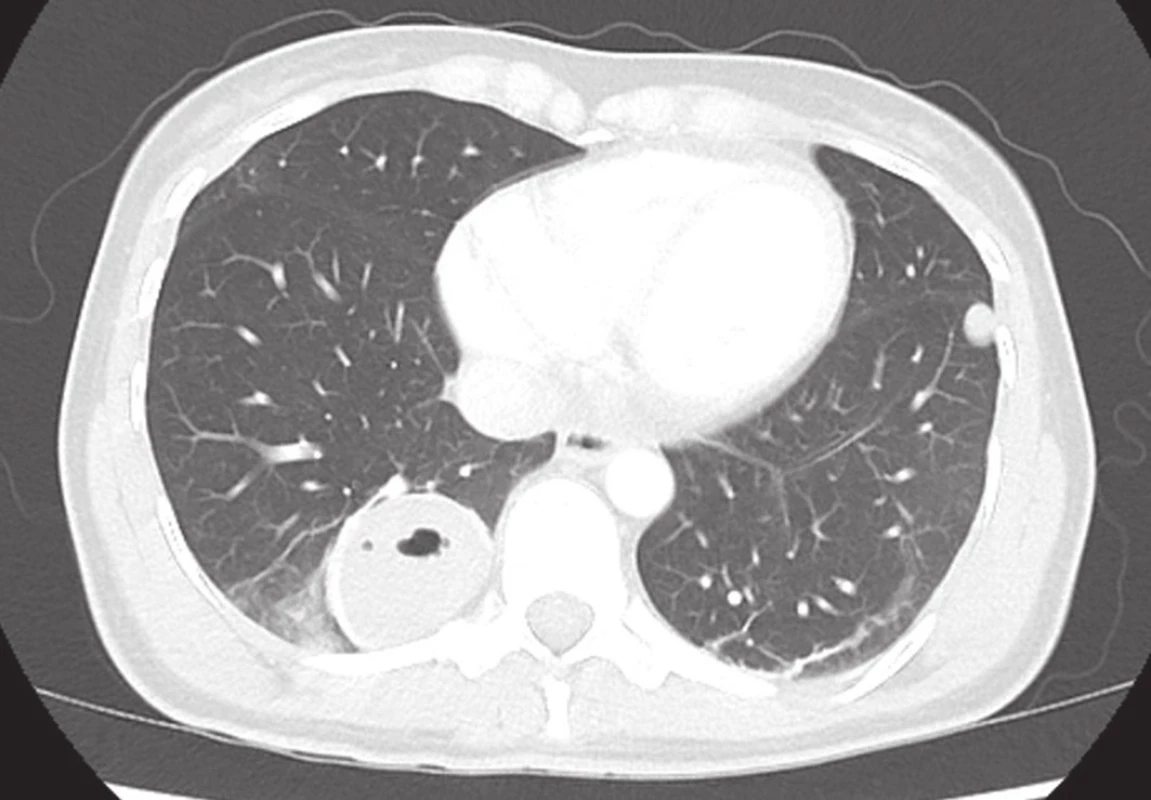
Diagnostika
Na skiagramu hrudníku je možné vidět plicní kontuzi jako nález kondenzace plicního parenchymu. Tento nález velmi často nerespektuje anatomické hranice segmentů nebo laloků. Zobrazuje se cca 4–6 hodin po úraze a při příznivém průběhu mizí během několika dní. Přítomnost hemothoraxu nebo pneumothoraxu může zamezit identifikaci plicní kontuze na skiagramu. Zdá se, že může být také úměra mezí rozsahem těchto kondenzací na skiagramu plic a závažností klinického stavu [2]. V současné době většina trauma center při tupých poraněních indikuje provedení celotělových CT vyšetření. To souvisí s lepší senzitivitou a specificitou CT proti prostému skiagramu hrudníku při diagnostice následku poranění hrudníku. Nález na CT hrudníku může být od nepravidelných obláčkových oblastí konsolidace do difuzní a rozsáhlé homogenní konsolidace. Vyšetření CT je vysoce senzitivní v detekci plicní kontuze. Objem postiženého plicního parenchymu může korelovat se závažností klinického stavu pacienta [4,6]. Rodriguez publikoval studii, kde porovnával pacienty po tupém poranění hrudníku [7]. Hodnotil přítomnost plicní kontuze na CT a skiagramu hrudníku a také přítomnost jiných sdružených poranění. Plicní kontuze byla u 26,5 % pacientů izolovaná. Ve zbylých 73,5 % případů měli pacienti další poranění hrudníku: frakturu žeber (55,8 %), pneumothorax (44,9 %), hemothorax (17,3 %) nebo frakturu sterna (9,7 %). Hospitalizace u pacientů s kontuzí a jiným typem poranění byla v 95 % případů. Mortalita této skupiny 5,1 %. Celkem 4,8 % pacientů s plicní kontuzí bylo napojeno na umělou plicní ventilaci. V této skupině mělo 82,4 % pacientů sdružené poranění hrudníku.
Plicní kontuze může být izolovaná nebo součástí polytraumatu. S cílem objektivním způsobem posoudit závažnost traumatu a stanovit prognózu pacienta je vhodné zvolit skórovací systém. Těch je několik. Jejich dělení může být na podkladě poškození anatomických struktur, na podkladě fyziologických parametrů nebo jejich kombinací [8]. Pro posouzení anatomického postižení u pacienta s polytraumatem se používá Injury Severity Score (ISS). Na základě tohoto systému je tělo pacienta rozděleno na oblasti a každou tuto oblast může postihnout postižení od lehkého až po kritické. Maximální skóre je 75. Při skóre ISS=40 ve věkové skupině 15−44 let je úmrtnost 50 % [8]. Jako závažné poranění se hodnotí ISS>16. Skórovací systém APACHE II (Acute Physiology And Chronic Health Evaluation) byl založen s cílem hodnocení závažnosti stavu pacienta na podkladě kvantifikace stupně poruchy jednotlivých fyziologických parametrů. V tomto systému se hodnotí celkem dvanáct fyzikálně, biochemický a hematologicky vyšetřovaných položek. Systém TRISS (TRauma ISS) kombinuje anatomické postižení (ISS) se změnou fyziologických parametrů (TS-Trauma Score). Při tomto skórovacím systému se zohledňuje také mechanismus úrazu, tj. jestli se jedná o tupé, nebo penetrující trauma. Tento systém umožňuje stanovit pravděpodobnost přežití pacienta. Radiologický skórovací systém hodnotí velikost, objem plicní kontuze na podkladě 3D rekonstrukcí na počítačové tomografii (Wagner Score – Grade 1 více než 28 %, Grade 2 19–27 %, Grade 3 méně než 19 %) [6]. Nevýhodou této klasifikace je, že nebere zřetel na asociované poranění nebo klinický stav pacienta. Miller provedl studii, kdy hodnotil velikost plicní kontuze na základě CT a vztah k rozvoji ARDS [6]. U pacientů s plicní kontuzí, která byla větší než 20 % plicního parenchymu dle CT, se ARDS vyskytlo u 82 %. U druhé skupiny pacientů, kteří měli velikost plicní kontuze <20 %, se ARDS vyskytlo jenom u 22 % pacientů. Riziko vzniku ARDS u těchto pacientů nestoupalo lineárně. Naopak, riziko se zásadně zvýšilo, pokud se objem plicní kontuze zvýšil nad 20 %.
Terapie
Terapie samotné plicní kontuze je hlavně konzervativní. U lehčích forem plicní kontuze, která se nachází u většiny pacientů, léčba spočívá ve starostlivosti o dýchací cesty (podávaní mukolytik, bronchodilatancí, aplikace nebulizace, dechová rehabilitace) [1,2,4]. Rutinní podávaní antibiotik, kortikoidů nebo diuretik není indikováno. Dle klinického stavu na podkladě kontroly krevních plynů Astrupa nebo pulzní oxymetrií podáváme oxygenoterapii. Dále je nutná adekvátní analgetická terapie. Bolest, která doprovází úrazy hrudníku, může následně vést k hypoventilaci u pacienta s plicní kontuzí. Výsledkem tohoto stavu může být atelektáza a další plicní komplikace. Účinná analgoterapie je základem prevence těchto stavů. Analgetika lze podávat jak v perorální, tak v parenterální formě. Jejich účinek nemusí být dostatečný, proto se doporučuje interkostální blokáda [4]. Jde o výkon vcelku jednoduchý, s minimem komplikací a s dobrým pokrytím bolesti pacienta. Další možností je zavedení epidurálního katétru. Bulger ve své prospektivní randomizované studii porovnával vliv epidurální analgezie a iv. opioidů na komplikace u 48 pacientů s traumatem hrudníku [9]. Obě skupiny měly podobné ISS skóre (25 vs. 26), APACHE II (13 vs. 11) a počet zlomených žeber (7,2 vs. 6,8) a incidenci plicní kontuze (59 % vs. 38 %). Ve skupině epidurální analgezie byl signifikantně nižší výskyt nozokomiální pneumonie (18 % vs. 38 %). Riziko pneumonie ve skupině iv. opioidů bylo vyšší (OR=6, CI 1,0-35, p=0,05). To se přičítá lepší terapii bolesti ve skupině pacientů s epidurálním katétrem s následnou lepší dechovou rehabilitací pacientů. Problémem může být, že ne vždy je možné zavést epidurální katétr. Jedná se o stavy s poraněním páteře, deformity páteře, infekce hrudní stěny, koagulopatie. Bulger do své studie nemohl zařadit celkem 69 % pacientů, protože z důvodů kontraindikací nebylo možné zavést epidurální katétr. Ale i tak existuje velká skupina pacientů (třetina všech po těžkých traumatech hrudníku), která by mohla mít benefit ze zavedení epidurálního katétru [1].
U těžkých forem plicní kontuze je nutné počítat s nutností různých forem neinvazivní nebo invazivní umělé plicní ventilace (UPV). Antonelli v roce 2001 provedl prospektivní studii u 354 pacientů s akutní respirační insuficiencí, kterým byla podaná neinvazivní pozitivní tlaková ventilace (noninvasive positive pressure ventilation – NPPV) [10]. U 30 % pacientů bylo nakonec nutno provést intubaci. Nejvyšší riziko nutnosti intubace bylo u pacientů s ARDS (51 %) a nozokomiální pneumonií (50 %). Nejnižší počet intubací byl u pacientů s kardiogenním plicním edémem (10 %) a plicní kontuzí (18 %). K provedení NPPV můžeme použít jak helmy, tak celoobličejové nebo oronazální masky. Co se týče komfortu pacienta a celkové doby použití NPPV, není většího rozdílu mezi oběma typy masek pro NPPV. V případě progrese respirační insuficience a nutnosti UPV je nutné, aby anesteziologové dle stavu pacienta a plicního parenchymu nastavili odpovídající ventilační režim s použitím PEEP. Ventilační podpora u pacienta s ARDS musí být komplexní. Compliance plic je redukovaná. Heterogenita míst poranění plicního parenchymu představuje pro pacienta riziko plicního poškození umělou plicní ventilací z nadměrné hyperinflace nepoškozeného plicního parenchymu [11]. V některých případech, kdy se ani při použití všech nástrojů umělé plicní ventilace u ARDS pacientů (pronační pozice, aplikace NO) stav pacientů nelepší, je možné uvažovat o použití ECMO (ExtraCorporal Membrane Oxygenation). Je několik možností konfigurace tohoto systému (VV-veno-venózní, VA-veno-arterialní, periferní, centrální). Použití VA konfigurace umožňuje plnou hemodynamickou podporu, která u refrakterních šokových stavů neodpovídá na konvenční terapii. Tím můžeme docílit hemodynamické stability a dostatečné systémové perfuze. Konfiguraci VV je možné použít u plicního selhání s cílem zlepšit oxygenii tkání a odstranění přebytečného CO2. Použití ECMO dává čas plicnímu parenchymu na zotavení. To nám umožňuje nepoužívat invazivní ventilační režimy, které by mohly prohloubit akutní plicní poškození. Bonacchi publikoval studii 18 pacientů po traumatu hrudníku s použitím ECMO [3]. Doba od traumatu po zavedení ECMO byla 356±216 minut. Celkem přežilo 5 pacientů (5/18, 28 %). Bosarge publikoval použití ECMO u 15 pacientů s ARDS jako následkem traumatu hrudníku [11]. U těchto pacientů bylo průměrné skóre ISS 26 a skóre APACHE II 24. U 10 pacientů byla použita konfigurace VV. Celková mortalita ECMO pacientů byla 66 % (10/15). Krvácivé komplikace (GIT krvácení, krvácení kolem kanyly) se vyskytly u 40 % pacientů. U 26 % pacientů se vyskytla tromboembolická komplikace v kanyle ECMO přístroje, bez další tromboembolické konsekvence pro pacienta. Tyto komplikace neovlivnily celkovou mortalitu souboru pacientů. Celkově autoři konstatují, že ECMO lze užít při terapii refrakterní ARDS, ale je vhodné jeho použití na začátku ARDS, kdy ještě není těžce porušena mikrocirkulace tkání [3,11]. Při těžkém šokovém stavu, který trvá delší dobu, již ECMO spíše není indikována, jelikož výsledky nejsou dobré a zásadně nezlepší prognózu pacienta.
Závěr
Plicní kontuze je častým následek tupého traumatu hrudníku. Klinický obraz pacienta závisí jak na velikosti plicní kontuze, tak na přítomnosti sdružených poranění hrudníku a celkovém stavu pacienta. Terapie samotné plicní kontuze je většinou konzervativní. K chirurgické intervenci dochází u nevelkého počtu pacientů, hlavně pro hemothorax spojený s kontuzí plíce nebo progresi A-V shuntů při lokalizované plicní kontuzi.
Konflikt zájmů
Autoři článku prohlašují, že nejsou v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise.
doc. MUDr. Alan Stolz
3. chirurgická klinika 1. LF UK a
FN Motol
V Úvalu 84
150 00 Praha 5
e-mail: alan.stolz@fnmotol.cz
Sources
1. Cohn SM, DuBose JJ. Pulmonary contusion: an update on recent advances in clinical management. World J Surg 2010;34 : 1959−70.
2. Ganie FA, Lone H, Lone GN, et al. Lung contusion: a clinico-pathological entity with unpredictable clinical course. Bull Emerg Trauma 2013;1 : 7−16.
3. Bonacchi M, Spina R, Torracchi L, et al. Extracorporeal life support in patients with severe trauma: an advanced treatment strategy for refractory clinical settings. J Thorac Cardiovasc Surg 2013;145 : 1617−26.
4. Fiala P, Lischke R. Tupé poranění hrudníku. Rozhl Chir 2005;84 : 334−41.
5. Cho HJ, Jeon YB, Ma DS, et al. Traumatic pulmonary pseudocysts after blunt chest trauma: prevalence, mechanism of injury, and computed tomography findings. J Trauma Acute Care Surg 2016;79 : 425−31.
6. Miller PR, Croce MA, Bee TK, et al. ARDS after pulmonary contusion: accurate measurement of contusion volume identifies high-risk patients. J Trauma 2001;51 : 223−30.
7. Rodriguez RM, Friedman B, Langdorf MI, et al. Pulmonary contusion in the pan-scan era. Injury 2016;47 : 1031−4.
8. Mommsen P, Zeckey C, Andruszkow H, et al. Comparison of different thoracic trauma scoring systems in regards to prediction of post-traumatic complications and outcome in blunt chest trauma. J Surg Res 2012;176 : 239−47.
9. Bulger EM, Edwards T, Klotz P, et al. Epidural analgesia improves outcome after multiple rib fractures. Surgery 2004;136 : 426−30.
10. Antonelli M, Conti G, Moro ML, et al. Predictors of failure of noninvasive positive pressure ventilation in patients with acute hypoxemic respiratory failure: a multicenter study. Intensive Care Med 2001;27 : 1718−28.
11. Bosarge PL, Raff LA, McGwinn G, et al. Early initiation of extracorporeal membrane oxygenation improves survival in adult trauma patients with severe adult respiratory distress syndrome. J Trauma Acute Care Surg 2016;81 : 236−43.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2017 Issue 12-
All articles in this issue
- Ruptury bránice
- Poranění hrudníku u dětí s polytraumatem
-
Assessment of thoracic trauma at the 1st Department of Surgery in Brno
(1 January 2011 – 31 December 2015) - Překvapivý nález při revizi hrudníku pro střelné poranění – kazuistika
- Myxoidní liposarkom v břišní dutině − kazuistika
- Překvapivý histologický nález v resekátu omenta pro uskřinutou pupeční kýlu
- Plicní kontuze
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Plicní kontuze
- Ruptury bránice
- Myxoidní liposarkom v břišní dutině − kazuistika
- Poranění hrudníku u dětí s polytraumatem
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

