-
Medical journals
- Career
Peroperační verifikace integrity kolorektální anastomózy
Authors: L. Martínek 1; R. Bergamaschi 2; J. Hoch 1
Authors‘ workplace: Chirurgická klinika 2. LF UK v Praze a Fakultní nemocnice Motol, přednosta: prof. MUDr. J. Hoch, CSc. 1; Division of Colon and Rectal Surgery, University of New York, Stony Brook, chief of division: prof. MD R. Bergamaschi, PhD. 2
Published in: Rozhl. Chir., 2015, roč. 94, č. 5, s. 185-188.
Category: Review
Overview
Časné pooperační komplikace hojení anastomózy představují pro pacienta významné riziko zvýšení morbidity, mortality i zhoršení dlouhodobých výsledků. Existuje řada opatření redukujících rizika vzniku těchto komplikací včetně peroperačního hodnocení kvality kolorektální anastomózy. Postupy hodnocení spolehlivosti anastomózy se vyvíjely od mechanického testování přes endoskopickou vizualizaci střevního lumen až po moderní techniky hodnotící mikroperfuzi perianastomotických tkání. Mechanické testování kolorektální anastomózy a částečně i endoskopické techniky prokazatelně do jisté míry redukují riziko pooperačních komplikací hojení kolorektální anastomózy. Moderní postupy hodnotící mikrocirkulaci, založené na fluorescenční angiografii pomocí indocyaninové zeleně, mají potenciál zásadně zlepšit posouzení bezpečnosti kolorektální anastomózy a významně přispět k rozhodnutí o dalším postupu včetně vynechání protektivní ileostomie.
Klíčová slova:
kolorektální chirurgie – komplikace – NIR angiografie – indocyaninová zeleňÚvod
Vytvoření spolehlivé kolorektální anastomózy je jedním z klíčových momentů chirurgie tlustého střeva a konečníku. Porucha hojení této anastomózy představuje komplikaci s obvykle závažnými důsledky. Z krátkodobého úhlu pohledu se selhání anastomózy projeví vyšší morbiditou a mortalitou, prodloužením doby hospitalizace a v neposlední řadě také významným navýšením nákladů. Z dlouhodobého hlediska pak poruchy hojení kolorektální anastomózy mohou u maligních onemocnění snižovat dlouhodobé přežívání [1] a přispívat ke zvýšení relativní četnosti výskytu recidiv [2], i když nutno pro objektivitu dodat, že v problematice onkologických důsledků chirurgických komplikací [3] a anastomotického leaku není literatura jednotná [4,5].
Je všeobecně známo, že hojení kolorektální anastomózy ovlivňuje v různém rozsahu celá řada faktorů. Tyto faktory a z nich vyplývající potenciální rizika poruchy hojení anastomózy [6,7] jsou chirurgem ovlivnitelné v různé míře. První skupinu potenciálních rizik bezpečného hojení anastomózy představuje pacient samotný, konkrétně zejména jeho věk, pohlaví, body mass index, nutriční stav, doprovodná onemocnění, medikace, kouření. Ve svém souhrnu se obecně jedná o rizikové faktory, které lze před operací ovlivnit jen minimálně. Výjimkou je stav výživy pacienta, kde předoperační zhodnocení nutrice a případná nutriční intervence mohou hojení kolorektální anastomózy pozitivně ovlivnit. Druhá skupina rizik je vázána na samotné onemocnění, které je obvykle indikací k operačnímu výkonu, to znamená hlavně grading a staging u maligních nádorů a rozsah postižení u benigních onemocnění. Rovněž tyto parametry lze předoperačně ovlivnit jen velmi málo. Třetí skupina rizikových faktorů je spojena s chirurgickým výkonem a zahrnuje operační techniku a perioperační péči [8]. Zde je možnost ovlivnit optimální hojení kolorektální anastomózy pro chirurga největší. Následující text přehledného sdělení bude zaměřen na jeden konkrétní bod operačního postupu, kterým je peroperační hodnocení integrity a kvality kolorektální anastomózy. Autor sdělení se věnoval této problematice v průběhu svého pobytu v USA (prof. R. Bergamaschi) zejména se zaměřením na vyšetření mikrocirkulace v oblasti anastomózy.
Metody
Subjektivní a objektivní hodnocení kvality kolorektální anastomózy
Peroperačně je určení vitální proximální resekční linie a hodnocení kvality následně vytvořené kolorektální anastomózy obvykle výsledkem kritického posouzení operujícím chirurgem. Jedná se tedy z pohledu EBM (evidence based medicine) o hodnocení čistě subjektivní, a tedy špatně měřitelné. Holandská studie publikovaná Karliczkem a kol. v roce 2009 zaměřená na problematiku spolehlivosti subjektivního hodnocení „kvality“ anastomózy operujícím chirurgem dospěla k závěru, že toto ohodnocení má velmi limitovanou prediktivní hodnotu a autoři doporučují objektivnější a spolehlivější testy [9]. Podobně vyznívají i další recentní práce [10,11].
Aktuálně existuje celá řada objektivnějších nástrojů a více či méně propracovaných technik k posouzení integrity a kvality kolorektální anastomózy. Jejich základním cílem je snížení četnosti pooperačních komplikací snížením rizika anastomotického leaku. Obecně lze tyto postupy rozdělit do tří skupin. V první skupině jsou techniky „mechanického“ posouzení integrity kolorektální anastomózy. Druhou skupinou jsou endoskopické postupy a ve třetí skupině je celá řada modernějších technik a postupů zaměřených na vyšetření cirkulace nebo mikrocirkulace (mikroperfuze) v anastomóze a v perianastomotické tkáni. Objektivní údaje o klinické efektivitě těchto postupů však v literatuře skoro chybějí.
Mechanické posouzení integrity kolorektální anastomózy
Mechanické posouzení integrity kolorektální anastomózy je nejběžněji používaným postupem. Provádí se obvykle transrektální aplikací vzduchu (air leak test, Jacuzzi) nebo transrektálním podáním tekutiny, např. metylenové modře při kompresi střeva orálně od anastomózy. Tyto postupy se používají dlouhodobě zhruba od roku 1980. Mechanický test integrity kolorektální anastomózy je jednoduchou časově nenáročnou zkouškou, určitou limitací však může být skutečnost, že hodnotí externím pohledem přítomnost/nepřítomnost leaku kolorektální anastomózy bez vizualizace střevního lumen. Pokud se jedná o spolehlivost a efektivitu těchto postupů, systematický přehled publikovaný v roce 2014 Nachiappanem a kol. [12], vycházející z analýzy 13 publikací včetně dvou randomizovaných studií [13,14], dospěl k závěru, že pooperační komplikace kolorektální anastomózy byly signifikantně nižší ve skupině, kde anastomóza byla peroperačně mechanicky testována ve srovnání s anastomózami, které testovány nebyly [12].
Endoskopické techniky
Tyto postupy dokládají, že endoskopická instrumentária se stala na řadě míst pevnou součástí operačních sálů. Potenciální výhodou je možnost přímé vizualizace mukózy střeva, která je na ischemii daleko citlivější než střevní seróza. Kromě vizuální kontroly kompletnosti anastomotického prstence endoskopické techniky rovněž poskytují možnost diagnostiky a eventuální intervence při viditelném krvácení v oblasti kolorektální anastomózy.
Efektivita endoskopických technik z pohledu EBM je nicméně limitovaná. V již dříve uvedeném systematickém přehledu Nachiappana a kol. nebyly prokázány signifikantní rozdíly ve výskytu anastomotických komplikací mezi endoskopicky testovanými a netestovanými anastomózami [12]. Nutno ale dodat, že tento závěr je postaven na poměrně malé skupině publikací se značně nehomogenními soubory a odlišným designem studie bez randomizace. Navíc peroperační opatření provedená jako důsledek „abnormálního“ endoskopického nálezu potenciální redukcí anastomotického leaku zkreslily objektivní porovnání výsledků. Endoskopické techniky lze jednoduše doplnit standardní mechanickou zkouškou (air leak test), což se prakticky obvykle provádí.
Techniky hodnotící (mikro)cirkulaci/perfuzi
Adekvátní prokrvení je klíčovým předpokladem nekomplikovaného zhojení anastomózy. Operující chirurg peroperačně hodnotí jednak vitalitu střeva v souvislosti se stanovením resekční linie a následně vitalitu nově vytvořené kolorektální anastomózy. Posuzuje obvykle krevní tok (viditelná nebo hmatná pulzace, krvácení z resekčních okrajů) a perfuzi tkání (barva). Tato hodnocení jsou částečně závislá i na operační technice (laparoskopický přístup, otevřená operace), a jak už bylo dříve uvedeno, posouzení je značně subjektivní a s limitovanou spolehlivostí [9]. Současná chirurgie z tohoto důvodu zaznamenala nástup celé řady moderních technik a technologií zaměřených na hodnocení cirkulace/perfuze anastomózy a prokrvení perianastomotických tkání s cílem minimalizovat riziko pooperačních komplikací [10,11]. V klinické praxi byly použity:
- transabdominální doplerovská sonografie,
- transabdominální laserová doplerovská flowmetrie,
- skenující laserová doplerovská flowmetrie,
- měření tkáňové kyslíkové saturace/tkáňového tlaku kyslíku,
- O2 spektroskopie ve viditelném spektru,
- O2 spektroskopie ve spektru blízkém infračervenému záření (NIR – near infrared) ,
- peroperační koloskopie s použitím NBI zobrazení (NBI – Narrow Band Imaging – zobrazení v úzkém svazku),
- laserová fluorescentní angiografie s použitím indocyaninové zeleně (ICG),
- fluorescentní angiografie ve spektru blízkém infračervenému záření s použitím indocyaninové zeleně (ICG),
- pH-metrie mukózy kolon.
Aktuálně se jako nejperspektivnější jeví postupy založené na fluorescenci ve spektru blízkém infračervenému záření (near infrared – NIR) s využitím indocyaninové zeleně (ICG). Ostatní techniky jsou vesměs poměrně komplikované, náročné na vybavení a s obtížnou reprodukcí výsledků.
NIR fluorescence znamená zjednodušeně schopnost fluorescentního barviva (indocyaninová zeleň) absorbovat světlo určité vlnové délky (NIR, laser) a následně záření v jiné vlnové délce emitovat (fluoreskovat). Z hlediska operační techniky je výhodou laparoskopický přístup, protože zdroj světla konkrétní vlnové délky může být součástí laparoskopické věže (Olympus, Carl Storz, Stryker), nicméně systém může být i samostatným zařízením (Novadaq). Emitované záření je pro lidské oko v neviditelné části spektra, ale pomocí speciálního filtru jako součásti kamery může být obraz chirurgovi zprostředkován. Intravenózně podaná ICG se váže na plazmatické proteiny a minimálně uniká do intersticia. Zhruba za jednu minutu poskytne obraz prokrvení (Obr. 1) a tento obraz vydrží 2−3 minuty. Po 8−15 minutách se ICG kompletně vyloučí játry [15]. V medicíně byla proto používána také k hodnocení funkční rezervy jater.
Image 1. NIR fluorescentní angiografie Fig. 1: NIR fluorescent angiography 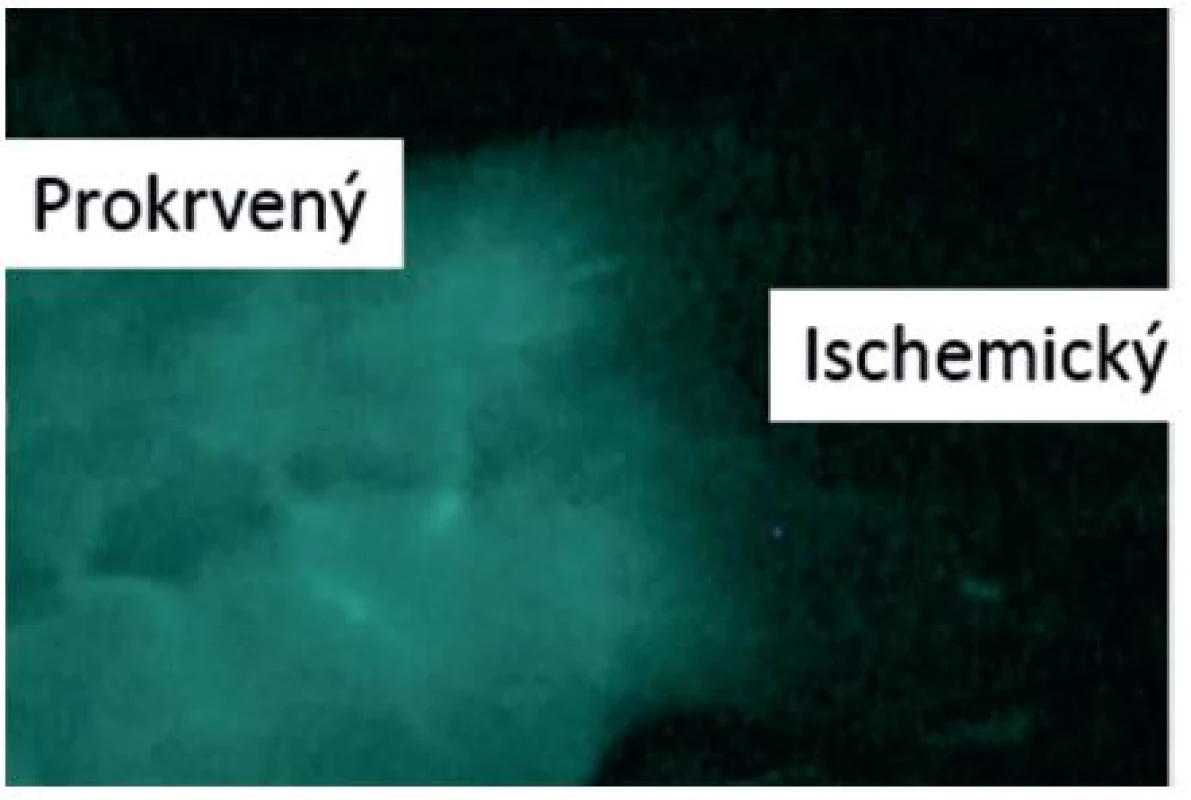
Výhodou tohoto vyšetření je jeho jednoduchost a rychlost, obraz je jako „real-time“ získán v několika minutách. V multicentrické studii PILLAR II bylo hodnotitelné prokrvení kolorektální anastomózy získáno v 97,6 % případů [16]. Porucha mikrocirkulace je navíc viditelná bezprostředně jako výpadek „kontrastu“, kdežto ischemické změny jsou na monitoru viditelné prostým okem až po minutách. Další výhodou je možnost hodnocení prokrvení proximální resekční linie i prokrvení dokončené anastomózy. Nitrožilní podání ICG lze i opakovat. Problémem může být přece jenom subjektivní hodnocení obrazu (dostatečnost prokrvení) a zobrazení hůře přístupných míst (zadní obvod anastomózy) či zobrazení oblasti anastomózy překryté jinou, nejčastěji tukovou tkání. Alergie na ICG byla popsána vzácně a vedlejší účinky podání ICG jsou raritní. Potenciální nevýhody subjektivního hodnocení angiografie se snaží minimalizovat PINPOINT® Endoscopic Fluorescence Imaging system (Novadaq Technologies Inc., Ontario, Canada), který černobílý obraz fluorescentní angiografie superponuje (augmented reality) do standardního peroperačního pohledu chirurga (Obr. 2) a umožňuje i číselné vyjádření prokrvení ve zvolené oblasti.
Image 2. Obraz NIR fluorescentní angiografie a superponovaný obraz v normálním světle Fig. 2: NIR perfusion assessment and superposition of NIR and normal light 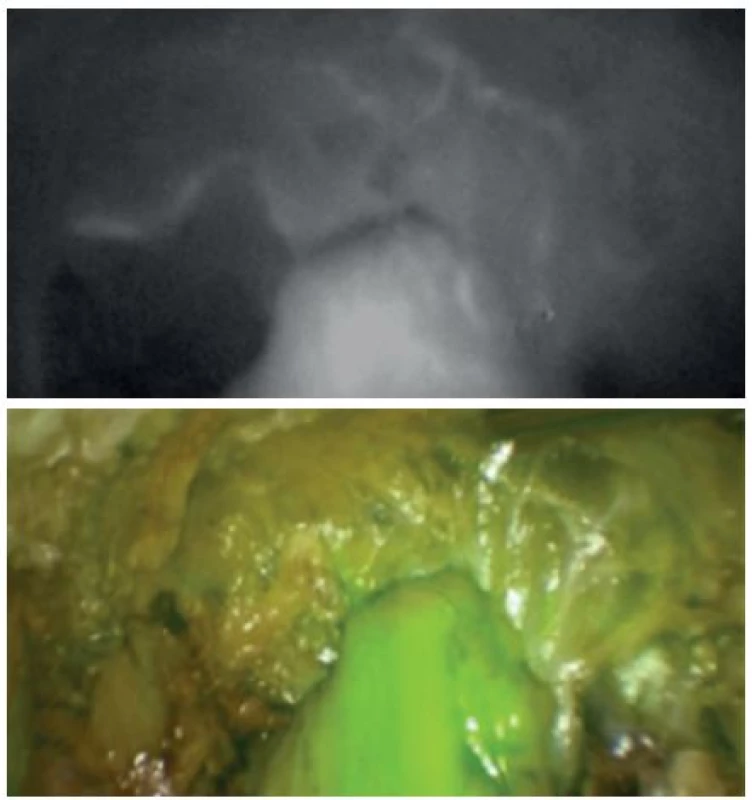
Limitace intraabdominálního zobrazení anastomózy (hůře přehledný zadní obvod, překrytí okolními tkáněmi) pak odstraňuje endoskopický pohled na kolorektální anastomózu a její prokrvení (Obr. 3).
Image 3. Transanální obraz kolorektální anastomózy (bílá šipka) Fig. 3: Transanal image of colorectal anastomosis (white arrow) 
Tato perspektivní technika už byla ověřena pilotními studiemi [10,14] na menších souborech a aktuálně jsou organizovány multicentrické, randomizované studie. Jednou z prvních multicentrických studií, která již prezentovala své výsledky, byla již dříve citovaná studie PILLAR II zahrnující 147 pacientů s kolorektální anastomózou z 11 center v USA. Do souboru byli zařazeni pacienti s laparoskopickou nebo robotem asistovanou resekcí. Autoři udávají, že v 8 % peroperační fluorescentní angiografie vedla ke změně operačního postupu, anastomotický leak byl 1,4 % a v hodnoceném souboru došlo ke snížení počtu protektivních stomií [16]. Za změnu operačního postupu je obvykle považována reresekce proximálního kolon v bezpečně prokrvené tkání nebo resekce již dokončené kolorektální anastomózy s vytvořením anastomózy nové. S možností sledování hojení anastomózy v časném pooperačním období nejsou zatím zkušenosti vzhledem ke krátké době používání této metodiky.
Pilotní zkušenosti autora z pracoviště v USA (Division of Colon and Rectal Surgery, University of New York, Stony Brook) potvrdily bezpečnost a efektivitu tohoto postupu. Malá skupina pacientů peroperačně vyšetřena systémem PINPOINT® bez protektivní ileostomie měla nekomplikovaný pooperační průběh bez poruchy hojení kolorektální anastomózy. Mechanické posouzení integrity anastomózy (air leak test) prováděné na mateřském pracovišti autora (FN Ostrava) bylo spojeno s poruchou hojení kolorektální anastomózy v 5 % u otevřených výkonů a ve 4 % u laparoskopických resekcí rekta. Možnost zásadní redukce počtu protektivních ileostomií je určitě výzvou do budoucna. Výsledky v současnosti probíhajících studií by v krátké době mohly slibné závěry pilotních studií potvrdit.
Závěr
Peroperační kontrola integrity kolorektální anastomózy by měla být standardní součástí operačního postupu. Je prokázáno, že mechanická kontrola vede ke snížení počtu pooperačních komplikací anastomózy. V případě endoskopické verifikace kolorektální anastomózy je vhodné doplnit i kontrolu mechanickou. Moderní postupy založené na hodnocení prokrvení cestou NIR fluorescence představují slibnou modalitu a mají potenciál nejen snížit rizika komplikací hojení anastomózy, ale mohou zároveň redukovat i počty protektivních ileostomií. Důkaz této skutečnosti by umožnil obhájit v současnosti poměrně vysoké náklady spojené s pořízením této technologie.
Seznam zkratek
EBM – Evidence Base Medicine (medicína založená na důkazech)
ICG – Indocyanin Green (indocyaninová zeleň)
NBI – Narrow Band Imaging (zobrazení v úzkém spektru)
NIR – Near Infrared (spektrum blízké infračervenému záření)
Konflikt zájmů
Autoři článku prohlašují, že nejsou v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise.
MUDr. Lubomír Martínek, Ph.D.
Odboje 1164
739 32 Vratimov
e-mail: lubomir.martinek@fnmotol.cz
Sources
1. Den Dulk M, Marijnen CAM, Collette L, et al. Multicentre analysis of oncological and survival outcomes following anastomotic leakage after rectal cancer surgery. Br J Surg 2009;96 : 1066–75.
2. Mirnezami A, Mirnezami R, Chandrakumaran K, et al. Increased local recurrence and reduced survival from colorectal cancer following anastomotic leak: systematic review and meta-analysis. Ann Surg 2011;253 : 890–9.
3. Liška V, Třeška V, Holubec L, et al. Prognostic factors of early recurrence of colorectal liver metastases and their usage in clinical praxis. Rozhl Chir. 2006;85 : 86−9.
4. Espín E, Ciga MA, Pera M, et al. The Spanish Rectal Cancer Project. Oncological outcome following anastomotic leak in rectal surgery. Br J Surg. 2015;102 : 416−22.
5. Martínek L, Zonča P, Ihnát P. Overall survival: is it an objective endpoint for assessing the quality of surgical treatment for colorectal cancer? Rozhl Chir 2013;92 : 690−3.
6. Park JS, Choi GS, Kim SH, et al. Multicenter analysis of risk factors for anastomotic leak-age after laparoscopic rectal cancer excision: the Korean laparoscopic colorectal surgery study group. Ann Surg 2013;257 : 665–71.
7. Kang CY, Halabi WJ, Chaudhry OO, et al. Risk factors for anastomotic leakage after anterior resection for rectal cancer. JAMA Surg 2013;148 : 65–71.
8. Kocián P, Neumann J, Majtan P, et al. Fluid therapy and surgical outcomes after low anterior resection. Rozhl Chir 2014;93 : 463−7.
9. Karliczek A, Harlaar NJ, Zeebregts CJ, et al. Surgeons lack predictive accuracy for anastomotic leakage in gastrointestinal surgery. Int J Colorectal Dis 2009;4 : 569–76.
10. Kudszus S, Roesel C, Schachtrupp A, et la. Intraoperative laser fluorescence angiography in colorectal surgery: a noninvasive analysis to reduce the rate of anastomotic leakage. Langenbeck’s Arch Surg 2010;395 : 1025−30.
11. Jafari MD, Lee KH, Halabi WJ, et al. The use of indocyanine green fluorescence to assess anastomotic perfusion during robotic assisted laparoscopic rectal surgery. Surgical Endosc 2013;27 : 3003–8.
12. Nachiappan S, Askari A, Currie A, et al. Intraoperative assessment of colorectal anastomotic integrity: a systematic review. Surg Endosc 2014;28 : 2513–30.
13. Beard JD, Nicholson ML, Sayers RD, et al. Intraoperative air testing of colorectal anastomoses: a prospective, randomized trial. Br J Surg 1990;77 : 1095–107.
14. Ivanov D, Cvijanovic R, Gvozdenovic L. Intraoperative air testing of colorectal anastomoses. Srp Arh Celok Lek 2011;139 : 333–8.
15. Cahill RA, Ris F, Mortensen NJ. Near-infrared laparoscopy for real-time intra-operative arterial and lymphatic perfusion imaging. Colorectal Dis. 2011;13 Suppl 7 : 12−7.
16. Jafari MD, Wexner SD, Martz JE, et al. Perfusion assessment in laparoscopic left-sided/anterior resection (PILLAR II): a multi-institutional study. J Am Coll Surg 2015;220 : 82−92.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2015 Issue 5-
All articles in this issue
- Peroperační verifikace integrity kolorektální anastomózy
- Léčba gastrointestinálních stromálních tumorů – komplexní pohled chirurga
- Metastázy do pankreatu − diagnostika a možnosti radikální léčby, komplikace, přežívání
- Perspektiva pacientů operovaných pro sekundární peritonitidu
- Střevní volvulus způsobený požitím magnetických kuliček: neočekávané riziko u dětí
- Femoropopliteální žilní trombóza a pseudoaneuryzma popliteální tepny jako komplikace mnohočetné hereditární osteochondromatózy
- Endometrióza apendixu s projevy akutní apendicitidy – kazuistika
- Using the new hemostatic gelatin GELITA-SPON RAPID3 to treat parenchymatous organs – a clinical observation
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Metastázy do pankreatu − diagnostika a možnosti radikální léčby, komplikace, přežívání
- Endometrióza apendixu s projevy akutní apendicitidy – kazuistika
- Střevní volvulus způsobený požitím magnetických kuliček: neočekávané riziko u dětí
- Femoropopliteální žilní trombóza a pseudoaneuryzma popliteální tepny jako komplikace mnohočetné hereditární osteochondromatózy
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

