-
Medical journals
- Career
Obskurní krvácení do zažívacího traktu
Authors: J. Pastor; S. Adámek
Authors‘ workplace: 3. chirurgická klinika 1. LF UK a FN Motol, přednosta: Prof. MUDr. R. Lischke, PhD.
Published in: Rozhl. Chir., 2013, roč. 92, č. 8, s. 424-428.
Category: Review
Overview
Obskurní krvácení do trávicího traktu představuje 5 % všech krvácení do GITu. Jde o krvácení, jehož příčina nebyla zjištěna gastroskopií a kolonoskopií – nejčastější příčinou je krvácení ze zdroje v tenkém střevě. Případně jde o krvácení z jiných částí trávicí trubice, které v době vstupní endoskopie již ustalo nebo bylo přehlédnuto. V diagnostice i léčbě se uplatňují metody zobrazovací (RTG, CT, MRI, scintigrafie) a endoskopické (enteroskopie flexibilní nebo kapslová). Není-li ani s využitím těchto metod zdroj nalezen a krvácení pokračuje anebo i při známém zdroji selže pokus o jeho zástavu radiologickou či endoskopickou intervencí, pak bývá indikováno operační řešení. Článek přináší přehled současných diagnostických a léčebných možností včetně návodu, jak v případě těchto diagnosticky obtížných situací postupovat.
Klíčová slova:
krvácení do GITu – enteroskopie – angiografieÚvod
Přednostní diagnostickou metodou při krvácení do zažívacího traktu je endoskopie. Široce dostupné gastroskopie a kolonoskopie jsou využívány jak v případech krvácení zjevného (klinicky se projevujícího hematemézou, melenou nebo enteroragií), tak okultního (mikrocytární anemie, pozitivní test na okultní krvácení ve stolici (TOKS). V některých případech se ale těmito endoskopickými metodami zdroj krvácení nalézt nepodaří – v tom případě stojíme před skupinou krvácení do zažívacího traktu, která je v zahraniční literatuře označována jako „obscure gastrointestinal bleeding“ (OGIB). Vhodný český překlad pro tato krvácení nemáme, jsou-li v naší literatuře zmiňována, pak jako „obskurní krvácení do GITu“.
Jako obskurní krvácení do GITu tedy označujeme skupinu krvácení do zažívacího traktu, jehož příčina nebyla zjištěna konvenční endoskopií (tj. gastroskopií a kolonoskopií) [1]. Přímo z této definice pak vyplývá, že se většinou jedná o krvácení ze zdroje v oblasti těmto vyšetřením nedostupné – tedy v jejunoileu. Menšinou je zdroj v jiné lokalizaci, a to v případě, že krvácení v době vstupní endoskopie již ustalo anebo při ní bylo přehlédnuto. Možné příčiny OGIB shrnuje Tab. 1 [2].
Table 1. Přehled příčin OGIB Tab. 1: Overview of OGIB causes 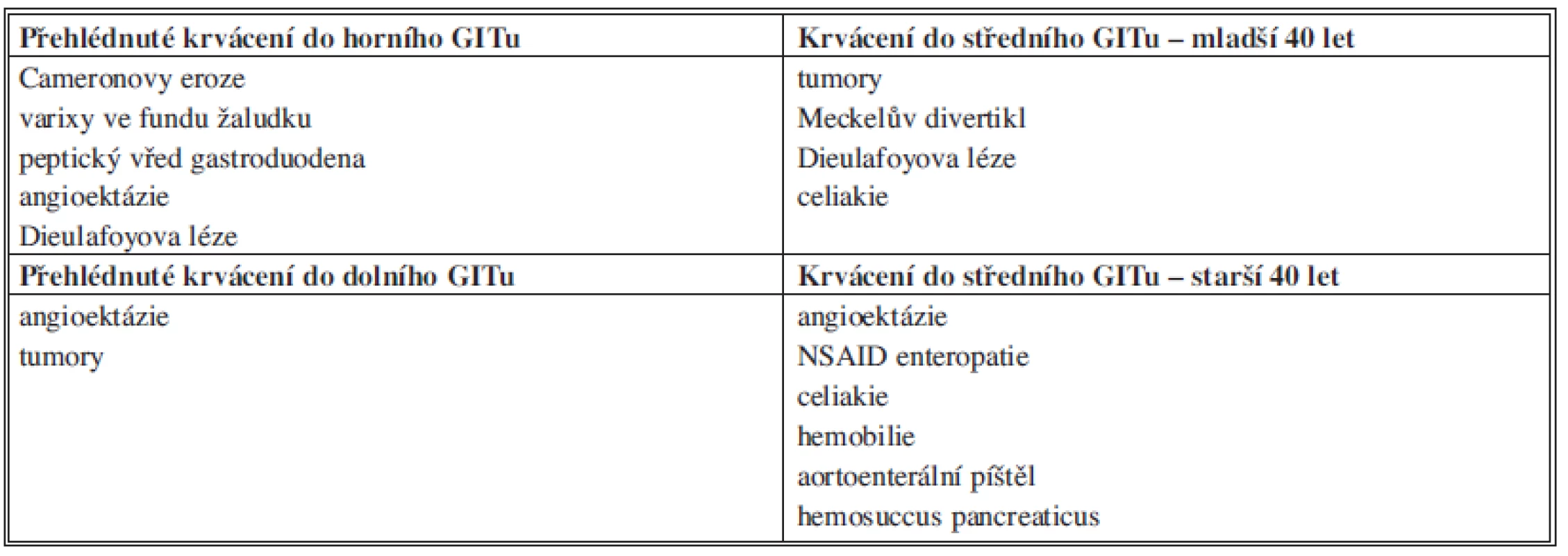
Četnost OGIB je udávána v 5 % všech krvácení do GITu [3].
Současné možnosti endoskopické diagnostiky opravňují poněkud modifikovat tradiční rozdělení krvácení do horního a dolního GITu s hranicí v oblasti Treitzova ligamenta. Gastroskopie a kolonoskopie snadno přehlédnou oblast jícnu, žaludku, duodena a tračníku, zatímco vyšetření zbylého úseku tenkého střeva je složitější. Proto někteří autoři prosazují rozdělení na krvácení do horního (do úrovně Treitzova ligamenta), středního (od Treitzova ligamenta po Bauhinskou chlopeň) a dolního GITu (od Bauhinské chlopně aborálně) [2,4].
Jak již bylo uvedeno, OGIB může mít podobu krvácení zjevného (hemateméza, melena, enteroragie) i skrytého (okultního – mikrocytární anemie, pozitivní TOKS) [5]. Nelze proto zaměňovat pojmy obskurního a okultního krvácení.
Diagnostika
Při zjišťování zdroje OGIB využíváme jednak zobrazovacích metod, jednak endoskopických vyšetření (přehled viz. Tab. 2). Nezřídka je nutné různá vyšetření kombinovat či opakovat.
Table 2. Přehled metod využívaných k diagnostice OGIB Tab. 2: Overview of the methods used in OGIB diagnosis 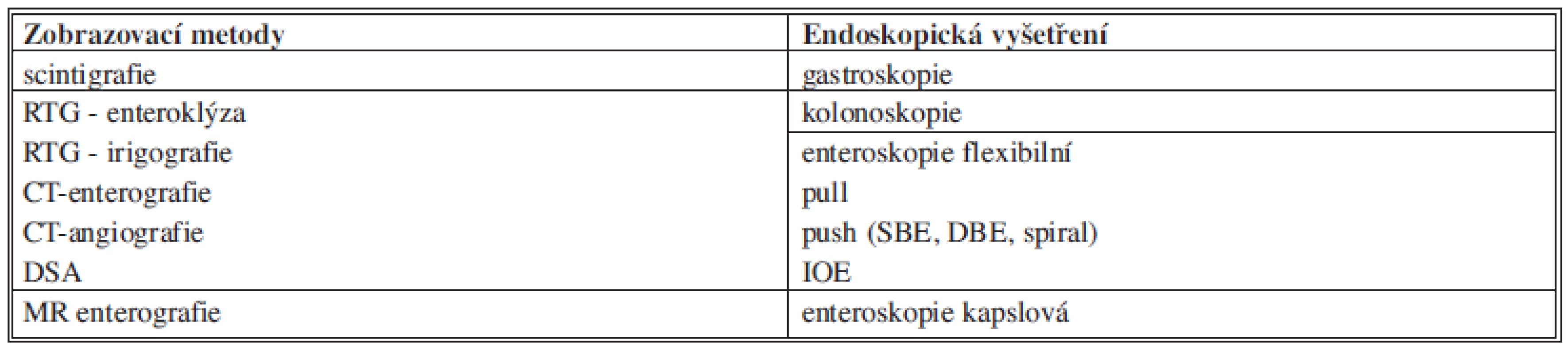
Zkratky: DSA - digitální subtrakční angiografie SBE - single baloon enteroscopy DBE - double baloon enteroscopy IOE - intraoperative enteroscopy CT - computed tomography MR - magnetic resonance Scintigrafie
Radionuklidový scan prokazuje krvácení únikem 99mTc značených erytrocytů do lumen střeva. Snímkuje se v určitých intervalech, může se tak zachytit i krvácení intermitentní. Udáván je záchyt krvácení 0,1–0,4 ml/min [1]. Má tedy vysokou senzitivitu, ale nízkou specificitu co do lokalizace zdroje krvácení. Své místo má v diagnostice nezávažných krvácení u oběhově stabilních pacientů.
Druhou možností využití scintigrafie je pertechnátový scan zjišťující přítomnost Meckelova divertiklu. 99mTc-pertechnát je selektivně vychytáván parietálními buňkami žaludeční sliznice a jeho kumulace mimo žaludek je známkou přítomnosti metaplastické žaludeční sliznice v divertiklu. Jde tudíž o nepřímý průkaz možného zdroje bez přímého záchytu krvácení. Krvácení z Meckelova divertiklu je nejčastější příčinou meleny u dětí a pertechnátový scan je v tomto případě doporučován jako diagnostická metoda první volby [6].
RTG zobrazovací metody
Skiagrafie (s podáním kontrastní látky per os, nazojejunální sondou či per rectum) je pro nízkou senzitivitu využívána velmi zřídka. Daleko větší možnosti skýtá CT. Výpočetní tomografie může jednak zobrazit zdroj krvácení (tumor či cévní léze ve střevní stěně), jednak zachytit aktivní krvácení s únikem kontrastu do lumen střeva.
Pro průkaz zdroje krvácení je jednoznačně preferována CT enterografie. Na rozdíl od klasického dvojkontrastního CT (i.v. kontrast + p.o. několik desítek ml pozitivní jodové kontrastní látky) se v případě enterografie podává velké množství neutrálního či negativního kontrastu (1300–2000 ml roztoku např. metylcelulózy), který naplní a distenduje kličky tenkého střeva a umožní tak detailní zhodnocení střevní stěny. Odhalí se tak nádorové, cévní a zánětlivé léze [2]. Zatímco při endoskopii se dobře hodnotí slizniční změny, CT má větší senzitivitu pro submukózní a hlubší procesy ve střevní stěně [7,8].
Pro průkaz aktivního krvácení – úniku kontrastní látky do lumen střeva – je vhodnější CT-angiografie.
Digitální subtrakční angiografie (DSA) představuje výhodnou miniinvazivní léčebnou metodu, umožňuje selektivně embolizovat krvácející cévu nebo lokálně aplikovat vazokonstrikční látku. Angiografie zachytí krvácení nad 0,5–1 ml/min, může detekovat i aktuálně nekrvácející zdroje, pokud mají zvýšenou vaskularizaci (cévní malformace, tumory). Současná doporučení uvádějí nejprve lokalizovat zdroj krvácení CT-angiografií a poté cíleně zavést katétr z třísla nebo axily a provést intervenci [9]. Není-li při angiografii (AG) zdroj krvácení patrný, pak lze využít i tzv. provokovanou AG – podáním vazodilatancií (nitroglycerin), antikoagulancií (heparin) nebo fibrinolytik (streptokináza) v průběhu vyšetření. AG je indikována v případě významnějších krvácení. Riziko infarktu střeva je udáváno v 7 %, pozdní ischemické striktury ve 14 % [10].
MRI
Variantou CT je MR-enterografie. Je vhodná u pacientů alergických na jodové kontrastní látky a ke snížení radiační zátěže u mladších pacientů, zvláště u nespecifických střevních zánětů (inflammatory bowel disease – IBD), kdy je předpoklad opakovaných vyšetření v průběhu nemoci. Všeobecně platí, že CT-enterografie lépe zobrazí tumory tenkého střeva, MRI zánětlivé změny u IBD.
Enteroskopie
Enteroskopie je vyšetření tenkého střeva, buď flexibilním tenkým enteroskopem, nebo spolknutou kapslí s kamerou. Zvláštním případem je endoskopické vyšetření střeva během operačního výkonu. Jednotlivé možnosti se liší svojí náročností (nutnost analgosedace), výtěžností a délkou přehlédnutého úseku tenkého střeva.
Možnosti enteroskopie:
- push,
- pull,
- deep (double-baloon enteroscopy (DBE), single-baloon enteroscopy (SBE), spiral),
- intraoperative,
- capsule.
Dnes již téměř opuštěnými metodami jsou pull - a push - enteroskopie. V prvním případě šlo o pasivní zaplavání tenkého enteroskopu peristaltikou do tenkého střeva. Vyšetření trvalo až 24 hod, nebyla možnost biopsie či koagulace. Ve druhém případě je aktivně zaveden enteroskop či dětský kolonoskop do tenkého střeva, maximální dosah vyšetření je uváděn 70–150 cm od Treitzova ligamenta, výtěžnost mezi 18–26 % [10].
Balonková enteroskopie (způsobem provedení označována také jako push-and-pull enteroscopy) využívá k pohybu enteroskopu střídavou insuflaci a desuflaci jednoho nebo dvou balonků, střevo je tak vlastně na enteroskop postupně navlékáno. Enteroskop může být zaveden antegrádně ústy nebo retrográdně konečníkem, popř. lze oba způsoby zkombinovat. Senzitivita je udávána 60–80 % [11]. Ve srovnávací studii byla větší výtěžnost DBE než SBE [12]. V průběhu enteroskopie je možné provést biopsii, koagulovat krvácející lézi, extrahovat cizí tělesa, provádět balonkové dilatace stenóz a tetováže. Možnými komplikacemi balonkové enteroskopie jsou postbioptické krvácení, perforace střeva a pankreatitida (tlakem balonku při průchodu duodenem).
Spirální enteroskopie nepoužívá k pohybu střevem balonků, ale spirály na povrchu enteroskopu. Má nižší riziko komplikací, ale také menší diagnostickou výtěžnost než DBE [11].
Provedení kapslové enteroskopie spočívá v polknutí kapsle s kamerou, která za svého průchodu trávicí trubicí snímá endoskopický obraz a přenáší jej do záznamového zařízení umístěného na těle pacienta. Kapsle má rozměry 26x11 mm, kamera snímá 2 snímky/sekundu, baterie vydrží 8 hod. V 80 % se za tuto dobu dostane až do tlustého střeva [13] a odejde per vias naturales. Má vysokou senzitivitu (až 80 %) srovnatelnou s DBE [4,14]. Nevýhodou je pouze pasivní pohyb peristaltikou a nemožnost léčebného zásahu, kapsle může uvíznout v místě zúžení střeva.
Jak flexibilní, tak kapslová enteroskopie nejsou vhodné při výraznějším krvácení, současná doporučení uvádějí jako první volbu kapslovou enteroskopii a při jejím pozitivním výsledku následuje DBE k cílené intervenci [4].
Intraoperační enteroskopie je endoskopické vyšetření během operace indikované buď pro akutní masivní krvácení, nebo k elektivní resekci léze neodstranitelné endoskopicky (např. tumor tenkého střeva). Ve druhém případě je samozřejmě vhodnější předoperační označení léze tetováží, byla-li diagnostikována endoskopicky. Zavedení endoskopu v průběhu operace je možné ústy, konečníkem nebo z enterotomie. Jako nejméně invazivní se doporučuje začít transorální enteroskopií, a pouze pokud nelze volně dosáhnout terminálního ilea tak pokračovat v enteroskopii z enterotomie [13]. Častými komplikacemi jsou poranění sliznice nebo serózy při nadměrné distenzi střeva, mezenterická ischemie a prolongovaný pooperační ileus [10].
Diagnosticko-léčebný algoritmus
Výše uvedený výčet diagnostických možností dokazuje, že v případě OGIB se jedná o složitou situaci, pro niž neexistuje jedna jediná univerzální a nejlepší diagnostická metoda. Jednotlivá vyšetření je třeba kombinovat a někdy i opakovat. Na jedné straně sice platí, že krvácení do GITu, jehož zdroj není zachycen gastroskopií ani kolonoskopií, se v naprosté většině případů zastaví spontánně, na druhé straně má však takovéto krvácení s nezjištěným zdrojem vysoké riziko recidivy.
Jsou uváděny různé diagnosticko-terapeutické algoritmy, přístup se zásadně se liší dle závažnosti krvácení.
V případě masivního krvácení je po vyloučení zdroje v horním a dolním GITu (vstupní gastroskopie a kolonoskopie po zkrácené přípravě – tzv. emergentní kolonoskopie [15]) indikována AG s cílem nalezení zdroje a zástavy krvácení embolizací. Pokud je AG negativní – nezobrazí zdroj krvácení nebo i v případě nalezení zdroje, kdy nelze krvácení zastavit endovaskulárně – je indikováno operační řešení. V jeho průběhu můžeme použít intraoperační endoskopii.
V případě krvácení nezávažného či okultního máme na výběr více možností. Doporučeno je zopakování gastroskopie nebo kolonoskopie k vyloučení přehlédnuté léze. Standardem v našich podmínkách je poté provedení kapslové enteroskopie a na základě nálezu event. cílená intervence flexibilním enteroskopem [4]. Alternativou je scintigrafie. Enterografie je metodou volby, pokud je kapslová enteroskopie negativní, nekompletní nebo nejednoznačná [6].
Indikací k operačnímu řešení jsou masivní krvácení z neznámého zdroje nebo ze zdroje známého, ale endoskopicky neošetřitelného, krvácení recidivující po endoskopickém ošetření a dále jde o elektivní výkony pro nálezy vyžadující střevní resekci (např. tumory tenkého střeva). Operační výkony jsou především resekční, lokální výkony (opich z enterotomie) nebývají uskutečnitelné vzhledem k obtížné lokalizaci zdroje krvácení a devaskularizace ohrožuje následnou ischemií s perforací nebo strikturou střeva. Je-li zdroj krvácení v tračníku, metodou volby je subtotální kolektomie [16]. Je vhodné vyhnout se resekcím naslepo pro vysokou rekurenci (30 %) a mortalitu s morbitidou (57 %) [10].
Další otázkou je, zda dovyšetřovat krvácení, které se zastavilo spontánně. Porovnáme-li možné příčiny, pak u mladších (do 40 let) bývají zdrojem především tumory tenkého střeva a zde je vhodné došetření (kapslová a/nebo balonková enteroskopie), u starších bývají hlavním zdrojem angiodysplazie a zde další vyšetřování není nutné, pokud nedochází k rekurenci krvácení.
Pro úplnost uveďme možnosti farmakologické léčby – její úspěšnost není vysoká a je rezervována pouze pro případy krvácení nezastavitelná jiným způsobem (endoskopicky, radiointervenčně a chirurgicky). Jde o hormonální preparáty (estrogeny, analoga somatostatinu), thalidomid, erytropoetin a von Willebrandův faktor [1].
Vlastní zkušenosti s diagnostikou a léčbou krvácení do GITu
Všichni pacienti se zjevným krvácením do GITu (hematemesa, melena) jsou v rámci FN Motol bez ohledu na předpokládaný zdroj a závažnost krvácení přijímáni na chirurgickou kliniku (3. chir. klinika 1. LF UK nebo Chirurgická klinika 2. LF UK). Ta zajišťuje ve spolupráci s gastroenterology a radiology diagnostiku a následně endoskopické či radiointervenční ošetření krvácení – prováděné příslušným specialistou za hospitalizace pacienta na chirurgické klinice. Pokud je takové ošetření úspěšné, nemocný je dále bez projevů krvácení (v indikovaných případech krvácení z horního GITu je s odstupem 24 hod provedena kontrolní gastroskopie), oběhově stabilní a nevyžaduje operační řešení, pak je po minimálně 24 hod observaci na chirurgické klinice přeložen na interní kliniku. Není-li možné krvácení výše uvedenými způsoby zastavit, je-li masivní nebo časně recidivující pak je řešíme operačně. Tento postup - v naprosté většině případů není chirurgická intervence nutná - je odůvodňován nedostatkem monitorovaných lůžek na interní klinice.
Z toho vyplývají vlastní zkušenosti – management pacientů s krvácením do GITu – zajištění diagnostických a intervenčních procesů, intenzivní péče o tyto pacienty, operační léčba krvácení do GITu (opichy krvácejících žaludečních vředů z gastrotomie, 2/3 resekce žaludku, střevní resekce, řešení krvácejících hemoroidů Barronovou ligaturou). Z krvácení spadajících do kategorie OGIB jde opět o diagnostiku ve spolupráci s gastroenterologem a radiologem (krvácení při IBD, angiodysplasie, polypy a tumory, opožděné pooperační krvácení např. po resekčních výkonech na pankreatu).
Podpořeno projektem (Ministerstva zdravotnictví ČR) koncepčního rozvoje výzkumné organizace 00064203 (FN MOTOL)
MUDr. Jan Pastor
Radčina 561
161 00 Praha
e-mail: jan.pastor@fnmotol.cz
Sources
1. Kochhar SG, Sanaka RM, Vargo JJ. Therapeutic management options for patients with obscure gastrointestinal bleeding. Ther Adv Gastroenterol 2012;5 : 71–81.
2. Gerson BL. Recurrent gastrointestinal bleeding after negative upper endoscopy and colonoscopy. Clinical Gastroenterology and hepatology 2009;7 : 828–833.
3. Rondonotti E, et al. The American society for gastrointestinal endoscopy diagnostic algorithm for obscure gastrointestinal bleeding: Eight burning questions from everyday clinical practice. Digestive and liver disease 2012; http://dx.doi.org/10.1016/j.dld. 2012.07.012
4. Heil U, Jung M. The patient with recidivent obscure gastrointestinal bleeding, Best practice and Research clinical gastroenterology. 2007;21 : 393–407.
5. American society for gastrointestinal endoscopy: Obscure gastrointestinal bleeding. Gatrointestinal endoscopy 2005;58 : 650–653.
6. USMLE step 2 – Lecture notes surgery, Ed. 2005–2006.
7. Bresci G. Occult and obscure gastrointestinal bleeding: Causes and diagnostic approach in 2009. World journal of gastrointestinal endoscopy 2009;1 : 3–6.
8. Fried AM, Poulos A, Hatfield DR. The effectiveness of the incidental small bowel series. Radiology 1981;140 : 45–46.
9. Ettore CC, Francioso G, Garribba AP, et al. Helical CT angiography in gastrointestinal bleeding of obscure origin. American journal of roentgenology 1997;168 : 727–731.
10. 1Speake D, Hill J. Obscure bleeding in the gastrointestinal tract. Surgery 2005;23 : 380–382.
11. Voelkel PJ, DiPalma AJ. Deep enteroscopy. South Med J 2010;103 : 1045–1048.
12. May A, Farber M, Aschmoneit I, et al. Prospective multicenter trial comparing push-and-pull enteroscopy with the single - and double-baloon techniques in patients with small-bowel disorders, American journal of gastroenterology 2010;105 : 575–581.
13. Bonnet S, Douard R, Malamut G, Cellier Ch, Wind P. Intraoperative enteroscopy in the management of obscure gastrointestinal bleeding, Digestive and liver disease 2012 http://dx. doi.org/10. 1016/j.did.2012.07.003
14. Pasha SF, Leighton JA, Das A, et al. Double-baloon enteroscopy and capsule endoscopy have coparable diagnostic yield in small-bowel disease: a metaanalysis, Clinical gastroenterology and hepatology 2008;6 : 671–676.
15. Dítě P, et al. Akutní stavy v gastroenterologii, Praha, Galen 2005.
16. Schein M, Rogers NP. Urgentní břišní chirurgie, Praha, Grada 2011.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2013 Issue 8-
All articles in this issue
- Intramurálna disekcia pažeráka
- Informovaný souhlas
- Právo na ochranu soukromí
- Lege artis
- Práce pod odborným dohledem
- Obskurní krvácení do zažívacího traktu
- Změny chirurgické techniky při řešení Pectus excavatum v letech 1991–2012
- Jak jsou dodržovány postupy moderní perioperační péče (Enhanced Recovery After Surgery) na chirurgických pracovištích v ČR – výsledky národní ankety
- Pozdní selhání endovaskulárního řešení aneuryzmatu subrenální aorty – diagnostika a léčba
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Práce pod odborným dohledem
- Jak jsou dodržovány postupy moderní perioperační péče (Enhanced Recovery After Surgery) na chirurgických pracovištích v ČR – výsledky národní ankety
- Informovaný souhlas
- Lege artis
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

