-
Medical journals
- Career
Roboticky asistované cévní rekonstrukce aorto-ilické oblasti
Authors: M. Dvořák; T. Novotný; R. Staffa
Authors‘ workplace: Centrum robotické chirurgie FN u sv. Anny v Brně ; II. chirurgická klinika LF MU a FN u sv. Anny v Brně, přednosta: prof. MUDr. Robert Staffa, Ph. D.
Published in: Rozhl. Chir., 2011, roč. 90, č. 1, s. 42-45.
Category: Monothematic special - Original
Overview
Cíl:
Cílem naší studie bylo vyhodnotit soubor 45 pacientů s roboticky asistovanou tepennou rekonstrukcí v aorto-ilicko-femorální oblasti.Materiál a metoda:
Robotický cévní výkon v aorto-ilicko-femorální oblasti využívá kombinaci 3 přístupů – konvenční při preparaci tepen v tříslech a našívání distálních anastomóz, laparoskopický pro preparaci břišní aorty a robotický pro našití proximální anastomózy. V období květen 2006–květen 2010 jsme provedli 45 roboticky asistovaných cévních rekonstrukcí (37 mužů, 8 žen, průměrný věk 57 let). Metodu jsme hodnotili na podkladě analýzy peroperačních a pooperačních dat.Výsledky:
Implantovali jsme 21 aorto-bifemorálních bypassů, 22 aorto-femorálních a 2 ilicko-femorální bypassy. Čas našití proximální anastomózy – medián 23 min (rozmezí 18–50 min), čas svorek – medián 60 min (rozmezí 40–95 min). Celkový operační čas – medián 295 min (rozmezí 180–475 min). Krevní ztráty – medián 265 ml (rozmezí 50–1200 ml). Doba pobytu na JIP po výkonu – medián 2 dny (rozmezí 1–8 dny). V průběhu sledování (medián 19 měsíců; rozmezí 2–50 měsíců) byly zaznamenány 3 (6,7 %) časné uzávěry rekonstrukce, všechny pro insuficientní výtok – vyřešeny prodloužením rekonstrukce. Nebyly pozorovány kardiální, pulmonální či renální komplikace, žádný pacient nezemřel. Pozdní komplikace: 1x kýla v portu (2,2 %). Sekundární průchodnost rekonstrukcí 100 %.Závěr:
Robotický systém da Vinci umožňuje velmi přesné našití cévní anastomózy a minimalizaci krevních ztrát. Dosažené výsledky (čas svorky, čas anastomózy) jsou srovnatelné s konvenční cévní chirurgií. Robotický systém odstraňuje technické limitace laparoskopické aortální anastomózy. Roboticky asistované aorto-ilicko-femorální bypassy se jeví jako bezpečná metoda s nízkým výskytem komplikací.Klíčová slova:
robotický systém da Vinci – laparoskopie – roboticky asistovaný aortofemorální bypassÚVOD
Rok 1993 se stává přelomovým rokem v cévní chirurgii. Dion v Kanadě provedl první laparoskopicky asistovaný aortofemorální bypass [1]. Laparoskopická chirurgie ale nedosáhla v cévní chirurgii takového rozšíření jako v jiných chirurgických oborech. Příčinou byl několikanásobně delší čas šití anastomózy a delší clamping time aorty.
Novým impulzem pro rozvoj miniinvazivních cévních operací se stala robotika. Je to nová technologie, která s narůstající zkušeností chirurga s tímto systémem přináší nové výhody v rámci miniinvazivních výkonů. Nevyžaduje přímý kontakt chirurga s pacientem, zvyšuje preciznost výkonu eliminací třesu rukou, poskytuje třídimenzionální obraz operačního pole, odstraňuje limitace laparoskopické chirurgie usnadněním většího rozsahu pohybu robotického instrumentaria [2]. Robotický systém da Vinci (Intuitive Surgical Inc., Sunnyvale, CA, USA) tak našel uplatnění v řadě chirurgických oborů. Je tedy dnes využíván např. v urologii, v kardiochirurgii, gynekologii, hrudní a také cévní chirurgii [3].
MATERIÁL A METODA
Od května 2006 do května 2010 jsme provedli na našem pracovišti (Obr. 1) v rámci robotického centra FN u sv. Anny v Brně, celkem 45 roboticky asistovaných cévních rekonstrukcí v aorto-ilicko-femorální oblasti. Celkový počet pacientů zahrnoval 37 mužů a 8 žen. Průměrný věk pacientů byl 57 let.
Image 1. Robotický systém da Vinci 1200 Fig. 1. The Robotic System da Vinci 1200 
Indikace k roboticky asistované cévní rekonstrukci jsou shodné s indikacemi otevřené chirurgie aterosklerotického obliterujícího onemocnění aorto-ilické oblasti [4]. Indikační schéma se začíná stále více rozšiřovat také o elektivní aneuryzma abdominální aorty (Obr. 2). Tento typ roboticky asistovaného cévního výkonu ale předpokládá již značnou laparoskopickou a robotickou zkušenost.
Image 2. Předoperační CTAG abdominální aorty a pánevních cév Fig. 2. Preoperative CTAG of abdominal aorta and iliac arteries 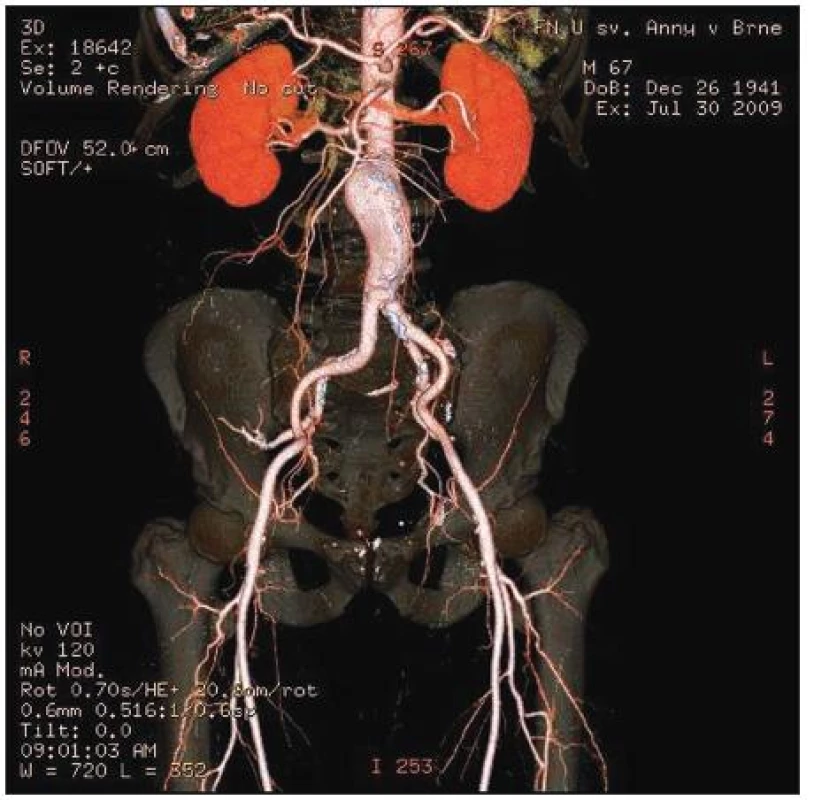
Kontraindikace jsou dány kardio-pulmonálními limity pacienta (pro instilaci kapnoperitonea či z důvodu delšího operačního času souvisejícího s learning curve), dále ruptura aneuryzmatu abdominální aorty, zánětlivé aneuryzma a také výrazné aterosklerotické postižení subrenálního segmentu aorty – porcelánová aorta. Mezi relativně kontraindikované patří pacienti po předchozích břišních operačních výkonech.
Operováni byli pacienti s různými komorbiditami podle klasifikace – American Society of Anaesthesiology (ASA I-III), pacienti s vážnými zdravotními onemocněními (ASA IV-V) nebyli do robotického programu zařazeni (Graf 1). Současně podle obecných zvyklostí, pacienti skupiny TASC A a B (TransAtlantic Inter-Society Consensus) byli léčeni endovaskulárními přístupy, pacienti skupiny TASC C a D pak byli indikováni k roboticky asistovanému cévnímu rekonstrukčnímu výkonu [5, 6].
Graph 1. Komorbidity souboru 45 pacientů u roboticky asistovaných tepenných rekonstrukcí aorto-ilicko-femorální oblasti Graph 1. Commorbidities of 45 patients robotic–assisted vascular reconstructions of aorto-iliac-femoral region 
Operační postup začíná úvodem do standardní anestezie, přípravou pacienta – kanylace, kontinuální monitoring, zahřívání pacienta, aplikace ohřívaných infuzních roztoků. Operace provádíme kombinovaným přístupem za použití laparoskopie a robotického systému da Vinci s použitím 30° operační optiky. Pacient leží na operačním stole na pravém boku v úhlu 45° s levou horní končetinou podél těla (Obr. 3). Operační konzola s přístrojovou věží robotického systému je umístěna na pravé straně pacienta. Výkon začínáme preparací femorálních tepen v jednom či obou tříslech, následuje zavedení kapnoperitonea – insuflace CO2 (nitrobřišní tlak 12 mm Hg) a dále rozmístění pěti 12mm pracovních trokarů standardním postupem. Podle potřeby zavádíme další 5 - či 12mm pomocné trokary (např. pro oplach aorty fyziologickým roztokem, odsávání, pomocné retraktory u obézního pacienta). Laparoskopickou část preparace provádíme pomocí harmonického skalpelu (Ethicon Endo-Surgery, Cincinnati, USA), pro přístup k aortě používáme modifikovaný transperitoneální přímý přístup. Aortu preparujeme od levé renální žíly až po bifurkaci aorty. Následuje zavedení umělé cévní protézy uni či bilaterální (Ra bv K nebo Ra 1v K, Výzkumný ústav pletařský, a.s., Brno, Česká republika) s předem připraveným zkráceným stehem Gore-Tex CV-3 (W. L. Gore & Associates, Flagstaff, AZ, USA) do břišní dutiny. Instalujeme robotický systém da Vinci a aplikujeme heparin (100 UI/kg). Po uplynutí dvou minut od podání heparinu naložíme endoskopické cévní svorky umístěné ve středních portech (proximální subrenálně, distální nad bifurkaci aorty), dočasně klipujeme i arteria mesenterica inferior a provedeme podélnou aortotomii. Při operaci standardně používáme jen tři robotická ramena (kamera a dva pracovní nástroje), u obézních pacientů s výhodou využíváme i čtvrtého ramene. Po provedené podélné aortotomii podle individuálního nálezu provádíme i endarterektomii aorty a následně roboticky našíváme centrální anastomózu. Poté provedeme kontrolu těsnosti proximální anastomózy uvolněním cévních svorek (Obr. 4). Pokud není přítomno krvácení následuje uzavření retroperitonea roboticky vstřebatelným šicím materiálem. Periferní anastomózy jsou našity standardně konvenční technikou. Po kontrole těsnosti periferních anastomóz je provedena neutralizace heparinu protaminsulfátem. Na závěr provádíme laparoskopickou kontrolu dutiny břišní, zejména v místě uzavření retroperitonea s následnou kontrolou vstupů po trokarech a uzávěr všech operačních ran. Drenáž retroperitonea či Douglasova prostoru neprovádíme.
Image 3. Poloha pacienta Fig. 3. Positioning of patient 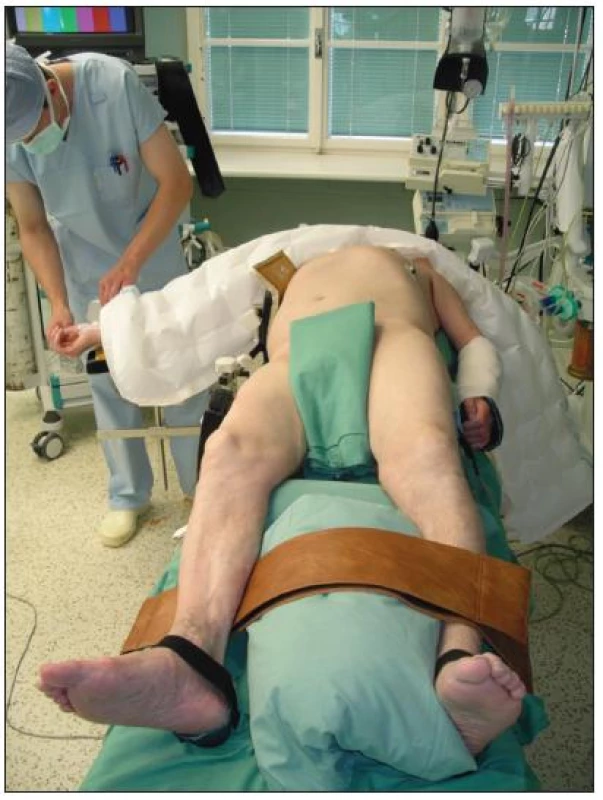
Image 4. Centrální anastomóza na abdominální aortě Fig. 4. Proximal anastomosis of abdominal aorta 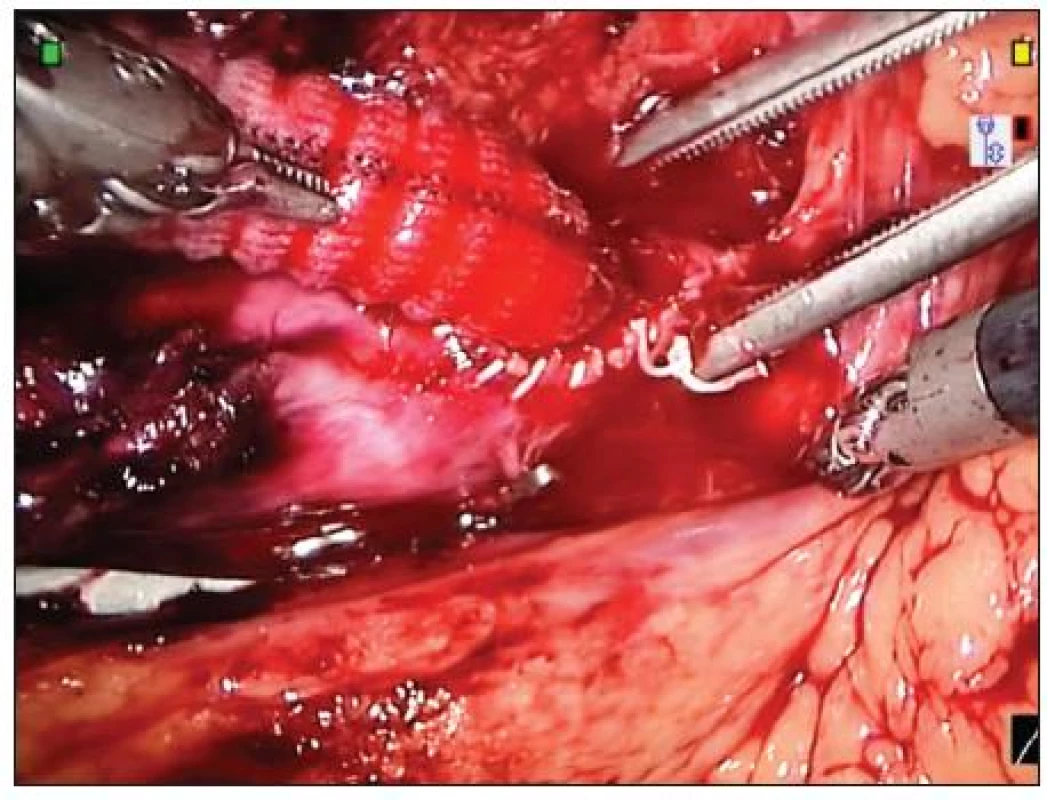
VÝSLEDKY
V uvedeném období jsme provedli celkem 45 roboticky asistovaných cévních rekonstrukcí aorto-ilicko-femorální oblasti. Implantovali jsme 21 aorto-bifemorálních bypassů, 22 aorto-femorálních a 2 ilicko-femorální bypassy. Medián času našití proximální anastomózy byl 23 min (rozmezí 18–50 min), medián času všech svorek byl 60 min (rozmezí 40–95 min). Medián celkového operačního času byl 295 min (rozmezí 180–475 min). Krevní ztráty – medián 265 ml (rozmezí 50–1200 ml). U dvou pacientů jsme provedli konverzi. Jedna byla pro těžce sklerotickou aortu, druhá pro neztišitelné krvácení z ilické žíly při preparaci. Doba pobytu pacienta na JIP po operačním výkonu – medián 2 dny (rozmezí 1–8 dnů). V průběhu sledování – medián 19 měsíců (rozmezí 2–50 měsíců) byly zaznamenány 3 (6,7 %) časné uzávěry rekonstrukce. Všechny uzávěry rekonstrukcí byly pro insuficientní výtok na arteria femoris profunda a byly vyřešeny prodloužením rekonstrukce (femoro-popliteální bypass). Z pozdních komplikací byla zaznamenána 1x kýla v portu (2,2 %). Nebyly zaznamenány žádné kardiální, pulmonální či renální komplikace, žádná infekce cévní rekonstrukce. Pooperační mortalita byla rovněž nulová (Tab. 1). Primární průchodnost rekonstrukcí ve sledovaném období byla 93 %, sekundární průchodnost byla 100 %.
Table 1. Peroperační a pooperační data souboru 45 pacientů u roboticky asistovaných tepenných rekonstrukcí aorto ilicko-femorální oblasti Tab. 1. Intraoperative and postoperative data collected from a group of 45 patients in robot-assisted arterial reconstructions in the aorto-iliac-femoral region 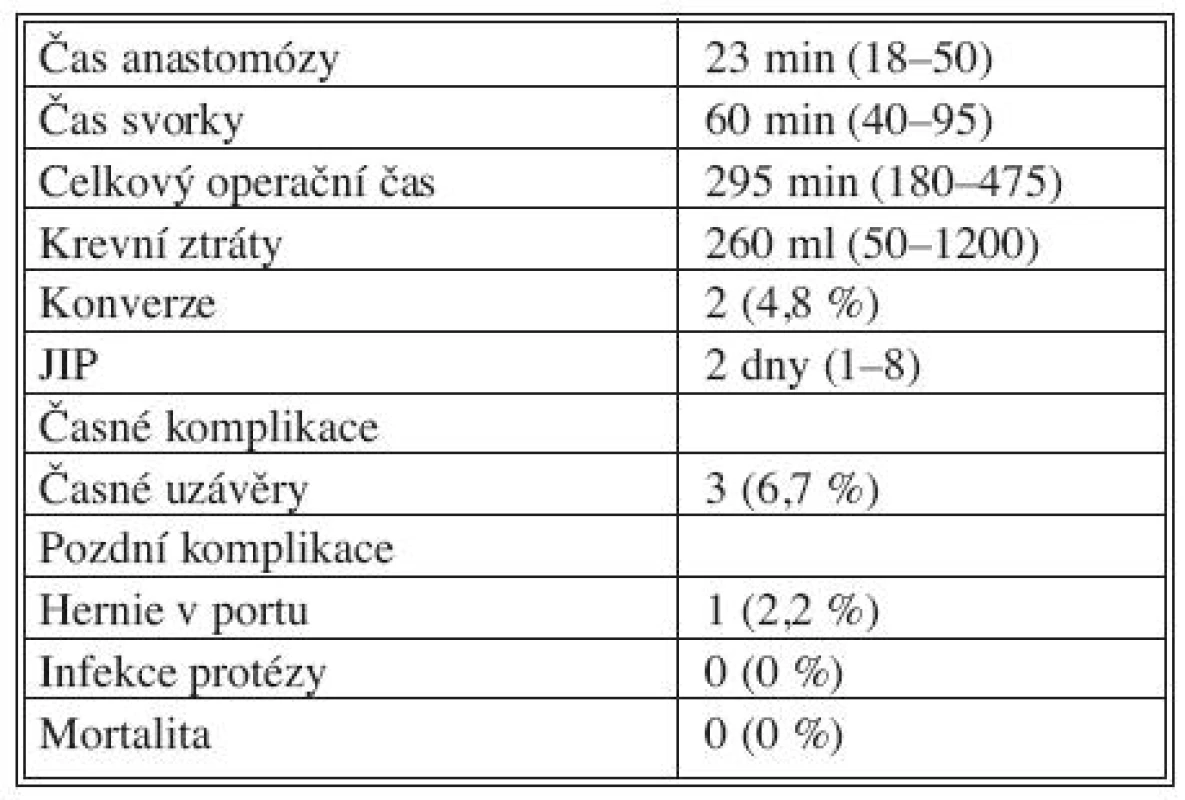
DISKUSE
V našem sdělení popisujeme soubor 45 pacientů s okluzivním onemocněním aorto-iliakální oblasti řešených miniinvazivním postupem – roboticky asistovanou cévní rekonstrukcí. V rámci miniinvazivní cévní chirurgie jsou popisovány různé přístupy k aortě. Např. Coggia při zajištění přístupu k aortě mobilizuje laparoskopicky levé colon a levou ledvinu [7]. My užíváme modifikovaný transperitoneální direktní přístup [8]. Výhodou tohoto přístupu je minimalizace retroperitoneální preparace a zkrácení času preparování.
Největší výhodou roboticky asistovaných cévních rekonstrukcí je rychlost provedení robotické cévní anastomózy [9]. Čas našití centrální anastomózy roboticky je srovnatelný s konvenční cévní anastomózou. Naproti tomu laparoskopicky našívaná cévní anastomóza bez použití robotického systému vykazuje nepoměrně delší čas svorky i čas anastomózy. Medián celkové krevní ztráty v našem souboru je 265 ml. Tato ztráta je výrazně nižší než uvádějí jiní autoři [10].
Také medián celkového operačního času (295 min) pacientů našeho souboru je delší než uvádí Štádler (235 min) [11]. Rozdíly v celkovém operačním čase mohou být dány rozdílnou velikostí souborů, a z toho vyplývající i rozdílnou zkušeností operatéra. Robotický systém v porovnání s laparoskopickou cévní chirurgií umožňuje téměř dokonalý pohyb nástrojů všemi směry v 3D obraze a zvyšuje přesnost při šití cévní anastomózy [12]. Výhodou robotického systému v cévní chirurgii je zkrácení „learning curve“. To ale zcela neplatí pro laparoskopickou část operace. Při použití robotického systému je tedy nezbytná i předchozí zkušenost v laparoskopické všeobecné a cévní chirurgii.
Krátkodobé pooperační výsledky robotických cévních výkonů jsou slibné. V našem souboru nebyly pozorovány žádné kardiální, pulmonální, renální ani hepatální komplikace. 30denní mortalita byla 0%. Medián pobytu na JIP byl 2 dny. Z tohoto pohledu se tato technika zdá být bezpečná i pro pacienty klasifikované jako ASA III.
ZÁVĚR
Roboticky asistované tepenné rekonstrukce umožňují velmi přesné našití cévní anastomózy s minimalizací krevních ztrát během výkonu. Dosažené výsledky (čas svorky, čas anastomózy) jsou srovnatelné s konvenční cévní chirurgií. Tento typ výkonů vyžaduje nezbytnou laparoskopickou zkušenost. Roboticky asistované aorto-ilicko-femorální bypassy se jeví jako bezpečná metoda s nízkým výskytem komplikací.
MUDr.Martin Dvořák, Ph.D.
II. chirurgická klinika LF MU a FN u sv. Anny v Brně
Pekařská 53
656 91 Brno
e-mail: martin.dvorak@fnusa.cz
Sources
1. Dion, Y. M., Katkhouda, N., Rouleau, C., Aucoin, A. Laparoscopic-assisted aortobifemoral bypass. Surg. Laparosc. Endosc., 1993; 3 : 425–429.
2. Ruurda, J. P., Wisselink, W., Cuesta, M. A., Verhagen, H. J., Broeders, I. A. Robot-assisted versus standard videoscopic aortic replacement. A comparative study in pigs. Eur. J. Vasc. Endovasc. Surg., 2004; 27 : 501–506.
3. Wisselink, W., Cuesta, M. A., Gracia, C., Rauwerda, J. A. Robot-assisted laparoscopic Aortobifemoral bypass for aortoiliac occlusive disease: A report of two cases. J. Vasc. Surg., 2002; 36 : 1079–1082.
4. Mehrabi, A., Yetimoglu, C. L., Nickkholgh, A., Kashfi, A., Kienle, P., Konstantinides, L., Ahmadi, M. R., Fonouni, H., Schemmer, P., Friess, H., Gebhard, M. M., Buchler, M. W., Schmidt, J., Gutt, C. N. Development and evaluation of a training module for the clinical introduction of the da Vinci robotic system in visceral and vascular surgery. Surg. Endosc., 2006; 20 : 1376–1382. Epub 2006 Jul 20.
5. Dormandy, J. A., Rutherford, R. B. Management of peripheral arterial disease (PAD). TASC Working Group. TransAtlantic Inter-Society Consensus (TASC). J. Vasc. Surg., 2000; 31: S1–S296.
6. Norgren, L., Hiatt, W. R., Dormandy, J. A., Nehler, M. R., Harris, K. A., Fowkes, F. G. TASC II Working Group. Inter-Society Consensus for the Management of Peripheral Arterial Disease (TASC II). J. Vasc. Surg. 2007; 45 Suppl. S: S5–67.
7. Coggia, M., Bourriez, A., Javerliat, I., GoĎau-Brissonni
8. Štádler, P., Šebesta, P., Vitásek, P., Matouš, P., El Samman, K. A modified technique of transperitoneal direct approach for totally laparoscopic aortoiliac surgery. Eur. J. Vasc. Endovasc. Surg. 2006; 32 : 266–269.
9. Diks, J., Nio, D., Jongkind, V., Cuesta, M. A., Rauwerda, J. A., Wisselink, W. Robot-assisted laparoscopic surgery of the infrarenal aorta: the early learning curve. Surg. Endosc., 2007; 10 : 1760–1763.
10. Garrett, H. E. Jr., Fernandez, J. D., Porter, Ch. Robot-assisted laparoscopic aortobifemoral bypass: initial experience developing a new program. J. Robotic. Surg., 2008; 2 : 247–251.
11. Štádler, P., Dvořáček, L., Vitásek, P., Matouš, P. Is Robotic Surgery Appropriate for Vascular Procedures? Report of 100 Aortoiliac CASE. Eur. J. Vasc. Endovasc. Surg., 2008; 36 : 401–404.
12. Desgranges, P., Bourriez, A., Javerliat, I., Van Laere, O., Losy, F., Lobontiu, A. et al. Robotically assisted aorto-femoral bypass grafting: lessons learned from our initial experience. Eur. J. Vasc. Endovasc. Surg., 2004; 27 : 507–511.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2011 Issue 1-
All articles in this issue
- Radikální operace infekce cévní protézy v aortofemorální pozici s pomocí čerstvého tepenného allograftu: naše střednědobé zkušenosti
- Současné trendy v chirurgické léčbě výdutě torakoabdominální aorty
- Změny velikosti pravého a falešného lumen ve viscerálním segmentu po endovaskulární léčbě disekcí aorty typu B
- Ischemická kolitída po operáciách pre AAA
- Plazmatické hladiny prozánětlivých cytokinů u aneuryzmatu abdominální aorty
- Roboticky asistované cévní rekonstrukce aorto-ilické oblasti
- Vliv infrainguinálních bypassů na dlouhodobou průchodnost pánevních intervencí – význam hybridních výkonů
- Žilní interponát při řešení krvácení z distální anastomózy pedálního bypassu
- Peroperační intraarteriální trombolýza v terapii akutní končetinové ischemie
- Aneuryzma lienální tepny jako příčina bolesti břicha s hypotenzí
- Simultánní karotická endarterektomie a koronární revaskularizace: indikace a výsledky
- Jednoduchá metoda odstranění infikované cévní protézy
- Dva mylné mýty flebologické chirurgie 20. století
- Cytostatická hypertermická perfuze izolované končetiny (HILP) ve VFN
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Aneuryzma lienální tepny jako příčina bolesti břicha s hypotenzí
- Současné trendy v chirurgické léčbě výdutě torakoabdominální aorty
- Cytostatická hypertermická perfuze izolované končetiny (HILP) ve VFN
- Radikální operace infekce cévní protézy v aortofemorální pozici s pomocí čerstvého tepenného allograftu: naše střednědobé zkušenosti
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

