-
Medical journals
- Career
Aproximační střevní anastomóza při multifokální nekrotizující enterokolitidě u novorozence
Authors: M. Rygl; R. Škába; K. Pýcha; J. Kučera *; Z. Straňák *
Authors‘ workplace: Klinika dětské chirurgie UK Praha, 2. LF a FN Motol, Katedra dětské chirurgie IPVZ, Praha přednosta: prof. MUDr. J. Šnajdauf, DrSc. ; Ústav pro péči o matku a dítě, Podolí, Katedra gynekologie a porodnictví IPVZ, Praha přednosta: doc. MUDr. J. Feyereisl, CSc. *
Published in: Rozhl. Chir., 2007, roč. 86, č. 8, s. 415-419.
Category: Monothematic special - Original
Overview
Multifokální nekrotizující enterokolitida (NEC) může být při rozsáhlém postižení příčinou syndromu krátkého střeva. Autoři uvádějí kazuistiku nezralého novorozence (PH 1700 g, gest. stáří 30 t.) s rozsáhlým postižením tenkého i tlustého střeva multifokální NEC. Při explorativní laparotomii byla ve zdravé části proximálního jejuna založena derivační jejunostomie ve vzdálenosti 28 cm od Treitzova ligamenta a ostatní postižené střevo bylo ponecháno in situ. Po 48 hodinách byly resekovány nekrotické segmenty tenkého střeva. Distálně od jejunostomie zůstalo 5 vitálních segmentů tenkého střeva o celkové délce 12 cm. Kontinuita těchto segmentů a vitálního ileocékálního přechodu bylo obnovena pěti aproximačními anastomózami. Každá aproximační anastomóza byla ušita omezeným počtem 4–6 jednotlivých stehů a všechny anastomózy se zhojily bez známek striktury či dehiscence. Kontinuita střeva mezi jejunostomií a rekonstruovaným segmentem ilea byla obnovena o 9 týdnů později. Celková délka tenkého střeva byla 50 cm. Pacient byl propuštěn domů v 5 měsících věku s váhou 4145 g na doplňkové parenterální výživě. Technika rychlé aproximační anastomózy může přispět k záchranně maximální střevní délky u pacientů s rizikem syndromu krátkého střeva.
Klíčová slova:
multifokální nekrotizující enterokolitida – syndrom krátkého střeva – aproximační anastomózaÚVOD
Novorozenecká nekrotizující enterokolitida (NEC) je akutní zánětlivé onemocnění střev, které postihuje převážně nezralé novorozence s nízkou porodní hmotností. NEC charakterizuje zánětlivé poškození střevní stěny nejčastěji v oblasti terminálního ilea a kolon. Poškození střeva je variabilní od slizničních změn (edém, prokrvácení, ulcerace) po gangrenózní zánět a koagulační nekrózu celé stěny. Onemocnění může postihovat jeden izolovaný úsek střeva (lokální NEC), více úseků (multifokální NEC) a nebo může být postiženo více než 75 % střeva (totální NEC, panintestinální NEC). Plně rozvinutá NEC u nezralých novorozenců je doprovázena 20–50% mortalitou.
Rozsáhlá ztráta tenkého střeva při NEC je spolu s volvulem středního střeva, jejunoileálními atréziemi a vrozenými defekty stěny břišní nejčastější příčinou syndromu krátkého střeva (SBS – short bowel syndrome) v dětském věku.
U donošeného novorozence lze za SBS považovat zachování méně než 70–75 cm (40 %) tenkého střeva. Wilmore (1972) uvedl, že pro přežití novorozence se SBS je nezbytných minimálně 30 cm tenkého střeva a zachovaná ileocékální chlopeň, přežití při zachování méně než 15 cm tenkého střeva je nepravděpodobné [1]. Zachování ileocékální chlopně je významné pro rychlejší adaptaci zbylého tenkého střeva a pro snížení výskytu enterogenních sepsí. Prevence vzniku SBS tedy začíná již při primární chirurgické léčbě NEC, při které je nutné zachovat každý potenciálně vitální úsek střeva.
Cílem sdělení je ukázat použití vícečetné aproximační střevní anastomózy v léčbě novorozence s rozsáhlou multifokální NEC. Technika aproximační anastomózy používá k obnovení kontinuity střevního lumen a k zajištění integrity anastomózy minimální množství jednotlivých stehů.
KAZUISTIKA
Chlapec, dvojče A (porodní hmotnost 1700 g, gestační stáří 30+ 6, Apgar 7-9-9) se narodil císařským řezem pro předčasný odtok plodové vody, nepravidelnou polohu dvojčat a neúspěšnou tokolýzu. Pro známky mírného RDS byl první den života na distenční dechové podpoře (nCPAP). V dalších dnech probíhala poporodní adaptace přiměřeně, od prvního dne života byl chlapec krmen stravou a od 12. dne byl na plné perorální výživě. 25. den života se objevily klinické i laboratorní známky nekrotizující enterokolitidy: enteroragie, distenze břicha, zbarvení břišní stěny, leukocytóza, trombocytopenie, vysoké zánětlivé parametry a na RTG snímcích byla zřejmá střevní pneumatóza. Byla zahájena konzervativní léčba – nic per os, oběhová podpora, umělá plicní ventilace (UPV) a kombinace antibiotik (Targocid, Meronem, Metronidazol). 27. den byla provedena operační revize pro RTG známky pneumoperitonea. Při operaci byla nalezena hemoragická nekrotizující entrokolitida v rozsahu od proximálních 28 cm jejuna po lienální ohbí kolon (Obr. 1). Vzhledem k rozsahu poškození střeva byla ve zdravé části jejuna založena odlehčující proximální jejunostomie a poškozené tenké střevo bylo ponecháno in situ k dalšímu řešení při second-look operaci. Pooperační průběh byl komplikován opakovaným krvácením do GIT, multiorgánovým selháním a rozvojem břišního kompartment syndromu, který byl řešen přechodným uzavřením laparotomie folií Steri-Drape (fa 3M Health Care) (Obr. 2). Po 48 hodinách při další operaci byly resekovány ohraničené nekrózy tenkého střeva. Vitálních zůstalo proximálních 28 cm jejuna a 5 oddělených úseků na hranici jejuna a ilea v celkové délce 12 cm. Ve snaze zabránit syndromu krátkého střeva bylo 5 oddělených, ale vitálních úseků spojeno technikou aproximační anastomózy s redukovaným množství 4–6 stehů Vicryl 5/0 (polyglactin, fa. Ethicon) (Obr. 3). Bauhinská chlopeň a ileocékální přechod zůstaly zachovány, nekrotická část colon ascendens byla podélně resekována a též aproximačně sešita. V dalším týdnu života byl chlapec 2x revidován pro krvácení z omenta a břišní stěny a pro přetrvávající břišní kompartment syndrom byla stěna břišní uzavřena pomocí záplaty z GORE-TEX (polytetrafluoretylen, fa W. L. Gore&Association). Po operaci byla po dobu 21 dní nutná podpora UPV a totální parenterální výživa (TPV). Od 45. dne byl opět zahájen enterální příjem. Pro velké ztráty ze stomie převažovala v následujících týdnech parenterální výživa s hrazením minerálů a jen zvolna se dařilo zvyšovat dávky enterální výživy (kombinace mateřského mléka a preparátu Neocate). Při dlouhodobé parenterální výživě se postupně rozvinula cholestatická hepatopatie. Devět týdnů po první operaci bylo přistoupeno k zanoření stomií. Při operaci bylo nutné pro pozánětlivou strikturu resekovat tlusté střevo od hepatálního ohbí po sigmoideum. U pacienta zůstala zachována Bauhinská chlopeň a vzestupný tračník, proximální jejunum a vitální byl také úsek tenkého střeva rekonstruovaný z 5 segmentů (aproximační anastomózy se zhojily bez známek striktury či dehiscence). Kontinuitu GIT se zdařilo obnovit anastomózami na tenkém střevě a acsendentosigmoideoanastomózou. Tenké střevo z původních vitálních 28 cm a 12 cm rekonstruovaných při second look operaci narostlo na celkem 50 cm. Čtvrtý den po výkonu byla nutná další revize břišní dutiny pro spontánní perforaci na kolon ascendens. Po operaci pokračovala TPV a postupně se zvyšoval perorální příjem potravy. Před propuštěním bylo střevo adaptováno na dávku 30 ml preparátu Neocate v rýžovém odvaru podávaný po 3 hodinách. Pacient byl propuštěn domů v pěti měsících věku v uspokojivém celkovém stavu s váhou 4145 g. Doma pokračovala kombinace domácí TPV a enterální výživy. V 8 měsících věku chlapec vážil 7,5 kg a při režimu intermitentní parenterální výživy byl jeho střevní trakt adaptovaný na dávky 60 ml stravy po 4 hodinách. V dlouhodobém výhledu je pravděpodobné úspěšné převedení chlapce na plný enterální příjem.
Image 1. Rozsah poškození při první operaci – multifokální nekrotizující entrokolitida od proximálních 28 cm jejuna po tlusté střevo Fig. 1. The lesion size during the first procedure – multifocal necrotizing enterocolitis extending from proximal 28 cm of the jejunum to the large intestine 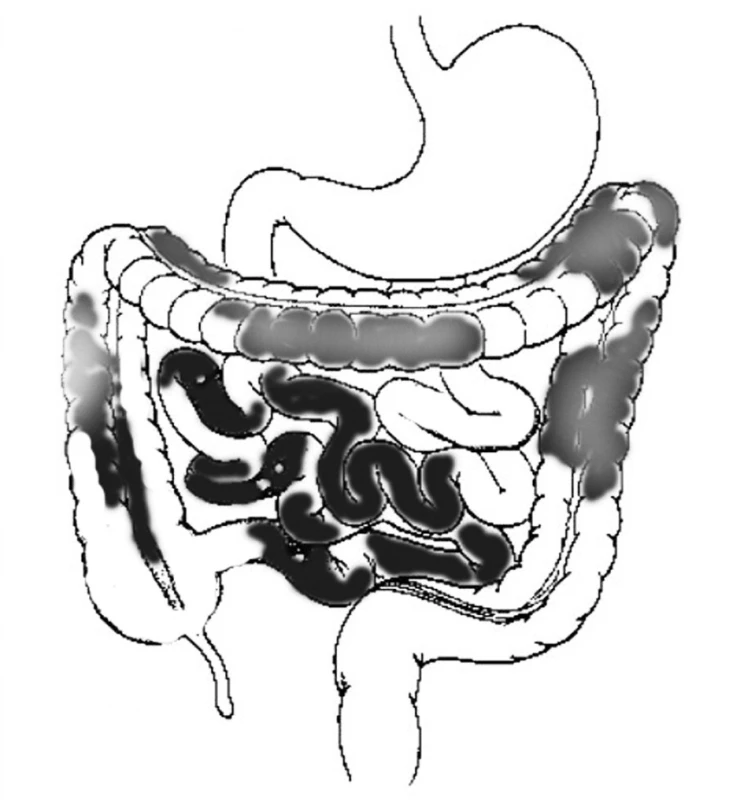
Image 2. Břišní kompartment syndrom byl řešen přechodným překrytím laparotomie folií Steri-Drape Fig. 2. The abdominal compartment syndrome was managed by temporary application of the Steri-Drape foil over the laparotomy site. 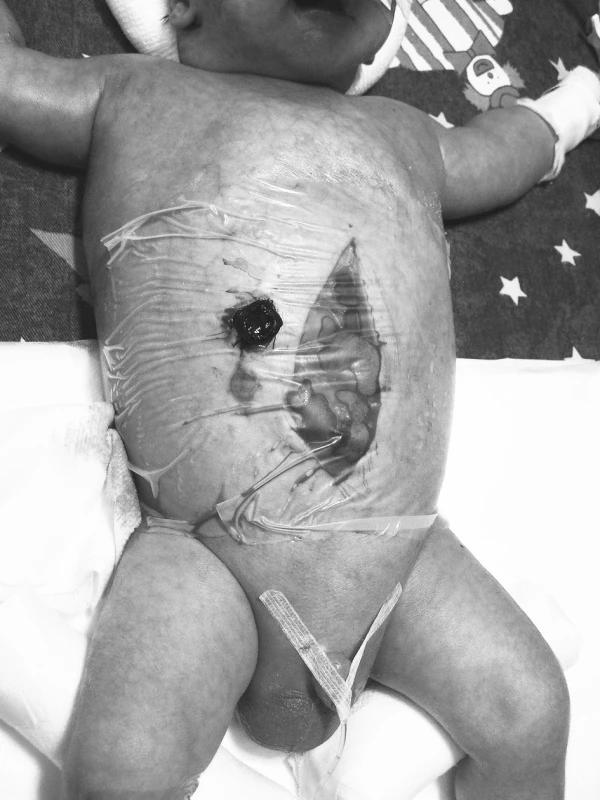
Image 3. Stav po second-look operaci: 5 oddělených, ale vitálních úseků spojeno technikou aproximační anastomózy. Poškození tlustého střeva nepokročilo do stadia nekrózy Fig. 3. Situation following the second-look procedure: 5 separated, however, vital sections were connected using the approximation anastomosis technique. Affection of the large instestine has not progressed to a necrotic stage. 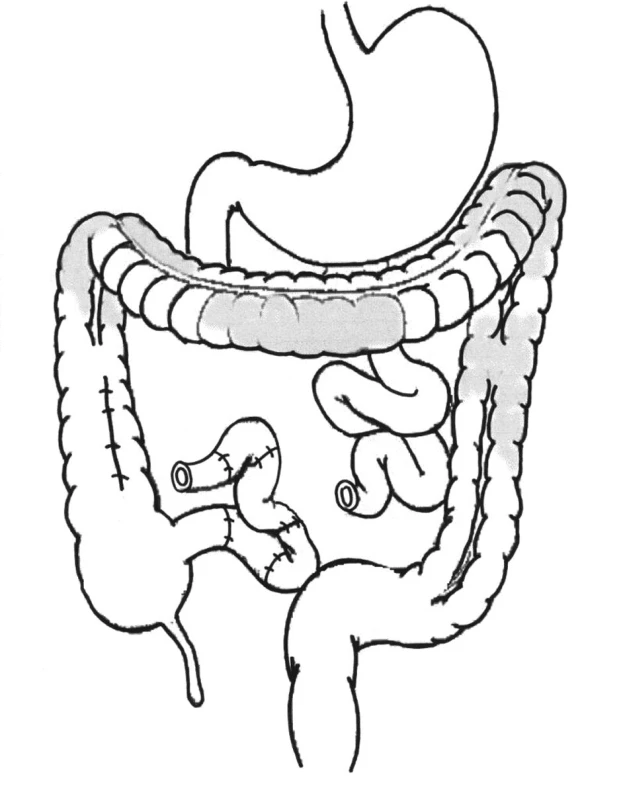
DISKUSE
Při rozsáhlé multifokální nebo panintestinální NEC je naděje na úspěšné chirurgické řešení velmi omezená a přežití pacientů bývá spojeno se syndromem krátkého střeva. V mnoha případech končí chirurgická léčba inoperabilním nálezem nekrózy celého tenkého střeva při explorativní laparotomii [2]. Rowe udává úmrtnost 93 % [3] a Voss dokonce 100 % [4].
V některých případech multifokální NEC zůstávají krátké úseky tenkého střeva vitální a o prognóze těchto pacientu rozhoduje zachování co největší délky tenkého střeva. V případě nezralých novorozenců s NEC se jedná o operace novorozenců v septickém šoku a kritickém celkovém stavu, který vyžaduje kontinuální respirační a oběhovou podporu. Nezbytné je proto provedení operace přímo na lůžku JIP, aby se tak vyloučila rizika spojená s transportem nestabilního, nezralého novorozence na operační sál.
Léčba nezralých novorozenců s rozsáhlou multifokální nebo panintestinální NEC zůstává kontroverzní [3, 5–10]. Založení vícečetných stomií nebo provedení více anastomóz jsou časově a technicky náročné, u nestabilního novorozence prakticky kontraindikované operační výkony. Cílem chirurgické léčby je odstranění nekrotických úseků střeva, zachování co největší délky střev a obnovení střevní kontinuity. Při rozsáhlé ischemii střeva se primárně neprovádí subtotální střevní resekce, neboť nekrózy střeva nejsou dobře ohraničené a rozsah poškození se může dále měnit. S definitivním výkonem se vyčkává na second look operaci nejméně po 48 hodinách. Prokrvení střeva se v té době může zlepšit a výsledná ztráta střeva bude v druhé době menší. V současnosti z těchto základních předpokladů vychází většina používaných operační řešení: peritoneální drenáž [11], proximální derivační jejunostomie [12], metoda „patch, drain and wait“ [13], metoda „clip and drop back“ [14] a metoda „damage control laparotomy“ [2].
Peritoneální drenáž jako počáteční resuscitační metodu pro léčbu nestabilních novorozenců s komplikovanou NEC zavedl v roce 1977 Ein [15]. Za metodu bezprostřední resuscitace ji považuje také Ahmed, v jeho souboru 23 dětí s NEC léčených peritoneální drenáži si 19 dětí (83 %) vyžádalo další operaci [16]. Cass použil peritoneální drenáž u 11 dětí s NEC [17]. Ve této skupině s NEC si následnou laparotomii vyžádalo 8 dětí tj. 72 % a dlouhodobé přežití bylo jen 27 %. Podle našeho názoru může peritoneální drén přispět k předoperační stabilizaci v šokovém stadiu. Vzhledem k rozsahu nekróz u rozsáhlých NEC, jak jej nalézáme při operacích, je nepravděpodobné, že by peritoneální drenáž mohla být definitivním řešením k obnovení kontinuity střeva.
Dalším řešením je založení proximální derivační jejunostomie s ponecháním nekrotických segmentů in situ s výhledem dalším chirurgických intervencí po stabilizaci. Sugarman tímto postupem dosáhl přežití pěti z deseti dětí s rozsáhlým postižením [12]. Baniengbal naopak použití proximální jejunostomie odmítá pro velké ztráty tekutin a vysoký výskyt stomických komplikací [2]. Moore popsal při rozsáhlém postižení s více perforacemi metodu „patch, drain and wait“ [13]. Při operační revizi se přešijí perforace a založí nitrobřišní drény. Metoda je spojena se vznikem píštělí a většina případů vyžaduje po úspěšné stabilizaci další operace. Vaughan doporučuje techniku „clip and drop-back“ kdy pomocí klipů nebo stapleru zresekuje nekrotické segmenty a uzavřené „vitální“ segmenty ponechá v peritoneální dutině [14]. Při druhé operaci za 48–72 hodin obnoví střevní kontinuitu anastomózami mezi vitálními úseky. Obdobnou možností je adaptační napojení krátkých vitálních segmentů na intubační sondě, Lessin uvádí dokonce spontánní autoanastomózu intestinálních segmentů na zavedené sondě [18].
Banieghbal a Davis popsali v roce 2004 techniku „damage control laparotomy“ [2]. Po krátké 12hodinové předoperační stabilizaci resekovali nekrotické střevní segmenty, ostatní části střeva buď anastomozovali nebo podvázali. K secoond look operaci přistupovali až za 48–72 hodin, kdy je rozsah poškození střeva zřejmý a umožňuje dokončit excizi nekróz a obnovení kontinuity střeva.
LÉČEBNÝ POSTUP AUTORŮ
Rozsáhlé formy onemocnění typu „multifokální NEC či totální NEC“ mají i podle našich skutečností velmi špatnou prognózu. Domníváme se, že primární výkon má u těchto případů zabezpečit derivaci obsahu břišní dutiny jako prevenci oběhové a ventilační nestability a derivaci gastrointestinálního traktu jako prevenci progrese NEC. K resekčním výkonům se má přistoupit s odstupem nejméně 48 hodin. V uvedené kazuistice jsme zvolili taktiku second-look operace s proximální derivační jejunostomií. Po demarkaci střevních nekróz zůstalo vitálních 28 cm proximálního jejuna a izolované krátké segmenty v oblasti ilea. Ve snaze o záchranu co nejdelší části tenkého střeva jsme při second-look operaci a přetrvávajícím nestabilním celkovém stavu novorozence použili novou techniku rychlé aproximační anastomózy. Technikou aproximační anastomózy jsme z pěti izolovaných segmentů rekonstruovali dalších 12 cm tenkého střeva. Podkladem pro použití techniky aproximační anastomózy byly jednak literární kazuistiky [18] a také slibné výsledky s touto technikou z naší experimentální práce na potkanech. K obnovení střevní kontinuity izolovaných segmentů ilea jsme použili aproximační anastomózy s redukovaným množstvím stehů (4–6 stehů vicryl 5/0). Předpokládali jsme, že malé množství použitých stehů způsobí menší strangulaci tkáně v místě anastomózy a přitom bude dostatečné pro obnovení střevní kontinuity a pro integritu anastomózy. Z hlediska hojení anastomózy v době celkové cirkulační nestability může být zachování místní cirkulace v oblasti anastomózy dokonce výhodnější než snaha o konvenční vodotěsnou anastomózu. Aproximačními anastomózami mezi 5 izolovanými segmenty jsme získali dalších 12 cm ilea a při zachované ileocékální chlopni tak výrazně vzrostla naděje pacienta na úspěšnou léčbu SBS adaptací vlastního střeva.
ZÁVĚR
Péče o nezralé novorozence s nízkou porodní hmotností vyžaduje komplexní spolupráci neonatologa a dětského chirurga. Vzhledem k stávající mortalitě NEC 20–50 %, je nutné dále hledat nové postupy a indikace v intestinální chirurgii nezralých novorozenců. Aproximační anastomóza tenkého střeva by mohla být v indikovaných případech vhodnou léčbou.
Práce je součástí výzkumného záměru FNM MZO 00064203/6309.
MUDr. M. Rygl
Klinika dětské chirurgie UK 2. LF a FN Motol
V Úvalu 84
150 00 Praha 5
e-mail: mrygl@yahoo.com
Sources
1. Wilmore, D. W. Factors correlating with a successful outcome following extensive intestinal resection in newborn infants. J. Pediatr., 1972; 80 : 88–95.
2. Banieghbal, B., Davies, M. R. Damage control laparotomy for generalized necrotizing enterocolitis. World J. Surg., 2004; 28 : 183–186.
3. Rowe, M. I., Reblock, K. K., Kurkchubasche, A. G., Healey, P. J. Necrotizing enterocolitis in the extremely low birth weight infant. J. Pediatr. Surg., 1994; 29 : 987–990; discussion 990–981.
4. Voss, M., Moore, S. W., van der Merwe, I., Pieper, C. Fulminanting necrotising enterocolitis: outcome and prognostic factors. Pediatr. Surg. Int., 1998; 13 : 576–580.
5. Blakely, M. L., Tyson, J. E., Lally, K. P., McDonald, S., Stoll, B. J., Stevenson, D. K., Poole, W. K., Jobe, A. H., Wright, L. L., Higgins, R. D. Laparotomy versus peritoneal drainage for necrotizing enterocolitis or isolated intestinal perforation in extremely low birth weight infants: outcomes through 18 months adjusted age. Pediatrics, 2006; 117: e680–687.
6. Fasoli, L., Turi, R. A., Spitz, L., Kiely, E. M., Drake, D., Pierro, A. Necrotizing enterocolitis: extent of disease and surgical treatment. J. Pediatr. Surg., 1999; 34 : 1096–1099.
7. Hall, N. J., Curry, J., Drake, D. P., Spitz, L., Kiely, E. M., Pierro, A. Resection and primary anastomosis is a valid surgical option for infants with necrotizing enterocolitis who weigh less than 1000 g. Arch. Surg., 2005; 140 : 1149–1151.
8. Hofman, F. N., Bax, N. M., van der Zee, D. C., Kramer, W. L. Surgery for necrotising enterocolitis: primary anastomosis or enterostomy? Pediatr. Surg. Int., 2004; 20 : 481–483.
9. Singh, M., Owen, A., Gull, S., Morabito, A., Bianchi, A. Surgery for intestinal perforation in preterm neonates: anastomosis vs stoma. J. Pediatr. Surg., 2006; 41 : 725–729; discussion 725–729.
10. Butter, A., Flageole, H., Laberge, J. M. The changing face of surgical indications for necrotizing enterocolitis. J. Pediatr. Surg., 2002; 37 : 496–499.
11. Goyal, A., Manalang, L. R., Donnell, S. C., Lloyd, D. A. Primary peritoneal drainage in necrotising enterocolitis: an 18-year experience. Pediatr. Surg. Int., 2006; 22 : 449–452.
12. Sugarman, I. D., Kiely, E. M. Is there a role for high jejunostomy in the management of severe necrotising enterocolitis? Pediatr. Surg. Int., 2001; 17 : 122–124.
13. Moore, T. C. Successful use of the „patch, drain, and wait“ laparotomy approach to perforated necrotizing enterocolitis: is hypoxia-triggered „good angiogenesis“ involved? Pediatr. Surg. Int., 2000; 16 : 356–363.
14. Vaughan, W. G., Grosfeld, J. L., West, K., Scherer, L. R. 3rd, Villamizar, E., Rescorla, F. J. Avoidance of stomas and delayed anastomosis for bowel necrosis: the ‘clip and drop-back’ technique. J. Pediatr. Surg., 1996; 31 : 542–545.
15. Ein, S. H., Marshall, D. G., Girvan, D. Peritoneal drainage under local anesthesia for perforations from necrotizing enterocolitis. J. Pediatr. Surg., 1977; 12 : 963–967.
16. Ahmed, T., Ein, S., Moore, A. The role of peritoneal drains in treatment of perforated necrotizing enterocolitis: recommendations from recent experience. J. Pediatr. Surg., 1998; 33 : 1468–1470.
17. Cass, D. L., Brandt, M. L., Patel, D. L., Nuchtern, J. G., Minifee, P. K., Wesson, D. E. Peritoneal drainage as definitive treatment for neonates with isolated intestinal perforation. J. Pediatr. Surg., 2000; 35 : 1531–1536.
18. Lessin, M. S., Schwartz, D. L., Wesselhoeft, C. W. Jr. Multiple spontaneous small bowel anastomosis in premature infants with multisegmental necrotizing enterocolitis. J. Pediatr. Surg., 2000; 35 : 170–172.
Labels
Surgery Orthopaedics Trauma surgery
Article was published inPerspectives in Surgery

2007 Issue 8-
All articles in this issue
- Diagnostické a léčebné postupy u torakoabdominálních poranění – současný stav
- Podtlaková terapie (vacuum-assisted closure) v léčbě ranných infekčních komplikací po kardiochirurgických výkonech
- Naše první zkušenost s rigidní fixací sterna
- Aproximační střevní anastomóza při multifokální nekrotizující enterokolitidě u novorozence
- Komplikace laparoskopické operace tříselné kýly diagnostikované kolonoskopicky
- Demografická a epidemiologická studie pacientů s poraněním pánve
- 10 let zkušeností s Barronovou ligaturou na chirurgické klinice Ostrava
- Radikální resekce u nemocných s karcinomem hlavy pankreatu. Retrospektivní analýza přežívání u souboru 307 nemocných
- Videotorakoskopie, standardní a méně časté indikace
- Laparoskopická cholecystektómia v ambulantnej chirurgii
- Perspectives in Surgery
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Komplikace laparoskopické operace tříselné kýly diagnostikované kolonoskopicky
- 10 let zkušeností s Barronovou ligaturou na chirurgické klinice Ostrava
- Videotorakoskopie, standardní a méně časté indikace
- Podtlaková terapie (vacuum-assisted closure) v léčbě ranných infekčních komplikací po kardiochirurgických výkonech
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

