-
Medical journals
- Career
Odhad přesnosti měření SUV na SPECT/CT GE Discovery 670
: Pavel Karhan; Jaroslav Ptáček
: Oddělení lékařské fyziky a radiační ochrany, LF UP a FN Olomouc, ČR
: NuklMed 2017;6:3-7
: Original Article
Úvod:
Byla provedena křížová kalibrace tomografické citlivosti SPECT/CT kamery GE Discovery 670 vůči lokálnímu měřiči aktivity BQMetr4.Materiál a metoda:
Chyba kalibračního koeficientu byla odhadnuta na 5,1 % v laboratorních podmínkách. Výsledná kalibrace byla ověřena sérií měření na fantomu Jaszczak bez vnitřních struktur a s horkými ložisky v různých geometriích a pro různé korekce.Výsledky:
Nejvyšší přesnost v nesymetricky rozptylujícím a pohlcujícím prostředí vykazuje pro objekty velikosti 25 mm kombinace korekcí na rozptyl akvizicí ve dvou energetických oknech a zeslabení pomocí CT 7,2 (± 2,9stat ± 10,3sys) % pro manuální segmentaci a 7,9 (± 1,5stat ± 8,2sys) % pro segmentaci založenou na hledání maximálního průměru oblasti pevné velikosti. V případě automatické segmentace je vhodné k těmto korekcím připojit i algoritmus resolution recovery, takže celková přesnost dosáhla 0,5 (± 0,9stat ± 7,9sys) %.Závěr:
Přesnost hodnot SUV je dána přesností křížové kalibrace, systematická chyba je oproti kalibraci zvýšená nepřesností měřiče aplikované aktivity a byla odhadnuta na nejvíce 7,1 % pro korekci na zeslabení a rozptyl a pro všechny uvažované metody segmentace.Klíčová slova:
kvantifikace SPECT, SUV, přesnost měřeníÚvod
Kvantifikace v emisní tomografii je ovlivněna řadou vlivů, které snižují její přesnost. Zatímco pro pozitronovou emisní tomografii (PET) je kvantifikace standardním postupem, ve vyšetřeních pomocí jednofotonové emistní počítačové tomografie (SPECT) se s kvantifikací setkáme zřídka. To je dáno tím, že u SPECT studií jsou tyto vlivy výraznější, ale s pokročilým vývojem technologií se chyba kvantifikace přiblížila hodnotám na PET. 1 Tato studie se pokouší odhadnout velikost chyby při kvantifikaci tomografických obrazů SPECT, zejména při stanovování standardized uptake value (SUV).
Konkrétními faktory omezujícími přesnost a spolehlivost kvantifikace u SPECT studií se zabývá řada prací (např. Rosenthal et al. 2, Willowson et al. 3, Buvat 4, Frey et al. 5), a proto budou zmíněny jen pro přehled. Tyto vlivy se obvykle dělí na fyzikální a technické (zeslabení a rozptyl, citlivost, rozlišení resp. efekt částečného objemu, rekonstrukce a šum) a faktory biologické (anatomie, biokinetika a také pohyb pacienta při vyšetření). Technické faktory je možné s omezenou přesností kompenzovat pomocí korekce na zeslabení (AC), korekce na rozptyl (SC), případně dekonvolučními metodami zahrnutými do iterativní rekonstrukce, jako např. resolution recovery (RR).
V literatuře se uvádí chyby kvantifikace pro SPECT obvykle nižší než 10 %. 6 Willowson et al. 3 uvádí přesnost -1 (± 7) % ve fantomové i klinické studii vyšetření ventilace plic pomocí 99mTc značeného MAA, v další práci 7 uvádí přesnost 4 % pro 201Tl. Frey et al. 5 shrnuje uváděné přesnosti pro ostatní radionuklidy: pro 131I na základě simulací 12 % pro kolimátor s vysokým rozlišením a 6 % pro kolimátor s ultra-vysokým rozlišením, 6 % pro játra a velké orgány a lepší než 5 % pro 111In ve velkých orgánech, zatímco statistická chyba se pohybuje několikanásobně níže.
Materiál a metoda
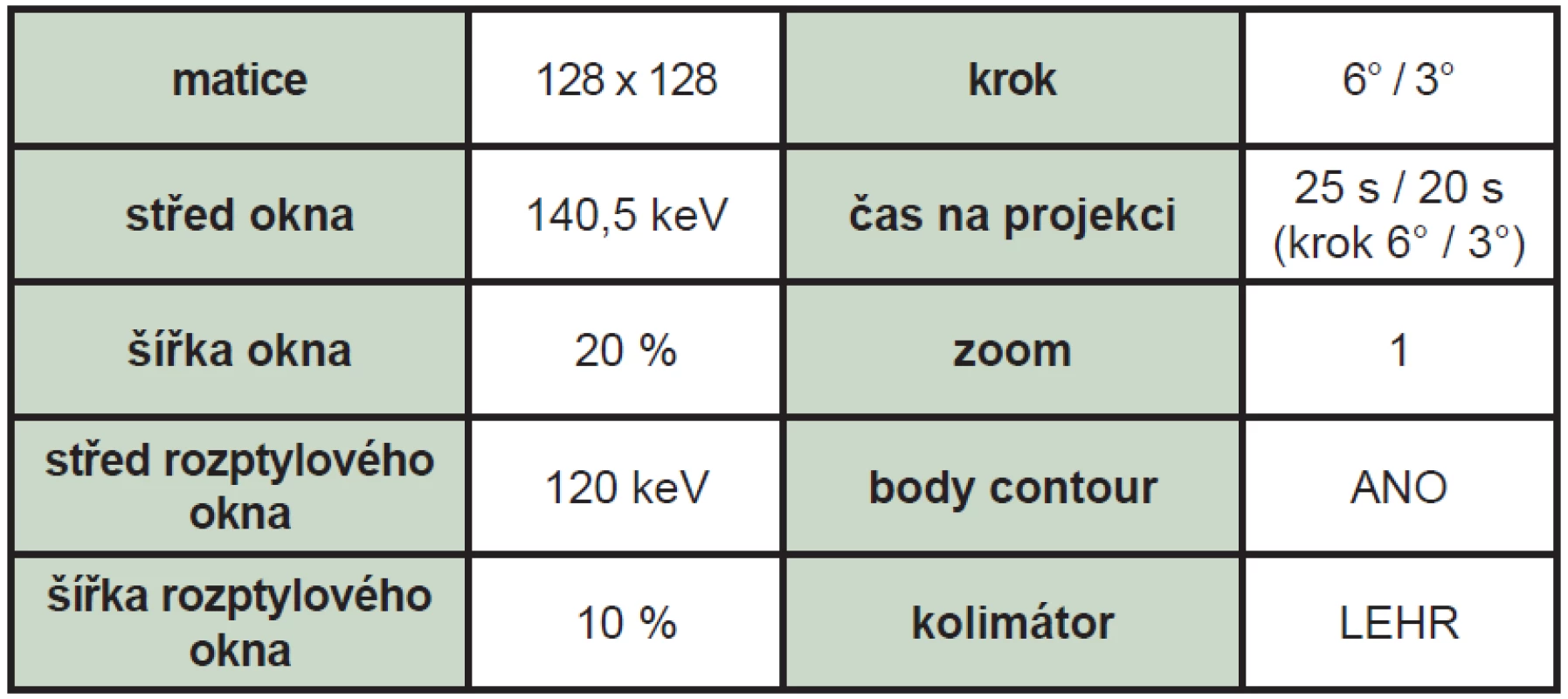
Křížová kalibrace kamery GE Discovery 670 byla provedena pomocí fantomu Jaczczak po vyjmutí všech vnitřních struktur. Fantom o celkovém objemu 5617 (± 10) ml byl naplněn 547 MBq (± 5 %) roztoku 99mTc. Akviziční parametry byly nastaveny tak, aby co nejvíce odpovídaly klinické praxi. (Tab. 1) Tomografická citlivost byla stanovena z celkového počtu impulsů v ROI pokrývající cca 75 % plochy řezu fantomem ve 12 po sobě jdoucích tomografických řezech v centrální oblasti fantomu.
Naměřená data byla rekonstruována na pracovní stanici GE Xeleris 3.1 rekonstrukcí OSEM se 4 iteracemi a 10 subsety 8 a různými korekcemi v těchto kombinacích: korekce zeslabení pomocí CT (ACCT), korekce zeslabení pomocí CT a korekce rozptylu pomocí obrazu z druhého energetického okna (SCACCT) a korekce na zeslabení a rozptyl Changovou metodou (s koeficientem útlumu 0,11 cm-1). Dále byla provedena rekonstrukce s resolution recovery algoritmem (RR) pro korekce ACCT a SCACCT. Koeficienty citlivosti musí být korigovány na mrtvou dobu. Převod počtu impulsů v jednotlivých voxelech na objemovou aktivitu byl proveden na základě hodnot tomografických citlivostí automaticky pomocí vlastní DICOM SCU/SCP aplikace vytvořené s využitím balíku DCMTK 3.6.1. 9
Pro ověření reprodukovatelnosti kalibrace a pro odlišení příspěvků k celkové chybě měření od jednotlivých kroků kalibrace a následného měření byla stanovena přesnost kalibrace na kalibračních datech s jinou volbou ROI a na datech získaných novým snímáním dat s tímtéž plněním fantomu po 21 hodinách s krokem 3° a po 45 hodinách s krokem 6°.
Akviziční i rekonstrukční parametry zůstaly stejné jako při kalibračním měření. Při ověřování byla porovnávána naměřená průměrná objemová aktivita v 6 stejně velkých plošných ROI různě umístěných v celém objemu fantomu. Díky tomu, že nebylo provedeno nové plnění fantomu, systematická chyba měřičů aktivity a objemu se neprojevila.
Statistická chyba σstat byla odhadnuta z průměrné výběrové směrodatné odchylky průměru v jednotlivých ROI, přičemž pruh značí průměr. Pokud předpokládáme homogenní šum, pak v nekonečné limitě platí10
kde je počet pixelů v ROI a je změřený šum. Protože počet pixelů je stejný ve všech ROI, použití průměru má smysl. Pokud by šum a průměry v jednotlivých ROI byly stejné, střední hodnota
by měla být rovna směrodatné odchylce průměru průměrů σp 6 studovaných ROI. V důsledku geometrické systematické chyby σg (vliv rekonstrukce, špatného rozmíchání radiofarmaka nebo efektu částečného objemu na krajích fantomu) ale přibližně platí
Na základě této úvahy byla geometrická systematická chyba odhadnuta jako výběrová směrodatná odchylka průměru průměrů v jednotlivých ROI v kvadrátu snížená o statistickou chybu.
Na základě této úvahy byla geometrická systematická chyba odhadnuta jako výběrová směrodatná odchylka průměru průměrů v jednotlivých ROI v kvadrátu snížená o statistickou chybu.
Dále byla provedena série měření fantomu Jaszczak s horkými lézemi se stejnými akvizičními parametry jako při kalibračním měření ale pouze s krokem 6°. Fantom byl naplněn 45,8 MBq (± 5 %) roztoku 99mTc do objemu 73 (± 2) ml horkých lézí a 400,5 MBq (± 5 %) roztoku 99mTc do objemu 5550 (± 10) ml pozadí. Celkem bylo provedeno 7 měření s časovými odstupy od prvního měření 1 : 14 h, 1 : 37 h, 3 : 51 h, 4 : 11 h, 12 : 17 h a 23 : 45 h. Měření byla provedena s různými předměty umístěnými kolem fantomu, které simulovaly vliv rozptylujících a zeslabujících tkání. (Obr. 1)
1. Příklady různých uspořádání objektů simulujících zvýšené zeslabení a rozptyl záření. Byly použity parafínové odlitky, vodě ekvivalentní balistický gel a kniha v různých kombinacích a uspořádáních. 
Rekonstrukce byla identická jako u kalibračního měření a byla provedena pro korekce ACCT, SCACCT a SCACCT s RR. Ve fantomu bylo provedeno měření objemové aktivity v centrální části fantomu a v pěti největších horkých lézích válcového tvaru třemi různými metodami. První metoda spočívala v měření průměrných hodnot ve VOI kulového tvaru o průměru 5 cm umístěného mezi studenými lézemi pro měření pozadí a v 5 kulových VOI o průměru 1 cm umístěných do centra horkých lézí. Všechny VOI byly umisťovány manuálně na hybridních SPECT/CT obrazech. Druhým způsobem měření objemové aktivity bylo použití automatické segmentace z nabídky nástrojů Xeleris 3.1 založené na prahování s prahem 60 % maxima a ve výsledných maskách byl měřen průměr detekovaného počtu impulsů. Třetí metodou byla měřena nejvyšší průměrná hodnota v objemu 1 cm3 v rámci zvolené VOI (nástroj „Peak“ v software Siemens syngo.via). V tomto případě byly jako základní oblast zájmu použity kulové VOI o průměru 5 cm umístěné tak, aby celý objem horké léze ležel uvnitř VOI.
Výsledky
Změřené tomografické citlivosti jsou uvedeny v tabulce 2. Pro přesnost kalibrace kamery pro měření objemové aktivity nebo hodnot SUV je nejkritičtější přesnost měřiče aplikované aktivity, jehož chyba činí 5 % (údaj výrobce). Ostatní vlivy, jako např. přesnost stanovení objemu, je řádově nižší. Geometrické vlivy ve smyslu nehomogenního rozmíchání radiofarmaka, efektu částečného objemu a rekonstrukčních artefaktů byly v době měření odhadnuty v průměru na 1 %. Statistická chyba kalibrace pro použitou aktivitu byla nižší než 0,5 %. Celková chyba kalibračního koeficientu tedy činila nejvýše 5,1 %.
2. Výsledné tomografické citlivosti v cnt s<sup>-1</sup> MBq<sup>-1</sup>. První uvedená chyba je statistická a byla odhadnuta jako výběrová směrodatná odchylka průměru, druhá je systematická a představuje odchylku měřícího řetězce. 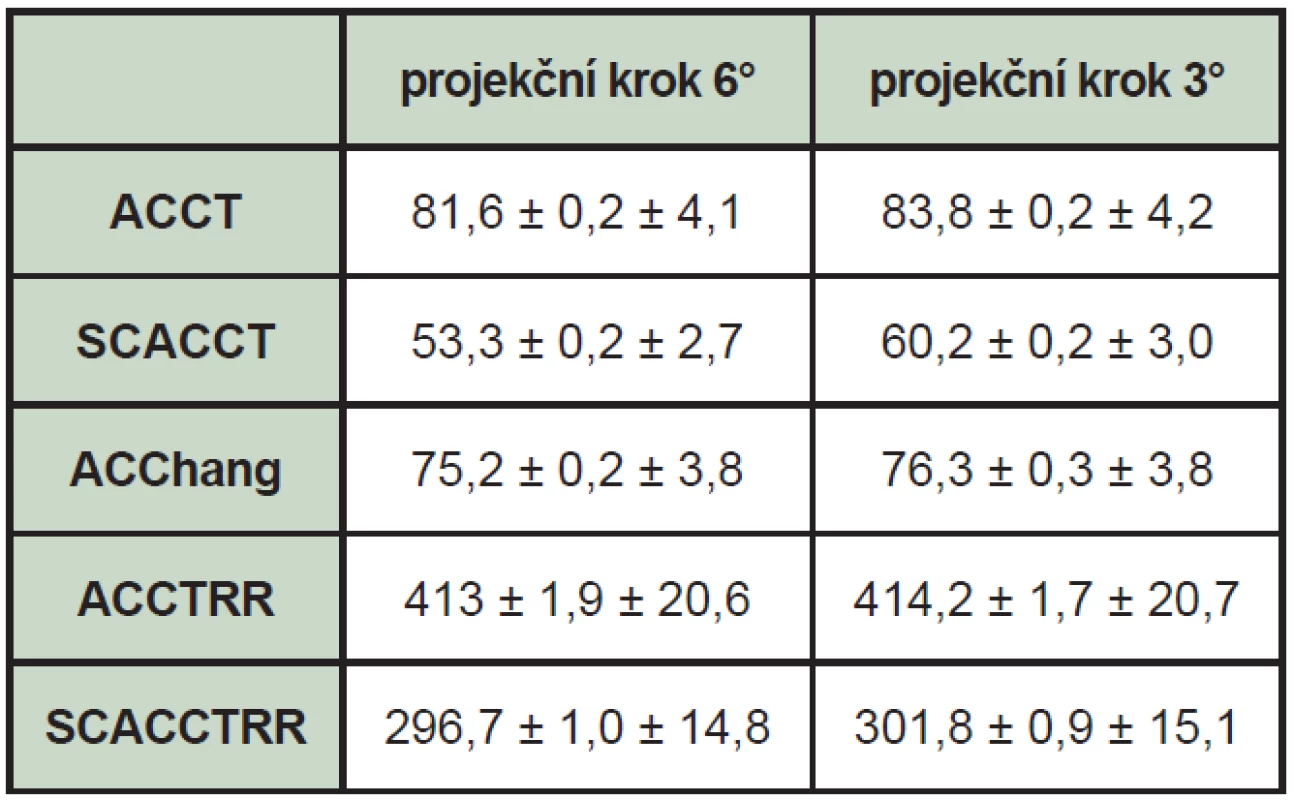
Výsledná přesnost kalibrace pro tentýž fantom s tímtéž plněním radiofarmakem je uvedena v tabulce 3. Opakované měření proběhlo po 21 hodinách pro krok 3° a 45 hodinách pro krok 6°.
3. Rozdíl změřené objemové aktivity po kalibraci od reálně aplikované v procentech. První uvedená chyba je statistická chyba, která byla odhadnuta jako výběrová směrodatná odchylka průměru v jednotlivých ROI, druhá chyba je geometrická a byla stanovena jako výběrová směrodatná odchylka průměru průměrů snížená v kvadrátu o statistickou chybu. Systematická chyba měřicího řetězce se v tomto případě neuplatňuje. 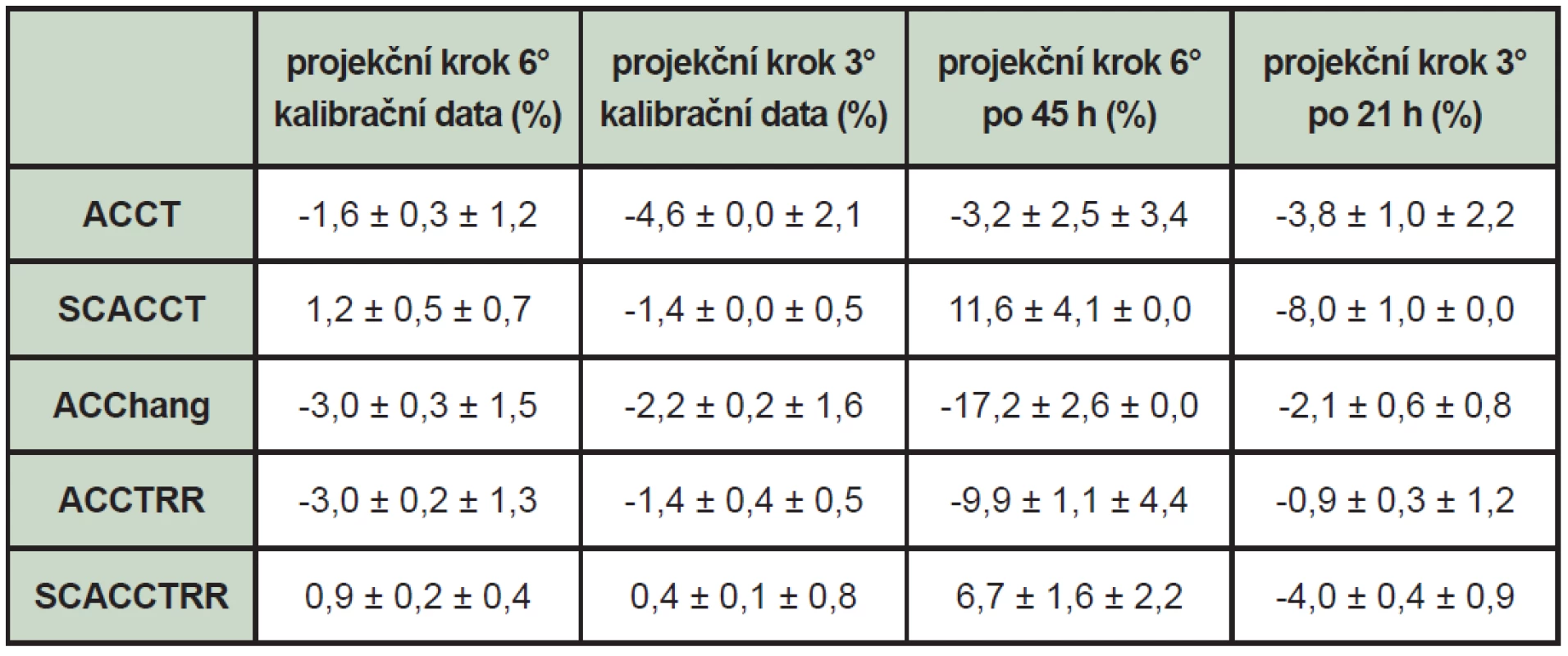
Přesnost určení objemové aktivity v nesymetrických rozptylujících a pohlcujících prostředích měřená pomocí fantomu Jaszczak s horkými lézemi je uvedena v tabulce 4 a zobrazena na Obr. 2.
4. Průměrný rozdíl změřené objemové aktivity po kalibraci od reálně aplikované v procentech. První z uvedených chyb je statistická, druhá systematická. Hodnoty pro léze o velikosti 25 mm jsou určeny jako průměr hodnot ve třech lézích. 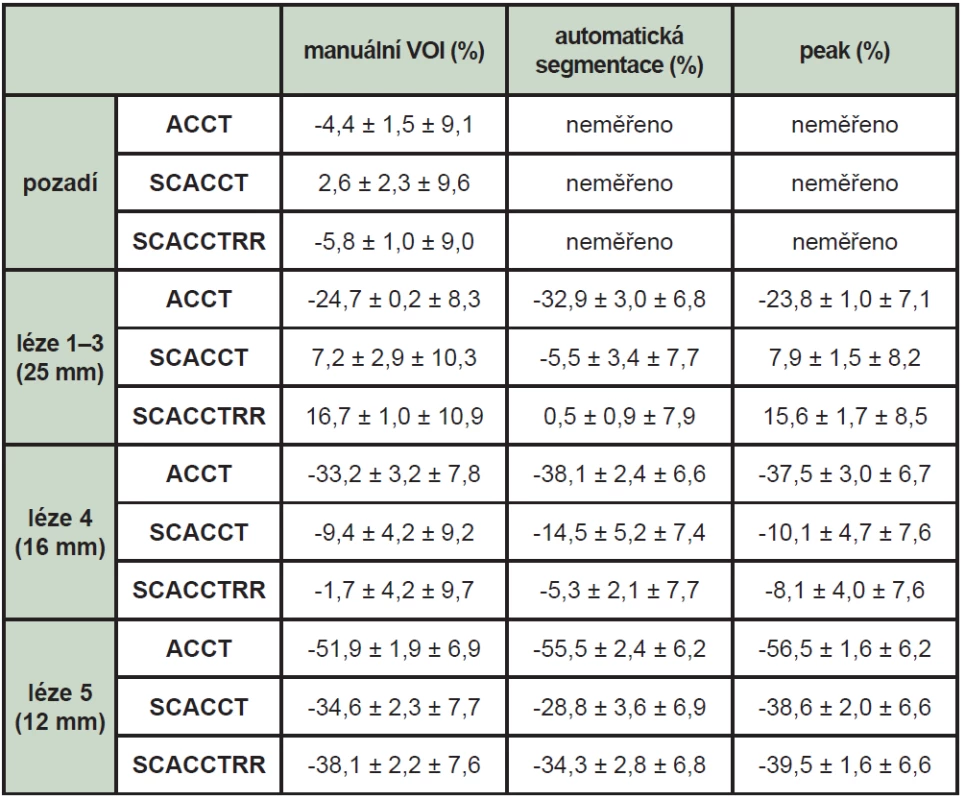
2. Průměrný rozdíl změřené objemové aktivity od reálně aplikované v procentech pro jednotlivé VOI (pozadí a 5 horkých lézí) a segmentace. Uvedené chybové úsečky odpovídají intervalu spolehlivosti 95 %. 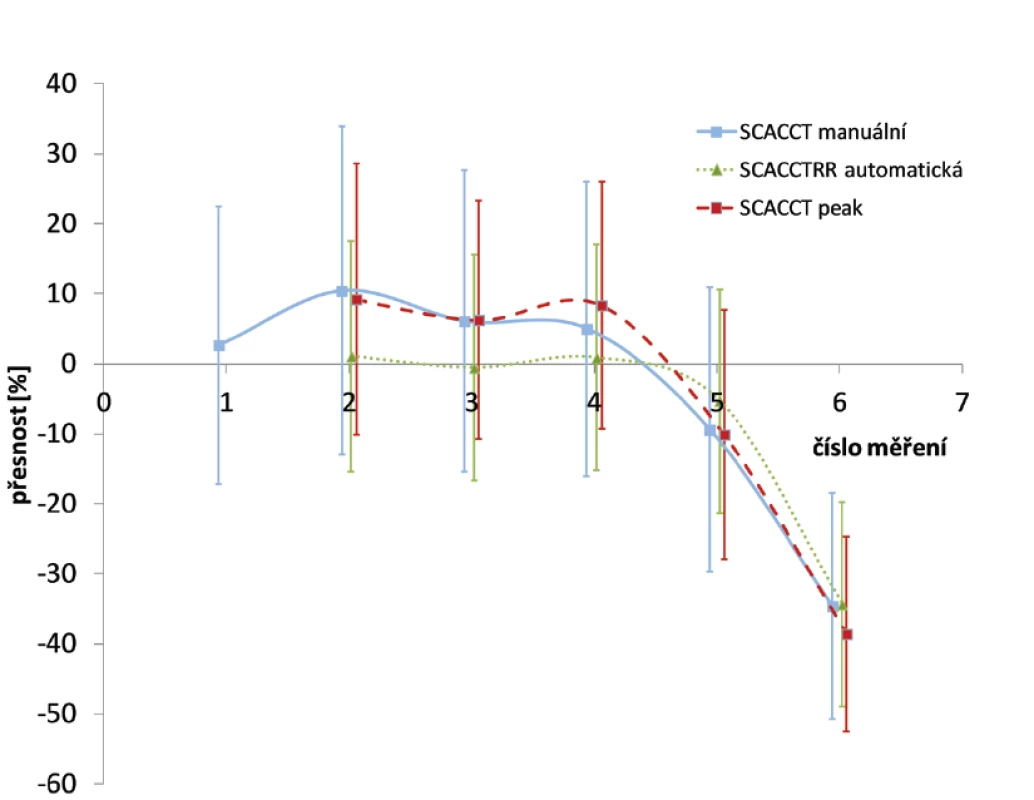
Byla pozorována závislost přesnosti na detekovaném počtu impulsů, resp. na aktuální objemové aktivitě pro metodu segmentace „peak“.
Diskuze
Objemové aktivity určené pomocí křížové kalibrace vykazují v rámci celého objemu fantomu systematické podhodnocení (Tab. 3), způsobené zřejmě efektem částečného objemu na okrajích fantomu. Ověření kalibrace po 21 a 45 h na kalibračním fantomu vykazuje významnou nepřesnost a variabilitu výsledků, což je nutné vzít v úvahu zejména při interpretaci obrazů s nízkým počtem detekovaných impulsů.
Hodnoty tomografické citlivosti pro různé korekce se vzájemně velmi liší a stejně tak se liší od planární citlivosti (72 cnt s-1 MBq-1) i systémové objemové citlivosti stanovené na základě doporučení NEMA 11 (68 cnt s-1 MBq-1). Takto určené citlivosti by tedy neměly být používány pro kalibraci určenou k tomografickému kvantitativnímu vyhodnocování, ale jen pro kontrolu kvality. Za povšimnutí také stojí 11% rozdíl mezi citlivostmi měření s krokem 6° a 3° pro SCACCT překračující 7% chybu měření.
Při měření v rozptylujícím absorbujícím prostředí lze za nejvhodnější korekci považovat SCACCT, která pro všechny metody segmentace vykazuje výsledky v rámci chyby ve shodě s reálnými aktivitami v době měření. Použití algoritmu RR vede k nižší přesnosti, ale nižší nebo srovnatelné preciznosti a tedy nižší variabilitě výsledků.
Při manuální segmentaci je zřejmý náznak systematického nadhodnocování, což může být dáno subjektivním výběrem VOI na hybridních obrazech, kdy vyhodnocující odborník mohl nevědomky upřednostňovat takové VOI, které mají silnější signál z modality SPECT. Proto by manuální zakreslování oblastí zájmu mělo probíhat na CT obrazech (tedy nikoliv v hybridním zobrazení), pokud to charakter vyšetření umožňuje.
Metoda segmentace „peak“ vykazuje závislost na objemové aktivitě v době měření, takže přesnost stanovení objemové aktivity klesá s aktivitou v době měření. Toto chování je očekávané a souvisí s výběrem maxima lokální průměrné hodnoty. Velikost maxima je dána mírou šumu a ta je určena počtem detekovaných impulsů. Stejné chování lze očekávat i u měření maxima SUVmax. Použití metody „peak“ nebo hledání maxima je tedy podmíněno srovnatelným šumem, resp. počtem detekovaných impulsů v obrazech. Metoda „peak“ také není vhodná při kvantifikaci malých objektů, protože tato metoda pracuje s lokálními průměry v kulovém objemu 1 cm3 (průměr koule 1,2 cm), takže u ložisek s menší velikostí dochází k započítání voxelů ležících mimo aktivní lézi a výsledek může být výrazně podhodnocený.
Nepřesnost stanovení hodnot SUV je dána nepřesností kalibrace a v laboratorních podmínkách pro SCACCT a manuální segmentaci činí 7,2 % pro lézi velikosti 25 mm a 2,6 % pro velké homogenní tkáně. Systematická chyba SUV je dána chybou kalibrace a chybou měřiče aktivity aplikované pacientovi a činí nejvíce 7,1 % při zanedbání chyby měření hmotnosti pacienta. Statistická chyba závisí na celkovém počtu impulsů nasbíraném ve studované ROI, tedy na celkové aplikované aktivitě a délce akvizice. Odhad statistické chyby je možné provést určením výběrové směrodatné odchylky ve studované ROI.
Zjištěné chyby jsou srovnatelné s hodnotami uváděnými v odborné literatuře.
Závěr
Pro křížovou kalibraci SPECT kamer pro kvantitativní hodnocení pomocí SUV hodnot je nutné dodržet akviziční a rekonstrukční parametry stejné jako při klinickém vyšetření, včetně kombinace korekcí. Jednotlivé citlivosti se mohou lišit i o stovky procent. Není vhodné používat hodnoty planárních citlivostí ani systémové tomografické citlivosti definované v NEMA. Celková chyba kalibračního koeficientu je dána zejména systematickou chybou měřiče aplikované aktivity ve studovaném detekčním řetězci a činila 5,1 %. Je nutné dbát na to, aby radiofarmakum bylo v kalibračním fantomu dobře rozmícháno.
V rozptylujícím a pohlcujícím prostředí je doporučeno použít korekci na zeslabení i korekci na rozptyl pomocí akvizice ve druhém energetickém okně, protože vykazuje ze všech korekcí nejvyšší přesnost pro všechny typy segmentací. Nejvyšší dosažené přesnosti činí 7,2 (± 10,7) % pro SCACCT a manuální segmentaci, 0,5 (± 8,0) % pro ACSCRR a automatickou segmentaci a 7,9 (± 8,3) % pro ACSC a metodu segmentace „peak“.
Nejvhodnější metodou segmentace z hlediska přesnosti a reprodukovatelnosti (tedy statistické chyby) se jeví automatická segmentace založená na prahování. Tam, kde není možné ji použít, je pro ložiska větší než 1,2 cm vhodná metoda „peak“, ale jen pro srovnávání pacientů s přibližně stejným počtem detekovaných impulsů a s uvážením její tendence nadhodnocovat výsledky.
Celková chyba hodnot SUV po křížové kalibraci provedené výše uvedeným způsobem byla dána systematickou chybou pocházející z měřících přístrojů 7,1 %, systematickou chybou v důsledku nepřesností korekčních metod a statistickou chybou závisející na nasbíraném počtu impulsů. Přesnost korekčních metod je rovna přesnosti stanovení objemové aktivity.
Pavel Karhan, Jaroslav Ptáček
Oddělení lékařské fyziky a radiační ochrany, LF UP a FN Olomouc, ČR
pavel.karhan@fnol.cz
Sources
1. Bailey DL, Willowson KP. Quantitative SPECT/CT: SPECT joins PET as a quantitative imaging modality. Eur J Nucl Med Mol Imaging 2014;41 Suppl 1:S17-25
2. Rosenthal MS, Cullom J, Hawkins W et al. Quantitative SPECT imaging: a review and recommendations by the Focus Committee of the Society of Nuclear Medicine Computer and Instrumentation Council. J Nucl Med 1195;36 : 1489-1513
3. Willowson K, Bailey DL, Baldock C. Quantitative SPECT reconstruction using CT-derived corrections. Phys Med Biol 2008;53 : 3099-3112
4. Buvat I. Quantification in emission tomography: Challenges, solutions, and performance. Nucl Instr Meth Phys Res A 2007;571 : 10–13
5. Frey EC, Humm JL, Ljungberg M. Accuracy and Precision of Radioactivity Quantification in Nuclear Medicine Images. Seminars in Nuclear Medicine 2012;42 : 208-218
6. Bailey DL, Willowson KP. An Evidence-Based Review of Quantitative SPECT Imaging and Potential Clinical Applications. J Nucl Med 2013; 54 : 83-89
7. Willowson K, Bailey DL, Schembri G et al. CT-based quantitative SPECT for the radionuclide 201Tl: experimental validation and a standardized uptake value for brain tumour patients. Cancer Imaging 2012;12 : 31–40
8. Karhan P, Ptáček J, Fiala P. Optimalizace rekonstrukčních parametrů pro SPECT a SPECT/CT. NuklMed 2015;4 : 66-72
9. DCMTK, OFFIS – Institute for Information Technology; verze 3.6.1 [online]. 2016. [cit. 2016-05-05]. Dostupné na: http://support.dcmtk.org/
10. Anděl J. Základy matematické statistiky – 3. vydání. Praha, Matfyzpress, 2011, 360 p
11. NEMA Standards Publication NU 1-2012: Performance Measurements of Gamma Cameras; National Electrical Manufacturers Association 2013, 60 p
Labels
Nuclear medicine Radiodiagnostics Radiotherapy
Article was published inNuclear Medicine

2017 Issue 1
Most read in this issue- Radiopharmaceuticals for imaging gliomas using positron emission tomography
- Estimation of the accuracy of SUV measurement on SPECT/CT GE Discovery 670
- Nuclear medicine remains independent medical specialty – what next?
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career