-
Medical journals
- Career
Populační screening kolorektálního karcinomu v České republice
Authors: prof. MUDr. Ph.D. Miroslav Zavoral 1; MUDr. Gabriela Vojtěchová 1; RNDr. Ph.D. Ondřej Májek 2; Mgr. Ondřej Ngo; MUDr. Tomáš Grega; doc. MUDr. Ph.D. Bohumil Seifert; doc. RNDr. Ph.D. Ladislav Dušek; MUDr. Ph.D. Štěpán Suchánek
Authors‘ workplace: Interní klinika 1. LF UK a ÚVN Praha 1; Institut biostatistiky a analýz Masarykovy univerzity v Brně 2; Ústav všeobecného lékařství 1. LF UK a VFN v Praze 3
Published in: Čas. Lék. čes. 2016; 155: 7-12
Category: Original Article
Overview
Kolorektální karcinom (KRK) je třetím nejčastějším zhoubným onemocněním ve vyspělých zemích a jeho incidence neustále narůstá. Tento trend má setrvalý charakter i přesto, že KRK patří mezi nejlépe prevencí ovlivnitelné malignity. Národní program screeningu KRK v České republice, zavedený v roce 2000, sleduje světové trendy vycházející z evidence based medicine. Aktuálně jsou jeho základními nástroji imunochemické testy na okultní krvácení do stolice (s kolonoskopií v případě jejich pozitivity) a screeningová kolonoskopie. Vzhledem ke stagnující účasti cílové populace bylo v lednu 2014 zavedeno cílené adresné zvaní, kdy jsou občané pravidelně vyzýváni k účasti na screeningu a jejich odezva je následně vyhodnocována. Screening, který takto organizovaně zasahuje celou cílovou populaci, nazýváme populační.
Klíčová slova:
kolorektální karcinom, populační screeningový program, kolonoskopie, testy na okultní krvácení, adresné zvaníÚvod
Kolorektální karcinom je genetické onemocnění vycházející z epitelových buněk tlustého střeva. Tzv. sporadická forma kolorektálního karcinomu tvoří cca 80–85 % všech KRK. Proces kancerogeneze, změna normální sliznice přes adenom na karcinom, trvá v průměru 8–10 let (1) a poskytuje nám dostatek času k odvrácení nepříznivé prognózy. V rámci screeningu lze premaligní léze detekovat, odstranit a zabránit tak vzniku zhoubného onemocnění nebo zachytit KRK v časném, snáze léčitelném stadiu. Populační screening kolorektálního karcinomu je program sekundární prevence usilující o včasný záchyt onemocnění v populaci (2).
Epidemiologie KRK
Kolorektální karcinom (KRK) představuje ve vyspělých zemích významný zdravotnický a socioekonomický problém. V Evropě je druhým nejčastějším zhoubným onemocněním u obou pohlaví (hned za karcinomem plic u mužů a karcinomem prsu u žen) a čtvrtou nejčastější příčinou úmrtí na malignitu (po karcinomu plic, jater a žaludku). V roce 2012 dosahovala celosvětová roční incidence tohoto onemocnění 1,4 milionu případů (3). Středoevropské země (Slovensko, Maďarsko, Česko) tradičně patřily mezi oblasti s nejvyšší incidencí a mortalitou na KRK v Evropě, s hodnotami dvoj - až trojnásobně vyššími než země s nejnižším výskytem (např. Bosna a Hercegovina, Řecko). Změna pro Českou republiku (ČR) nastala až v roce 2012, kdy byla sesazena ze 3. místa v obou ukazatelích na 9. příčku v mortalitě a 5. v incidenci tohoto zhoubného onemocnění (3).
Dle Národního onkologického registru (NOR) byl v ČR mezi lety 2002 a 2012 zaznamenán mírný vzestup incidence KRK (+0,8 %) při významném poklesu mortality (-15,1 %) (obr. 1). Tento trend s sebou přináší dramatický nárůst pacientů s anamnézou kolorektálního karcinomu (+55,3 %), které je třeba mj. kolonoskopicky dispenzarizovat. V roce 2012 bylo v ČR diagnostikováno 8336 nových případů KRK a 3628 úmrtí na toto onemocnění.
Image 1. Časový vývoj incidence a mortality KRK v ČR (zdroj: Národní onkologický registr [NOR], www.svod.cz) ![Časový vývoj incidence a mortality KRK v ČR (zdroj: Národní onkologický registr [NOR], www.svod.cz)](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/27f3d31c484be42d383bb64f8b01dac9.png)
Prognóza pacientů je závislá na stadiu onemocnění v době diagnózy. Od roku 2000 do roku 2010 vzrostl záchyt KRK ve stadiu I ze 16 na 24 % (obr. 2). Tato epidemiologická data jsou důkazem efektivního screeningu KRK v ČR. Typický věk českého pacienta s kolorektálním karcinomem leží v intervalu 63–77 let. Téměř čtvrtina jedinců je však v době diagnózy mladší 60 let. Celoživotní riziko vzniku KRK nezanedbatelně stoupá na začátku 6. decenia, proto je screening KRK v ČR zaměřen na bezpříznakové jedince starší 50 let.
Image 2. Podíl klinických stadií KRK v ČR (zdroj: Národní onkologický registr) 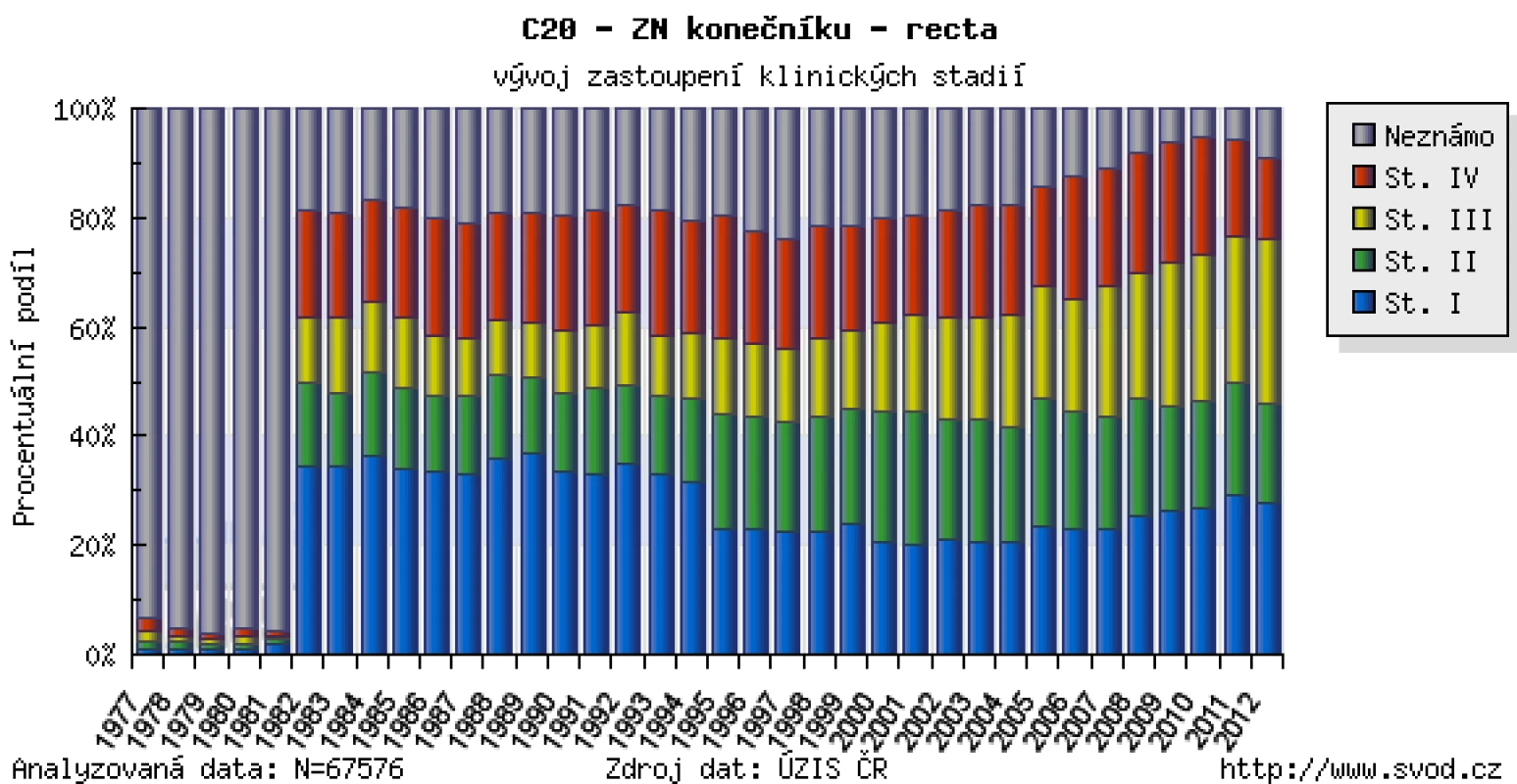
Prevence KRK
Primární prevence spočívá v úpravě jídelníčku a životosprávy. Sekundární prevence zahrnuje dvě metody: screening (časné rozpoznání nemoci u asymptomatických jedinců) a surveillance vysokorizikových skupin (dispenzarizace). Screening je zaměřen na záchyt tzv. sporadického kolorektálního karcinomu, jehož nejvýznamnějším rizikovým faktorem je neovlivnitelný endogenní faktor – věk.
Screening KRK
Cílem screeningu KRK je zvýšení četnosti záchytu zhoubných nádorů kolorekta, tzv. pokročilého adenomu, a dále zvýšení podílu časných stadií KRK na úkor stadií pokročilých. Očekávaným výstupem je redukce incidence a mortality KRK. Bylo prokázáno, že stanovení časné diagnózy KRK u asymptomatického jedince je spojeno s 90% pravděpodobností 5letého přežití. V případě trvání symptomů 3 měsíce nebo 7 měsíců dochází k poklesu pravděpodobnosti pětiletého přežití na 40, resp. 25 % (4).
Klíčovým bodem screeningových programů je dosažení co největšího pokrytí cílové populace. Z tohoto důvodu je preferován organizovaný celoplošný populační screeningový program založený na včasné identifikaci a následném cíleném pozvání každého jedince k provedení screeningu (5).
Screeningové metody
Obecně rozlišujeme screeningové programy jednoetapové a dvouetapové. Jednoetapové programy spočívají v provádění samotné screeningové kolonoskopie (6), flexibilní sigmoideoskopie (7, 8) nebo CT kolonografie (9). Dvouetapové screeningové programy využívají testy na okultní krvácení do stolice (TOKS) a kolonoskopii, která následuje po pozitivním TOKS.
Testy na okultní krvácení do stolice
TOKS je neinvazivní vyšetření, které detekuje pouhým okem neviditelné stopy krve ve stolici. Adenomové polypy krvácejí sporadicky a polypy menší než 15 mm nekrvácejí prakticky vůbec. K detekci signifikantní kolorektální neoplazie je tedy nezbytné pravidelné opakování vyšetření. V současné době máme k dispozici dva hlavní typy TOKS:
Guajakový test (gTOKS) je založen na peroxidázové reakci, která je zatížena falešnou pozitivitou (např. po pozření červeného masa) i falešně negativními výsledky (např. po užití vitaminu C). Vyšetření tedy musí předcházet dieta s omezením určitých potravin. Výhodou gTOKS je kromě nízkých nákladů a snadné manipulace i randomizovanými studiemi prokázané snížení mortality na KRK o 15–21 % při dvouletém a o 33 % při ročním intervalu (10).
Imunochemické TOKS (fecal immunochemical test [FIT]) jsou založené na přímé detekci lidského hemoglobinu a nemocní se před vyšetřením nemusejí dietně omezovat. Nedávno publikované studie prokázaly vyšší senzitivitu FIT pro kolorektální neoplazii a vyšší compliance cílové populace oproti gTOKS (11, 12). Rozlišujeme kvalitativní, semikvantitativní a kvantitativní FIT. Je známo, že fyziologická koncentrace fekálního hemoglobinu závisí na věku a pohlaví. Většina studií preferuje nastavit pozitivní hodnotu testů (tzv. cut-off) v rozmezí od 75 do 100 ng/l (13).
Kolonoskopie
Kolonoskopie je považována za zlatý standard screeningu KRK, i když dosud nebyla provedena randomizovaná studie potvrzující snížení mortality KRK pomocí této metody. Randomizované studie prokázaly snížení mortality KRK o 43 % a vyšší compliance pacientů v porovnání s kolonoskopií při použití flexibilní sigmoideoskopie (14, 15).
Pankolonoskopie byla prováděná jen v případě nálezu adenomu většího než 10 mm, s tubulovilózní či vilózní složkou, nebo při nálezu mnohočetných adenomů. Alternativní metody (CT kolonografie, kolonická kapsle, molekulární testování) se pro nedostatečný průkaz efektivity a finanční nákladnost zatím nestaly rutinní součástí evropských screeningových programů.
Screening KRK v ČR
Screening KRK má v České republice letitou tradici. Již v roce 2000 byl v ČR (jako v pořadí 2. zemi na světě) zahájen národní program screeningu KRK u asymptomatických jedinců. Bezpříznakovým jedincům od 50 let věku byl nabídnut guajakový test na okultní krvácení do stolice, následovaný kolonoskopií v případě jeho pozitivity. Vzhledem ke zvyšujícím se nárokům na kvalitu programu byla v roce 2006 vytvořena ve spolupráci s Institutem biostatistiky a analýz Masarykovy univerzity v Brně (IBA) on-line databáze (Registr screeningových kolonoskopií) založená na sběru anonymně individuálních dat. Údaje zde uložené slouží ke kontrole kvality screeningového programu.
Počátkem roku 2009 došlo k úpravě programu zavedením imunochemických testů na okultní krvácení do stolice (FIT) a jednostupňového screeningu v podobě screeningové kolonoskopie. Asymptomatickým jedincům ve věku od 50 do 54 let je nyní nabízen test na okultní krvácení do stolice (TOKS) v jednoročním intervalu. V případě jeho pozitivity následuje TOKS + kolonoskopie. Od 55 let věku byla zavedena možnost volby testu na okultní krvácení do stolice ve dvouletém intervalu nebo screeningové kolonoskopie, která může být zopakována v intervalu deseti let. Současně byla vytvořena široká národní síť specializovaných pracovišť pro screeningovou kolonoskopii. Do screeningu jsou od roku 2009 kromě praktických lékařů a gastroenterologů zapojeni také ambulantní gynekologové.
Národní program screeningu kolorektálního karcinomu prochází kontinuálním vývojem. Od roku 2013 dochází – v souladu s nejnovějšími poznatky – k útlumu gTOKS a postupnému přechodu na FIT. Využívané jsou všechny typy FIT bez stanovení jednotné mezní hodnoty (cut-off).
Populační screening
Ani sebelepší preventivní program není funkční, pokud se do něj nezapojí cílová skupina občanů. Zavedením imunochemických testů na okultní krvácení do stolice, screeningové kolonoskopie a zapojením ambulantních gynekologů došlo v roce 2013 k nárůstu pokrytí cílové populace na 26,5 % (obr. 3). Dle Evropských doporučení je však pro signifikantní změnu incidence a mortality KRK nezbytná účast minimálně 45 % (optimálně až 65 %) obyvatel (16).
Image 3. Celkové pokrytí cílové populace screeningovým programem 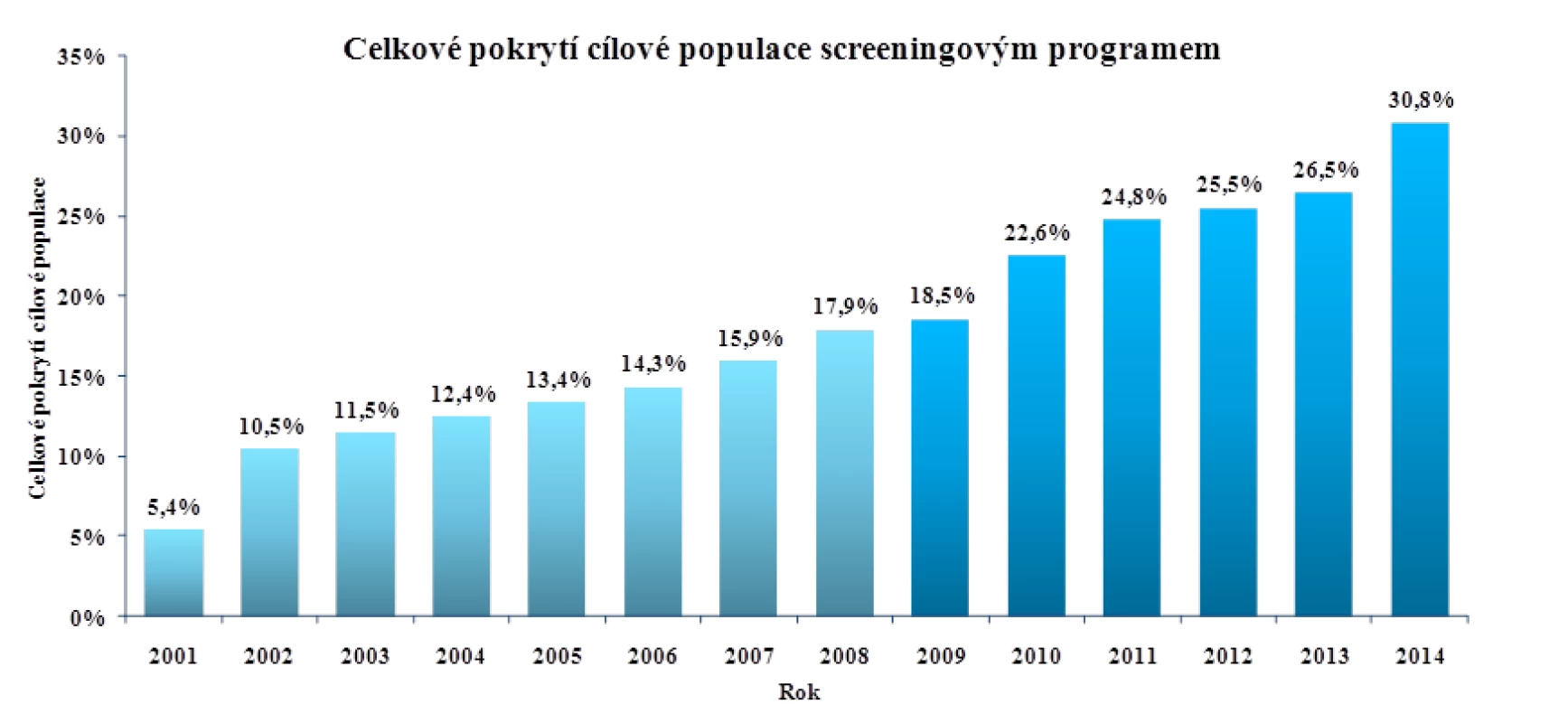
Ve snaze o zvýšení adherence cílové populace byl v lednu 2014 změněn stávající oportunní screeningový program na populační, a to zavedením státem organizovaného adresného zvaní. Občané jsou svými zdravotními pojišťovnami korespondenčně vyzýváni k participaci na screeningu KRK a ženy též na screeningu nádorů hrdla děložního a nádorů prsu. Program zvaní je koordinován Ministerstvem zdravotnictví ČR ve spolupráci s plátci zdravotní péče a s odbornými lékařskými společnostmi.
Pojištěnec ve věku 50–70 let je pozván k účasti na kolorektálním screeningu, pokud splňuje následující požadavky: nebyl léčen pro KRK, neabsolvoval v posledních 3 letech TOKS či v posledních 5 letech preventivní kolonoskopii, nebyl u něj v minulosti (nebo minimálně v posledních 4 letech) vykázán terapeutický endoskopický či chirurgický výkon, nebyl léčen pro KRK a je pojištěncem dané zdravotní pojišťovny alespoň čtyři roky. Pokud se zvaný pojištěnec do screeningu nezapojil (tzn. nebyl u něj vykázán příslušný screeningový kód), je pozván opakovaně.
Další inovací programu, zavedenou od roku 2015, je změna úhrady preventivních kolonoskopií (zvýšení ocenění výkonu a režie, úhrada nad rámec regulace a prodloužení času výkonu).
Výsledky screeningového programu KRK
Od zavedení on-line sběru individuálních dat v roce 2006 do října 2015 bylo v rámci screeningu KRK provedeno (resp. dosud do on-line databáze zadáno) 191 082 kolonoskopií, 154 996 z nich bylo TOKS-pozitivních a 36 086 tzv. screeningových (tab. 1).
Table 1. Výsledky kolonoskopických vyšetření v ČR dle indikace (zdroj: Registr screeningových kolonoskopií) 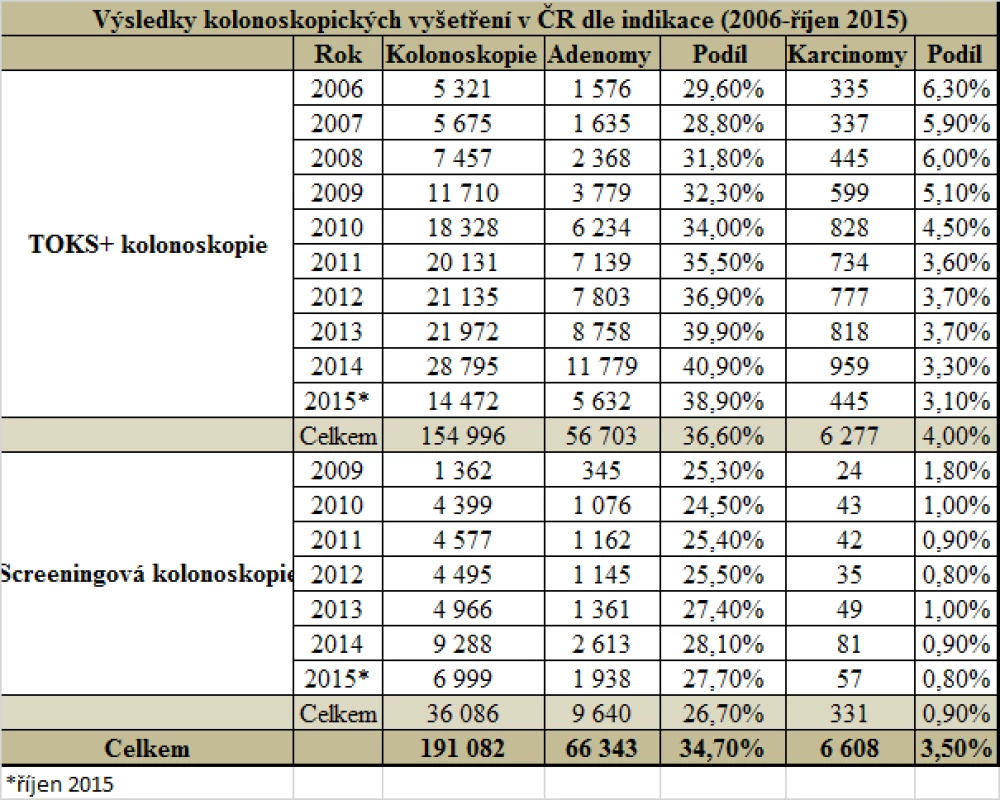
Jedním z indikátorů kvality kolonoskopie je adenoma detection rate (ADR), tedy podíl pacientů, u kterých byl diagnostikován adenomový polyp. U TOKS-pozitivní kolonoskopie činí ADR za výše uvedené období 36,6 % (celkem 56 703 jedinců s adenomy), u screeningové kolonoskopie pak 26,7 % (celkem 9640 jedinců). Tab. 1 dále dokládá postupné zvyšování ADR u TOKS-pozitivní kolonoskopie (z 29,6 % v roce 2006 na 40,9 % v roce 2014). Polská studie prokázala spojitost mezi ADR konkrétního endoskopisty a rizikem intervalového karcinomu. Hodnota ADR by neměla být nižší než 20 % (17).
U 6608 pacientů (3,5 %) byl v rámci screeningového programu nalezen karcinom. V detekci karcinomů je – na rozdíl od adenomů – patrný sestupný trend. Dochází ke snížení podílu pacientů s KRK z 6,3 % v roce 2006 na 2,7 % v roce 2014 (tab. 2). Následující tab. 3 dokládá vysokou kvalitu preventivních kolonoskopií v Česku, která obstojí i v mezinárodním srovnání.
Table 2. Přehledné výsledky screeningu KRK (zdroj: Registr screeningových kolonoskopií) 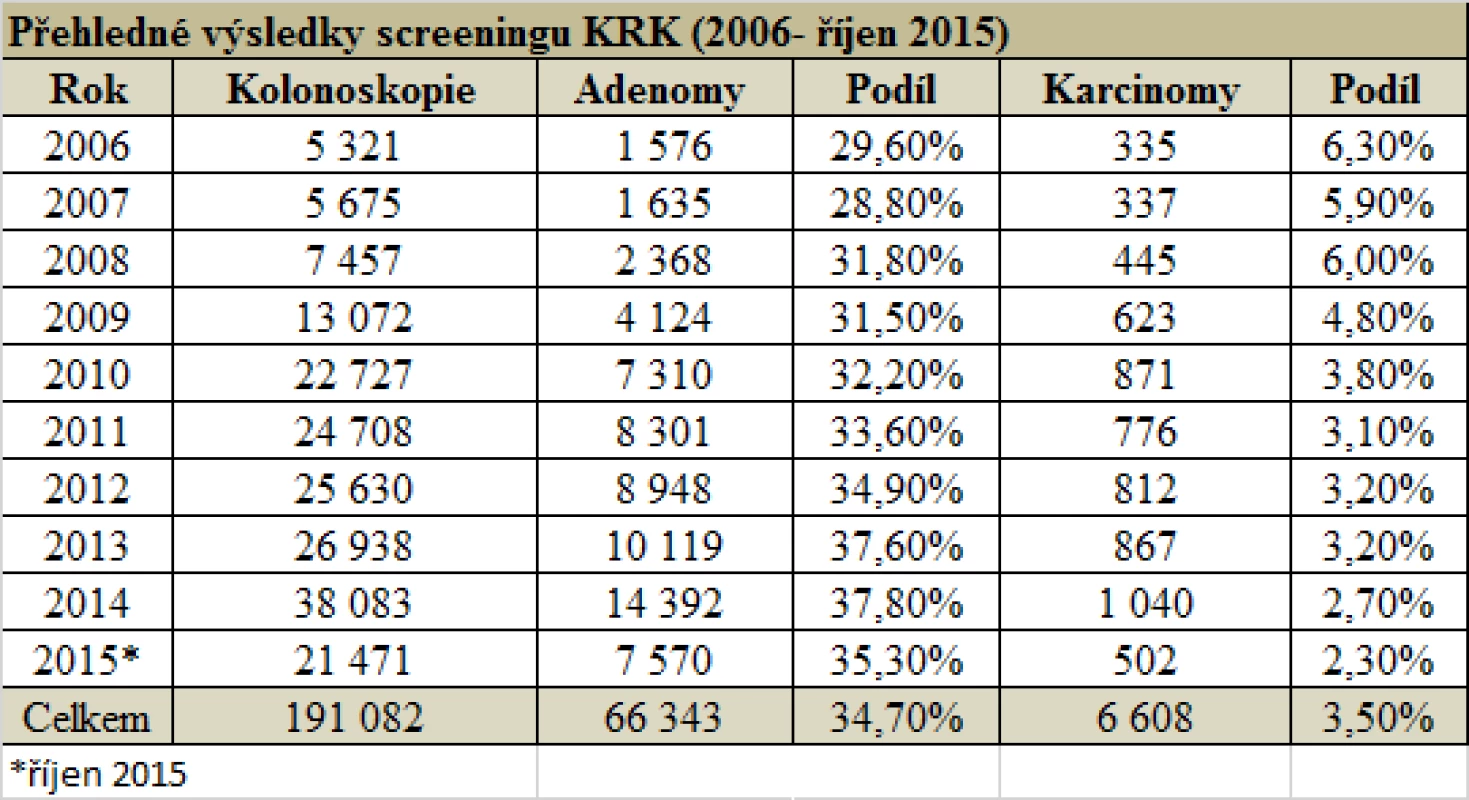
Table 3. Srovnání českého programu s doporučeními EU (2006–2014) (zdroj: Registr screeningu KRK a Evropská doporučení pro screening KRK) 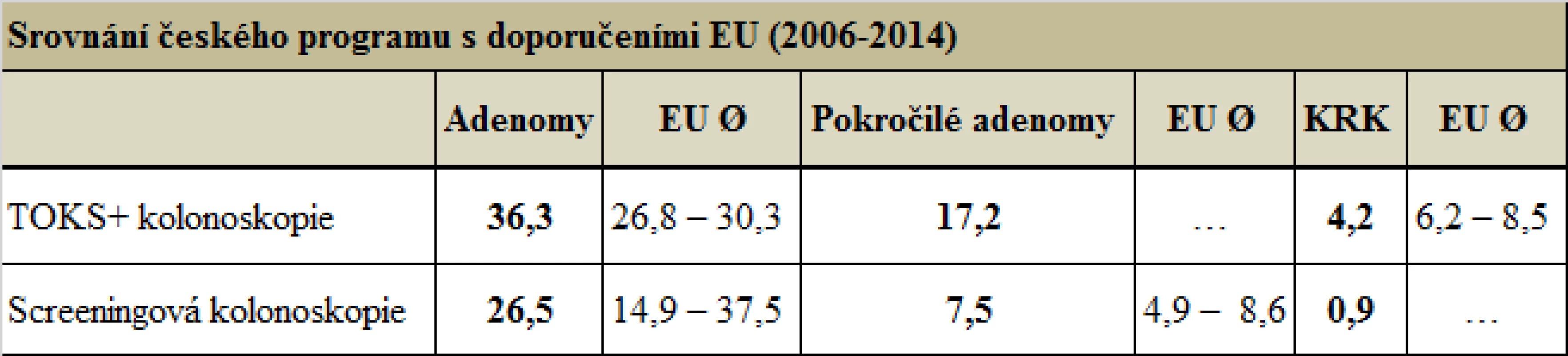
Adresné zvaní − výsledky
Během prvního roku působení populačního screeningu KRK bylo osloveno 1 500 897 jedinců, tedy 52,7 % cílové populace (obr. 4). Na pozvání k participaci na screeningovém programu zareagovala téměř pětina osob (17,3 %) absolvováním TOKS či screeningové kolonoskopie (obr. 5). Ve druhé polovině roku 2014 obdrželo 95 097 pojištěnců druhý zvací dopis, na základě kterého se více než desetina (11,8 %) dostavila k vyšetření. Zavedením institutu adresného zvaní došlo k vzestupu pokrytí cílové populace o 4,3 % oproti roku 2013 (obr. 3) a bylo dosaženo historicky nejvyšší účasti za dobu působení programu (30,8 %). Mezi lety 2013 a 2014 byl dále zaznamenán nárůst vyšetření TOKS o 30 % a screeningových kolonoskopií o 87 % (tab. 1).
Image 4. Adresné zvaní, poprvé pozvaní pojištěnci v roce 2014 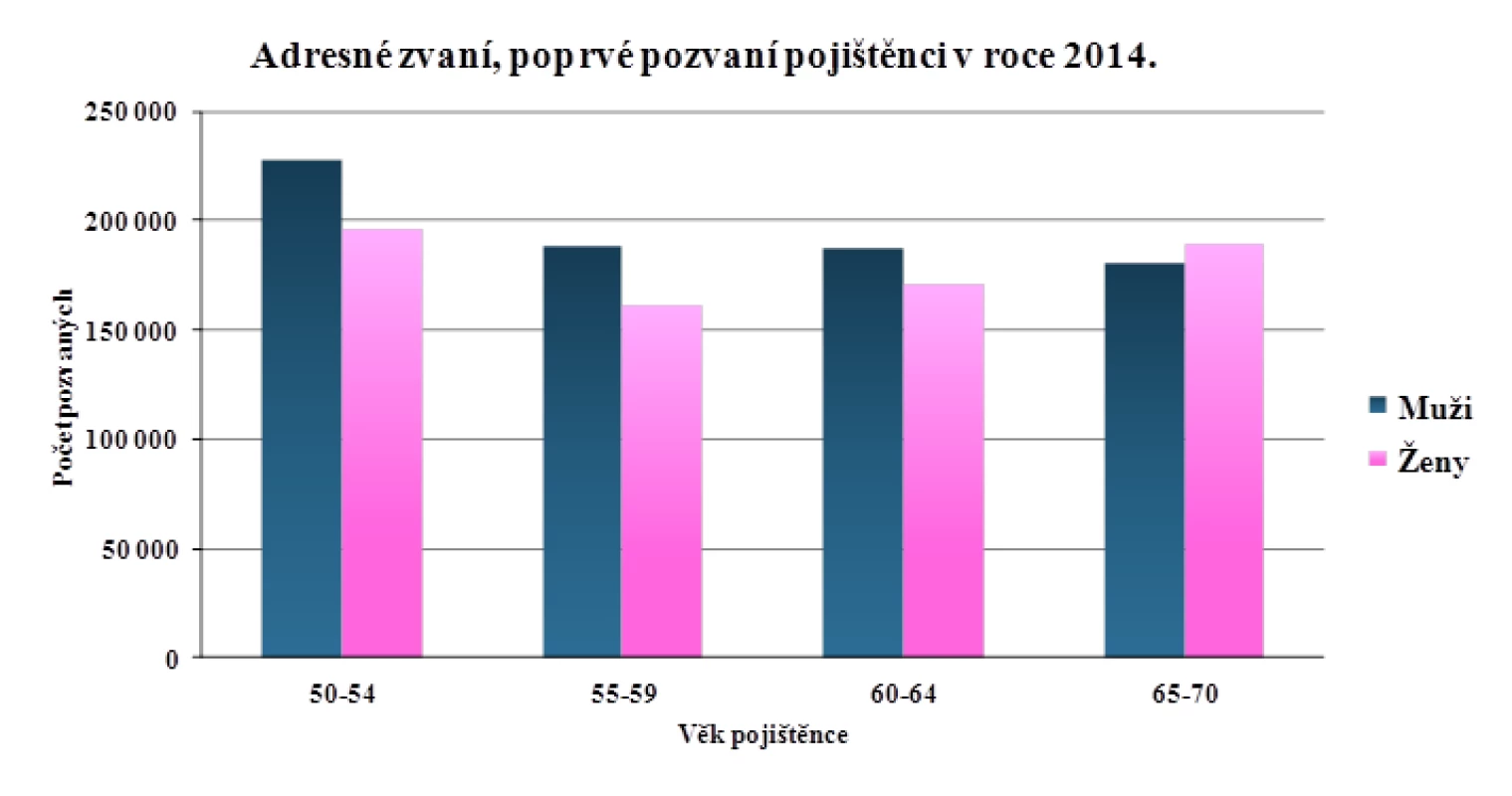
Image 5. Míra účasti po adresném zvaní u poprvé pozvaných pojištěnců 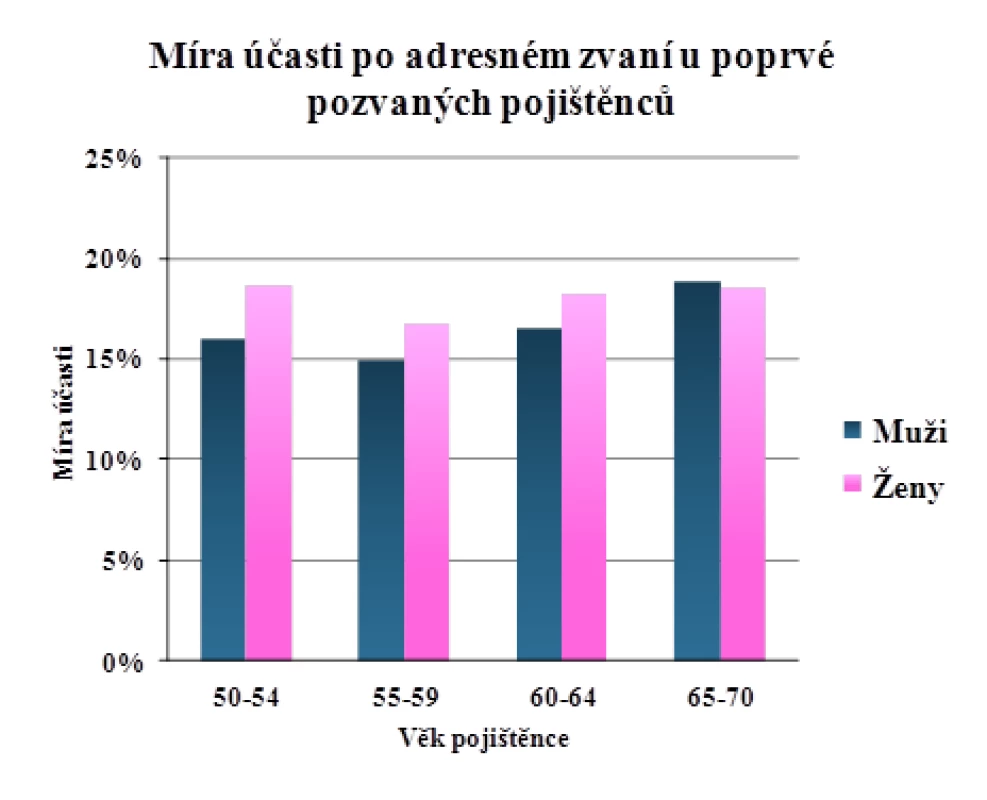
Díky adresnému zvaní bylo v roce 2014 detekováno o 42 % více adenomů a o 20 % více karcinomů než v předchozím roce. O pozitivním vlivu na konkrétního jednotlivce, kterému byl časně diagnostikován KRK nebo bylo odstraněním adenomu zabráněno jeho vzniku, není pochyb. Z populačního hlediska je však adherence cílové populace ke screeningu KRK stále suboptimální a nelze zatím očekávat významný vliv na incidenci a mortalitu tohoto zhoubného onemocnění. Mezi faktory, které jsou obecně spojeny s nižší adherencí, patří mužské pohlaví, mladší věk, nižší vzdělání a příslušnost k etnické menšině (16).
Budoucnost screeningu KRK
Mezi hlavní výzvy screeningového programu patří navýšení účasti cílové populace. Cest k úspěchu je hned několik: zvýšení akceptability a senzitivity vyšetření, modifikace dosavadních screeningových metod, eventuálně využití metod nových.
Španělská multicentrická randomizovaná studie Colon Prev porovnává FIT ve dvouletém intervalu se screeningovou kolonoskopií. Dle předběžných výsledků jsou obě metody ekvivalentní v detekci KRK (shodně 0,1 %), kolonoskopie lépe zachycuje pokročilé adenomy (1,9 vs. 0,9 %) a adenomy (4,2 vs. 0,4 %). Na druhou stranu jedinci zařazení do skupiny FIT se ochotněji zapojovali do screeningu (18).
Dosavadní screeningové metody se neustále vyvíjejí. V ČR již dochází k postupné náhradě guajakových TOKS imunochemickými. Důvodem je vyšší senzitivita a specificita FIT pro adenomy i KRK, vyšší akceptabilita cílovou populací a možnost nastavení cut-off s ohledem na věk a pohlaví jedince (19). Dalším krokem by mohlo být zavedení tzv. kombinovaných fekálních testů, které detekují lidský hemoglobin a zároveň abnormální DNA ve stolici. Kombinované testy se vyznačují vyšší senzitivitou (92,3 vs. 73,8 % u FIT), ale zatím nižší specificitou (86,6 vs. 94,9 % u FIT) (20).
Kapslová kolonoskopie (KK) druhé generace, se senzitivitou a specificitou pro diagnostiku kolorektální neoplazie (88, resp. 99 %), se zdá být přijatelnou screeningovou metodou pro cílovou populaci (21). V irské prospektivní studii byla kolonická kapsle použita u screeningové populace s pozitivním FIT. Tento druhý „filtr“ snížil nutnost kolonoskopie o 71 % (22). V současné době probíhají dvě randomizované studie zkoumající využití CT kolonografie v první linii screeningu KRK v porovnání s FIT a s flexibilní sigmoideoskopií.
Dle recentních studií se zdá, že pacienti s metabolickým onemocněním, zejména diabetici 2. typu, a nemocní s ICHS mohou mít vyšší riziko kolorektální neoplazie (23). Proto od roku 2013 probíhá v ČR multicentrická prospektivní studie s cílem ověření tohoto předpokladu v české populaci a s možností využití těchto výsledků ve screeningovém programu KRK (24). Na základě retrospektivní analýzy rizikových faktorů KRK (věk, pohlaví, pozitivní rodinná anamnéza, nikotinismus, BMI ≥ 30 kg/m2) u screeningové populace ve věku 40–66 let bylo stanoveno skóre pravděpodobnosti detekce kolorektální neoplazie (25). Úprava programu dle individuálního rizika vzniku sporadického KRK se zdá být tou správnou cestou, po které se screeningový program v budoucnu vydá.
Závěr
Screening kolorektálního karcinomu má klíčovou úlohu v kontrole incidence a mortality na toto onemocnění. Jeho efektivita závisí na dostatečné účasti cílové populace. Již v prvním roce po zavedení adresného zvaní došlo k nárůstu počtu screeningových výkonů a zvýšení detekce kolorektální neoplazie. Výhledově předpokládáme modifikaci screeningového programu dle individuálního rizika kolorektální neoplazie a zavedení méně invazivních screeningových metod.
Podpořeno grantem IGA MZ ČR NT 13673.
Adresa pro korespondenci
prof. MUDr. Miroslav Zavoral, Ph.D.
Interní klinika 1. lékařské fakulty UK a Ústřední vojenské nemocnice − Vojenské fakultní nemocnice
U Vojenské nemocnice 1200
169 02 Praha 6
Tel.: 973 203 061
e-mail: miroslav.zavoral@uvn.cz
Sources
1. Conteduca V, Sansonno D, Russi S et al. Precancerous colorectal lesions (Review). Int J Oncol 2013; 43 : 973–984.
2. Dušek L, Májek O, Blaha M, Daneš J, Zavoral M et al. Koncepce populačního screeningu v České republice, metodika a první výsledky adresného zvaní občanů do preventivních onkologických programů. Klin Onkol 2014; 27 (Suppl 2): 2S59–2S68.
3. Ferlay J, Soerjomataram I, Ervik M et al. Globocan 2012 v1.0, cancer incidence and mortality worldwide: IARC CancerBase No. 11 [Internet]. International Agency for Research on Cancer, Lyon, 2013. URL: http://globocan.iarc.fr
4. Deyhle P. Colonic cancer-diagnosis, check-up, prevent. Internist (Berl) 1979; 20 : 39–43.
5. Zavoral M, Suchánek S, Závada F et al. Colorectal cancer screening in Europe. World J Gastroenterol 2009; 15 : 5907–5915.
6. Brenner H, Hoffmeister M, Brenner G et al. Expected reduction of colorectal cancer incidence within 8 years after introduction of the German screening colonoscopy programme: estimates based on 1,875,708 screening colonoscopies. Eur J Cancer 2009; 45 : 2027–2033.
7. Schoen RE, Pinsky PF, Weissfeld JL et al. Colorectal-cancer incidence and mortality with screening flexible sigmoidoscopy. N Engl J Med 2012; 366 : 2345–2357.
8. Atkin W, Kralj-Hans I, Wardle J et al. Colorectal cancer screening. Randomised trials of flexible sigmoidoscopy. BMJ 2010; 341: c4618.
9. Johnson CD, Chen MH, Toledano AY et al. Accuracy of CT colonography for detection of large adenomas and cancers. N Engl J Med 2008; 359 : 1207–1217.
10. Mandel JS, Bond JH, Church TR et al. Reducing mortality from colorectal cancer by screening for fecal occult blood. Minnesota Colon Cancer Control Study. N Engl J Med 1993; 328 : 1365–1371.
11. Rabeneck L, Rumble RB, Thompson F et al. Fecal immunochemical tests compared with guaiac fecal occult blood tests for population-based colorectal cancer screening. Can J Gastroenterol 2012; 26 : 131–147.
12. Bowyer HL, Vart G, Kralj-Hans I et al. Patient attitudes towards faecal immunochemical testing for haemoglobin as an alternative to colonoscopic surveillance of groups at increased risk of colorectal cancer. J Med Screen 2013; 20 : 149–156.
13. Nakama H, Zhang B, Zhang X. Evaluation of the optimum cut-off point in immunochemical occult blood testing in screening for colorectal cancer. Eur J Cancer 2001; 37 : 398–401.
14. Atkin WS, Edwards R, Kralj-Hans I et al. Once-only flexible sigmoidoscopy screening in prevention of colorectal cancer: a multicentre randomised controlled trial. Lancet 2010; 375 : 1624–1633.
15. Robb K, Power E, Kralj-Hans I et al. Flexible sigmoidoscopy screening for colorectal cancer: uptake in a population-based pilot programme. J Med Screen 2010; 17 : 75–78.
16. Segnan N, Patnick J, Von Karsa L. European guidelines for quality assurance in colorectal cancer screening and diagnosis (1st ed.). European Union, 2010 : 206–232.
17. Kaminski MF, Regula J, Kraszewska E et al. Quality indicators for colonoscopy and the risk of interval cancer. N Engl J Med 2010 May 13; 362(19): 1795–1803.
18. Quintero E, Castells A, Bujanda L et al. Colonoscopy versus fecal immunochemical testing in colorectal-cancer screening. N Engl J Med 2012 Feb 23; 366(8): 697–706.
19. van Rossum LG, van Rijn AF, Laheij RJ et al. Random comparison of guaiac and immunochemical fecal occult blood tests for colorectal cancer in a screening population. Gastroenterology 2008 Jul; 135(1): 82–90.
20. Imperiale TF, Ransohoff DF, Itzkowitz SH et al. Multitarget stool DNA testing for colorectal-cancer screening. N Engl J Med 2014 Apr 3; 370(14): 1287–1297.
21. Zavoral M, Májek O, Tachecí I, Beneš M, Drastich P, Vojtěchová G et al. Porovnání účinnosti kolonické kapslové endoskopie a kolonoskopie v detekci polypů a karcinomů tlustého střeva a konečníku – multicentrická, prospektivní, cross-over studie. Gastroent Hepatol 2014; 68(3): 218–224.
22. Holleran G, Leen R, O'Morain C et al. Colon capsule endoscopy as possible filter test for colonoscopy selection in a screening population with positive fecal immunology. Endoscopy 2014 Jun; 46(6): 473–478.
23. Krämer HU, Müller H, Stegmaier C et al. Type 2 diabetes mellitus and gender-specific risk for colorectal neoplasia. Eur J Epidemiol 2012; 27 : 341–347.
24. Suchánek Š, Májek O, Grega T, Ngo O, Mináriková P, Brogyuk N, Seifert B, Dušek L, Zavoral M. Cílený screening kolorektálního karcinomu u diabetiků 2. typu a osob s vysokým kardiovaskulárním rizikem – první průběžné výsledky multicentrické prospektivní studie. Gastroent Hepatol 2014; 68(5): 411–416.
25. Kaminski MF, Polkowski M, Kraszewska E et al. A score to estimate the likelihood of detecting advanced colorectal neoplasia at colonoscopy. Gut 2014 Jul; 63(7): 1112–1119.
Labels
Addictology Allergology and clinical immunology Angiology Audiology Clinical biochemistry Dermatology & STDs Paediatric gastroenterology Paediatric surgery Paediatric cardiology Paediatric neurology Paediatric ENT Paediatric psychiatry Paediatric rheumatology Diabetology Pharmacy Vascular surgery Pain management Dental Hygienist
Article was published inJournal of Czech Physicians

-
All articles in this issue
- Populační screening kolorektálního karcinomu v České republice
- Nové zobrazovací metody v endoskopické diagnostice nádorů trávicího ústrojí
- Onemocnění horní části trávicího traktu: zhoubná onemocnění foregutu
- Maligní biliární obstrukce
- Karcinom pankreatu – současný efektivní diagnosticko-terapeutický postup
- Časná detekce sporadického karcinomu pankreatu
- Vyšetření mutace KRAS v EUS-FNA preparátech pacientů s tumorem pankreatu
- Prognostický význam ART skóre u pacientů s intermediárním hepatocelulárním karcinomem
- Prof. MUDr. Josef Marek, DrSc., osmdesátiletý
- Za profesorem Vratislavem Schreiberem
- Journal of Czech Physicians
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Karcinom pankreatu – současný efektivní diagnosticko-terapeutický postup
- Maligní biliární obstrukce
- Onemocnění horní části trávicího traktu: zhoubná onemocnění foregutu
- Populační screening kolorektálního karcinomu v České republice
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

