-
Medical journals
- Career
Prognostický význam ART skóre u pacientů s intermediárním hepatocelulárním karcinomem
Authors: MUDr. Petr Hříbek; MUDr. Kristýna Kubíčková; MUDr. Hana Parobková; Ing. Ph.D. Nikola Kaspříková; prof. MUDr. Petr Urbánek Csc
Authors‘ workplace: Interní klinika 1. LF UK a ÚVN Praha: U Vojenské nemocnice 1 00, Praha 6, 169 0 1; Radiodiagnostické oddělení ÚVN Praha: U Vojenské nemocnice 1200, Praha 6, 169 2; Oddělení biomedicínské statistiky 1. LF UK Praha 3
Published in: Čas. Lék. čes. 2016; 155: 52-55
Category: Original Article
Overview
Pacienti s hepatocelulárním karcinomem (HCC) ve stadiu B dle barcelonské klasifikace (BCLC) jsou indikováni k paliativní transarteriální chemoembolizaci jakožto metodě volby. Tato skupina pacientů je velice široká a heterogenní. Pro lepší diferenciaci těchto nemocných a racionalizaci indikace druhé etapy transarteriální chemoembolizace bylo navrženo skóre ART.
Cílem následující práce bylo prokázat, že skóre ART umožňuje ve skupině pacientů s HCC ve stadiu BCLC-B definovat podskupiny s významně lepším a horším celkovým přežitím (OS) při opakované léčbě transarteriální chemoembolizací. Jedná se o kombinovanou retrospektivně prospektivní studii OS kohorty pacientů s HCC ve stadiu B dle klasifikace BCLC sledovaných a léčených na Interní klinice 1. LF UK a ÚVN v Praze. Byla provedena analýza křivky přežití s využitím Kaplanovy-Meierovy metody odhadu. Výpočty byly provedeny v softwaru R.
Medián OS zkoumaného souboru činil 18 měsíců (95% CI 12–33), medián OS skupiny s příznivým skóre ART dosáhl 33 měsíců (95% CI 17–36), medián OS skupiny s prognosticky nepříznivým skóre ART pak byl 12 měsíců (95% CI 6–18). Rozdíl OS mezi skupinami diferencovanými dle skóre ART byl statisticky významný (p < 0,01). Vzhledem k takto významnému rozdílu OS pacientů diferencovaných dle skóre ART je třeba se zabývat případnou revizí současných doporučených postupů léčby nemocných ve stadiu B dle klasifikace BCLC.Klíčová slova:
hepatocelulární karcinom, transarteriální chemoembolizace, cirhózaÚvod
Hepatocelulární karcinom (HCC) je nejčastějším primárním zhoubným nádorem jater, jeho incidence navíc celosvětově roste. V současné době je v globálním měřítku třetí nejčastější příčinou úmrtí na nádorové onemocnění a v převážné většině případů se rozvíjí v terénu jaterní cirhózy jakékoli etiologie (1). Klinicky všeobecně respektovaným a užívaným klasifikačním systémem pro HCC je klasifikace BCLC (Barcelona Clinic Liver Cancer) (obr. 1).
Image 1. Barcelona Clinic Liver Cancer klasifikace (2) 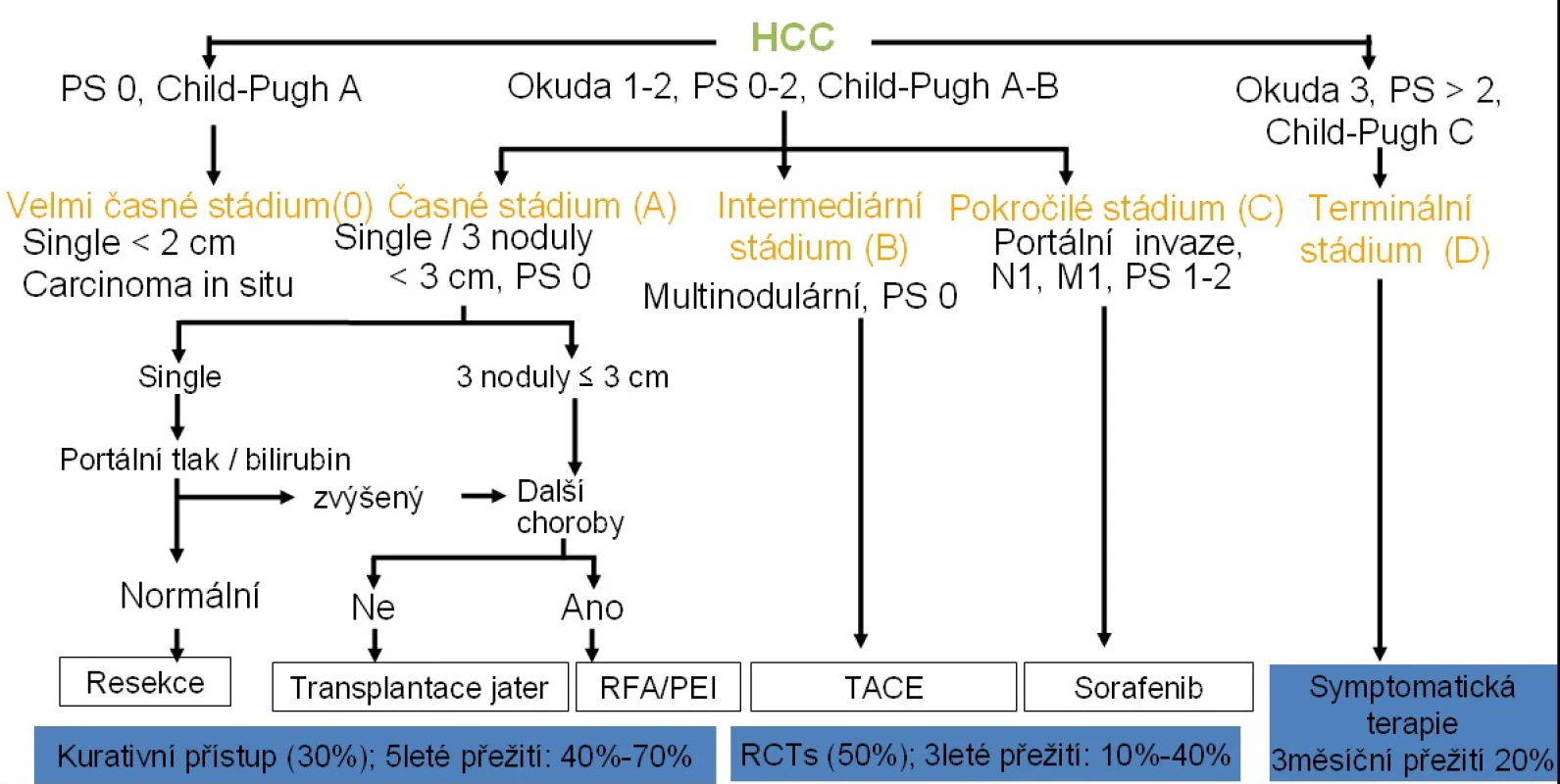
Staging dle této klasifikace přímo determinuje způsob léčby. Pouze přibližně třetina pacientů se ve chvíli diagnózy nachází ve velmi časném a časném stadiu (0 nebo A), a jsou tak kandidáty chirurgické, potenciálně kurativní léčby (2). Pro intermediární stadium (BCLC-B) je terapií volby transarteriální chemoembolizace (TACE, resp. DEB-TACE − viz dále) (3). Konvenční TACE (cTACE) je radiontervenční metoda paliativní léčby pacientů s hypervaskularizovanými jaterními ložisky, kdy je do nutritivní tepny nádoru aplikována emulze cytostatika s lipiodolem. Tato léčba kombinuje efekt ischemizace ložiska a dosažení vysoké lokální koncentrace cytostatika v něm (4). Jako cytostatikum se v terapii HCC užívá v současné době doxorubicin (5). DEB-TACE používá k tomuto účelu mikrosféry z hydrogelu, na které je přímo doxorubicin navázán (drug eluting beads [DEB]). Výhodou metody DEB-TACE oproti cTACE je prokázané nižší riziko systémových nežádoucích účinků cytostatika a vyšší standardizace metody (6).
Stadium B představuje velice širokou, heterogenní skupinu pacientů. Do této skupiny řadíme pacienty, kteří velikostí nádoru nebo počtem ložisek nesplňují kritéria stadia 0 nebo A. Další podmínkou je absence extrahepatálního postižení HCC, pacienti musejí být v celkově dobrém výkonnostním stavu (performance status [PS] = 0), s dobře zachovanou funkční zdatností jater (maximálně Child-Pugh B, 7 bodů, bez ascitu) (2). Extrémním protipólem tak může být na straně jedné nemocný, který jen mírně překračuje kritéria transplantace a chirurgické resekce, a naproti tomu pacient s mnohočetným bilobárním postižením na samé hranici technické proveditelnosti TACE.
Je snahou tyto nemocné lépe rozdělit a predikovat u nich profit z provedení, respektive neprovedení další etapy transarteriální chemoembolizace. K tomuto účelu bylo rakouskými autory navrženo skóre ART (Assessment for Retreatment with TACE) (7). Tento skórovací systém hodnotí efektivitu první etapy transarteriální chemoembolizace a umožňuje v rámci skupiny pacientů ve stadiu B vyčlenit 2 skupiny s významným rozdílem v celkovém přežívání (overall survival [OS]). Bezprostředně před provedením druhého cyklu transarteriální chemoembolizace se hodnotí 3 veličiny: radiologická odpověď na předchozí TACE, vzestup aktivity aspartátaminotransferázy oproti výchozím hodnotám a změna v Childově-Pughově skóre (tab. 1). Klinicky širokou škálou pacientů ve stadiu B jsou vysvětlovány velké rozdíly v celkovém přežívání v rámci různých souborů pacientů léčených TACE (tab. 2) (8).
Table 2. Značně rozdílné přežívání mezi různými soubory pacientů stadia B dle klasifikace BCLC 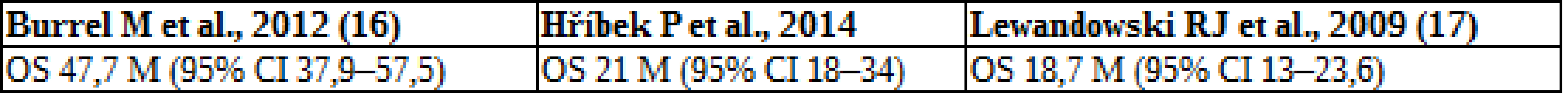
Cíl studie
V naší studii jsme se pokusili prokázat, že skóre ART umožňuje ve skupině pacientů s HCC ve stadiu BCLC-B definovat podskupiny s významně lepším/horším přežitím (OS) při opakované léčbě metodou DEB-TACE.
Použité metody
Kombinovaná retrospektivně prospektivní studie OS se týkala kohorty pacientů s HCC ve stadiu B dle klasifikace BCLC sledovaných a léčených na Interní klinice 1. LF UK a ÚVN v Praze. Byla provedena analýza křivky přežití s využitím Kaplanovy-Meierovy metody odhadu. Zhodnocení statistické významnosti odlišného OS na základě diferenciace pomocí skóre ART bylo provedeno Coxovým modelem. Výpočty byly provedeny v softwaru R.
Schválení studie Etickou komisí Ústřední vojenské nemocnice – Vojenské fakultní nemocnice Praha nebylo požadováno. Péče o pacienty s HCC se v naší instituci řídí aktuálními doporučenými postupy České hepatologické společnosti ČLS JEP. Od těchto standardů jsme se neodchýlili. Před provedením každé DEB-TACE byl od všech pacientů získán písemnou formou standardní institucionální informovaný souhlas dle standardu ÚVN Praha.
Soubor nemocných
Soubor pacientů tvořilo celkem 18 pacientů (16 mužů, 2 ženy; medián věku v době diagnózy 64,5 roku, rozmezí 42–72 let) (tab. 3). Zařazeni byli pacienti splňující následující vstupní kritéria:
- biopticky verifikovaný nebo dle zobrazovacích metod diagnostikovaný HCC (EASL kritéria) (9)
- terapie ≥ 2 etapy
- TACE stadium B dle klasifikace BCLC
- odstup mezi etapami TACE 90 ± 15 dní
Table 3. Složení souboru Hříbek et al. 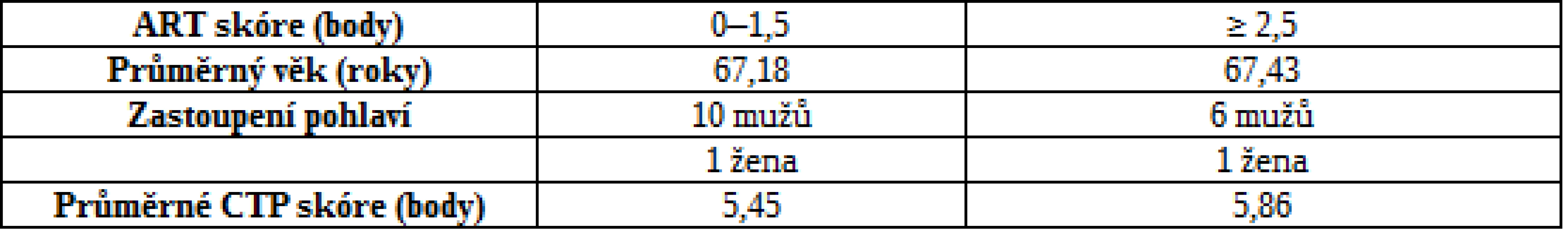
Do studie byli zařazeni jen nemocní, kteří v letech 2007−2015 podstoupili minimálně 2 etapy DEB-TACE, všichni ve stadiu B dle klasifikace BCLC, a bylo u nich zároveň možno spočítat skóre ART. Další podmínkou pro zařazení byl odstup mezi cykly chemoembolizace 90 ± 15 dní. Mezi příčiny nezařazení pacienta do souboru patřilo zejména nedodržení limitu odstupu mezi jednotlivými etapami DEB-TACE, dále některé chybějící laboratorní odběry bezprostředně před druhou etapou transarteriální chemoembolizace nutné k výpočtu ART skóre a absence informací o okamžiku úmrtí pacienta. Z těchto důvodu bylo vyřazeno celkem 10 pacientů. V takto definovaném souboru pacientů byla cirhóza jater způsobena ve 44 % případů alkoholickou chorobou jater, ve 28 % chronickou infekcí HCV, nealkoholové ztukovatění jater a chronická infekce HBV byly zastoupeny shodně v 11 % a u 6 % byla cirhóza kryptogenní.
V souboru pacientů bylo spočítáno skóre ART vždy den před 2. etapou DEB-TACE a proběhlo rozdělení do 2 skupin dle skóre ART. Další etapa transarteriální chemoembolizace byla provedena bez ohledu na výsledek skóre, a to dle aktuálně platných standardů. Rozhodnutí o další etapě tedy bylo uskutečněno na základě hodnocení efektu předchozí terapie dle kontrolního CT nebo MRI vyšetření za použití kritérií mRECIST (10), poklesu sérové hladiny alfa-fetoproteinu a klinického stavu pacienta. V analýze jsme následně porovnávali medián OS (měsíce) skupin dle skóre ART a celého souboru bez diferenciace dle skóre (tedy léčených podle nynějších doporučení).
Výsledky
Průměrný věk žen (n = 2) v době diagnózy v tomto souboru činil 57 let, průměrný věk mužů (n = 16) pak 64,5 roku. Medián OS celého zkoumaného souboru byl 18 měsíců (95% CI 12–33), medián OS skupiny s příznivým skóre ART 33 měsíců (95% CI 17–36; 1 žena, 10 mužů) a medián OS skupiny s prognosticky nepříznivým skóre ART pak 12 měsíců (95% CI 6–18; 1 žena, 6 mužů) (tab. 4, obr. 2). Rozdíl OS mezi skupinami diferencovanými dle skóre ART byl dle Coxova modelu statisticky významný (p < 0,01).
Table 4. Výsledky OS dle ART skóre v souboru Hříbek et al. 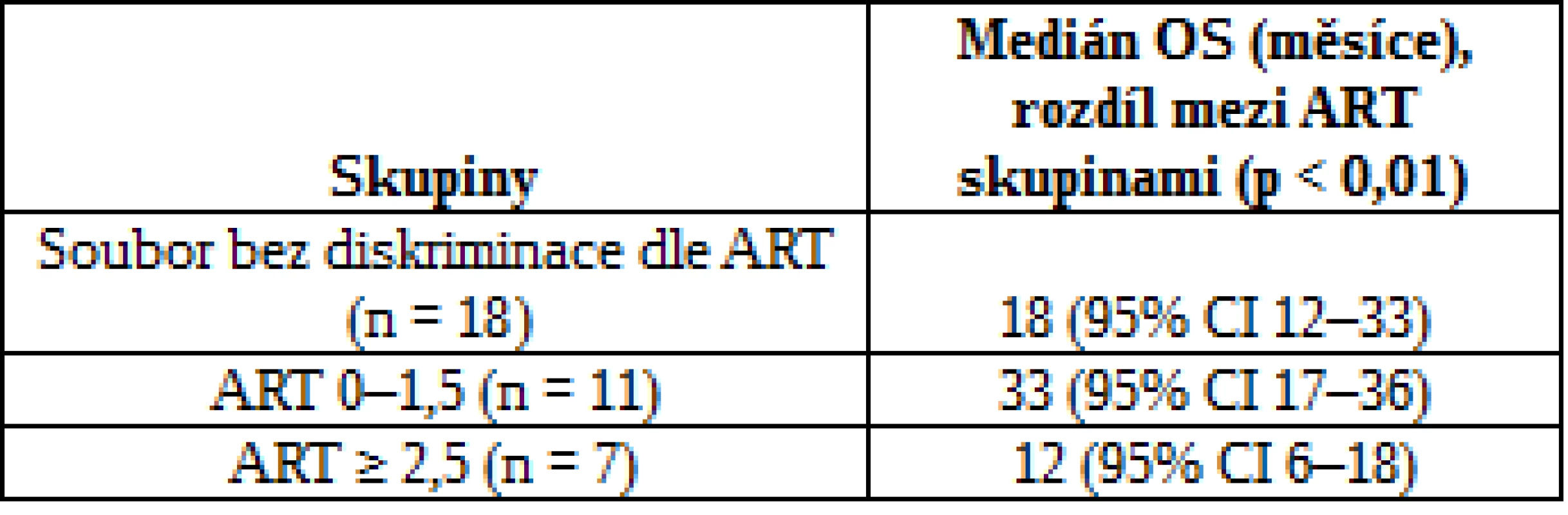
Image 2. Kaplanovy-Meierovy křivky přežití souboru Hříbek et al. 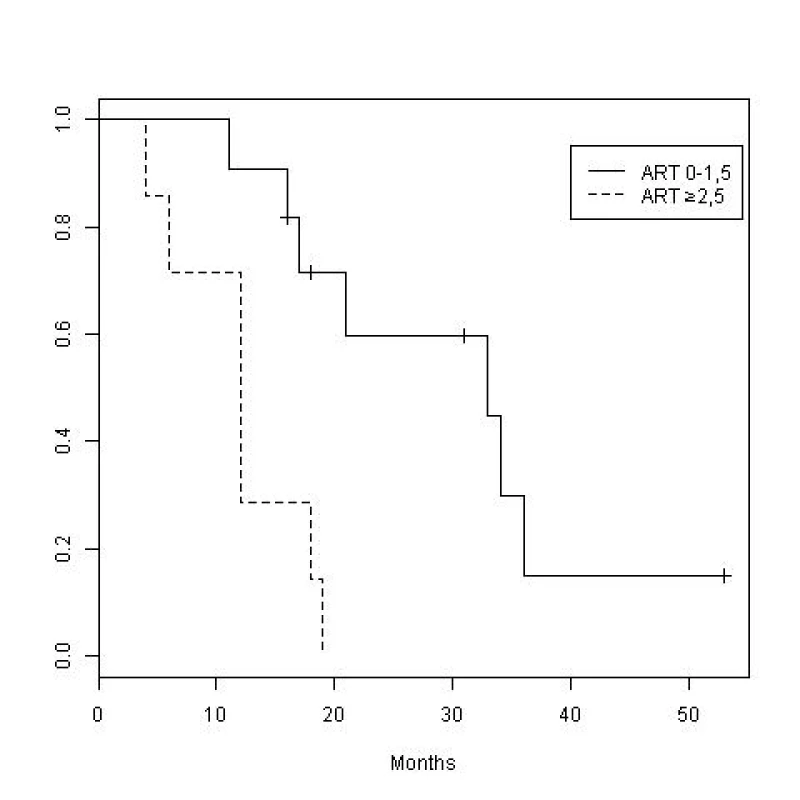
Diskuse
I přes omezenou velikost našeho souboru jsou rozdíly celkového přežívání ve skupinách dle skóre ART statisticky významné a trend Kaplanových-Meierových křivek se neliší od práce autorů skóre. Medián OS u pacientů s intermediárním HCC a nepříznivým skóre ART v práci Siegharta et al. (7) činil 6,6 měsíce (tab. 5). Důvod, proč v našem souboru bylo OS této skupiny téměř dvojnásobné, lze při zpětné analýze nemocných vidět s nejvyšší pravděpodobností v chybě malých čísel.
Table 5. Srovnání našeho souboru pacientů a souboru autorů ART skóre 
Pacienti s hepatocelulárním karcinomem v pokročilém stadiu (C dle klasifikace BCLC) jsou indikováni k terapii sorafenibem (Nexavar, Bayer) (11). K zavedení sorafenibu do klinické praxe vedla především studie SHARP. V ní pacienti ve stadiu C, kteří byli léčeni sorafenibem, dosáhli mediánu celkového přežívání 10,7 měsíce, naproti tomu placebová skupina dosáhla mediánu OS 7,9 měsíce (12). Hlavními kritérii stadia C dle klasifikace BCLC jsou extrahepatální šíření HCC (N1 a/nebo M1), portální invaze a PS 1–2 (2).
Možný význam a potenciální použití skóre ART spatřujeme v následujícím rozporu: Pacienti s pokročilým HCC (dle klasifikace BCLC stadium C) jsou indikováni k podání sorafenibu. Často přitom dosahují delšího přežití než část pacientů s intermediárním HCC stadia B (tj. nižšího vstupního stadia), kteří jsou opakovaně léčeni prostřednictvím DEB-TACE. Intenzivní invazivní terapie (tj. DEB-TACE) tedy u části pacientů nižšího stadia HCC nevede k významnějšímu prodloužení života než sorafenib u HCC stadia vyššího. Problém je v širokém spektru pacientů splňujících kritéria pro zařazení do stadia B dle klasifikace BCLC.
Pokud bychom v úvaze pokračovali, lze dojít k závěru, že již nastala doba pro revizi barcelonské klasifikace a přístupu k léčbě HCC stadia B. Nástrojem k racionální revizi barcelonské klasifikace by se přitom mohlo stát právě skóre ART. Výsledky v našem malém souboru nemocných, ale i zmíněná studie rakouských autorů tento názor podporují. Dosavadní praxe, kdy zařazení pacienta do stadia B vede automaticky pouze k chemoembolizaci, by mohla být revidována v tom směru, že bude doporučeno DEB-TACE u některých pacientů (diskriminace podle ART skóre?) kombinovat s další metodou či metodami. Například: HCC stadia B s jedním větším ložiskem a drobnými satelity bude indikováno k ošetření kombinací DEB-TACE (malé satelity) a radiofrekvenční ablací (RFA, největší ložisko). Samozřejmě při dodržení obecných pravidel pro použití obou metod (13, 14, 15). Pacienti s nepříznivým skóre ART by pak teoreticky mohli profitovat z časnější indikace k terapii sorafenibem namísto opakování DEB-TACE či její kombinace s RFA.
Závěr
Skupina pacientů s intermediárním hepatocelulárním karcinomem je značně široká a heterogenní. Skóre ART se zdá být efektivním nástrojem citlivější stratifikace těchto nemocných podle jejich prognózy, mohlo by vést k racionalizaci indikace dalších etap TACE a případné revizi stávajících doporučených postupů.
Autor práce prohlašuje, že v souvislosti s tématem, vznikem a publikací tohoto článku není ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou. Toto prohlášení se týká i všech spoluautorů.
Seznam zkratek
ART – Assesment for Retreatment with Transarterial chemoembolization
BCLC – Barcelona Clinic Liver Cancer
cTACE – konvenční transarteriální chemoembolizace
CT – výpočetní tomografie
DEB-TACE – drug-eluting beads transarteriální chemoembolizace
HCC – hepatocelulární karcinom
MRI – magnetická rezonance
mRECIST – modified Response Evaluation Criteria in Solid Tumors
OS – celkové přežití (overall survival)
RFA – radiofrekvenční ablace
TACE – transarteriální chemoembolizace jater
Adresa pro korespondenci
MUDr. Petr Hříbek
Oddělení gastroenterologie, hepatologie a metabolismu
Interní klinika 1. LF UK a Ústřední vojenské nemocnice – Vojenské fakultní nemocnice Praha
U Vojenské nemocnice 1200
169 02 Praha 6
e-mail: petr.hribek@uvn.cz
Sources
1. Bruix J, Sherman M. American Association for the Study of Liver Diseases. Management of Hepatocellular Carcinoma: An Update. Hepatology 2010 July; Dostupné na: http://www.aasld.org/practiceguidelines 2010
2. Llovet JM et al. Arterial embolisation or chemoembolisation versus symptomatic treatment in patients with unresectable hepatocellular carcinoma: a randomised controlled trial. Lancet 2002; 359 : 1734–1739.
3. Vogl TJ, Naguib NN, Nour-Eldin NE et al. Review on transarterial chemoembolization in hepatocellular carcinoma: palliative, combined, neoadjuvant, bridging, and symptomatic indications. Eur J Radiol 2009 Dec; 72(3): 505–516; doi: 10.1016/j.ejrad.2008.08.007.
4. Malagari K. Drug-eluting particles in the treatment of HCC: chemoembolization with doxorubicin-loaded DC bead. Expert Rev Anticancer Ther 2008; 8(10): 1643–1650.
5. Lammer J, Malagari K, Vogl T et al. Prospective randomized study of doxorubicin-eluting-bead embolization in the treatment of hepatocellular carcinoma: results of the PRECISION V study. Cardiovasc Intervent Radiol 2010; 33(1): 41–52; doi: 10.1007/s00270-009-9711-7.
6. Sieghart W, Hucke F, Pinter M et al. The ART of decision making: retreatment with transarterial chemoembolization in patients with hepatocellular carcinoma. Hepatology 2013 Jun; 57(6): 2261–2273; doi: 10.1002/hep.26256.
7. Bolondi L, Burroughs A, Du
8. Parkin DM, Bray F, Ferlay J, Pisani P. Global cancer statistics, 2002. CA Cancer J Clin 2005 Mar-Apr; 55(2): 74–108.
9. four JF et al. Heterogeneity of patients with intermediate (BCLC B) hepatocellular carcinoma: proposal for a subclassification to facilitate treatment decisions. Semin Liver Dis 2012; 32 : 348–359
10. European Association for the Study of the Liver, European Organisation for Research and Treatment of Cancer. EASL-EORTC clinical practice guidelines: management of hepatocellular carcinoma. J Hepatol 2012; 56 : 908–943.
11. Lencioni R, Llovet JM. Modified RECIST (mRECIST) assessment for hepatocellular carcinoma. Semin Liver Dis 2010 Feb; 30(1): 52–60; doi: 10.1055/s-0030-1247132.
12. Bruix J et al. Efficacy and safety of sorafenib in patients with advanced hepatocellular carcinoma: subanalyses of a phase III trial. J Hepatol 2012; 57 : 821–829.
13. Llovet JM, Ricci S, Mazzaferro V et al.; SHARP Investigators Study Group. Sorafenib in advanced hepatocellular carcinoma. N Engl J Med 2008 Jul 24; 359(4): 378–390; doi: 10.1056/NEJMoa0708857.
14. Wang Z, Zhou W, Zhang H, Qiao L. Combination of anti-angiogenesis agents and transarterial embolization: Is it a promising approach for the treatment of liver cancer? Discov Med 2015 Aug; 20(108): 51–55.
15. Carr BI. Some new approaches to the management of hepatocellular carcinoma. Semin Oncol 2012 Aug; 39(4): 369–373; doi: 10.1053/j.seminoncol.2012.05.007.
16. Peng ZW, Zhang YJ, Chen MS et al. Radiofrequency ablation with or without transcatheter arterial chemoembolization in the treatment of hepatocellular carcinoma: a prospective randomized trial. J Clin Oncol 2013; 31 : 426–432.
17. Burrel M, Reig M, Forner A et al. Survival of patients with hepatocellular carcinoma treated by transarterial chemoembolisation (TACE) using drug eluting beads. Implications for clinical practice and trial design. J Hepatol 2012; 56(6): 1330–1335.
18. Lewandowski, RJ, Kulik LM, Riaz A et al. A comparative analysis of transarterial downstaging for hepatocellular carcinoma: chemoembolization versus radioembolization. Am J Transplant2009; 9(8): 1920–1928.
Labels
Addictology Allergology and clinical immunology Angiology Audiology Clinical biochemistry Dermatology & STDs Paediatric gastroenterology Paediatric surgery Paediatric cardiology Paediatric neurology Paediatric ENT Paediatric psychiatry Paediatric rheumatology Diabetology Pharmacy Vascular surgery Pain management Dental Hygienist
Article was published inJournal of Czech Physicians

-
All articles in this issue
- Populační screening kolorektálního karcinomu v České republice
- Nové zobrazovací metody v endoskopické diagnostice nádorů trávicího ústrojí
- Onemocnění horní části trávicího traktu: zhoubná onemocnění foregutu
- Maligní biliární obstrukce
- Karcinom pankreatu – současný efektivní diagnosticko-terapeutický postup
- Časná detekce sporadického karcinomu pankreatu
- Vyšetření mutace KRAS v EUS-FNA preparátech pacientů s tumorem pankreatu
- Prognostický význam ART skóre u pacientů s intermediárním hepatocelulárním karcinomem
- Prof. MUDr. Josef Marek, DrSc., osmdesátiletý
- Za profesorem Vratislavem Schreiberem
- Journal of Czech Physicians
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Karcinom pankreatu – současný efektivní diagnosticko-terapeutický postup
- Maligní biliární obstrukce
- Onemocnění horní části trávicího traktu: zhoubná onemocnění foregutu
- Populační screening kolorektálního karcinomu v České republice
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career


