-
Medical journals
- Career
Finerenon: další možnost léčby u pacientů s chronickým onemocněním ledvin a diabetem 2. typu
Authors: Roman Dvořák; Miroslav Souček
Authors‘ workplace: II. interní klinika LF MU a FN U sv. Anny v Brně
Published in: Vnitř Lék 2023; 69(5): 335-338
Category: Advertorial
Overview
Finerenon je selektivní nesteroidní antagonista mineralokortikoidních receptorů. Inhibuje nadměrnou aktivaci těchto receptorů, která u pacientů s chronickým onemocněním ledvin (CKD) a diabetem mellitem 2. typu spouští zánět a fibrózu a vede k progresi renálních a KV onemocnění. Doporučená cílová dávka je 20 mg finerenonu jednou denně podávaná per os. Nejčastějším nežádoucím účinkem finerenonu byl mírný narůst hyperkalemie. Nevykazuje však antiandrogenní nežádoucí účinky. V programu klinických studií finerenon prokázal účinnost při snížení progrese renální insuficience a výskytu KV příhod a příznivý bezpečnostní profil v léčbě pacientů s chronickou renální insuficiencí u diabetiků 2. typu.
Úvod
Diabetes mellitus (DM) je jednou z hlavních příčin konečného stadia onemocnění ledvin. Rozvoj chronického onemocnění ledvin navíc dále zvyšuje již tak výrazně zvýšené KV riziko pacientů s diabetem. Albuminurie i zhoršená funkce ledvin predikuje mortalitu související s KV onemocněním. Multifaktoriální patogeneze CKD související s DM zahrnuje strukturální, fyziologické, hemodynamické a zánětlivé procesy. V současné době je zapotřebí interdisciplinární koncepce léčby, která by zabránila další progresi CKD a snížila riziko kardiovaskulárních příhod a terminálního poškození ledvin (nutnost dialýzy, transplantace). Základem je kombinovaná léčba hypertenze, diabetu a hypolipidemická terapie, která brání progresi diabetického onemocnění ledvin. Často progrese CKD postupuje i u dobře kompenzovaného diabetika z pohledu tlaku a glykemie. Dalším efektivním nástrojem ke zlepšení nefroprotekce u CKD je přídatná léčba nesteroidním antagonistou mineralokortikoidních receptorů (1) (Obr. 1). V minulosti byly do klinické praxe zavedeny dvě látky steroidní povahy antagonizující mineralokortikoidní receptor. Prvním byl spironolakton jako diuretikum pro léčbu hypertenze, edémů a primárního hyperaldosteronismu. Na něj navázal selektivní derivát eplerenon. Obě látky prokázaly příznivý efekt na kardiovaskuiární morbiditu a mortalitu v kombinační léčbě srdečního selhání se sníženou ejekční frakcí, avšak indikaci v léčbě CKD nemají. Jejich nevýhodou byl vysoký výskyt epizod hyperkalemie, který vedl k nutnosti přerušování léčby. Dalším nežádoucím účinkem byl výskyt steroidních nežádoucích účinků, zejména gynekomastie. Novou třídou antagonistů mineralokortikoidního receptoru jsou látky nesteroidní chemické struktury. Jejich vývoj měl za cíl lepší bezpečnost a účinnost v léčbě kardiorenálních onemocnění. Finerenon je prvním zástupcem této skupiny, který se dostává do klinické praxe (2).
Mechanismus účinku finerenonu
Finerenon je selektivní antagonista mineralokortikoidního receptoru třetí generace. Jedná se o nesteroidní látku dihydropyridinové povahy s vysokou selektivitou. Přirozeným agonistou mineralokortikoidního receptoru je aldosteron. Za fyziologických okolností se podílí na udržování tekutinové, minerálové a hemodynamické homeostázy a také na reparaci tkání. Finerenon se na mineralokortikoidní receptor váže jiným způsobem než látky steroidní chemické struktury a inhibuje tak aktivaci specifických kofaktorů zapojených v expresi genů zapojených do patofyziologie zánětu, fibrotizace a hypertrofie tkání. Chronické onemocnění ledvin a další kardiorenální onemocnění jsou spojena s nadměrnou aktivací mineralokortikoidního receptoru, který je jednou z příčin zánětu a fibrotizace ve tkáních ledvin a kardiovaskulárního systému (2, 3). Finerenon je schopen zablokovat genovou expresi prozánětlivých a profibrotických faktorů zapojených v trvalém poškození těchto tkání. Tento mechanismus účinku ovlivňuje jeden z hlavních patofyziologických mechanismů progrese chronického poškození ledvin u diabetu 2. typu. Firenenon jako první účinná látka významně ovlivňuje mechanismus progrese poškození ledvin – zánět a fibrotizaci tkání. Finerenon je tedy v současné době indikován k léčbě chronického onemocnění ledvin (s albuminurií) spojeného s diabetem 2. typu u dospělých pacientů (4).
Image 1. Současné terapie pro pacienty s CKD a DM2 primárně ovlivňující hemodynamické a metabolické faktory 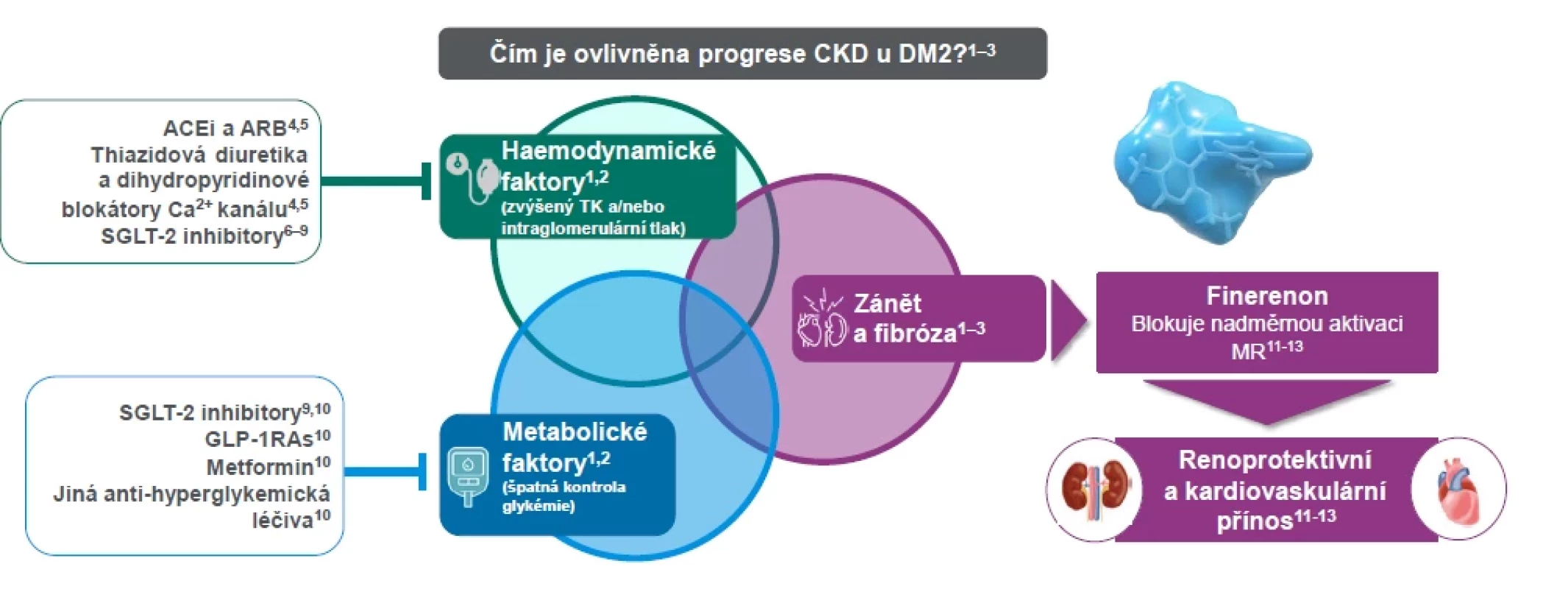
1. Alicic RZ, et al. Clin J Am Soc Nephrol 2017;12:2032–2045; 2. Mora-Fernández C, et al. J Physiol 2014;18:3997; 3. Bauersachs J, et al. Hypertension 2015;65:257–263; 4. American Diabetes Association. Diabetes Care 2020;43:S135-151; 5. American Diabetes Association. Diabetes Care 2020;43:S111–1340; 6. Kidokoro K, et al. Circulation 2019:140;303–315; 7. Zelniker TA & Braunwald E. J Am Coll Cardiol 2018;72:1845–1855; 8. Heerspink HJ, et al. Circulation 2016;134:752–772; 9. Zelniker TA & Braunwald E. J Am Coll Cardiol 2020;75:422–434; 10. American Diabetes Association. Diabetes Care 2020;43:S98–S110; 11. Alicic RZ, et al. Adv Chronic Kidney Dis 2018;25:1941–191. 12. Kolkhof P, et al. J Cardiovasc Pharm 2014;64:69–78; 13. Grune J, et al. Hypertension 2018;71:599–608 CKD, chronické onemocnění ledvin; DM2, diabetes mellitus 2. typu; ACEi, inhibitor angiotenzin-konvertujícího enzymu; ARB, blokator angiotenzinového receptoru; GLP-1RA, glukagon-like peptide receptor 1 agonista; TK, tlak krve; MR, mineralokrtikoidní receptor Klinické studie s finerenonen
V randomizované, dvojitě zaslepené placebem kontrolované studii fáze III FIDELIO-DKD (n = 5674) u pacientů s diabetem 2. typu a CKD (poměr albuminu ke kreatininu v moči (UACR) 30 až < 300 mg/g (3,39 g/ mol až <33,9 g/mol), odhadovaná rychlost glomerulární filtrace (eGFR) 25 až < 60 ml/min/1,73 m2 a diabetická retinopatie) nebo UACR 300 až 5 000 mg/g (33,9 g/mol až 565 g/mol) a eGFR 25 až < 75 ml/min/1,73 m2) snížil finerenon incidenci renálního složeného parametru, který zahrnoval selhání ledvin, trvalý pokles eGFR od vstupu do studie o ≥ 40 % nebo úmrtí z renálních příčin, relativně o 18 % (HR 0,82; 95% CI 0,73–0,93; p = 0,0014). Během mediánu doby sledování 2,6 roku se tento složený renální parametr vyskytl u 17,8 % pacientů s finerenonem a u 21,1 % pacientů s placebem. Ve stejné studii byl zároveň hodnocen sekundární složený KV parametr, který zahrnoval úmrtí z KV příčin, nefatální infarkt myokardu, nefatální cévní mozkovou příhodu nebo hospitalizaci pro srdeční selhání. Po mediánu doby sledování 2,6 roku vedl finerenon k poklesu rizika těchto KV příhod relativně o 14 % (HR 0,86; 95% CI 0,75-0,99; p = 0,034), a to bez ohledu na přítomnost KV onemocnění při vstupu do studie. Účinek léčby na primární a hlavní sekundární cílový parametr byl obecně konzistentní mezi podskupinami, včetně regionu, eGFR, UACR, systolického krevního tlaku, HbA1c při výchozím stavu, nebo současném podávání GLP 1 agonistů nebo SGLT2i (5, 6, 7).
Studie FIGARO–DKD byla studie fáze III s trochu odlišnou populací pacientů (n = 7437). Randomizovaní pacienti měli o něco mírnější stupeň CKD (UACR 30 až < 300 mg/g (3,39 g/mol až <33,9 g/ mol) a eGFR 25 až 90 ml/min/1,73 m2 nebo UACR 300 až 5 000 mg/g a eGFR > 60 ml/min/1,73 m2. Obdobně jako v předešlé studii byli pacienti léčeni blokádou systému renin-angiotenzin-aldosteron, která byla před randomizací upravena na maximálně tolerovanou dávku. Hodnotil se stejný kombinovaný KV i renální parametr jako ve studii FIDELIO. Během mediánu doby sledování 3,4 roku se vyskytla primární KV příhoda u 12,4 % ve skupině s finerenonem a u 14,2 % pacientů ve skupině s placebem (HR 0,87; 95% CI 0,76-0,98; p = 0,03), přičemž nejvýraznější přínos byl způsoben především snížením výskytu hospitalizace pro srdeční selhání (HR 0,71; 95% CI 0,56-0,90). Léčba finerenonem vedla rovněž k nižšímu výskytu složeného ledvinového cílového parametru, ke kterému došlo u 9,5 % pacientů léčených finerenonem a u 10,8 % v placebové větvi (HR 0,87; 95 %Cl 0,761,01; p=0,07). Incidence trvalého přerušení léčby v souvislosti s hyperkalemií byla očekávaně mírně vyšší u finerenomu (1,2 %) než u placeba (0,4 %) (8).
Souhrnná analýza FIDELITY
FIDELITY byla předem specifikovaná metaanalýza kombinující data na úrovni jednotlivých pacientů z FIDELIO-DKD a FIGARO-DKD. Jejím cílem bylo vyhodnotit vztah mezi stadiem CKD a účinností finerenonu na kompozitní kardiovaskulární a renální cíle. Do analýzy bylo zahrnuto více než 13 000 pacientů (Obr. 2). Kardiovaskulárním cílovým parametrem této analýzy byl čas do prvního výskytu kompozitu kardiovaskulární smrti, nefatálního infarktu myokardu, nefatální cévní mozkové příhody nebo hospitalizace pro srdeční selhání. Renálním cílovým parametrem byl čas do prvního výskytu kompozitu selhání ledvin, snížení eGFR o 57 % nebo více od výchozího stavu trvajícího po dobu nejméně čtyř týdnů nebo úmrtí na podkladě onemocnění ledvin. Kompozitní kardiovaskulární cílový parametr se vyskytl u 825 (12,7 %) pacientů užívajících finerenon a 939 (14,4 %) pacientů, kteří dostávali k jinak standardní léčbě placebo. Finerenon snížil riziko sledovaných kardiovaskulárních příhod relativně o 14 % ve srovnání placebem (HR 0,86; 95% CI 0,78–0,95; p = 0,0018, NNT po 3 letech = 46). Snížení rizika výskytu kardiovaskulárního cíle bylo dosaženo zejména redukcí hospitalizací pro srdeční selhání a snížením kardiovaskulární mortality. Výsledek byl nezávislý na vstupní úrovní UACR, eGFR a na léčbě GLP-1 nebo SGLT2 inhibitory. Kompozitní renální cíl se vyskytl u 360 (5,5 %) pacientů užívajících finerenon a 465 (7,1 %) pacientů, kteří dostávali placebo. Riziko výskytu tohoto výsledku bylo relativně o 23 % nižší u finerenonu než u placeba (HR 0,77; 95% CI 0,67–0,88, p = 0,0002). Výskyt všech složek kompozitního renálního cíle byl významně nižší u finerenonu než u placeba, kromě úmrtí z renálních příčin, ke kterému došlo zřídka na to, aby bylo možné provést mezi skupinami validní porovnání. Pokud jde o bezpečností, výsledky byly mezi léčebnými rameny obecně podobné. Finerenon měl mírný vliv na hladinu draslíku v séru, s největším nárustem po 1. měsíci léčby (9). Hyperkalemie byla sice častější u finerenonu (14,0 %) než u placeba (6,9 %), ale trvalé přerušení léčby v důsledku hyperkalemie nebylo časté (1,7 % ve skupině s finerenonem proti 0,6 % ve skupině s placebem). Souhrnná analýza FIDELITY ukazuje, že u diabetiků 2. typu finerenon ve srovnání s placebem snížil nad rámec standardní farmakoterapie riziko kardiovaskulárních komplikací a progrese onemocnění ledvin v celém spektru CKD. Kardiovaskulární a renální přínos léčiva byl konzistentní napříč kategoriemi eGFR a UACR, což naznačuje uplatnění finerenonu již v časných stadiích onemocnění ledvin u pacientů s diabetem 2. typu.
Dávkování
Doporučená cílová dávka je 20 mg finerenonu, jednou denně, per os. Při zahájení léčby je třeba stanovit aktuální hodnotu odhadované glomerulární filtrace (eGFR) a kalemie. Podávání finerenonu je možné zahájit při koncentraci sérového draslíku ≤ 4,8 mmol/l. Při hodnotách kalemie mezi 4,8 a 5,0 mmol/l lze zvážit zahájení léčby při dalším sledování kalemie během prvních 4 týdnů. Nad tuto hodnotu již léčba nemá být zahajována. Pokud jde o renální funkce, při hodnotě eGFR ≥ 60 ml/min/1,73 m2 se léčba zahajuje dávkou 20 mg jedenkrát denně. Při hodnotách < 60 ml/min/1.73 m2 volíme zahajovací dávku 10 mg jedenkrát denně. Při eGFR < 25 ml/ min/1,73 m2 není doporučeno léčbu zahajovat. Po prvních 4 týdnech léčby je třeba znovu stanovit kalemii a eGFR k rozhodnutí, zda lze v léčbě pokračovat, respektive zda je možné dávku zvýšit na 20 mg. Pokračování léčby je možné při eGFR ≥ 15 ml/min/1,73 m2 a při kalemiii ≤ 5,5 mmol/l. Pokud je hladina kalemie ≤ 4,8 mmol/l, zvyšuje se nebo ponechává na dávce 20 mg. Pokud je hladina sérového draslíku mezi 4,8 a 5,5 mmol/l, ponechává se zahajovací dávka. Je-li nutné přerušit podávání pro vysokou kalemii (>5,5 mmol/l), může se začít znovu po jejím poklesu ≤ 5,0 mmol/l dávkou 10 mg jednou denně (11).
Image 2. Finerenon se sledoval v rámci rozsáhlého klinického programu s CKD a DM 2. typu (1–8) 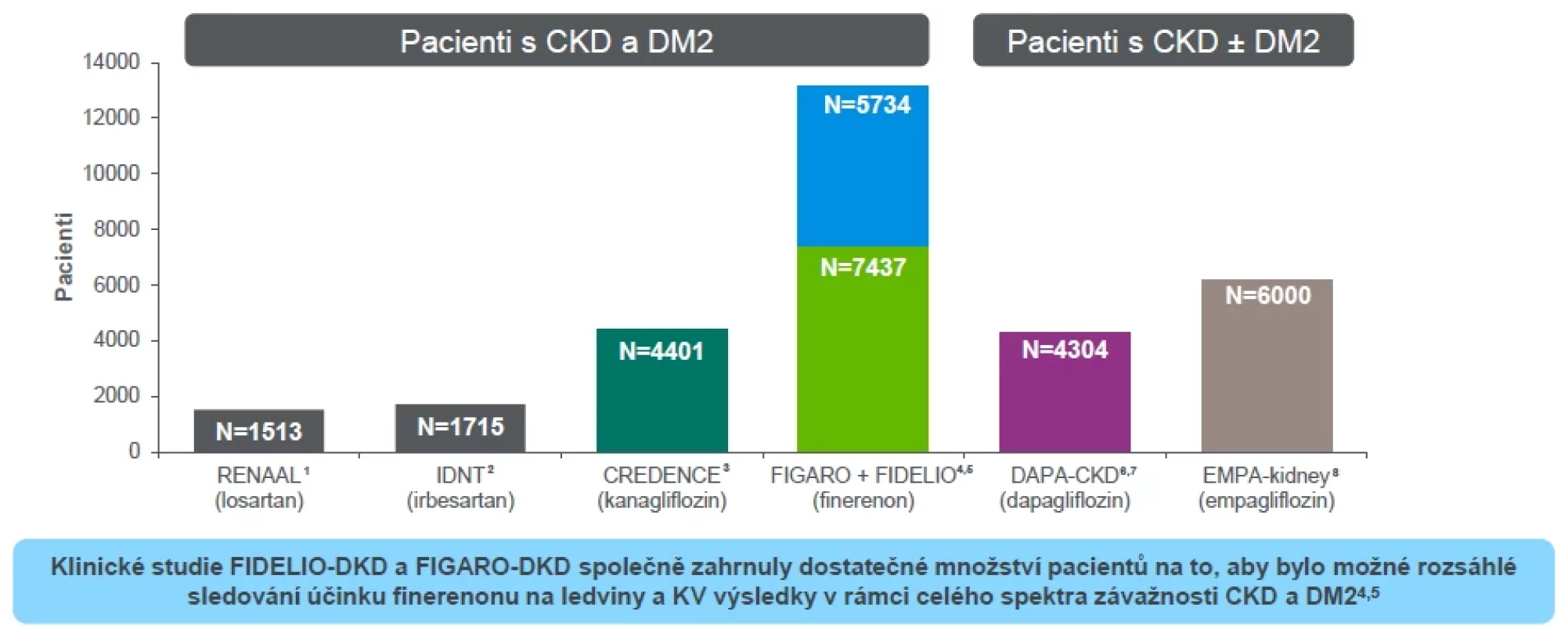
Vzhledem k rozdílným vstupním charakteristikám pacientů není možné porovnávat výsledky jednotlivých studií. CKD, chronické onemocnění ledvin; DM2, diabetes mellitus 2. typu1. Brenner B, a kol. N Engl J Med 2001;345:861–869; 2. Lewis EJ, a kol. N Engl J Med 2001;345:851–860; 3. Perkovic V, a kol. N Engl J Med 2019;380:2295–2306; 4. Bakris GL, a kol. Am J Nephrol 2019;50:333–344; 5. Ruilope LM, a kol. Am J Nephrol 2019;50:345–356; 6. Heerspink HJL, a kol. Nephrol Dialy Transplant 2020;35:274–282; 7. AstraZeneca https://clinicaltrials.gov/ct2/show/NCT03036150 [Datum náhledu: 24.června 2020]; 8. Boehringer Ingelheim, https://clinicaltrials.gov/ct2/show/NCT03594110 [Datum náhledu: 24. června 2020] Image 3. Profil pacienta vhodný na zahájení léčby finerenonem (v souladu s indikačním omezením úhrady přípravku Kerendia*) 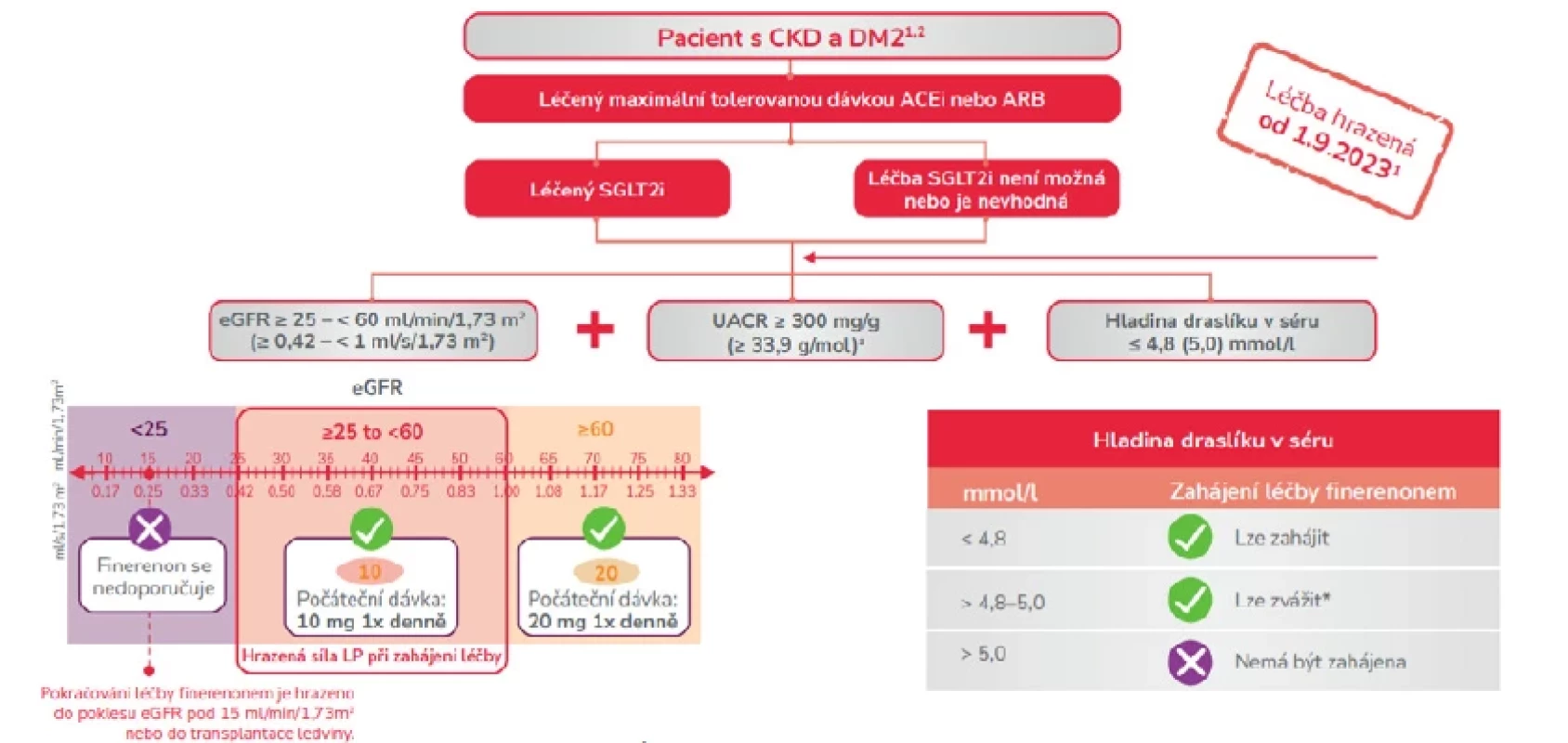
*Zahájení léčby finerenonem lze zvážit při dalším sledování hladiny draslíku v séru během prvních 4 týdnů založeném na charakteristikách pacienta a hladinách draslíku v séru. a V registrační studii FIDELIO-DKD byli pacienti vybíráni na základě prokázané perzistentní albuminurie, UACR > 30 mg/g - 5 000 mg/g (3,39 g/mol - 565 g/mol).3 CKD, chronické onemocnění ledvin; DM2, diabetes mellitus 2. typu; eGFR, odhadovaná rychlost glomerulární filtrace; UACR,(ACR), poměr albuminu ke kreatininu v moči; ACEi, inhibitor angiotenzin konvertujícího enzymu; ARB, blokátor angiotenzinových receptorů; SGLT2i, inhibitory sodíko-glukozového kotransportéru typu 2; LP, léčivý přípravek Upraveno dle: 1. www.sukl.cz; 2. SPC přípravku Kerendia® , dostupné z: https://www.bayer.com/sites/default/files/Kerendia_SPC.pdf; 3. Bakris GL, et al. FIDELIO-DKD Investigators. Effect of Finerenone on Chronic Kidney Disease Outcomes in Type 2 Diabetes. N Engl J Med. 2020 Dec 3;383(23):2219-2229. Nežádoucí účinky
Nejčastěji hlášeným nežádoucím účinkem finerenonu, který je závislý na dávce, byla hyperkalemie, která však byla mírná. V klinických studiích se vyskytovala u 14 % léčených finerenonem. Další časté poruchy iontové rovnováhy byly hyponatremie a hyperurikemie. Na dávce závislé a reverzibilní byly i hypotenze a pokles glomerulární filtrace. Méně častý byl pokles sérového hemoglobinu a hematokritu a anemie. Vyskytnout se mohou i alergické reakce. Finerenon má absenci antiandrogenních nežádoucích účinků, jako jsou gynekomastie nebo erektilní dysfunkce u mužů a poruchy menstruačního cyklu či bolestivost prsů u žen. Z interakcí je nejvýznamnější potenciace hyperkalemizujícího účinku finerenonu jinými léky. Není vhodné současné užívání jiných antagonistů aldosteronu (spironolaktonu nebo eplerenonu), nedoporučuje se ani kombinace s klasickými kalium šetřícími diuretiky (amilorid, triamteren). Současné podávání silných inhibitorů cytochromu P450 je přímo kontraindikováno. Nejčastěji v úvahu připadají klaritromycin, itrakonazol a ritonavir. Stejně tak se nedoporučuje užívat grapefruitovou šťávu (11).
Přípravek Kerendia (finerenon) má od 1. 9. 2023 stanovenou úhradu.
Jaká jsou indikační omezení úhrady přípravku (Obr. 3)?
Finerenon je hrazen jako přídatná terapie u dospělých pacientů s diabetem 2 typu a současným diabetickým onemocněním ledvin stupně 3 a 4 a odhadovanou glomerulární filtací (eGFR) v rozmezí 25 až 60 ml/min/1,73 m2 a albuminurií (alespoň 33,9 g/mol., odpovídá 300 mg/g kreatininu) kteří jsou:
- léčeni maximální tolerovanou dávkou inhibitoru angiotenzin-konvertujícího enzymu (ACEI) nebo blokátoru receptoru typu 1 pro angiotenzin II (ARB) a u kterých není možná nebo vhodná léčba gliflozinem,
- léčeni maximálně tolerovanou dávkou inhibitoru angiotenzin-konvertujícho enzymu (ACEI) nebo blokátoru receptoru typu 1 pro angiotenzin II (ARB) a gliflozinem.
Z prostředků veřejného zdravotního pojištění je hrazena maximálně 1 tableta denně. Léčba finerenonem je hrazena do poklesu eGFR pod 15 ml/min/1,73 m2 nebo do transplantace ledviny.
Závěr
Firenenon je lék, který odlišným způsobem ovlivňuje hyperaktivitu mineralokortikodního receptoru a tím příznivě zasahuje do patofyziologie kardiorenálních onemocnění. V dosud nejrozsáhlejším programu klinických studií finerenon prokázal účinnost a příznivý bezpečnostní profil v léčbě chronické renální insuficience u diabetiků 2. typu.
Podpořeno společností Bayer, s. r. o. (číslo schválení: PP-KER-CZ-0149-1, 08/2023).
Sources
- Vachek J, Tesař V. Finerenon. Vniř Lék. 2023; 69(3): E20-E23.
- Folkerts K, Millier A, Smela B, et al. Real-world evidence for steroidal mineralocorticoid receptor antagonists in patients with chronic kidney disease. J Nephrol. 2022; Nov 23 doi: 10.1007/s40620-022-01492-w. Epub ahead of print. PMID: 36422853. J Nephrol. 2022; Nov 23 doi: 10.1007
- Epstein M. Aldosterone and Mineralocorticoid Receptor Signaling as Determinants of Cardiovascular and Renal Injury. From Hans Seley to the Present. Am J Nephrol. 2021; 52 : 209-216.
- Urbánek K. Finerenon: farmakologický profil. Klin Farmakol Farm. 2023; 37(1): 29-32.
- Agarwal R, Anker SD, Bakris G, et al. Investigating new treatment opportunities for patients with chronic kidney disease in type 2 diabetes: the role of finerenon. Nephrol Dial Transplant. 2022; 37(6): 1014-1023.
- Bakris G, Agarwal R, Chan JC, et al. Effect of Firenenone on Albuminuria in Patients With Diabetic Nephropathy. A Randomised Clinical Trial. JAMA 2015; 314(9): 884-894.
- Bakris G, Agarwal R, Anker SD, et al. Effect of Finerenone on Chronic Kidney Disease Outcomes in Type 2 Diabetes. N Engl J Med. 2020; 383(23): 2219-2229.
- Pitt B, Filippatos G, Agarwal R, et al. Cardiovascular Events with Finerenone in Kidney Disease and Type 2 Diabetes. N Engl J Med. 2021; 385(24): 2252-2263.
- Bakris G, Riulope L, Anker SD, et al. FIDELIO-DKD and FIGARE-DKD Investigators. A prespecified exploratory analysis from FIDELIT examined finerenone use and kidney outcomes in patiets with chronic kidney disease and type 2 diabetes. Kidney Int. 2023 Jan; 130(1): 196-206.
- A trial to Learn How Well Finerenone Works and How Safe it is in Adult Participants With Non-diabetic Chronic Kidney disease (FIND-CKD). Available from: https://beta.clinicaltrials.gov/study/NCT05047263.
- SPC přípravku Kerendia® Available from: https://www.bayer.com/sites/default/files/ Kerendia_SPC.pdf.
Zkrácené informace o léku Kerendia® naleznete na straně 339.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2023 Issue 5-
All articles in this issue
- Acute kidney injury in patients with cirrhosis – practical summary
- Cardiovascular disease and kidney transplantation
- Implications of highly suppressive treatment HIV infection
- Internal comorbidities and complications of multiple sclerosis therapy – don’t be caught off guard!
- Dyslipidemia – the known unknown
- Differentiated thyroid cancer – possible risks of treatment, suppressive therapy and adherence to current recommendations
- Atypical form of Goodpasture’s disease
- Pharmacological profile of mepolizumab
- News in respiratory medicine
- Finerenon: další možnost léčby u pacientů s chronickým onemocněním ledvin a diabetem 2. typu
- Zemřela prof. MUDr. Marie Brodanová, DrSc.
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Acute kidney injury in patients with cirrhosis – practical summary
- Dyslipidemia – the known unknown
- Cardiovascular disease and kidney transplantation
- News in respiratory medicine
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career
