-
Medical journals
- Career
Disekcia ascendentnej aorty, diagnóza na ktorú treba myslieť
Authors: Veronika Jankovičová; Margita Belicová; Milan Ochodnický; Marián Mokáň
Authors‘ workplace: I. interná klinika, Univerzitná nemocnica a JLF UK v Martine
Published in: Vnitř Lék 2020; 66(8): 55-60
Category: Case Report
Overview
Akútna disekcia aorty typu A je život ohrozujúci stav a významnou príčinou morbidity a mortality. Jej typickým symptómom je náhle vzniknutá bolesť na hrudníku, ktorá sa vyskytuje u viac ako 85% pacientov. Akútna bolesť na hrudníku vedie k podozreniu na akútny koronárny syndróm a ak zmeny na elektrokardiograme naznačujú možnú ischémiu, pacientom je podaná antitrombotická liečba. U niektorých pacientov bolesť na hrudníku nemusí byť prítomná, môže byť prítomný ložiskový neurologický deficit, ktorý sa objavuje ako jedna z komplikácií šírenia dissekcie na veľké artérie. Autori v práci popisujú troch pacientov s akútnou disekciou aorty typu A. Dvaja z nich nemali akútne bolesti na hrudniku, dominoval u nich ložiskový neurologický deficit. Tretí pacient mal typické akútne bolesti na hrudníku, na elektrokardiograme suspektné ischemické zmeny, čo viedlo k podozreniu na akútny koronárny syndróm. Autori prezentujú, že akútna disekcia aorty typu A môže byť ľahko prehliadnutá, preto je potrebné na túto diagnózu myslieť, aby sa včas diagnostikovala a bola zahájená okamžitá adekvátna liečba.
Klíčová slova:
aorta – akútny koronárny syndróm – cievna mozgová príhoda – disekcia aorty typu A.
Úvod
Akútna disekcia ascendentnej aorty (ADAA) je závažný, život ohrozujúci stav. Medzi jej najčastejšie príznaky patrí náhle vzniknutá intenzívna bolesť na hrudníku, môže sa prejaviť aj dysfunkciou iných orgánových systémov z dôvodu ischémie, akútne vzniknutým šokom, alebo náhlou smrťou. Nie je to časté ochorenie a má mnoho príznakov spoločných s inými ochoreniami, nielen kardiálnymi, preto často dochádza k jej oneskorenej diagnostike, ak sa vôbec na túto diagnózu myslí (1). Osobitnú skupinu tvoria pacienti s vysoko rizikovým profilom, čo zahŕňa najmä aneuryzmu aorty, bikuspidálnu aortálnu chlopňu, stav po predchádzajúcej kardiochirurgickej operácii či raritné, no o to závažnejšie genetické syndrómy ako je Marfanov, Ehlers‑Danlosov a Loeys‑Dietzov syndróm (2). Jej zákernosť spočíva hlavne v tom, že bolesť na hrudníku nemusí byť prítomná alebo nemusí byť dominantná. Aj dnes sa na ADAA myslí len u 15% až 43% pacientov, u ktorých je táto diagnóza potvrdená a 50% neliečených pacientov zomiera v prvých 48 hodinách (3). ADAA patrí medzi akútne hrudné aortálne syndrómy a napriek tomu, že liečba ochorení aorty zaznamenala v poslednom desaťročí zásadný progres, jej liečba naďalej ostáva doménou kardiochirurgie a pre život zachraňujúcu liečbu je nesmierne dôležitá rýchla diagnostika (1).
Popis pacientov
V práci uvádzame troch pacientov s ADAA, ktorí boli diagnostikovaní v priebehu 4 mesiacov v roku 2016 na Oddelení urgentného príjmu (OUP) v Univerzitnej nemocnici v Martine (UNM).
Prvý pacient bol 62-ročný muž, normostenik, s negatívnou RA na kardiovaskulárne ochorenia, fajčiar, hypertonik v liečbe inhibítormi angiotenzín konvertujúceho enzýmu (ACEI), ktoré užíval pravidelne a hodnoty tlaku krvi (Tk) sa podľa dokumentácie dlhodobo pohybovali v pásme vyšších normálnych hodnôt. V deň príhody pri oprave auta sa chcel postaviť z viac ako 10minút trvajúcej skrčenej polohy, zatočila sa mu hlava, nohy ho neudržali, nedokázal chodiť, padal k zemi, súčasne mal problémy s artikuláciou, bolesti hlavy nemal. S uvedenými ťažkosťami bol rýchlou zdravotnou službou (RZS) privezený na OUP v UNM. Pri vstupnom vyšetrení pacient bolesti na hrudníku nemal, dýchavičný nebol. Vstupné EKG bolo bez patológie a boli realizované základné krvné odbery. Vyšetrujúci lekár nepopisuje šelest na srdci, akcia srdca bola pravidelná 88/min., Tk bol 120/78 mmHg, pulzácie na periférnych artériách boli hmatné. Vstoji pacient padal. Vhľadom na uvedené bolo realizované neurologické vyšetrenie so záverom: Suspektná náhla cievna mozgová príhoda (NCMP) v oblasti mozgového kmeňa pod obrazom vestibulo‑cerebelárneho syndrómu, s doporučením doplniť CT mozgu s angiografiou mozgových artérií na vylúčenie ischémie v oblasti mozgového kmeňa. Počas CT vyšetrenia boli vyhodnotené laboratórne vyšetrenia, ktoré boli bez patológie, D‑dimér vyšetrený nebol. Pacient podstúpil CT mozgu s angiografiou so záverom: Multiinfarktová encefalopatia, ascendentná aorta je dilatovaná na 45 mm, disekcia aorty začína od aortálnej chlopne v celom jej priebehu, šíri sa na truncus brachiocephalicus dx. a a. subclavia dx. a proximálnu tretinu a. carotis communis (ACC) dx., pokračuje na descendentnú aortu, z pravého lumenu odstupujú truncus coeliacus, a. mesenterica superior a a. renalis sin., a. renalis dx. odstupuje z nepravého lumen, disekcia končí v oblasti bifurkácie abdominálnej aorty (obr. 1). Pacient bol prevezený na Kardiochirurgiu v SÚSCCH v Banskej Bystrici, kde podstúpil operáciu: Extirpáciu a suprakoronárnu náhradu ascendentnej aorty lineárnou protézou Albograft N. 28 mm. Pooperačný priebeh bol komplikovaný paroxyzmálnou fibriláciou predsiení, febrilným stavom bez potvrdeného zdroja infekcie, ktorý bol zvládnutý empirickou antibiotickou liečbou a akútnym obličkovým zlyhávaním, zvládnutým konzervatívne. Za 3 mesiace od urgentnej operácie bol kontrolne vyšetrený na Ambulancii pre choroby aorty v SÚSCCH v Banskej Bystrici, kde podstúpil kontrolné transtorakálne echokardiografické (TTE) vyšetrenie srdca so záverom: dilatácia ľavej komory (ĽK) srdca na 63 mm bez jej dysfunkcie, aortálna chlopňa s ľahkými degeneratívnymi zmenami všetkých troch cípov s regurgitáciou do 1. stupňa a kontrolné CT vyšetrenie s kontrastom so záverom: Reziduálna disekcia torakoabdominálnej aorty s patentným falošným lumenom, v proximálnej časti aortálneho oblúka široké entry a subtotálny kolaps hrudnej aorty, a. renalis dx. sa plní z falošného lumen, bez známok malperfúzie, propagácia disekcie na proximálne úseky vetiev aortálneho oblúka bez progresie.Uvedený nález bol konzultovaný na kardiochirurgickom seminári v NÚSCCH v Bratislave ako aj na intervenčnom pracovisku s doporučením konzervatívneho postupu vzhľadom na morfológiu postihnutia. Na ďalšiu plánovanú kontrolu sa nedostavil, ostal v evidencii spádového kardiológa. V decembri 2019, tri roky po operácii je pacient bez ťažkostí, pokračuje v liečbe ACEI, betablokátor a warfarín. S ďalším invazívnym postupom napriek poučeniu o svojom zdravotnom stave nesúhlasí.
Image 1. CT vyšetrenie, ascendentná aorta 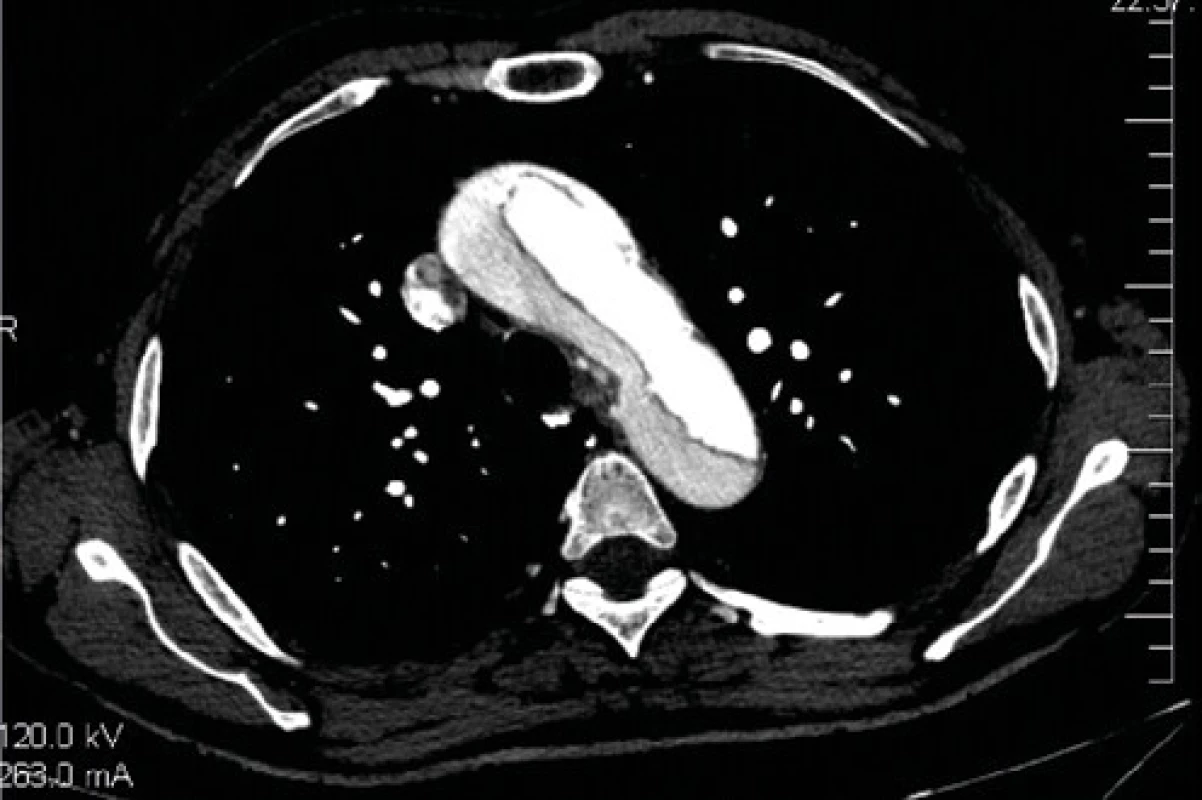
Druhý pacient bol 44 ročný muž, s negatívnou RA na kardiovaskulárne ochorenia, normostenik, bez chronických ochorení, nefajčiar.V deň príhody v kľude pocítil nevýraznú bolesť na hrudníku, ktorá spontánne ustúpila do 15 min. Následne mu ochrnula pravá dolná končatina, čo bolo príčinou jeho prevozu RZS na OUP v UNM. Pri vyšetrení na OUP pacient bolesti na hrudníku nemal, dýchavičný nebol, bol plne orientovaný, vyšetrujúci lekár popisuje na srdci pravidelný rytmus 88/min., systolický šelest s maximom nad aortou s propagáciou do karotíd, Tk bol 117/80mmHg, pravá dolná končatina bola paretická, periférne pulzácie boli hmatné. Vstupné EKG bolo bez patológie, v krvnom obraze bola prítomná leukocytóza 11,00 (3,9…10), bola zvýšená hodnota D‑diméru na 4,14 mg/l (0,10…0,50), zvyšné výsledky boli v norme. Vzhľadom na dominujúcu pravostrannú monoparézu pravej dolnej končatiny bol vyšetrený neurológom so záverom: NCMP supratentoriálne bilaterálne a cerebellum bilataterálne. Pacientovi bolo doplnené CT vyšetrenie mozgu s kontrastom so záverom: Ascendentná aorta je dilatovaná na 44 mm, oblúk aorty na 33 mm, descendentná aorta a brušná aorta bez dilatácie, je prítomná disekcia celej torakálnej a abdominálnej aorty, disekcia ascendentnej aorty sa šíri na truncus brachiocephalicus, a. carotis communis dx., do odstupu a. carotis communis sin. a na proximálny úsek a. subclavia sin., disekcia končí v úrovni a. illica externa a a. femoralis communis bilaterálne (Obr. 2). S uvedeným nálezom bol pacient akútne prevezený do NÚSCCH v Bratislave, kde v deň príjmu vzhľadom na disekciou postihnutú aortálnu chlopňu podstúpil Bentallovu operáciu s protézou SJM No. 23, sec. Bentall deBono, konduitom ascendentnej aorty a naložením stentgraftu Thoraflex No. 26/28 do aortálneho oblúka. 2. deň po operácii bol stav komplikovaný respiračným zlyhávaním pre bilaterálny pneumothorax, ktorý bol zadrénovaný, a ďalší deň došlo k vývoju NCMP s ľavostrannou hemiparézou, pre ktorú urgentne podstúpil stenting a. carotis interna dx. a súčasne endovaskulárnu intervenciu hrudnej aorty (TEVAR). Neurologický nález sa upravil v nasledujúcich dňoch. Napriek komplikovanému priebehu sa stav pacienta nasledujúce týždne kompletne upravil, ostal v starostlivosti spádového kardiológa. V decembri 2019, tri roky po operácii je bez ťažkostí a neurologického deficitu, podstúpil kontrolné TTE vyšetrenie srdca so záverom: Protéza v aortálnej pozícii je bez leaku, peak gradient na chlopni 23mmHg, bulbus aorty 28 mm, ĽK bez dilatácie a dysfunkcie a ultrasonografiu extrakraniálnych mozgových artérií so záverom: Laminárne prúdenie v dostupných artériách, bez známok disekcie a bez stenózy v mieste stentu. Pacient pokračuje v liečbe warfarín a betablokátor.
Image 2. CT vyšetrenie, ascendentná aorta 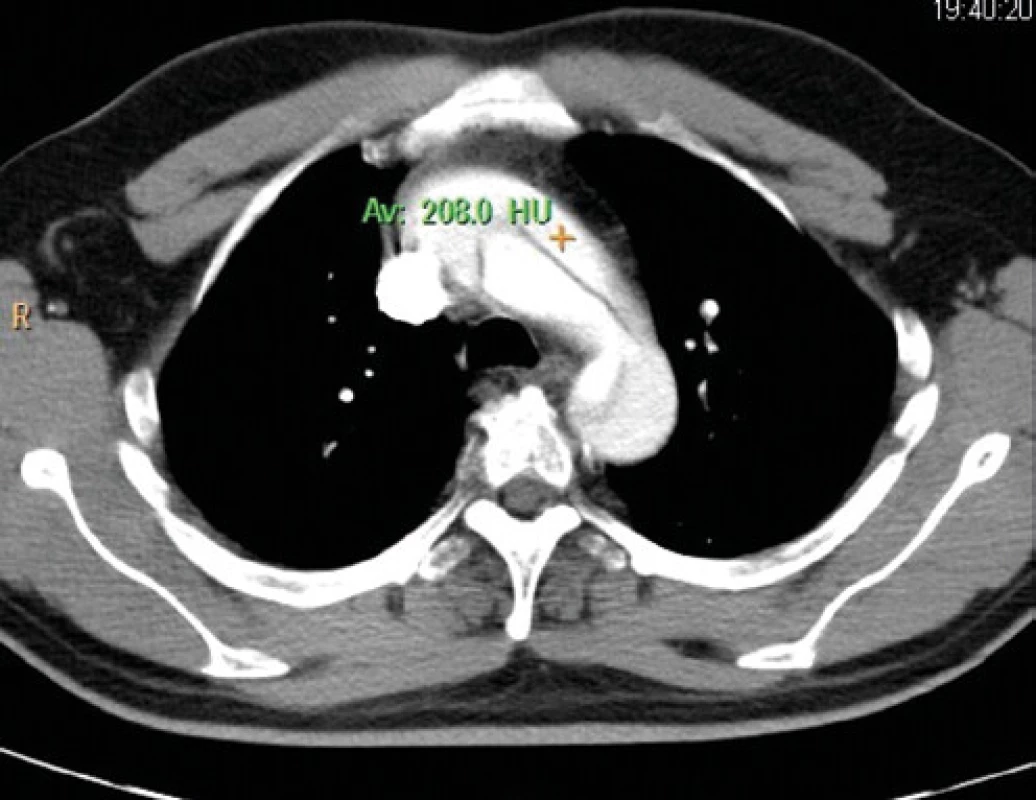
Tretí pacient bola 52-ročná žena, normostenička, s negatívnou RA na kardiovaskulárne ochorenia, bez chronických ochorení, nefajčiarka. V deň príhody v ranných hodinách počas bežnej činnosti pocítila prasknutie na hrudníku, ktorému nasledovala intenzívna retrosternálna bolesť s propagáciou do oboch horných končatín, dýchavičná nebola. Bola ošetrená lekárom RZS, kde lekár na základe bolestí na hrudníku a zmien na EKG (Obr. 3) stav hodnotil ako akútny koronárny syndróm s eleváciami ST segmentu, po podaní tabletiek 200 mg aspirín + a 180 mg ticagrelol bola prevezená na OUP v UNM v Martine. Pri vstupnom vyšetrení u pacientky pretrvávali bolesti na hrudníku v menšej intenzite, dýchavičná nebola, akcia na srdci bola pravidelná 77/min., bol prítomný diastolický šelest nad aortou, Tk bol 130/55mmHg, na peri ‑ férnych artériách boli hmatné pulzácie. Vzhľadom na nejednoznačné zmeny na EKG a auskultačný nález na srdci bolo doplnené bedside TTE vyšetrenie srdca, pri ktorom bola odhalená dilatácia ascendentnej aorty na 45 mm, dvojlumen v ascendentnej aorte a aortálna regurgitácia do 3. stupňa (Obr. 4). Následne bolo doplnené urgentné CT vyšetrenie s kontrastom, ktoré potvrdilo disekciu aorty, ktorá začínala v bulbe aorty, šírila sa celým priebehom hrudnej a brušnej aorty, a končila v infrarenálnej časti abdominálnej aorty v úrovni odstupu lumbálnych tepien pre L3 (Obr. 5). U pacientky boli realizované základné odbery a bola prevezená do NÚSCCH v Bratislave, kde podstúpila operáciu podľa Bentalla, pooperačný priebeh bol bez závažnejších komplikácií. Aktuálne pacientka žije v zahraničí, v decembri 2019, tri roky po operácii bol kontakt možný telefonicky, pacientka je bez ťažkostí, pokračuje v liečbe podľa spádového kardiológa.
Image 3. Elevácie ST v II, III, aVF, V5-V6 bez kontralaterálnych depresií ST na EKG hodnotené ako inferolaterálny STEMI 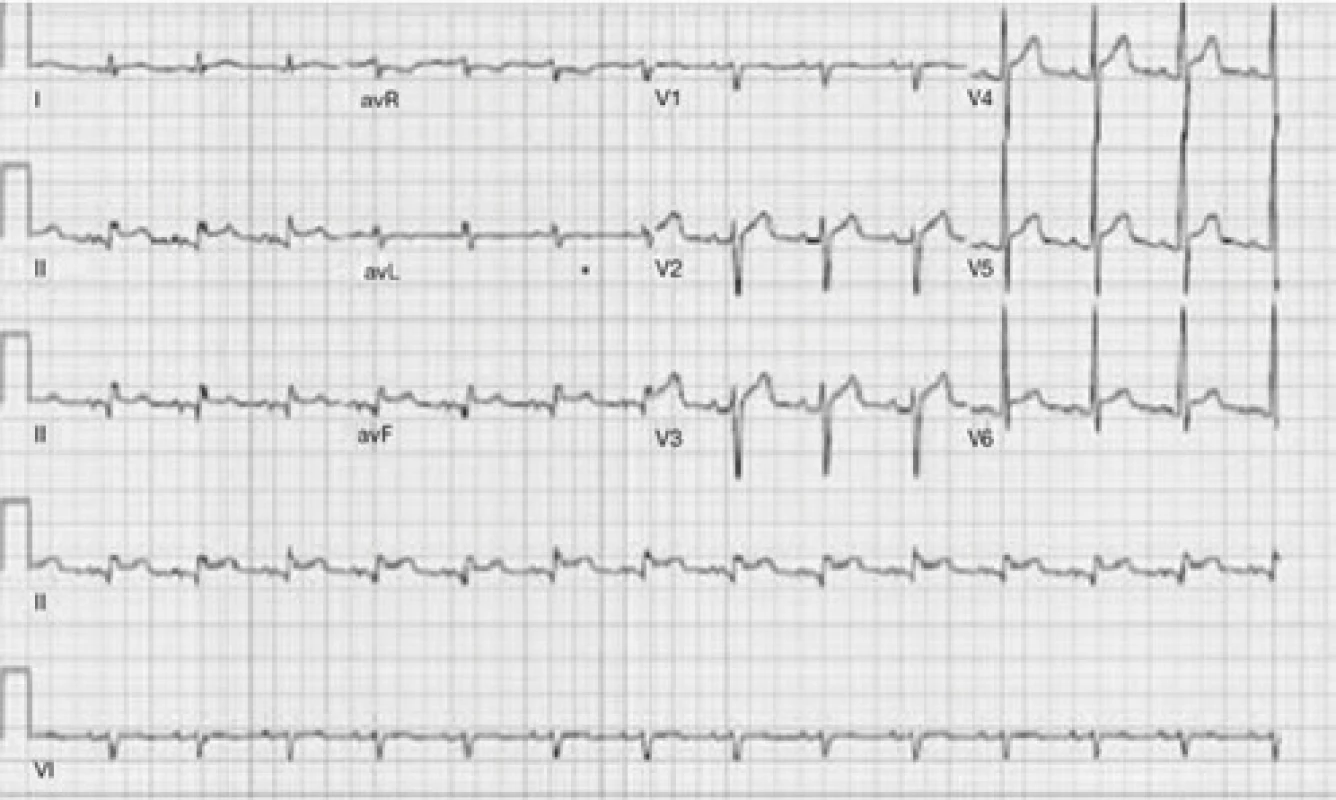
Image 4. Transtorakálne echokardiografické vyšetrenie srdca odhalilo dilatovaný koreň aorty a intimálny flap 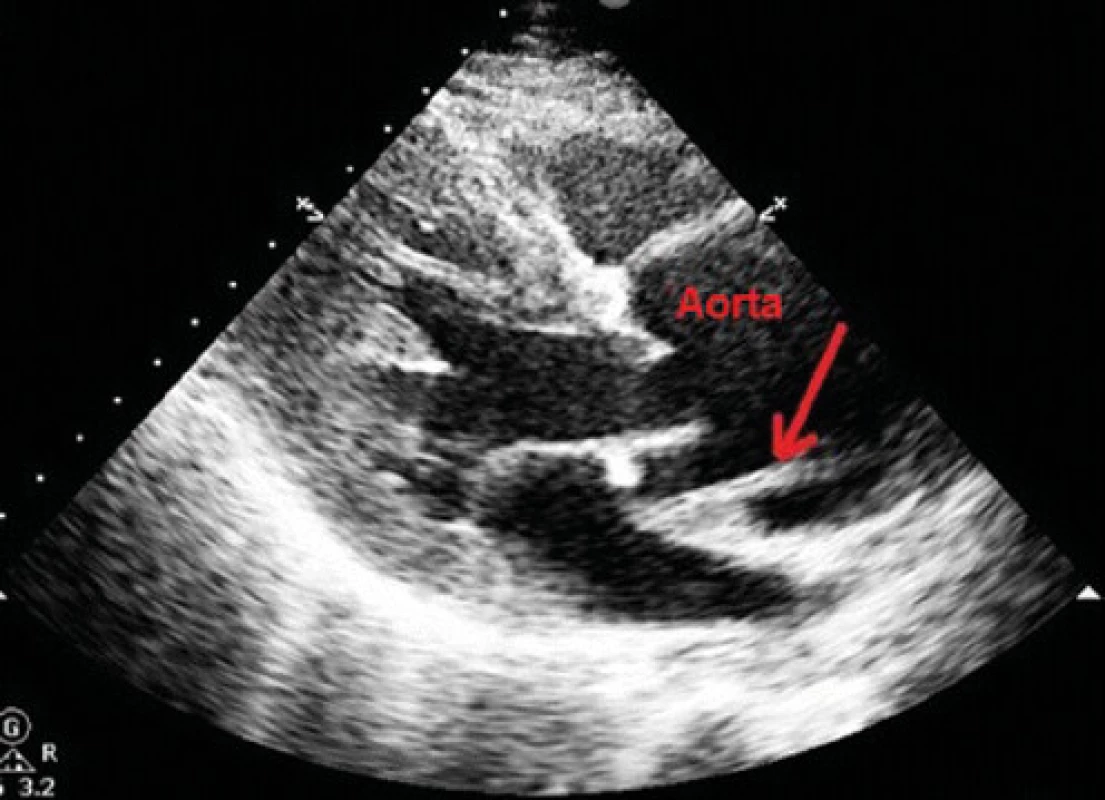
Image 5. CT vyšetrenie, ascendentná aorta 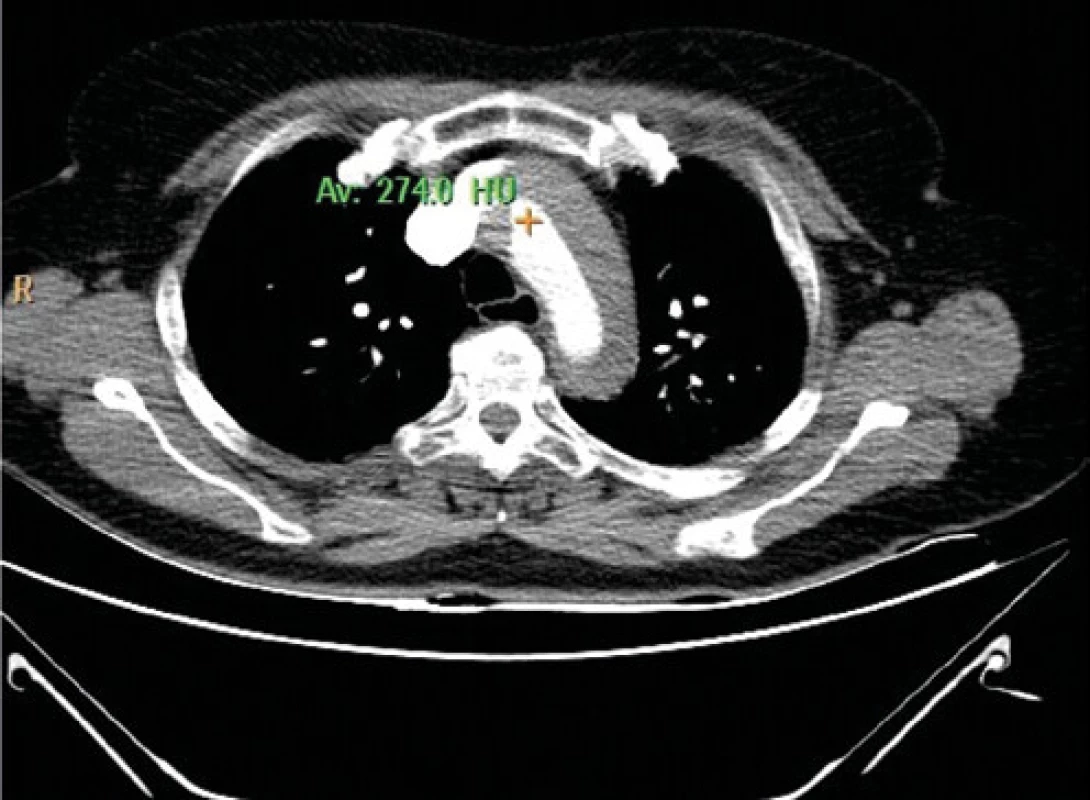
Diskusia
Disekcia aorty (DA) patrí spolu s intramurálnym hematómom a penetrujúcim aterosklerotickým vredom do skupiny akútnych aortálnych syndrómov, ktorých spoločným rysom je prienik krvi do médie aorty a spoločným príznakom intenzívna hrudná, tzv. aortálna bolesť. DA je spôsobená roztrhnutím intimy a médie s následnou redistribúciou toku krvi z aorty (pravé lumen) cez poškodenú intimu, čim sa oddelí od adventície a následne sa pod tlakom šíri a vzniká nové (falošné, nepravé) lumen. Primárna trhlina intimy postihuje väčšinou viac ako 50 % obvodu aorty a máva špirálovitý priebeh, pričom falošné lumen býva väčšie ako pravé (4). Osud disekcie a tým i pacienta závisí do značnej miery od miesta jej vzniku a rozsahu jej progresie. To viedlo k rôznym klasifikačným schémam a pôvodná DeBakeyho klasifikácia na tri základné typy je dnes nahradená Dailyho (stanfordskou) klasifikáciou, ktorá rozlišuje dva typy, typ A a typ B podľa miesta vzniku disekcie. U typu A je disekciou zasiahnutá ascendentná aorta s prípadnou propagáciou na ďalší úsek hrudnej alebo brušnej aorty. Typ B je chakterizovaný postihnutím descendentnej aorty s prípadnou progresiou na brušnú aortu. Z hľadiska spontánneho priebehu ochorenia a liečebnej stratégie je toto rozdelenie zásadné, pričom disekcia ascendentnej aorty oproti descendentnej je 2x častejšia (5). K najčastejším rizikovým faktorom DA patrí nedostatočne kontrolovaná artériová hypertenzia, ďalej vek, mužské pohlavie, fajčenie, preexistujúce ochorenie aorty alebo aortálnej chlopne, stavy po operácii srdca, tupé úrazy hrudníka, užívanie intravenóznych drog (kokaín, amfetamíny), pozitívna RA na ochorenia aorty (2, 6). Z preexistujúcich ochorení aorty a aortálnej chlopne sú to hlavne aneuryzmy aorty a a bikuspidálna aortálna chlopňa. Aneuryzmy postihujú rôzne časti aorty, typicky je to ascendentná časť aorty. Pacienti s torakálnou aneuryzmou aorty (TAA) sú najčastejšie asymptomatickí, až kým nedôjde k jej disekcii, alebo fatálnej ruptúre, preto bývajú odhalení najčastejšie pri zobrazovacom vyšetrení hrud ‑ níka z iného dôvodu alebo v rámci skríninku. Užitočnosť skríninku rizikových pacientov je dobre známa u pacientov s Marfanovým syndrómom a bikuspidálnou aortálnou chlopňou (1, 7, 8). Marfanov syndróm je autozomálne dominantne prenosné ochorenie spojiva, spojené s mutáciami génu pre fibrilin-1 na 15.chromozóne. Pacienti majú postihnuté všetky orgánové systémy, najzávažnejšie je postihnutie kardiovaskulárneho systému (v 80 %), pretože defektný fibrilín-1 spôsobuje chybné usporiadanie elastínových filamentov a nestabilitu steny aorty, čo vedie k vývoju aneuryzny aorty so závažnou aortálnou regurgitáciou, a najčastejšou príčinou smrti je disekcia alebo ruptúra aneuryzmy (7). Aortálna chlopňa je síce trojcípa, ale u 1–2 % populácie sa vyskytuje tzv. bikuspidálna aortálna chlopňa (BAV). V prípade vrodenej chyby je chlopňa už založená ako dvojcípa, može byť však založená aj ako trojcípa a vekom dôjde ku fúzii komisúry medzi dvomi cípmi, čím sa vytvorí funkčne bikuspidálna chlopňa. Za mechanizmus vzniku tejto anomálie pri vrodenej chybe sa považuje zápalový proces počas embryonálneho vývoja. Zhrubnuté spojivové tkanivo v úrovni komisúr sa nazýva raphe. BAV môže mať najprv normálnu funkciu, no vekom má oveľa vyššiu tendenciu vyvinúť stenotické zmeny a aj krvný tok pri „zdravej“ BAV je už alterovaný kvôli nepriaznivým hemodynamickým pomerom so vznikom aneuryzmy (9). Veľkosť aneuryzmy aorty je kľúčovým faktorom pre rozhodovanie pre intervenciu, pretože riziko disekcie alebo ruptúry prudko stúpa, ak priemer ascendentnej aorty presiahne 60 mm. Podľa posledných odporučení Európskej kardiologickej spoločnosti u pacientov s Marfanovým syndrómom by sa mala vykonať operácia pri maximálnom priemere aorty ≥ 50 mm a hranica ≥ 45 mm sa môže zvážiť u pacientov s ďalšími rizikovými faktormi ako pozitívna rodinná anamnéza, nárast aneuryzmy o viac ako 3 mm za rok, ťažká aortálna regurgitácia alebo plánovanie tehotenstva. U pacientov s BAV by sa mala vykonať operácia v prípade maximálneho priemeru aorty ≥ 55 mm, u týchto pacientov je nižšie riziko komplikácii ako u pacientov s Marfanovym syndrómom a hranica ≥ 50 mm sa môže zvážiť u pacientov s ďalšími rizikovými faktormi ako pozitívna rodinná anamnéza, arteriová hypertenzia, koarktácia aorty alebo nárast aneuryzmy o viac ako 3 mm za rok. U všetkých pacientov bez ohľadu na etiológiu by sa mala operácia vykonať s maximálnym priemerom aorty ≥ 55 mm (1). U našich pacientov bolo zaujímavé, že všetci traja mali síce dilatovanú ascendentnú aortu, ktorú ešte nebolo možné hodnotiť ako aneuryzma, v prípade, že by boli sledovaní, neboli by ešte indikovaní na intervenciu, k disekcii u nich došlo na relatívne benigne dilatovanej aorte. Pokým nie je indikovaná intervencia u pacientov s TAA postačuje podporná medikamentózna liečba a pravidelné sledovanie. Samozrejmosťou je adekvátna kontrola rizikových faktorov kardiovaskulárnych ochorení ako je strikná kontrola Tk, ako prvá liečba voľby by mali byť použité betablokátory, ktoré okrem zníženia Tk znižujú inotropiu srdca a srdcový výdaj, znižujú srdcovú frekvenciu a tým znižujú napätie cievnej steny. Pri ich nedostatočnom efekte možno pridať ACEI alebo blokátory receptorov 1 pre angiotenzín II. Vhodné je znižovať Tk na čo najnižšie tolerované hodnoty a vyhýbať sa výkyvom hodnôt Tk. Z ďalších liekov ovplyvňujúcich rizikové faktory kardiovaskulárnych ochorení sú indikované statíny, samozrejmosťou je stop fajčenie a vylúčenie veľkej fyzickej námahy (8). Hlavné symptómy ADAA sú zhrnuté na Obr. 6, náhle vzniknutá bolesť na hrudníku je jej najčastejším a najtypickejším príznakom. Nevyskytuje sa však u všetkých pacientov, alebo nemusí byť dominantná (1, 3), ako sme to videli u nášho prvého a druhého pacienta. DA je takmer vždy spojená s komplikáciami, príčinou ktorých je antegrádna a/alebo retrográdna propagácia disekcie na odstupujúce artérie (koronárne, cerebrálne, spinálne, viscerálne), ktoré vedú k ischémii v postihnutej oblasti a DAA môže byť príčinou tamponády, ruptúry aorty alebo aortálnej regurgitácie (10). Aortálna regurgitácia je spôsobená dilatáciou alebo roztrhnutím anulu a chlopňových cípov, dislokáciou cípov chlopne alebo interferenciou intimálneho flapu s jej cípmi (1, 11). Ischémia myokardu sa môže prejaviť u 10–15 % pacientov a je zapríčinená okrem propagácie disekcie upchatím lumenu koronárnej artérie intimálnym flapom, na EKG sa väčšinou prejavuje ako infarkt myokardu a spolu so zvýšenými hladinami troponínu môže spôsobiť fatálne chyby pri diagnostike bolesti na hrudníku (1, 12), ako sme to videli u našej pacientky. U našej pacientky bolo prvé EKG hodnotené lekárom RZS, ako vidieť na EKG (Obr. 3), sú prítomné elevácie ST segmentu, ale chýbajú recipročné depresie ST segmentu, teda nejednalo sa o typický EKG obraz akútneho koronárneho syndrómu s eleváciami ST segmentu, čo potvrdil aj operačný nález, ostium pravej koronárnej artérie nebolo postihnuté disekciou. Neurologické komplikácie sú často dramatické a zastierajú pravú príčinu javu (1, 13), ako sme to videli u našich dvoch pacientov. Základ v diagnostike ADAA tvorí anamnéza, fyzikálne vyšetrenie, EKG, zhodnotenie hemodynamického stavu a u stabilných pacientov stratifikácia pravdepodobnosti DA. V roku 2010 Americká asociácia ACC/AHA publikovala odhad rizika disekcie založený na troch skupinách rizikových faktorov: vysoko rizikové predisponujúce stavy, vysoko rizikový charakter bolesti a vysoko rizikové znaky pri klinickom vyšetrení (Obr. 7). Ak je prítomný faktor z jednotlivých skupín, počíta sa ako jeden bod, čiže pri 0-1-2-3 bodoch sa postupne zvyšuje odhadované riziko DA a treba to zvážiť pri diagnostickom postupe (1). Rogers a spol. v roku 2011 zhodnotili pacientov registrovaných v rokoch 1996-2009 v International Registry of Acute Aortic Dissectiona potvrdili, že uvedené klinické znaky, ktoré boli navrhnuté ACC/AHA v roku 2010 sú vysoko senzitívna pomôcka v stratifikácii pravdepodobnosti DA u stabilných pacientov ako ADD‑RS (Aortic Dissection Detection Risk Score) (14). U nášho prvého a druhého pacienta v úvode ochorenia nebol známy predisponujúci rizikový stav, chýbala náhle vzniknutá bolesť na hrudníku, dominoval neurologický deficit, čo viedlo k tomu, že na ADAA nemyslelo. U tretieho pacienta, ženy, rovnako chýbal známy predisponujúci rizikový stav, dominovala charakteristická bolesť na hrudníku, prvým vyšetrujúcim lekárom bol prehliadnutý diastolický šelest nad aortou a na základe chybne zhodnoteného EKG bola pacientka manažovaná ako akútny koronárny syndróm. Dnes najbežnejšie používaným vyšetrením pri podozrení na DA je CT vyšetrenie s kontrastom, ktoré je rýchlo vykonateľné a bežne dostupné, má senzitivitu 100% a špecificitu 98% a dokáže ju temer s istotou vylúčiť alebo potvrdiť. Kľúčovým nálezom je zistenie intimálneho flapu, ktorý oddeľuje dva lumeny, ďalej zistenie priemeru aorty, dĺžku a priemer falošného a pravého lumenu, a vzdialenosť intimálnej trhliny k odstupujúcim vitálnym artériám (6, 15). Môžeme sa však stretnúť aj s falošne pozitívnymi nálezmi, pričom väčšina diagnostických omylov je spôsobená kombináciou malej skúsenosti vyšetrujúceho lekára a prítomnosti pohybových artefaktov simulujúcich flap v ascendentnej aorte, ktorý sa zobrazuje ako pohyblivý intraluminálny defekt náplne a je spôsobený pohybom pulzujúcej ascendentnej aorty medzi end‑diastolou a end‑systolou, pretože koreň aorty a priľahlá časť proximálnej ascendentnej aorty sa pobybuje s ľavou komorou (16). V tomto prípade je potrené zmraziť pulzácie a pohyby aortálnej steny a tak efektívne eliminovať pohybové artefakty predovšetkým v oblasti aortálnej chlopne a koronárnych artérií, čo je možné pomocou CT vyšetrenia s EKG gatingom, ktorý rozlíši flap od artefaktu (1). Napriek tomu CT vyšetrenie s kontrastom má superiórnu výpovednú hodnotu v diagnostike a zistenie rozsahu ADAA a detekcii ostatných akútnych aortálnych syndrómov. Na druhej strane TTE vyšetrenie srdca sa využíva hlavne u kriticky ne ‑ stabilných pacientov, u ktorých môže potvrdiť diagnózu ADAA a taktiež sa môže používať za účelom monitoringu na operačnej sále prípadne v pooperačnom období (1). Iniciálnou liečbou pacientov s ADAA je medikamentózna liečba na kontrolu arteriovej hypertenzie a bolesti.V liečbe arteriovej hypertenzie sú preferované krátko účinkujúce betablokátory podávané intravenózne, ktoré znižujú Tk a pulz a ochraňujú myokard pred ischémiou. Hodnoty systolického Tk by sa mali pohybovať v rozmedzí 100 až 120 mmHg a pulzu 60/min., na kontrolu bolesti je preferovaný morfín (6). Vazodilatačná liečba ako blokátory kalciového kanála alebo nitráty sú indikované v emergentnej situácii na redukciu vysokých hodnôt Tk (1), ktorú naši pacienti nevyžadovali. Na rozdiel od akútnej disekcie descendentnej aorty, kde sú dnes preferované intervenčné výkony v subakútnom štádiu po predchádzajúcej konzervatívnej liečbe, zlatým štandardom v liečbe ADAA je chirurgická liečba, ktorej hlavným cieľom je prevencia ruptúry aorty, tamponády srdca a zníženie aortálnej regurgitácie. Ďalšou dôležitou súčasťou operácie je zlepšiť prekrvenie disekciou postihnutých artérií (1, 3, 12). Základom chirurgickej liečby je resekcia poškodeného segmentu aorty a zabránenie vstupu krvi do falošného lumenu, ako primárnu intimálnu trhlinu (entry), tak aj prípadne ďalšie trhliny (reentry) v priebehu aorty. Pri voľbe operácie zohráva dôležitú úlohu aortálna chlopňa. V prípade, že aortálna chlopňa je trojcípa a nie je postihnutá aortálnou regurgitáciou alebo centrálnou regurgitáciou kvôli dilatácii anulu, je možné vykonať tzv. záchovnú operáciu aortálnej chlopne. Jednou z nich je Davidova operácia, reimplantácia aortálnej chlopne do tubulárneho graftu, nakoniec sa do graftu reimplantujú koronárne artérie. Ďalšou alternatívnou je klasická alebo modifikovaná Yacoubova operácia, ktorá bola realizovaná u nášho prvého pacienta, pri ktorej sa reimplantuje len aortálny sínus a tým pádom je tu väčšie riziko pre neskoršiu dilatáciu anulu. Môže to vyriešiť dodatočná anuloplastika, kde sa pomocou anulárnych ringov alebo sutúr posilňuje samotný anulus. Davidova operácia na špecializovaných pracoviskách môže byť uplatnená taktiež u pacientov s BAV a s aortálnou regurgitáciou, ktorá má iný pôvod ako dilatácia anulu. Tieto tzv. záchovné operácie napriek časovej a technickej náročnosti zbavujú pacienta nevýhod spojených s implatnovnými chlopňovými náhradami (1, 17). V prípade akýchkoľvek pochybností o trvácnosti výsledku po záchovnej operácii ako aj v prípade, že je minimálne jeden Valsavov sínus postihnutý, je potrebné nahradiť celý koreň aorty a nie len vykonať suprakoronárnu náhradu aorty, pretože hrozí riziko redisekcie, resp. opätovnej dilatácie a vzniku aortálnej regurgitácie. V tomto prípade prichádza do úvahy operácia podľa Bentalla, pri ktorej sa vykoná resekcia aneuryzmy a taktiež aortálneho anulu s aortálnou chlopňou, môže sa vykonať klasická náhrada aorty s graftom, ktorý obsahuje mechanický alebo biologický kompozit aortálnej chlopne do ktorého sú všité koronárne artérie vo forme terčíkov, a výber typu protézy závisí od veku, komorbidít, prípadných kontraindikácií pacienta. Táto operácia bola vykonaná u našej tretej pacientky. Hybridná operácia pozostáva z kombinácie chirurgickej a endovaskulárnej liečby v „jednom sedení“ (1, 18, 19) bola vykonaná u nášho druhého pacienta. Z pooperačných komplikácií sa vyskytuje NCMP u 2–16 % pacientov, k veľkým pooperačným komplikáciám patrí obličkové zlyhanie, poškodenie miechy, krvácanie do mediastína, chylotorax a mediastinitída u 3–10 % pacientov. Z našich pacientov u druhého bol pooperačný priebeh komplikovaný NCMP a zlyhávaním obličiek, a zlyhávanie obličiek komplikovalo pooperačný priebeh aj u prvého pacienta.V oboch prípadoch pacienti nevyžadovali hemodyalýzu a stav bol zvládnutý konzervatívne. Včasná pooperačná mortalita ostáva vysoká, varíruje od 5 % do 20 %, no nespornou výhodou operačnej liečby je, že znižuje jednomesačnú mortalitu z 90 % na 30 %. Mortalita pacientov s ADAA je stále vysoká, 30 % pacientov zomiera po príchode na urgentný príjem, mnohokrát pred stanovením diagnózy. Celková mortalita varíruje od 20 % do 30 %, najviac pacientov zomiera v prvých 10 dňoch. Viaceré štúdie dokázali, že multidisciplinárny tím zložený z kardiológov, invazívnych rádiológov, kardiochirurgov, anesteziológov, nefrológov a pulmológov vo väčších centrách pacientom s ADAA zvyšujú šancu nielen na prežitie, ale aj na kvalitnejší život po operácii (19, 20, 21).
Image 6. Symptómy akútnej disekcie ascendentnej aorty (voľne spracované podľa 1, 3) 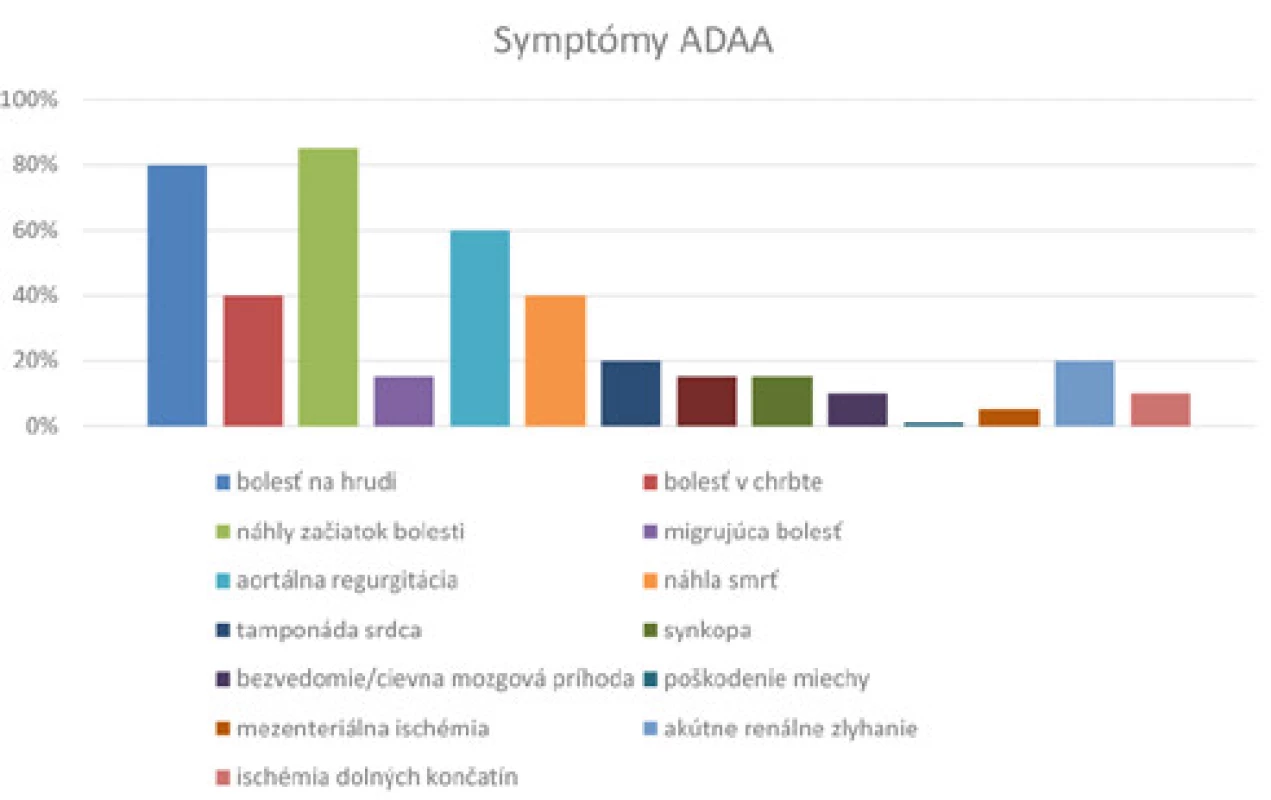
Table 1. Odhad rizika disekcie aorty (voľne spracované podľa 1, 12) 
Záver
CT vyšetrenie s kontrastom má centrálnu úlohu nielen v diagnostike, ale aj v stratifikácii rizika a v manažmente akútnych aortálnych syndrómov. Jeho výhodou je aj krátky čas potrebný na získanie a spracovanie obrazu, možnosť získať komplexný trojrozmerný obraz celej aorty a tiež jeho široká dostupnosť. Aj napriek tomu môže dôjsť k omylu, a to najčastejšie z artefaktov pulzácie, ktoré môžu imitovať intimálny flap, preto je dôležité pri podozrení na DAA používať CT vyšetrenie s EKG gatingom. Na druhej strane bežne dostupné CT vyšetrenie s kontrastom v rukách skúseného lekára môže odhaliť DAA, na ktorú sa v úvode vyšetrenia nemyslí, ak v klinickom obraze dominujú jej komplikácie, ako sme to videli u prezentovaných pacientov.
Poznámka: Diskusiu napísala Veronika Jankovičová Pacientov vyšetrila a opísala Margita Belicová
KORESPONDENČNÍ ADRESA AUTORA:
doc. MUDr. Margita Belicová, PhD.,
I. interná klinika, Univerzitná nemocnica,
Kollárova 2,
03659 Martin,
Slovensko
Cit. zkr: Vnitř Lék 2020; 66(8): e55–e60
Článek přijat redakcí: 18. 3. 2020
Článek přijat po recenzích k publikaci: 20. 11. 2020
Sources
1. Erbel R, Aboyans V, Boileau C, et al. The Task Force for the Diagnosis and Treatment of Aortic Diseases of the European Society of Cardiology (ESC). Eur Heart J 2014; 35 : 2873–2926.
2. Gawinecka J, Schonrath F, von Eckardstein A. Acute aortic dissection: pathogenesis, risk factors and diagnosis. Swiss Med Wkly. 2017; (25); 147: w14489. doi: 10.4414/smw.2017.14489. e Collection 2017.
3. Lau C, Leonard JR, Iannacone E, Gaudino M, Girardi LN. Surgery for Acute Presentation of Thoracoabdominal Aortic Disease. Semin. Thorac. Cardiovasc. Surg. 2019; 31(1): 11-16.
4. Baliyan V, Parakh A, Prabhakar AM, Hedgire S. Acute aortic syndromes and aortic emergencies. Cardiovasc Diagn Ther. 2018; 8(1): S82–S96.
5. Berretta P, Cefarelli M, Montalto A, et al. Surgical indications for thoracic aortic disease: beyond the „magicnumbers“ of aortic diameter. Ital Cardiol. 2018; 19(7): 429–436.
6. Nienaber CA, Powell JT. Management of acute aortic syndromes. Eur Heart J. 2012; 33 : 26–35 b.
7. Isselbacher EM, Lino Cardenas CL, Lindsay ME. Hereditary influence in thoracic aortic aneurysm and dissection. Circulation. 2016; 133(24): 2516–2528.
8. Rozado J, Martin M, Pascual I, et al. Comparing American, European and Asian practice guidelines for aortic diseases. J Thocac, DiS. 2017; 9(6): S551–S560.
9. Catherine M. Otto. Textbook of clinical echocardiography. 5th edition. Philadephia: El ‑ sevier, 2013. ISBN 978-1-14557-287-2. Chapter 11, Valvular stenosis, p. 271–298.
10. Zeng T, Shi L, Ji Q, et al. Cytokines in aortic dissection. Clin. Chim. Acta. 2018; 486 : 177–182.
11. Klompas M. Does this patient have an acute thoracic aortic dissection? JAMA 2002; 287 : 2262–2272.
12. Kreibich M, Bavaria JE, Branchetti E, et al. Management of Patients With Coronary Artery Malperfusion Secondary to Type A Aortic Dissection. Ann Thorac Sur. 2019; 107(4): 1174–1180.
13. Di Eusanio M, Trimarchi S, Patel HJ et al. Clinical presentation, management, and short‑term out come of patients with type A acute dissection complicated by mesenteric malperfusion: observations from the International Registry of Acute Aortic Dissection. J Thorac Cardiovasc Surg. 2013; 145 : 385–390.
14. Rogers AM, Hermann LK, Booher AM, et al. Sensitivity of the aortic dissection detection risk score, a novel guideline‑based tool for identification of acute aortic dissection at initial presentation: results from the international registry of acute aortic dissection. Circulation 2011; 123 : 2213–2218.
15. Nienaber CA, Clough RE. Management of acute aortic dissection. Lancet 2015; 385 : 800–811.
16. Hansen MS, Nogareda GJ, Hutchison SJ. Frequency of and inappropriate treatment of misdiagnosis of acute aortic dissection. Am J Cardiol 2007; 99 : 852–856.
17. Bechtel JF, Erasmi AW, Misfeld M, Sievers HH. Reconstructive surgery of the aortic valve: the Ross, David and Yacoub procedures. Herz 2006; 31(5): 413–422.
18. Goldfinger JZ, Halperin JL, Marin ML, et al. Thoracic aortic aneurysm and dissection. J Am CollCardiol. 2014; 64 : 1725–1739.
19. Nishida H, Tabata M, Fukui T, et al. A systemic approach to improve the outcomes of type A aortic dissection. J ThoracCardiovacsSurg. 2017; 154 : 89–96.
20. Gomibuchi T, Seto T, Komatsu M, Tanaka H, Ichimura H, Yamamoto T, Ohashi N, Wada Y, Okada K. Impact of Frailty on Outcomes in Acute Type A Aortic Dissection. Ann. Thorac. Surg. 2018; 106(5): 1349–1355.
21. Kim JH, Choi JB, Kim TY, Kim KH, Kuh JH. Simplified surgical approach to improve surgical outcomes in the center with a small volume of acute type A aortic dissection surgery. Technol Health Care. 2018; 26(4): 675–685.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2020 Issue 8-
All articles in this issue
- Změny farmakokinetiky léčiv u obézních pacientů
- Chirurgická léčba těžké obezity – bariatrie
- Současnost a perspektivy farmakoterapie obezity
- Fyzická aktivita v léčbě obezity v praxi
- Jak léčit obézního hypertonika?
- Suplementácia vitamínu D ako dôležitý faktor v prevencii a liečbe ochorenia COVID-19: aké máme dôkazy?
- Protidestičková léčba v sekundární prevenci nekardioembolických ischemických mozkových cévních příhod
- Věkem podmíněná remodelace myokardu: mýtus nebo realita?
- Fixní kombinace rosuvastatinu s ezetimibem
- Vplyv ageizmu na správnosť indikácie antikoagulancií u seniorov s fibriláciou predsiení v práci kardiologickej ambulancie medzi rokmi 2012 a 2017
- Akutní infekce, žilní trombóza a doporučená tromboprofylaxe
- Hypogonadismus obézních mužů
- Péče o hospitalizovaného dialyzovaného pacienta z pohledu internisty
- Monitorování farmakokinetiky infliximabu u idiopatických střevních zánětů
- Heparínom indukovaná trombocytopénia a aktuálne možnosti liečby – prehľad literatúry
- Neobvyklá manifestace CMV infekce – cirkulární stenóza žaludku
- Nebezpečí číhající v mořích – komplikace setkání s jedovatou rybou ropušnicí obecnou (Scorpion fish)
- Disekcia ascendentnej aorty, diagnóza na ktorú treba myslieť
- Prof. Jiří Šonka a obezitologie
- Molekula erdostein společnosti Recipharm byla s pozitivním výsledkem testována jako součást léčby pacientů s COVID-19
- Antioxidační a bronchoprotektivní účinek erdosteinu
- Zkrácená informace o přípravku ERDOMED
- K 100. výročí narození prof. MUDr. Jiřího Šonky, DrSc.
- 2020: rok, kdy ambulantní internisté vzali budoucnost do svých rukou. Konečně!
- Programy kvality Q‑OSTEOPORÓZA a Q‑DYSLIPIDEMIE – cesta k dlouhodobé stabilitě v oboru
- 110. výročí narození primáře Kadeřábka
- Role metabolického syndrome v indukci chronické pankreatitidy po první atace akutní pankreatitidy – multicentrická studie
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Péče o hospitalizovaného dialyzovaného pacienta z pohledu internisty
- Změny farmakokinetiky léčiv u obézních pacientů
- Heparínom indukovaná trombocytopénia a aktuálne možnosti liečby – prehľad literatúry
- Nebezpečí číhající v mořích – komplikace setkání s jedovatou rybou ropušnicí obecnou (Scorpion fish)
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

