-
Medical journals
- Career
Chřipka a její komplikace
Authors: Adam Vitouš; František Stejskal
Authors‘ workplace: Technická univerzita Liberec, Klinika infekčních nemocí, 2. LF UK a Nemocnice Na Bulovce, Praha ; Ústav imunologie a mikrobiologie, 1. LF UK a VFN, Praha ; Infekční oddělení, Krajská nemocnice Liberec, a. s.
Published in: Vnitř Lék 2020; 66(6): 360-362
Category:
Overview
Chřipka je akutní virová respirační infekce. V oblastech mírného pásma způsobuje v chladném období sezónní epidemie různého rozsahu. V populaci při nich dochází nejen k významnému nárůstu nemocnosti a pracovních neschopností, ale nemalá část nemocných na infekci nebo její komplikace každoročně umírá, i přes existující terapii a efektivní vakcinaci.
Klíčová slova:
chřipka – infekce – komplikace – vakcína – Influenza
Historie a etiologie
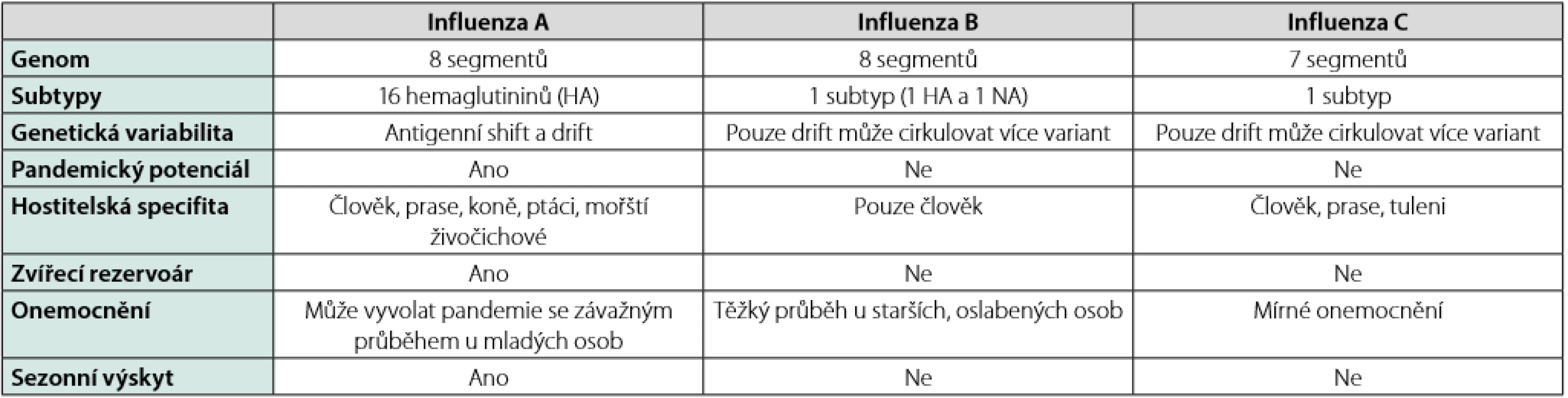
Původcem chřipky (influenza) jsou obalené RNA viry patřící do čeledi Orthomyxoviridae, které se řadí do tří samostatných rodů: influenza A, influenza B a influenza C. Charakteristickým rysem chřipkových virů je segmentovaný genom, který tvoří jednořetězcová ribonukleová kyselina negativní polarity (ssRNA). Virus chřipky typu A a B obsahuje osm segmentů RNA uložených ve formě ribonukleoproteinu, virus chřipky typu C nese pouze sedm segmentů. Na povrchu virionů u chřipky typu A a B jsou dva glykoproteiny, hemaglutinin (HA) a neuraminidáza (NA). Viry chřipky typu A se na základě struktury povrchového hemaglutininu (H1‑16) a neuraminidázy (N1‑9) dále dělí na subtypy (tabulka 1). Tyto povrchové glykoproteiny jsou odpovědné za vazbu na povrch hostitelské buňky a HA indukují tvorbu protilátek. Protilátky proti neuraminidáze mohou blokovat uvolňování viru z hostitelské buňky.
Virus chřipky A je geneticky labilní. Četnost mutací jeho genomu je přibližně 300× vyšší než u jiných mikroorganismů (1). Antigenní drift je způ ‑ soben bodovými mutacemi povrchových antigenů viru. Změna ovlivňuje virulenci jednotlivých subtypů a obchází imunitní obranné mechanismy (např. drift typu A/H2N2 Singapore 225/99 na A/H2N2 New Delhi 033/01). Druhou, větší, ale méně frekventní genetickou změnou u influenzy je antigenní shift. Při shiftu dochází k výměně celého segmentu genů pro jednotlivé antigeny. Vzniká pravděpodobně při současné infekci různými typy chřipky u prasat, která jsou vnímavá jak k humánní, tak aviární influenze. Drift při zachování základní antigenní struktury nepůsobí významné změny v morbiditě. Naproti tomu shift s objevením se nového (či dlouho necirkulujícího kmene) má potenciál způsobit pandemii, protože populace nemá proti novému typu chřipky protilátky.
Nejdramatičtější dokumentovaná lidská pandemie vyvolaná novým kmenem chřipky byla chřipka španělská. V letech 1918–1920 typ A/H1N1 usmrtil mezi 20–40 miliony lidí, což představovalo 1–2 % tehdejší populace. Asijská chřipka v roce 1957 (typ A/H2N2) usmrtila 2–4 miliony lidí, chřipka Hongkong 1968 (A/H3N2) měla také kolem 2 miliónů obětí. Sezónně se odhaduje, že na chřipku a její komplikace zemře kolem 0,5 milionu lidí. Vysoká mortalita na španělskou chřipku se vysvětluje meziválečnou chudobou a neznalostí antiinfekční léčby (2), další pandemie již naštěstí takto vysokých čísel nedosáhly.
Patofyziologie a epidemiologie
Influenza A působí nejvíce infekcí u lidí i zvířat. Typ B je u lidí druhý nejčastější a typ C se vyskytuje minoritně a nezpůsobuje epidemie. Inkubační doba chřipky je 1–4 dny. Vylučování viru začíná zhruba den před nástupem příznaků, trvá obvykle 2–5 dnů a zhruba koreluje s febrilní fází onemocnění. U imunosuprimovaných osob a u dětí může být vylučování viru prodlouženo, na 2–3 týdny (3). K mezilidskému přenosu dochází kapénkovou cestou. Infikovaný člověk vykašlává kapénky o velikosti 2–10 mikrometrů do svého okolí, arbitrárně se uvádí až do vzdálenosti 2 metrů (4). Virus se v aerosolu z dýchacích cest dostává do okolí i na větší vzdálenost, ale v menší míře, i při hlasitém mluvení, křiku nebo například zpěvu. Proto může být pro své okolí infekční i člověk, který nekašle (4). Avšak oproti přímému kontaktu tváří v tvář s kašlajícím člověkem je tento způsob přenosu méně rizikový a zpravidla vyžaduje delší kontaktní dobu s nemocným. Virus je poměrně rezistentní vůči zevnímu prostředí, a proto dochází k přenosu infekce též kontaminovanými předměty. Při pokojové teplotě si zachovává infekčnost na tvrdých neporézních předmětech (ocel, plast) 24–48 hodin, na porézních suchých materiálech (papír, plátno) 8–12 hodin, na porézních vlhkých materiálech až 72 hodin, na bavlněných tkaninách několik týdnů a na suchých rukou 15 minut až 3 hodiny. Virus je citlivý vůči všem běžně používaným dezinfekčním činidlům a lze jej poměrně snadno a účinně zlikvidovat jakýmkoli detergentem (mýdlo, prostředky na umývání nádobí, prací prášky apod.). Ptačí chřipka se může na člověka přenést přímým kontaktem s infikovaným zvířetem nebo jeho trusem a sporadicky vyvolat i těžká onemocnění (5).
Po vdechnutí infekčního aerosolu se virus naváže prostřednictvím hemaglutininu na receptory epitelu respiračního traktu a endocytózou vstupuje do buněk. Uvnitř buňky se replikují nové viriony, dochází k buněčné dysfunkci s následnou apoptózou. Z odumírajících buněk jsou pomocí neuraminidázy uvolňovány viriony, které infikují další epiteliální buňky. Vyplavením zánětlivých cytokinů se spouští systémové projevy infekce.
Klinické příznaky
Chřipku obvykle charakterizuje náhlý (během 24 hodin) rozvoj příznaků: horečka, kašel, bolest v hrdle, myalgie, bolesti hlavy, slabost a únava, tachykardie. Hyperémie spojivek dokresluje obraz virové respirační infekce. Kašel je zpravidla suchý, objevuje se s latencí za iniciální horečkou a může být provázen pleurálními bolestmi. Infekce některými subtypy chřipky jsou první hodiny až dny charakterizovány kromě respiračních příznaků i průjmem a zvracením, které bývají častější u dětí. Horečka a další celkové příznaky obvykle do 3 dnů ustoupí, k úplné úpravě stavu dochází do týdne. Klinický průběh může být mitigován předchozí vakcinací nebo dřívější infekcí, rovněž může být provázen i rýmou a vytvářet tak obraz nezávážné respirační virózy. Pacienti s mírnými průběhy většinou v klinické praxi lékaře nevyhledají, ale mají epidemiologický význam v šíření viru. Typicky se však chřipka projevuje jako akutní horečnaté onemocnění s celkovým obrazem těžší systémové infekce, častěji u rizikových skupin pacientů (tabulka 2).
Table 2. Rizikové skupiny pacientů 
Diagnostika
Ribonukleová kyselina chřipky je detekována polymerázovou řetězcovou reakcí (real‑time, RT ‑PCR). Materiál je získán nasofaryngeálním stěrem, může být vyšetřeno i sputum nebo bronchoalveolární aspirát u ventilovaných pacientů. Sérologické a další nepřímé metody jsou v akutním stavu nepřínosné. Rychlotesty na bázi imunoenzymatických reakcí detekující antigeny chřipky mají i přes poměrně vysokou specifitu nízkou senzitivitu, proto se v klinické praxi upřednostňuje metoda RT ‑PCR. K vyšetření jsou v chřipkové sezóně indikováni všichni pacienti hospitalizovaní pro akutní respirační infekci a v ambulantní praxi všichni pacienti s vysokým rizikem těžšího průběhu (stejná skupina pacientů, která je indikována k vakcinaci, tabulka 2). U lehkých a středně těžce probíhajících infekcí nevykazují výsledky běžných laboratorních vyšetření významné odchylky, u těžších průběhů včetně primární virové pneumonie bývají laboratorní změny již zřetelné, včetně elevace zánětlivých parametrů imitující bakteriální infekci. U virové pneumonie jsou však antibiotika neúčinná a je třeba rychlé diagnostiky a terapie virostatiky.
Terapie
Aktuálně se v léčbě influenzy doporučují inhibitory neuraminidázy – perorální oseltamivir v dávce 75 mg à 12 h, inhalační zanamivir 10 mg à 12 h a intravenózní peramivir v jednorázové dávce 600 mg u dospělých. Inhalační virostatikum může být upřednostněno v graviditě pro omezené systémové působení. Standardní délka terapie je 5 dní. Vyšší dávkování a prodloužená doba terapie u kriticky nemocných či obézních pacientů je široce akceptována, ale nemá jednoznačně prokázaný efekt oproti dávkování standardnímu (7). V posledních letech jsou uváděny do praxe nové protivirové léky jako favipiravir (inhibitor RNA polymerázy) nebo baloxavir marboxil (inhibitor endonukleázy), se slibnými výsledky (8). Léčba chřipky je nejefektivnější, pokud se zahájí včas (do 48 h), a je plně indikována u pacientů s rizikem komplikovaného průběhu (tabulka 2).
Komplikace
Nejvážnější komplikací influenzy je pneumonie. Primární virová pneumonie se manifestuje obvykle mezi 5.–7. dnem nemoci progresivní dušností, hypoxemií a oboustrannými plicními infiltráty v RTG či CT obraze. Riziko rozvoje této obávané primární komplikace je vyšší v graviditě (3. trimestr), u pacientů s kardiovaskulárním rizikem a v pokročilém věku. Během pandemií byla však intersticiální pneumonie pozorována i u mladých nemocných bez známých rizikových faktorů.
Sekundární bakteriální infekce (sinusitida, pneumonie) v terénu poškozeného respiračního epitelu vyvolává nejčastěji Staphylococcus aureus a Streptococcus pneumoniae, méně frekventně Streptococcus pyogenes, Hemophilus influenzae a další gramnegativní bakterie. Komplikující bakteriální pneumonie se objevují po přechodném zlepšení stavu při probíhající chřipce s novým vzestupem teploty, vykašláváním sputa s příměsí krve, leukocytózou nad 15 tisíc/µl, elevací prokalcitoninu a CRP, hypoxemií a změnou RTG nálezu. Obávané mohou být stafylokokové pneumonie, zejména v lokalitách s výskytem MRSA (meticilin rezistentní S. aureus) pro opožděný či minimální efekt běžně používaných antibiotik (6).
Myositida se prezentuje trvajícími myalgiemi s elevací svalových enzymů z probíhající rhabdomyolýzy s myoglobinurií, která může vzácně vést až renálnímu selhání. Rovněž myokarditaida a perikarditaida je občasnou komplikací chřipky.
Pacienti s kardiovaskulárním onemocněním mají prokazatelně vyšší riziko komplikací při chřipce než ostatní populace (9, 10). Relativní riziko rozvoje akutního infarktu myokardu (IM) v horizontu týdne od diagnostiky respirační infekce bylo v několika studiích u chřipky B 10,1 (95% CI 4,37–23,38), u chřipky A 5,17 (95% CI 3,02–9,84), RS viru 3,51 (95% CI 1,11–11,12) a 2,77 pro ostatní virové respirační infekce (9). Rozvoj myokardiálního poškození nelze vysvětlit jen klimatickými jevy, hypoxemií, tachykardií či zánětem indukovaným prokoagulačním stavem a nestabilitou aterosklerotického plátu, ale i vlastním působením viru influenzy, neboť vakcinace proti chřipce snižuje i riziko akutního IM (11, 12, 13, 14).
Komplikace centrální nervové soustavy pod obrazem encefalitidy, myelitidy nebo syndromu Guillain ‑Barré jsou naštěstí vzácné.
Prevence
Nejvýznamnější prevencí chřipky je vakcinace. Světová zdravotnická organizace (WHO) každoročně vydává doporučení k vakcinaci nebo úpravě stávajících vakcín podle aktuálního výskytu cirkulujících typů chřipky. Pro sezónu 2019/20 tak byly doporučeny vakcíny obsahující 2 kmeny chřipky A (H1N1 a H3N2) a dva různé kmeny chřipky B. Pro sezónu 2020/21 bude opět doporučena kvadruvalentní vakcína s mírnými úpravami jednotlivých komponent. Celosvětově existuje více typů vakcín, parenterální inaktivované, rekombinantní, vysokodávkované a intradermální nebo živé oslabené intranazální. Řada z nich není v ČR registrována, v našich podmínkách zůstávají standardem intramuskulární inaktivované vakcíny. U dospělých se aplikuje jedna dávka, ideálně těsně před začátkem chřipkové sezóny. Dle zkušeností z posledních let je optimální vakcinovat od října do začátku prosince. Účinnost vakcíny je sezónní a nastupuje nejdříve po 7 dnech od vakcinace.
Mimovakcinační formy prevence jsou založeny na omezení vylučování viru u nemocných: distanční omezení, nošení roušky a dodržování hygienických návyků ve smyslu správné etikety kašle a mytí rukou. V nemocnicích i sociálních zařízeních se v prevenci šíření chřipky doporučuje očkování zaměstnanců a principy kapénkových a kontaktních izolačních režimů.
Závěr
Influenza patří mezi časté respirační infekce. Vyskytuje se celosvětově v sezónních epidemiích. Rozsah lokálního výskytu s potenciálem vzniku pandemie při vzniku nového kmene po genetické mutaci nelze spolehlivě předvídat. I přes existující antivirovou léčbu a bezpečné efektivní vakcíny jsou stále v souvislosti s touto nemocí nebo jejími komplikacemi hospitalizovány miliony lidí a statisíce jich na tuto nemoc každý rok umírá. Očkování je významným preventivním opatřením, které zabrání vážnému průběhu, a tudíž i komplikacím chřipky, ale bohužel je proočkovanost proti chřipce v České republice ve srovnání se západními zeměmi Evropy na nízké úrovni. Je tedy potřeba soustavnou osvětou vyvracet vědou nepodložené argumenty odmítačů očkování a tuto situaci změnit. Zejména u rizikových pacientů je žádoucí, aby doporučení k vakcinaci bylo aktivně podpořeno i jejich ošetřujícími specialisty (kardiolog, pneumolog, nefrolog ad.).
KORESPONDENČNÍ ADRESA AUTORA:
MUDr. Adam Vitouš,
Infekční oddělení,
Krajská nemocnice Liberec, a.s.,
Technická univerzita Liberec,
Husova 10,
460 01 Liberec
Cit. zkr: Vnitř Lék 2020; 66(8): 360–362 Článek přijat redakcí: 28. 7. 2020 Článek přijat po recenzích k publikaci: 1. 9. 2020
Sources
1. Drake JW. Rates of spontaneous mutation among RNA viruses. Proc Natl Acad Sci, USA 1993. 90(9): 4171–4175.
2. Kilbourne ED. Influenza pandemics of 20th century. Emerg Infect, DiS. 2006 Jan. 12(1): 9–14.
3. Centers for Disease Control and Prevention, National Center for Immunization and Respiratory Diseases (NCIRD), www.cdc.gov/flu/about/disease/spread.htm
4. Bridges CB, Kuehnert MJ, Hall CB. Transmission of influenza: implications for control in health care settings. Clin Infect, DiS. 2003; 37 : 1094–1101 10.1086/378292.
5. Avian influenza: fact sheet. World Health Organization. www.who.int/mediacentre/ factsheet/avian_influenza/en/print.html
6. Tasher D, Stein M, Simoea EA, et al. Invasive bacterial infections in relation to influenza outbreaks, 2006–2010. Clin Inf, DiS. 2011 Dec. 53(12): 1199–207.
7. Won Suk Choi, Ji Hyeon Baek, Yu Bin Seo, et al. Severe influenza treatment guidelines. Transgovernmental Enterprise for Pandemic Influenza in Korea Korean J Intern Med 2014; 29 : 132–147. 2014 pISSN 1226‑3303 eISSN 2005–6648 http://www.kjim.org.
8. Kotey E, Lukosaityte D, et al. Current and Novel Approaches in Influenza Management. Vaccines (Basel). 2019 Jun; 7(2): 53.9.
9. Kwong JC, Schwartz KL, Cempitelli MA, et al. Acute Myocardial Infarction after Laboratory ‑confirmed Influenza Infection. N Engl J Med 2018, 378 : 345. 10.
10. Waren ‑Gash C, Bhaskaran K, Hayward A, et al. Circulating influenza virus, clima ‑ tic factors and acute myocardial infarction: a time series study in England and Wales and Hong Kong. J Infect Dis 2011. 203 : 1710.
11. Naghavi M, Barlas Z, Siadaty S, et al. Association of influenza vaccination and reduced risk of recurrent myocardial infarction. Circulation 2000;102 : 3039–45.
12.Puig ‑Barbera J, Diez ‑Domingo J, Varea A, et al. Effectiveness of MF59‑adjuvanted subunit influenza vaccine in preventing hospitalisations for cardiovascular disease, cerebrovascular disease and pneumonia in the elderly. Vaccine 2007; 25 : 7313–7321.
13. Siriwardena AN, Gwini SM, Coupland CA. Influenza vaccination, pneumococcal vaccination and risk of acute myocardial infarction: matched case ‑control study. CMAJ 2010; 182 : 1617–1623.
14. Warren ‑Gash C, Blackburn R, et al. Laboratory ‑confirmed respiratory infections as triggers for acute myocardial infarction and stroke: a self ‑controlled case series analysis of national linked datasets from Scotland. European Respiratory Journal 2018 51 : 1701794.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2020 Issue 6-
All articles in this issue
- Anafylaxe – akutní a dlouhodobý management
- Potravinová alergie a intolerance
- Poruchy v komplementovém systému
- Imunosenescence – západ slunce nad imunitním systémem
- Chřipka a její komplikace
- Familiární plicní fibróza – doporučení pro diagnostiku a léčbu
- Nové dělení krystalopatií z pohledu nefrologa
- Infarkt myokardu nebo syndrom zlomeného srdce?
- Dieulafoy lézia jejuna ako zdroj život ohrozujúceho krvácania
- Co nového internistům přinášejí doporučené postupy pro diagnostiku a léčbu plicní embolie z roku 2019?
- Perkutánní okluze ouška levé síně
- Současné postavení dietních opatření u pacientů s pokročilým stupněm chronického onemocnění ledvin
- Dysfunkčný dialyzačný cievny prístup a jeho endovaskulárna liečba
- Histiocytózy a neoplazie odvozené od makrofágů a dendritických buněk. Srovnání WHO klasifikace z roku 2017 a klasifikace Histiocyte society z roku 2016
- Glykovaný hemoglobín ako marker zvýšenia LDL a TAG – kohortná štúdia
- Deriváty sulfonylurey a riziko hypoglykemie u diabetiků 2. typu
- Endoskopická diagnostika a terapie pankreatobiliárních onemocnění u osob po resekci žaludku podle Billrotha I
- Nozokomiální methemoglobinemie
- Alergie a imunopatologie – hlavní téma
- Postihnutie tráviaceho traktu pri zmiešanej chorobe spojivového tkaniva (Sharpovom syndróme)
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Infarkt myokardu nebo syndrom zlomeného srdce?
- Postihnutie tráviaceho traktu pri zmiešanej chorobe spojivového tkaniva (Sharpovom syndróme)
- Potravinová alergie a intolerance
- Poruchy v komplementovém systému
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career