-
Medical journals
- Career
Chirurgická léčba chronické tromboembolické plicní hypertenze
: Matúš Nižňanský 1; David Ambrož 2; Tomáš Prskavec 1; Pavel Jansa 2; Jaroslav Lindner 1
: II. chirurgická klinika kardiovaskulární chirurgie 1. LF UK a VFN v Praze 1; II. interní klinika – klinika kardiologie a angiologie 1. LF UK a VFN v Praze 2
: Vnitř Lék 2019; 65(5): 353-358
:
Chronická tromboembolická plicní hypertenze (CTEPH) je onemocnění charakterizované vzestupem středního tlaku v plicním řečišti ≥ 25 mm Hg na podkladě intraluminálně organizovaných trombů, stenóz a uzávěrů jednotlivých větví plicnice a periferní cévní remodelace. Jedná se o chronickou komplikaci akutní plicní embolie. Důsledkem obstrukce plicnice je vzestup plicní cévní rezistence (Pulmonary Vascular Resistance – PVR) vedoucí k zatížení pravé komory srdeční a k pravostrannému srdečnímu selhání. Metodou volby v léčbě pacientů s CTEPH je chirurgická endarterektomie plicnice (PEA), výkon prováděný v hluboké hypotermii, v cirkulační zástavě. Jediným centrem specializujícím se na chirurgickou léčbu pacientů s CTEPH v ČR je Kardiocentrum VFN a 1. LF UK v Praze, na němž bylo v letech 2004–2017 operováno 314 pacientů (včetně 50 pacientů ze Slovenské republiky, kde tato léčba dostupná není). Pacienti s periferním typem postižení, u nichž nález není operabilní, a zároveň pacienti po PEA s reziduální plicní hypertenzí, jsou indikováni ke specifické vazodilatační terapii. V indikovaných případech se v léčbě pacientů uplatňuje také balonková angioplastika a transplantace plic.
Klíčová slova:
balonková plicní angioplastika – chirurgická technika – chronická tromboembolická plicní hypertenze – možnosti léčby – plicní endarterektomie – riociguat
Úvod
Chronická tromboembolická plicní hypertenze (Chronic Thromboembolic Pulmonary Hypertension – CTEPH) je onemocnění charakterizované vzestupem středního tlaku v plicním řečišti ≥ 25 mm Hg a je třetí nejčastější příčinou chronické plicní hypertenze. Jedná se o chronickou komplikaci akutní plicní embolie u pacientů, u kterých trombolytická anebo antikoagulační terapie nevede ke kompletnímu rozpuštění trombotických hmot a dochází k jejich intraluminální organizaci s následným vznikem stenóz a uzávěrů jednotlivých větví plicnice. Zároveň dochází k periferní cévní remodelaci a oba tyto mechanizmy vedou k vzestupu plicní vaskulární rezistence. Metodou volby v léčbě pacientů s CTEPH je chirurgická endarterektomie plicnice (Pulmonary EndArterectomy – PEA). Důležitým kritériem pro indikaci k PEA je lokalizace obstrukce plicního řečiště. Zatímco proximálně lokalizované stenózy a uzávěry jsou chirurgické léčbě přístupné a pomocí PEA tedy dobře řešitelné, periferně lokalizované léze (distálně od subsegmentárních větví) chirurgicky přístupné nejsou a pacienti s tímto nálezem jsou proto považováni za technicky inoperabilní.
Patofyziologie, epidemiologie
Patofyziologie CTEPH souvisí s akutní plicní embolií, tento vztah nicméně zatím nebyl zcela objasněn. Absence rozpuštění embolizovaných trombotických hmot, ke kterému jinak dochází u většiny pacientů po plicní embolii, není totiž jediným vysvětlením vzniku onemocnění. Anamnéza plicní embolie není přítomna u více než 20 % nemocných s CTEPH [1]. Teorie opakovaných embolizací do plic rovněž nejsou spolehlivým vysvětlením vzniku CTEPH, jelikož za recidivy plicní embolie jsou často mylně považovány epizody dušnosti, což je většinou v rozporu se stacionárním nálezem na plicní perfuzní scintigrafii.
Je tedy zřejmé, že v patofyziologii vzniku CTEPH se musí kromě embolizačního mechanizmu uplatňovat i mechanizmus neembolizační, a to je rozvoj remodelačních změn v oblasti zejména malých plicních cév. Akutní plicní embolie zde figuruje zřejmě jako iniciátor kaskády dalších dějů, u kterých se uplatňují lokální zánět, sekundární in situ trombóza, či genetická dispozice. U pacientů s CTEPH je známý vyšší výskyt prokoagulačních stavů (např. vyšší hladina antifosfolipidových protilátek, přítomnost lupus antikoagulans).
Incidence CTEPH není přesně známa, a to z důvodu již zmíněného nejasného vztahu s akutní plicní embolií. Uvádí se, že CTEPH se rozvíjí u 2–4 % pacientů po prodělané embolizaci do plic [2].
CTEPH je 3. nejčastější příčinou chronické plicní hypertenze a v klasifikaci plicní hypertenze se řadí do 4. skupiny (4.1), do níž jsou zahrnuty i další příčiny obstrukce plicních cév (4.2.1 angiosarkom, 4.2.2 jiné intravaskulární tumory, 4.2.3 arteriitidy, 4.2.4 vrozené stenózy plicnice, 4.2.5 parazitární onemocnění – hydatidóza) [1,3].
Klinický obraz
Příznaky CTEPH se u pacientů po prodělané akutní plicní embolii typicky začínají projevovat po bezpříznakovém období, které může trvat měsíce až roky. U pacientů bez anamnézy plicní embolie jsou to právě tyto příznaky, které by měly vést k podezření na onemocnění a k dovyšetření. Symptomatologie pacientů s CTEPH je identická jako u jiných forem chronické plicní hypertenze a zahrnuje zejména progredující námahovou dušnost, únavu, presynkopy až synkopy, sníženou fyzickou výkonnost. Mohou se objevit i bolesti na hrudi. V pokročilém stadiu onemocnění dochází k otokům dolních končetin, zvýšené náplni krčních žil a k cyanóze.
Diagnostika
Základní vyšetřovací metodou vedoucí k podezření na CTEPH je echokardiografické vyšetření, které prokáže známky plicní hypertenze. Echokardiografie by měla být provedena u všech pacientů na konci hospitalizace pro akutní plicní embolii. Při průkazu plicní hypertenze je nutno nemocného opět vyšetřit během 3–6 měsíců. Pokud nález plicní hypertenze není vysvětlitelný srdečním nebo plicním onemocněním, měl by pacient podstoupit ventilačně-perfuzní scintigrafii plic (obr. 1), jejíž negativní nález diagnózu CTEPH prakticky vylučuje [4]. V opačném případě by měl být pacient referován do centra zabývajícího se diagnostikou a léčbou plicní hypertenze k dovyšetření. Podrobná vyšetření se provádějí po nejméně 3měsíční antikoagulační léčbě. Aktivní vyhledávání CTEPH u asymptomatických pacientů po plicní embolii není obecně doporučeno.
1. Ventilační a perfuzní scintigrafie plic u nemocného s chronickou tromboembolickou plicní hypertenzí zobrazující četné defekty v přítomnosti radiofarmaka na perfuzních scanech oboustranně 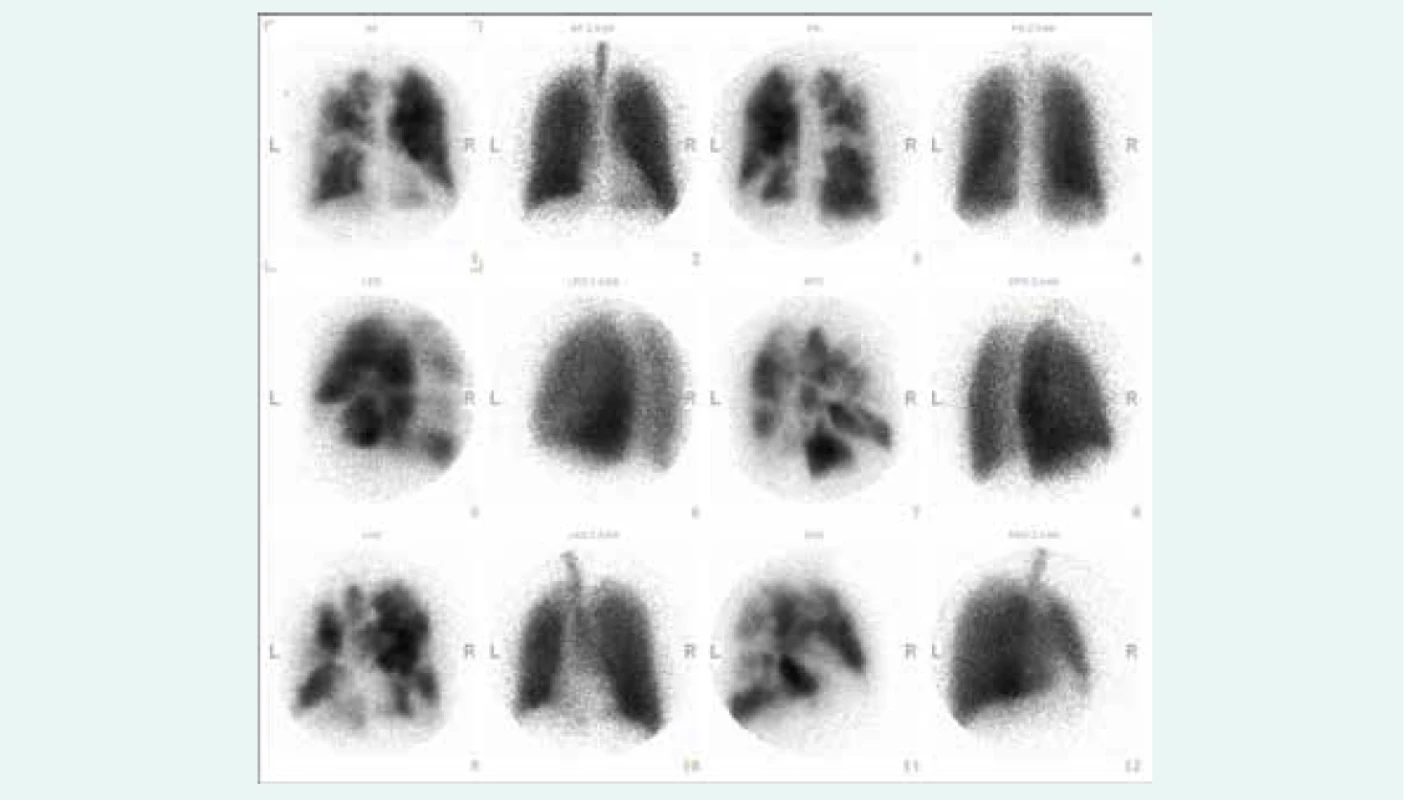
V rámci definitivního vyšetření ve specializovaném centru pacient podstupuje konvenční angiografii plicních tepen (obr. 2), která je nezbytná pro posouzení lokalizace obstrukcí a stenóz plicního řečiště, a tedy i pro posouzení vhodnosti pacienta k chirurgickému řešení. Angiografie se provádí současně s pravostrannou srdeční katetrizací k posouzení hemodynamických parametrů. Nezbytná je rovněž angiografie koronárních tepen. Konvenční angiografii doplňuje CT angiografie (obr. 3), která umožňuje víceprojekční zobrazení plicního řečiště včetně rekonstrukcí. Pacienti dále podstupují podrobné echokardiografické vyšetření k posouzení ev. přidružených kardiochirurgicky řešitelných komorbidit, bodypletyzmografii, USG krčních tepen, vyšetření infekčních fokusů a podrobné interní vyšetření včetně genetického vyšetření prokoagulačních stavů.
2. Angiogram zobrazující anatomicky operabilní nález u nemocného s chronickou tromboembolickou plicní hypertenzí 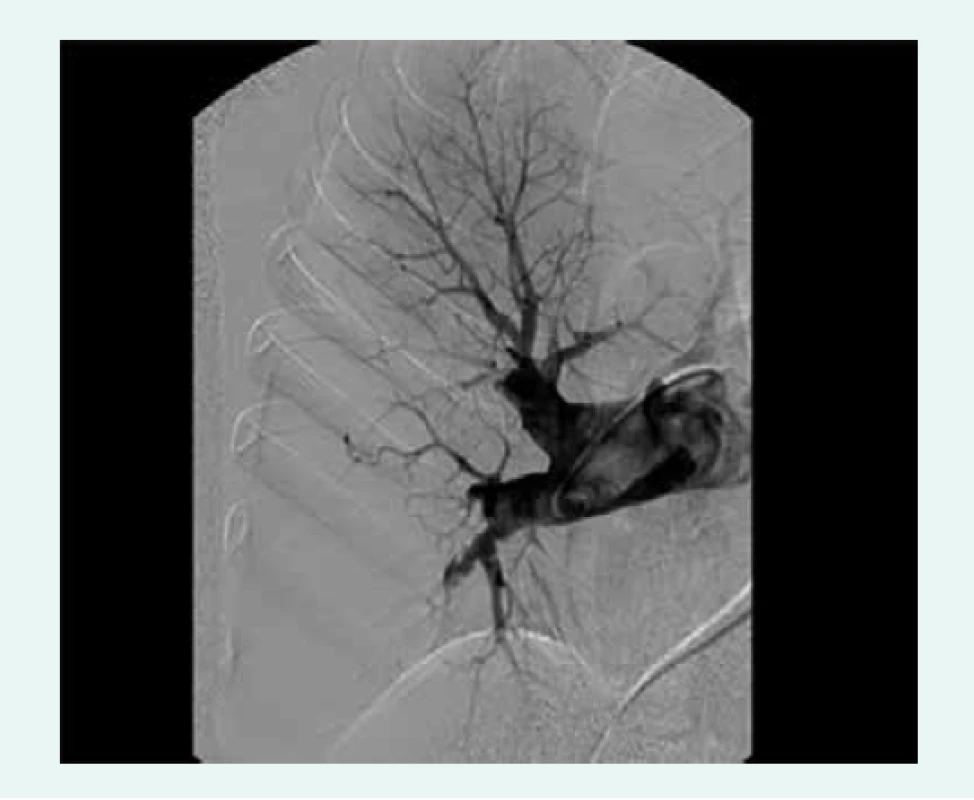
3. CT angiogram zobrazující objemný obtékaný trombus v pravé větvi plicnice u nemocného s chronickou tromboembolickou plicní hypertenzí 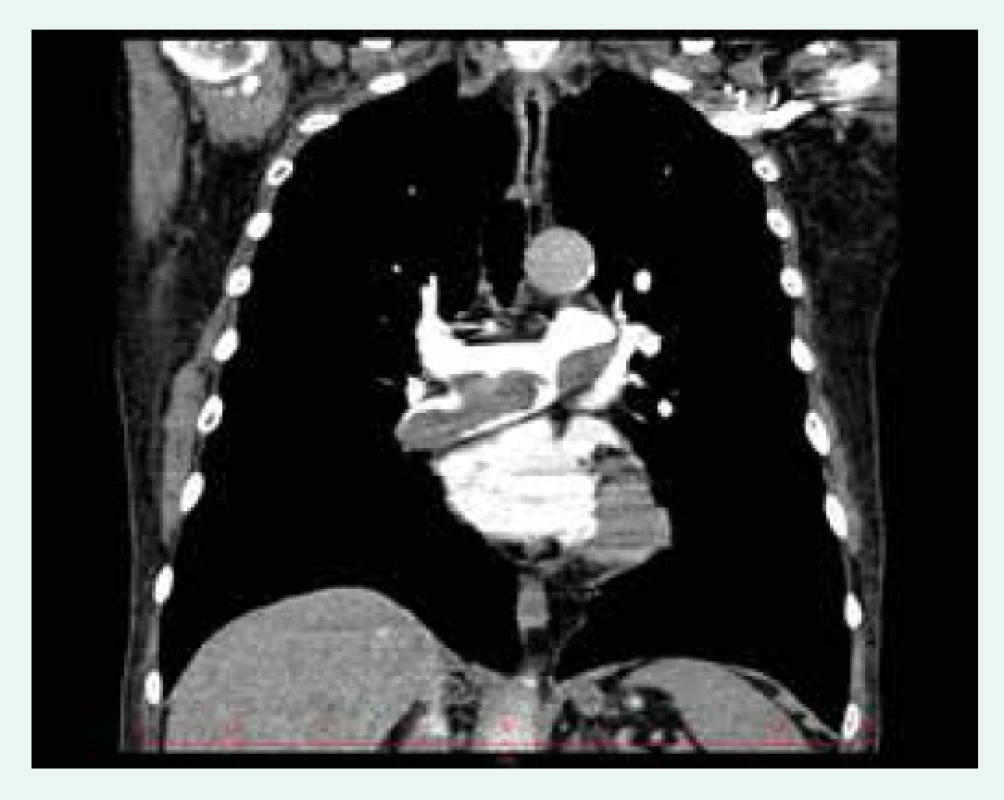
Indikační kritéria
U pacientů s diagnostikovanou CTEPH je indikována dlouhodobá antikoagulační terapie. Pokud v průběhu 3 měsíců od nasazení antikoagulace dojde ke zlepšení hemodynamických parametrů a funkční třídy, je u oligosymptomatických a asymptomatických pacientů bez plicní hypertenze nebo s hraničními tlaky v plicnici indikován většinou konzervativní postup a pravidelná echokardiografická a klinická monitorace. V opačném případě prochází pacient indikačním seminářem, na kterém je na základě výsledků vyšetření hodnocena vhodnost pacienta ke kauzální terapii – k chirurgickému řešení [5]. Zásadní je lokalizace obstrukce plicního cévního řečiště a tedy chirurgická dostupnost lézí, dále odhad přítomnosti periferních remodelačních změn, které i po úspěšně provedené endarterektomii plicních tepen mohou vést k významné reziduální plicní hypertenzi. Důležitý je rovněž biologický stav pacienta a přítomnost případných komorbidit.
Technicky operabilních je asi 60 % pacientů [6]. Hlavní příčiny inoperability jsou chirurgická nedostupnost trombotických obstrukcí, komorbidity a odmítnutí chirurgického výkonu ze strany pacienta [7].
Chirurgická technika
Operační výkon je prováděn v celkové anestezii, u pacientů je kromě standardní peroperační monitorace sledován také tlak v plicnici pomocí Swanova-Ganzova katétru a saturace ve frontálních lalocích mozku pomocí NIRS (Near Infra Red Spectroscopy). Operačním přístupem je střední sternotomie. Pacient je napojen na mimotělní oběh (MO): arteriální kanyla do ascendentní aorty, 2 samostatné žilní kanyly do horní a dolní duté žíly, venty do kmene plicnice a cestou pravé horní plicní žíly do levé síně. Po spuštění MO je pacient uveden do hluboké hypotermie, referenční je teplota v močovém měchýři, v němž dosahuje 16–18 °C. Teplota je dále monitorována i z čidel v rektu a v jícnu. Doba chlazení je individuální, závisí na hmotnosti a tělesné konstituci pacienta, většinou se pohybuje kolem 45–60 min. Dodržuje se protokol chlazení pacienta s 10stupňovým teplotním gradientem. Na chlazení se kromě mimotělního oběhu podílí i nižší teplota na operačním sále, termopodložka s cirkulující tekutinou uložená pod pacientem a selektivně je chlazena také hlava a srdce pomocí speciálního obložení s cirkulující tekutinou. Po zchlazení pacienta je na ascendentní aortu naložena příčná svorka a do kořene aorty pomocí Cooleyho jehly aplikována studená krystaloidní kardioplegie (Custodiol) [8]. Začíná se endarterektomií vpravo. Pomocí speciálního rozvěráčku (obr. 4) je odtažena horní dutá žíla od aorty a je vypreparována viditelná část pravé větve plicnice k hraně perikardu (obr. 5). Je provedena podélná tomie tepny a zahájena endarterektomie ve viditelném rozsahu.
4. Speciální instrumentárium používané v průběhu plicní endarterektomie 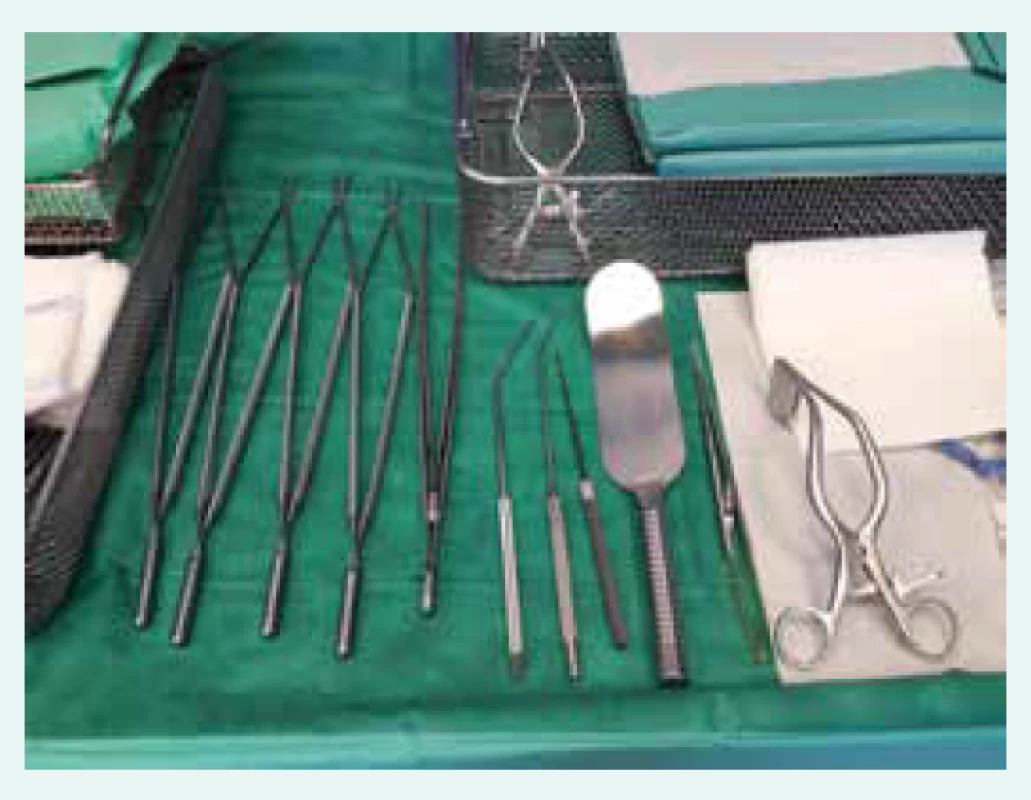
5. Operační pole v průběhu plicní endarterektomie. Nástroj směřuje do otevřené obturované pravé větve plicnice 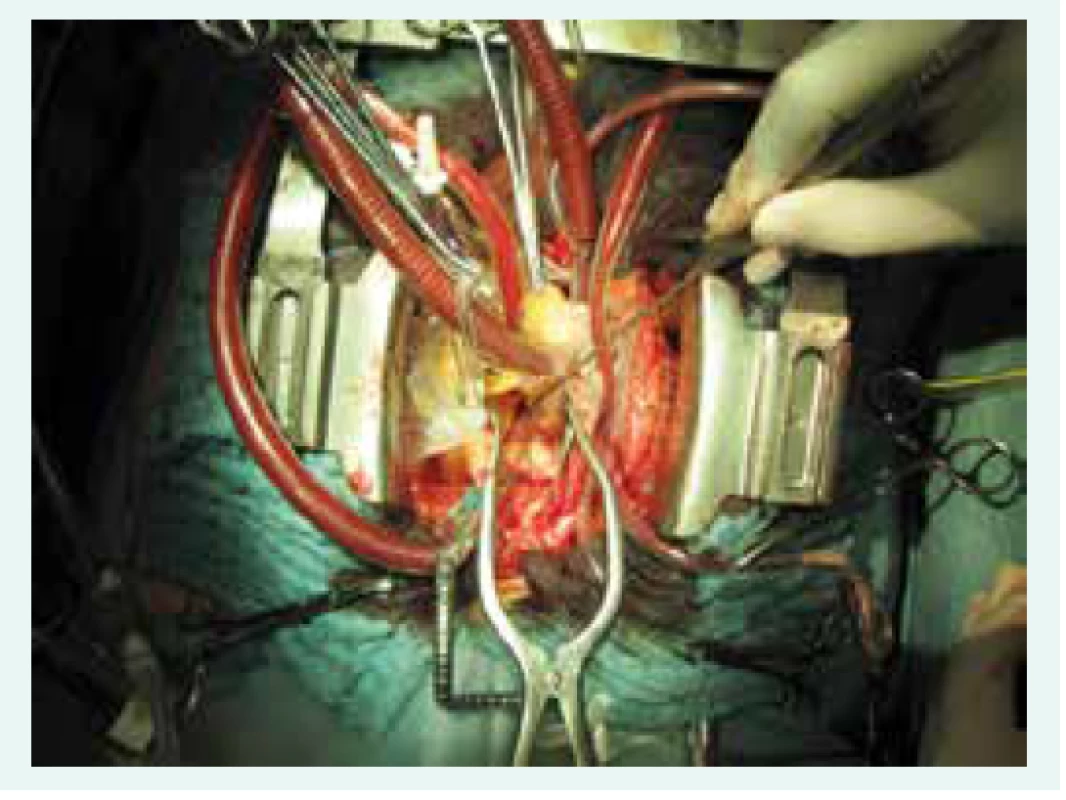
Podstatou výkonu je skutečná endarterektomie, nikoliv embolektomie. V průběhu endarterektomie je totiž odstraněna intimální vrstva tepny s organizovanými trombotickými hmotami, na rozdíl od embolektomie, u které se zpravidla odstraňují čerstvé tromby. Provedení kompletní endarterektomie (obr. 5) ve správné vrstvě je základní podmínkou pro úspešnost operace [9,10]. Vzhledem k bohatému zastoupení kolaterál v bronchiálním oběhu plic je operační pole znepřehledňováno neustálým zaplavováním krví, z toho důvodu je nevyhnutelná celková cirkulační zástava. Bezpečnost tohoto postupu je zachována díky hluboké hypotermii, která snižuje metabolické nároky tkání, včetně mozku, a době trvání zástavy. Ta by neměla překročit 30 min. Zároveň je monitorována saturace kyslíkem ve frontálních lalocích pomocí NIRS, jehož hodnota by neměla klesnout pod 40 % – v opačném případě musí být oběh obnoven a pokračovat lze až po krátké reperfuzi.
Po zastavení MO je pomocí několika manuálních dechových exkurzí vytlačena reziduální krev z plicního řečiště. V nyní již přehledném operačním poli může proběhnout samotná endarterektomie. Ta se provádí everzní technikou pomocí speciálního mikroraspatoria, chirurgicky dostupné jsou většinou lobární, segmentární a částečně subsegmentární větve plicnice. Vzhledem ke kalibru tepen a hloubce, ve které se nacházejí, je potřeba používat speciální pinzety s kloubem, umožňující otevření branží i v úzkém prostoru.
Po ukončení endarterektomie je znovu spuštěn MO za účelem reperfuze, která trvá zpravidla 10–15 min. V průběhu reperfuze je provedena sutura arteriotomie pomocí 6/0 polypropylenového stehu. Místo sutury je zpevněno pomocí tkáňového lepidla.
Následuje endarterektomie vlevo, srdce se rotuje pomocí speciálního retraktoru, aby se vizualizovala levá větev plicnice, která je podélně otevřena k okraji perikardu. Obdobně jako vpravo se začíná bez zástavy oběhu v rozsahu, který závisí na přehlednosti operačního pole. Ta je udržována 2 odsávačkami odsávajícími krev přitékající z větví plicnice. Po zástavě oběhu pokračuje endarterektomie standardním způsobem, dokud není kompletní (obr. 6). Následně je spuštěn MO, je zahájeno ohřívání pacienta, v průběhu kterého je provedena sutura tepny stejnou technikou jako na pravé straně. Ohřívání trvá 1,5–2násobek doby chlazení za dodržení teplotních gradientů. V průběhu ohřívání pacienta je zároveň prostor pro kombinované kardiochirurgické výkony, jako jsou aortokoronární bypassy, výkony na srdečních chlopních, MAZE, či sutura defektu septa síní. Následně je odstraněna svorka z ascendentní aorty a zahájena reperfuze srdce společně s reperfuzí plic za trvalého odlehčení průtoku odsáváním plicnicovým ventem. Časně je zahájena šetrná tlaková ventilace s nízkou frekvencí a dechovými objemy s PEEP. Tato opatření snižují riziko reperfuzního edému plic, který může vést i ke krvácení do dýchacích cest.
6. Endarterium odstraněné u nemocného s těžkou tromboembolickou plicní hypertenzí při plicní endarterektomii (typ postižení I) 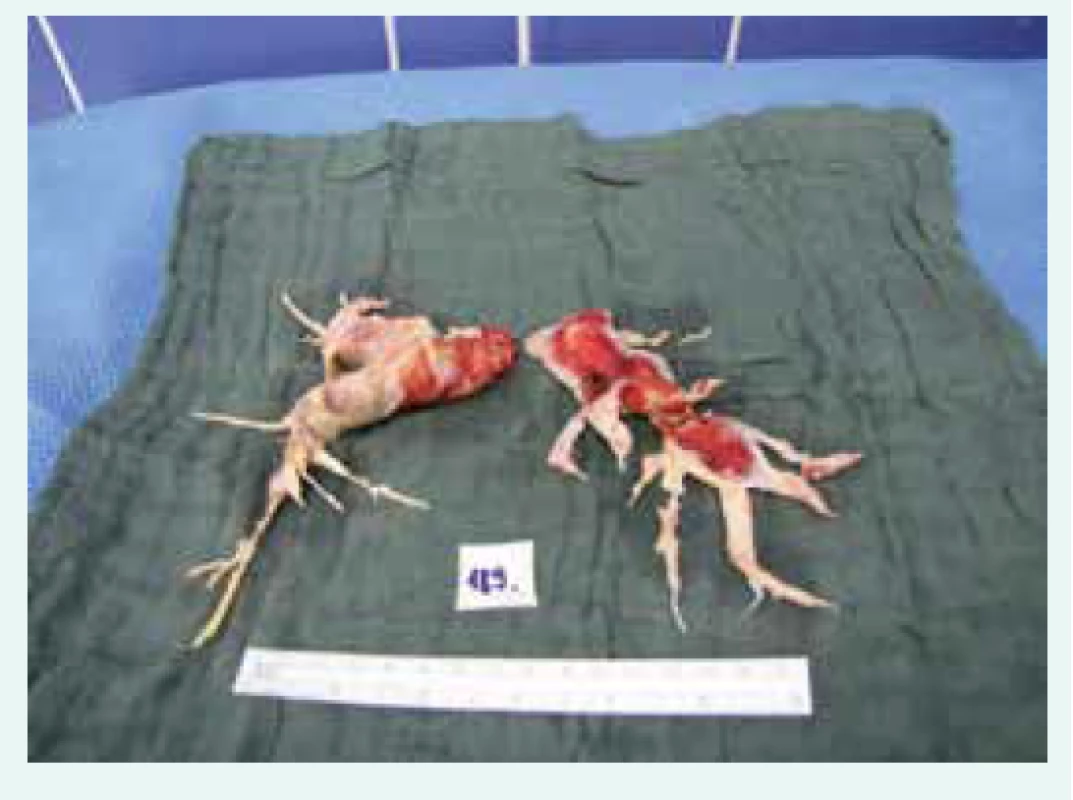
Po ohřátí pacienta na 36 °C jsou zavedeny 2 síňové a 2 komorové dočasné stimulační elektrody, postupně je ukončen a dekanylován MO. Dříve užívaný levosíňový katétr k podávání noradrenalinu se v současnosti již nepoužívá. Následuje úprava koagulace, stavění krvácení, do hrudníku je zaveden retrokardiální a retrosternální drén, v případě otevření pleury také silastikový drén do pleurální dutiny. Je provedena sutura sternotomie po anatomických vrstvách a pacient je transportován na pooperační oddělení. Zde je 4–6 hod po operačním výkonu v případě přiměřených krevních ztrát zahájena antikoagulace heparinem, pacient je extubován standardně po 12–16 hod. V průměru 3.–6. pooperačního den je pacient přeložen na standardní oddělení, na němž je zahájena intenzivní rehabilitace. Po odstranění elektrod a drénu je pacient převeden na perorální antikoagulaci, preferenčně na warfarin s cílovou hodnotou INR 2,5–3,0.
Další možnosti léčby
Specifická farmakoterapie ovlivňující plicní cévní remodelaci je indikována u inoperabilních pacientů a u pacientů s reziduální plicní hypertenzí po PEA [11]. V současné době jsou jedinou skupinou léků specificky zasahujících do remodelačních změn u CTEPH stimulátory guanylátcyklázy. Mechanizmus působení je v zesílení účinku oxidu dusnatého na guanylátcyklázu a zároveň ve zvýšení senzitivity guanylátcyklázy na nízkou hladinu NO. Jediným registrovaným přípravkem pro léčbu inoperabilní CTEPH nebo reziduální plicní hypertenze je perorální preparát riociguat. Jeho účinnost a bezpečnost byla ověřena v randomizované multicentrické placebem kontrolované klinické studii CHEST-1 [12] a v navazující studii CHEST-2 [13].
Balonková plicní angioplastika (BPA) je metoda, která se v léčbě CTEPH začala uplatňovat od roku 1988 [14], zpočátku pouze sporadicky, a ani v dnešní době nicméně není zcela běžnou léčebnou metodou a rozhodně není alternativou PEA. Metoda nedosahuje takového zlepšení hemodynamiky jako u PEA. Jsou nutné opakované intervence na řadě segmentů. BPA je rovněž zatížena řadou komplikací, jako je krvácení či reperfuzní edém. Nezanedbatelná je také radiační zátěž spojená s výkonem [15]. BPA by měla být indikována v přísně selektovaných případech u pacientů nevhodných k PEA pro vysoké riziko operace nebo v případě chirurgicky nedosažitelného, nicméně k BPA vhodného nálezu. BPA může být rovněž kombinována s PEA, a to jak formou hybridního, tak sekvenčního výkonu.
Transplantace plic přichází v úvahu u nemocných nevhodných k PEA po vyčerpání možností léčby pomocí farmakoterapie a BPA. Další indikací je selhání PEA. Dlouhodobé přežití po transplantaci plic je horší než po PEA.
Výsledky
V kardiocentru VFN v Praze bylo od zahájení programu chirurgické léčby CTEPH v roce 2004 do konce roku 2017 provedeno 314 endarterektomií plicnice, z toho 50 odoperovaných pacientů bylo ze Slovenské republiky (graf). Průměrný věk pacienta byl 59,7 let (nejmladší pacientce bylo 22 let, nejstaršímu 80 let), bylo odoperováno celkem 119 žen a 195 mužů. Průměrná délka operace byla 380 min, délka cirkulační zástavy 33 min (17 min vpravo, 16 min vlevo) při tělesné teplotě 17,1 °C.
1. Počet plicních endarterektomií provedených v Kardiocentru VFN v Praze 
U 90 pacientů byla PEA kombinována s dalším kardiochirurgickým výkonem (sutura foramen ovale patens 34krát, aortokoronární bypass 32krát, MAZE 16krát, implantace kardiostimulátoru 7krát, náhrada aortální chlopně 6krát, výkon na mitrální chlopni 2krát, plastika trikuspidální chlopně 1krát, korekce anomálního vyústění plicních žil 1krát). Ze závažných komplikací se u pacientů po PEA nejčastěji vyskytují: reperfuzní edém (5,5 %), krvácení/srdeční tamponáda s nutností chirurgické revize (4,5 %), krvácení do plic (4,1 %), neurologické komplikace (3,1 %), infekce operační rány (2,4 %). Časná mortalita se pohybuje do 5 %. Kardiocentrum VFN v Praze je jedním z 27 center zapojených do Evropského registru CTEPH a výsledky kardiocentra jsou dlouhodobě srovnatelné se souhrnnými výsledky registru [16].
Jednoleté přežití u operovaných pacientů je 89 %, 3leté 87 %, 5leté 82 % a 10leté 75 %. Naproti tomu ve skupině inoperabilních nemocných je přežívání výrazně horší a závisí na výši tlaku v plicnici [17,18].
Závěr
CTEPH je relativně vzácná chronická komplikace akutní plicní embolie s nepříznivou prognózou u neléčených pacientů. V diagnostice pacientů s podezřením na CTEPH hraje klíčovou roli echokardiografické vyšetření a ventilačně perfuzní scintigrafie plic. Metodou volby v terapii CTEPH je endarterektomie plicnice, která je pro většinu pacientů kurativní léčbou. Prognosticky nejvýznamnějším faktorem pro časnou i pozdní mortalitu je hemodynamicky významný pokles plicní cévní rezistence (Pulmonary Vascular Resistance – PVR) po operaci. U inoperabilních pacientů a u pacientů s reziduální plicní hypertenzí po PEA je indikována specifická léčba ovlivňující plicní cévní remodelaci. Další možností léčby u inoperabilních pacientů a u nemocných s reziduální plicní hypertenzí po PEA je v selektovaných případech balonková angioplastika. V případě selhání těchto léčebných postupů přichází v úvahu transplantace plic.
MUDr. Matúš Nižnanský
II. chirurgická klinika kardiovaskulární chirurgie 1. LF UK a VFN v Praze
Doručeno do redakce 10. 5. 2018
Přijato po recenzi 15. 10. 2018
Sources
- Kim NH, Delcroix M, Jenkins DP et al. Chronic Thromboembolic Pulmonary Hypertension. J Am Coll Cardiol 2013; 62(25 Suppl): D92-D99. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jacc.2013.10.024>.
- Ende-Verhaar YM, Cannegieter SC, Vonk Noordegraaf A et al. Incidence of chronic thromboembolic pulmonary hypertension after acute pulmonary embolism: a contemporary view of the published literature. Eur Respir J 2017; 49(2). pii: 1601792. Dostupné z DOI: <http://dx.doi.org/10.1183/13993003.01792–2016>.
- Aschermann M. Nová verze klasifikace plicní hypertenze. Vnitř Lék 2015; 61(5): 387–391.
- Galie N, Humbert M, Vachiery JL et al. 2015 ESC/ERS Guidelines for the diagnosis and treatment of pulmonary hypertension: The Joint Task Force for the Diagnosis and Treatment of Pulmonary Hypertension of the European Society of Cardiology (ESC) and the European Respiratory Society (ERS) Endorsed by: Association for European Paediatric and Congenital Cardiology (AEPC), International Society for Heart and Lung Transplantation (ISHLT). Eur Respir J 2015; 46(6): 903–975. Dostupné z DOI: <http://dx.doi.org/10.1183/13993003.51032–2015>.
- Vavera Z. Chronická tromboembolická plicní hypertenze. Vnitř Lék 2015; 61(3): 228–235.
- Pepke-Zaba J, Delcroix M, Lang I et al. Chronic Thromboembolic Pulmonary Hypertension (CTEPH) Results From an International Prospective Registry. Circulation 2011; 124(18): 1973–1981. Dostupné z DOI: <http://dx.doi.org/10.1161/CIRCULATIONAHA.110.015008>.
- Mayer E, Jenkins D, Lindner J et al. Surgical management and outcome of patients with chronic thromboembolic pulmonary hypertension: Results from an international prospective registry. J Thorac Cardiovasc Surg 2011; 141(3): 702–710. Dostupné z DOI: <http://dx.doi.org/10.1016/j.jtcvs.2010.11.024>.
- Lindner J, Jansa P. Chronická tromboembolická plicní hypertenze. Maxdorf: Praha 2009. ISBN 978–80–7345–181–3.
- Jenkins D, Madani M, Fadel E et al. Pulmonary endarterectomy in the management of chronic thromboembolic pulmonary hypertension. Eur Respir Rev 2017; 26(143). pii: 160111. Dostupné z DOI: <http://dx.doi.org/10.1183/16000617.0111–2016>.
- Madani MM, Jamieson SW. Technical advances of pulmonary endarterectomy for chronic thromboembolic pulmonary hypertension. Semin Thorac Cardiovasc Surg 2006; 18(3): 243–249. Dostupné z DOI: <http://dx.doi.org/10.1053/j.semtcvs.2006.09.003>.
- Pepke-Zaba J, Jansa P, Kim NH et al Chronic thromboembolic pulmonary hypertension: role of medical therapy. Eur Respir J 2013; 41(4): 985–990. Dostupné z DOI: <http://dx.doi.org/10.1183/09031936.00201612>.
- Ghofrani HA, D‘Armini AM, Grimminger F et al. Riociguat for the treatment of chronic thromboembolic pulmonary hypertension. CHEST-1 Study Group. N Engl J Med 2013; 369(4): 319–329. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa1209657>.
- Simonneau G, D’Armini AM, Ghofrani HA et al. Riociguat for the treatment of chronic thromboembolic pulmonary hypertension: a long-term extension study (CHEST-2). Eur Respir J; 45(5): 1293–1302. Dostupné z DOI: <http://dx.doi.org/10.1183/09031936.00087114>.
- Voorburg JA, Cats VM, Buis B et al. Balloon angioplasty in the treatment of pulmonary hypertension caused by pulmonary embolism. Chest 1988; 94(6): 1249–1253.
- Ogo T. Balloon pulmonary angioplasty for inoperable chronic thromboembolic pulmonary hypertension. Curr Opin Pulm Med 2015; 21(5): 425–431. Dostupné z DOI: <http://dx.doi.org/10.1097/MCP.0000000000000188>.
- Delcroix M, Lang I, Pepke-Zaba J et al. Long-term outcome of patients with chronic thromboembolic pulmonary hypertension (CTEPH): Results from an international prospective registry. Circulation 2016; 133(9):859–871. Dostupné z DOI: <http://dx.doi.org/10.1161/CIRCULATIONAHA.115.016522>.
- Thistlethwaite PA, Madani M, Jamieson SW. Outcomes of pulmonary endarterectomy surgery. Semin Thorac Cardiovasc Surg 2006; 18(3): 257–264. Dostupné z DOI: <http://dx.doi.org/10.1053/j.semtcvs.2006.09.008>.
- Jansa P, Ambrož D, Lindner J. Minulost a současnost problematiky plicní cirkulace ve Všeobecné fakultní nemocnici v Praze. Vnitř Lék 2014; 60(12): 1051–1054.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2019 Issue 5-
All articles in this issue
- Limited ambulatory night sleep testing in patients with a suspicion of sleep apnoea syndrome: Is its indication tenable?
- Surgical treatment of chronic thromboembolic pulmonary hypertension
- Communication with cancer patient
- Multimodal treatment of thymic carcinoid: a case report
- Nontuberculous mycobacterial disease: a case report-based review
- Use of idarucizumab in clinical practice: a case report
- Otto Kahler and his family: II. Ripening years in Prague
- Compliance with ethical rules for scientific publishing in biomedical Open Access journals indexed in Journal Citation Reports
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Communication with cancer patient
- Surgical treatment of chronic thromboembolic pulmonary hypertension
- Limited ambulatory night sleep testing in patients with a suspicion of sleep apnoea syndrome: Is its indication tenable?
- Nontuberculous mycobacterial disease: a case report-based review
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

