-
Medical journals
- Career
Karotická stenóza – diagnostika a léčba
: Tomáš Novotný; Robert Staffa
: Centrum cévních onemocnění II. chirurgické kliniky LF MU a FN u sv. Anny Brno, přednosta prof. MUDr. Robert Staffa, Ph. D.
: Vnitř Lék 2015; 61(12): 1049-1066
: Reviews
Diagnostika a léčba karotické stenózy prochází neustálým vývojem. Zejména v posledních letech můžeme zaznamenat velmi výrazné změny v názorech jak na podkladě výsledků metaanalýz starších důkazů, tak důkazů nových. Významným faktorem je také rychlý rozvoj nových endovaskulárních terapeutických metod. V reakci na tyto změny byly řadou odborných společností vydány doporučené postupy zaměřené na diagnostiku a léčbu karotické stenózy. Přestože jsou podloženy prakticky stejnými medicínskými důkazy, ne vždy se ve svých doporučeních shodují. Cílem práce bylo sumarizovat aktuální doporučení, která se týkají diagnostiky a léčby karotické stenózy. Diagnostika a intervenční terapie u asymptomatických a symptomatických pacientů byla zpracována odděleně, neboť se jedná o 2 velmi rozdílné skupiny. Podrobně byla zpracována také doporučení, která se týkají volby typu intervence a rozhodování mezi karotickou endarterektomií a karotickým stentingem.
Klíčová slova:
doporučené postupy – guidelines – karotická endarterektomie – karotický stenting – stenóza karotidyÚvod
V posledních letech dochází k podstatným změnám názorů na léčbu karotické stenózy. V reakci na tyto změny vydala řada odborných společností své doporučené postupy (guidelines) nebo odborná stanoviska k diagnostice a léčbě tohoto onemocnění. Všechny aktuální dokumenty jsou podloženy prakticky stejnými daty, ať už těmi z chronicky známých velkých karotických studií (North American Symptomatic Carotid Endarterectomy Trial – NASCET [1], European Carotid Surgery Trial – ECST [2], Veterans Affairs Cooperative Study – VACS [3]) nebo novými studiemi zaměřenými převážně na srovnání účinnosti a bezpečnosti karotického stentingu (CAS) vůči karotické endarterektomii (CEA). Přes společný důkazový základ nejsou doporučení vždy v souladu.
Cílem práce je sumarizovat optimální postup diagnostiky a léčby karotické stenózy na základě aktuálních guidelines i poukázat na sporné oblasti, jež jsou obvykle podmíněny nedostatkem důkazů.
Metodika
Byl proveden PubMed Advanced Search pro klíčová slova: carotid[Title] AND guidelines[Title] bez dalších filtrů. Vyhledávání poskytlo 76 výsledků. Z toho bylo vyřazeno: 33 odborných prací, u nichž se nejednalo o doporučené postupy, a 25 doporučených postupů, které se nezabývaly diagnostikou a léčbou extrakraniálního karotického a vertebrálního onemocnění (ECVD), šlo již o nahrazené starší doporučené postupy nebo se jednalo o jednooborové doporučené postupy národní úrovně. Zbylých 18 výsledků identifikovalo 6 aktuálních doporučených postupů, jmenovitě: 2011 ASA/ACCF/AHA/AANN/AANS/ACR/ASNR/CNS/SAIP/SCAI/SIR/SNIS/SVM/SVS guideline on the management of patients with extracranial carotid and vertebral artery disease [4] (2011 AHA/ASA) – 7 výsledků; Updated Society for Vascular Surgery guidelines for management of extracranial carotid disease [5] (2011 SVS) – 3 výsledky, ESC Guidelines on the diagnosis and treatment of peripheral artery diseases [6] (2011 ESC) – 1 výsledek, ESVS Guidelines. Invasive Treatment for Carotid Stenosis: Indications, Techniques [7] (2009 ESVS) – 3 výsledky, a dále 2 doporučené postupy, které se specificky věnovaly karotickému stentingu: Guidelines for patient selection and performance of carotid artery stenting [8] (2011 Australasian; společné doporučené postupy australských, novozélandských a asijských odborných společností) – 3 výsledky a Carotid artery stenting: the 2011 NICE guidelines [9] (2011 NICE; guidelines UK National Institute for Health and Clinical Excellence) – 1 výsledek. Při studiu těchto pramenů byl dále identifikován dokument z roku 2014 navazující na 2011 AHA/ASA, a to Guidelines for the prevention of stroke in patients with stroke and transient ischemic attack: a guideline for healthcare professionals from the American Heart Association/American Stroke Association [10] (2014 AHA/ASA).
Byla zpracována doporučení pro diagnostiku, medikamentózní léčbu, indikaci intervencí a volbu jejich typu. Doporučení byla přeložena, tematicky roztříděna a zpracována do přehledových tabulek. Byly také shrnuty klasifikační systémy úrovně kvality důkazů a tříd doporučení použité v jednotlivých doporučených postupech.
Výsledky
Klasifikace úrovně kvality důkazů a tříd doporučení
2011 AHA/ASA, 2014 AHA/ASA a 2011 ESC používaly prakticky shodný 3stupňový systém hodnocení úrovně kvality důkazů (ÚKD) i značení tříd doporučení (4 stupně). 2011 SVS používaly velmi obecně definovaný 3stupňový systém ÚKD a 2stupňový systém tříd doporučení rozlišující pouze silná a slabá doporučení. 2009 ESVS používaly také 3stupňový systém ÚKD. Tento byl definovaný přesněji, ale kritéria pro úroveň důkazů A a B byla proti AHA/ASA a ECS výrazně mírnější. Síla doporučení pak byla přímo určována úrovní důkazů. 2011 Australasian hodnotí současné dostupné důkazy pro CAS souhrnně jako C a od toho vyvozují také sílu svých doporučení (C). 2011 NICE ve svých doporučeních pro CAS neaplikovaly žádný systém hodnocení úrovně kvality důkazů a tříd doporučení.
Klasifikace úrovně kvality důkazů je shrnuta v tab. 1 a klasifikaci tříd doporučení ukazuje tab. 2.
1. Přehled klasifikací úrovní kvality důkazů 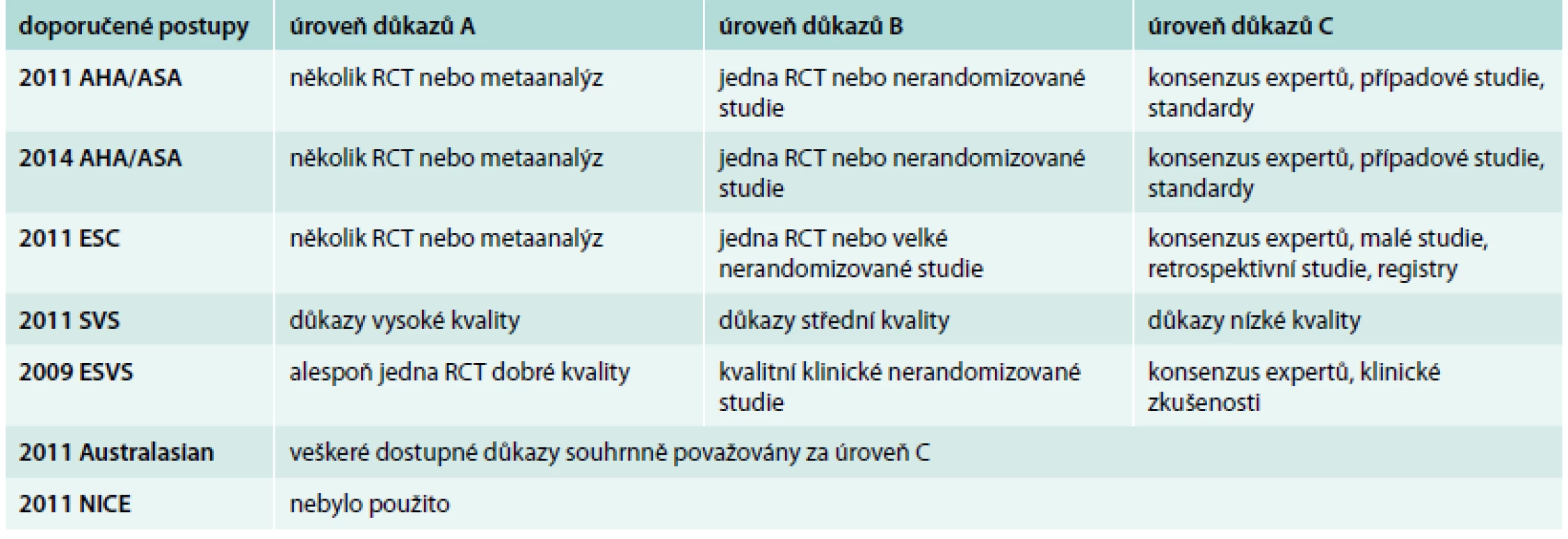
AHA/ASA – American Heart Association/American Stroke Association, ESC – European Society of Cardiology, ESVS – European Society for Vascular Surgery Australasian – Australian, New Zeland and Asian Society for Vascular Surgery, NICE – UK National Institute for Health and Clinical Excellence, RCT – randomizovaná kontrolovaná studie (randomized controlled trial), SVS – Society for Vascular Surgery 2. Přehled tříd doporučení 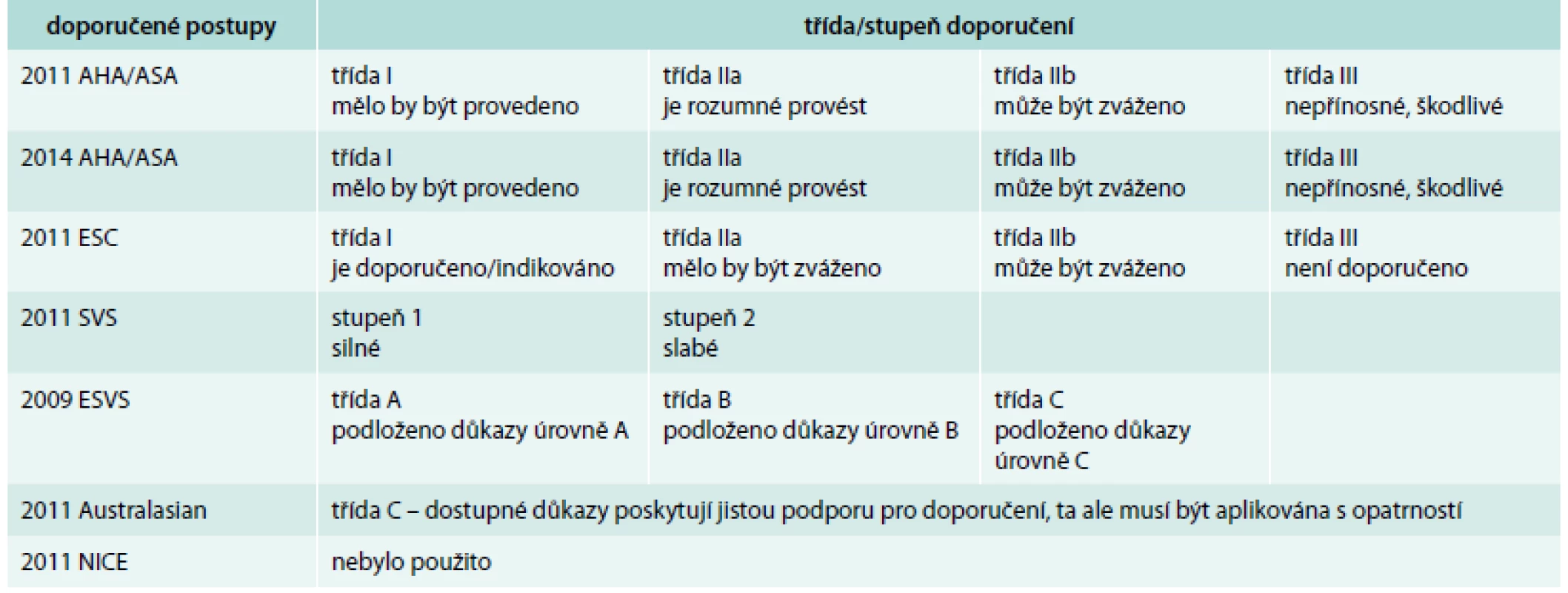
AHA/ASA – American Heart Association/American Stroke Association, ESC – European Society of Cardiology, ESVS – European Society for Vascular Surgery Australasian – Australian, New Zeland and Asian Society for Vascular Surgery, NICE – UK National Institute for Health and Clinical Excellence, SVS – Society for Vascular Surgery Doporučení pro diagnostiku karotické stenózy
Doporučení pro diagnostiku karotické stenózy obsahují 2011 AHA/ASA a 2011 SVS. Jsou velmi odlišná pro pacienty symptomatické a asymptomatické, proto byla zpracována odděleně. Pro úplnost je uvedeno i jediné a velmi vágní doporučení v oblasti diagnostiky obsažené v 2011 ESC. Doporučení pro diagnostiku karotické stenózy u symptomatických pacientů shrnuje tab. 3, doporučení pro diagnostiku karotické stenózy u asymptomatických pacientů shrnuje tab. 4.
3. Doporučení pro diagnostiku karotické stenózy u symptomatických pacientů 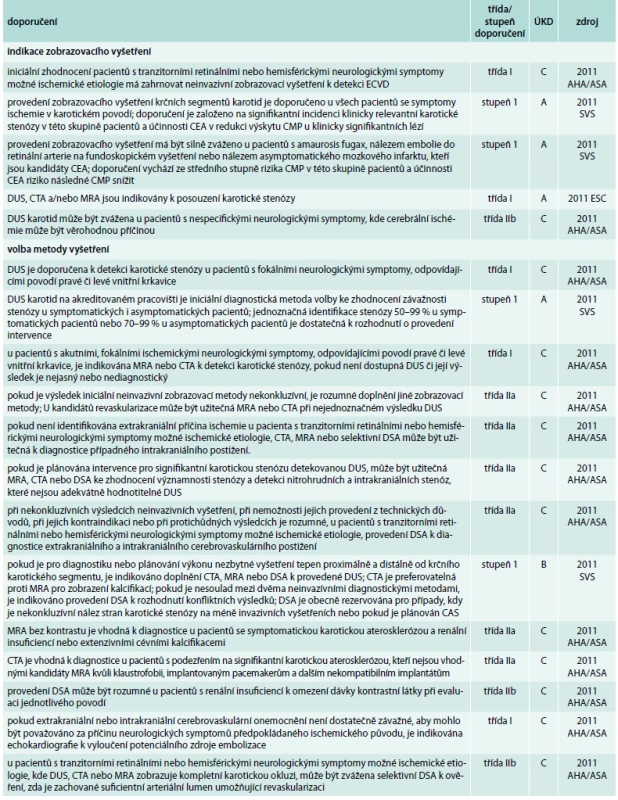
AHA/ASA – American Heart Association/American Stroke Association Australasian – Australian, New Zeland and Asian Society for Vascular Surgery, CAS – karotický stenting, CEA – karotická endarterektomie, CMP – cévní mozková příhoda, CTA – CT angiografie, DSA – digitální subtrakční angiografie, DUS – duplexní ultrasonografie, ECVD – extrakraniální karotické a vertebrální arteriální onemocnění, ESC – European Society of Cardiology, ESVS – European Society for Vascular Surgery, MRA – magnetická rezonance angiografie, NICE – UK National Institute for Health and Clinical Excellence, SVS – Society for Vascular Surgery, ÚKD – úroveň kvality důkazů 4. Doporučení pro diagnostiku karotické stenózy u asymptomatických pacientů 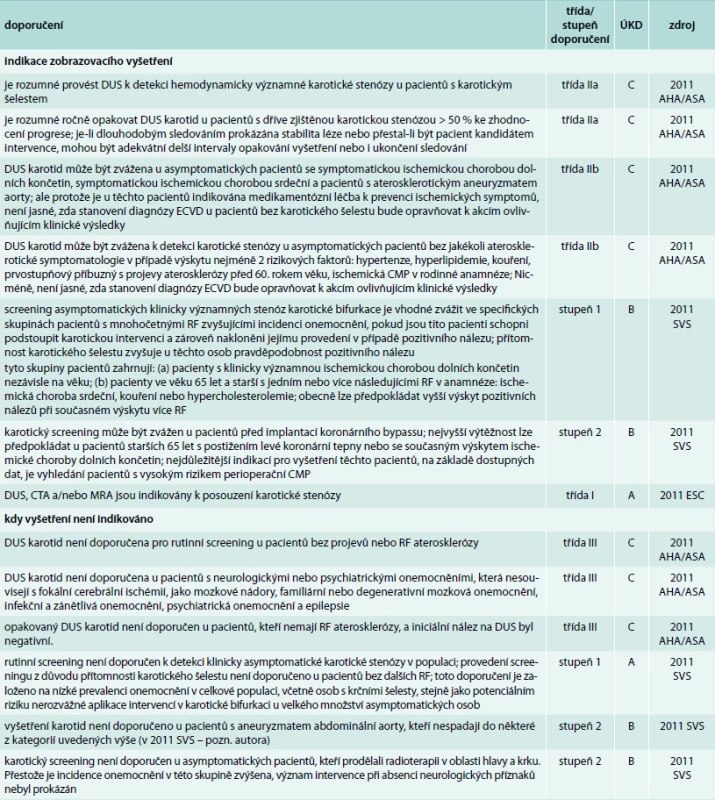

CMP – cévní mozková příhoda, CTA – CT angiografie, DSA – digitální subtrakční angiografie, DUS – duplexní ultrasonografie, ECVD – extrakraniální karotické a vertebrální arteriální onemocnění, MRA – MR angiografie, RF – rizikové faktory ÚKD – úroveň kvality důkazů Doporučení pro diagnostiku u symptomatických pacientů
Indikace zobrazovacího vyšetření
2011 AHA/ASA i 2011 SVS doporučují provedení neinvazivního zobrazovacího vyšetření u symptomatických pacientů, ať už s příznaky hemisférickými nebo retinálními. Indikací je také nález retinální embolie při fundoskopickém vyšetření nebo asymptomatického infarktového ložiska na zobrazovacím vyšetření mozku. Dále je možno zvážit vyšetření u pacientů s nespecifickými neurologickými symptomy, které mohou být vysvětleny mozkovou ischemií.
Volba metody vyšetření
Iniciální metodou je u symptomatického pacienta duplexní ultrasonografie (DUS), která sama o sobě umožňuje stanovit indikaci k intervenci. Pokud je DUS nedostupná, nediagnostická, je na jejím základě indikována intervence nebo je podezření na stenózu v karotickém povodí mimo krční segment, je indikována CT angiografie (CTA) nebo MR angiografie (MRA). Angiografie, v dnešní době prakticky vždy ve formě digitální subtrakční angiografie (DSA), je jako nejinvazivnější diagnostická metoda rezervována pro sporné nálezy již uvedených vyšetření nebo je-li plánován CAS. 2011 AHA/ASA dále podrobněji rozvádí situace, kdy je možné upřednostnit některou z metod.
Doporučení pro diagnostiku u asymptomatických pacientů
Indikace zobrazovacího vyšetření
Indikace vyšetření u asymptomatických pacientů lze rozdělit do několika skupin: sledování již diagnostikované stenózy, šelest, diagnostikované jiné aterosklerotické onemocnění u pacienta a rizikové faktory (RF) aterosklerózy (AS). V jednotlivých detailech se však doporučené postupy liší. 2011 AHA/ASA i 2011 SVS uvádějí také doporučení, v jakých případech vyšetření karotid indikováno není. Je to screening u pacientů bez projevů AS nebo jejích RF, opakování vyšetření u pacientů bez RF při iniciálním negativním nálezu. Vyšetření není indikováno u neurologických a psychiatrických onemocnění, která nesouvisejí s cerebrální ischemií, a také u pacientů po radioterapii v oblasti hlavy a krku.
Dvě indikace, u nichž jsou doporučení zcela protichůdná, jsou karotický šelest a aneuryzma abdominální aorty (AAA). Zatímco 2011 AHA/ASA doporučují šelest a AAA jako indikaci k vyšetření karotid, 2011 SVS je naopak bez přítomnosti dalších projevů AS nebo RF za indikaci nepovažují. Indikace zobrazovacího vyšetření pro diagnostiku u asymptomatických pacientů shrnuje tab. 4.
Volba metody vyšetření
Metodou volby je u asymptomatického pacienta DUS, která sama o sobě umožňuje stanovit indikaci k intervenci. Pokud je DUS nediagnostická, je podezření na stenózu střední závažnosti (50–69 %) nebo je na základě DUS indikována intervence nebo je podezření na stenózu v karotickém povodí mimo krční segment, je indikována CTA nebo MRA. DSA je jako nejinvazivnější diagnostická metoda rezervována pro sporné nálezy již uvedených vyšetření nebo je-li plánován CAS.
Doporučení pro medikamentózní terapii karotické stenózy
Doporučení pro optimální medikamentózní terapii (best medical therapy) obsahují 2011 AHA/ASA, 2014 AHA/ASA, 2011 SVS a 2011 ESC. Doporučení pro antiagregační léčbu v období revaskularizace uvádí také 2011 ESVS.
Přehled optimální medikamentózní terapie přináší tab. 5, která shrnuje léčbu hypertenze, hyperlipidemie, doporučení k zanechání kouření a doporučení pro pacienty s onemocněním diabetes mellitus. Doporučení pro antiagregační léčbu shrnuje tab. 6.
5. Optimální medikamentózní terapie mimo antitrombotickou léčbu 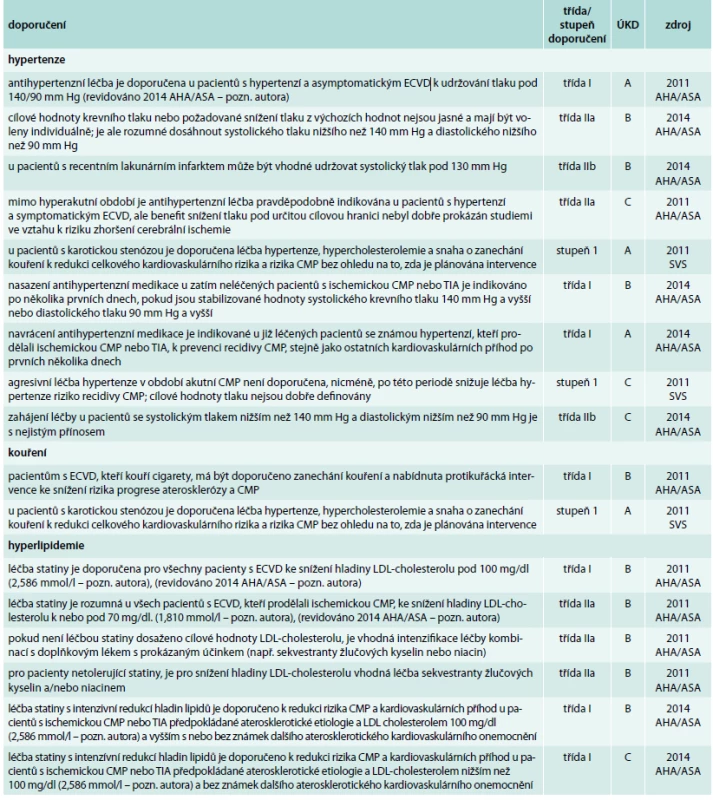

CMP – cévní mozková příhoda, DM – diabetes mellitus, ECVD – extrakraniální karotické a vertebrální arteriální onemocnění, TIA – tranzitorní ischemická ataka, ÚKD – úroveň kvality důkazů 6. Antitrombotická léčba včetně periprocedurálního období 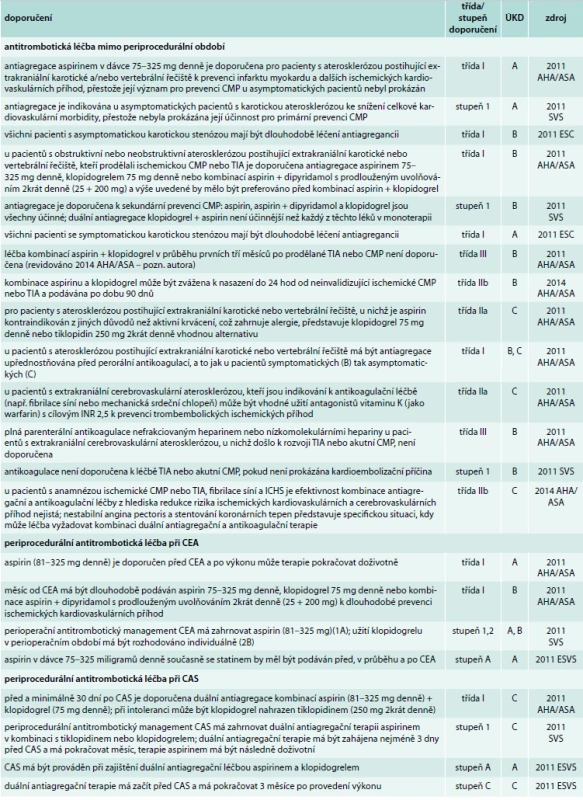
CAS – karotický stenting, CEA – karotická endarterektomie, CMP – cévní mozková příhoda, ICHS – ischemická choroba srdeční, TIA – tranzitorní ischemická ataka, ÚKD – úroveň kvality důkazů Léčba hypertenze
K léčbě hypertenze se vyjadřují 2014 AHA/ASA, 2011 AHA/ASA a 2011 SVS. Všechny doporučené postupy považují antihypertenzní léčbu za indikovanou u asymptomatických pacientů. Doporučení 2011 AHA/ASA bylo revidováno v 2014 AHA/ASA, kdy byla upřesněna formulace cílových hodnot a snížena třída doporučení i ÚKD. Terapie symptomatických pacientů je považována za indikovanou mimo akutní periodu několika prvních dnů po příhodě, nicméně benefit snížení tlaku pod určitou hranici nebyl prokázán studiemi ve vztahu k riziku zhoršení cerebrální ischémie. 2014 AHA/ASA také upozorňují, že nasazení antihypertenzní terapie při systolickém tlaku < 140 mm Hg nebo diastolickém tlaku < 90 mm Hg je s nejistým přínosem.
Kouření
2011 AHA/ASA a 2011 SVS doporučují pacientům navrhnout zanechat kouření a nabídnout možnost intervence.
Hyperlipidemie
2011 AHA/ASA i 2011 SVS doporučují léčbu hypercholesterolemie u všech pacientů s ECVD, přičemž 2011 AHA/ASA specifikuje i cílové hladiny LDL-cholesterolu. V 2014 AHA/ASA byla doporučení revidována a upravena do souladu s AHA/ASA cholesterol guidelines [11] z roku 2013 a podobně jako v 2011 ESC je nyní doporučena léčba statiny u všech symptomatických pacientů s karotickou stenózou, nezávisle na hladině cholesterolu.
Diabetes mellitus
2011 AHA/ASA i 2011 SVS se shodují na léčbě diabetu standardním způsobem. Význam agresivní kompenzace diabetu s cílem těsné kontroly glykemie pro prevenci recidivy cévní mozkové příhody (CMP) nebyl prokázán. 2011 AHA/ASA doporučují u diabetiků nižší cílovou hladinu LDL-cholesterolu. 2014 AHA/ASA doporučují vyšetření k vyloučení či potvrzení diabetu u všech pacientů po prodělané CMP.
Antitrombotická léčba
Antiagregace je ve všech doporučených postupech považována za metodu volby primární i sekundární prevence CMP u pacientů s karotickou stenózou. U asymptomatických pacientů je doporučen aspirin 75–325 mg denně ke snížení kardiovaskulárního rizika, přestože jeho účinnost v prevenci CMP nikdy nebyla prokázána. Pro sekundární prevenci CMP u pacientů symptomatických je doporučen aspirin ve stejném dávkování a jako možné alternativy jsou uváděny klopidogrel 75 mg denně, aspirin 25 mg + dipyridamol 200 mg s prodlouženým uvolňováním 2krát denně. Jako alternativa aspirinu při kontraindikaci z důvodu alergie je doporučován tiklopidin 250 mg 2krát denně. 2011 AHA/ASA uvádějí, že duální antiagregace aspirin + klopidogrel není účinnější než každý z léků v monoterapii, a tuto léčbu nedoporučují první 3 měsíce po tranzitorní ischemické atace (TIA) nebo CMP. 2014 AHA/ASA naopak doporučují zvážit možnost nasazení duální antiagregace aspirin + klopidogrel u pacientů po neinvalidizující CMP nebo TIA do 24 hod od příhody, a tu pak podávat 90 dní (IIbB). Antiagregace mát být vždy upřednostňována před antikoagulační léčbou. Výjimkou jsou situace, v nichž je u pacienta indikovaná antikoagulační léčba z důvodu jiného onemocnění (např. fibrilace síní). Plná parenterální antikoagulace také není doporučena k léčbě akutní CMP. Výjimkou je prokázaná kardioembolizační příčina. Dle 2014 AHA/ASA je význam kombinace antiagregace a antikoagulace z hlediska redukce rizika ischemických kardiovaskulárních a cerebrovaskulárních příhod nejistý, může však mít kardiologickou indikaci.
Antitrombotická léčba při CEA
Aspirin by měl být podáván před, v průběhu a po CEA, bez perioperačního vysazení. 2011 SVS připouští perioperační zajištění klopidogrelem v monoterapii, rozhodování má být individuální. Měsíc po CEA je možná volba ze 3 preparátů: aspirin 75–325 mg denně, klopidogrel 75 mg denně nebo kombinace aspirin 25 mg + dipyridamol 200 mg s prodlouženým uvolňováním 2krát denně.
Antitrombotická léčba při CAS
CAS má být zajištěn duální antiagregační terapií aspirin + klopidogrel, která má být nasazena minimálně 3 dny před výkonem, pokračovat v jeho průběhu a po něm. Doporučení se liší v délce podávání po výkonu – 2011 AHA/ASA a 2011 SVS udávají měsíc, 2011 ESVS udávají 3 měsíce.
Doporučení pro intervence u karotické stenózy
Doporučení pro intervence obsahuje všech 7 aktuálních doporučených postupů. V případě 2011 Australasian a 2011 NICE se jedná pouze o soubor doporučení pro CAS. V tabulkách jsou tato doporučení uvedena odděleně od ostatních. Podobně jako v případě diagnostiky jsou doporučení zcela odlišná pro pacienty symptomatické a asymptomatické, proto byla také zpracována samostatně. Tab. 7 shrnuje doporučení pro intervence u symptomatických pacientů, tab. 8 doporučení pro intervence u asymptomatických pacientů.
7. Indikace intervence u symptomatických pacientů 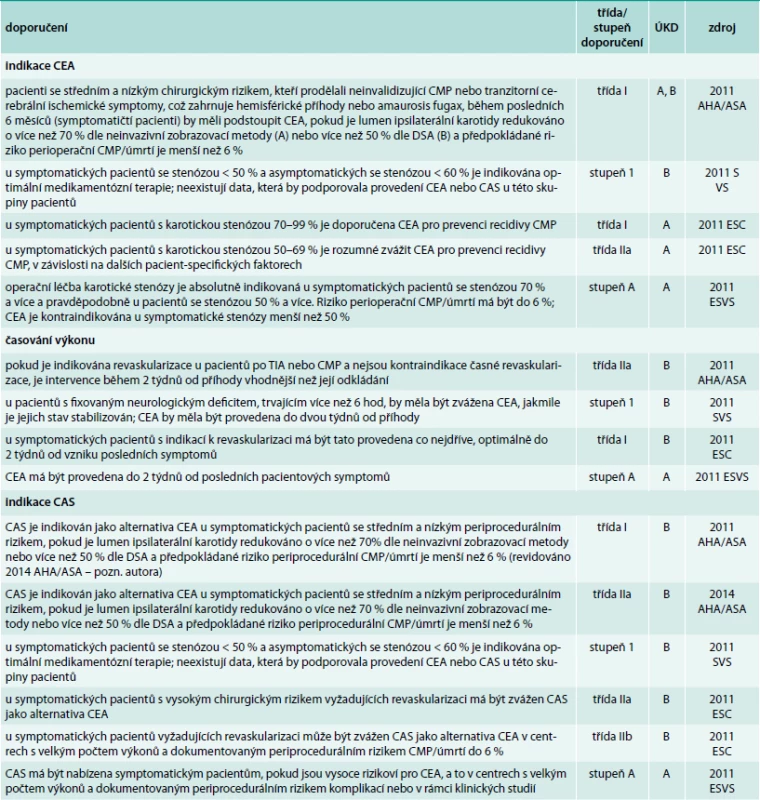

CAS – karotický stenting, CEA – karotická endarterektomie, CMP – cévní mozková příhoda, DSA – digitální subtrakční angiografie, TIA – tranzitorní ischemická ataka, ÚKD – úroveň kvality důkazů 8. Indikace intervence u asymptomatických pacientů 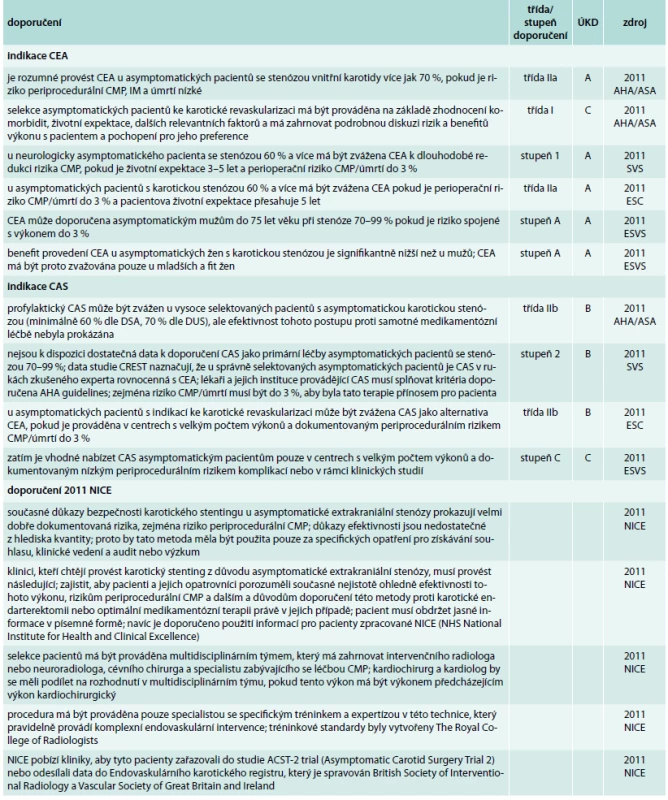
CAS – karotický stenting, CEA – karotická endarterektomie, CMP – cévní mozková příhoda, DSA – digitální subtrakční angiografie, DUS – duplexní ultrasonografie, IM– infarkt myokardu, TIA – tranzitorní ischemická ataka, ÚKD – úroveň kvality důkazů Doporučení pro intervence u symptomatických pacientů
2011 AHA/ASA, 2011 ECS a 2011 ESVS doporučují provedení CEA u symptomatického pacienta při stenóze větší než 50 %. 2011 SVS jsou v souladu, indikační hranici ale mají vyjádřenou nepřímo, a to kontraindikací intervence u symptomatického pacienta při stenóze < 50 %. Všechna 4 guidelines doporučují zcela uniformě provedení výkonu do 2 týdnů od příhody. Doporučení týkající se CAS jsou velmi odlišná. 2011 AHA/ASA doporučují CAS jako alternativu CEA za stejných indikačních kritérií. V 2014 AHA/ASA zůstal po revizi text doporučení beze změn, ale doporučení bylo zmírněno z třídy I na třídu IIa. 2011 ESC nepovažují CAS za adekvátní alternativu CEA a doporučují ji zvážit u pacientů s vysokým chirurgickým rizikem. Jako alternativa CEA může být dle 2011 ESC zvážen CAS v centrech s velkým počtem výkonů a dokumentovaným periprocedurálním rizikem. 2011 ESVS doporučuje nabízet CAS pacientům za obou předpokladů (vysoké chirurgické riziko + centrum s velkým počtem výkonů) nebo v rámci klinických studií. 2011 Australasian uvádějí jako indikaci CAS u symptomatických pacientů vysoké chirurgické riziko a účast pacienta v klinické studii. 2011 NICE považují CAS za metodu akceptovatelnou pro symptomatické pacienty za předpokladu selekce pacientů multidisciplinárním týmem a provádění výkonu zkušeným specialistou za podmínek umožňujících audit výsledků. Důraz je kladen na plnou informovanost pacienta a vysvětlení periprocedurálních rizik a zejména důvodů, proč je pacientovi doporučen CAS proti CEA.
Doporučení pro intervence u asymptomatických pacientů
Indikační hranici udávají 2011 AHA/ASA a 2011 ESVS na úrovni 70 %, naopak 2011 SVS a 2011 ESC na úrovni 60 %. Podmínkou je dále perioperační riziko do 3 % a životní expektace 3–5 let (2011 SVS), 5 let (2011 ESC) nebo věk do 75 let a mužské pohlaví (2011 ESVS). 2011 ESVS také specificky zmiňují známý menší benefit intervence u asymptomatických žen. Podobně 2011 AHA/ASA uvádějí, že selekce má brát v potaz všechny relevantní faktory a je třeba podrobná diskuse s pacientem, vysvětlení benefitu a rizik a respektování jeho volby. Indikace CAS pro asymptomatické pacienty je v guidelines uváděna různě, s velkou formulační obezřetností při vědomí, že nejsou dostupné dostatečné důkazy efektivity tohoto postupu. 2011 Australasian uvádějí, že nejsou dostupná data, která by opravňovala doporučení CAS pro asymptomatické pacienty. 2011 NICE považují CAS za metodu s dobře dokumentovanými riziky pro asymptomatické pacienty a nedostatkem dat potvrzujících efektivnost tohoto postupu. V případě, že je prováděna CAS u asymptomatického pacienta, měla by být selekce pacientů prováděna multidisciplinárním týmem, výkon zkušeným specialistou za podmínek umožňujících audit výsledků a s plnou informovaností pacienta. Důraz je kladen na vysvětlení periprocedurálních rizik výkonu, současné nejistotě ohledně jeho efektivnosti a důvodů, proč je pacientovi nabízen. NICE současně pobízí kliniky k randomizaci pacientů do ACST2, která srovnává CEA a CAS u asymptomatických pacientů.
Kontraindikace karotické intervence a vysoce rizikový pacient
Stenóza < 50 % u symptomatického a < 60–70 % u asymptomatického pacienta je kontraindikací jakékoli intervence. CAS je dále kontraindikován při dokumentovaném výskytu periprocedurálních komplikací vyšším než 3 % a u pacientů s nevhodnou morfologií karotického řečiště pro endovaskulární intervenci při provádění mimo centra s velkým počtem výkonů (2011 ESVS). Jakákoli intervence je také kontraindikována u totální okluze karotické arterie a dále u pacientů, kteří jsou těžce invalidizováni proběhlou CMP, a není u nich předpoklad zachování soběstačnosti (tab. 9).
9. Kontraindikace karotické intervence a vysoce rizikový pacient 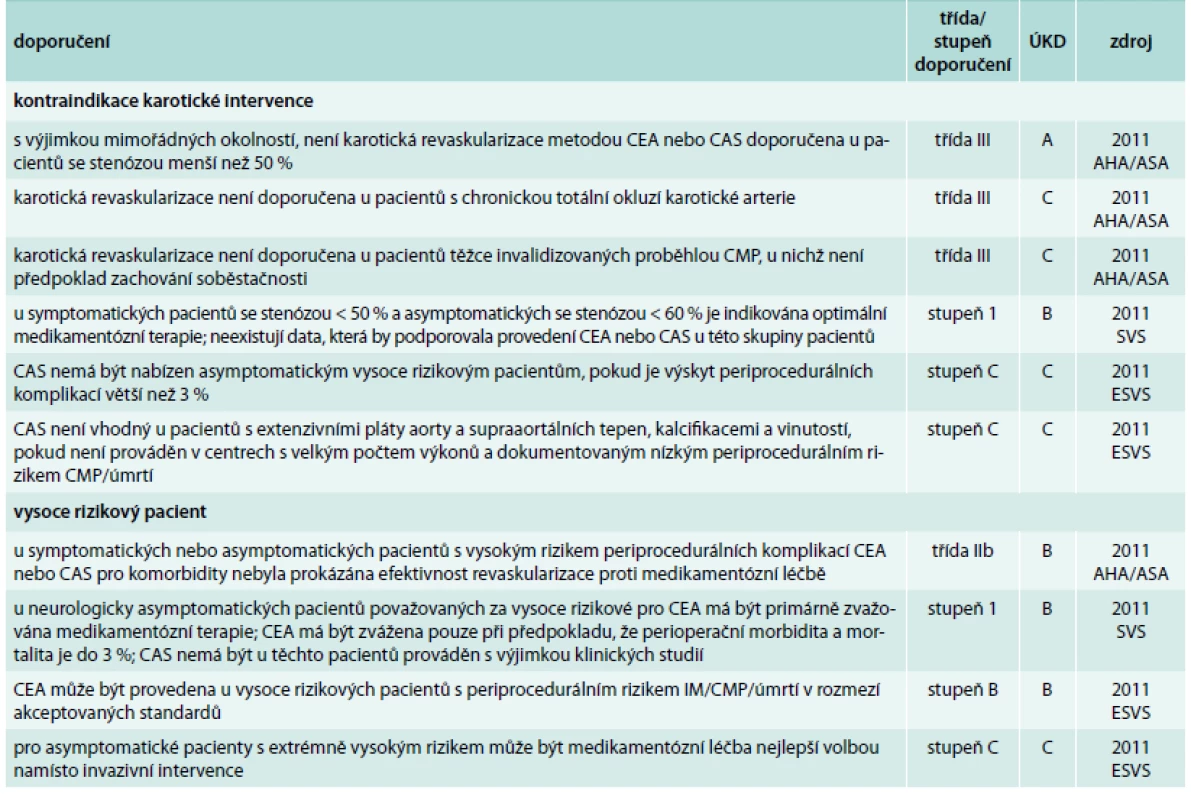
CAS – karotický stenting, CEA – karotická endarterektomie, CMP – cévní mozková příhoda, IM – infarkt myokardu, ÚKD – úroveň kvality důkazů U vysoce rizikových pacientů symptomatických a především asymptomatických by měla být vždy zvažována možnost medikamentózní léčby bez intervence.
Volba intervence mezi CEA a CAS
2011 AHA/ASA uvádí jako jeden z důležitých faktorů při volbě intervence věk pacienta, neboť recentní studie CAS svědčí pro horší výsledky endovaskulární intervence u pacientů starších 70 let. Tomu odpovídají i doporučení, kdy preferovat CEA proti CAS. 2011 SVS a 2011 ESVS shodně považují za nejlepší metodu léčby karotické stenózy indikované k intervenci CEA a doporučují její preferenci ve všech případech. Opět tato doporučení platí zejména pro věkovou kategorii nad 70 let a při nevhodné arteriální patologii pro endovaskulární řešení. Upřednostnit CAS je doporučeno u pacientů s nepříznivou anatomií krku pro chirurgické řešení, dále při přítomnosti tracheostomie, jizvách po radikální krční disekci nebo při restenóze po provedené CEA, dále u pacientů po radioterapii v oblasti hlavy a krku a při lézích kraniálních nervů. CAS má být také upřednostněn u karotických lézí přesahujících do chirurgicky nedostupných oblastí. Navrhováno je také upřednostnění CAS u významně kardiopulmonálně kompromitovaných symptomatických pacientů (tab. 10).
10. Volba intervence mezi karotickou endarterektomií a karotickým stentingem 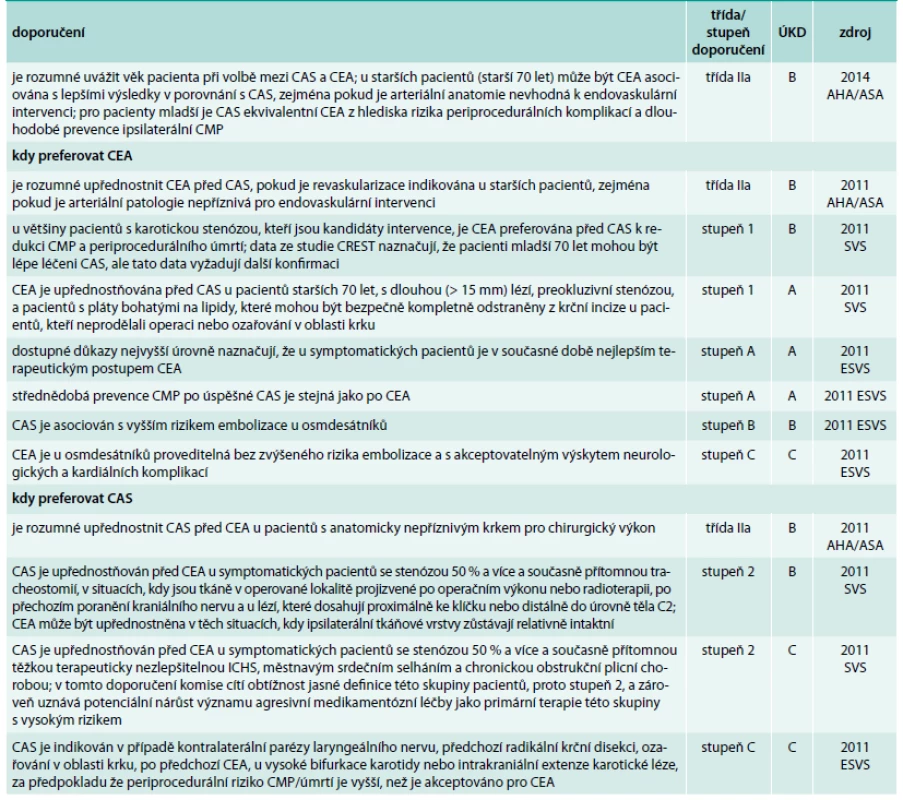
CAS – karotický stenting, CEA – karotická endarterektomie, CMP – cévní mozková příhoda, ICHS – ischemická choroba srdeční, ÚKD – úroveň kvality důkazů Diskuse
Doporučení pro diagnostiku karotické stenózy u symptomatických pacientů
Indikace zobrazovacího vyšetření karotid u symptomatického pacienta je jednoznačná. Důvodem je dostupnost účinné intervence ke snížení rizika recidivy při pozitivním nálezu. Kromě TIA, CMP a retinálních příznaků ve formě amaurosis fugax jsou v doporučeních uvedeny 2 indikace, které zcela nesplňují kritérium symptomatičnosti, a to nález retinální embolie při fundoskopickém vyšetření oka a dále nález asymptomatického infarktového ložiska na zobrazovacím vyšetření mozku. Jsou však racionální.
Volba vyšetřovacích metod je standardní, od metod nejméně invazivních k nejinvazivnějším. Typicky lze předpokládat 2 postupy – DUS, CTA, a případně DSA nebo DUS, MRA a případně DSA. Vzhledem k rychlosti vyšetření, 24hodinové dostupnosti a ceně bude preferována spíše varianta s CTA (obr. 1). Tento postup bude častý u pacientů mimo trombolytické okno (6 hod od počátku symptomů). V době trombolytického okna je diagnostický postup maximálně zredukován, aby byla zkrácena doba od iktu po podání intravenózní nebo intraarteriální trombolýzy [12]. Diagnostika karotického postižení bude obvykle probíhat až po prvotní urgentní diagnostice a nasazení trombolytické terapie. Volba zobrazovací metody pak bude modifikována zvoleným terapeutickým postupem a stavem pacienta.
1. CT angiografické vyšetření zobrazující těsnou odstupovou stenózu (šipka) a. carotis interna vlevo (vessel analysis) 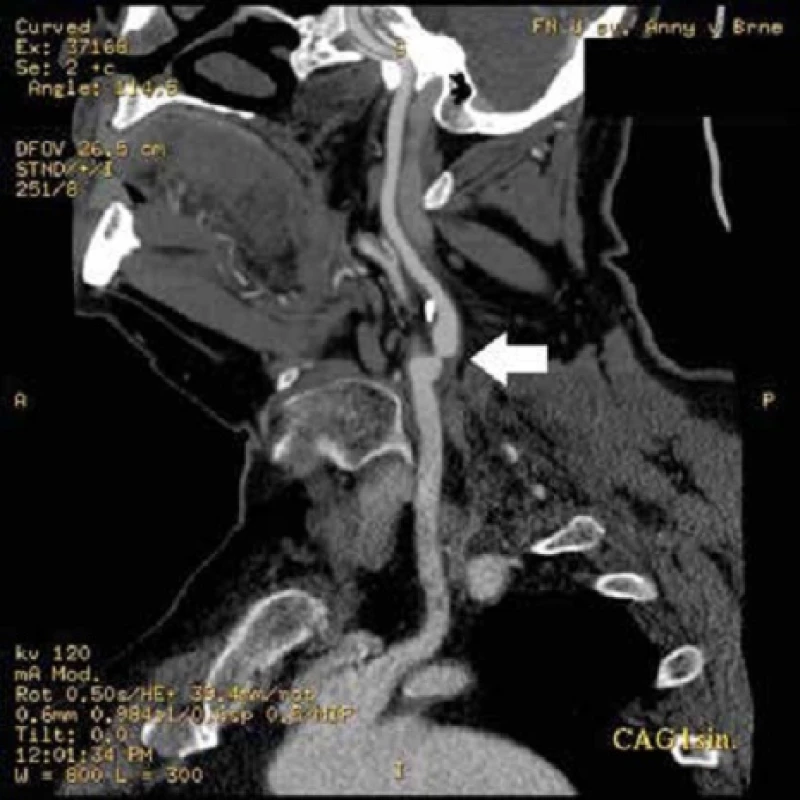
Diagnostika symptomatické karotické stenózy by měla ideálně proběhnout maximálně efektivně za hospitalizace na lůžkovém neurologickém nebo interním pracovišti v režimu akutní péče. Význam rychlosti diagnostiky narůstá zvláště s ohledem na současnou změna přístupu k časování intervence u symptomatických pacientů.
Doporučení pro diagnostiku karotické stenózy u asymptomatických pacientů
Indikace vyšetření karotid u asymptomatických pacientů jsou, podobně jako u jiných screeningových vyšetření určovány na základě zhodnocení prevalence onemocnění v populaci, rizik vyšetření, senzitivity a specifity diagnostické metody a její ceny, stejně jako terapeutickými možnostmi při pozitivním nálezu. Vědecké důkazy nejsou dostupné. Není proto překvapivé, že jsou některá doporučení v jednotlivých doporučených postupech až protichůdná. Oba hlavní doporučené postupy (2011 AHA/ASA a 2011 SVS) se také nevyhnuly drobným nepřesnostem. Začneme-li z opačného konce, tedy v jakých případech vyšetřování doporučeno není, tak se oba dokumenty shodují, že u asymptomatických pacientů bez RF aterosklerózy nemá být zobrazovací vyšetření prováděno. Důvodem je relativně nízký výskyt karotické stenózy v celkové populaci, senzitivita, specifita a cena DUS, a v poslední době značně zpochybňovaný přínos intervence u asymptomatických pacientů. 2011 AHA/ASA dále nedoporučují vyšetření u pacientů s neurologickými a psychiatrickými onemocněními, která nesouvisejí s fokální cerebrální ischemií, a opakovat vyšetření u pacientů bez RF aterosklerózy, kteří měli na iniciálním vyšetření karotid negativní nález. 2011 SVS guidelines pak explicitně nedoporučují vyšetření karotid u pacientů, kteří prodělali radioterapii v oblasti hlavy a krku. Je známo, že u těchto pacientů se vyvíjí relativně často karotická stenóza. Postiradiační stenóza se ale od běžné aterosklerotické liší tím, že se obvykle jedná o postižení difuzní a řada pacientů zůstává dlouhodobě asymptomatická. Navíc se provedení karotické endarterektomie realizuje v ozářeném terénu se zvýšeným chirurgickým rizikem a je relativně indikován karotický stenting. Dlouhodobé výsledky CAS u této skupiny pacientů přitom také nejsou k dispozici.
V jakých případech tedy vyšetření provést? Doporučení uvádějí prakticky 4 indikace: sledování již diagnostikované stenózy, šelest, známý výskyt jiného aterosklerotického onemocnění u pacienta a RF aterosklerózy. 2011 AHA/ASA doporučuje opakovat vyšetření 1krát ročně u pacientů s dříve diagnostikovanou stenózou > 50 % ke sledování progrese onemocnění, což je jistě akceptovatelné. Karotický šelest je indikace s protichůdným doporučením. 2011 AHA/ASA považují za rozumné provést vyšetření u pacientů s karotickým šelestem. Autoři 2011 SVS naopak nedoporučují provádět vyšetření u asymptomatických pacientů se šelestem, pokud nemají RF aterosklerózy. Odůvodnění doporučení či nedoporučení indikace vyšetření karotid při výskytu šelestu se v obou doporučených postupech opírají o největší studii karotického DUS screeningu u asymptomatických pacientů [13]. Autoři hodnotili prevalenci karotické stenózy > 75 % ve 4 skupinách pacientů (CMP, TIA, asymptomatický karotický šelest, asymptomatické kontroly bez šelestu). Zjištěná prevalence byla CMP – 29 %, TIA – 18 %, asymptomatický šelest – 17 %, asymptomatický pacient bez šelestu – 1,2 %. V 2011 SVS je jako vysvětlení uvedena chybná interpretace výsledků studie. Autoři uvádějí prevalenci karotické stenózy > 75 % při výskytu šelestu 1,2 %, což byla prevalence kontrolní skupiny bez šelestu. Z toho hlediska je možno se spíše přiklonit k doporučení 2011 AHA/ASA, nicméně efektivita v oblasti prevence CMP v této skupině pacientů nikdy nebyla prokázána.
Dalšími 2 indikacemi jsou výskyt jiného AS onemocnění u pacienta a RF aterosklerózy. 2011 AHA/ASA a 2011 SVS shodně doporučují vyšetření u pacientů s ischemickou chorobou dolních končetin (ICHDKK). Druhým AS onemocněním hodným zřetele je ischemická choroba srdeční (ICHS). 2011 AHA/ASA doporučují zvážit vyšetření u všech pacientů s ICHS, 2011 SVS doporučují zvážit vyšetření u pacientů připravovaných ke koronárnímu bypassu a pacientů starších 65 let. Vyšetření karotického řečiště je tedy možno zvážit u převážné většiny pacientů s ICHS. Posledním explicitně uváděným onemocněním je aneuryzma abdominální aorty (AAA). 2011 AHA/ASA doporučují provedení vyšetření u pacientů s aterosklerotickým AAA. 2011 SVS naopak nedoporučují vyšetření karotid u pacientů s AAA, pokud nemají jinou indikaci. 2011 AHA/ASA uvádějí jako indikaci přesně aterosklerotické AAA. Náhled na etiopatogenezi převážné většiny AAA se v poslední době změnil. Za hlavní mechanizmus jsou nyní považovány genetické faktory nikoli ateroskleróza. 2011 SVS svá doporučení zakládají na relativně malé prevalenci karotické stenózy u pacientů s AAA a neexistenci důkazů, které by prokázaly zvýšené riziko periprocedurální CMP v této skupině. Práce, které studovaly prevalenci asymptomatické karotické stenózy > 70 % u pacientů s AAA, udávají relativně malý výskyt: Marsico [14] – 0 ze 100 pacientů (0 %); Axelrod [15] – 2 z 206 pacientů (1 %); Vranes [16] 50 z 650 mužů (7,7 %), 0 z 90 žen (0 %), celkem 50 ze 740 (6,8 %). Data prokazující zvýšené perioperační riziko CMP při resekci AAA u pacientů s asymptomatickou karotickou stenózou > 70 % nejsou k dispozici, stejně jako není k dispozici důkaz lepších operačních výsledků po předchozím provedení CEA. Indikaci vyšetření karotického řečiště u asymptomatických pacientů s AAA je tedy možno považovat přinejmenším za spornou.
Doporučení vyšetření karotického řečiště z důvodu RF aterosklerózy jsou nízké třídy. 2011 AHA/ASA doporučují zvážit vyšetření u pacientů s alespoň dvěma RF z následujících: hypertenze, hyperlipidemie, kouření, prvostupňový příbuzný s projevy aterosklerózy před 60. rokem věku, ischemická CMP v rodinné anamnéze. 2011 SVS doporučují zvážit vyšetření u pacientů nad 65 let s alespoň jedním z následujících RF: ICHS, kouření, hypercholesterolemie. V obou guidelines je však zmíněno, že není jasné, zda diagnostika extrakraniálního karotického onemocnění bude opravňovat k intervencím, které budou mít pozitivní přínos pro tyto pacienty. Indikace je tedy především na uvážení každého lékaře.
Metodou volby je DUS, následovaná CTA nebo MRA. DSA je jako nejinvazivnější metoda vyhrazena k rozhodnutí konfliktních výsledků méně invazivních vyšetření a při indikaci CAS.
Souhrnně se dá konstatovat, že jasnou indikací vyšetření karotid u asymptomatických pacientů jsou dříve diagnostikovaná stenóza karotidy a pravděpodobně karotický šelest. Vyšetření z důvodu jiného AS onemocnění nebo RF aterosklerózy je diskutabilní, zvláště v souvislosti se zpochybňovaným přínosem intervencí na karotidách u asymptomatických pacientů. Nicméně, alespoň v případě ICHDKK a ICHS se zdá vhodné.
Doporučení pro medikamentózní terapii karotické stenózy
Optimální medikamentózní léčba je indikovaná u všech pacientů s karotickou stenózou nezávisle na plánované intervenci. Doporučení nejsou v rozporu. Je indikována léčba hypertenze s úskalím její indikace v době akutní CMP, zanechání kouření, standardní léčba diabetu a terapie statiny, která je indikovaná u všech pacientů s karotickou stenózou, a to nezávisle na hladině cholesterolu.
Antiagregační léčba je standardní a dlouhodobě zavedený terapeutický postup u všech pacientů s karotickou stenózou. U asymptomatických pacientů je doporučován aspirin a při alergii tiklopidin. U symptomatických pacientů jsou doporučeny 3 preparáty, které jsou co do účinnosti srovnatelné. Je to aspirin, klopidogrel nebo kombinace aspirin + dipyridamol s prodlouženým uvolňováním. Vývoj prodělávají v poslední době především názory na duální antiagregaci. Zatímco 2011 AHA/ASA nedoporučovala duální antiagregaci aspirin + klopidogrel po dobu 3 měsíců po TIA nebo CMP, 2014 AHA/ASA uvádějí, že může být zváženo nasazení duální antiagregace do 24 hod od neinvalidizující CMP nebo TIA s délkou podávání po dobu 90 dnů (IIbB). Toto doporučení bylo postaveno na základě výsledků 2 nových studií CHANCE [17] a FASTER [18], které prokázaly lepší výsledky při časné administraci duální antiagregace u pacientů po neinvalidizující CMP. Vždy je ale třeba zvážit riziko recidivy CMP proti riziku krvácivých komplikací. Antikoagulační terapie je preferována pouze, je-li indikována pro jiné onemocnění (fibrilace síní, umělá srdeční chlopeň, apod).
U pacientů v hyperakutní periodě TIA či CMP není indikována plná antikoagulace ani nefrakcionovaným ani frakcionovaným heparinem! Toto doporučení je zdůrazněno i v aktuálních 2013 AHA/ASA doporučených postupech pro management akutní CMP [12].
V rámci správné indikace antitrombotické terapie je třeba zmínit ještě jeden důležitý problém, a to je antitrombotické zajištění během intervence na karotidě. Situace je odlišná pro CEA a CAS. CEA je otevřený chirurgický výkon a tradičním, desítky let aplikovaným přístupem bylo vysazování antiagregační terapie v perioperačním období. V současné době jsou periferní vaskulární výkony prováděny bez vysazování antiagregace a recentní data potvrzují, že tento postup nevede ke zvýšení krvácivých komplikací [19,20]. Individuálně je však třeba zvažovat ponechání či vysazení alespoň jednoho z preparátů u duální antiagregace. CAS je prováděn vždy za duální antiagregace, kterou je třeba zahájit alespoň 3 dny před výkonem a následně podávat po dobu 1–3 měsíců.
Doporučení pro intervence u symptomatické karotické stenózy
Všechny aktuální doporučené postupy doporučují provedení CEA u stenózy > 70 % a v různé síle také při stenóze 50–69 %. Důvodem je prokázaný přínos CEA pro prevenci recidivy CMP u symptomatických pacientů [21]. Při stenóze < 50 % je revaskularizace kontraindikovaná. CEA je metoda dlouhodobě zavedená, ověřená v klinické praxi a představuje zlatý standard, s kterým je třeba nové metody srovnávat (obr. 2).
2. Peroperační snímek zobrazující výsledek konvenční karotické endarterektomie. Uzávěr arteriotomie a. carotis communis a interna byl proveden pomocí žilní záplaty 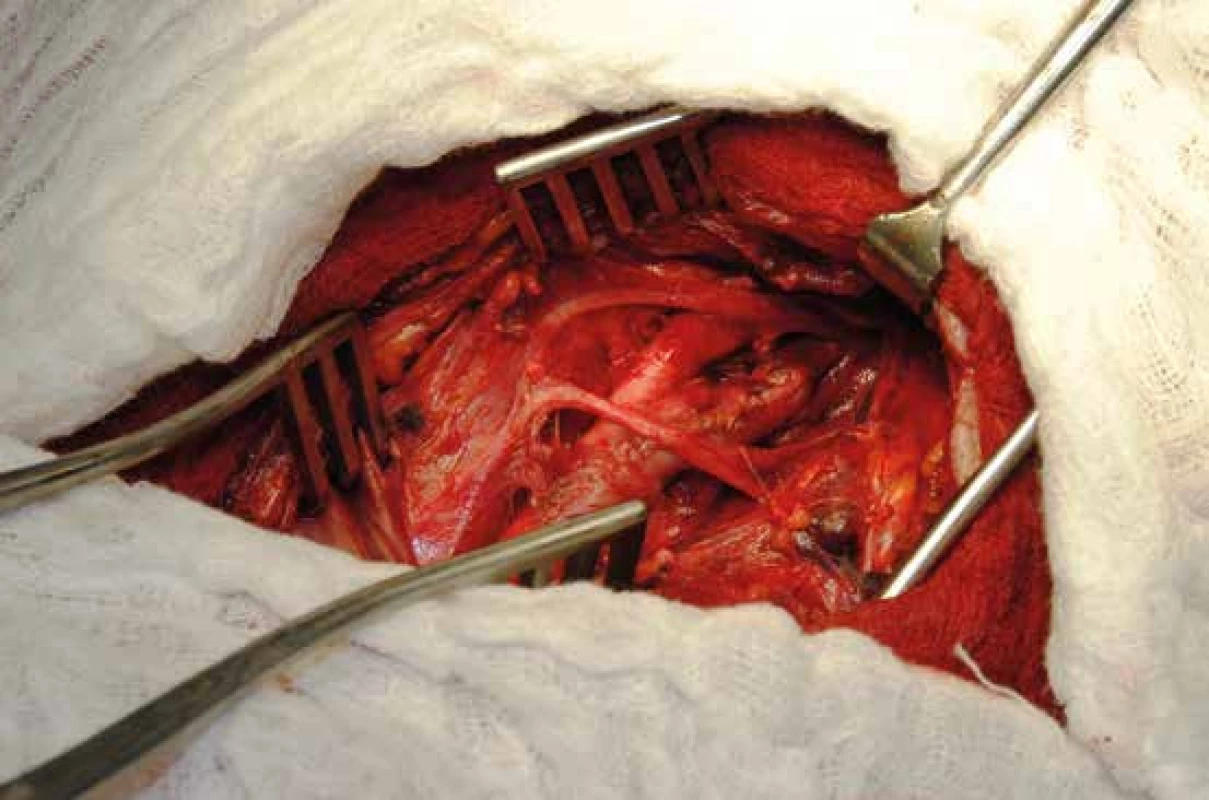
Indikace CAS se v jednotlivých dokumentech velmi liší. AHA/ASA považují u symptomatické stenózy CAS za alternativu CEA. Třída doporučení však byla v update 2014 zmírněna (I na IIa). Odlišný přístup k této otázce zaujímají všechny ostatní doporučené postupy, které upřednostňují CEA před CAS. Za indikaci CAS je obvykle považována intervence na karotidě u pacienta s vysokým chirurgickým rizikem indikovaným k CEA nebo účast ve studii. Protichůdná doporučení jsou podmíněna mnoha faktory. Kvalitních studií, které by byly metodologicky bez větších problémů, není dostatek. Dostupné práce poskytují často protichůdné výsledky, stejně jako je obtížná i jejich interpretace. Typickým příkladem je jedna z největších recentní studií srovnávající CAS a CEA – The Carotid Revascularization Endarterectomy Versus Stenting Trial (CREST) [22]. Do této studie bylo randomizováno celkem 2 502 pacientů. Primárním endpointem byl kumulativní výskyt periprocedurální CMP, infarktu myokardu (IM), úmrtí a ipsilaterální CMP do 4 let od intervence. Výsledky byly bez statisticky signifikantního rozdílu (CAS vs CEA; 7,2 % vs 6,8 %; hazard ratio 1,11; 95 % CI 0,81–1,51; P > 0,51). Analýza jednotlivých složek kumulativního endpointu ale prokázala vyšší výskyt CMP/úmrtí ve větvi CAS (6,0 % vs 3,2 %) a naopak vyšší výskyt IM ve větvi CEA (2,3 % vs. 1,1 %). Interpretace výsledku je pak i otázkou posouzení důležitosti jednotlivých typů komplikací pro další život pacienta. Výskyt komplikací v této studii se také zdá být poměrně vysoký, neboť interim analýza probíhající studie the Asymptomatic Carotid Surgery Trial 2 (ACST2) v souboru 986 randomizovaných pacientů vykázala kumulativní riziko periprocedurální invalidizující CMP, fatálního IM a úmrtí 1 % ve větvi CEA i CAS [23]. Vzhledem k odlišné definici endpointů ale přímé srovnání není možné.
Endovaskulárních instrumentů, stentů, protekcí proti distální embolizaci jsou v současné době na trhu stovky a extrapolace výsledků jednoho produktu na ostatní může být velmi zavádějící. Z hlediska omezených zdrojů je také nutné zmínit, že CAS představuje v současné době nejdražší metodu řešení karotické stenózy [24], která zatím neprokázala lepší výsledky proti metodám zavedeným. V neposlední řadě také sílí hlasy zpochybňující platnost dat NASCET, ECST a VACS pro současnost. Výsledky CEA i konzervativního postupu budou při moderní medikamentózní léčbě pravděpodobně odlišné a benefit intervence může být tímto zredukován. Vyjdeme-li ovšem z důkazů, které k dispozici máme, je možno uzavřít, že u symptomatických pacientů se stenózou karotidy > 50 % je intervence indikována. Zdá se také rozumné upřednostňovat CEA před CAS u převážné většiny symptomatických pacientů. CAS by měl být vyhrazen pro pacienty s vysokým chirurgickým rizikem a randomizované kontrolované klinické studie. Centralizace těchto vysoce komplexních intervencí a jejich provádění zkušeným specialistou s dostatečným počtem výkonů ročně se zdá být také racionálním požadavkem.
Časování výkonu u symptomatického pacienta je jedním z nejuniformnějších doporučení aktuálních guidelines. Zároveň jde pravděpodobně o největší posun v chirurgické léčbě symptomatické karotické stenózy v poslední době. Tradičním přístupem bylo odkládání operačního výkonu o 6 týdnů a déle pro prokázané horší výsledky akutních výkonů [25]. Tato praxe ještě stále ve vysokém procentu přetrvává [26–28]. Ve srovnání s rizikem recidivy v prvních dnech po CMP je však akutní operace i při horších operačních výsledcích prokazatelně přínosná [21,29]. Podmínkou tohoto řešení je úzká spolupráce neurologa nebo internisty s cévním chirurgem, rychlá stabilizace kandidátů intervence a jejich příprava k časné revaskularizaci, stejně jako změna tradičního chirurgického pohledu na časné výkony na karotidách.
Doporučení pro intervence u asymptomatické karotické stenózy
Indikace intervence u asymptomatického pacienta je stále velice sporná a názory odborníků nejednotné [30]. Pokud je v současné době zpochybňována platnost dat NASCET, ECST a VACS, pro asymptomatické pacienty toto platí dvojnásob. Teoreticky je možné, že zavedením moderní medikamentózní léčby došlo již k tak velké redukci ročního rizika CMP, že přínos intervence pro asymptomatické pacienty může být statisticky vzato minimální. Konečné rozhodnutí o intervenci by proto mělo vycházet převážně ze strany pacienta po podrobném vysvětlení terapeutických možností, jejich přínosů a rizik a mělo by být respektováno. Otázka nemalých nákladů spojených s operačními intervencemi na velkém množství asymptomatických pacientů při minimálním přínosu je také zcela na místě.
Kontraindikace karotické intervence a vysoce rizikový pacient
V doporučených postupech uvedené kontraindikace odpovídají recipročně indikacím. Specifický indikační problém však představuje tzv. vysoce rizikový pacient. Doporučení v tomto smyslu obsahují 2011 AHA/ASA, 2011 SVS, 2011 ESC a 2011 ESVS. U vysoce rizikových pacientů je vhodné zvažovat jako primární terapeutický postup medikamentózní léčbu, zejména jedná-li se pacienty asymptomatické. Intervenci je pak možno indikovat v případě, že je předpokladatelné provedení výkonu v rámci akceptovaných standardů periprocedurálních komplikací. 2011 SVS doporučuje u těchto pacientů neprovádět CAS mimo klinické studie, 2011 ESC naopak zvážení CAS jako alternativy CEA doporučuje. Kromě těchto protichůdných doporučení, přestože každé z nich má jakousi logiku, je velkým problémem neexistence jasných kritérií, kdo je vlastně „vysoce rizikový pacient“. Data z randomizovaných kontrolovaných klinických studií pro tuto skupinu pacientů je také obtížné najít, protože např. pokročilá kardiopulmonální onemocnění bývají často exkluzivními kritérii. Třída doporučení je proto nízká. Rozhodnutí o léčbě rizikových pacientů budou pravděpodobně vždy na klinickém úsudku specialisty než rozhodnutími podloženými jednoznačnými důkazy.
Volba druhu intervence
Volba druhu intervence je aktuální a velmi diskutovanou otázkou, zejména z hlediska rychlého rozvoje CAS. Ze strany výrobců endovaskulárních instrumentárií byl ve velmi krátké době trh téměř zahlcen produkty pro CAS, ovšem velmi rozdílných konstrukcí i kvality. Dle výsledků recentních studií vykazuje CAS horší výsledky u symptomatických pacientů starších 70 let. Nelze však říci, zda běžící nebo připravované studie toto zjištění potvrdí. Na základě dostupných důkazů se zdá rozumné u většiny pacientů upřednostnit CEA před CAS. Prostor pro CAS je zejména u symptomatických pacientů indikovaných k intervenci, u nichž řešení není chirurgicky možné z důvodu extenzivní nedosažitelné léze a u pacientů s vysokým chirurgickým rizikem. Jsou to např. stavy po iradiaci, předcházející operace v oblasti postižené karotidy (CEA, blokové krční disekce), tracheostomie apod. Každý CAS by měl být indikován multioborovým týmem po zvážení všech potenciálních rizik a prováděn zkušenými specialisty s dostatečným objemem těchto výkonů ročně. Indikace CAS u asymptomatických pacientů je v současné době velice sporná. Jedná se o nejdražší metodu řešení karotické stenózy a zároveň nejméně ověřenou z hlediska efektivity. V době, kdy je stále více zpochybňována i úloha CEA v léčbě asymptomatické stenózy, je pro CAS pravděpodobně prostor pouze v rámci randomizovaných kontrolovaných klinických studií, jak doporučuje i převážná část aktuálních doporučených postupů. Nesmíme také zapomínat, že do současné doby nebyl žádnou studií prokázán jasný benefit CAS proti CEA.
Závěr
Karotická stenóza je závažným zdravotnickým a socioekonomickým problémem. Ideální diagnostické a terapeutické postupy se neustále vyvíjejí. U symptomatických pacientů je zobrazovací vyšetření karotid indikováno vždy. Léčba je medikamentózní a při stenóze > 50 % má být kombinována s intervencí. Zlatým standardem je karotická endarterektomie. Karotický stenting je vhodný pro pečlivě selektované pacienty a měl by být centralizován do center s velkým počtem výkonů. Diagnostika a terapie asymptomatických pacientů je velmi kontroverzní téma. Tato skupina pacientů je málo riziková z hlediska CMP/úmrtí již při samotné medikamentózní terapii. Dostupná data jsou z dob, kdy v terapii nebyly zavedeny statiny a další moderní léky. Do doby než budou dostupná data z nových studií u asymptomatických pacientů, které neopomenou k ramenům karotické endarterektomie a karotického stentingu přidat větev konzervativní terapie, je nutno indikovat výkony s vědomím těchto skutečností. Rozhodnutí by proto mělo být do značné míry na pacientovi po podrobném vysvětlení možností léčby.
MUDr. Tomáš Novotný, Ph.D.
tomas.novotny@fnusa.cz
Centrum cévních onemocnění II. chirurgické kliniky LF MU a FN u sv. Anny, Brno
www.fnusa.cz
Doručeno do redakce 14. 9. 2015
Přijato po recenzi 20. 10. 2015
Sources
1. North American Symptomatic Carotid Endarterectomy Trial Collaborators. Beneficial effect of carotid endarterectomy in symptomatic patients with high-grade carotid stenosis. N Engl J Med 1991; 325(7): 445–453.
2. European Carotid Surgery Trialists’ Collaborative Group. Randomised trial of endarterectomy for recently symptomatic carotid stenosis: final results of the MRC European Carotid Surgery Trial (ECST). Lancet 1998; 351(9113): 1379–1387.
3. Mayberg MR, Wilson SE, Yatsu F et al. Carotid endarterectomy and prevention of cerebral ischemia in symptomatic carotid stenosis. Veterans Affairs Cooperative Studies Program 309 Trialist Group. JAMA 1991; 266(23): 3289–3294.
4. Brott TG, Halperin JL, Abbara S et al. 2011 ASA/ACCF/AHA/AANN/AANS/ACR/ASNR/CNS/SAIP/SCAI/SIR/SNIS/SVM/SVS guideline on the management of patients with extracranial carotid and vertebral artery disease: executive summary. A report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines, and the American Stroke Association, American Association of Neuroscience Nurses, American Association of Neurological Surgeons, American College of Radiology, American Society of Neuroradiology, Congress of Neurological Surgeons, Society of Atherosclerosis Imaging and Prevention, Society for Cardiovascular Angiography and Interventions, Society of Interventional Radiology, Society of NeuroInterventional Surgery, Society for Vascular Medicine, and Society for Vascular Surgery. Circulation 2011; 124(4): 489–532.
5. Ricotta JJ, Aburahma A, Ascher E et al. Updated Society for Vascular Surgery guidelines for management of extracranial carotid disease. J Vasc Surg 2011; 54(3): e1-e31. Dostupné z DOI: http://dx.doi.org/10.1016/j.jvs.2011.07.031.
6. European Stroke Organisation. Tendera M, Aboyans V, Bartelink ML et al. ESC Guidelines on the diagnosis and treatment of peripheral artery diseases: Document covering atherosclerotic disease of extracranial carotid and vertebral, mesenteric, renal, upper and lower extremity arteries: the Task Force on the Diagnosis and Treatment of Peripheral Artery Diseases of the European Society of Cardiology (ESC). Eur Heart J 2011; 32(22): 2851–2906.
7. Liapis CD, Bell PR, Mikhailidis D et al. ESVS guidelines. Invasive treatment for carotid stenosis: indications, techniques. Eur J Vasc Endovasc Surg 2009; 37(4 Suppl):S1-S19.
8. Carotid Stenting Guidelines Committee: an Inter-collegiate Committee of the RACP (ANZAN, CSANZ), RACS (ANZSVS) and RANZCR. Guidelines for patient selection and performance of carotid artery stenting. Intern Med J 2011; 41(4): 344–347.
9. Neequaye SK, Halliday AW. Carotid artery stenting: the 2011 NICE guidelines. Heart 2012; 98(4): 274–275.
10. Kernan WN, Ovbiagele B, Black HR et al. Guidelines for the prevention of stroke in patients with stroke and transient ischemic attack: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke 2014; 45(7): 2160–2236. Erratum in Correction. [Stroke. 2015]
11. Stone NJ, Robinson JG, Lichtenstein AH et al. 2013 ACC/AHA guideline on the treatment of blood cholesterol to reduce atherosclerotic cardiovascular risk in adults: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. Circulation 2014; 129(25 Suppl 2): S1-S45. Erratum in Circulation. 2014; 129(25 Suppl 2): S46-S48.
12. Jauch EC, Saver JL, Adams HP Jr et al. Guidelines for the early management of patients with acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Stroke 2013; 44(3): 870–947.
13. Zhu CZ, Norris JW. Role of carotid stenosis in ischemic stroke. Stroke 1990; 21(8): 1131–1134.
14. Marsico F, Giugliano G, Ruggiero D et al. Prevalence and severity of asymptomatic coronary and carotid artery disease in patients with abdominal aortic aneurysm. Angiology 2015; 66(4): 360–364.
15. Axelrod DA, Diwan A, Stanley JC et al. Cost of routine screening for carotid and lower extremity occlusive disease in patients with abdominal aortic aneurysms. J Vasc Surg 2002; 35(4): 754–758.
16. Vranes M, Davidovic L, Vasic D et al. Coexistence of internal carotid artery stenosis in patients with abdominal aortic aneurysm. Korean Circ J 2013; 43(8): 550–556.
17. Wang Y, Wang Y, Zhao X et al. Clopidogrel with aspirin in acute minor stroke or transient ischemic attack. N Engl J Med 2013; 369(1): 11–19.
18. Kennedy J, Hill MD, Ryckborst KJ et al. Fast assessment of stroke and transient ischaemic attack to prevent early recurrence (FASTER): a randomised controlled pilot trial. Lancet Neurol 2007; 6(11): 961–969.
19. Stone DH, Goodney PP, Schanzer A et al. Clopidogrel is not associated with major bleeding complications during peripheral arterial surgery. J Vasc Surg 2011; 54(3): 779–784.
20. Batchelder A, Hunter J, Cairns V et al. Dual Antiplatelet Therapy Prior to Expedited Carotid Surgery Reduces Recurrent Events Prior to Surgery without Significantly Increasing Peri-operative Bleeding Complications. Eur J Vasc Endovasc Surg 2015; 54(3):779–784. Dostupné z DOI: http://dx.doi.org/10.1016/j.ejvs.2015.07.019.
21. Rothwell PM, Eliasziw M, Gutnikov SA et al. Endarterectomy for symptomatic carotid stenosis in relation to clinical subgroups and timing of surgery. Lancet 2004; 363(9413): 915–924.
22. Mantese VA, Timaran CH, Chiu D et al. The Carotid Revascularization Endarterectomy versus Stenting Trial (CREST): stenting versus carotid endarterectomy for carotid disease. Stroke 2010; 41: (10 Suppl): S31-S34.
23. ACST-2 Collaborative Group. Halliday A, Bulbulia R, Gray W et al. Status update and interim results from the asymptomatic carotid surgery trial-2 (ACST-2). Eur J Vasc Endovasc Surg 2013; 46(5): 510–518.
24. Eslami MH, McPhee JT, Simons JP et al. National trends in utilization and postprocedure outcomes for carotid artery revascularization 2005 to 2007. J Vasc Surg 2011; 53(2): 307–315.
25. Rockman CB, Maldonado TS, Jacobowitz GR et al. Early carotid endarterectomy in symptomatic patients is associated with poorer perioperative outcomes. J Vasc Surg 2006; 44(3): 480–487.
26. Fairhead JF, Mehta Z, Rothwell PM. Population-based study of delays in carotid imaging and surgery and the risk of recurrent stroke. Neurology 2005; 65(3): 371–375.
27. Dellagrammaticas D, Lewis S, Colam B et al. Carotid endarterectomy in the UK: acceptable risks but unacceptable delays. Clin Med 2007; 7(6): 589–592.
28. Gladstone DJ, Oh J, Fang J et al. Urgency of carotid endarterectomy for secondary stroke prevention: results from the Registry of the Canadian Stroke Network. Stroke 2009; 40(8): 2776–2782.
29. Coull AJ, Lovett JK, Rothwell PM et al. Population based study of early risk of stroke after transient ischaemic attack or minor stroke: implications for public education and organisation of services. BMJ 2004; 328(7435): 326.
30. Naylor AR, Gaines PA, Rothwell PM. Who benefits most from intervention for asymptomatic carotid stenosis: patients or professionals? Eur J Vasc Endovasc Surg 2009; 37(6): 625–632.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2015 Issue 12-
All articles in this issue
- Regional registry of pulmonary embolism
- Antithrombotic therapy and nonvariceal upper gastrointestinal bleeding
- Ventilatory function in patients with silicosis or coal workers’ pneumoconiosis
- Lenalidomide treatment in myelodysplastic syndrome with 5q deletion – Czech MDS group experience
- Investigation of tubular reabsorption of phosphates in patients with chronic kidney disease
- Role of soluble receptor ST2 measurment in diagnosis and prognostic stratification in patients with heart failure
- Geriatric multimorbidity – one of the key problem of contemporary medicine
- Carotid stenosis – diagnosis and treatment
-
PATHWAY-2 Study: spironolactone vs placebo, bisoprolol and doxazosin to determine optimal treatment of resistant hypertension.
Spironolactone high effective in lowering blood pressure in drug resistant hypertension - Monoclonal immunoglobulin (M-Ig) and skin diseases from the group of mucinoses – scleredema adultorum Buschke and scleromyxedema. Description of four cases and an overview of therapies
- Uncorrected Tetralogy of Fallot – a case report of a 69-year-old patient
- Medicine at a polar station in Antarctica
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Carotid stenosis – diagnosis and treatment
- Geriatric multimorbidity – one of the key problem of contemporary medicine
- Investigation of tubular reabsorption of phosphates in patients with chronic kidney disease
- Ventilatory function in patients with silicosis or coal workers’ pneumoconiosis
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

