-
Medical journals
- Career
Vliv jaterní cirhózy na farmakokinetiku a farmakodynamiku léčiv
Authors: F. Perlík
Authors‘ workplace: Farmakologický ústav 1. lékařské fakulty UK a VFN Praha, přednosta doc. MU Dr. Ondřej Slanař, Ph. D.
Published in: Vnitř Lék 2013; 59(7): 584-586
Category:
Overview
Metabolické funkce jater se významně podílejí na celkové clearance řady léčiv. U jaterní cirhózy se na snížené eliminaci léčiv uplatňují průtok krve játry, funkce hepatocytů a množství jaterní tkáně. Farmakokinetické a farmakodynamické změny závisejí na charakteru a stupni jaterního poškození a na vlastnostech podaného léčiva. Hepatocyty mají různou extrakční schopnost ve vztahu k jednotlivým léčivům. Mezi léčiva s vysokou jaterní extrakcí patří např. anodyna, propranolol, metoprolol, verapamil a lidokain. Tato léčiva výrazně závisejí na prvním průchodu játry. Při intrahepatálním a extrahepatálním zkratování krve se podstatně zvyšuje jejich biologická dostupnost a snižuje se clearance. Snížení jaterní clerance u léčiv s nízkým extrakčním koeficientem, např. chlordiazepoxidu, diazepamu nebo furosemidu, je dáno omezením vlastní funkční kapacity eliminovat léčivo. Predikce jaterní metabolické poruchy na základě běžného biochemického vyšetření enzymových aktivit není postačující. U pokročilé jaterní cirhózy mají zvýšené riziko léčiva s malou terapeutickou šíří. Vždy je potřebné zvážit, zda je farmakoterapie nutná, používat malé dávky a pečlivě sledovat nemocného.
Klíčová slova:
clearance léčiv – farmakodynamika – farmakokinetika – jaterní cirhóza – úprava dávkováníÚvod
Játra mají mimořádný význam pro farmakokinetiku i farmakodynamiku řady léčiv a jejich metabolitů. Eliminační funkce jater má značnou funkční rezervu a závisí na charakteru a stupni jaterního poškození a na vlastnostech podaného léčiva. U nemocných s jaterní cirhózou může být farmakokinetika léčiv ovlivněna biotransformační funkcí jater, krevním průtokem, vazbou na krevní bílkoviny a biliární exkrecí. Nemocní s poruchou funkce jater mohou také odlišně reagovat na terapeutické, případně toxické působení některých léčiv. Cílem přehledu je upozornit na farmakokinetické a farmakodynamické změny a na zásady úpravy dávkování léčiv u nemocných s jaterní cirhózou.
Farmakokinetika léčiv
Metabolické funkce jater se významně podílejí na celkové clearance řady léčiv. Jejich eliminace je ovlivňována několika faktory, které mohou být postiženy rozdílným způsobem.
Jaterní clearance (CLH) závisí na průtoku krve játry (QH) a extrakčním koeficientem léčiva (EH):
EH je závislý na jaterním krevním průtoku, vnitřní clearance nevázaného léčiva (CLint) a na podílu nevázaného léčiva (fu). Platí následující vztah:
CLint zahrnuje souhrnnou aktivitu biotransformačních enzymů, transportérů a exkreci látek žlučí. Podle schopnosti jater odstraňovat léčiva z cirkulace rozlišujeme látky s vysokou extrakcí (EH > 0,7) s nízkou extrakcí (EH < 0,3) nebo se střední extrakcí (0,3 < EH < 0,7). Clearance léčiv s vysokou extrakcí je převážně podmíněna krevním průtokem a je relativně nezávislá na vazbě na krevní komponenty a na aktivitě enzymů a transportérů. Snížení jaterní clearance léčiv s vysokým extrakčním koeficientem spočívá v omezení krevního proudu vedeného kolem funkčních hepatocytů. Mezi léčiva s vysokou jaterní extrakcí patří některá anodyna, propranolol, metoprolol, verapamil a lidokain. Do této skupiny se řadí také trimekain [1]. Při intrahepatálním a extrahepatálním zkratování krve se při perorálním podání podstatně zvyšuje biologická dostupnost léčiv (tab. 1) [2].
Table 1. Zvýšená biologická dostupnost při perorálním podávání léčiv s vysokou jaterní extrakcí u nemocných s jaterní cirózou. 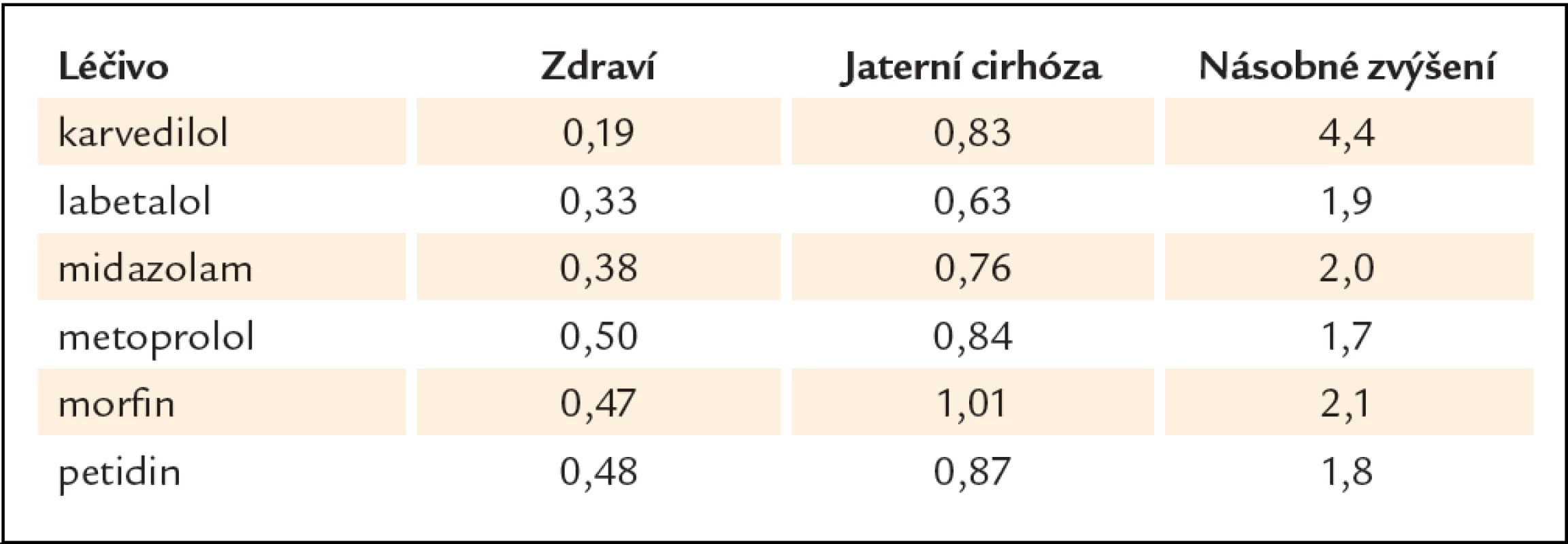
Naopak clearance léčiv s malou jaterní extrakcí je převážně ovlivněna změnou vazby na krevní bílkoviny a enzymatickou aktivitou jater. Snížená jaterní clearance byla prokázána např. u chlordiazepoxidu, diazepamu a furosemidu. Pokles metabolických funkcí u jaterní cirhózy shrnuli Doligalski et al [3]. Uplatňuje se absolutní pokles funkčních hepatocytů a snížení enzymatické aktivity. Široce používaným substrátem pro hodnocení metabolické funkce jater je kofein. Jako indikátor aktivity CYP1A2 se nám osvědčila fenotypizace tímto substrátem [4]. Reakce I. fáze biotransformace, většinou katalyzované monooxygenázovým systémem cytochromu P ‑ 450, jsou obvykle postiženy výrazněji než konjugační reakce II. fáze. Ukazuje se, že substráty CYP2C19 mohou být hůře metabolizovány již při lehké formě jaterní cirhózy, naopak snížená clearance substrátů CYP1A2, CYP2D6 a CYP2E1 se manifestuje až u dekompenzovaného onemocnění.
Farmakodynamika léčiv
V závislosti na typu léčiva bylo u nemocných s jaterní cirhózou pozorováno jak snížené, tak i zvýšené působení některých látek. Pokles účinku se projevil např. u beta‑blokátorů a diuretik.
Teoreticky lze předpokládat snížení účinku všech beta‑blokátorů, protože je prokázána významná korelace mezi sníženou jaterní funkcí a poklesem chronotropní aktivity izoprenalinu [5]. Při klinickém hodnocení jsme např. zjistili snížené bradykardizující účinky metipranololu i při vyšších koncentracích léčiva u nemocných s pokročilou jaterní cirhózou [6]. Domníváme se, že to lze vysvětlit nižší citlivostí b‑adrenoreceptorů u nemocných s jaterní cirhózou. Snížení účinku diuretik bylo pozorováno u nemocných s pokročilou cirhózou jater [7]. Ve srovnání s kontrolami je u cirhotiků nutná vyšší koncentrace furosemidu v renálních tubulech k vyloučení stejného množství sodíku.
Zvýšenou citlivost nemocných lze pozorovat při používání analgetik, anxiolytik a sedativ. Při stejné koncentraci léčiva jako u zdravých subjektů je u cirhotiků výraznější centrální tlumivé působení. Příčinou mohou být změny prostupnosti hematoencefalické bariéry a zvýšená stimulace receptorů kyseliny γ ‑ aminomáselné. Mimořádně významná nežádoucí reakce se projevuje jako renální selhání po podání nesteroidních antirevmatik, u nemocných s jaterní cirhózou provázenou ascitem.
Hodnocení jaterní funkce
Predikce osudu léčiv u nemocných s jaterní cirhózou není snadná. Současně se uplatňuje více faktorů, zejména hepatocelulární porucha a portosystémové zkratování krve. K hodnocení krevního průtoku se používaly látky s vysokou jaterní extrakcí, např. indocyaninová zeleň, galaktóza a sorbitol. Vlastní zkušenosti s posuzováním portosystémového zkratování u nemocných s jaterní cirhózou jsme získali s použitím glycerol ‑ trinitrátu [8]. K hodnocení metabolické funkce hepatocytů se používají látky, jejichž osud je málo ovlivněn krevním průtokem, např. antipyrin, kofein a midazolam. Praktické používání těchto testů komplikuje skutečnost, že jaterní extrakční koeficient není na rozdíl od ledvin konstantní a závisí na krevním průtoku. Proto není lineární vztah mezi clearance léčiva a clearance referenční látky, jakou je např. endogenní kreatinin při snížené renální funkci. Tato okolnost podstatně snižuje predikci osudu léčiv u jaterních onemocnění. Dosud nebyl prokázán význam testovacích látek pro predikci farmakokinetiky, použitelný v klinické praxi. Současné kvantitativní vyšetření nezávislého metabolického parametru může, společně s klasifikací dle Childa a Pugha (tab. 2), predikci dále zlepšit. Hypoalbuminemie je klinicky důležitým údajem bodového hodnocení. Odhaduje se, že při hodnotách albuminu > 30 g/ l je průtok krve játry snížen o 16 % a 27 % krevního proudu je zkratováno. Při poklesu albuminu < 30 g/ l lze předpokládat snížení krevního průtoku o 50 % a zkratování podléhá až 60 % krevního proudu.
Table 2. Skóre dle Childa a Pugha. 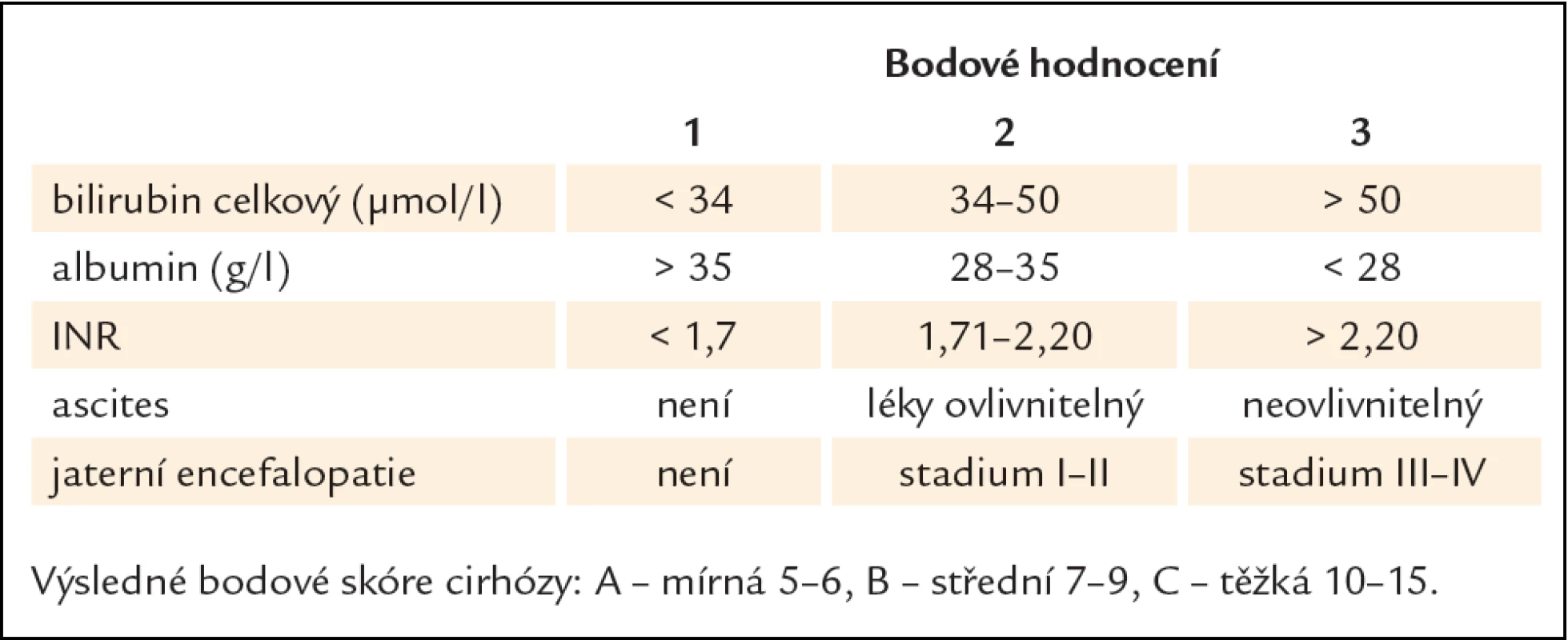
Úprava dávkování
Pro úpravu dávkování léčiv u nemocných s jaterní cirhózou platí následující obecná doporučení [2]:
- a) Léčiva s relativně vysokým jaterním extrakčním poměrem: pokud perorální podání zvyšuje biologickou dostupnost, je nutné snížit dávkování. Při poklesu jaterního průtoku se při systémové aplikaci snižuje plazmatická clearance.
- b) Léčiva s nízkou jaterní extrakcí a s vysokou vazbou na krevní bílkoviny (> 90 %): při perorálním i nitrožilním podání závisí clearance těchto léčiv na vnitřní eliminační schopnosti jater a na nevázaném podílu léčiva v krvi. Úprava dávkování je nutná i při nezměněné celkové koncentraci léčiva, protože hypoalbuminemie u pokročilé jaterní cirhózy zvyšuje volnou frakci léku.
- c) Léčiva s nízkou jaterní extrakcí a s malou vazbou na krevní bílkoviny (< 90 %): při perorálním i nitrožilním podání závisí clearance těchto léčiv na vnitřní eliminační schopnosti jater a na nevázaném podílu léčiva v krvi. Snížená funkce jater vyvolává pouze nevýznamné kolísání volného podílu a úprava dávkování může být nutná pouze při změně celkové koncentrace, která je součtem vázané i nevázané části léčiva.
- d) Léčiva zčásti eliminovaná v nezměněné formě ledvinami: eliminace těchto látek se významně zhoršuje u nemocných s hepatorenálním syndromem.
- e) Zvětšení distribučního prostoru hydrofilních léčiv u nemocných s ascitem a otoky: pokud je nutný rychlý nástup účinku, je vhodné zvýšit nárazovou dávku. Protože se hydrofilní látky eliminují renálně, je nutné respektovat eliminační funkci ledvin.
- f) Léčiva s malou terapeutickou šíří: u nemocných s pokročilou jaterní cirhózou je nutná mimořádná obezřetnost.
Tématu úpravy dávkování jednotlivých skupin léčiv u nemocných se sníženou funkcí jater se věnují samostatné přehledy, týkající se např. léčiv chronického srdečního selhání [9], antivirotik [10] a antiarytmik [11].
Závěr
U pacientů s jaterní cirhózou je při zahájení farmakoterapie nutná mimořádná opatrnost. Platí to zejména u nemocných s pokročilým stadiem onemocnění provázeným ascitem, ikterem a encefalopatií. Vždy je potřebné zvážit, zda je farmakoterapie nutná, používat malé dávky a pečlivě sledovat nemocného. Zvýšené riziko mají léčiva s malou terapeutickou šíří, sedativa, centrálně působící analgetika a anxiolytika, která mohou vyvolat jaterní encefalopatii. Zvláštní pozornost vyžadují také léčiva, jejichž hepatotoxicita je závislá na dávce, ale také látky, které působí závažné poškození jater různými na dávce nezávislými imunopatologickými mechanizmy. Některá léčiva mají vysokou pravděpodobnost hepatotoxického působení, a jsou proto u nemocných se středně těžkým až těžkým onemocněním jater relativně kontraindikována. Do této skupiny patří např. izoniazid, rifampicin, erythromycin, deoxymykoin a vysoké dávky paracetamolu.
Práce vznikla za podpory projektu PRVOUK P25/ LF1/ 2.
prof. MU Dr. František Perlík, DrSc.
http:/ / www. lf1.cuni.cz
e‑mail: fperl@lf1.cuni.cz
Doručeno do redakce: 6. 3. 2013
Sources
1. Perlík F, Haller A, Brodanová M et al. Změny farmakokinetiky trimekainu u nemocných s jaterní cirhózou. Sb Lék 1991; 93 : 287 – 292.
2. Verbeeck RK. Pharmacokinetics and dosage adjustment in patients with hepatic dysfunction. Eur J Clin Pharmacol 2008; 64 : 1147 – 1161.
3. Doligalski CT, Tong Logan A, Silverman A. Drug interactions: a primer for the gastroenterologist. Gastroenterol Hepatol (NY) 2012; 8 : 376 – 383.
4. Slanař O, Perlík F. Izoenzym cytochromu P450 – 1A2 a jeho fenotypizace. Klin Farmakol Farmac 2002; 16 : 19 – 22.
5. Ramond MJ, Comoy E, Lebrec D. Alterations in isoprenaline sensitivity in patients with cirrhosis: evidence of abnormality of the sympathetic nervous activity. Br J Clin Pharmacol 1986; 21 : 191 – 196.
6. Janku I, Perlik F, Tkaczykova H et al. Disposition kinetics and concentration-effect relationship of metipranolol in patients with cirrhosis and healthy subjects. Eur J Clin Pharmacol 1992; 42 : 337 – 340.
7. Dao MT, Villeneuve JP. Kinetics and dynamics of triamterene at steady ‑ state in patients with cirrhosis. Clin Invest Med 1988; 11 : 6 – 9.
8. Slanar O, Aubrecht J, Perlík F. Noninvasive evaluation of portal ‑ systemic shunting by glyceryl ‑ trinitrate. Physiol Res 2002; 51 : 413 – 416.
9. Sokol SI, Cheng A, Frishman WH et al. Cardiovascular drug therapy in patients with hepatic diseases and patients with congestive heart failure. J Clin Pharmacol 2000; 40 : 11 – 30.
10. McCabe SM, Ma Q, Slish JC et al. Antiretroviral therapy: pharmacokinetic considerations in patients with renal or hepatic impairment. Clin Pharmacokinet 2008; 47 : 153 – 172.
11. Klotz U. Antiarrhythmics: elimination and dosage considerations in hepatic impairment. Clin Pharmacokinet 2007; 46 : 985 – 996.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2013 Issue 7-
All articles in this issue
- Onemocnění jater u diabetiků
- Účinky GLP-1 (glucagon‑like peptide 1) na játra
- Polypózy trávicího traktu
- Vrozené hyperbilirubinemie a molekulární mechanizmy žloutenky
- Cystické nádory pankreatu – naše zkušenosti
- Wilsonova choroba
- Vliv jaterní cirhózy na farmakokinetiku a farmakodynamiku léčiv
- Katetrizace jaterních žil – vybrané aspekty hodnocení
- Reaktivace chronické hepatitidy B
- Akutní pankreatitida – novinky v léčbě
- Postižení jater u nemocných s ne-Hodgkinovým lymfomem
- Léčba chronické infekce virem hepatitidy C na začátku nové éry
- Vztah bilirubinu k nemocem vyvolaným zvýšeným oxidačním stresem
- Inhibitory tyrozinových kináz – zásadní změna v prognóze chronické myeloidní leukemie
- Mnohočetný myelom
- Pokroky v léčbě chronické lymfocytární leukemie
- Myelodysplastický syndrom – pokrok v léčbě v 21. století
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Vztah bilirubinu k nemocem vyvolaným zvýšeným oxidačním stresem
- Cystické nádory pankreatu – naše zkušenosti
- Onemocnění jater u diabetiků
- Akutní pankreatitida – novinky v léčbě
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career



