-
Medical journals
- Career
SAVOR-TIMI 53 – Saxagliptin and Cardiovascular Outcomes in Patients with Type 2 Diabetes Mellitus
Authors: J. Špinar 1; A. Šmahelová 2,3
Authors‘ workplace: Interní kardiologická klinika Lékařské fakulty MU a FN Brno, pracoviště Bohunice, a ICRC Brno, přednosta prof. MU Dr. Jindřich Špinar, CSc., FESC 1; III. interní gerontologická a metabolická klinika Lékařské fakulty UK a FN Hradec Králové, přednosta prof. MU Dr. Luboš Sobotka, CSc. 2; Subkatedra diabetologie Lékařské fakulty UK Hradec Králové, vedoucí doc. MU Dr. Alena Šmahelová, Ph. D. 3
Published in: Vnitř Lék 2013; 59(11): 1003-1007
Category: Review
Overview
Pozadí:
Léčba diabetes mellitus 2. typu je v současnosti účinná, ale bohužel ještě není ideální. Jistému ideálu se již blíží terapie založená na inkretinech, která je významným kvalitativním pokrokem. První ukončenou mortalitní studií s inhibitory dipeptidyl peptidázy (DPP 4) je studie SAVOR prezentovaná v Amsterdamu na Evropském kardiologickém kongresu v roce 2013.Metodika:
SAVOR (Saxagliptin and Cardiovascular Outcomes in Patients with Type 2 Diabetes Mellitus) randomizovala 16 492 nemocných s diabetes mellitus 2. typu a vysokým rizikem kardiovaskulárních příhod léčených běžnou léčbou perorálními antidiabetiky a navíc na léčbu saxagliptinem či placebem. Na léčbu saxagliptinem bylo randomizováno 8 280, na léčbu placebem 8 212 nemocných. Průměrná doba sledování byla 2,1 roku.Výsledky:
Primární cíl (kardiovaskulární úmrtí, nefatální infarkt myokardu a nefatální CMP) se vyskytl u 7,3 % (613) nemocných léčených saxagliptinem a u 7,2 % (609) nemocných léčených placebem (HR 1,00, p < 0,001 pro non inferioritu). Hlavní sekundární cíl (kardiovaskulární úmrtí, infarkt myokardu, cévní mozková příhoda, hospitalizace pro srdeční selhání či anginu pectoris a revaskularizace myokardu) byl u 12,8 % (1 059) nemocných léčených saxagliptinem a u 12,4 % (1 034) nemocných léčených placebem. Počet hospitalizací pro srdeční selhání byl 289 (3,5 %) ve větvi se saxagliptinem a 228 (2,8 %) ve větvi s placebem (p = 0,007).Závěr:
DPP ‑ 4 inhibitor saxagliptin nezvýšil výskyt ischemických kardiovaskulárních příhod, měl ale trend ke zvýšení hospitalizací pro srdeční selhání u pacientů s již přítomným srdečním selháním. Nezvyšoval výskyt pankreatitidy. Současně signifikantně zlepšoval kontrolu diabetes mellitus, což by mohlo být signálem na budoucí zlepšení kardiovaskulárních cílů.Klíčová slova:
diabetes mellitus – DPP ‑ 4 inhibitory – saxagliptin – mortalita – srdeční selháníÚvod
Diabetes mellitus 2. typu je progresivně se zhoršující onemocnění. Důsledkem snížení schopnosti adekvátní sekrece inzulinu je zhoršující se kompenzace diabetu, která vyžaduje intenzivnější (nebo extenzivnější) terapii. Podle současných názorů je cílem terapie hyperglykemie dosažení tzv. těsné kompenzace – hodnot glykemie shodných jako u zdravého člověka nebo jim blízkých, a to bez nebezpečí hypoglykemie. Základním ukazatelem úspěšnosti terapie je pak glykovaný hemoglobin (HbA1c) a současně nepřítomnost nežádoucích účinků terapie. Nejzávažnějším nežádoucím účinkem léčby se u pacientů s diabetem 2. typu ukázala být hypoglykemie. Proto je v terapii diabetu 2. typu v současnosti kladen důraz na zavádění nových farmak, pro něž je kromě dostatečné účinnosti charakteristické snížené riziko hypoglykemie. Mezi typické představitele bezpečné terapie patří i DPP ‑ 4 inhibitory.
Léčba diabetes mellitus 2. typu je v současnosti účinná, ale bohužel ještě není ideální. Jistému ideálu se již blíží terapie založená na inkretinech, která je významným kvalitativním pokrokem. U této léčby jsou s nadějí očekávány výsledky dlouhodobých studií, které zhodnotí její vliv na kardiovaskulární riziko. Pokud se naplní všechny předpoklady a gliptiny (inhibitory DPP ‑ 4) i agonisté receptoru pro GLP‑1 sníží riziko srdečně‑cévních onemocnění, dostane se jistě tato léčba v algoritmech na jedno z prvních míst v léčbě diabetes mellitus 2. typu.
Jako inkretinové hormony, mezi něž v současné době řadíme GLP‑1 (glukagon‑like peptide 1) a GIP (gastric inhibitory polypeptide), jsou označovány látky polypeptidické povahy. Tyto látky jsou u zdravých osob produkovány specifickými enteroendokrinními buňkami tenkého střeva. Po svém uvolnění do krevního oběhu spouští přes aktivaci příslušných receptorů kaskádu dějů, které ve svém důsledku vedou ke zvýšení produkce inzulinu B buňkami pankreatu a zároveň tlumí produkci glukagonu v jeho A buňkách. GLP‑1 zvyšuje sekreci inzulinu v závislosti na zvýšení glykemie, tedy při příjmu potravy.
Oba inkretinové hormony, tedy GLP‑1 i GIP, jsou v krevním oběhu během několika málo minut odbourávány enzymem dipeptidyl peptidázou 4 (DPP 4). Mechanizmus účinku gliptinů spočívá v inhibici enzymu dipeptidyl peptidázy 4. V dnešní době máme v klinické praxi k dispozici 4 gliptiny – saxagliptin (Onglyza), sitagliptin (Januvia), vildagliptin (Galvus) a linagliptin (Trajenta).
Saxagliptin snižuje glykovaný hemoglobin (HbA1c) až o 1 %. Výskyt hypoglykemií a ovlivnění tělesné hmotnosti je při léčbě saxagliptinem minimální. V roce 2009 schválily použití tohoto léku European Medicines Agency (EMEA) v Evropě a Food and Drug Administration (FDA) ve Spojených státech amerických.
Studie SAVOR
Na Evropském kardiologickém kongresu v Amsterodamu 31. 8. 2013 až 3. 9. 2013 byly v sekci HOT lines prezentovány výsledky studie SAVOR (Saxagliptin Assessment of Vascular Outcomes Recorded in patients with Type 2 Diabetes Mellitus – Thrombolysis in Myocardial Infarction – SAVOR ‑ TIMI 53 Study) [1–3].
SAVOR ‑ TIMI 53 byla multicentrická, randomizovaná, dvojitě slepá, placebem kontrolovaná studie fáze IV s cílem ukázat, zda saxagliptin může ovlivnit smíšený hlavní cíl: snížení kardiovaskulárních úmrtí, nefatálních infarktů myokardu a nefatálních cévních mozkových příhod. Plánováno bylo zařadit 16 500 diabetiků 2. typu s jakýmkoli typem antidiabetické léčby kromě inkretinových léků randomizovaných navíc 1 : 1 k léčbě saxagliptinem či placebem a předpokládaná doba trvání studie byla 5 let. Studie byla zahájena v květnu roku 2010 a zúčastnilo se jí 788 center, 26 zemí z 6 kontinentů, včetně ČR. Vstupním kritériem byl diabetes mellitus 2. typu a všechny následující body:
- věk > 40 let,
- HbA1c 6,5 – 12 % (DCCT) (v posledních 6 měsících),
- vysoké riziko kardiovaskulární příhody charakterizované buď jako anamnéza kardiovaskulárního onemocnění, nebo kumulace rizikových faktorů.
Randomizováno bylo nakonec 16 492 nemocných, průměrný věk 65 ± 8,6 roku, průměrná doba trvání diabetu 11,9 ± 8,9 roku. Všichni pacienti v obou větvích studie užívali běžnou antidiabetickou terapii. Průměrný krevní tlak 137,3 ± 17,3/ 78,7 ± 10,4 mm Hg, průměrný HbA1c na začátku studie 8,0 ± 1,4 % (DCCT), 81,4 % nemocných mělo hypertenzi, 70,8 % dyslipidemii, 13,4 % kouřilo v době zařazení, 37,8 % bylo po infarktu myokardu, 26,7 % bylo po angioplastice koronárních tepen, 23,8 % po bypassové operaci, 78,3 % užívalo statiny, 81,3 % antiagreagaci, 53,8 % ACE inhibitory, 27,6 % sartany a 61,2 % beta‑blokátory. Studie byla ukončena po dosažení plánovaného počtu konečných cílů.
Základní charakteristiku pacientů ukazuje tab. 1.
Table 1. Vstupní charakteristika ve studii SAVOR. 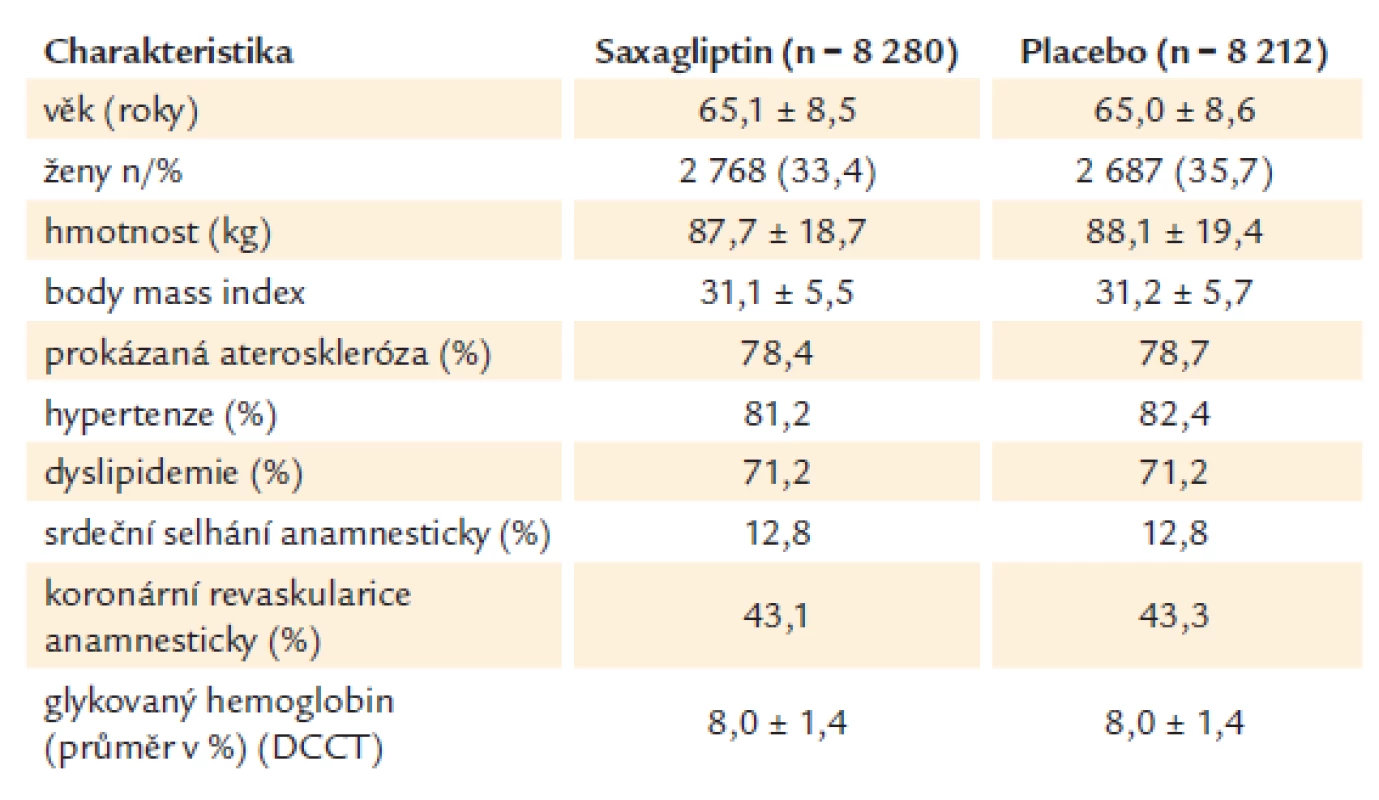
Průměrná doba sledování byla 2,1 roku a primární cíl (kardiovaskulární úmrtí, nefatální infarkt myokardu a nefatální CMP) se vyskytl u 7,3 % (613) nemocných léčených saxagliptinem a u 7,2 % (609) nemocných léčených placebem (HR 1,00, p < 0,001 pro non inferioritu) (graf 1). Hlavní sekundární cíl (kardiovaskulární úmrtí, infarkt myokardu, cévní mozková příhoda, hospitalizace pro srdeční selhání či angina pectoris a revaskularizace myokardu) byla u 12,8 % (1 059) nemocných léčených saxagliptinem a u 12,4 % (1 034) nemocných léčených placebem (graf 2, tab. 2).
Graph 1. Primární cíl ve studii SAVOR-TIMI-53 – KV mortalita, infarkt myokardu, ischemická cévní mozková příhoda. 
Graph 2. Sekundární cíl ve studii SAVOR-TIMI-53 – primární cíl + hospitalizace pro srdeční selhání, nestabilní anginu pectoris a revaskularizace myokardu. 
Table 2. Sekundární cíle ve studii SAVOR. 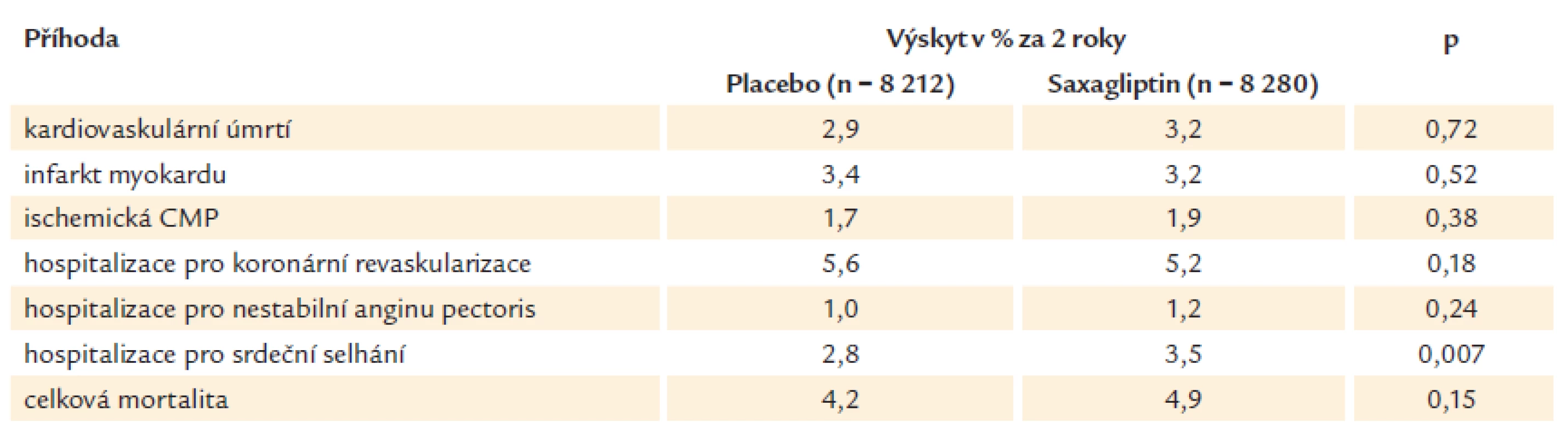
Z pohledu léčby diabetes mellitus dosáhlo 36,2 % nemocných glykovaného hemoglobinu méně než 7 % ve skupině léčené saxagliptinem, ale pouze 27,9 % ve skupině léčené placebem (p < 0,001). Na druhé straně 15,3 % nemocných léčených saxagliptinem mělo epizodu hypoglykemie, na rozdíl od 13,4 % léčených placebem (p < 0,001). Celkem 3,5 % nemocných léčených saxagliptinem mělo hospitalizaci pro srdeční selhání, ve srovnání s 2,8 % léčenými placebem (p = 0,007). Týkalo se to především nemocných s vyšším BNP (brain natriuretic peptid) již na začátku studie.
Výskyt pankreatitidy i nádorů pankreatu byl stejný v obou skupinách. Podávání saxagliptinu je tedy bezpečné.
Výsledky glykovaného hemoglobinu v průběhu studie ukazuje tab. 3.
Table 3. Kontrola HbA<sub>1c</sub> v průběhu studie. 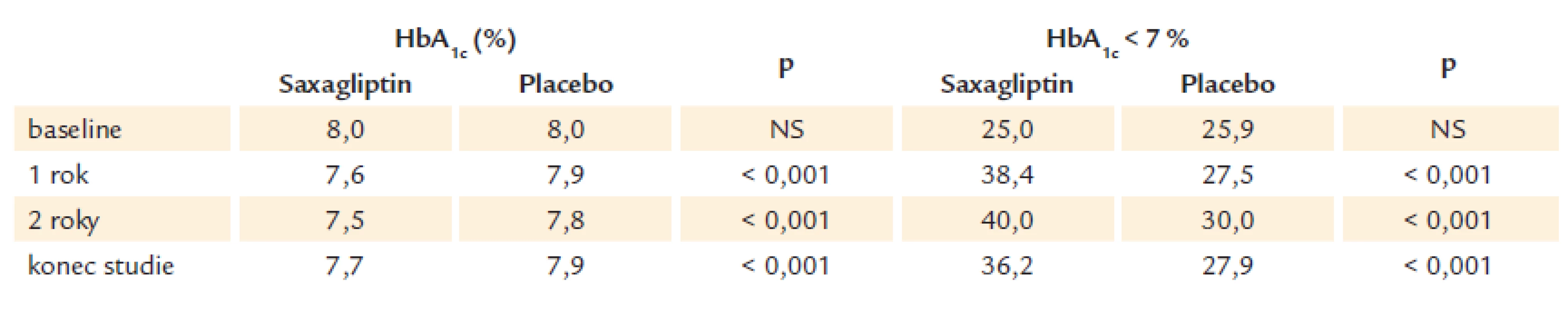
Pozitivní trend byl pozorován v ovlivnění mikroalbuminurie, která se po saxagliptinu zhoršila ve 13 % a po placebu v 16 %. Naopak zlepšení po saxagliptinu bylo pozorováno v 11 % a po placebu jen v 9 % (p < 0,001) (graf 3). Výskyt hypoglykemie byl vyšší po saxagliptinu (15,3 % vs 13,4 %, p < 0,001), jednalo se ale o lehké hypoglykemie. Výskyt významných hypoglykemií nebyl statisticky významný mezi oběma skupinami (2,1 % vs 1,7 %; p = 0,47) podobně jako výskyt hypoglykemií vyžadujících hospitalizaci (0,6 % vs 0,5 %; p = 0,33).
Graph 3. Ovlivnění mikroalbuminurie. 
Diskuze
V této randomizované, placebem kontrolované klinické studii DPP ‑ 4 inhibitor saxagliptin nezvýšil ani nesnížil riziko primárního cíle – kardiovaskulární úmrtí, infarkt myokardu, cévní mozková příhoda, když byl přidán ke standardní terapii nemocných s diabetes mellitus 2. typu a vysokým kardiovaskulárním rizikem a tím splnil kritéria pro noninferioritu. K tomuto neutrálnímu výsledku je třeba doplnit, že saxagliptin:
- zlepšil kontrolu glykemie,
- snížil potřebu inzulinu a dalších perorálních antidiabetik,
- zvýšil sice výskyt hypoglykemií, ale ne hypoglykemií závažných či vyžadujících hospitalizaci; navíc pouze při současném podávání saxagliptinu a derivátů sulfonylurei nebo inzulinu,
- snížil progresi mikroalbuminurie,
- nezvýšil riziko pankreatitidy či rakoviny pankreatu.
Studie SAVOR ukázala jasně na velkou potřebu provést velké klinické studie s léky na diabetes mellitus zaměřenou na kardiovaskulární cíle. Je třeba i co nejpřesněji popsat souvislost mezi kontrolou HbA1c a kardiovaskulárními příhodami. V současné době jsou uzavírány nebo probíhá řada kardiovaskulárních mortalitních studií s dalšími inkretinovými léky.
Autoři na závěr rozebírají několik otázek, proč studie SAVOR skončila s tímto neutrálním efektem:
- studie trvala relativně krátce, efekt na makrovaskulární komplikace nelze z dlouhodobého hlediska jednoznačně hodnotit. Studie UKPDS potřebovala 10 let na průkaz, že lepší kontrola glykemie snižuje riziko infarktů myokardu,
- efekt na zvýšení hospitalizací pro srdeční selhání byl překvapující a nemá zatím vysvětlení. Zvýšený výskyt těchto hospitalizací se ale vyskytoval u pacientů, kteří již se srdečním selháním vstupovali do studie,
- snížení glykovaného hemoglobinu bylo statisticky významné a pozitivní,
- je třeba připomenout, že ani některé jiné klinické studie s jiným typem perorálních antidiabetik, jako ADVANCE či PROACTIVE, přes pokles HbA1c neprokázaly pokles makrovaskulárních příhod,
- velké procento nemocných ve studii SAVOR užívalo antiagregační léčbu, statiny či antihypertenziva. Je pak otázkou, zda další lékové skupiny mohou ještě výrazně zlepšit prognózu těchto nemocných, či zda se máme zaměřit na sekundární cíle, např. mikroalbuminurii, renální selhání, slepotu atd.
- lepší kontrola diabetes mellitus snižuje především mikrovaskulární komplikace – tyto výsledky ze studie SAVOR nebyly zatím prezentovány. Pozitivní je příznivé ovlivnění mikroalbuminurie,
- ve studii SAVOR nebyl statisticky významně vyšší výskyt pankreatitidy a nádorů pankreatu.
Ve stejný den byly na ESC 2013 sděleny výsledky studie EXAMINE u pacientů s diabetes mellitus po akutním infarktu myokardu randomizovaných k alogliptinu či placebu. Studie randomizovala 5 380 nemocných, z toho 2 701 na alogliptin a 2 679 na placebo. Průměrná doba sledování byla 18 měsíců a smíšený primární cíl (úmrtí, nefatální infarkt myokardu a nefatální CMP) se vyskytl u 11,3 % (305) nemocných léčených alogliptinem a u 11,8 % (316) na placebu (HR 0,96, p < 0,001 pro non inferioritu). Pokles glykovaného hemoglobinu po alogliptinu byl nižší o 0,33 %, po placebu vyšší o 0,03 %. Výskyt hypoglykemií či pankreatitidy se nelišil mezi oběma skupinami.
V současné době probíhají minimálně 2 další velké mortalitní studie s DPP ‑ 4 inhibitory. Je to studie CAROLINA s linagliptinem, která randomizovala 6 000 nemocných s diabetes mellitus 2. typu a vysokým kardiovaskulárním rizikem, a studie TECOS se sitagliptinem, která randomizovala 14 000 nemocných s diabetes mellitus a prokázaným kardiovaskulárním onemocněním.
Výzkum v této oblasti pokračuje a teprve budoucnost ukáže jasné zařazení inhibitorů dipeptidyl peptidáz 4 v léčbě diabetes mellitus a prevenci mikrovaskulárních i makrovaskulárních komplikací.
prof. MU Dr. Jindřich Špinar, CSc., FESC
www.fnbrno.cz
e‑mail: jspinar@fnbrno.cz
Doručeno do redakce: 17. 9. 2013
Přijato po recenzi: 26. 9. 2013
Sources
1. Scirica BM, Bhatt DL, Braunwald E et al. The design and rationale of the Saxagliptin Assessment of Vascular Outcomes Recorded in patients with diabetes mellitus – Thrombolysis in Myocardial Infarction (SAVOR ‑ TIMI) 53 Study. Am Heart J 2011; 162 : 818 – 825.
2. Mosenzon O, Raz I, Scirica BM et al. Baseline characteristics of patients population in the Saxagliptin Assessment of Vascular Outcomes Records in patients with diabetes mellitus (SAVOR ‑ TIMI) 53 Trial. Diabetes Metab Res Rev 2013; 29 : 417 – 426.
3. Scirica BM, Bhatt DL, Braunwald E. SAVOR ‑ TIMI 53 Steering Committee and Investigators. Saxagliptin and Cardiovascular Outcomes in Patients with Type 2 Diabetes Mellitus. N Engl J Med 2013; 1317 – 1326.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2013 Issue 11-
All articles in this issue
- Prevalencia diabetickej retinopatie, distálnej symetrickej diabetickej polyneuropatie a screening glomerulárnej filtrácie v čase diagnózy diabetes mellitus 2. typu – kohortná štúdia
- Léčba těžké sepse na pracovištích intenzivní péče v České republice – pilotní výsledky projektu EPOSS
- Nový krevní test biomarkeru SEPT9 a screening kolorektálního karcinomu
- Možnosti genetickej diagnostiky nádorových a zápalových ochorení čriev na Slovensku
- SAVOR-TIMI 53 – Saxagliptin and Cardiovascular Outcomes in Patients with Type 2 Diabetes Mellitus
- Manažment povrchovej tromboflebitídy. Odporúčania Angiologickej sekcie Slovenskej lekárskej komory (2013)
- Význam hodnotenia EKG v diagnostike pľúcnej embólie
- Atypická fraktura metatarzální kosti u pacienta s mnohočetným myelomem, který byl dlouhodobě léčen bisfosfonáty
- Zánětlivá reakce a význam C‑ reaktivního proteinu u pacientů s akutním koronárním syndromem
- Tyreostatická liečba a jej nežiadúce účinky
- Úloha kardiálnych biomarkerov v monitorovaní kardiotoxicity po transplantácii kmeňových krvotvorných buniek
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Tyreostatická liečba a jej nežiadúce účinky
- Zánětlivá reakce a význam C‑ reaktivního proteinu u pacientů s akutním koronárním syndromem
- Význam hodnotenia EKG v diagnostike pľúcnej embólie
- Manažment povrchovej tromboflebitídy. Odporúčania Angiologickej sekcie Slovenskej lekárskej komory (2013)
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

