-
Medical journals
- Career
Atypická fraktura metatarzální kosti u pacienta s mnohočetným myelomem, který byl dlouhodobě léčen bisfosfonáty
Authors: Z. Adam 1; A. Šprláková‑ puková 2; R. Chaloupka 3; M. Krejčí 1; L. Pour 1; Z. Král 1; J. Mayer 1
Authors‘ workplace: Interní hematologická a onkologická klinika Lékařské fakulty MU a FN Brno, pracoviště Bohunice, přednosta prof. MU Dr. Jiří Mayer, CSc. 1; Radiologická klinika Lékařské fakulty MU a FN Brno, pracoviště Bohunice, přednosta prof. MU Dr. Vlastimil A. Válek, CSc., MBA 2; Ortopedická klinika Lékařské fakulty MU a FN Brno, pracoviště Bohunice, přednosta doc. MU Dr. Martin Repko, Ph. D. 3
Published in: Vnitř Lék 2013; 59(11): 1022-1026
Category: Case Report
Overview
První zprávy o léčebném použití jednoduchých bisfosfonátů, které jsme našli v odborné literatuře, začínají rokem 1972. První zprávu o použití bisfosfonátu obsahujícího ve své molekule dusík, jsme našli v publikaci z roku 1990. Některé z nežádoucích účinků jednotlivých typů bisfosfonátů byly popsány v registračních studiích. Nicméně 2 závažné nežádoucí účinky této skupiny léků byly popsány až po roce 2000. První popis osteonekrózy čelisti v souvislosti s dlouhodobou aplikací bisfosfonátů jsme našli v publikaci z roku 2002 a první popis atypické fraktury kosti, která vznikla bez odpovídajícího traumatického děje, v místě, kde nebylo přítomno žádné osteolytické ložisko, jsme našli v článku z roku 2006. Tyto tzv. atypické zlomeniny, zvané též zlomeniny bez odpovídajícího traumatického děje (low energy fractures), jsou popsány ve femurech, v pánvi a výjimečně též v metatarzu. „Atypické zlomeniny“ se dávající do souvislosti s dlouhodobým podáváním bisfosfonátů, které sice signifikantně zvyšují denzitu kosti a brzdí osteolýzu, ale také zvyšují křehkost kosti a snižují její pružnost. V definici atypické zlomeniny skeletu je zdůrazněna skutečnost, že vznikají působením neadekvátně malé síly (energie), ve výše uvedených predilekčních lokalizacích. V textu přinášíme obraz a popis pacienta léčeného pro mnohočetný myelom, s atypickou zlomeninou II. metatarzu. Tato zlomenina vznikla při běžné chůzi, bez jakékoli nadměrné zátěže, bez toho, že by si pacient mohl vzpomenout na odpovídající úraz či na delší chůzi. Pacient dostával bisfosfonáty před vznikem atypické zlomeniny metatarzu po dobu 34 měsíců. Zlomenina metatarzální kosti byla léčena odlehčením chodidla a do měsíce bolesti vymizely. Při srovnání s publikovanými údaji o atypických frakturách jde v našem případě o krátký interval od zahájení podávání bisfosfonátu do vzniku atypické fraktury. V dostupné literatuře jsou tyto fraktury popisovány po více než 5 letech aplikace bisfosfonátu. Nové bolesti v nosném skeletu u pacientů léčených bisfosfonáty jsou proto vždy důvodem k zobrazovacímu vyšetření a mimo jiné k vyloučení atypické fraktury vlivem zvýšené křehkosti kosti.
Klíčová slova:
bisfosfonát – atypická fraktura (low energy fracture) – klodronát – pamidronát – zoledronát – lenalidomid – osteoporóza – monoklonální imunoglobulinÚvod
Každý lék prochází standardní fází klinického testování a v rámci tohoto testování jsou popsány běžné nežádoucí účinky. Na příkladu bisfosfonátů je možné demonstrovat obecné pravidlo, že některé nežádoucí účinky nových léků nemusejí být rozpoznány v době registračních studií a že záleží na pozornosti a vnímavosti lékařů, zda jsou schopni si všimnout určité odchylky, která není běžná a která se ani v učebnicích zatím nepopisovala. První závažný nežádoucí účinek bisfosfonátů, který nebyl popsán v rámci registračních studií a dlouho zůstal nepovšimnut, byla osteonekróza čelisti. O několik let později byl v literatuře popsán další velmi vzácný, ale závažný nežádoucí účinek – atypické fraktury při dlouhodobém užívání bisfosfonátů.
Bisfosfonáty brzdí odbourávání hydroxyapatitu, zvyšují kostní hustotu (denzitu), ale současně brzdí také vlastní přestavbu kosti. To vede ke zmenšování pružnosti a k narůstání křehkosti kostí. U křehké kosti malá energie způsobí frakturu, zatímco u kosti s fyziologickou pružností působením stejné energie fraktura nevznikne.
Zahraniční literatura popisuje „atypické zlomeniny“ neboli též fraktury způsobené malou silou (low energy fractures) u pacientů dlouho léčených bisfosfonáty. Jejich incidence či prevalence zatím není přesně stanovena.
Příznaky mnohočetného myelomu zůstávají po staletí stejné, zatímco výsledky léčby se postupně zlepšují [1]. Přibývají nové léky a s nimi i nové komplikace, o nichž je nutné vědět.
Cílem následujícího textu je dokumentovat fakt, že atypická fraktura metatarzální kosti bez odpovídajícího traumatického děje vznikla u našeho pacienta již po necelých 3 letech podávání bisfosfonátu, a v diskuzi upozornit na tento zatím méně známý nežádoucí účinek bisfosfonátů.
Popis případu
Muž, narozený roku 1959, šel dle doporučení v roce 2009 po svých 50. narozeninách na preventivní vyšetření, i když se cítil být zcela zdráv. Preventivní vyšetření odhalilo vysokou sedimentaci a tedy nutnost dalšího vyšetřování. Později, v květnu roku 2010, byla odhalena příčina této vysoké sedimentace, mnohočetný myelom typu IgG κ, klinického stadia IIIA dle Durieho a Salomona. Pacient měl mnohočetná, do té doby asymptomatická osteolytická ložiska a měření kostní hustoty prokázalo osteopenii s denzitometricky naměřenou hustotou kosti – 1,6 SD.
Léčba byla zahájena v květnu roku 2010 perorální léčbou lenalidomidem + dexametazonem v rámci klinické studie. Mnohočetná osteolytická ložiska byla důvodem, aby ihned po stanovení diagnózy byla zahájena léčba klodronátem, doplněná suplementací vitaminu D a vápníku (preparát Caltrate). V listopadu roku 2010, po 4 cyklech (měsících) lenalidomidu a dexametazonu, byl proveden sběr kmenových krvetvorných buněk. Po sběru nenásledovala ihned vysokodávkovaná chemoterapie, ale pacient dále dostával chemoterapii s lenalidomidem, dexametazonem a cyklofosfamidem. Celkem dostal 6 cyklů (měsíců) této trojkombinace. Při této léčbě (lenalidomid, cyklofosfamid a dexametazon) se dostal do kompletní remise. Od září roku 2011 byla zahájena udržovací léčba, lenalidomid 10 mg denně po dobu 21 dnů v měsíčních intervalech, a byla podávána jeden rok, až do září roku 2012, kdy byla pro progresi nemoci ukončena. Po zjištění progrese se léčba změnila na trojkombinaci obsahující cyklofosfamid, bortezomib a dexametazon a pacient byl směřován k vysokodávkované chemoterapii.
V únoru roku 2012 si začal stěžovat na bolest v levém chodidle, v oblasti metatarzu (v nártu). Bolesti nepředcházela žádná zvýšená námaha, ani delší chůze, ani úraz. RTG snímek odhalil šikmou (víceúlomkovou) frakturu II. metatarzu s diskrétním zkrácením, lomné linie byly dobře zřetelné, byly bez známek přemostění, tedy čerstvého data. Zesílení kortikalis a nehomogenní struktura diafýzy IV. metatarzu, bez přesvědčivé lomné linie lze interpretovat jako možné posttraumatické změny staršího data. Jinak zobrazení metatarzální kostí bylo bez ložiskových projasnění, typických pro mnohočetný myelom. Osteolytická ložiska, typická pro myelom, jsou patrná na diafýze tibie vlevo (obr. 1).
Image 1. RTG snímek odhalil šikmou (víceúlomkovou) frakturu II. metatarzu s diskrétním zkrácením, lomná linie je dobře zřetelná, tč. bez známek přemostění, tedy čerstvého data. Zesílení kortikalis a nehomogenní struktura diafýz IV. metatarzu, bez přesvědčivé lomné linie – možné potraumatické změny staršího data. Jinak zobrazení kosti bez ložiskových projasnění, typického pro mnohočetný myelom. Osteolytické změny typické pro myelom jsou patrné na diafýze tibie vlevo. 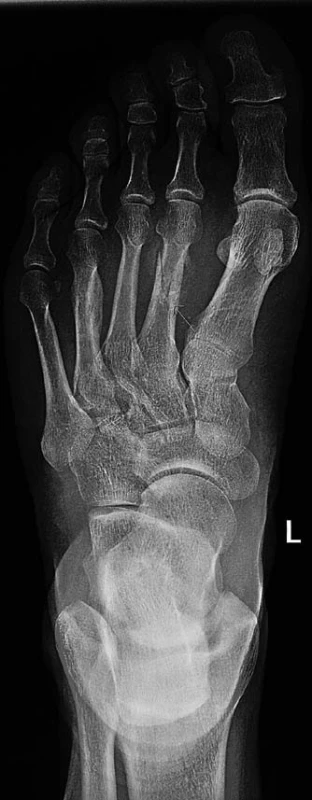
Diagnóza atypické fraktury metatarzální kosti, tedy fraktury, které nepředcházel úrazový děj, byla stanovena po necelých 3 letech podávání bisfosfonátů ve formě perorálních tablet klodronatu, tedy po 34 měsících. Pacientovi bylo doporučeno odlehčit nohu s pomocí berlí. Bolestivost nártu po měsíci vymizela.
V dubnu roku 2013 následovala vysokodávkovaná chemoterapie s autologní transplantací krvetvorných buněk, po níž dlouhodoběji přetrvávala nechuť k jídlu. Oba důvody, hojící se fraktura a nechuť k jídlu, vedly k dočasnému vysazení klodronatu. Další aplikace bisfosfonátů se pak bude odvíjet od míry aktivity mnohočetného myelomu. Pokud bude zřetelná osteolytická aktivita mnohočetného myelomu, budeme muset zvážit, co bude menší zlo, zda nepodat či podat bisfosfonát s vědomím rizika atypických kostních fraktur.
Při RTG kontrole v červnu roku 2013 byl popsán již hypertrofický svalek II. metatarzu, lomná linie byla již téměř nečitelná. Zřetelný byl svalek po staré fraktuře IV. metatarzu. Tyto změny byly hodnoceny jako pokročilé hojení fraktury II. metatarzu. Vzhledem k tomu, že po vysokodávkované chemoterapii aktivita nemoci výrazně poklesla, i když pacient není v kompletní remisi, zatím zůstává podávání bisfosfonátů přerušeno.
Diskuze
Mnohočetný myelom je choroba charakteristická tvorbou četných osteolytických ložisek, která se vyskytují u 80 – 90 % nemocných s touto diagnózou. Dalším charakteristickým znakem mnohočetného myelomu je osteoporóza. Ložisková osteolýza a osteoporóza je důsledkem působení určitých cytokinů, které produkují myelomové buňky. Další četné a pestré příznaky mnohočetného myelomu způsobuje monoklonální imunoglobulin, produkovaný patologickými plazmatickými buňkami, což popisují četné publikace, které se zabývají různými aspekty mnohočetného myelomu [2 – 10].
Bisfosfonáty jsou používány s cílem inhibovat patologicky zvýšenou osteolýzu, způsobenou mnohočetným myelomem či kostními metastázami anebo při osteoporóze jakékoli etiologie. Bisfosfonáty jsou v klinické praxi již od počátku 70. let minulého století. První klinické publikace z let 1972 – 1976 popisují jejich použití u osteoporózy a dále u Pagetovy choroby. V obou těchto indikacích jsou stále používány [11 – 14].
U mnohočetného myelomu se bisfosfonáty začaly používat o pár let později. První publikace popisující použití bezdusíkatých bisfosfonátů u mnohočetného myelomu vyšly v roce 1980, tedy před 33 lety, a první popis použití pamidronatu, tedy dusík obsahujícího bisfosfonátu u mnohočetného myelomu, je z roku 1990. Takže bisfosfonáty, které ve své molekule obsahují atom dusíku, se používají již nejméně 23 let [15 – 23].
V mnoha klinických studiích bylo u pacientů s mnohočetným myelomem potvrzeno, že bisfosfonáty zpomalují patologickou osteolýzu, snižují počet nových kostních komplikací, snižují počet hyperkalcemických epizod a zmenšují spotřebu analgetik [24]. Ve více studiích bylo potvrzeno zvyšování kostní hustoty při léčbě bisfosfonáty [25].
Lze říci, že koncem 90. let minulého století jsme bisfosfonáty považovali za excelentní léky bez závažných nežádoucích účinků, které bylo možné dlouhodobě podávat jak v případě osteolýzy způsobené metastázami solidních nádorů, tak u osteolýzy způsobené maligními krevními chorobami. To odrážejí četné české a slovenské publikace na toto téma [26 – 31].
Tomu odpovídala i starší doporučení pro aplikaci bisfosfonátů u mnohočetného myelomu – podávat je od stanovení diagnózy až do konce života pacienta s mnohočetným myelomem.
Jenže v životě nic není tak krásné, jak se nám zpočátku zdá. A naopak i na věcech zpočátku jasně negativních se často podaří najít zárodek něčeho pozitivního. Abychom to však zjistili, musíme být dostatečně pozorní a vnímaví.
Tak tomu bylo i s bisfosfonáty. První komplikací, o níž se dlouho nevědělo a která se nezjistila v době registračních studií, byla osteonekróza čelisti. Až v roce 2002 popsal stomatochirurg Rugiero skupinku nemocných, kteří měli zánětlivé onemocnění čelisti, které se nehojilo. Díky tomu, že nepodceňoval důležitost anamnézy, si všiml, že jeho pacienti s nehojícími se defekty v čelisti dlouhodobě užívali bisfosfonáty. Toto své pozorování zveřejnil [32,33]. O něco později byl i v ČR popsán první pacient s touto komplikací [34,35].
Následně došlo k explozivnímu nárůstu počtu publikací v celém světě o osteonekróze v průběhu léčby bisfosfonáty. V literární databázi Medline ‑ Pubmed bylo k datu 24. 4. 2013 celkem 978 publikací o osteonekróze čelisti při léčbě bisfosfonáty.
První publikace, popisující zvýšenou křehkost kosti u pacientů léčených bisfosfonáty, se objevila až v roce 2006. Autoři popsali tzv. „atypické fraktury“, které vznikají bez odpovídajícího traumatického děje (low energy fractures) v místech, kde nejsou žádná patologická osteolytická ložiska. První popisy této vzácné komplikace se objevují více než po 20 letech podávání těchto léků. Dnes lze najít již poměrně hodně publikací, které se tomuto problému věnují [36 – 51]. Při zadání hesla „atypical fracture and bisphosphonate“ do literární databáze Medline Pubmed jsme v Medline 24. 4. 2013 nalezli 193 publikací.
Bisfosfonáty inhibují nejen patologickou osteolýzu, a tak zmenšují počet kostních komplikací a zvyšují denzitu kosti, ale také blokují fyziologickou přestavbu kosti, což vede ke ztrátě pružnosti a zvýšené křehkosti. Nejčastěji jsou popisovány atypické subtrochanterické fraktury femuru a fraktury pánve. Fraktury metatarzálních kostí jsou popisovány méně často, první popis je z roku 2006 [52].
Když jsme hledali v literární databázi Medline ‑ Pubmed, kdy byly atypické fraktury v důsledku bisfosfonátů popsány u pacientů s mnohočetným myelomem, první popisy jsme objevili až v letech 2008 a 2009. Popisují spontánní fraktury femuru u pacientů s mnohočetným myelomem, jeden dostával bisfosfonáty po dobu 9 let a druhý po dobu 11 let [53,54].
Největší soubor pacientů s atypickými frakturami metatarzálních kostí popsali autoři z Kalifornie. Popisují osud 6 pacientů s mnohočetným myelomem, kteří mimo jiné byli léčeni také bisfosfonáty obsahujícími dusík. K fraktuře metatarzálních kostí u těchto 6 pacientů došlo nejdříve po 5,5 roku podávání bisfosfonátů, medián intervalu podávání bisfosfonátů do vzniku první fraktury uvádějí 7,55 roku. Uvedených 6 pacientů patřilo do skupiny 300 pacientů, sledovaných v kalifornském centru. Z tohoto souboru pouze 49 pacientů dostávalo bisfosfonáty při mnohočetném myelomu déle než 5,5 roku. Takže metatarzální fraktury se objevily u 12 % pacientů, kteří dostávali bisfosfonáty déle než 5,5 roku. Autoři z toho soudí, že tento typ fraktur po 5 letech nitrožilní aplikace bisfosfonátů nemůže být nijak vzácný [55].
Fraktury metatarzálních kostí byly dříve popisovány u zdravých osob, např. u vojáků po dlouhých pochodech se zátěží, jako tzv. únavové fraktury. Nyní je můžeme vidět u osob užívajících dlouhodobě bisfosfonáty i bez zvýšené fyzické námahy [56].
Spontánní fraktury či fraktury bez odpovídající traumatizující síly (low energy fractures) byly u pacientů s mnohočetným myelomem popsány po roce 2010 i v dalších lokalizacích [57,58].
Otázkou je, co s nimi. V případě metatarzálních fraktur se doporučuje fyzické šetření chodidla. Ortopedové doporučují funkční léčbu dle klinického nálezu. Při menším otoku a bolestivosti chůze o berlích s odlehčením, bandáže. Při větších potížích a otoku sádrová dlaha, nechodit 3 týdny a pak kontrola.
Mají se vysadit bisfosfonáty či nemají? Na to není jednoznačná odpověď. To, zda lékař po vzniku atypické fraktury vlivem dlouhodobé léčby bisfosfonáty vysadí, bude vždy individuální rozhodnutí. Lékař musí zvážit, co je pro pacienta menší zlo, zda pokračovat v podávání bisfosfonátů i při atypické fraktuře, či zda je přestat podávat. Jistě na rozhodnutí bude mít vliv míra agresivity maligní choroby a intenzita osteolýzy vlivem této nemoci.
Proto i poslední doporučení pro léčbu mnohočetného myelomu, které vydala Česká myelomová skupina, hovoří o přerušení podávání bisfosfonátů, pokud je pacient v kompletní remisi, bez prokazatelné aktivity nemoci [59].
Závěr pro praxi
- Jako atypická fraktura se označuje zlomenina, která vznikla v místě, kde není žádné patologické osteolytické ložisko, a která vznikla bez odpovídajícího úrazového děje. Příčinou je zvýšená křehkost kosti.
- Když přijde pacient se stížností na novou bolest ve skeletu, je vždy vhodné se jej otázat, zda neužívá dlouhodobě bisfosfonáty. Pokud je užívá, pak zvážit možnost atypické fraktury a tuto možnost ověřit RTG vyšetřením.
- Postup léčby atypické fraktury vždy konzultovat s ortopedem a zvážit ukončení podávání bisfosfonátů.
Tato práce byla podpořena granty IGA Ministerstva zdravotnictví NT12215, NT12130 a NT13190, ale také MUNI/ A/ 0723/ 2012, a dále NT 12215-4/ 2011 a také NT 13190 - 3/ 2012. Podpořeno MZ ČR – RVO (FNBr, 65269705).
prof. MU Dr. Zdeněk Adam, CSc.
www.fnbrno.cz
e‑mail: z.adam@fnbrno.cz
Doručeno do redakce: 15. 5. 2013
Přijato po recenzi: 10. 7. 2013
Sources
1. Ščudla V, Bačovský J, Indrák K et al. Results of therapy and changing prognosis of multiple myeloma during the last 40 years in the region of North and Middle Moravia: group of 562 patients. Hematol J 2003; 4 : 351 – 357.
2. Ščudla V, Minařík J, Pika T. Light chain deposition disease. Vnitř Lék 2012; 58 : 38 – 43.
3. Ščudla V, Herman M, Minařík J et al. Přínos celotělovém magnetické rezonance pro diagnostiku monoklonální gamapatie nejistého významu, mnohočetného myelomu a stanovení Durie ‑ Salmon Plus stagingového systému. Vnitř Lék 2011; 57 : 52 – 60.
4. Mysliveček M, Bačovský J, Ščudla V et al. 18F ‑ FDG PET/ CT a 99mTc ‑ MIBI scintigrafie při hodnocení pacientů s mnohočetným myelomem a monoklonální gamapatií nejistého významu. Klin Onkol 2010; 23 : 325 – 331.
5. Bačovský J, Myslivecek M, Ščudla V et al. Tc ‑ 99m MIBI scintigrafie u mnohočetného myelomu. Clin Nucl Med 2010; 35 : 667 – 670.
6. Ščudla V, Petrová P, Minařík J et al. Příspěvek k hodnocení plazmatických hladin vybraných biologických parametrů u monoklonální gamapatie nejistého významu a u pacientů s mnohočetným myelomem Vnitř Lék 2010; 56 : 591 – 601.
7. Ščudla V, Zemanova M, Minarik J et al. International prognostic index (IPI) – a critical comparison with five multiple myeloma staging systems in the group of 270 patients treated by conventional chemotherapy. Neoplasma 2006; 53 : 277 – 284.
8. Bačovský J, Ščudla V, Vytřasová M et al. Monitoring of bone resorption and bone formation in multiple myeloma. Biomed Pap Med Fac Univ Palacky Olomouc Czech Repub 2002; 146 : 59 – 61.
9. Vytřasová M, Ščudla V, Nekula J et al. Magnetická rezonance při vyšetřování páteře u pacientů s mnohočetným myelomem. Vnitř Lék 2001; 47 : 694 – 698.
10. Bačovský J, Ščudla V, Pospíšil Z et al. Single photon bone densitometry in multiple myeloma. Acta Univ Palacki Olomuc Fac Med 1999; 142 : 83 – 84.
11. Saville PD, Heaney R. Treatment of osteoporosis with diphosphonates. Semin Drug Treat 1972; 2 : 47 – 50.
12. Bonjour JP, Fleisch HA. Diphosphonates and vitamin‑D metabolism in Paget’s disease. Lancet 1973; 2 : 375 – 376.
13. Fromm G, Schajowicz F, Mautalen CA. Letter: Disodium ethane ‑ 1 – hydroxy ‑ 1,1 – diphosphonate (E.H.D.P.) in Paget’s disease. Lancet 1975; 2 : 666.
14. Heaney RP, Saville PD. Etidronate disodium in postmenopausal osteoporosis. Clin Pharmacol Ther 1976; 20 : 593 – 604.
15. Siris ES, Sherman WH, Baquiran DC et al. Effects of dichloromethylene diphosphonate on skeletal mobilization of calcium in multiple myeloma. N Engl J Med 1980; 302 : 310 – 315.
16. Charhon S, Chapuy MC, Valentin‑Opran Aet al. Treatment of hypercalcemia of myelomatous origin with intravenous diphosphonates. Presse Med 1983; 12 : 2983 – 2986.
17. Jung A, Chantraine A, Donath A et al. Use of dichloromethylene diphosphonate in metastatic bone disease. N Engl J Med 1983; 308 : 1499 – 1501.
18. Kanis JA, Paterson AD, Russell RG. The use of diphosphonates in myeloma. Br J Haematol 1983; 53 : 688 – 690.
19. Delmas PD, Charhon S, Chapuy MC et al. Long‑term effects of dichloromethylene diphosphonate (CI2MDP) on skeletal lesions in multiple myeloma. Metab Bone Dis Relat Res 1982; 4 : 163 – 168.
20. Man Z, Otero AB, Rendo P et al. Use of pamidronate for multiple myeloma osteolytic lesions. Lancet 1990; 335 : 663.
21. Merlini G, Parrinello GA, Piccinini L et al. Long‑term effects of parenteral dichloromethylene bisphosphonate (CL2MBP) on bone disease of myeloma patients treated with chemotherapy. Hematol Oncol 1990; 8 : 23 – 30.
22. Bonjour JP, Philippe J, Guelpa G et al. Bone and renal components in hypercalcemia of malignancy and responses to a single infusion of clodronate. Bone 1988; 9 : 123 – 130.
23. Attardo ‑ Parrinello G, Merlini G, Pavesi F et al. Effects of a new aminodiphosphonate (aminohydroxybutylidene diphosphonate) in patients with osteolytic lesions from metastases and myelomatosis. Comparison with dichloromethylene diphosphonate. Arch Intern Med 1987; 147 : 1629 – 1633.
24. Adam Z, Ševčík P, Vorlíček J et al. Kostní nádorová choroba. Praha: Grada 2004.
25. Tomíška M, Adam Z, Prokeš B et al. Bone mineral density in multiple myeloma patients after intravenous clodronate therapy. Acta Med Austriaca 2001; 28 : 38 – 43.
26. Zajíčková K. Primární hyperparathyreidismus jako příčina hyperkalcemie u pacientky s karcinomem prsu a hyperkalcémií. Čas Lék Česk 2010; 149 : 546 – 548.
27. Fínek J, Prausová J, Cmejlová V et al. IKARUS Projekt – incidence kostních komplikací u pacientek s karcinomem prsu. Retrospektivní analýza pacientů v centrech České a Slovenské republiky. Klin Onkol 2009; 22 : 154 – 162.
28. Málek Z. Přínos ibandronatu u léčby postmenopauzální osteoporózy. Vnitř Lék 2007; 53 : 1114 – 1118.
29. Lastůvková I, Adam Z. Dotazníkový průzkum tolerance a nežádoucích účinků kloronatu u pacientů s mnohočetným myelomem. Vnitř Lék 2002; 48 : 1049 – 1053.
30. Fojtík Z, Kandusová M. Bisfosfonáty při léčbě osteoporózy. Vnitř Lék 1997; 43 : 696 – 699.
31. Slabý J, Špička I, Hulejová H et al. Účinek klodronatu u pacientů s mnohočetným myelomem. Hodnocení specifických markerů kostní resorpce. Čas Lék Česk 1997; 136 : 57 – 60.
32. Ruggiero SL, Mehrotra B, Rosenberg TJ et al. Osteonecrosis of the jaws associated with the use of bisphosphonates: a review of 63 cases. J Oral Maxillofac Surg 2004; 62 : 527 – 534.
33. Migliorati CA. Bisphosphonate‑associated oral osteonecrosis. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 2005; 99 : 135.
34. Adam Z, Kozumpliková M, Pour L et al. Osteonekróza čelisti v průběhu léčby mnohočetného myelomu a podávání bisfosfonátů. Vnitř Lék 2006; 52 : 176 – 180.
35. Machálka M. Osteonekróza čelisti následují po kompletní protinádorové léčby a podávání bisfosfonátů. Vnitř Lék 2006; 52 (79Suppl 2), 81 – 82.
36. Visekruna M, Wilson D, McKiernan FE. Severely suppressed bone turnover and atypical skeletal fragility. J Clin Endocrinol Metab 2008; 93 : 2948 – 2952.
37. Kwek EB, Koh JS, Howe TS. More on atypical fractures of the femoral diaphysis. N Engl J Med 2008; 359 : 316 – 317.
38. Lee P, Seibel MJ. More on atypical fractures of the femoral diaphysis. N Engl J Med 2008; 359 : 317 – 318.
39. Whyte MP. Atypical femoral fractures, bisphosphonates, and adult hypophosphatasia. J Bone Miner Res 2009; 24 : 1132 – 1134.
40. Abrahamsen B, Eiken P, Eastell R. Subtrochanteric and diaphyseal lemur fractures in patients treated with alendronate: a register‑based national cohort study. J Bone Miner Res 2009; 24 : 1095 – 1102.
41. Abrahamsen B. Bisphosphonate adverse effects, lessons from large databases. Curr Opin Rheumatol 2010; 22 : 404 – 409.
42. Girgis CM, Sher D, Seibel MJ. Atypical femoral fractures and bisphosphonate use. N Engl J Med 2010; 362 : 1848 – 1849.
43. Lee JK. Bilateral atypical femoral diaphyseal fractures in a patient treated with alendronate sodium. Int J Rheum Dis 2009; 12 : 149 – 154.
44. Black DM, Kelly MP, Genant HK et al. Fracture Intervention Trial Steering Committee; HORIZON Pivotal Fracture Trial Steering Committee. Bisphosphonates and fractures of the subtrochanteric or diaphyseal femur. N Engl J Med 2010; 362 : 1761 – 1771.
45. Breglia MD, Carter JD. Atypical insufficiency fracture of the tibia associated with long‑term bisphosphonate therapy. J Clin Rheumatol 2010; 16 : 76 – 78.
46. Compston JE. Bisphosphonates and atypical femoral fractures: a time for reflection. Maturitas 2010; 65 : 3 – 4.
47. Somford MP, Draijer FW, Thomassen BJ et al. Bilateral fractures of the femur diaphysis in a patient with rheumatoid arthritis on long‑term treatment with alendronate: clues to the mechanism of increased bone fragility. J Bone Miner Res 2009; 24 : 1736 – 1740.
48. Agarwal S, Agarwal S, Gupta P et al. Risk of atypical femoral fracture with long‑term use of alendronate (bisphosphonates): a systemic review of literature. Acta Orthop Belg 2010; 76 : 567 – 571.
49. Charopoulos I, Orme S, Giannoudis PV. Fracture risk associated with chronic use of bisphosphonates: evidence today. Expert Opin Drug Saf 2011; 10 : 67 – 76.
50. Rizzoli R, Akesson K, Bouxsein M et al. Subtrochanteric fractures after long‑term treatment with bisphosphonates: a European Society on Clinical and Economic Aspects of Osteoporosis and Osteoarthritis, and International Osteoporosis Foundation Working Group Report. Osteoporos Int 2011; 22 : 373 – 390.
51. Rogers LF, Taljanovic M. FDA statement on relationship between bisphosphonate use and atypical subtrochanteric and femoral shaft fractures: a considered opinion. AJR Am J Roentgenol 2010; 195 : 563 – 566.
52. Schneider JP. Should bisphosphonates continued indefinitely. An unusual fracture in healthy woman on long‑term bisphosphonate. Geriatrics 2006; 61 : 31 – 33.
53. Wernecke G, Namduri S, DiCarlo EF et al. Case report of spontaneous nonspinal fracture in multiple myeloma pacient on long term pamidronate and zoledronic acid. HSS J 2008; 4 : 123 – 127.
54. Grasko JM, Hermann RP, Vasikaran SD. Recurrent low ‑ energy femoral Shift fratures and osteonecrosis of the jaw in a case of multiple myeloma treated with bisphosphonates. J Oral Maxillofac Surg 2009; 67 : 645 – 649.
55. Waterman GN, Yellin O, Jamshidinia K et al. Metatarsal stress fractures in patients with multiple myeloma treated with long‑term bisphosphonates: a report of six cases. J Bone Joint Surg Am 2011; 93: e106.
56. Pradhan P, Saxena V, Yadav A et al. Atypical metatarsal fracture in a patient on long term bisphosphonate therapy. Indian J Orthop 2012; 46 : 589 – 592.
57. Puhaindran ME, Farooki A, Steensma MR et al. Atypical subtrochanteric femoral fractures in patients with skeletal malignant involvement treated with intravenous bisphosphonates. J Bone Joint Surg Am 2011; 93 : 1235 – 1242.
58. Chang ST, Tenforde AS, Grimsrud CD et al. Atypical femur fractures among breast cancer and multiple myeloma patients receiving intravenous bisphosphonate therapy. Bone 2012; 51 : 524 – 527.
59. Hájek R. za Českou myelomovou skupinu: Diagnostika a léčba mnohočetného myelomu. Transfuze a hematologie dnes 2012; 18 : 1 – 90.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2013 Issue 11-
All articles in this issue
- Prevalencia diabetickej retinopatie, distálnej symetrickej diabetickej polyneuropatie a screening glomerulárnej filtrácie v čase diagnózy diabetes mellitus 2. typu – kohortná štúdia
- Léčba těžké sepse na pracovištích intenzivní péče v České republice – pilotní výsledky projektu EPOSS
- Nový krevní test biomarkeru SEPT9 a screening kolorektálního karcinomu
- Možnosti genetickej diagnostiky nádorových a zápalových ochorení čriev na Slovensku
- SAVOR-TIMI 53 – Saxagliptin and Cardiovascular Outcomes in Patients with Type 2 Diabetes Mellitus
- Manažment povrchovej tromboflebitídy. Odporúčania Angiologickej sekcie Slovenskej lekárskej komory (2013)
- Význam hodnotenia EKG v diagnostike pľúcnej embólie
- Atypická fraktura metatarzální kosti u pacienta s mnohočetným myelomem, který byl dlouhodobě léčen bisfosfonáty
- Zánětlivá reakce a význam C‑ reaktivního proteinu u pacientů s akutním koronárním syndromem
- Tyreostatická liečba a jej nežiadúce účinky
- Úloha kardiálnych biomarkerov v monitorovaní kardiotoxicity po transplantácii kmeňových krvotvorných buniek
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Tyreostatická liečba a jej nežiadúce účinky
- Zánětlivá reakce a význam C‑ reaktivního proteinu u pacientů s akutním koronárním syndromem
- Význam hodnotenia EKG v diagnostike pľúcnej embólie
- Manažment povrchovej tromboflebitídy. Odporúčania Angiologickej sekcie Slovenskej lekárskej komory (2013)
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

