-
Medical journals
- Career
Výskyt aterogénnej dyslipidémie vo vzorke asymptomatických probandov vyšetrením pomocou metódy Lipoprint
Authors: A. Dukát 1; S. Oravec 1; M. Wawruch 2; P. Gavornik 1; P. Sabaka 1
Authors‘ workplace: II. interná klinika Lekárskej fakulty UK a UN Bratislava, Slovenská republika, prednosta prof. MUDr. Andrej Dukát, CSc., FESC 1; Ústav farmakológie Lekárskej fakulty UK Bratislava, prednostka prof. MUDr. Viera Kristová, CSc. 2
Published in: Vnitř Lék 2011; 57(3): 258-260
Category: 60th birthday of prof. Mudr. Jiřího Vítovce, CSc, FESC
Overview
Metóda delenia lipoproteínov na polyakrylamidovom géli Lipoprint umožňuje presnejšie kvantifikovať neaterogénne a aterogénne lipoproteíny plazmy. Pre použitie v humánnej medicíne bola táto metóda FDA schválená iba pred nedávnom. Podľa prevahy neaterogénnych alebo aterogénnych lipoproteínov v lipoproteínovom spektre metóda umožňuje odlíšiť neaterogénny typ A od aterogénneho B typu. Po ich identifikácii je následne možné presnejšie určiť spôsob potrebného liečebného postupu u pacientov so zvýšeným kardiovaskulárnym rizikom. Aj v skupine tzv. zdravých, asymptomatických kontrol s normolipémiou je možné pomocou tejto metódy vyčleniť skupinu, ktorá má vyššie riziko včasného vývoja aterotrombózy.
Kľúčové slová:
kardiovaskulárne ochorenia – diagnostika – dyslipoproteinémie – liečbaÚvod
Aterotrombóza a jej závažné komplikácie predstavujú v súčasnosti najčastejšiu príčinu predčasnej mortality vo všetkých populáciách vo svete. Jednou z podstatných faktorov, ktoré sa podieľajú na urýchlení celého procesu aterotrombózy, predstavujú dyslipoproteinémie. Ich určenie pomocou metódy Lipoprint v skupine asymptomatických, klinicky zdravých dobrovoľníkov bolo predmetom sledovanej štúdie.
Pacienti a použité metódy
Vyšetrili sme 150 pacientov, spomedzi asymptomatických tzv. zdravých probandov, dobrovoľníkov, študentov medicíny na lekárskej fakulte. Všetci súhlasili s účasťou na štúdii podpísaním informovaného súhlasu. Sledovanie bolo schválené lokálnou etickou komisiou. Išlo o nefajčiarov, normotenzných probandov, bez známeho kardiovaskulárneho alebo iného metabolického ochorenia, bez nadhmotnosti alebo obezity.
Vek sledovaných bol 19–24 rokov (± 3,5 SD roka), 69 mužov a 81 žien s negatívnou anamnézou akéhokoľvek závažného kardiovaskulárneho, alebo iného internistického ochorenia. Žiaden zo sledovaných nebral v čase vyšetrenia akúkoľvek medikamentóznu liečbu a tiež nebol addiktorom ku známym látkam.
Vzorka krvi z kubitálnej žily bola odobraná ráno po 12-hodinovom lačnení na stanovenie rutínnych biochemických parametrov, vrátane úplného lipidového spektra z plazmy EDTA-K2. Z lipidových parametrov sa vyšetrili celkový cholesterol a triacylglyceroly v plazme enzymatickou metódou CHOD, PAP, Roche Diagnostics, Nemecko. Na určenie neaterogénneho lipoproteínového fenotypu A a aterogénneho lipoproteínového fenotypu B bol použitý systém LDL Lipoprint Quantimetrics, USA. Skóre aterogénneho rizika (SAR) sa vypočítalo ako pomer neaterogénnych a aterogénnych plazmatických lipoproteínov. Hodnoty SAR nad 10,8 predstavovali neaterogénny lipoproteínový profil, kým menej ako 9,8 charakterizovali aterogénny lipoproteínový profil.
Prostacyklín (PGI2), jeho chemicky stabilnú formu 6-keto-PGF1 α a tromboxan A2 (TxA2), jeho chemickú formu tromboxan B2 (TxB) v plazme sme analyzovali ELISA metódou DRG, USA. Štatistické hodnotenie meraných hodnôt bolo vyhodnotené nepárovým Studentovýmt-testom. Štatistická významnosť predstavovala hodnotu menšiu než p < 0,005.
Výsledky
V tab. 1 sú uvedené získané namerané hodnoty v celej veľkej skupine 150 asymptomatických, tzv. zdravých dobrovoľníkov, ktorí neboli nositeľmi známych závažných rizikových faktorov. U 140 zo sledovanej vzorky bol prítomný neaterogénny lipoproteínový profil A. Avšak u 10 zo sledovanej vzorky, napriek prítomnej normolipémii (normálnych hodnôt sérového cholesterolu a triacylglycerolov) bolo možné pomocou metódy Lipoprint diagnostikovať aterogénny lipoproteínový profil B.
Table 1. Plazmatické koncentrácie lipidov a lipoproteínov v sledovanej vzorke probandov. 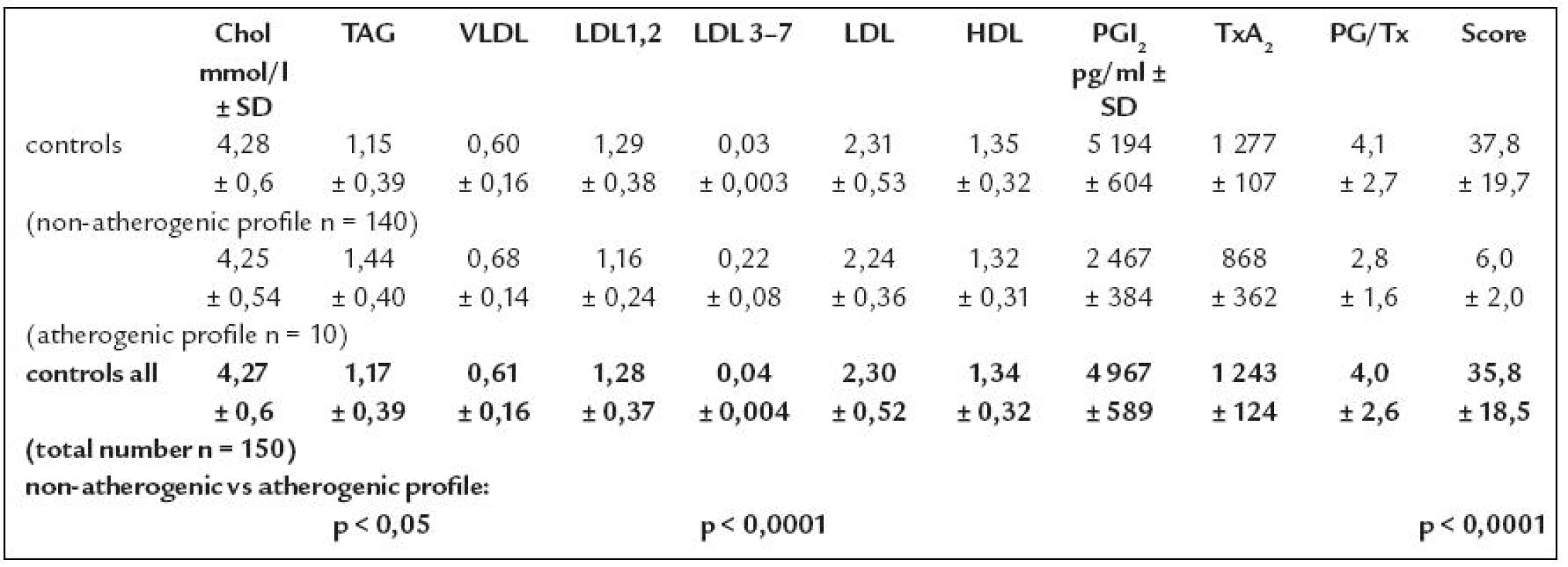
Určenie prítomnosti malých hustých lipoproteínov v sére probandov môže preto mať pre nich prognostický význam. Predstavujú totiž skupinu s vyšším rizikom predčasného vývoja aterotrombózy, ktoré nie je možné určiť pomocou bežných rutínnych vyšetrení pri súčasných tzv. screeningových vyšetreniach.
Diskusia
Ateroskleróza s jej závažnými komplikáciami ako aterotrombóza predstavuje v súčasnosti vôbec najčastejšiu príčinu predčasných úmrtí vo všetkých krajinách vo svete. Predčasný rozvoj tohto základného ochorenia začína u osoby s vysokým rizikom už vo včasnom veku života a predstavuje dôležité miesto v oblasti preventívnych opatrení [1,2].
Dyslipoproteinémia je jednou z primárnych príčin vzniku a rozvoja aterosklerózy a jej následných komplikácií. Z tohto dôvodu iba účinná a včasná prevencia a intervencia v diagnostike a liečbe dyslipoproteinémií ako integrálna súčasť komplexnej stratégie môže zabezpečiť účinné predchádzanie kardiometabolických a všeobecne kardiovaskulárnych ochorení i ostatných komorbidít [3,4].
Inovovaná laboratórna diagnostická metóda v oblasti porúch metabolizmu lipoproteínov, elektroforéza lipoproteínov na polyakrylamidovom géli Lipoprint LDL systém umožňuje identifikovať a kvantitatívne vyhodnotiť aterogénne lipoproteíny prítomné v lipoproteínovom spektre séra/plazmy u sledovanej osoby [5]. Vyhodnocuje lipoproteínové spektrum a určuje neaterogénny lipoproteínový profil ako fenotyp A, resp. ako aterogénny lipoproteínový profil fenotyp B [6] podľa toho, či v lipoproteínovom spektre prevládajú neaterogénne, alebo aterogénne lipoproteínové entity [7,8]. Aterogénne lipoproteínové spektrá sa vyznačujú bohatým zastúpením aterogénnych lipoproteínov veľmi nízkej hustoty (VLDL), intermediárnej hustoty IDLc a IDLb a najmä prítomnosťou malých denzných lipoproteínov nízkej hustoty mdLDL. V ich prípade ide o silne aterogénne LDL subpopulácie, ktoré vytvárajú frakciu LDL 3–7. Sú malé, s priemerom menším, ako 26,5 nm (265 Angströmov) a flotujú v hustotnom rozmedzí medzi d = 1,048–1,065 g/ml. Ich silná aterogénnosť spočíva v ich biologických vlastnostiach, charakterizujúcich ich silný aterogénny potenciál [9,10].
Je užitočné pre klinickú prax stanoviť skóre aterogénneho rizika. Predstavuje pomernú hodnotu neaterogénnych a aterogénnych lipoproteínov v sére. Má dobrú koreláciu s fenotypom lipoproteínového profilu u sledovaných osôb, ktorú generuje Lipoprint LDL systém [10].
Dnes sme konfrontovaní s novou klinicko-diagnostickou skutočnosťou, ktorú predstavuje fenomén „aterogénna normolipémia“, ako ukazujú výsledky nami sledovanej skupiny osôb. Takýto výskyt v populácii nie je zanedbateľný a podľa literárnych údajov až 28% osôb môže mať prítomný tento druh lipidového spektra [11].
Aterogénna normolipémia rozširuje rizikovú skupinu osôb ohrozených vznikom predčasnej manifestácie komplikácií aterotrombózy. Doposiaľ ju tvorili pacienti diagnostikovaní ako aterogénna dyslipoproteinémia. Rozdiel medzi osobami s aterogénnou normolipémiou a pacientmi s diagnostikovanou dyslipoproteinémiou možno následne určí v adekvátnom medicínskom prístupe k týmto pacientom, nakoľko obe skupiny predstavujú nositeľov zvýšeného kardiovaskulárneho rizika [12–14].
Záver
Včasné zahájenie prevencie a intervencie (nefarmakologickej i farmakologickej liečby) dnes predstavuje moderný smer v liečbe porúch metabolizmu lipidov [15–17]. Je nevyhnutnou súčasťou nielen k úprave hladín lipidového spektra, ale aj k redukcii reziduálneho kardiovaskulárneho rizika [15,16]. K ovplyvneniu rizika u pacientov s aterogénnou dyslipoproteinémiou je potrebný komplexný prístup [17]. Predchádza mu potrebná včasná identifikácia osoby, ktorá je nositeľom rizika, ktoré predstavuje aterogénna dyslipidémia. Metóda presného stanovenia veľkostí lipoproteínových partikúl Lipoprint prináša v tejto súvislosti možný benefit. Umožňuje totiž získať dodatočné informácie, ktoré bežné odporúčané screeningové vyšetrenie v súčasnosti nedokáže presne odhaliť. Určovanie aterogenity lipoproteínového profilu predstavuje prínos v doterajšej interpretácii lipidových parametrov a posúva interpretáciu dyslipoproteinémií nad rámec doteraz zabehnutých schém.
Práca bola podporená z grantov Interreg III-AT/SK a VEGA 1/0135/09.
prof. MUDr. Andrej Dukát, CSc., FESC
www.fnspba.sk
e-mail: andrej.dukat@faneba.skDoručeno do redakce: 31. 12. 2010
Sources
1. Češka R, Krutská L, Zlatohlávek L et al. Komplexní léčba kardiovaskulárního rizika. Zaměřeno na telmisartan. Vnitř Lék 2010; 56 : 839–844.
2. Rosolová H, Petrlová B, Šimon J et al. Makrovaskulární a mikrovaskulární komplikace u diabetiků 2. typu. Vnitř Lék 2008; 54 : 229–237.
3. Vaverková H, Soška V, Rosolová H et al. Doporučení pro diagnostiku a léčbu dyslipidemií v dospělosti, vypracované výborem České společnosti pro aterosklerózu. Vnitř Lék 2007; 53 : 181–197.
4. Widimský J. Jaké jsou optimální hodnoty systolického tlaku u diabetiků? Studie ACCORD Blood Pressure dokončena. Cor Vasa 2010; 52 : 700–705.
5. Oravec S. Nová laboratórno-medicínska pomoc v diagnostike dyslipoproteinémií a kardiovaskulárnych ochorení: Identifikácia LDL podskupín. Med Milit Slov 2006; 8 : 28–32.
6. Oravec S. Den drohenden Herztod erkennen – und vermeidem. Der Mediziner 2010; 4 : 6–7.
7. Oravec S, Dukát A, Gavorník P et al. Lipoproteínový profil séra pri novozistenej artériovej hypertenzii. Úloha aterogénnych lipoproteínov v patogenéze ochorenia. Vnitř Lék 2010; 56 : 967–971.
8. Kučera M, Oravec S, Očadlík I. Význam fenofibrátu v liečbe aterogénnej dyslipoproteinémie. Vnitř Lék 2010; 56 : 865–870.
9. Shoji T, Hatsuda S, Tsuchikura S et al. Small dense low-density lipoprotein cholesterol concentration and carotid atherosclerosis. Atherosclerosis 2009; 202 : 582–588.
10. Vaverková H, Karásek D, Jackuliaková D et al. Klasifikace dyslipidemií založená na koncentraci apolipoproteinu B a triglyceridú. Vnitř Lék 2010; 56 : 889–892.
11. Van J, Pan J, Charles MA et al. Atherogenic lipid phenotype in a general group of subjects. Arch Pathol Lab Med 2007; 131 : 1679–1685.
12. Assmann G, Cullen P, Schulte H. Non-LDL related dyslipidaemia and coronary risk: a case-control study. Diab Vasc Dis Res 2010; 7 : 204–212.
13. Carey VJ, Bishop L, Laranjo N et al. Contribution of High Plasma Triglycerides and Low High-Density Lipoprotein Cholesterol to Residual Risk of Coronary Heart Disease After Establishment of Lown-Density Lipoprotein Cholesterol Control. Am J Cardiol 2010; 106 : 757–763.
14. Souček M, Kára T et al. Klinická patofyziologie hypertenze. Praha: Grada Publishing 2002.
15. Fruchart JC, Sacks FM, Hermans MP et al. Residual Risk Reduction Initiative (R3I). The Residual Risk Reduction Iniciative: a call to action to reduce residual vascular risk in dyslipidaemic patient. Diab Vasc Dis Res 2008; 5 : 319–335.
16. Fábryová Ľ. Manažment aterogénnej dyslipidémie pri metabolickom syndróme. Via Pract 2007; S4 : 13–18.
17. Berger JS, Jordan CO, Lloyd-Jones D et al. Screening for cardiovascular risk in asymptomatic patients. J Am Coll Cardiol 2010; 55 : 1169–1177.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2011 Issue 3-
All articles in this issue
- Interna a kardiologie, internisté a kardiologové
- Systolický wall stress ľavej komory srdca pri antihypertenzívnej liečbe
- Dyslipidemie a obezita 2011. Jak spolu souvisejí a v čem se liší
- Autoimunitní pankreatitida a IgG pozitivní sklerotizující cholangitida
- Výskyt aterogénnej dyslipidémie vo vzorke asymptomatických probandov vyšetrením pomocou metódy Lipoprint
- Zevní vlivy podmiňující vznik nádorů nebo ochraňující před jejich vznikem
- Vyskytují se v medicíně „módní“ choroby?
- Rostoucí problém – lidský papilomavirus a nádory hlavy/krku
- Mikroalbuminurie. Od diabetu ke kardiovaskulárnímu riziku
- Kotníko-pažní index u nemocných s diabetes mellitus 2. typu
- Trombohemoragický syndrom u nemocných s myeloproliferativním onemocněním s trombocytemií
- Reziduální riziko kardiovaskulárních komplikací a jeho snížení kombinací hypolipidemik
- Síť komplexních onkologických center České republiky
- Variabilita krevního tlaku a arteriální hypertenze
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Mikroalbuminurie. Od diabetu ke kardiovaskulárnímu riziku
- Zevní vlivy podmiňující vznik nádorů nebo ochraňující před jejich vznikem
- Interna a kardiologie, internisté a kardiologové
- Systolický wall stress ľavej komory srdca pri antihypertenzívnej liečbe
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

