-
Medical journals
- Career
Projevy histocytózy z Langerhansových buněk v ORL oblasti
Authors: P. Smilek 1; M. Pažourková 2
Authors‘ workplace: Klinika otorinolaryngologie a chirurgie hlavy a krku Lékařské fakulty MU a FN u sv. Anny Brno, přednosta prof. MUDr. Rom Kostřica, CSc. 1; Klinika zobrazovacích metod Lékařské fakulty MU a FN u sv. Anny Brno, přednosta doc. MUDr. Petr Krupa, CSc. 2
Published in: Vnitř Lék 2010; 56(Supplementum 2): 76-84
Category: Langerhans cell histiocytosis and some other Hematology rare diseases
Overview
Oblast hlavy a krku bývá postižena až v 90 % případů nemocných s histiocytózou z Langerhansových buněk (LCH). Příznaky v oblasti hlavy a krku mohou být vůbec prvními příznaky u multisystémových forem. Podezření na LCH by měl vzbudit dlouhodobý výtok z ucha nereagující na antibiotickou léčbu, zvětšení mízních uzlin a tumory v orbitě. Multisystémová forma LCH se může vyskytnout u dospělých osob s osteolytickými lézemi lebky, které jsou sdruženy s endokrinologickými a/nebo neurologickými symptomy (např. centrální diabetes insipidus). Těžiště léčby u multisystémových forem spočívá spíše v chemoterapii a event. ozáření, chirurgická léčba má pouze paliativní charakter. Mastoidektomie u rozsáhlé destrukce pyramidy přináší úlevu od bolestí. U izolovaných lézí připadá v úvahu exstirpace ložiska a lokální aplikace steroidů. Autor popisuje 3 kazuistiky nemocných s multisystémovou formou LCH. První pacientka je sledována 33 let, byla léčena vinblastinem (více než 125 bolusů 10 mg i.v.), prednisonem, ozářením (ložisková dávka na pyramidu vpravo přesáhla 100 Gy) a mastoidektomií se dvěma revizemi. V současné době přetrvává diabetes insipidus, kožní projevy a rozsáhlá destrukce kosti spánkové, týlní a atlantookcipitálního skloubení a pravděpodobně postižení pravého spánkového laloku. Nemocná je nyní léčena kladribinem a dexametazonem. Druhý pacient je sledován 4 roky s postižením spánkové kosti a plic, byl léčen mastoidektomií, leustatinem a ozářením, nyní se nachází v kompletní remisi. Třetí pacient je sledován 3 roky pro postižení plic a chronický zánět zevního zvukovodu dobře reagující na obvyklou antibiotickou a antimykotickou léčbu (diagnóza ze zvukovodu nebyla potvrzena). Probíhá léčba kladribinem.
Klíčová slova:
histiocytóza z Langerhansových buněk v oblasti hlavy a krku – mastoidektomie – léčba chirurgická – chemoterapie a radioterapieÚvod
Incidence histiocytózy z Langerhansových buněk (LCH) u dospělých je udávána v počtu 1–2 případy na milion obyvatel [3]. Přibližně ve 30 % je LCH diagnostikována u dospělých osob [25]. Oblast hlavy a krku bývá postižena až v 90 % případů [17]. Podle jiných odhadů více než 60 % pacientů s LCH má postižení hlavy a krku v době diagnózy a u dalších asi 20 % nemocných se objeví léze hlavy a krku v dalším průběhu choroby [9,14]. Nejčastěji se vyskytuje postižení plochých kostí lebky, následuje léze temporální kosti, kůže, mandibuly anebo maxily a cervikální lymfadenopatie [14]. Izolované extraoseální léze v oblasti hlavy a krku byly pozorovány na kůži, sliznici patra, nosu, hrtanu a příušní slinné žlázy, ale tyto výskyty jsou extrémně vzácné.
Otologické projevy
Výskyt ušní symptomatologie je uváděn v literatuře [12,19–21] od 15 do 61 %. Asi u 1/3 pacientů bývá postižení uší oboustranné, oboustranný výskyt je častější u dětí mladších 10 let [2].
LCH může probíhat samostatně pod obrazem zánětu kůže zevního zvukovodu s ušními polypy nebo bez nich a vyskytuje se až u 50 % pacientů [21]. Tento samostatný zánět kůže zvukovodu nereaguje na obvyklou antibiotickou léčbu, ale poměrně dobře reaguje na topickou léčbu mechlorethaminem (nitrogene mustard, mustin). V retroaurikulárních rýhách je možné pozorovat kožní změny – papulózní až nekroticko-pustulózní morfy.
Při postižení temporální kosti při LCH se léze nejčastěji šíří do zevního zvukovodu, aroduje zadní stěnu, otoskopicky se jeví jako polyp nebo granulace ve zvukovodu, přičemž středouší i bubínek bývá intaktní. Klinicky se jeví tato fáze jako zánět zvukovodu, neodpovídající na obvyklou léčbu antibiotiky. Při dalším šíření může být postižena kortikální vrstva mastoidu, tegmen, labyrint a kostní léze se může šířit do šupiny kosti spánkové a do processus zygomaticus [12]. Klinickým projevem je bolest hlavy, pocit plnosti v uchu, porucha sluchu, někdy bolestivé zduření retroaurikulárně, závrať a periferní paréza lícního nervu. Kostěné pouzdro labyrintu silně odolává invazi tumoru, a proto se objevuje percepční nedoslýchavost až při pokročilejší destrukci spánkové kosti. Mírná převodní nedoslýchavost je obvyklá v důsledku přímé invaze tumoru do zevního zvukovodu a středouší. Klinický obraz specifického onemocnění mastoidu je obvykle zkreslen sekundární infekcí s projevy akutní mastoiditidy. Klinicky a RTG pokročilá LCH temporální kosti připomíná cholesteatom a s touto diagnózou je pacient často operován. Při trepanaci výběžku se zjistí ložisko vyplněné nahnědlými hmotami nebo žlutošedými granulacemi, které jsou fragilní, krvácejí, působí destrukci kosti a které se kromě barvy od cholesteatomu liší i neostrým ohraničením [2]. V granulacích také bývají pokrvácená nekrotická ložiska. Při postižení os petrosum spánkové kosti může být přítomný výtok z ucha, pulzatorický šelest, závratě a periferní paréza lícního nervu. Diferenciálně diagnosticky je nutné odlišit zánět středouší s cholesteatomem, zánět zevního zvukovodu a akutní mastoiditidu, karcinom, glomus tumor, osteomyelitis, Wegenerovu granulomaózu a fibrózní dysplazii. Podezření na LCH posiluje nález polypu v zevním zvukovodu při celistvém bubínku.
Většina autorů se shoduje na tom, že vyjma diagnostické biopsie může chirurgická léčba u diseminovaných forem nabídnout pro léčbu LCH jen velmi málo [14]. Chirurgická léčba má v těchto případech pouze paliativní význam [8]. Těžiště léčby spočívá spíše u postižení více systémů v chemoterapii (vinblastin, prednison, kladribin) a ozáření. U izolovaných lézí připadá v úvahu exstirpace ložiska a lokální aplikace steroidů.
Postižení krčních uzlin
K abnormální proliferaci histiocytárních elementů dochází i v cervikálních lymfatických uzlinách. Smith et al [26] udávají výskyt palpačně zjistitelných krčních uzlin asi ve 30 % LCH. Ty mohou být postiženy např. ve formě generalizované lymfadenopatie, nejčastěji jsou však postiženy laterocervikální a submandibulární krční uzliny. Zvětšení uzlin může být prvním příznakem choroby [11]. Izolované postižení lymfatických krčních uzlin bez postižení kůže nebo kostí je velmi vzácné [28]. Nejsou popisovány zvláštní vlastnosti těchto uzlin, které by umožnily jejich makroskopické odlišení od jiných onemocnění lymfatických uzlin, pro diagnózu je rozhodující histologické vyšetření s průkazem CD 1a anebo CD 207 [23]. Cervikální lymfadenopatie se vyskytuje často při multisystémové formě nemoci a převládá názor, že celková systémová léčba má přednost před léčbou chirurgickou, poněvadž většinou dochází k dobré odpovědi na systémovou léčbu [14].
Postižení ostatních lokalizací v ORL oblasti
LCH může představovat diagnostický hlavolam a může postihnout jakoukoliv lokalizaci hlavy a krku: klínovou kost, paranazální dutiny, kosti čelistí, dutinu ústní, kořen jazyka, epiglottis a průdušnici. Většinou jde o velmi vzácný výskyt popsaný v ojedinělých pozorováních. Určitou výjimku představuje lokalizace LCH ve sliznici dutiny ústní, kde je výskyt častější, např. Smith [26] udává výskyt u 15 % nemocných. Pacienti si stěžují na „afty“ v ústech, které znesnadňují příjem potravy. Bývá postižena sliznice gingivy, tvrdého i měkkého patra, patrových oblouků a bukální sliznice. Klinicky se tyto léze jeví jako šířící se dlouhotrvající a progresivně se zhoršující ulcerace s granulační tkání. Při postižení kostí čelistí dochází k vypadávání zubů, patologické změny na kostech čelistí ale nemusí být pozorovány [5]. U žen bývá postižení slizniční výstelky dutiny ústní spojeno s postižením vaginální sliznice [5].
Kazuistiky
Kazuistika 1
Na Klinice otorinolaryngologie a chirurgie hlavy a krku (KOCHHK) FN u sv. Anny v Brně je léčena nemocná narozená v roce 1955. Až do svých 22 let byla zcela zdráva. V roce 1977 byla provedena excise granulomatózní léze z maxilly, jež byla histologicky popsána jako resorpční granulom, ale cíleně na LCH tehdy vyšetřena nebyla. Ve věku 23 let, 5 měsíců po porodu zdravého dítěte, byla diagnostikována hormonální hypofyzární dysfunkce včetně diabetes insipidus. V roce 1979 byla z ulkusu na sliznici vulvy stanovena histologicky diagnóza LCH, objevily se též ulcerace a píštěle v axilách a seborrhoická dermatitida. Nemocná byla léčena protizánětlivým ozářením a cytostatiky (cyklofosfamid, metotrexát, 5-flourouracil, prednison, adriamycin, vincristin, vinblastin). Nejvýraznější remise následovaly po léčbě prednisonem a vinblastinem. Vinblastin byl podáván v týdenních bolusech 10 mg i.v. Nemocná v roce 1985 i přes hypofyzární hormonální dysfunkci a chemoterapii vinblastinem v 1. trimestru gravidity porodila zdravé dítě. V srpnu roku 1991 (po14 letech průběhu) se objevila v obou zvukovodech píštěl se smetanově žlutým obsahem. Po chemoterapii (pro projevy LCH v jiných lokalizacích) došlo ke zhojení zvukovodů. Od září roku 1992 opět úporný zánět zevního zvukovodu vpravo s granulacemi a hojnou sekrecí. Kultivačně byl zjištěn opakovaně Staphylococcus aureus, nereagující na antibiotickou léčbu (Augmentin, Lincocin). V prosinci roku 1992 byla z granulační tkáně ve zvukovodu vpravo potvrzena histologicky diagnóza LCH, bez RTG známek postižení temporální kosti. V lednu roku 1993 proto ozářena na cesioteraxu z jednoho přímého pole na pravý zvukovod a byla aplikována ložisková dávka 15 Gy. Po této léčbě infiltrát ze zvukovodu vymizel, výtok ustal. Od května roku 1993 se objevila silná bolestivost retroaurikulárně vpravo, většinou navečer a v noci, pulzujícího charakteru. Nemocná byla bez teplot, RTG spánkové kosti opět bez zřetelné destrukce, zvukovod vpravo byl prostornější, bez známek infiltrace či zánětu, bubínek byl otoskopicky normální, ale za ním byl patrný sekret, při paracentéze se vyprázdnilo větší množství jantarové tekutiny. Při vyšetření sluchu byla zjištěna převodní nedoslýchavost vpravo (kochleární rezerva až 50 dB). Po 2 měsících již byly na pravé spánkové kosti RTG známky destrukce, byla zvýšená sedimentace erytrocytů (FW 75/106), přitom ale byla nemocná afebrilní. Při antromastoidektomii vpravo byla zjištěna změklá zevní kortikalis v oblasti celého hrotu. Sklípky hrotu, v zóně intersinofaciální a retrosinózní byly vyplněny chabou šedě růžovou granulační tkání. Aditus ad antrum byl úzký, blokovaný zduřelou sliznicí, viditelná část horizontálního kanálku byla intaktní, stejně tak krátké raménko kovadlinky. Histologické vyšetření odpovídalo diagnóze LCH. Pro přetrvávající výtok z trepanační dutiny bylo ještě po dvou měsících provedeno histologické vyšetření granulací a byla potvrzena recidiva. Proto byla pacientka ozářena na cesioteraxu (137Cesium) z jednoho přímého pole na oblast pravého mastoidu, aplikována celková ložisková dávka 19,2 Gy ve 12 frakcích.
Pro přetrvávající výtok a píštěl byla během roku 1994 aplikována další aktinoterapie (28 Gy), chemoterapie (vinblastin) a nemocná užívala Wobe-Mugoz. V roce 1995 byla provedena exkochleace tumoru v dolní čelisti vpravo, histologicky byla opět potvrzena LCH. V listopadu roku 1995 byla provedena chirurgická revize středouší a trepanační dutiny, histologicky byla verifikována persistence LCH – proto byla podána další aktinoterapie a chemoterapie (vinblastin + prednison). Na CT lebeční spodiny v září roku 1995 byla zjištěna infiltrace a osteolýza pravé pyramidy, bez průkazu průniku mas do intrakraniálního prostoru. V listopadu roku 1999 byla provedena 3. operační revize antromastoidektomie vpravo a zjištěna opět rozsáhlá infiltrace celé pyramidy bledě růžovou granulační tkání.
Pro přetrvávající výtok a granulace v trepanační dutině a opakovaně histologicky ověřenou persistenci LCH byla nemocná léčena opakovně v průběhu let 1998–2006 ozářením a chemoterapií vinblastinem. Celkem bylo podáno asi 125 dávek vinblastinu à 10 mg. Celkové ozáření zevního ucha a pravé pyramidy v průběhu onemocnění přesáhlo 120 Gy ložiskové dávky.
Od roku 2004 do roku 2008 byla nemocná léčena bifosfonáty. Na CT snímcích z let 2005–2007 je patrná rozsáhlá destrukce spánkové a okcipitální kosti (obr. 1 a 2). V březnu roku 2004 bylo při pozitronové emisní tomografii (PET) zjištěno drobné ložisko patologické kumulace pod pravou hemisférou mozečku, téměř s ní splývající – ložisko se promítalo do místa destruované okcipitální kosti dorzolaterálně za foramen occipitale.
Image 1. Destrukce spánkové a okcipitální kosti vpravo (v roce 2005) u pacientky 1. 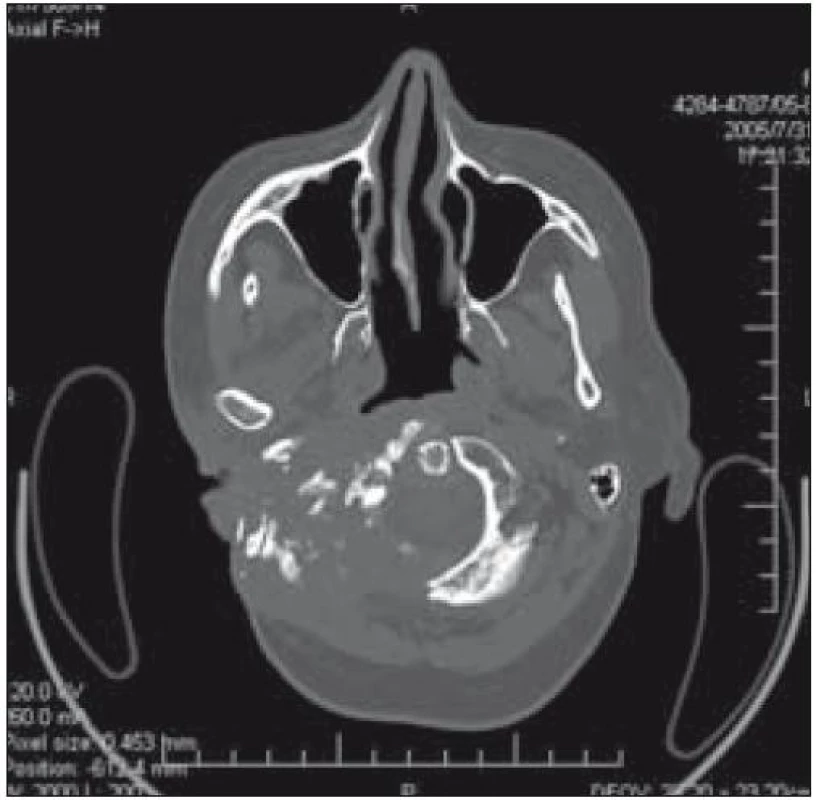
Image 2. Rozsáhlá destrukce spánkové a okcipitální kosti vpravo (v roce 2007) u pacientky 1. 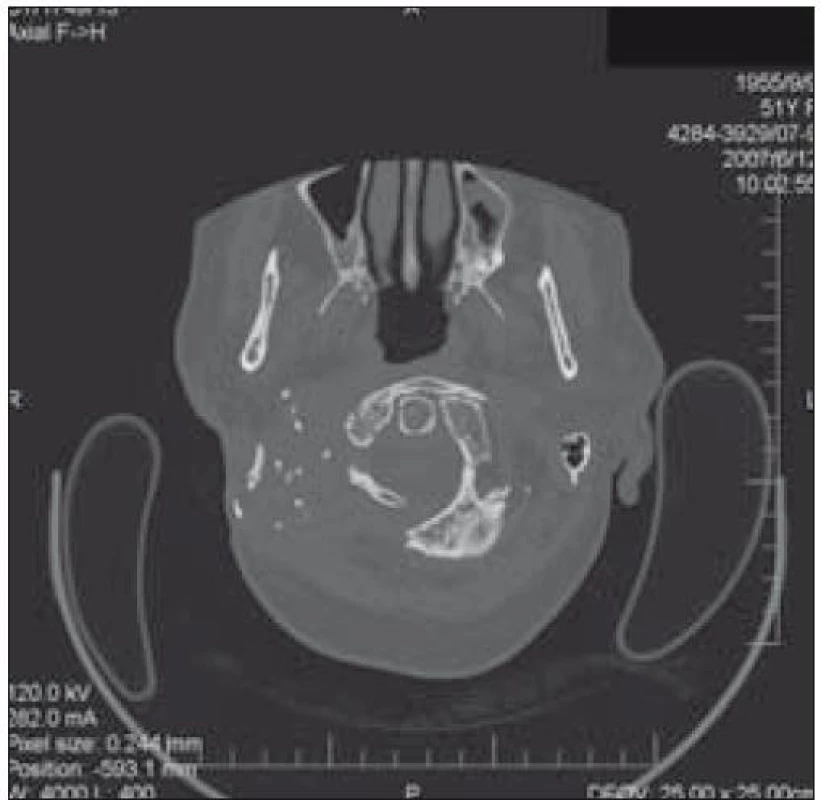
V říjnu roku 2004 byla CT vyšetřením baze lební zjištěna destrukce v oblasti atlantookcipitálního skloubení (obr. 3). Funkční snímky C páteře ale neprokázaly patologický posun, a proto byl doporučen konzervativní postup (při chudém klinickém nálezu s bohatým nálezem na NMR).
Image 3. Destrukce atlantookcipitálního skloubení vpravo u pacientky 1. 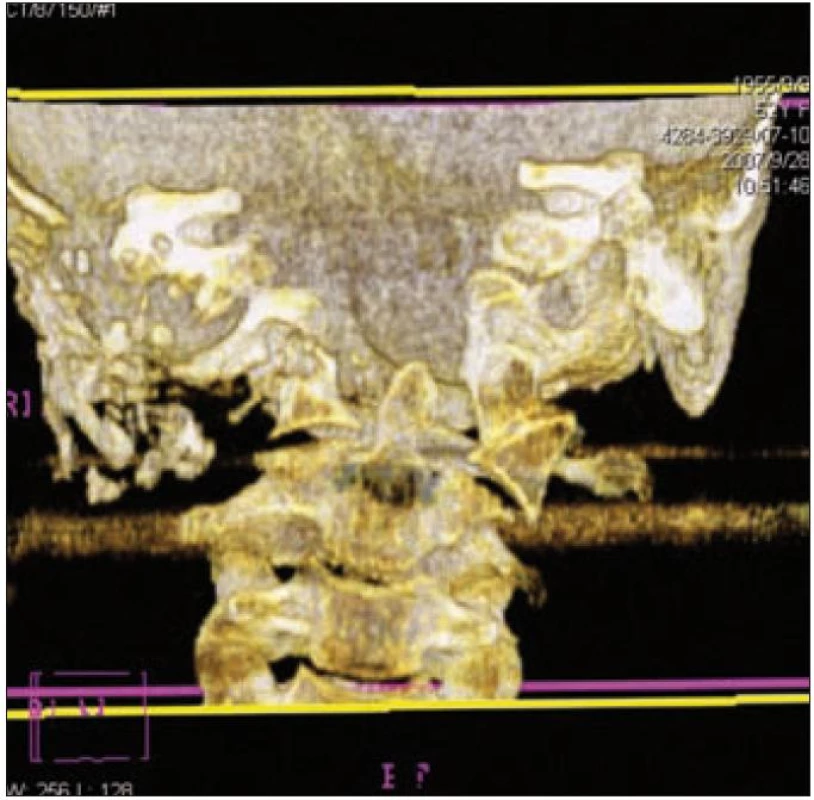
Od února roku 2005 do června roku 2005 bylo podáno 6 sérií paliativní chemoterapie Lastetu p.o. (Lastet 25 mg 2–0–0 den 1.–14. den, interval 28 dní). Na HRCT pyramid byla v červenci roku 2005 zjištěna stabilizace nálezu na atlantooccipitálním skloubení a rozsáhlá destrukce pyramidy a okcipitální kosti s porušením ohraničení vůči zadní a střední jámě lební. Dále byly popsány v.s. postradiační změny bílé hmoty mozkové temporookcipitálně vpravo.
Od srpna roku 2006 postupně narůstala periferní paréza n. VII. V říjnu roku 2008 si nemocná stěžovala na zvýšenou únavnost a spavost; na CT mozku byla zjištěna nitrolební hypertenze, dislokace středočarových struktur o 8 mm a 2 ložiska (obr. 4 a 5). 29. 10. 2008 byla provedena exstirpace tumoru (ložisko o průměru asi 1 cm) oblasti temporálního mozkového laloku vpravo. Patolog při histologickém vyšetření našel pouze postaktinické změny mozkové tkáně s fokální vaskulární hyperplazií typu teleangiektatického kapilárního hemangiomu s absencí exprese CD 1a. Dále byla nemocná léčena vyššími dávkami kortikoidů.
Image 4. CT mozku: dislokace středočarových struktur o 8 mm a ložiska v temporálním laloku vpravo u pacientky 1. 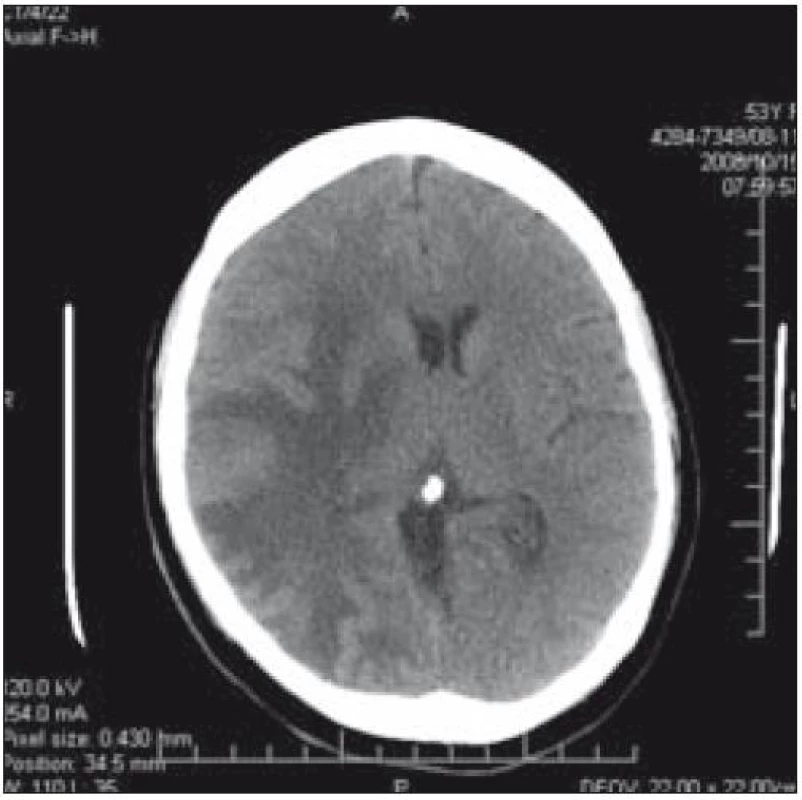
Image 5. CT mozku – ložiska v temporálním laloku vpravo u pacientky 1. 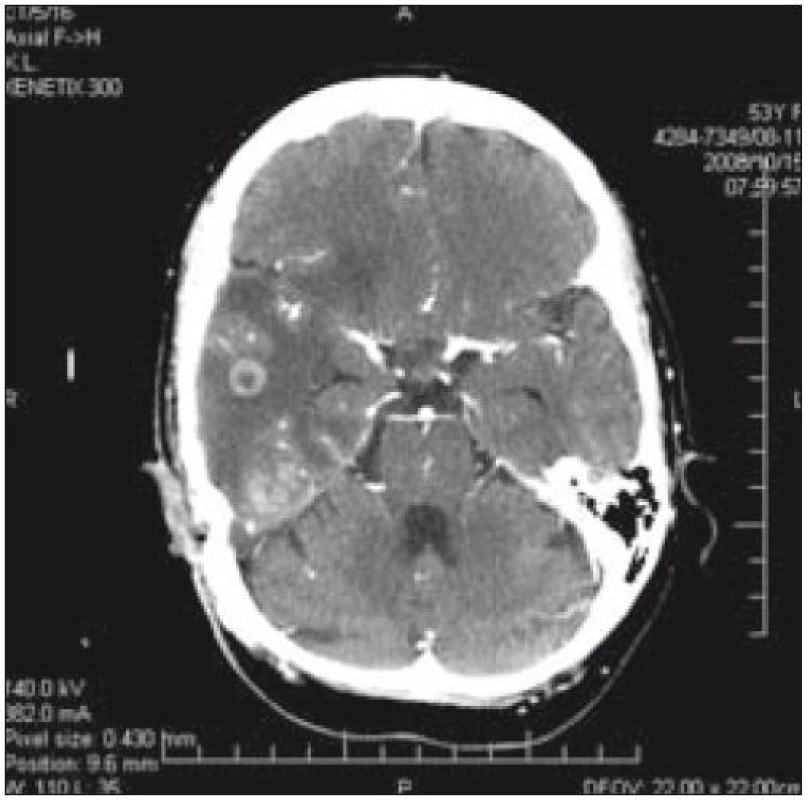
K vyhodnocení aktivity onemocnění bylo provedeno v březnu roku 2010 celotělové PET-CT, při tom se zobrazilo solitární ložisko vyšší akumulace radiofarmaka temporálně vpravo, SUV max. 12,53 (obr. 6). Mimo tohoto ložiska byla distribuce radiofarmaka fyziologická. Kostní defekty v oblasti baze lební a AO spojení vykazují jenom nepatrně vyšší akumulaci radiofarmaka.
Image 6. Pozitronová emisní tomografie mozku – solitární ložisko vyšší akumulace radiofarmaka temporálně vpravo, SUV<sub>max</sub> 12,53 (u pacientky 1). 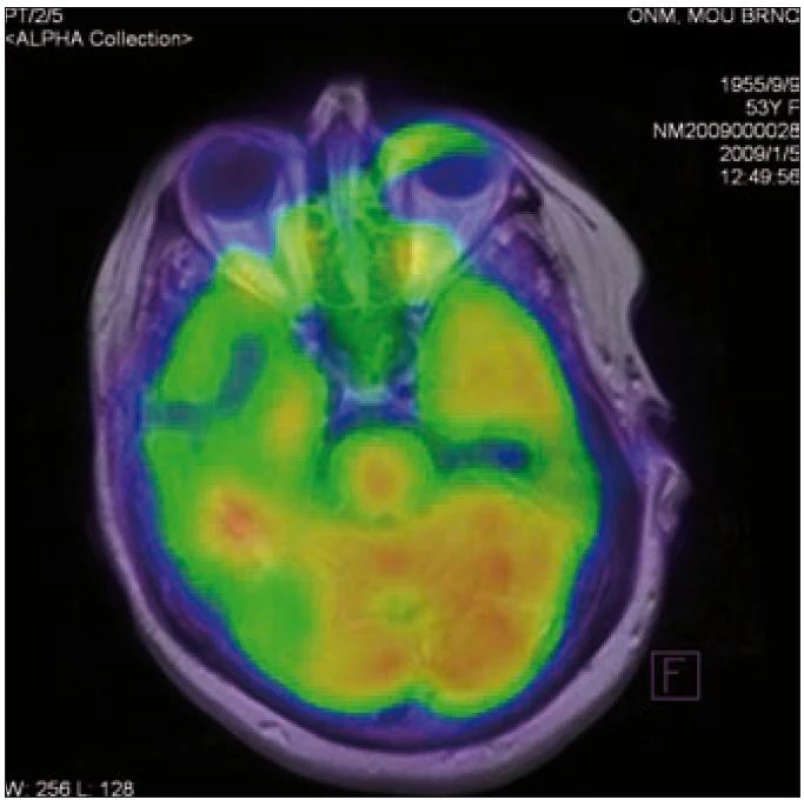
Nyní, po 32 letech průběhu onemocnění, je trepanační dutina mírně zavlhlá, zvukovod je slepě uzavřen, retroaurikulárně je secernující píštěl, je těžká smíšená nedoslýchavost až praktická hluchota vpravo se ztrátou kolem 90 dB (obr. 7), přetrvává paréza lícního nervu vpravo, je výrazná seborrhoická dermatitida ve vlasaté části hlavy a v zapářkových oblastech celého těla. Na kůži v okolí pravého boltce jsou těžké trofické změny (obr. 8). Centrální diabetes insipidus je kompenzován Minirinem. Na poslední MR mozku v lednu roku 2010 je stacionární obraz sledovaných postradiačních a posthemoragických změn.
Image 7. Těžká smíšená nedoslýchavost vpravo, praktická hluchota u pacientky 1. 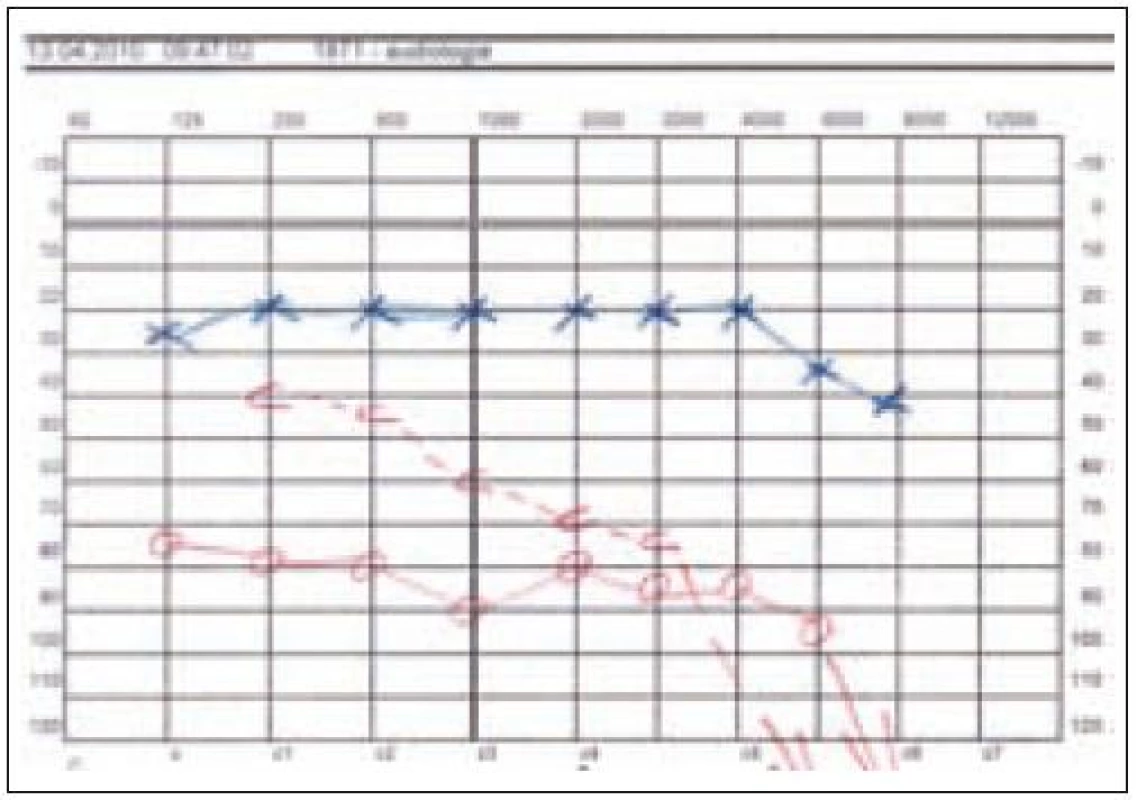
Image 8. Trofické kožní změny v oblasti pravého ušního boltce, slepě uzavřený zvukovod, seborrhoická dermatitida ve vlasaté části hlavy u pacientky 1. 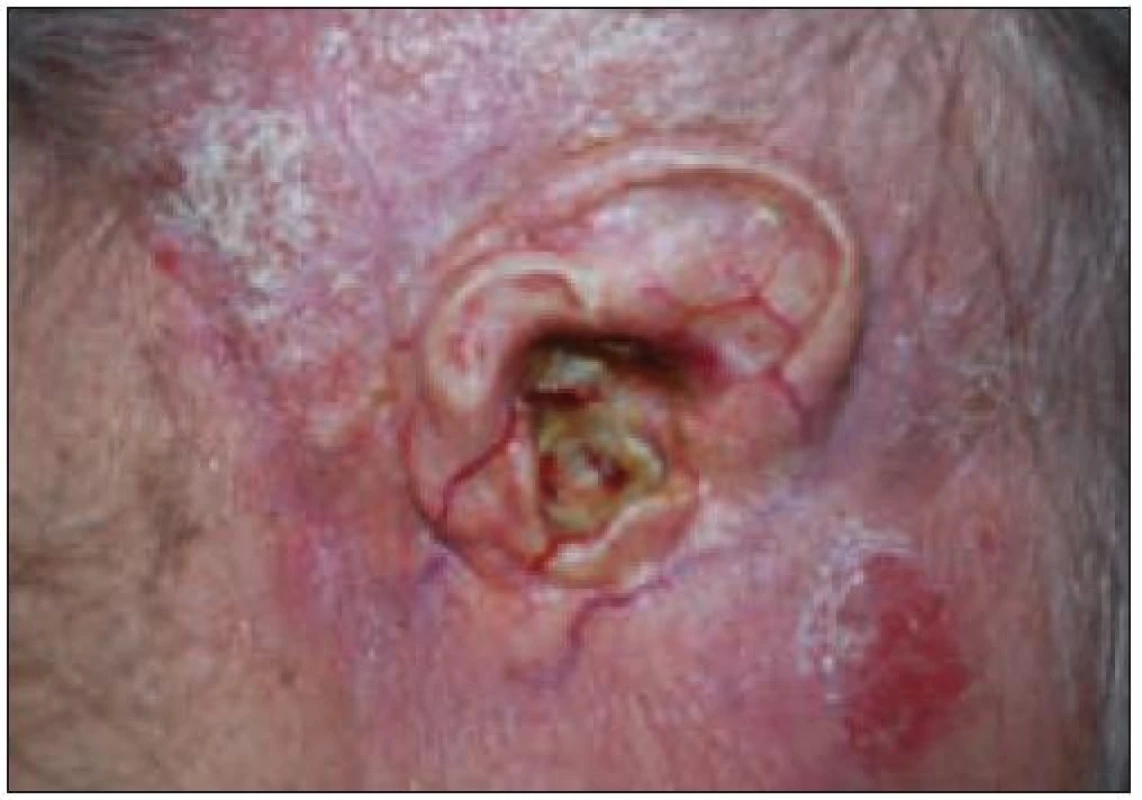
V červenci roku 2010 se u nemocné objevila těžká parciální respirační insuficience. Překvapením při CT vyšetření (obr. 9 a 10) bylo zjištění, že plicní parenchym je v celém rozsahu bulózně změněný ve smyslu emfyzému, podél zadní plochy obou plicních křídel s prevalencí bazálně a vpravo je vidět zvýšení denzity ve smyslu zánětlivé infiltrace hypostatické lokální pneumonie v terénu rozedmy a emfyzematózně-fibrózních intersticiálních změn. Po intenzivní protizánětlivé léčbě a oxygenoterapii respirační insuficience postupně odezněla. Při cíleném pátrání v anamnéze jsme zjistili, že nemocná si na dechové obtíže sice nestěžovala, ale přiznala, že při větší námaze měla pocit nedostatku kyslíku již několik let. Rovněž prosté snímky plic (obr. 11) byly popisovány bez zvláštních patologických změn, nebo bylo vyjádřeno jenom určité podezření. Je jasně patrné, že pro diagnózu plicní formy LCH je přínosnější CT vyšetření plic než prostý snímek plic. Vzhledem ke kožnímu nálezu, suspektnímu ložisku v mozkové tkáni a postižení plic u nemocné tč. probíhá léčba 2-chlorodeoxyadenosinem.
Obr. 9 a 10. CT 3D rekonstrukce vzdušných prostor plicního parenchymu nativ. CT 3D rekonstrukce vzdušných prostor ukazuje difuzní prostoupení plicního parenchymu emfyzematózními bulami velikosti 4–15 mm prakticky bez reziduální normální plicní tkáně. Bazální partie obou plicních křídel jsou prostoupeny převážně intersticiální zánětlivou infiltrací, jak ukazuje pohled z boku, soustředěnou v zadních dolních partiích plicních křídel. Závěr: Difuzní pokročilý emfyzém plic, hypostatická pneumonie v typických oblastech. CT vyšetření plic vykazuje zřetelnou převahu výpovědních schopností před prostým snímkem plic do té míry, že stojí za úvahu používat toto zobrazení na prvním místě zvláště u pacientů komplikovaných nebo ve složité klinické situaci (Popsal doc. MUDr. Petr Krupa, CSc., přednosta Kliniky zobrazovacích metod FN u sv. Anny v Brně.). 
Image 9. Prostý PA RTG snímek hrudníku nativ. Transparence plicního parenchymu vpravo apikálně a oboustranně v okolí hilů je zřetelně snížená, oboustranně zesílená interlobia, oboustranně při bazích plic naopak se transparence plicního parenchymu difuzně zvyšuje více, než bývá obvyklé. Kontury bránice jsou hladké, siny kostofrenické jsou volné. Srdce příčně uložené, nerozšířené (Popsal doc. MUDr. Petr Krupa, CSc., přednosta Kliniky zobrazovacích metod FN u sv. Anny v Brně.). 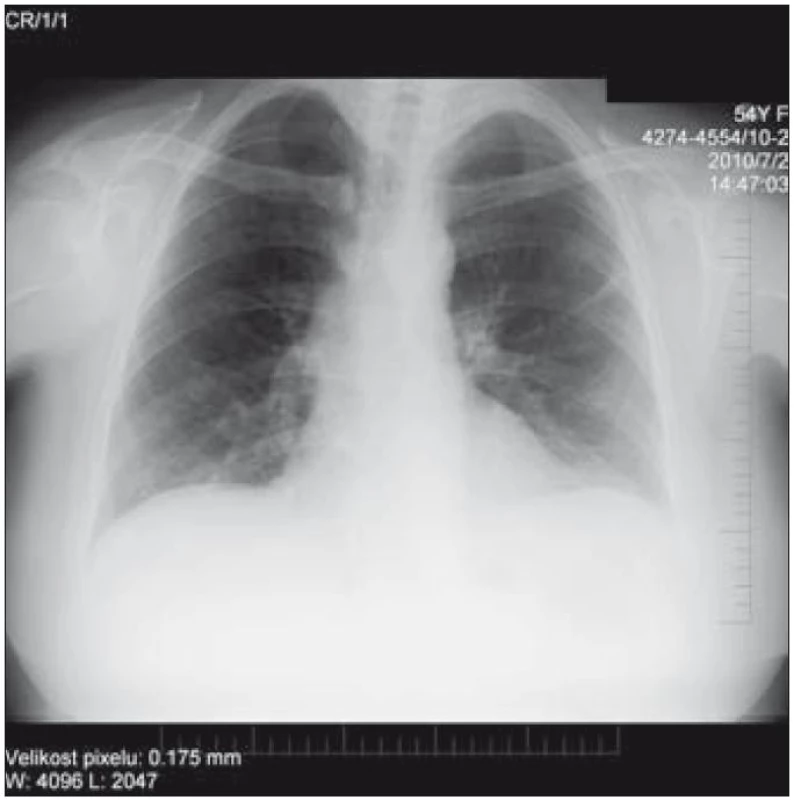
Kazuistika 2
45letý muž, jehož prvním problémem byla závažná dušnost vedoucí k hospitalizaci na interním oddělení v roce 2006. Nějakou dobu před tím mu začaly vypadávat zuby, příčina nebyla rozpoznána. Výsledkem diagnostického vyšetření byl závěr, který neodpovídal pravdě – rozedma plic. A z toho plynuly pouze kontroly u místních plicních specialistů.
Asi od června roku 2008 se přidalo mokvání a výtok z levého ucha. Nemocný byl léčen na sektorové ORL ambulanci pro urputný zánět zevního zvukovodu vpravo. V prosinci roku 2008 byl pacient přijat na klinické pracoviště s asi 4denní anamnézou závratí, bolestmi levého ucha a výtokem z ucha. Otoskopicky byl patrný téměř uzavřený zvukovod se stagnujícím zkaleným sekretem, inervace lícního nervu vlevo byla správná. Na CT pyramid byl v prosinci roku 2008 nalezen rozsáhlý destruktivní proces levé pyramidy (zastření zevního zvukovodu s destrukcí jeho dorzální stěny a s rozpadovou dutinou v processus mastoideus o průměru kolem 2 cm) (obr. 12 a 13). V prosinci roku 2008 byla provedena antromastoidektomie vlevo. Ve výčnělku byla nalezena bledá granulační tkáň, která destruuje septa a kortikalis zadní stěny zvukovodu v oblasti vchodu a v místě přechodu 2. a 3. úseku n. VII. Histologicky byla potvrzena diagnóza LCH (CD1a+, S-100+, mitotický index Ki– 67–25 %).
Image 10. CT lebeční spodiny – obraz destrukce levé pyramidy u pacienta 2. 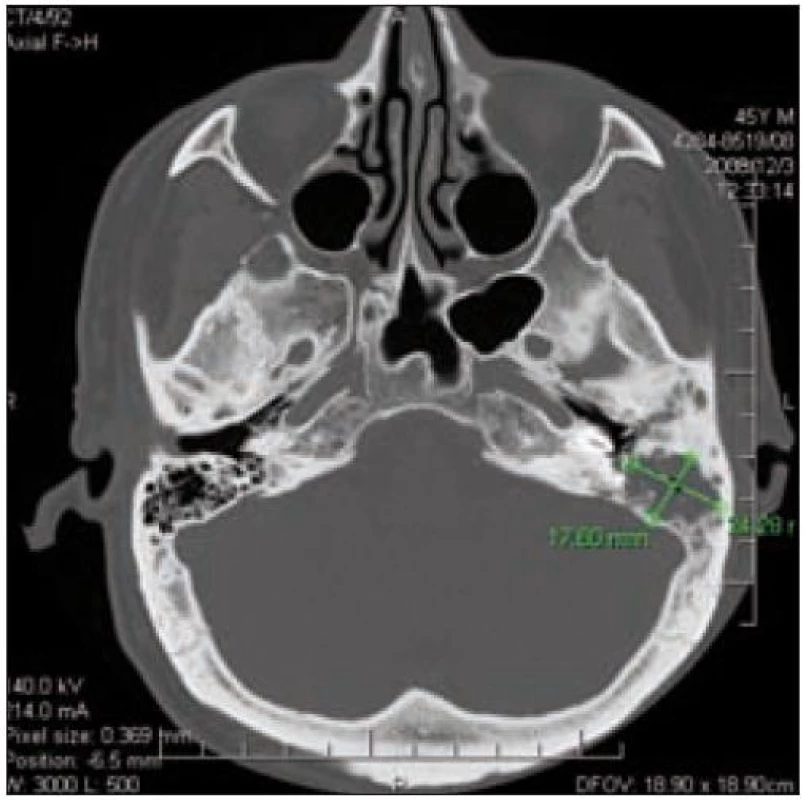
Image 11. CT lebeční spodiny – zastření zevního zvukovodu s destrukcí jeho dorzální stěny a s rozpadovou dutinou v processus mastoideus o průměru kolem 2 cm u pacienta 2. 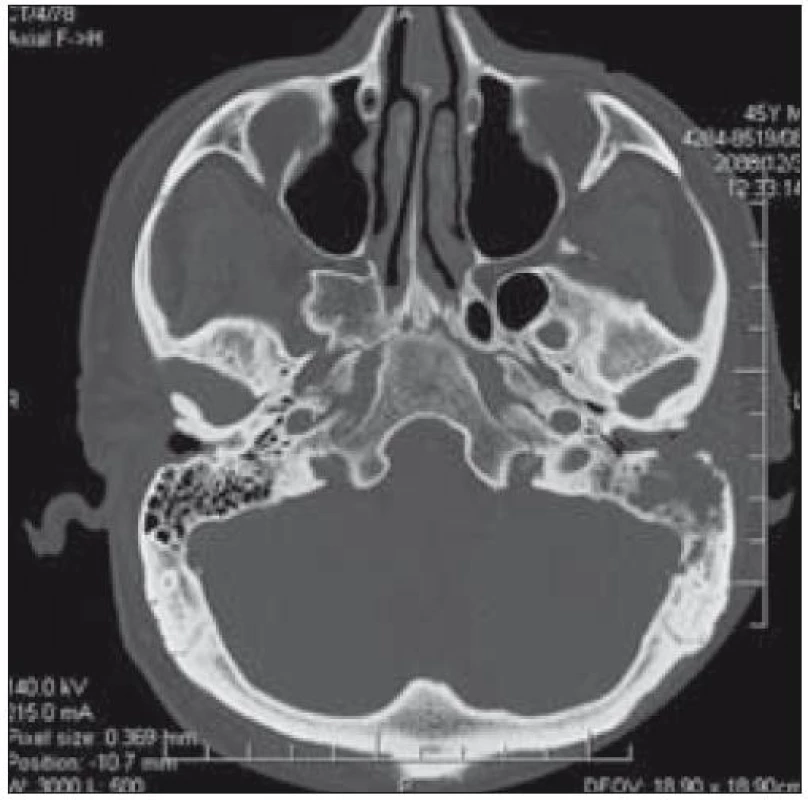
V rámci pátrání po rozsahu nemoci byla provedena další vyšetření. Při HRCT plic (březen roku 2009) bylo nalezeno difuzní postižení plicního parenchymu – mnohočetné oboustranné silnostěnné formace velikosti 3–80 mm, maximální změny byly dorzobazálně, kde cysty splývaly a byla zřetelná voštinovitá struktura plic s podílem fibrózních změn. Dále byly patrné drobné nodularity v plicním parenchymu a subpleurálně. Při scintigrafii skeletu (leden roku 2009) byly nalezeny jedině aktivity v oblasti levého processus mastoideus.
PET-CT vyšetření (březen roku 2009) potvrdilo patologické změny plicního parenchymu a hraniční konzumaci glukózy v oblasti levého středního ucha – v defektu po antromastoidektomii.
Kontrolní PET-CT vyšetření (srpen roku 2009) již neprokazovalo aktivitu v oblasti levého ucha a ubylo nodularit v plicním parenchymu.
Vzhledem k postižení 2 orgánů – plic a levé spánkové kosti – byla k léčbě použita radioterapie na oblasti levého ucha v dávce 20 Gy a celková chemoterapie leustatinem v monoterapii 5 mg/m2 5 dní po sobě.
Subjektivně se nemocný cítí dobře, sluch vlevo je uspokojivý (obr. 14), levé ucho je bez výtoku, spontánní bolesti ucha nemá. Zevně je ucho bez známek onemocnění.
Image 12. Stav sluchu po antromastoidektomii vlevo u pacienta 2. 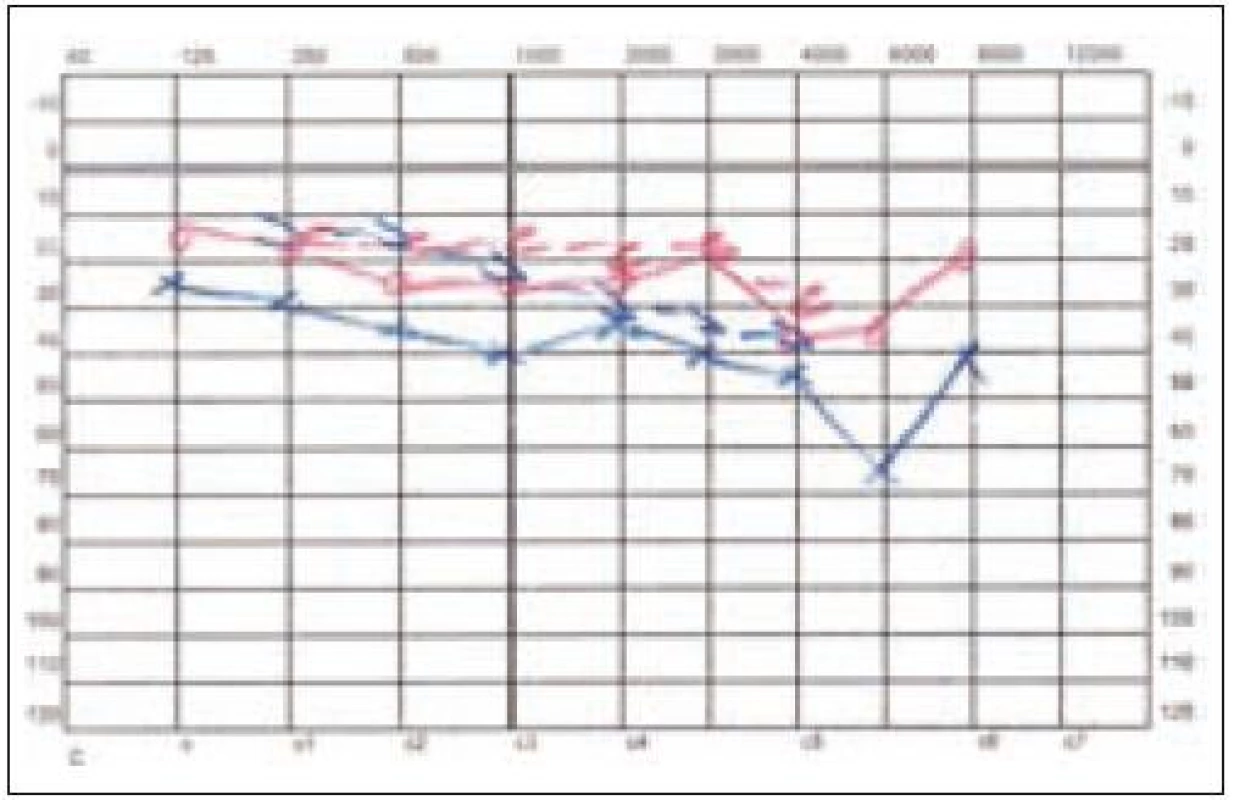
Kazuistika 3
Pacient (kuřák), narozen v roce 1974, byl zdráv až do prosince roku 2007, kdy se něj projevil diabetes insipidus. Při vyšetření na endokrinologii byl zjištěn deficit dalších hormonů, dominantně androgenů a při vyšetření na MR byla zjištěna rozšířená stopka hypofýzy (obr. 15). Při detailním rozboru anamnézy bylo zjištěno, že od roku 2007 pacient také trpí na chronický zánět zevních zvukovodů. Zánět zvukovodů dobře reagoval na ušní kapky a výplachy, sluch byl dobrý. Při otoskopickém vyšetření byl zjištěn vlevo fyziologický obraz, vpravo je kůže zvukovodu v kostěné části zarudlá, macerovaná, bubínek je celistvý bledý. Při dalším vyšetření je již kůže klidná. Při CT vyšetření pyramid nebyla nalezena destrukce kosti. Vzhledem k absenci klinických obtíží při posledním vyšetření a téměř fyziologickému nálezu probatorní excise nebyla provedena. Dalším problémem bylo svědění kůže v oblasti perianální.
Image 13. MR mozku, bobulovitě rozšířené infundibulum hypofýzy u pacienta 3. 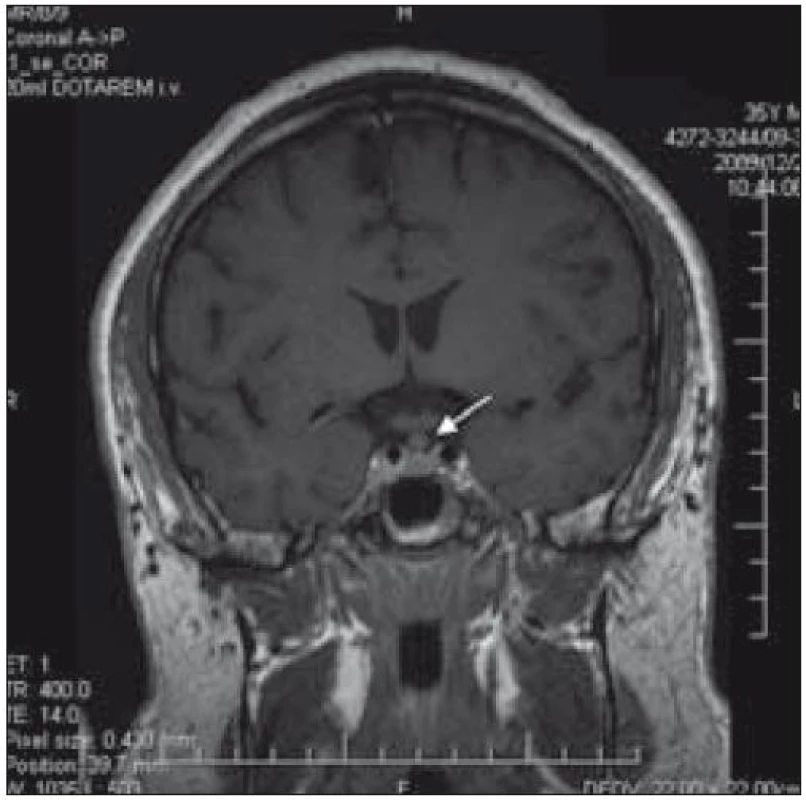
V rámci diferenciální diagnostiky patologické infiltrace v oblasti hypofýzy bylo v únoru roku 2009 provedeno PET CT s následujícím výsledkem: v oblasti plicního parenchymu byly prokázány četné drobné cystické útvary různého tvaru, velikosti od 0,8 do 0,9 cm, některé s poměrně dobře vyznačenou stěnou. Výsledkem PET-CT vyšetření byl jednoznačný průkaz patologických změn plicního parenchymu. To bylo potvrzeno HCRT vyšetřením plicního parenchymu. V dubnu roku 2009 byla provedena bronchoalveolární laváž s průkazem 10 % CD1 pozitivních elementů a pozitivity proteinu S-100. Tento nález odpovídal plicnímu postižení LCH. Jinak byla v PET obraze nalezena fyziologická kumulace radioaktivní glukózy, pouze v oblasti nosohltanu byla kumulace hraničně zvýšená.
V prosinci roku 2009 na kontrolním MR mozku bylo patrné, že stále chybí typický hyperintenzivní signál neurohypofýzy. Adenohypofýza měla normální velikost bez zřetelného ložiska. Bobulovitě rozšířené infundibulum se mírně oproti předchozí kontrole zvětšilo o 1 mm z 4,5 na 5,5 mm. Vzhledem k přání pacienta založit rodinu nebyla podána medikamentózní léčba. Pacientovi bylo vysvětleno riziko plynoucí z kouření.
Pacient je v subjektivně dobrém stavu, opakované výtoky z uší jsou minimální. Je sledován a léčen na sektorové ORL ambulanci, kde opakovaně vyjádřeno podezření na mykotickou infekci a podávána lokální antimykotika. Klinicky je vpravo zvukovod zarudlý, je zde silnější kůže, ale bez polypů, sekretu, zvukovod je normálně prostorný. Bubínek celistvý, šedý, s reflexem. Vlevo je vcelku normální nález. Vzhledem k prokázanému mírnému zvětšení infiltrátu hypofýzy byla zahájena léčba 2-chlorodeoxyadenosinem, která probíhá dosud.
Zobecnění pro diagnostiku a léčbu
LCH může být pro diagnostiku velmi obtížná – jednak proto, že se na tuto chorobu při diagnostické rozvaze nemyslí a také proto, že nemoc může nabývat velmi bizarní symptomatologie [4]. Oblast hlavy a krku bývá postižena až v 90 % případů. Příznaky v oblasti hlavy a krku mohou být vůbec prvními příznaky u multisystémových forem. Podezření na LCH by měl vzbudit dlouhodobý výtok z ucha nereagující na antibiotickou léčbu, zvětšení mízních uzlin, tumory v orbitě. Při diagnóze je třeba mít na mysli, že multisystémová LCH se může vyskytnout u dospělých osob s osteolytickými lézemi lebky, které jsou sdruženy s endokrinologickými nebo neurologickými symptomy. Je nutná týmová spolupráce s lékaři ostatních oborů a je nezbytný komplexní pohled na onemocnění. Většina autorů se shoduje na tom, že vyjma diagnostické biopsie, chirurgická léčba může nabídnout pro léčbu multisystémové LCH jen velmi málo [8,14]. Chirurgická léčba může hrát určitou roli u nemocných s diseminovanými formami, ale má pouze paliativní charakter, např. mastoidektomie u rozsáhlé destrukce pyramidy přináší úlevu od bolestí. Všeobecně je doporučován při chirurgické léčbě minimalistický přístup, poněvadž rozsáhlé resekce mohou přinést větší morbiditu než samotná choroba [8,20]. Těžiště léčby u multisystémových forem spočívá spíše v chemoterapii (vinblastin, prednison, kladribin, cílená léčba anti CD1a, anti CD207) a ozáření. U izolovaných lézí připadá v úvahu exstirpace ložiska a lokální aplikace steroidů.
doc. MUDr. Pavel Smilek, Ph.D.
www.fnusa.cz
e-mail: smilek@med.muni.cz
Doručeno do redakce: 21. 7. 2010
Sources
1. Adam Z, Balšíková K, Krejčí M et al. Centrální diabetes insipidus u dospělých osob – první příznak histiocytózy z Langerhansových buněk a Erdheimovy-Chesterovy choroby. Popis tří případů a přehled literatury. Vnitř Lék 2010; 56 : 138–148.
2. Akisada T, Harada T, Yoshihiro T et al. A case of bilateral eosinophilic granuloma in the temporal bone. Auris Nasus Larynx 1999; 26 : 343–348.
3. Allen CE, McClain KL. Langerhans cell histiocytosis: a review of past, current and future therapies. Drugs Today 2007; 43 : 627–643.
4. Aricò M, Girschikofsky M, Généreau T et al. Langerhans cell histiocytosis in adults, report from the International Registry of the Histiocyte Society. Eur J Cancer 2003; 39 : 2341–2348.
5. Bottomley WK, Gabriel SA, Corio RL et al. Histiocytosis X: Report of an oral soft tissue lesion without bony involvement. Oral Surg Oral Med Oral Pathol 1987; 63 : 228–231.
6. Perez CA, Brady LW. Principles and practice or radiation oncology. 2nd ed. Philadelphia: JB Lippincott 1992.
7. Ceci C, de Terlizzi M, Colella R et al. Langerhans cell histiocytosis in childhood: results from the Italian Cooperative AIEOP-CNR-H.X ’83 study. Med Pediatr Oncol 1993; 21 : 259–264.
8. Davis SE, Rice DH. Langerhans’ cell histiocytosis: current trends and the role of the head and neck surgeon. Ear Nose Throat J 2004; 83 : 340–350.
9. Devaney KO, Putzi MJ, Ferlito A et al. Head and neck Langerhans cell histiocytosis. Ann Otol Rhinol Laryngol 1997; 106 : 526–532.
10. Fradis M, Podoshin J, Ben-David J et al. Eosinophilic granuloma of the temporal bone. J Laryngol Otol 1985; 99 : 475–479.
11. Gianotti F, Caputo R. Histiocytic syndromes: a review. J Am Acad Dermatol 1985; 13 : 383–404.
12. Greenberger JS, Rocker AC, Vawter G et al. Results of treatment of 127 patients with systemic histiocytosis. Medicine 1981; 60 : 311–338.
13. Hudson WR, Kenan PD. Otologic manifestations of histiocytosis X. Laryngoscope 1969; 79 : 678–693.
14. Irving RM, Broadbent V, Jones NS. Langerhans’ cell histiocytosis in childhood: management of head and neck manifestations. Laryngoscope 1994; 104 : 67–70.
15. Ishii E, Matsuzaki A, Okamura J et al. Treatment of Langerhans cell histiocytosis in children with etoposide. Am J Clin Oncol 1992; 15 : 515–517.
16. Ben-Ezra JM, Koo CH. Langerhans’ cell histiocytosis and malignancies of the M-PIRE system. Am J Clin Pathol 1993; 99 : 464–471.
17. García de Marcos JA, Dean Ferrer A, Alamillos Grandos F et al. Langerhans cell histiocytosis in the maxillofacial area in adults. Report of three cases. Med Oral Pathl Oral Cir Bucal 2007; 12: E145–E150.
18. Mottl H, Mráček J, Kabelka Z et al. Histiocytóza z Langerhansových buněk u dětí. Čs Pediat 1992; 47 : 530–533.
19. Najbrt V. Příspěvek k léčbě Histiocytózy X u dětí. Česk Dermatol 1978; 53 : 24–27.
20. Nicollas R, Rome A, Belaïch H et al. Head and neck manifestation and prognosis of Langerhans’ cell histiocytosis in children. Int J Pediatr Otorhinolaryngol 2010; 74 : 669–673.
21. O’Hare TJ. Granulomaouts and Lymphoproliferative Diseases of the Head and Neck. In: Thawley SE, Panje WR, Batsakis JG et al (eds). Comprehensive management of head and neck tumors. Philadelphia: W.B. Saunders company 1999 : 1931–1981.
22. Ornvold K, Nielsen MH, Caluse N. Disseminated histiocytosis X. Acta Path Microbiol Immunol Scand 1985; 93 : 311–316.
23. Satter EK, High WA. Langerhans cell histiocytosis: a review of the current recommendations of the Histiocyte Society. Pediatr Dermatol 2008; 25 : 291–295.
24. Sawamura M, Yamaguchi S, Marayama Ket al. Cyclosporine therapy for Langerhans cell histiocytosis. Br J Haematol 1993; 83 : 178–179.
25. Scolozzi P, Lombardi T, Monnier P et al. Multisystem Langerhans’ cell histiocytosis (Hand-Schüller-Christian disease) in an adult: a case report and review of the literature. Eur Arch Otorhinolaryngol 2004; 261 : 326–330.
26. Smith RJ, Evans JN. Head and neck manifestations of histiocytosis X. Laryngoscope 1984; 94 : 395–399.
27. Straka JA, Caparosa RJ. Eosinophilic granuloma of the temporal bone. Laryngoscope 1972; 82 : 41–44.
28. Tantiwongkosi B, Goske MJ, Steele M. Congenital solid neck mass: a unique presentation of Langerhans cell histiocytosis. Pediatr Radiol 2008; 38 : 575–578.
29. Tazi A, Bonay M, Grandsaigne M et al. Surface phenotype of Langerhans cells and lymphocytes in granulomatous lesions from patients with pulmonary histiocytosis X. Am Rev Respir Dis 1993; 147 : 1531–1536.
30. Toohill RJ, Kidder TM, Eby LG. Eosinophilic granuloma of the temporal bone. Laryngoscope 1973; 83 : 877–889.
31. Vincent T, De Vita H Jr. Cancer, principles and practice of Oncology. 3rd ed. Philadelphia: J.B. Lippincott company 1989.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2010 Issue Supplementum 2-
All articles in this issue
- Postižení CNS histiocytózou z Langerhansových buněk a Erdheimovou-Chesterovou nemocí. Přínos PET-CT vyšetření pro diagnostiku a vyhodnocení léčebné odpovědi
- Postižení plic u pacientů s multiorgánovou formou histiocytózy z Langerhansových buněk. Popis 8 pacientů a přehled literatury
- Přínos PET-CT pro diagnostiku a sledování plicní formy histiocytózy z Langerhansových buněk
- Přehled léčby histiocytózy z Langerhansových buněk u osob dospělého věku
- Použití kladribinu v první linii léčby multifokální anebo multiorgánové formy histiocytózy z Langerhansových buněk u dospělých osob
- Radioterapie histiocytózy z Langerhansových buněk
- Hemofagocytující lymfohistiocytóza
- Erdheimova-Chesterova nemoc v obrazech
- Nekrobiotický xantogranulom – vzácná kožní komplikace u nemocného s mnohočetným myelomem
- Leukemie z dendritických buněk CD4+56+, typ DC2
- Systémová mastocytóza
- Představení histiocytárních chorob, o nichž pojednává toto supplementum časopisu Vnitřní lékařství
- Histiocytóza z Langerhansových buněkz pohledu patologa
- Diagnostická patológia non-Langerhansových histiocytóz
- Histiocytóza z Langerhansových buněk u dětí a dospívajících
- Granulomatóza z Langerhansových buněk
- Projevy histocytózy z Langerhansových buněk v ORL oblasti
- Projevy histiocytózy z Langerhansových buněk v orofaciální oblasti
- Histiocytóza z Langerhansových buněk – kožní aspekty onemocnění
- Histiocytóza z Langerhansových buněk u dospělých
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Hemofagocytující lymfohistiocytóza
- Erdheimova-Chesterova nemoc v obrazech
- Systémová mastocytóza
- Histiocytóza z Langerhansových buněk u dětí a dospívajících
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

