-
Medical journals
- Career
Vyšetření taktilních poruch u diabetiků a spolupráce s neurologem
Authors: A. Jirkovská; P. Bouček
Authors‘ workplace: Centrum diabetologie Institutu klinické a experimentální medicíny Praha, přednostka prof. MUDr. Terezie Pelikánová, DrSc.
Published in: Vnitř Lék 2007; 53(5): 489-494
Category:
Overview
Vyšetření poruch senzorických funkcí může být obtížné jak pro lékaře, tak pro pacienta, protože subjektivní pocity jsou zavádějící a neodrážejí závažnost neurologického postižení. Senzorické testy poskytují objektivní výsledky měření, které mohou být srovnány s normálními hodnotami a umožňují určit stupeň závažnosti neuropatie. Vyšetření senzorických funkcí na nohou u diabetiků je nezbytné, protože jejich ztráta je hlavním rizikovým faktorem pro ulcerace. Toto vyšetření zahrnuje testování vibračního čití ladičkou nebo biothesiometrem a testování povrchového čití monofilamenty. Podrobnějším vyšetřením je testování prahu citlivosti na proud pomocí různých modelů neurometru, který umožňuje vyšetření všech 3 hlavních skupin senzorických nervových vláken - Aβ (velkých myelinizovaných), Aδ (malých myelinizovaných) a C (nemyelinizovaných). V naší studii jsme hodnotili rozdíly mezi rutinní diagnostikou polyneuropatie v diabetologických ambulancích a vyšetřením biothesiometrem a monofilamenty a zjistili jsme, že pacienti s těžkou polyneuropatií diagnostikovanou neinvazivním semikvantitativním vyšetřením měli diagnostikovanou neuropatii v ambulancích pouze v 54 %, což prokazuje nutnost rozšíření neinvazivních vyšetření v ambulancích. Neuropathis Disability Score (NDS) hodnotí celkově neurologické funkce, je ale časově náročnější než jednoduché senzorické testy. Perspektivní se jeví selfmonitoring neuropatie s rizikem diabetické nohy pacientem specielním diagnostickým testem (Neuropad). Diabetolog se obrací na neurologa především při diferenciální diagnostice neuropatie, při léčbě bolestivých forem a klasifikaci závažnosti postižení.
Klíčová slova:
diabetická neuropatie - syndrom diabetické nohy - neinvazivní vyšetřeníÚvod
Diabetická neuropatie je definována jako „přítomnost symptomů a/nebo známek periferní nervové dysfunkce u diabetiků po vyloučení jiných příčin“ [1]. Dále může být diabetická neuropatie charakterizována podle klinické manifestace, nejčastěji používaná klasifikace rozděluje diabetickou neuropatii do následujících skupin [2]:
Generalizovaná symetrická polyneuropatie
- akutní senzorická
- chronická senzomotorická
- autonomní
Fokální a multifokální neuropatie
- kraniální
- trunkální
Fokální končetinové neuropatie (včetně úžinových syndromů)
- proximální motorická (amyotrofie)
- koexistující chronická zánětlivá demyelinizační polyneuropatie
Chronická senzomotorická polyneuropatie a periferní autonomní neuropatie jsou známými rizikovými faktory pro syndrom diabetické nohy. Jako hlavní rizikové faktory pro rozvoj ulcerací byly ve studiích vytipovány poruchy taktilního čití, především ztráta citlivosti na bolestivé podněty a teplotu a na vibrace, tlak a dotyk. Ve studii Younga et al došlo v průběhu jednoročního sledování ke vzniku ulcerace u téměř 20 % diabetiků, kteří měli snížené vibračního čití oproti necelým 3 % ulcerací ve skupině bez významnější senzorické poruchy [3]. V rozsáhlé jednoroční prospektivní studii analyzovala rizikové faktory vzniku diabetických ulcerací i Abbottová et al - statisticky významnými prediktivními faktory byly poruchy vibračního čití, věk a hodnoty parametrů svalové síly a reflexů v rámci Michiganského skóre diabetické polyneuropatie [4].
Syndrom diabetické nohy může být jediným projevem diabetické neuropatie, aniž by byly současně přítomny neuropatické symptomy jako je např. pálení a bodání v nohou, parestezie, pocity tepla či chladu, hyperestezie. Proto nelze diagnostikovat diabetickou neuropatii pouze podle anamnézy a je bezpodmínečně nutné doplnit neurologické vyšetření, které může provádět jak orientačně diabetolog, tak podrobněji neurolog.
Spolupráce diabetologa s neurologem
Mezi nejčastější indikace vyšetření diabetika neurologem patří především dle našich zkušeností diferenciální diagnostika chronické senzomotorické neuropatie, která může mít vedle diabetu celou řadu metabolických, toxických a dalších příčin. K neurologovi by měli být odesláni také pacienti s výrazně symptomatickou formou diabetické neuropatie, která nereaguje na běžná léčebná opatření, jako je kompenzace diabetu, či na běžnou symptomatickou léčbu. Neurolog provádí podrobnou funkční klasifikaci chronické senzomotorické polyneuropatie na základě snížení reflexů, vyšetření ladičkou, vyšetření kožního čití a klinických známek svalové hypotonie, poruchy polohocitu apod. [5].
V neposlední řadě je nezbytné neurologické vyšetření specialistou při diferenciální diagnostice jiných forem diabetické neuropatie než chronické senzomotorické polyneuropatie. Např. při kraniálních neuropatiích mívají pacienti závažné příznaky jako diplopii, strabizmus, ptózu víček či neuralgii trigeminu nebo parézu facialis a je nutné je odlišit např. od cévní etiologie či ložiskového intrakraniálního procesu, torakolumbální neuropatie je nutné diferenciálně diagnosticky odlišit např. od vertebrogenní etiologie. Proximální motorické neuropatie bývají doprovázené často amyotrofií a těžkou kachexií a je bezpodmínečně nutné stanovit správnou diagnózu. U úžinových neuropatií je třeba doplnit elektromyografické vyšetření a racionálně indikovat chirurgickou léčbu, což je opět vhodné ponechat v rukou zkušeného neurologa.
V případě diagnostiky těžší chronické senzomotorické neuropatie, která je riziková pro syndrom diabetické nohy, ale většinou postačí orientační semikvantitativní vyšetření poruch taktilního čití, které může provést sám diabetolog v diabetologické nebo podiatrické ambulanci.
Patofyziologie kožních smyslových orgánů pro vnímání mechanické stimulace
Stimulace kůže dotykem nebo tlakem, teplem nebo chladem a bolestí je vnímána pomocí kožních smyslových orgánů, mezi než patří volná nervová zakončení, rychle se adaptující mechanoreceptory (rozšířená nervová zakončení, např. Ruffiniho zakončení, Merkelovy disky) a pomalu se adaptující mechanoreceptory (opouzdřená nervová zakončení, např. Meissnerova tělíska, Paciniho tělíska, Krauseho tělíska). V aferentních neuronech, jejichž buněčná těla bývají v gangliích zadních kořenů míšních nebo v gangliích hlavových neuronů, se vyskytují různé typy nervových vláken vedoucích podněty z kožních receptorů, jejichž přehled ukazuje tab. 1.
Tzv. C-vláknová polyneuropatie [7] patří k časným známkám diabetické neuropatie, protože nemyelinizovaná tenká vlákny mohou být náchylná k metabolickému poškození. Tato vlákny jsou spolu s Aδ vlákny zodpovědná za aferentní podněty v rámci protektivního čití. Zprostředkují nejen ochranu proti poranění (tepelné poškození, bolest), ale vedou také eferentní autonomní podněty do svalových buněk a žláz s vnitřní sekrecí. „Nebolestivá neuropatie“ z poruchy C-vláken je proto nebezpečná nejen z hlediska syndromu diabetické nohy, ale i z hlediska dalších projevů autonomní neuropatie. Zajímavá je koncepce obousměrné signální cesty mezi centrální a periferní nervovou soustavou a imunitním a endokrinním systémem, do které jsou zapojena tenká vlákna a neuromediátory aktivující specifické buněčné receptory a ovlivňující hojení ran.
Orientační vyšetření taktilních poruch na dolních končetinách diabetiků
K vyšetření diabetické neuropatie se nejvíce doporučují kvantitativní senzorické testy zaměřené na povrchové a hluboké čití [1,8-10]. Psychofyzikální kvantitativní senzorické testy mají větší variabilitu než elektrofyziologické testy, jsou ale dobře použitelné v ambulantní praxi. Elektrofyziologické testy (např. hodnocení rychlosti vedení nervem) jsou považovány za zlatý standard pro diagnostiku periferní neuropatie, avšak pro screening ztráty protektivního čití, tzn. určitého stupně neuropatie, který představuje zvýšené riziko syndromu diabetické nohy, jsou vhodnější kvantitativní senzorické testy [11].
Mezi nejpoužívanější kvantitativní senzorické testy patří vyšetření:
- prahu hluboké kožní citlivosti (vibrační práh - vibration pressure threshold - VPT) - testuje se biothesiometrem nebo ladičkou, předchází často abnormalitám reflexů, lehkého dotyku i propriorecepce,
- prahu povrchové kožní citlivosti (lehký dotyk - cutaneous pressure perception threshold) - testuje se vlákny normované síly (monofilamenty). Jinou možností vyšetření je diskriminace dvou bodů (ostrý, tupý) - pozitivní nález je při méně než 6 správných odpovědích z 10,
- prahu citlivosti na teplo (thermal perception threshold ) - porucha se diagnostikuje při nerozeznání rozdílu 10 stupňů, je velmi variabilní, měl by svědčit pro počínající poškození a diferenciaci bolestivé a nebolestivé neuropatie,
- prahu citlivosti na proud (current perception threshold - CPT) - testuje se neurometrem, podle frekvence proudu dochází k selektivní stimulaci silných myelinizovaných vláken (vibrace, propriorecepce) nebo tenkých myelinizovaných i nemyelinizovaných vláken (bolest a teplota).
Povrchové čití vyšetřujeme nejčastěji kvantitativně monofilamenty. K diagnostice těžší neuropatie, rizikové pro syndrom diabetické nohy, používáme 10 g monofilamenta (označená 5,07). Dotýkáme se jimi chodidla v místech předpokládaných ulcerací, nejčastěji pod palcem, 1. a 5. metatarzofalangeálním kloubem (obr. 1). Protektivní čití na noze je porušeno, pokud pacient necítí alespoň 2 ze 3 testovaných míst na každé noze, tento pacient je rizikový pro vznik ulcerace [1]. V některých případech se testují 4 místa (plantární plocha palce a plochy pod hlavičkami 1., případně i 3. a 5. metatarzu) a k průkazu přítomnosti neuropatie obvykle postačuje porucha čití v jediném z nich, i když s počtem míst s prokázanou poruchou vnímání tlaku stoupá senzitivita i specifita vyšetření [11].
Image 1. Vyšetření povrchového taktilního čití monofilamenty. 
Hluboké vibrační čití testujeme nejčastěji ladičkou (128 Hz) nebo tzv. biothesiometrem (obr. 2). Místem testování je nejčastěji dorzální strana palce nohy pod nehtovým lůžkem, v blízkosti periostu. Pacient má rizikovou neuropatii, pokud při vyšetření biothesiometrem má VPT nad 25 V a pokud při vyšetření ladičkou 128 Hz necítí správně 2 ze 3 aplikací (abnormální odpovědí je ztráta vnímání vibrací pacientem v době, kdy jsou ještě vnímány vyšetřujícím). Graduovaná ladička Rydel-Seiffer c 64 Hz umožňuje i semikvantitativní hodnocení vibračního čití. Na osmibodové stupnici závaží na hrotech ladičky lze odečíst práh vibračního čití jako místo styku dvou virtuálních trojúhelníků v okamžiku, kdy vyšetřovaná osob hlásí konec vnímání vibrací. Úroveň normálních hodnot prahu vibračního čití je závislá na věku. Testování se obvykle provádí na dorzu palce nohy a vnitřním kotníku. I když měření vibračního čití biothesiometrem a měření povrchového čití monofilamenty patří k nejčastěji doporučovaným testům pro posouzení taktilního čití z hlediska rizika syndromu diabetické nohy [10,12], dosud není úplná jednota v definici prahových hodnot obou vyšetření [13-16].
Image 2. Vyšetření vibračního čití biothesiometrem. 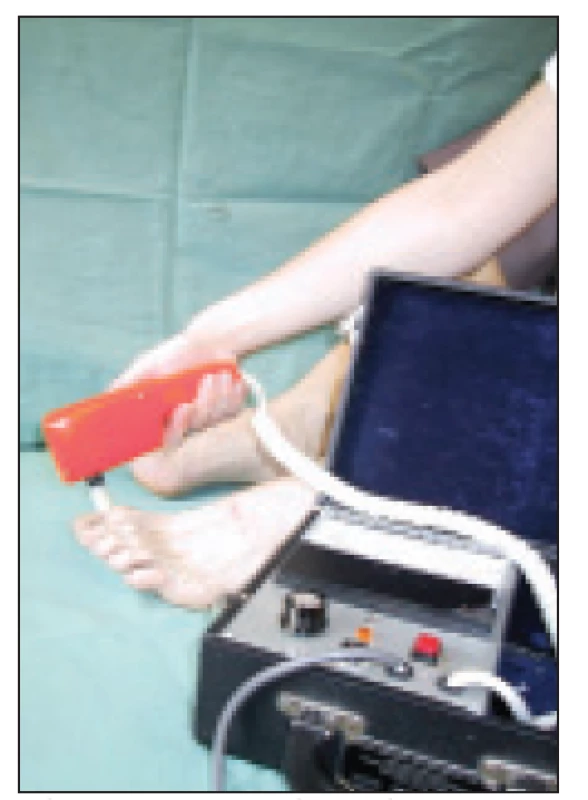
Pomocí vyšetření monofilamenty byly identifikovány osoby se zvýšený rizikem vzniku nožních ulcerací ve 3 prospektivních studiích [17-19] se specificitou 34 - 86 % a senzitivitou 66 - 91 %. Při vyšetření biothesiometrem měli osoby s vibračním prahem nad 25 V 2,2násobné riziko vzniku ulcerace na nohou během 4 let, senzitivita tohoto vyšetření byla 83 % a specificita 63 % [3,20]. Vyšetření vibračního čití pomocí ladičky závisí na zkušenostech vyšetřujícího, obvykle má menší prediktivní hodnotu pro ulcerace než vyšetření monofilamenty [11].
Vlastní zkušenosti s orientačním neurologickým vyšetřením u diabetiků
Orientační neurologické vyšetření monofilamenty a biothesiometrem jsme sami otestovali při screeningové studii u 322 osob z diabetologických ambulancí v modelové oblasti Prahy [21,22]. Objektivní vyšetření, které prováděly zaškolené edukační sestry, spočívalo ve vyšetření povrchového čití monofilamenty a hlubokého vibračního čití biothesiometrem. Z celkového počtu 322 vyšetřených osob mělo diabetickou nohu 44 osob (14 %) a vysoké riziko diabetické nohy 162 osob (50 %). Pacienti se syndromem diabetické nohy měli ve srovnání s pacienty bez syndromu diabetické nohy signifikantně častěji VPT nad 30 V (74 vs 47 %, p < 0,001) i více než 3 necitlivé body při testování monofilamenty (84 vs 40 %, p < 0,001). Práh vibračního čití nad 30 V se jevil v naší studii výhodnější než práh 25 V, protože měl mírně vyšší specificitu pro určení rizika syndromu diabetické nohy (55 vs 44,2), zatímco senzitivita byla v obou případech vysoká (84 a 82 %). Zatímco Young ve své studii doporučuje používat práh 25 V [34], Vileikyte uvádí pro tento práh rovněž nižší specificitu [23].
Při srovnání neinvazivních vyšetření neuropatie s údaji o neuropatii v dokumentaci jsme zjistili, že ze 196 pacientů se závažnou neuropatií (VPT nad 30 V a/nebo necitlivost k monofilamentům) byla v dokumentaci uvedena neuropatie pouze u 54 % osob. Naše studie tak potvrdila nutnost provádět orientační vyšetření neuropatie pomocí standardizovaných kvantitativních senzorických testů přímo v diabetologických ambulancích.
Další vyšetření neuropatie u pacientů z hlediska rizika syndromu diabetické nohy
Diagnostické skórovací systémy jsou založené na souboru klinických projevů. Neuropathy Disability Score (NDS) a jeho různé modifikace jsou využívány ke klinickému výzkumu, např. k hodnocení efektů různých typů léčebných intervencí [24,25]. Vyšetřuje se:
- kotníkový reflex,
- vibrace pomocí ladičky 128 Hz,
- bolestivost špendlíkem,
- teplota (chladná ladička).
Hodnocení vyšetření se provádí na každé noze a boduje se: reflex - normální = 0, vyvolané jen s posilovacím manévrem = 1, nepřítomen = 2; ostatní vyšetření - normální = 0, redukováno/nepřítomno = 1. Součet bodů: maximum 10 bodů, skóre nad 6 = těžká neuropatie, odpovídá VPT nad 25 V, skóre nad 3 se hodnotí někdy jako významná neuropatie. Vyšetření NDS může provádět i vyškolená osoba bez neurologické specializace.
Vyšetření neuropatie pomocí neurometru CPT/C
Jedná se o moderní přístroj, který automaticky určuje selektivně práh vedení nervem (Nerve Conduction Threshold - sNCT) na podkladě CPT. Neuroselektivní elektrické stimuly objektivně hodnotí jednotlivá nervová vlákna z hlediska vedení vzruchu a funkční integrity. Pomocí vyšetření neurometrem je možné provádět diferenciální diagnostiku axonální a demyelinizační polyneuropatie, radikulopatie, kompresivní neuropatie i diferenciální diagnostiku postižení velkých a malých vláken (především myelinizovaných velkých Aβ a malých Aδ a nemyelinizovaných C). Dále je možná i klinická monitorace závažnosti neuropatie a monitorace efektu terapie. Předností vyšetření tímto neurometrem je malá variabilita ve srovnání s biothesiometrem a menší časová náročnost ve srovnání s měřením termálního prahu a EMG. Manipulace s přístrojem je poměrně jednoduché a není nutné, aby ji prováděli pouze specialisté [26].
Vyšetření neuropatie pomocí Neuropadu
Neuropad je novější test pro sudomotorické dysfunkce na nohou. Porucha pocení jako známka autonomní neuropatie může být jedním ze základních patogenetických faktorů vedoucích k diabetickým ulceracím i Charcotově osteoartropatii [9]. V podstatě se jedná o specielní náplast napuštěnou činidlem na bázi kovů reagujícím změnou zbarvení na pocení nohou (dochází ke změně zbarvení chloridu kobaltu z modré na růžovou po absorpci vody). Po 10 min aplikace náplasti na chodidlo pod bříško palce nohy dochází za normálních okolností ke změně zbarvení náplasti z modré na růžovou, patologickým nálezem je přetrvávající modré zbarvení nebo skvrnité modrorůžové zbarvení. Je nutné dodržet všechny podmínky testu dle návodu, aby nedocházelo k jeho zkreslení artefakty. Neuropad má sloužit především samostatné kontrole pacientů pro učení rizika syndromu diabetické nohy [27]. Otázkou zůstává, v jakém stadiu je možné pomocí Neuropadu identifikovat nejen sudomotorickou poruchu a riziko syndromu diabetické nohy, ale také chronickou senzomotorickou polyneuropatii. Nedávná práce Papanase et al [28] se snaží prokázat shodu vyšetření Neuropadem s Michiganským klasifikačním systémem neuropatie na podkladě odlišné doby, v níž dochází ke kompletní barevné změně Neuropadu, v různých stadiích neuropatie. V jiné práci Didangelos et al [29] prokazují shodu vyšetření Neuropadem s diagnostikou neuropatie pomocí biothesiometru, monofilament i Michiganského skóre, která byla dobrá (shoda v 70 - 90 %). Je však třeba podotknout, že pro průkaz využití Neuropadu k detekci neuropatie dosud chybí větší publikované studie, zatímco pro senzorické testy již řada studií srovnávající jednotlivé metody existuje. Např. z hlediska detekce pacientů s neuropatickými ulceracemi [30] byla zjištěna nejvyšší senzitivita a specificita pro vyšetření biothesiometrem, a to 79,5 a 91, dále pro NDS (84,7 a 41,7) a pro testování monofilamenty (77,9 a 43,1) a obdobně i pro testování tepelného prahu (87,2 a 36,1).
Závěr
Zjištění taktilních poruch patří k základním vyšetřením pacienta s diabetem. Orientačně by je měl provádět diabetolog v ambulanci, především pro určení rizika syndromu diabetické nohy, které je často podhodnoceno. Je možné použít kvantitativní senzorické testy - testování vibračního čití ladičkou nebo biothesiometrem a povrchového taktilního čití monofilamenty i zjišťování komplexního neuropatic disability score. Přesnější diagnostika je v rukou neurologa, zejména se zaměřením na diferenciální diagnostiku neuropatií a terapii výrazně symptomatických pacientů. Mezi preciznější metody diagnostiky taktilních poruch patří vyšetření neurometrem s možností diferenciace postižení jednotlivých vláken. Aktuální je i selfmonitoring pacientů z hlediska testování periferní sudomotorické neuropatie pomocí Neuropadu a určení rizika syndromu diabetické nohy, chybí však větší publikované studie o vztahu tohoto testu k včasné diagnostice chronické periferní neuropatie.
doc. MUDr. Alexandra Jirkovská,CSc.
www.ikem.cz
e-mail : alji@ikem.cz
Doručeno do redakce: 31. 1. 2007
Sources
1. Bakker K (ed), Mezinárodní pracovní skupina pro syndrom diabetické nohy. Syndrom diabetické nohy. Mezinárodní konsenzus. Praha: Galén 2000.
2. Boulton A, Vinik A, Arezzo J et al. Diabetic neuropathies. A statement by the American Diabetes Association. Diabetes Care 2005; 28 : 956-962.
3. Young MJ, Veves A, Breddy JL et al. The prediction of diabetic neuropathic foot ulceration using vibration perception thresholds: a prospective study. Diabetes Care 1994; 17 : 557-560.
4. Abbott CA, Vileykite L, Williamson S et al. Multicentre study of the incidence of and the predictive factors for diabetic neuropathic foot ulcers. Diabetes Care 1998; 21 : 1071-1075.
5. Mazárová V, Bouček P. Diabetická neuropatie. In: Bartoš V, Pelikánová T (eds). Praktická diabetologie. 3. ed. Praha: Maxdorf 2003 : 259-270.
6. Ganong WF. Přehled lékařské fyziologie. Praha: H+H 1995.
7. Quattrini C, Jeziorska M, Malik R. Small fiber neuropathy in diabetes: clinical consequence and assessment. Int J Low Extrem Wounds 2004; 3 : 16-21.
8. American Diabetes Association: Preventive foot care in people with diabetes. Diabetes Care 2000; 23(Suppl 1): 55-56.
9. Jirkovská A et al. Syndrom diabetické nohy. Praha: Maxdorf 2006.
10. Young M, Jones G. Diabetic neuropathy: symptoms, signs and assessment. Boulton AJM, Carnforth H (eds). Diabetic neuropathy. Carnforth (UK): Marius Press 1997 : 41-61.
11. Singh N, Armstrong DG, Lipsky BA. Preventing foot ulcers in patients with diabetes. J Am Med Assoc 2005; 293 : 217-227.
12. American Diabetes Association: Consensus statement: diabetic neuropathy. Standardized measures in diabetic neuropathy. Diabetes Care 1995; 18(Suppl 1): 53-82.
13. Young MJ, Boulton AJM, Macleod AF et al. A multicentre study of the prevalence of diabetic peripheral neuropathy in the United Kingdom hospital clinic population. Diabetologia 1993; 36 : 150-154.
14. Bloom S, Till S, Sonksen P et al. Use of biothesiometer to measure individual vibration threshold and their variation in 519 non-diabetic subjects. Brit Med J 1984; 288 : 1793-1795.
15. Williams G, Jaswinder SG, Aber V et al. Variability in vibration perception threshold among sites: a potential source of error in biothesiometry. Brit Med J 1988; 296 : 233-235.
16. Neely MJ, Boyko EJ, Ahroni JH et al. The independent contributions of diabetic neuropathy and vasculopathy in foot ulceration. Diabetes Care 1995; 18 : 216-219.
17. Boyko EJ, Ahroni JH, Stensel V et al. A prospective study of risk factors for diabetic foot ulcer: the Seattle Diabetic Foot Study. Diabetes Care 1999; 22 : 1036-1042.
18. Rith-Najarian S, Stolusky T, Gohdes D. Identifying diabetic patients at high risk for lower-extremity amputation in a primary health care setting. Diabetes Care 1992; 15 : 1386-1389.
19. Pham H, Armstrong DG, Harvey C et al. Screening techniques to identify the at risk patients for developing diabetic foot ulcers in a prospective multicenter trial. Diabetes Care 2000; 23 : 606-611.
20. Mason J, O´Keeffe C, Hutchionson A et al. A systematic review of foot ulcer in patients with type 2 diabetes mellitus, II: treatment. Diabet Med 1999; 16 : 889-909.
21. Jirkovská A, Wosková V, Bartoš V et al. Význam neinvazivní diagnostiky angiopatie a neuropatie při screeningovém vyšetření syndromu diabetické nohy. Vnitř Lék 1998; 44 : 269-273.
22. Jirkovská A, Bouček P, Wosková V et al. Identification of patients at risk for diabetic foot: a comparison of standardized noninvasive testing with routine practice at community diabetes clinics. J Diabet Complications 2001; 16 : 63-68.
23. Vileikyte L, Hutchings G, Hollis S et al. The tactile circumferential discriminator. A new, simple screening device to identify diabetic patients at risk of foot ulceration. Diabetes Care 1997; 20 : 623-626.
24. Grant IA, O’Brien P, Dyck PJ. Neuropathy tests and normative results. In: Dyck P, Thomas P (eds). Diabetic neuropathy. 2nd ed. Philadelphia: WB Saunders 1999 : 123-141.
25. Boulton A, Malik R, Arezzo J et al. Diabetic somatic neuropathies. Diabetes Care 2004; 27 : 1458-1486.
26. Masson E, Boulton A. The Neurometer: Validation and comparison with conventional tests for diabetic neuropathy. Diabet Med 1991; 8 (zvláštní číslo): S63-S66.
27. Manes C, Mikoudi K, Sossidou E et al. Evaluation of new indicator plaster in identifying diabetic patients at risk of foot ulceration. Diabetologia 2004; 47 (Suppl 1): A376.
28. Papanas N, Giassakis G, Papatheodorou K et al. Use of the new indicator test (Neuropad) for the assessment of the staged severity of neuropathy in type 2 diabetic patients. Exp Clin Endocrinol Diabetes. 2007;115(1): 58-61.
29. Didangelos T, Zografou I, Papageorgiou A et al. Validation of new diabetic autonomic neuropathy bedside test (plaster) vs. the MNSI, monofilament of 10 g test and biothesiometer. Diabet Med 2006; 23(Suppl 4): P186.
30. Papanas N, Gries A, Maltezos E et al. The steel ball-bearing test: a new test for evaluating protective sensation in the diabetic foot. Diabetologia 2006; 49 : 739-743.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2007 Issue 5-
All articles in this issue
- Stručná fyziologie a patofyziologie smyslů
- Čich a chuť diabetika
- Diabetes mellitus a kognitivní poruchy
- Vyšetření taktilních poruch u diabetiků a spolupráce s neurologem
- Diabetická oftalmopatie
- Patogeneze diabetické retinopatie
- Katarakta, glaukom a diabetes mellitus
- Chirurgická léčba diabetické retinopatie
- Farmakologická léčba diabetické retinopatie
- Zánětlivá onemocnění oka
- Tyreoidální orbitopatie a diabetes
- Percepční vady sluchu u diabetu, sluchová protetika
- Tinnitus a diabetes
- Vývoj názorů na pohybovou aktivitu u diabetika
- Pohybová léčba u pacientů s metabolickým syndromem
- Metabolický význam svalu a sport u diabetika
- Výživa diabetika při fyzické zátěži
- Úpravy terapie při pohybové aktivitě diabetika
- Zvýšená aktivita sympatiku a možnosti terapeutického ovlivnění
- Stanovení intenzity fyzické aktivity u obézních diabetiků
- Rekondiční centrum VŠTJ MEDICINA Praha - rekondice diabetika
- Rehabilitační a protetická péče o pacienty - diabetiky po amputaci končetiny
- Úvodník
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Zánětlivá onemocnění oka
- Tinnitus a diabetes
- Zvýšená aktivita sympatiku a možnosti terapeutického ovlivnění
- Čich a chuť diabetika
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career


