-
Medical journals
- Career
Specifika revmatoidní artritidy v seniorském věku
: MUDr. Jan Klán 1; MUDr. Hana Ciferská; Ph.D. 2; Prof. MUDr. Eva Topinková, CSc. 1
: Geriatrická klinika 1. LF UK a VFN, Praha 1; Revmatologický ústav, Praha 2
: Geriatrie a Gerontologie 2014, 3, č. 1: 18-24
: Review Article
Nemoci pohybového aparátu patří mezi hlavní příčiny disability ve stáří. V přehledovém článku uvádíme nové poznatky o revmatoidní artritidě se zaměřením na formu revmatoidní artritidy (RA) začínající ve vyšším věku po 65. roce života – tzv. LORA (late onset rheumatoid arthritis). Dokumentujeme často odlišný klinický obraz revmatoidní artritidy u pacientů vyššího věku, který může být také důvodem diferenciálnědiagnostických obtíží. V posledních letech došlo k výraznému pokroku v diagnostice a léčbě revmatoidní artritidy. Hlavním terapeutickým cílem je dosažení remise a předcházení vzniku nevratného postižení kloubů včasnou a účinnou terapií. Základem léčebné strategie je systémová terapie chorobu modifikujícími léky (DMARD), v posledním desetiletí se stále více uplatňuje zejména u těžkých forem revmatoidní artritidy biologická léčba.
Klíčová slova:
revmatoidní artritida – stáří – LORA – disabilita – DMARD – biologická léčbaÚvod
Revmatoidní artritida (RA) je chronické autoimunitní zánětlivé onemocnění, které primárně postihuje kloubní aparát a je charakterizované typicky symetrickou polyartritidou, u zvláště aktivního onemocnění mohou být přítomny i mimokloubní orgánové projevy(1, 2). RA má celosvětový výskyt s incidencí mezi 10–50 na 100 000 obyvatel(3). U žen bývá až 3x častější než u mužů. Typicky se onemocnění manifestuje mezi 40. až 50. rokem. U určitého počtu nemocných však dochází k primomanifestaci RA po 65. roku věku – označuje se jako revmatoidní artritida s pozdním začátkem (late onset rheumatoid arthritis – LORA), synonymum je revmatoidní artritida se začátkem ve vyšším věku (elderly onset rheumatoid arthritis – EORA)(4, 5).
Zatímco prevalence RA v dospělé populaci se pohybuje mezi 0,5–0,8 %, ve vyšších věkových skupinách (v populaci nad 60 let) se udává prevalence RA 2–3 %(5). Přesná etiopatogeneze RA není dosud plně objasněna. Etiologie onemocnění je pravděpodobně multifaktoriální. Předpokládá se určitá vrozená predispozice pro rozvoj onemocnění u nositelů některých alel HLA-DR4 nebo HLA-DR1.
Proces zánětu je pravděpodobně zahájen reakcí trimolekulárního komplexu (antigen – antigen prezentující buňka – T lymfocyt s příslušným receptorem), což vede ke stimulaci zejména Th1 lymfocytů, sekreci prozánětlivých cytokinů (interferon gama, interleukin 2) a aktivaci monocyto-makrofágového systému s následnou produkcí cytokinů (TNFalfa, interleukin 1). Účinky těchto cytokinů odpovídají za většinu patologických reakcí, které probíhají v revmatoidním kloubu.
Na vzniku a udržení zánětu se podílí autoprotilátky, jednak revmatoidní faktory (RF – protilátky namířené proti Fc části imunoglobulinu G, produkované hlavně plazmatickými buňkami v synoviální membráně), jednak jsou nově prokazovány protilátky proti filagrinu (s vyšším obsahem aminokyseliny citrulinu), jedná se o tzv. protilátky proti citrulinovaným peptidům (ACPA), které mají ve srovnání s RF vyšší specificitu(2, 6).
Klinický obraz revmatoidní artritidy a jeho odlišnosti ve vyšším věku
Průběh choroby je individuální, s exacerbacemi a remisemi, ale onemocnění je progresivní a vede k destrukci kloubů. K akutnímu začátku onemocnění dochází u 1/3 pacientů s LORA(5).
U pacientů s LORA se vyskytuje větší počet komorbidit, zejména arteriální hypertenze, ischemická choroba srdeční, diabetes mellitus, chronická onemocnění dýchacích cest, osteoporóza(7).
Zatímco u pacientů s RA se začátkem v mladším věku do 65. roku (younger onset rheumatoid arthritis – YORA) se častěji jedná o symetrickou polyartritidu s postižením drobných kloubů rukou (metakarpofalangeální, proximální interfalangeální, radiokarpální klouby) a nohou (metatarzofalangeální, proximální interfalangeální klouby), revmatoidní artritida s pozdním začátkem (LORA) začíná častěji jako monoartritida či oligoartritida (méně než 5 postižených kloubů) a postihuje spíše velké klouby (ramena, kyčle, kolena) (tab. 1)(2, 5, 8).
1. Základní odlišnosti u revmatoidní artritidy se začátkem ve vyšším věku (podle Vencovského)<sup>(2)</sup> 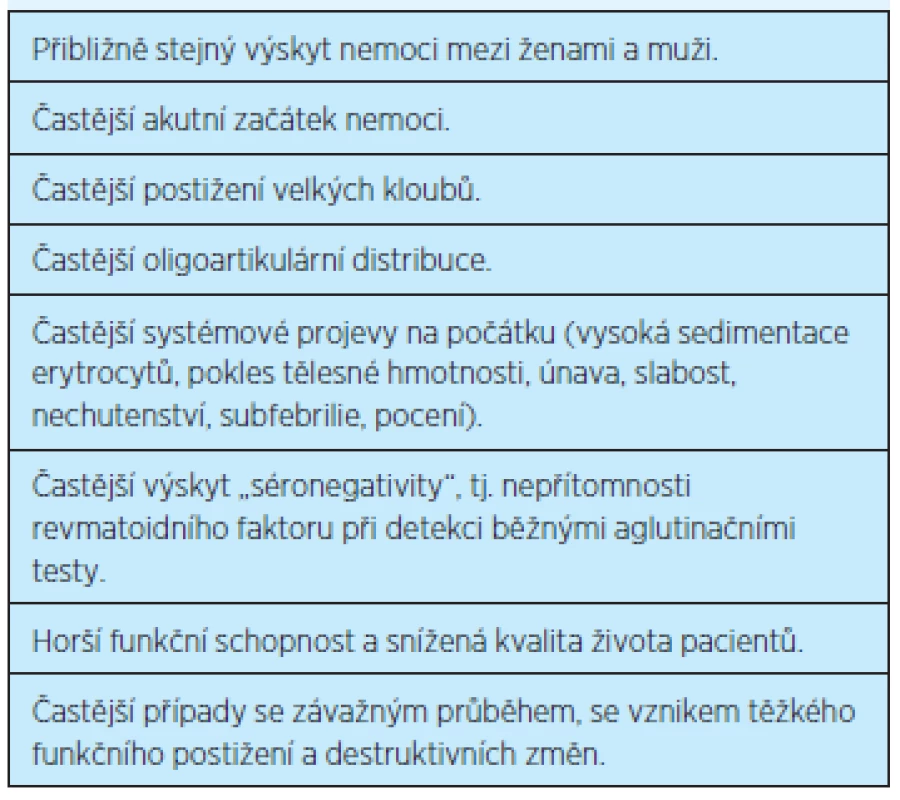
Typickou lokalizací LORA jsou ramenní klouby, kde onemocnění často začíná (postižení glenohumerálního i akromioklavikulárního kloubu), přibližně u 20 % nemocných nacházíme ruptury rotátorové manžety(2, 8). Kyčelní klouby bývají také častěji postiženy ve stáří, přičemž revmatoidní koxitida je známkou nepříznivého vývoje. V případě postižení kolenních kloubů dochází k vývoji osových deformit a flekčním kontrakturám, synoviální tekutina může z kolenního kloubu pronikat do popliteální burzy (Bakerova cysta), ruptura této cysty s vyprázdněním obsahu mezi lýtkové svaly způsobuje bolestivé zduření, což může vést k záměně s flebotrombózou. Časté bývá též postižení temporomandibulárních kloubů, které způsobuje bolesti při žvýkání (možná záměna se zubním postižením). Závažnou komplikací RA je postižení krční páteře s destrukcí atlantoaxiálního kloubu a subluxací atlasu s rizikem komprese míchy a náhlé smrti(8, 9). Kromě postižení kloubů se nemoc může projevovat i extraartikulárně s rozvojem orgánových komplikací.
V důsledku stárnutí dochází k úbytku svalové hmoty (sarkopenii), porucha mobility vede k atrofiím a svalové slabosti. Osteoporóza (zpočátku periartikulární, později difuzní) se vznikem patologických fraktur bývá ve spojení s revmatoidní artritidou a též s dlouhodobou terapií glukokortikoidy ve stáří závažnější(10).
Tendosynovitida se vyskytuje zejména v oblasti rukou a zápěstí, ruptura šlach způsobuje vznik deformit (labutí šíje, knoflíková dírka). Revmatoidní uzly vyskytující se hlavně v podkoží (lokty, drobné ruční klouby, Achillova šlacha), ale i ve vnitřních orgánech, jsou u pacientů s LORA méně časté.
V důsledku edému tkání mohou vznikat kompresivní syndromy (nejčastěji syndrom karpálního tunelu), u závažných forem RA dochází ke vzniku senzoricko-motorické neuropatie.
Z hematologických abnormalit se vyskytují nejčastěji anemie (patří mezi anemie chronických onemocnění) a trombocytóza (je výrazem aktivity RA). Snížená imunitní rezistence způsobuje zvýšené riziko k různým infektům a sekundární infekci postižených kloubů.
Plicní postižení se může projevit pleuritidou nebo intersticiální plicní fibrózou. Obávaný je rozvoj tzv. methotrexátové plíce u nemocných léčených methotrexátem(8).
Postižení srdce se nejčastěji manifestuje ve formě perikarditidy (většinou asymptomatické). Sekundární amyloidóza (AA typu) se projevuje především postižením ledvin, vyskytuje se asi u 7 % případů pokročilých stadií onemocnění RA (starší pacienti s dlouhodobým průběhem)(2, 11). Revmatoidní vaskulitida se vyskytuje obvykle u závažnějších forem RA. Typickým očním postižením u pacientů s RA je suchá keratokonjunktivitida (u 10–35 % nemocných)(6).
Diagnostika revmatoidní artritidy
U pacientů s LORA se vyskytují v laboratorních nálezech častěji vysoké hodnoty sedimentace erytrocytů (FW) a C-reaktivního proteinu (CRP), které korelují s aktivitou onemocnění. Pozitivita revmatoidního faktoru (RF) v séru není pro RA zcela specifická (výskyt pouze asi v 70 % případů), může se vyskytovat též u jiných zánětlivých revmatických onemocnění, u chronických zánětů, a dokonce také u zdravých osob (ve věku nad 70 let v 10–25 % případů)(5). U pacientů s LORA se doporučuje uvažovat jako první pozitivní titr RF 1 : 1280 v latexovém fixačním testu (u mladších pacientů je to 1 : 160). Pomocí metody ELISA je možné určit izotypy RF (IgG RF je asociován s přítomností vaskulitidy, IgA RF s vývojem kostních erozí)(2, 8). Antiperinukleární faktory (APF) a antinukleární faktory (ANF) zejména v časných stadiích RA bývají pozitivní až u 55 % nemocných(6).
V diagnostice RA je významné vyšetření protilátek proti citrulinovaným peptidům /proteinům (ACPA), ve srovnání s RF mají vyšší specificitu, korelují se závažností onemocnění a jejich přítomnost na počátku choroby může mít významnou prognostickou cenu(3, 11).
Pokud je přítomen kloubní výpotek, bývá sterilní se zmnoženými polynukleáry a mononukleáry. Provádí se vyšetření synoviálního výpotku cytologické, mikrobiologické a imunologické (na přítomnost RF a dalších autoprotilátek)(9). Ze zobrazovacích metod je zlatým standardem při hodnocení progrese RA rentgenové vyšetření (rtg) (tab. 2)(12).
2. Hodnocení strukturální progrese RA podle rtg (Steinbrocker)<sup>(12)</sup> 
Ultrasonografické vyšetření (USG) pomáhá k určení rozsahu postižení zejména měkkých částí, k odhalení počínajících erozí, synovitidy a k detekci výpotku v kloubech méně dostupných při fyzikálním vyšetření (kyčelní kloub). Výhodné je též užití USG při cílených punkcích a obstřicích kloubů(5, 6).
Pro časnou detekci erozí, synovitidy, otoku kostní dřeně, osteonekrózy a v případě postižení krční páteře se používá vyšetření magnetickou rezonancí (MRI)(5, 10).
Doporučená diagnostická kritéria
Klasifikační kritéria revmatoidní artritidy ACR/EULAR 2010 (ACR = American College of Rheumatology, EULAR=European League Against Rheumatism) shrnují jak rozsah kloubního postižení, tak laboratorní a imunologické nálezy s přihlédnutím k délce trvání onemocnění (tab. 3)(13).
3. Klasifikační kritéria RA (ACR/EULAR 2010)<sup>(13)</sup> 
Ke zhodnocení terapeutické odpovědi RA na podávanou léčbu se nejčastěji v klinické praxi využívá DAS 28 (disease activity score – 28 kloubů). Toto skóre zahrnuje počet oteklých a bolestivých kloubů z celkového počtu 28, globální hodnocení zdravotního stavu pacientem a výsledek vyšetření sedimentace erytrocytů nebo C-reaktivního proteinu.
Při hodnotě (DAS 28) > 5,1 se jedná o vysokou aktivitu RA, (DAS 28) 3,2–5,1 znamená střední aktivitu RA, (DAS 28) 2,6–3,2 značí nízkou aktivitu RA. Hodnota (DAS 28) < 2,6 je definována jako remise(14).
O úplné klinické remisi hovoříme v případě, pokud ranní ztuhlost nepřesahuje 15 minut, není únavnost, nejsou artralgie, není bolestivost palpační ani při pasivním pohybu, není nikde zduření periartikulární ani šlachových pochev, sedimentace erytrocytů < 30/h u žen a < 20/h u mužů. Remisi vylučuje přítomnost aktivní vaskulitidy, perikarditidy, pleuritidy, myozitidy, teploty a hubnutí(9).
Negativní prognostické ukazatele
Významným faktorem je také možnost lepšího vyhodnocení negativních prognostických ukazatelů průběhu RA časně se vyskytujících – pro destruktivní vývoj RA (tab. 4)(17).
4. Negativní prognostické ukazatele průběhu RA<sup>(17)</sup> 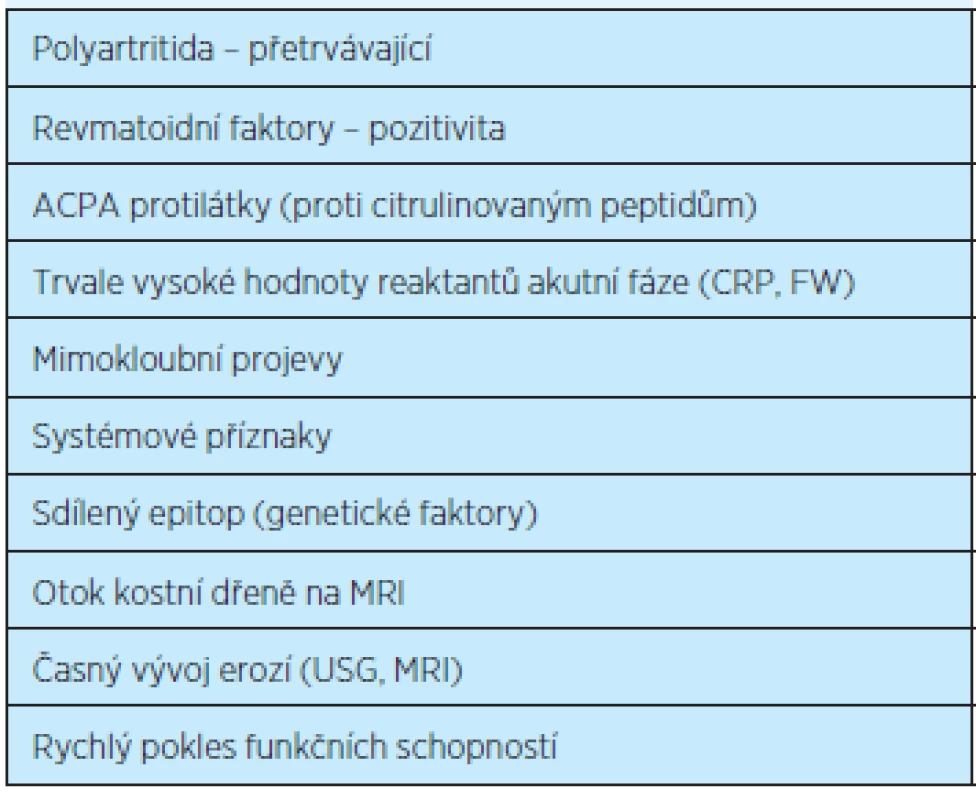
Diferenciální diagnóza revmatoidní artritidy
V diferenciální diagnostice RA je třeba vyloučit erozivní osteoartrózu, revmatickou polymyalgii, polyartritidu jako součást jiného systémového onemocnění (lupus erythematodes), psoriatickou artritidu, dnu (či jiné krystalové artropatie), artritidu jako paraneoplastický syndrom, karcinomatózní polyartritidu(15).
V případě erozivní osteoartrózy jsou ovšem především postiženy distální interfalangeální klouby a pouze výjimečně metakarpofalangeální klouby (u pacientů s LORA naopak), typickým rtg obrazem jsou centrálně uložené kostní eroze (u RA marginální eroze)(2).
U revmatické polymyalgie (PMR) jsou typické bolesti a ztuhlost ve svalech ramenního pletence, uvádí se, že u 15 % pacientů s LORA se také na počátku onemocnění vyskytují myalgie, ale u pacientů s PMR nelze laboratorně prokázat RF ani ACPA protilátky(5, 16), pacienti s PMR mají lepší terapeutickou odpověď na aplikaci kortikoidů(2, 16).
Dna u pacientů vyššího věku může začínat i ve formě pomaleji se rozvíjející symetrické polyartritidy s postižením prstů rukou a nohou. Onemocnění z ukládání krystalů kalcium pyrofosfátu bývá častější ve vyšším věku (až 30% prevalence u osob starších 75 let)(2).
Při výskytu artritidy ve vyšším věku (s častějším postižením kloubů dolních končetin) je nutné uvažovat též o paraneoplastické artritidě, nejčastěji asociované tumory jsou karcinom prsu a karcinom prostaty(2, 7).
Léčba revmatoidní artritidy
Léčba RA je komplexní, zahrnuje režimová opatření, rehabilitaci, farmakoterapii a v některých případech i chirurgickou intervenci (ve stáří je nutné zvážit přínos a rizika operačního výkonu)(10, 17). Vzhledem k polymorbiditě pacientů s LORA je nezbytný multidisciplinární přístup k těmto nemocným (revmatolog, geriatr, ortoped, rehabilitační lékař atd.). Primárním cílem terapie RA je dosažení remise onemocnění, odstranění bolesti a zmenšení rozsahu kloubního poškození se zachováním dobré kvality života seniorů(17, 18).
Farmakoterapie revmatoidní artritidy se zaměřením na LORA
V současné době je hlavní metodou léčby RA farmakoterapie. Terapie LORA se v hlavních principech neliší od léčby RA u mladších pacientů, ale bývá mnohdy obtížnější v důsledku častého nerozpoznání této nozologické jednotky, polymorbidity seniorů a polypragmazie, která často vede k potenciaci běžně užívaných chorobu modifikujících léků (DMARD). Klinická data mapující terapeutickou odpověď na běžně podávané DMARD i léky biologické povahy jsou velmi nekonzistentní a limitována častým věkovým omezením v klinických sledováních(17, 18).
U pacientů se začátkem RA ve vyšším věku (LORA) se při stejné době trvání onemocnění a srovnatelné aktivitě i funkčním stavu doporučuje méně agresivní léčba než u mladších pacientů(19).
Chorobu modifikující léky revmatoidní artritidy (DMARD)
Základem farmakologické léčby RA je aplikace tzv. chorobu modifikujících léků revmatoidní artritidy (disease modifying anti-rheumatic drugs – DMARD), které zlepšují a zmírňují příznaky RA, jejich rychlé nasazení často vede k navození remise a zpomalení, či dokonce zastavení rentgenové progrese onemocnění(17, 18).
V praxi nejčastěji používané DMARD s dávkováním a nežádoucími účinky uvádí tabulka 5.
5. Chorobu modifikující léky RA, dávkování a nejčastější nežádoucí účinky<sup>(1)</sup> 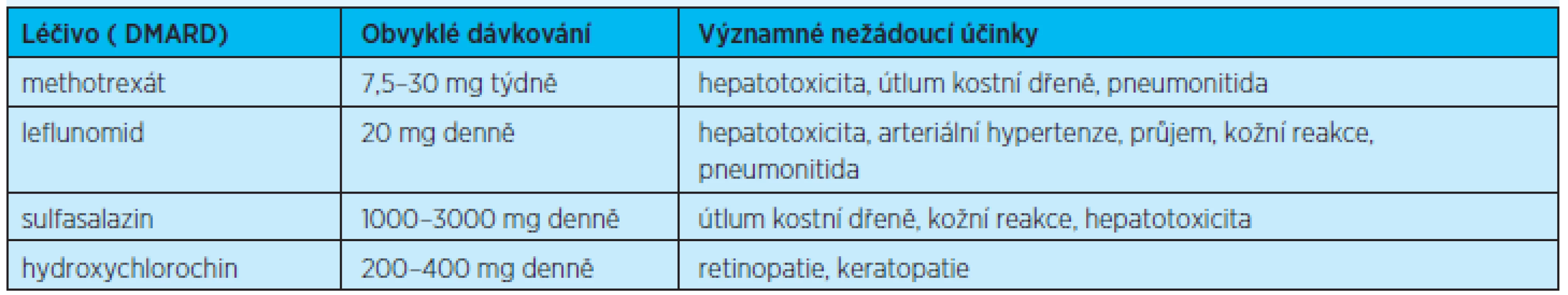
Methotrexát (MTX) je základním lékem volby u pacientů s RA. Jeho farmakologický profil je dobře znám, stejně tak jako jeho toxicita (tab. 5)(1).
S ohledem na sníženou funkci ledvin, jater a často přítomnou hypalbuminemii se pacientům ve vyšším věku doporučuje aplikovat methotrexát v dávce nižší (až poloviční) ve srovnání s mladšími pacienty(20), obvykle nepřekračujeme dávku 15 mg/týden, doporučuje se začít dávkami nižšími – 7,5 mg 1x týdně (nebo i méně) a dávku pozvolna titrovat nahoru(21, 22).
Při nedostatečném efektu či intoleranci perorální léčby MTX je možno změnit aplikační formu na parenterální (subkutánní). Efektu léčby MTX by mělo být dosaženo v intervalu 3–6 měsíců(17, 21). Z důvodu snížení rizika nežádoucích účinků léčby MTX se podává kyselina listová (aplikuje se den po podání MTX)(21).
Praktické využití leflunomidu (v monoterapii či v kombinaci s MTX) u seniorů je všeobecně menší z obavy ze zvýšené toxicity(23, 24). Hydroxychlorochin a sulfasalazin jsou méně potentní v terapii RA než MTX, ale mají své zastoupení v případě, kdy je terapie MTX kontraindikována nebo u mírných forem LORA(17, 24). Při aplikaci antimalarik (hydroxychlorochin) je vhodné provádět oční kontroly 1–2x za rok (riziko vzniku retinopatie)(7, 25). Pro závažné systémové projevy onemocnění nebo pro pacienty refrakterní na léčbu je rezervován cyklosporin a azathioprin(17,18). Cyklosporin A je indikován v případě přítomnosti vaskulitidy, s ohledem na možný vývoj arteriální hypertenze je nutná monitorace krevního tlaku(7, 25).
Biologické léky v terapii revmatoidní artritidy
V případě, že terapie syntetickými DMARD nebyla účinná, jsou indikovány u vysoce aktivních a rychle progredujících forem RA tzv. biologické léky(17, 26). Tato léčba je ovšem velice nákladná a je vyhrazena pro specializovaná revmatologická centra. Před případným zahájením léčby je nutné vyloučit aktivní tuberkulózu (TBC)(26).
Status 1. linie má nejstarší a nejvíce využívaná skupina biologických léčiv – inhibitory tumor nekrotizujícího faktoru alfa (anti-TNFalfa), mechanismem jejich účinku je blokáda protizánětlivých cytokinů TNFalfa a interleukinu 1 (infliximab, adalimumab, etanercept, golimumab, certolizumab), a dále blokátor receptoru pro interleukin 6 (tocilizumab). Status 2. linie (v případě selhání nebo kontraindikací léků 1. linie) mají blokátor kostimulace aktivace T buněk (abatacept) a depleční terapie proti B buňkám (rituximab)(17, 26).Zejména u seniorů je anti-TNF terapie spojena s vyšším rizikem reaktivace latentní TBC(26). U pacientů s LORA se méně často podává biologická léčba (ve srovnání s mladšími pacienty) v důsledku obavy ze zvýšeného rizika výskytu infekcí ve stáří (26, 27), ale také proto, že pacienti s LORA častěji dosahují klinické remise při aplikaci syntetických DMARD(5).
Glukokortikoidy v terapii revmatoidní artritidy
Glukokortikoidy (GK) v malých dávkách (<10 mg prednisonu či jeho ekvivalentu denně) se s úspěchem využívají k rychlé kontrole onemocnění do nástupu účinku DMARD, zmírňují některé symptomy RA (bolest, ranní ztuhlost) a do jisté míry zpomalují rentgenovou progresi(7, 28). Dlouhodobá terapie GK u seniorů přináší řadu nežádoucích účinků, jako je rozvoj osteoporózy, zvýšený sklon k infekcím, indukce steroidního diabetu a dalších(5, 28).
Pro systémovou aplikaci se užívá prednison, a především methylprednisolon(17), který je u starších osob vhodnější alternativou, protože má vyšší protizánětlivý účinek než prednison a prakticky nulovou mineralokortikoidní aktivitu(10).
U mimokloubní manifestace RA podáváme vyšší dávky GK. V případě závažného postižení vnitřních orgánů nebo při extrémně vysoké aktivitě onemocnění při exacerbaci RA lze využít tzv. pulzní léčbu (500–1000 mg methylprednisolonu v intravenózní infuzi 3 dny po sobě či obden)(17). Při přítomnosti zánětlivé artritidy a paraartikulárních projevů (burzitida, tendosynovitida) lze využít lokální intraartikulární aplikace kortikosteroidů (betamethason acetát, methylprednisolon acetát)(10).
Pokud předpokládáme léčbu GK delší než 3 měsíce (dávkou vyšší než 5 mg prednisonu denně), je indikováno provedení kostní denzitometrie s vyšetřením kostní denzity (BMD) nejlépe před zahájením terapie (a dále v intervalech 1 roku) a je doporučena preventivní léčba glukokortikoidy indukované osteoporózy (GIOP) – kalcium v dávce 1500 mg/den, vitamin D v dávce 400–800 IU/den, u pacientů s BMD < –1,5 SD jsou indikovány bisfosfonáty(17). Riziko GK indukované gastropatie snižuje současné podávání inhibitorů protonové pumpy(5).
Nesteroidní antirevmatika v terapii revmatoidní artritidy
Součástí symptomatické léčby RA s prokázanou symptomatickou účinností jsou nesteroidní antirevmatika (NSA). Tlumí symptomy kloubního zánětu, bolest a ztuhlost, zlepšují funkční zdatnost, ale neovlivňují progresi RA. Pokud nejsou známy kontraindikace k podávání NSA, aplikují se v době aktivity onemocnění plné protizánětlivé dávky, které jsou ovšem u starších osob zatíženy řadou nežádoucích účinků (riziko vzniku žaludečního vředu, gastrointestinální krvácení, rozvoj či zhoršení renální insuficience, zhoršení srdečního selhávání, dysfunkce centrálního nervového systému).
Aplikace neselektivních NSA ve vyšších dávkách po delší dobu může být asociována se zvýšeným rizikem arteriálních trombotických příhod (infarkt myokardu, cévní mozková příhoda)(25).
Coxiby, které selektivně inhibují cyklooxygenázu typu 2 (COX-2), mají menší riziko gastrotoxicity, ale nemají anti-agregační účinek, a proto je možné zvýšené riziko kardiovaskulárních komplikací. Epidemiologická data ze studií APC, PreSAP, APPROVE a z metaanalýz ukazují na zvýšenou incidenci trombotických komplikací (infarkt myokardu, cévní mozková příhoda) při užívání coxibů, celkové riziko se zvyšuje u osob s anamnézou kardiovaskulárního onemocnění(25).
U pacientů se zvýšeným rizikem je doporučena současná aplikace inhibitorů protonové pumpy (omeprazol). U starších pacientů se NSA doporučují podávat v nejnižší možné účinné dávce a po nejkratší možnou dobu(5).
Doporučený postup pro léčbu revmatoidní artritidy je uveden v tabulce 6(17).
6. Algoritmus léčby revmatoidní artritidy (RA) dle doporučení EULAR (European League Against Rheumatism) a České revmatologické společnosti (2010)<sup>(17)</sup> 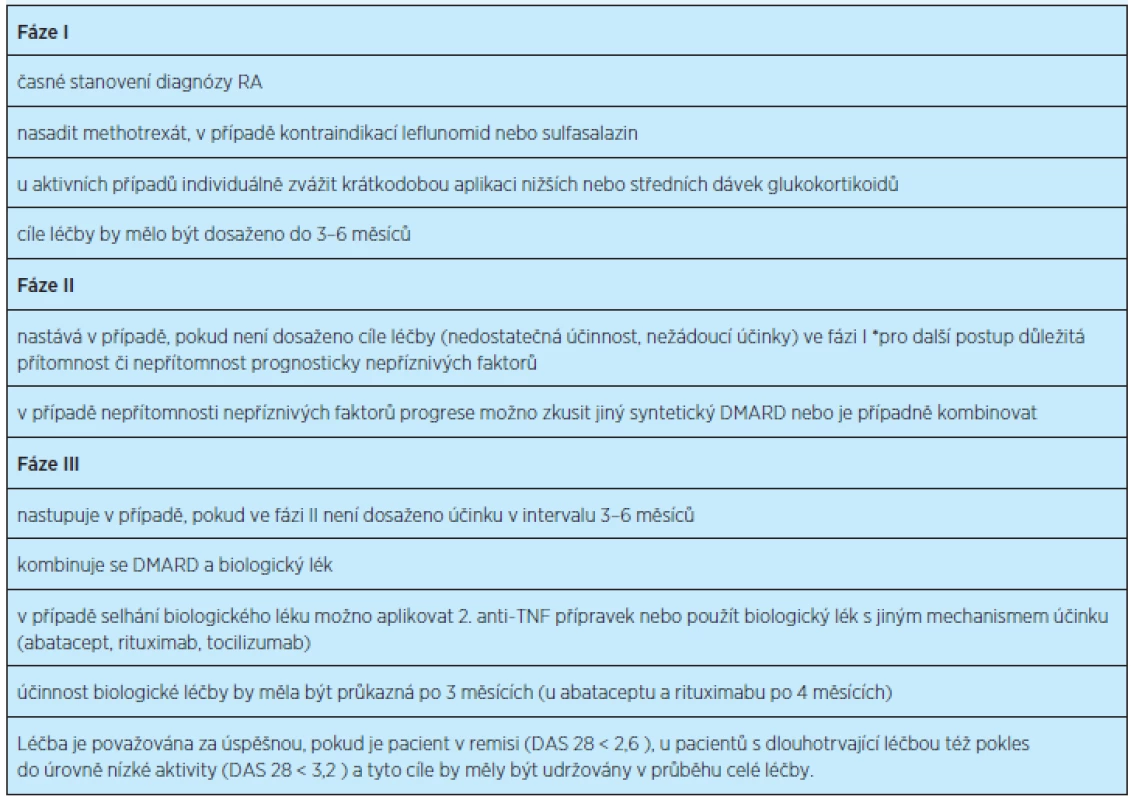
Závěr
Revmatoidní artritida je nemoc chronická, obvykle celoživotní, která vyvolává u pacientů chronickou bolest, ztuhlost, zhoršuje funkční stav a kvalitu života.
Revmatoidní artritida s pozdním začátkem (LORA) má určité specifické projevy, kterými se významně odlišuje od pacientů s revmatoidní artritidou se začátkem v mladším věku (YORA).
Diferenciálnědiagnosticky je nutné především odlišit revmatoidní artritidu s pozdním začátkem (LORA) od revmatické polymyalgie a erozivní osteoartrózy, je nutné myslet i na to, že artritida může být také projevem maligního onemocnění. Vzhledem k tomu, že došlo ke zpřesnění diagnostiky revmatoidní artritidy v časnějších stadiích, je možné dřívější nasazení účinné léčby. S ohledem na častou polymorbiditu, polypragmazii, změny farmakokinetiky a farmakodynamiky léčiv u seniorů, sníženou funkci ledvin a jater, možný zvýšený výskyt nežádoucích účinků léků a též mnohdy obtížnou compliance pacienta je nutné věnovat pozornost výběru léčebné strategie a individuálně zvážit přínos a možná rizika léčby u pacientů s revmatoidní artritidou ve vyšším věku(20).
MUDr. Jan Klán1
MUDr. Hana Ciferská, Ph.D.2
prof. MUDr. Eva Topinková, CSc.1
1Geriatrická klinika 1. LF UK a VFN, Praha
2Revmatologický ústav, Praha
MUDr. Jan Klán
e-mail : jan.klan@vfn.cz
Absolvoval 1. lékařskou fakultu UK v Praze. Od roku 2001 pracuje na Geriatrické klinice 1. LF UK a VFN Praha. V rámci výzkumných aktivit této kliniky spolupracoval pod vedením prof. MUDr. E. Topinkové na evropské multicentrické studii AD HOC (Aged in Home Care) zaměřené na zdravotně-sociální problematiku a rizika seniorů v domácí péči. Atestaci z interního lékařství 1. stupně složil v roce 2005, specializovanou způsobilost k výkonu povolání lékaře v oboru geriatrie získal v roce 2008. V rámci pedagogické činnosti se podílí na výukových programech pregraduálního i postgraduálního vzdělávání v oboru geriatrie a gerontologie. Je členem České gerontologické a geriatrické společnosti ČLS JEP.
Sources
1. Mann H: Revmatoidní artritida. Interní medicína pro praxi 2012; 14 (4): 177–181.
2. Vencovský J: Revmatoidní artritida ve vyšším věku. Postgraduální medicína 2004; 6 : 73–77.
3. Shanmuganandan LCK, Arunachalam CR: Late onset rheumatoid arthritis. Indian Journal of Rheumatology 2009; (6), Volume 4, Number 2; 56–60.
4. Bajocchi G, La Corte R, Locaputo A et al.: Elderly onset rheumatoid arthritis – clinical aspects. Clin Exp Rheumatol 2000; 18(4 Suppl. 20); 49–50.
5. Huscher D, Sengler C, Ziegler S, Gromnica-Ihle E; komentář Šenolt L: Revmatoidní artritida ve stáří. Medicína po promoci 2009; 6 : 28–34.
6. Alušík Š: Revmatologie. Triton 2002. str. 20–28.
7. Pavelka K: Některé aspekty gerontorevmatologie. Česká geriatrická revue 2004; 4 : 5–14.
8. Turkcapar N, Demir O, Atli T et al.: Late onset rheumatoid arthritis: clinical and laboratory comparisons with younger onset patients. Arch Gerontol Geriatr 2006; 42 : 225–231
9. Hrba J: Revmatoidní artritida. Doporučené postupy pro praktické lékaře ČLS JEP, 2002. Projekt MZ ČR zpracovaný ČLS JEP za podpory grantu IGA MZ ČR 5390–3.
10. Topinková E: Geriatrie pro praxi. Galén 2005. str. 167–184.
11. Lopez-Hoyos M, de Ruiz Alegria C, Blanco R et al: Clinical utility of anti-CPP antibodies in the differential diagnosis of elderly-onset rheumatoid arthritis and polymyalgia rheumatica. Rheumatology (Oxford) 2004; 43 : 655–657.
12. Gatterová J, Seidl Z, Vaněčková M et al.: Skórovací systémy při hodnocení progrese revmatoidní artritidy. Čes Revmatol 2008; 16(2): 89–91.
13. Aletaha D, Neogi T, Silman AJ, Funovits J, Felson DT et al.: 2010 Rheumatoid Arthritis Classification Criteria An American College of Rheumatology / European League Against Rheumatism Collaborative Initiative. Ann Rheum Dis 2010; 69 : 1580–1588.
14. Smolen J, Breedveld FC, Schiff MH et al.: A simplified disease activity index for rheumatoid arthritis for use in clinical practise. Rheumatology (Oxford) 2003; 42 : 244–257.
15. Topinková E: Muskuloskeletální a revmatická onemocnění ve stáří. Postgraduální medicína 2004; 6 : 57–65.
16. Pease CT, Haugeberg G, Montague B et al.: Polymyalgia rheumatica can be distinguished from late onset rheumatoid arthritis at baseline: results of a 5-yr prospective study. Rheumatology (Oxford) 2009; 48 : 123–127.
17. Pavelka K, Vencovský J: Doporučení České revmatologické společnosti pro léčbu revmatoidní artritidy. Čes Revmatol 2010; 18(4), 182–191.
18. Smolen JS, Landewe R, Breedveld FC et al.: EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs. Ann Rheum Dis 2010; 69 : 964–975.
19. Tutuncu Z, Reed G, Kremer J, Kavanaugh A: Do patients with older-onset rheumatoid arthritis receive less aggressive treatment? Ann Rheum Dis 2006; 65 : 1226–1229.
20. Fialová D, Topinková E: Specifické rysy geriatrické farmakoterapie z pohledu farmakokinetických a farmakodynamických změn ve stáří. Remedia 2002; 12 : 434–440.
21. Visser K, Katchmart W, Loza E et al.: Multinational evidence based recommendations for the use of methotrexate in rheumatic disorders with a focus on rheumatoid arthritis: integrating systematic literature research and expert opinion of a broad international panel of rheumatologists in the 3E initiative. Ann Rheum Dis 2009; 68 : 1086–1093.
22. Visser K, van der Heijde D.: Optimal dosage and route of administration of methotrexate in rheumatoid arthritis: a systematic review of the literature. Ann Rheum Dis 2009; 68 : 1094–1099.
23. Strand V, Cohen S, Schiff M et al.: Treatment of active rheumatoid arthritis with leflunomide compared with placebo and methotrexate. Arch Intern Med 1999; 159 : 242–255.
24. Smolen JS, Kalden J, Scott DL et al.: Efficacy and safety of leflunomide compared with placebo and sulphasalazine in active rheumatoid arthritis: a double blind, randomized, multicenter study. Lancet 1999; 353 : 259–266.
25. Šedová L, Štolfa J, Horák P, Pavelka K: Doporučení České revmatologické společnosti pro monitorování bezpečnosti léčby revmatoidní artritidy. Čes Revmatol 2009; 17(1): 4–15.
26. Vencovský J a výbor České revmatologické společnosti: Bezpečnost biologické léčby – doporučení České revmatologické společnosti. Čes Revmatol 2009; 17(3): 146–160.
27. Sidiropoulos P, Flouri ID, Drosos A: Geriatric patients receiving anti-TNFA agents have comparable to younger adults response but increased incidence of serious adverse events. Ann Rheum Dis 2008; 67 (Suppl II): 180.
28. Kirwan JR: The effect of glucocorticoids in joint destruction in rheumatoid arthritis, N Engl J Med 1995; 333 : 142–146.
Labels
Geriatrics General practitioner for adults Orthopaedic prosthetics
Article was published inGeriatrics and Gerontology

2014 Issue 1-
All articles in this issue
- Home-based care for patients with dementia in the context of burden on non-expert/non-professional caregivers
- The issue of arterial hypertension in questions and answers
-
Jsou cílové hodnoty pro léčbu arteriální hypertenze odlišné ve středním a vyšším věku?
Co říkají klinické studie, guidelines a jaká jsou současná doporučení pro klinickou praxi. - Specific clinical features of late-onset rheumatoid arthritis
- Prevention and management of instability and falls in geriatric patients
- Use of mobility aids in decubitus patients in selected facilities in The Czech Republic and Germany
- Social background of elderly patients with mental disorders – a comparison between 2003 and 2013
- Geriatrics and Gerontology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- The issue of arterial hypertension in questions and answers
- Specific clinical features of late-onset rheumatoid arthritis
- Prevention and management of instability and falls in geriatric patients
- Home-based care for patients with dementia in the context of burden on non-expert/non-professional caregivers
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

