-
Medical journals
- Career
Problematika arteriální hypertenze v otázkách a odpovědích
: MUDr. Marie Berková; Ph.D. 1; MUDr. Zdeněk Berka 2; Prof. MUDr. Eva Topinková, CSc. 1
: Geriatrická klinika 1. LF UK a VFN Praha 1; II. interní klinika LF UP a FN Olomouc 2
: Geriatrie a Gerontologie 2014, 3, č. 1: 5-11
: Review Article
Arteriální hypertenze představuje nejčastější kardiovaskulární onemocnění, které vede ke zvýšené kardiovaskulární a cerebrovaskulární mortalitě. Zvláště frekventovaná je tato diagnóza v seniorské populaci, kde postihuje přes 60 % osob starších 65 let. Vybraná aktuální problematika z oblasti arteriální hypertenze a její léčby je probrána formou otázek a odpovědí.
Klíčová slova:
arteriální hypertenze – variabilita krevního tlaku – seniorský věk – dippers – non-dippersArteriální hypertenze představuje nejčastější kardiovaskulární onemocnění, které vede ke zvýšené kardiovaskulární morbiditě. Klinicky se může manifestovat fibrilací síní, srdečním selháním, infarktem myokardu, cévní mozkovou příhodou ischemické či hemoragické etiologie, poškozením renálních funkcí nebo hypertenzní retinopatií. Hypertenze rovněž významně zvyšuje kardiovaskulární mortalitu. V seniorské populaci osob starších 65 let je prevalence arteriální hypertenze více než 60 %. Proto je tato problematika stále aktuální a nabízí řadu otázek.
Vybrané otázky
Jaké jsou aktuálně doporučované hodnoty krevního tlaku pro seniorskou populaci?
Zatím jsou stále platná Doporučení pro léčbu hypertenze České společnosti pro hypertenzi z roku 2012, podle kterých se doporučuje docílit krevního tlaku (TK) pod 140/90, a to i u osob seniorského věku, i když při dosahování tohoto cíle nemusíme být u osob pokročilého věku bez závažných rizikových faktorů (diabetes mellitus, stav po CMP apod.) tak striktní.
Jedna z nejpřesvědčivějších studií, které ukázaly prospěšnost snižování TK u osob vysokého stáří (80–105 let), byla studie HYVET, jejímž cílem však bylo dosažení TK pod 150/90. K léčbě hypertenze byl použit indapamid (1,5 mg denně) s případným přidáním perindoprilu (2 až 4 mg denně). Tato dvojkombinace byla aplikována u ¾ intervenovaných. V aktivně léčené skupině osob klesl krevní tlak o 29,5/12,9 mmHg a TK se nakonec snížil na průměrnou hodnotu 144/78 mmHg. To vedlo k 30% redukci cévních mozkových příhod a statisticky významné redukci srdečního selhání (o 64 %), větších kardiovaskulárních příhod a celkové mortality (o 21 %). Na základě těchto výsledků byla studie HYVET předčasně z etických důvodů ukončena (neboť pacienti v kontrolní placebové skupině byli poškozováni absencí antihypertenzní léčby) a terapie hypertenze byla doporučena i u osob ve věku nad 80 let. Studie HYVET sice zahrnovala osoby pokročilého stáří, ale byly to osoby relativně zdravé, bez jiných kardiovaskulárních chorob, v dobré fyzické a psychické kondici. Ačkoli alterace baroreceptorů je u osob pokročilého stáří častá, pacienti ve studii HYVET měli dokonce i na léčbě podobný TK vsedě i vestoje, což svědčí o relativně zdravých osobách. Polymorbidní a křehcí senioři nebyli do studie zahrnuti. Incidence nežádoucích účinků byla nižší ve větvi s aktivní antihypertenzní medikací než ve větvi s placebem, což vypovídá o dobré toleranci antihypertenziva, a většina nežádoucích účinků byla způsobena spíše samotnou hypertenzí než její léčbou.
V roce 2013 byla publikována randomizovaná, multicentrická studie SPS 3 (The Secondary Prevention of Small Subcortical Stroke). Ta rozdělila seniory po lakunárním mozkovém infarktu do dvou skupin s cílovými hodnotami systolického TK < 130 mmHg a TK v rozmezí 130–149 mmHg a srovnávala výsledky léčby v obou skupinách. Ve skupině s cílovým TK < 130 mmHg došlo k nesignifikantnímu 16% snížení výskytu ischemických cévních mozkových příhod (CMP), ale signifikantnímu 63% poklesu hemoragických CMP oproti kontrolní skupině s cílovým TK 130–149 mmHg(1). Osoby s nižším cílovým TK pod 130 mmHg užívaly průměrně 2,4 antihypertenziv, osoby s cílovým TK v rozmezí 130–149 mmHg měly 1,8 antihypertenzní medikace. Průměrný věk pacientů v této studii však byl 63 (±11,0) let, takže se jednalo o relativně „mladé osoby“. K tomu, aby se zabránilo vzniku jedné CMP, bylo zapotřebí léčit 200 osob. Je otázkou, zda je vhodné aplikovat intenzivní terapii také na pacienty vyššího věku, než byli zahrnuti do studie, u kterých je riziko pádů nebo synkopy větší než u jednoho ze 200 pacientů.
Při jakém tlaku je nejnižší mortalita?
Stále je studována hranice, ke které lze krevní tlak pacientů snižovat tak, aby byla co nejvíce snížena mortalita. Na základě post hoc studie ONTARGET byla diskutována existence J-křivky, kdy sice při systolickém TK pod 120 mmHg došlo u rizikových pacientů k dalšímu snížení cévních mozkových příhod, ale zvýšil se výskyt jiných závažných nežádoucích účinků, především srdečních příhod.
Ve studii ACCORD snížila intenzivní antihypertenzní léčba (dosažený TK 119,3 mmHg) ve srovnání se skupinou se standardní léčbou (dosažený TK 133,5 mmHg) výskyt CMP o dalších 41 %, ale výskyt dalších kardiovaskulárních příhod a celková úmrtnost se statisticky nezměnily. Při snížení TK pod 130 mmHg ve studii PROGRESS došlo k poklesu recidiv CMP, ale riziko kardiovaskulárních příhod se zvýšilo.
Riziko kardiovaskulárních příhod stoupá také s poklesem diastolického TK pod 70 mmHg. Cílovou hodnotu TK pro celkovou dospělou populaci s rizikem CMP lze hledat na J-křivce s nadirem kolem 130–140/80. Rozhodnutí o léčbě však musí být učiněno na individuální bázi a snižování TK by mělo být v každém případě postupné a lékařem pečlivě sledované. Zvláště zodpovědně je nutno postupovat u seniorů, kde jsme si vědomi nežádoucích následků nadměrně sníženého TK.
Co je to pulzní tlak?
Pulzní tlak se dříve nazýval tlaková amplituda a je to rozdíl mezi hodnotou systolického a diastolického TK. Pulzní tlak se zvyšuje s věkem v důsledku narůstající cévní rezistence. Hodnota pulzního tlaku nad 60 mmHg je považována za rizikový faktor kardiovaskulárních komplikací.
Krevní tlak však není stále stejný, kolísá během dne…
Změny krevního tlaku v závislosti na čase patří k nejdůležitějším biorytmům organismu. Krevní tlak však nekolísá jenom během dne, ale také během týdne, ročních období a roku. S tím koresponduje i variabilita incidence náhlé srdeční smrti. Externí vlivy, které působí na organismus živočichů a mohou se odrazit na změnách krevního tlaku, nazýváme synchronizátory. K silným synchronizátorům patří např. světlo, teplota, příjem potravy a další vlivy vnějšího prostředí. Za slabé synchronizátory se považují meteorologické vlivy, např. tlak či vlhkost vzduchu.
K vnitřním faktorům, které ovlivňují krevní tlak, se řadí kromě pružnosti tepen a náplně cévního řečiště především funkce nervové a hormonální soustavy, obzvláště sympatoadrenálního systému, na který má vliv fyzická a psychická aktivita organismu. Aktivizace sympatoadrenálního systému se vzestupem krevního tlaku v ranních hodinách vede k maximu výskytu akutního infarktu myokardu, arytmií a náhlých úmrtí ráno a dopoledne. Stejně tak nejvíce krvácivých cévních mozkových příhod a subarachnoideálních krvácení se vyskytuje v ranních hodinách po nárůstu krevního tlaku. Incidence ischemických CMP je největší od půlnoci do dopoledních hodin(2, 3). Cirkadiánní rytmus krevního tlaku může být narušen např. prací v noci, častým buzením, přesunem v časových pásmech apod.
Co se týká roční variability krevního tlaku – vyšší hodnoty krevního tlaku jsou měřeny v zimě než v létě. To se dává do souvislosti s vyšší aktivitou sympatického nervového systému v zimních měsících. V létě je někdy nutno antihypertenzní terapii snížit i kvůli častější tendenci k dehydrataci starších osob v horkém počasí.
Jaký význam má zvýšená variabilita krevního tlaku?
Zvýšená variabilita krevního tlaku představuje významnou kardiovaskulární patologii. Variabilita TK nejen během 24hodinového monitorování, ale zejména dlouhodobá variabilita TK při jednotlivých kontrolách u lékaře je nejsilnějším prediktorem kardiovaskulárního rizika, především cévních mozkových, ale i srdečních příhod. Jak ukázala analýza studie ASCOT-BPLA, zvýšená variabilita krevního tlaku naměřená při jednotlivých návštěvách u lékaře, je mnohem silnějším prediktorem komplikací než průměrné hodnoty TK. Zvyšující se věk, stejně jako diabetes mellitus a kouření jsou faktory vedoucí ke snížené pružnosti tepen a jejich zvýšené rigiditě a přispívající ke zvýšení variability TK(4). Zvýšená variabilita krevního tlaku je riziková obzvláště pro mozkovou tkáň, která je na výkyvy TK velmi citlivá. V důsledku zvýšené variability TK vznikají atrofie mozkové tkáně, drobné lakunární infarkty a postižení kognitivních funkcí.
Proč a kdy je vhodné provést ambulantní monitorování krevního tlaku?
Ambulantní (většinou 24hodinové, ale také 48hodinové nebo 7denní) monitorování krevního tlaku (AMTK) je vhodné jako doplňující a zpřesňující metoda hodnocení TK. Přístroj pro ambulantní monitorování TK měří krevní tlak v pravidelných, nejčastěji půlhodinových či hodinových intervalech. Umožňuje získat přehled o hodnotách krevního tlaku v delším časovém úseku, zhodnotit denní či vícedenní variabilitu krevního tlaku, reakci krevního tlaku na různé zátěžové situace, ať již fyzické, či psychické, kterým je pacient vystaven během běžného života. Umožní zhodnotit pokles krevního tlaku v nočních hodinách. Manžeta přístroje se přikládá na nedominantní paži tak, aby co nejméně bránila vyšetřovanému ve výkonu manuálních činností. Podle písemných záznamů, které si pacient vede během ambulantního monitorování krevního tlaku, lze zjistit, při jaké činnosti došlo ke zvýšení nebo snížení krevního tlaku, či při jakých tlakových hodnotách se eventuálně vyskytly subjektivní potíže. AMTK umožní také zhodnocení účinnosti farmakoterapie a případně její úpravu. Ambulantní monitorování TK je hrazeno v indikovaných případech pojišťovnami 4x ročně (tabulka 1, 2).
1. Indikace ambulantního monitorování krevního tlaku 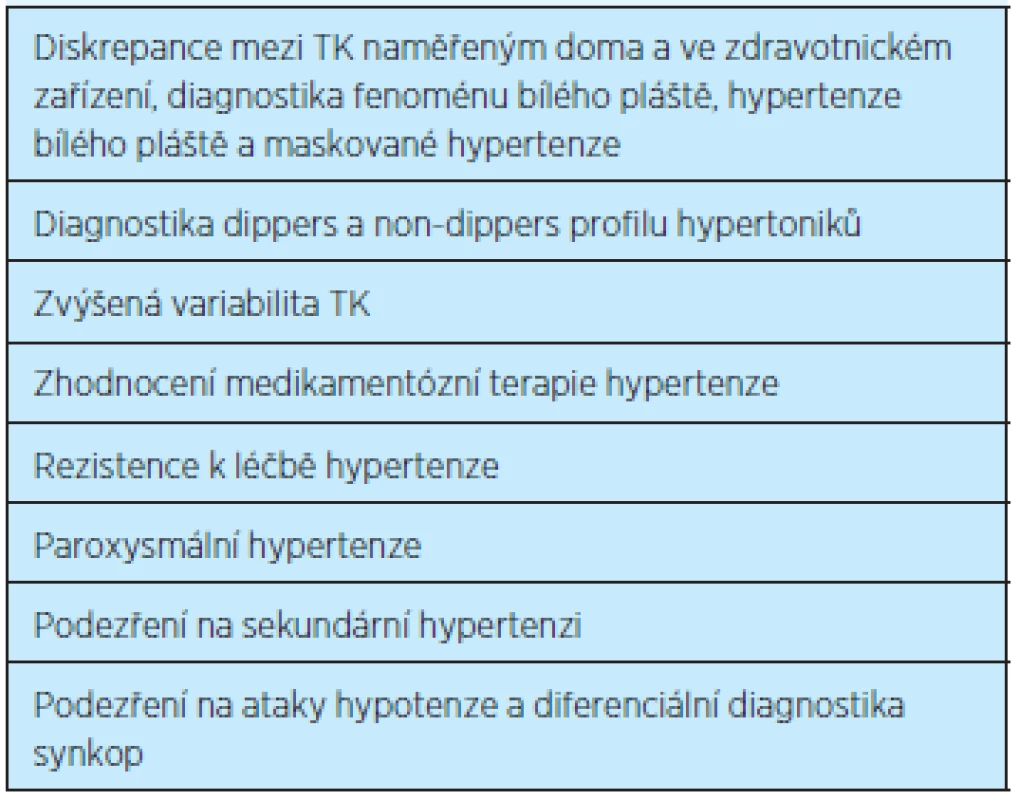
2. Referenční normální hodnoty krevního tlaku při ambulantním monitorování TK pro dospělou populaci 
Z naměřených hodnot během 24hodinového monitorování TK lze odvodit tlakovou zátěž, tj. procentuální vyjádření části dne, po kterou se krevní tlak pohyboval nad stanoveným limitem. Některé přístroje samy tento údaj vypočítají. Tlaková zátěž je nezávislým rizikovým faktorem orgánového poškození způsobeného hypertenzí.
Co je to diurnální index?
Během 24hodinového biologického cyklu dochází v nočních hodinách fyziologicky k poklesu průměrného nočního TK o 10–20 % oproti průměrnému TK v bdělém stavu. Diurnální index vyjadřuje v procentech, o kolik se TK v noci skutečně snížil oproti dennímu TK. Osoby s dostatečným nočním poklesem TK nazýváme „dippers“ (dip = angl. klesat, snížit se). Pacienty, u kterých nedojde k poklesu krevního tlaku alespoň o 10 %, označujeme „non-dippers“. Jedná se o patologii, která vede k vyššímu orgánovému postižení hypertoniků, především k hypertrofii levé komory, ztluštění stěny karotid, mikroalbuminurii, retinopatii a vyššímu riziku vzniku CMP a kognitivního postižení(5). Až 25 % hypertoniků má non-dippers profil. K non-dippers profilu vedou i další chorobné stavy spojené s vysokým krevním tlakem, např. sekundární hypertenze, diabetes mellitus, asthma bronchiale, obstrukční spánková apnoe, chronická renální insuficience, léčba kortikoidy, vaskulární demence, Alzheimerova choroba, ale i spánková deprivace. S non-dippers profilem se můžeme setkat u žen hypertoniček po menopauze, kdy vlivem hormonálních změn dochází ke zvýšenému výskytu redukovaného nočního poklesu TK. U některých osob jsou dokonce průměrné hodnoty TK v noci vyšší než během dne (risers = reverzní dippers). Je to především u těžkých sekundárních hypertenzí, ale také u pracovníků nočních směn nebo u Parkinsonovy choroby. U těchto pacientů je zvýšené riziko kardiovaskulárních příhod.
Osoby s poklesem průměrných nočních hodnot TK o více než 20 % se označují za extrémní dippers. Mezi extrémní dippers se řadí osoby s autonomními neuropatiemi nebo osoby s nadměrnou terapií hypertenze, která vede v nočních hodinách k významnému poklesu TK. Nadměrně snížený TK v nočních hodinách v důsledku razantní antihypertenzní terapie může přivodit CMP ischemické etiologie.
Jednorázové 24hodinové monitorování krevního tlaku však má nízkou reproducibilitu pro stanovení dipper a non-dipper profilů a k získání validních výsledků se doporučuje měření několikrát opakovat.
Mezi pacienty s abnormálním 24hodinovým tlakovým profilem jsou zmiňováni i nemocní s Parkinsonovou chorobou?
Parkinsonova nemoc je neurodegenerativní onemocnění, postihující především oblasti substantia nigra, putamen a pallidum, ale také periferní buňky autonomního sympatického nervstva, včetně buněk paravertebrálních sympatických řetězců i paravertebrálních mezenterických ganglií. Přestože jsou tito pacienti obvykle považováni podle naměřených hodnot v ambulanci za hypotoniky, u kterých je navíc sklon k postprandiální hypotenzi a manifestní ortostatické hypotenzi (až 40 %)(6), je pro ně kromě toho typický reverzní rytmus kolísání TK (93 %) a noční hypertenze, vedoucí k orgánovému poškození(5, 6).
Co bylo zjištěno ambulantním monitorováním krevního tlaku u seniorů?
Ambulantní monitorování krevního tlaku u seniorů přineslo několik zjištění:
- Častější výskyt izolované systolické hypertenze
- Častější prudký ranní vzestup krevního tlaku po probuzení
- Zvýšená variabilita TK během dne, pravděpodobně na základě změněné senzitivity baroreceptorů
- Častější ortostatické hypotenze
- Redukce nočního poklesu TK, zvýšený počet non-dippers
- Častější výskyt fenoménu bílého pláště
- Častější postprandiální hypotenze
- Zvýšené riziko noční hypotenze při antihypertenzní léčbě
Jaký je rozdíl mezi fenoménem bílého pláště a hypertenzí bílého pláště?
Fenomén (= efekt) bílého pláště se vyskytuje u hypertoniků. Pacienti si doma naměří normální hodnoty TK, ale při kontrole ve zdravotnickém zařízení naměří lékař hypertenzní hodnoty. Riziko fenoménu bílého pláště spočívá v nadhodnocení hypertenze. Hypertenze bílého pláště je popisována u osob, které nejsou hypertoniky. Přesto při měření TK lékařem v ambulanci jsou naměřeny zvýšené hodnoty TK. Prevalence hypertenze bílého pláště se v populaci udává 15–50 %(7). Hypertenze bílého pláště může dosahovat až 30 mmHg nad denní průměr AMTK, většinou kolem 20 mmHg pro systolický a 10 mmHg pro diastolický TK(8). V etiologii jak fenoménu bílého pláště, tak i hypertenze bílého pláště hraje roli nadměrná aktivace sympatoadrenálního systému.
Jak zvolit optimální farmakoterapii hypertenze?
Při volbě antihypertenziv bereme v úvahu především kardiovaskulární riziko pacienta, koincidující choroby, jako je diabetes mellitus, ischemická choroba srdeční, dyslipidemie nebo chronická renální insuficience. Musíme zvažovat kontraindikace medikace. Při výskytu nežádoucích účinků či alergie je nutné léčbu upravit. Stále máme k dispozici 4 základní skupiny antihypertenziv, tj. ACE inhibitory/sartany, blokátory kalciových kanálů, diuretika a beta-blokátory, teprve při nedostatečném efektu či kontraindikaci těchto antihypertenziv sáhneme po dalších, např. ze skupiny antagonistů mineralokortikoidních receptorů, alfablokátorů nebo centrálně účinkujících antihypertenziv.
Podle účinku na metabolismus dělíme antihypertenziva na metabolicky negativní, neutrální a pozitivní. K těm, která ovlivňují metabolismus cukrů a tuků v negativním smyslu, patří především betablokátory a diuretika. Je to také jeden z důvodů, proč se preferují antihypertenziva zasahující do renin-angiotenzin-aldosteronového systému a blokátory kalciových kanálů.
Týká se negativní metabolický profil všech diuretik? Diuretika přece bývají ve starším věku doporučována...
Nejvíce negativních vlivů má z používaných sulfonamidových diuretik především hydrochlorothiazid, který přesto zůstává zatím nejpředepisovanějším antihypertenzivem na světě. Hydrochlorothiazid může potenciálně zvýšit hladinu glykemie a vyvolat dnavý záchvat. Oproti němu, jak prokazují studie, je metabolicky neutrální thiazidové analogum indapamid. Britská doporučení pro léčbu hypertenze NICE proto doporučila zaměňovat hydrochlorothiazid při léčbě hypertenze za indapamid. Diuretika však zůstávají doporučovanou skupinou antihypertenziv ve stáří, protože starší organismus se hůře vyrovnává se solnou zátěží.
Proč nepatří furosemid k základním diuretikům pro léčbu nekomplikované hypertenze?
Furosemid patří ke kličkovým diuretikům, která působí v Henleho kličce nefronu. Je to silné diuretikum, jehož poločas je poměrně krátký a jeho účinek nemusí pokrýt celých 24 hodin, proto může způsobit kolísání TK. Jeho místo je tam, kde je stav hypertonika komplikován srdečním nebo renálním selháním s nízkou glomerulární filtrací a významnou retencí tekutin, kdy sulfonamidová diuretika již nejsou účinná. Uplatní se i při zvládání akutních hypertenzních stavů.
Ovlivňují všechna antihypertenziva stejně účinně variabilitu krevního tlaku, která je, jak již bylo dříve zmíněno, jedním z nezávažnějších rizikových faktorů morbidity a mortality?
Sledování variability krevního tlaku byla věnována subanalýza studie ASCOT-BPLA, ve které byli pacienti aktivně léčeni v jedné skupině amlodipinem (5–10 mg) ± perindoprilem (4–8 mg) a ve druhé intervenované skupině atenololem (50–100 mg) ± diuretikem bendroflumethiazidem (1,25–2,5 mg). Amlodipin významně snižoval variabilitu krevního tlaku mezi jednotlivými kontrolními měřeními TK u lékaře s efektivní redukcí cévních mozkových příhod ve srovnání s terapií atenololem, který variabilitu TK zvyšoval, přestože dosahované průměrné hodnoty systolického tlaku byly v obou skupinách podobné(9).
Ve světle dalších studií se blokátory kalciových kanálů, zejména amlodipin, jeví jako nejvhodnější léky na snížení variability krevního tlaku k prevenci cerebrovaskulárních příhod. Thiazidová diuretika rovněž snižují variabilitu TK, ale v menší míře než blokátory kalciových kanálů. Z hlediska snížení variability krevního tlaku a prevence CMP byly betablokátory, reprezentované atenololem, nejméně účinné. Jeho nevýhoda tkví především v krátkém poločasu, který nezaručuje efektivní snížení TK po dobu celých 24 hodin.
V kterou denní dobu máme podávat antihypertenziva?
Moderní antihypertenziva s dlouhodobým účinkem se podávají většinou ráno, s předpokládaným efektem po dobu 24 hodin. U pacientů s dippers profilem může při večerní dávce antihypertenziv hrozit nadměrné snížení krevního tlaku se zvýšeným rizikem kardiovaskulární příhody. U pacientů s non-dippers profilem a nekontrolovaným ranním vzestupem krevního tlaku je možné podat dávku antihypertenziva večer.
Ve studiích se k léčbě těchto pacientů osvědčily valsartan nebo trandolapril ze skupiny ACE inhibitorů, u kterého při podání ve večerní dávce nedošlo k nadměrnému poklesu TK v nočních hodinách(10). Hydrochlorothiazid je schopen pacienty bez fyziologického nočního poklesu TK převést na dippers profil i při aplikaci v ranní dávce(11).
Co je to rezistentní hypertenze a jak ji léčit?
O rezistentní hypertenzi hovoříme, pokud TK naměřený dosahuje nad 140 mmHg přes léčbu nejméně trojkombinací antihypertenziv v maximálních tolerovaných dávkách. Jedním z těchto antihypertenziv musí být vždy diuretikum. Rezistentní hypertenze se vyskytuje u 5–10 % hypertoniků. K nejvhodnějším trojkombinacím k léčbě hypertenze patří ACE inhibitor (eventuálně sartan), blokátor kalciového kanálu dihydropyridinového typu a dlouhodobě působící diuretikum, ke kterým se jako čtvrtý lék doporučuje antgonista mineralokortikoidních receptorů – spironolakton (studie ASCOT). K nejdůležitějším faktorům nekontrolované hypertenze patří non-compliance a suboptimální terapie.
Ke sledování adherence pacienta k léčbě nám může pomoci stanovení hladin antihypertenziv v séru. Příčinou sekundární rezistentní hypertenze je nejčastěji primární hyperaldosteronismus. Často se však místo rezistentní hypertenze jedná o pseudorezistenci (20–38 % všech rezistentních hypertenzí, prokázáno AMTK), etiologicky způsobenou např. fenoménem bílého pláště. K odlišení se doporučuje právě ambulantní monitorování TK.
Ve vztahu k užívání léků pacientem se hovoří o compliance a adherenci k léčbě. Jaký je v tom rozdíl?
Výraz „compliance“ vyjadřuje „dodržení doporučené léčby“. Compliance zahrnuje dva faktory:
- adherenci k léku, tj. podíl léků, které pacient skutečně využíval, k celkovému množství předepsaných léků v určitém časovém období,
- perzistenci, tzn. dobu trvání léčby od jejího začátku do svévolného vysazení léku pacientem.
Proč bývá compliance a adherence u léčby hypertenze snížená?
Hypertonici mají skutečně jednu z nejhorších adherencí k léčbě. Je to dáno z velké části tím, že dokud nedojde ke komplikacím, je hypertenze asymptomatická, nebolí a nedává o sobě vědět.
Důležitou roli hraje také vztah lékař–pacient. Nedostatek poskytnutých informací nenutí pacienta k pravidelnému užívání. Podle studie Chenga et al.(12) více než 50 % osob občas léky zapomene užít a 14 % pacientů si nemyslí, že je trvalá léčba nutná, i když adherence starších pacientů bývá větší než u mladších. Ve stáří se však přidávají kognitivní poruchy, zejména poruchy mnestických funkcí, které mohou užívání léků ztížit. Nezanedbatelnou roli hraje také počet užívaných tablet, nežádoucí účinky léků či alergie, v některých případech i finanční náročnost terapie. Z antihypertenziv je nejhorší compliance u diuretik a betablokátorů, nejlepší u ACE inhibitorů a sartanů.
Jak zlepšit compliance k farmakoterapii hypertenze?
Compliance a adherence k léčbě nejen hypertenze se dá zlepšit zmenšením počtu léků a jejich dávek. My však víme, že ve většině případů s monoterapií hypertenze nevystačíme a je nutná kombinovaná léčba více druhy antihypertenziv, která je až 5x účinnější než použití maximální dávky jedné antihypertenzní látky. Ke snížení dávek a množství léků, které musí pacient užívat, přispívají jednak dlouhodobě účinná antihypertenziva, jež se užívají 1x denně, a fixní kombinace antihypertenziv, kdy v jedné tabletce jsou zkombinovány 2 účinné látky. Optimální fixní kombinace 2 antihypertenziv by měla být tvořena účinnými látkami, z nichž obě mají dlouhý poločas, spolehlivě pokrývající 24 hodin denně, a měly by působit na různých úrovních patogenetických mechanismů hypertenze. Nejvhodnější fixní kombinace tvoří:
ACE inhibitor s blokátorem kalciového kanálu
AT1-blokátor (sartan) s blokátorem kalciového kanálu
ACE inhibitor s diuretikem
AT1-blokátor s diuretikem
Nejméně vhodná pro nepříznivé metabolické účinky je kombinace betablokátoru s diuretikem a je vyhrazena pro případy, kdy jsou tyto léky předepisovány i z jiné indikace (např. koincidence ICHS, srdečního selhání, arytmií apod.). Kombinace ACE inhibitoru a sartanu se nedoporučuje pro jejich společný vliv na renin-angiotenzin-aldosteronový systém a potenciaci nežádoucích účinků (studie ONTARGET).
Nevýhodou, a to ne zcela nepodstatnou, zejména ve farmakoterapii seniorů, je obtížná titrace dávek kombinovaných preparátů. Fixních kombinací antihyperteziv je na trhu řada a je si z čeho vybrat (tabulky 3 a 4).
3. Kombinované terapie preferované při léčbě hypertenze 
4. Příklady nejčastěji používaných fixních kombinací antihypertenziv 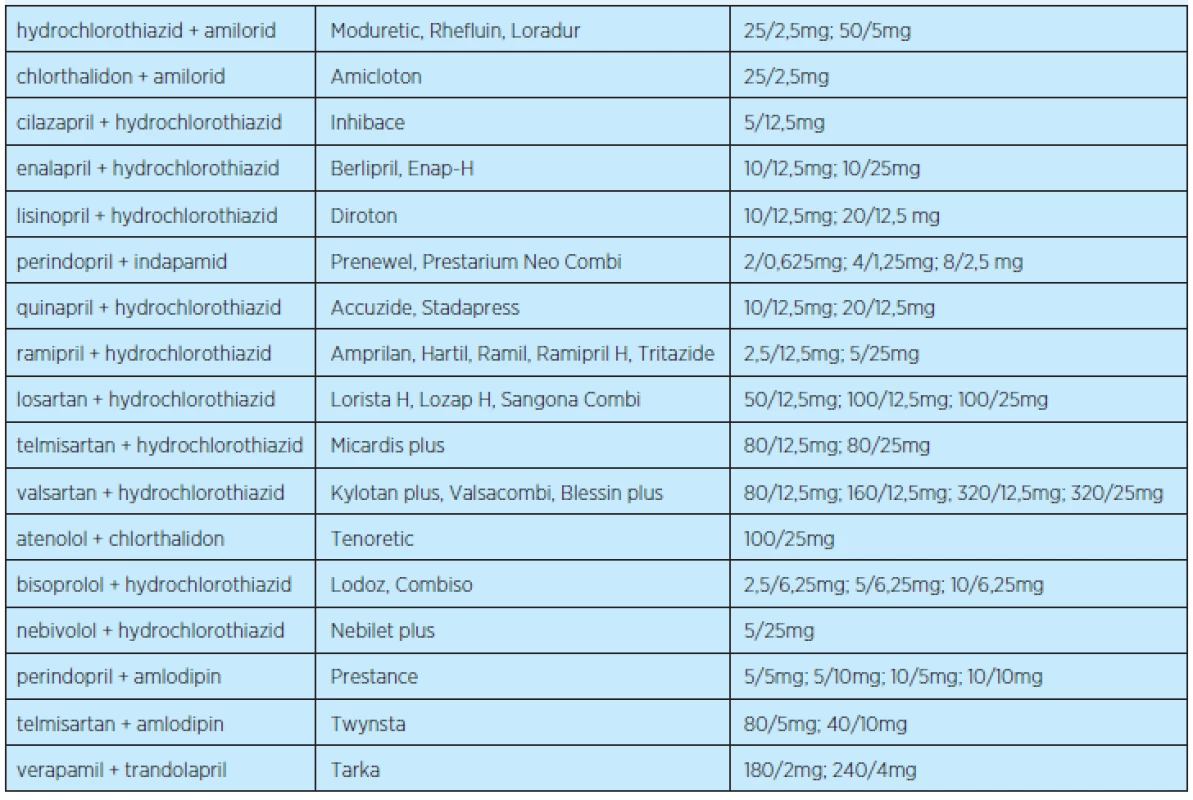
Další novinkou, která přišla v poslední době na trh a má zlepšit adherenci pacientů k léčbě, je orodisperzní forma antihypertenziv (v současné době dostupný perindopril arginin), která se nechá pouze volně rozpustit na jazyku v dutině ústní a není nutno ji zapíjet tekutinou.
Jaké postavení má v léčbě rezistentní hypertenze nefarmakologický přístup – renální denervace tepen?
Denervace renálních tepen je novější metoda léčby rezistentní hypertenze. První výkony byly v České republice provedeny v roce 2011. Indikací je v ordinaci měřený systolický TK vyšší než 160 mmHg a zároveň průměr systolického TK za 24 hodin při ambulantním monitorování nad 130 mmHg při léčbě nejméně 3 antihypertenzivy v maximálních tolerovaných dávkách včetně diuretik. Doporučovaný věk pacientů pro výkon se pohybuje od 18 do 85 let. Glomerulární filtrace by měla dosahovat nad 0,75 ml/s/1,73 m2 (13). Před výkonem se provádí přehledná angiografie břišní aorty k zobrazení jejích větví. Zákrok se dělá v analgosedaci, protože ablace v renální tepně může vyvolávat nepříjemnou bolest v bederní krajině. Renální denervace se provádí technikou radiofrekvenční ablace renálního sympatiku endovaskulární katetrizační cestou přes přístupovou a. femoralis. Cílem je přes lumen renální tepny zasáhnout nervová zakončení aplikací radiofrekvenční energie, která se přemění na tepelnou(45–60 st. Celsia) a destruuje sympatická nervová zakončení(14). Denervace se provádí na obou renálních tepnách, 4–6 ablací na každé z nich.
Jednou ze studií, které hodnotily efekt renální denervace, je studie Symplicity HTN 2 Trial 3, do které bylo zařazeno 106 pacientů, z nichž u poloviny byla provedena denervace renálních tepen. Při kontrolním hodnocení TK půl roku po výkonu byl zjištěn pokles krevního tlaku měřeného v ordinaci o 32/12 mmHg (p < 0,0001), zatímco v kontrolní skupině ke změně TK nedošlo. Denervací renálních tepen se snižuje jak systolický, tak diastolický TK. Výkon má však i další pozitivní účinky: zlepšuje inzulinovou senzitivitu a snižuje glykemii nalačno, studuje se i vliv renální denervace na srdeční selhání a spánkovou apnoi. Přesto se jedná pouze o aditivní léčbu. Denervace renálních tepen nevede k úplnému vyléčení hypertenze. I přes provedenou renální denervaci je nutno pokračovat dále v chronické farmakoterapii. Většinou se podaří snížit medikaci o jedno farmakum, u části pacientů je tato léčba neefektivní. Kontraindikace denervace renálních tepen uvádí tabulka 5(13).
5. Kontraindikace denervace renálních tepen 
Závěr
V současnosti dostupné diagnostické i léčebné metody nám umožňují individualizovat a optimalizovat léčbu hypertenze podle potřeb pacienta. Je k tomu však také nezbytná dobrá spolupráce lékaře s pacientem.
MUDr. Marie Berková, Ph.D.1
MUDr. Zdeněk Berka2
prof. MUDr. Eva Topinková, CSc.1
1Geriatrická klinika 1. LF UK a VFN Praha
2II. interní klinika LF UP a FN Olomouc
MUDr. Marie Berková, Ph.D.
e-mail: marie.berkova@lf1.cuni.cz
Pracuje na Geriatrické klinice 1. LF UK a Všeobecné fakultní nemocnice v Praze..
Sources
1. Souček M: Doporučení pro antihypertenzní léčbu u pacientů po cévní mozkové příhodě: cílový krevní tlak. Komentář. Medicína po promoci 2013; 14 (2): 16–21.
2. Casetta L, Granieri E, Fallica E: Patient demographic and clinical features and circadian variation in onset of ischemic stroke. Arch Neurol 2002; 59 (1): 48–53.
3. Kocer A, Ilhan A, Ince N: The related cause in very early morning onset of stroke. Progress in Neuro-Psychopharmacology & Biological Psychiatry 2005; 29 : 983–988.
4. Cífková R, Souček M: Co nového v problematice hypertenze? Kap Kardiol 2011; 3 : 3–7.
5. Homolka P. Dippers a non dippers. In: Homolka P et al.: Monitorování krevního tlaku. Grada Publishing, Praha 2010 : 133–137.
6. Biaggioni I. Parkinson’s Disease: Autonomic neuropathy with impaired cardiovascular regulation. Hypertension 2007; 49 : 21–22.
7. Celis H, Fagard R: White-coat hypertension: a clinical review. European Journal of Internal Medicine 2004; 15 : 348–357.
8. Verdecchia P, Steassen J, White W: Properly defining white coat hypertension. Eur Heart J 2001; 21 : 106.
9. Rothwell PM, Howard SC, Dolan E et al.: ASCOT-BPLA and MRC Trial Investigators. Effects of beta blockers and calcium-channel blockers on within-individual variability in blood pressure and risk of stroke. Lancet Neurol 2010; 9(5): 469–80.
10. Kuroda T, Kario K, Hoshide S et al.: Effects of bedtime vs. morning administration of the long-acting lipophilic angiotensin-converting enzyme inhibitor trandolapril on morning blood pressure in hypertensive patients. Hypertens Res 2004; 27 (1): 15–20.
11. Lemmer B: The importance of circadian rhythms on drug response in hypertension and coronary heart disease – from mice and man. Pharmacol Ther 2006; 111(3): 629-51.
12. Cheng JW, Kalia MM, Feifer S: Patient-reported adherence to guidelines of the Sixth Joint National Committee on prevention, detection, evaluation and treatment of high blood pressure. Pharmacotherapy 2001; 21 : 828-841.
13. Widimský J jr.: Renální denervace u arteriální hypertenze, naděje pro nemocné s rezistentní hypertenzí? Kap Kardiol 2013; 5 : 48–51.
14. Monhart V: Renální denervace v léčbě rezistentní hypertenze. Postgraduální medicína 6/2013. http://zdravi.e15.cz/clanek/postgradualni-medicina/renalni-denervace-v-lecbe-rezistentni-hypertenze-470768
Labels
Geriatrics General practitioner for adults Orthopaedic prosthetics
Article was published inGeriatrics and Gerontology

2014 Issue 1-
All articles in this issue
- Home-based care for patients with dementia in the context of burden on non-expert/non-professional caregivers
- The issue of arterial hypertension in questions and answers
-
Jsou cílové hodnoty pro léčbu arteriální hypertenze odlišné ve středním a vyšším věku?
Co říkají klinické studie, guidelines a jaká jsou současná doporučení pro klinickou praxi. - Specific clinical features of late-onset rheumatoid arthritis
- Prevention and management of instability and falls in geriatric patients
- Use of mobility aids in decubitus patients in selected facilities in The Czech Republic and Germany
- Social background of elderly patients with mental disorders – a comparison between 2003 and 2013
- Geriatrics and Gerontology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- The issue of arterial hypertension in questions and answers
- Specific clinical features of late-onset rheumatoid arthritis
- Prevention and management of instability and falls in geriatric patients
- Home-based care for patients with dementia in the context of burden on non-expert/non-professional caregivers
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career


