-
Medical journals
- Career
Diagnostika a terapie karcinomu laryngu
Authors: B. Maxová; A. Čoček
Authors‘ workplace: Thomayerova nemocnice, Praha, ORL oddělení, Primář: MUDr. Jan Paska, MBA
Published in: Prakt. Lék. 2019; 99(5): 201-204
Category: Reviews
Overview
Nádory hlavy a krku se s 2000 nově diagnostikovanými pacienty v České republice za rok řadí na 6. příčku nejčastějších nádorů u mužů a 17. u žen (1). Incidence karcinomu hrtanu představuje přibližně 8,8/100 000 obyvatel (mortalita 4,1/100 000) a pohybuje se v setrvalém trendu. Nádory postihují 9krát častěji muže než ženy, nejčastěji ve věkovém rozmezí 55–70 let. V etiologii se uplatňují zejména exogenní faktory. Hlavní příčinou je kouření, jehož rizikovost je násobena současnou konzumací alkoholu, dalšími jsou virové infekce HPV. Mluvíme-li o zhoubném nádoru hrtanu, pak se v téměř 95% jedná o spinocelulární neboli dlaždicobuněčný karcinom. Prognóza tohoto nádoru je ovlivněna lokalitou, ale významněji rozsahem malignity, proto je kladen důraz na včasnou diagnostiku. Díky technologickému vývoji se do klinické praxe dostávají moderní vyšetřovací metody umožňující rozpoznání slizničních změn typických pro neoplaziemi infiltrovanou tkáň, využívá se například metody úzkopásmového zobrazení (NBI – Narrow Band Imaging), metod autofluorescence, kontaktní endoskopie. Terapie karcinomu hrtanu se ubírá cestou hrtan záchovných protokolů.
Klíčová slova:
rakovina hlavy a krku – spinocelulární karcinom hrtanu – endoskopie – narrow band imaging – hrtan preservující terapie
ÚVOD
Maligním tumorem hrtanu je v 95 % různě zralý dlaždicobuněčný karcinom (vzácně se může vyskytnout papilokarcinom, verukózní karcinom, sarkom, adenokarcinom, neuroendokrinní karcinoid, malobuněčný karcinom) (2). Metastatické postižení laryngu je raritní, například při primárním tumoru ledvin, prsu, plic, prostaty, gastrointestinálního traktu.
Incidence karcinomu hrtanu představuje přibližně 8,8/100 000 obyvatel (mortalita 4,1/100 000) a pohybuje se v setrvalém trendu. Nádory postihují 9krát častěji muže než ženy, nejčastěji ve věkovém rozmezí 55–70 let. V etiologii se uplatňují zejména exogenní faktory (tab. 1).
Table 1. Rizikové faktory pro vznik karcinomu laryngu 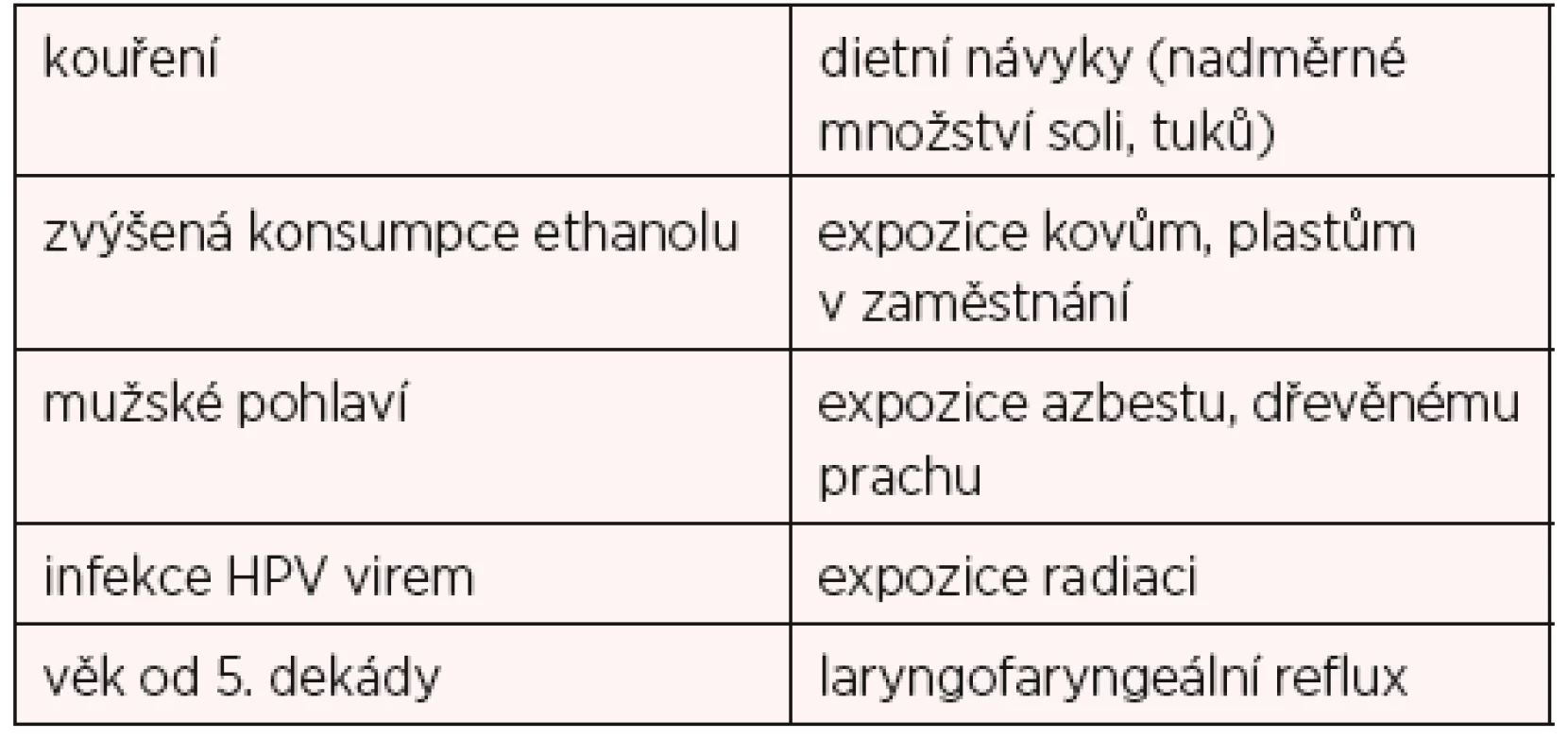
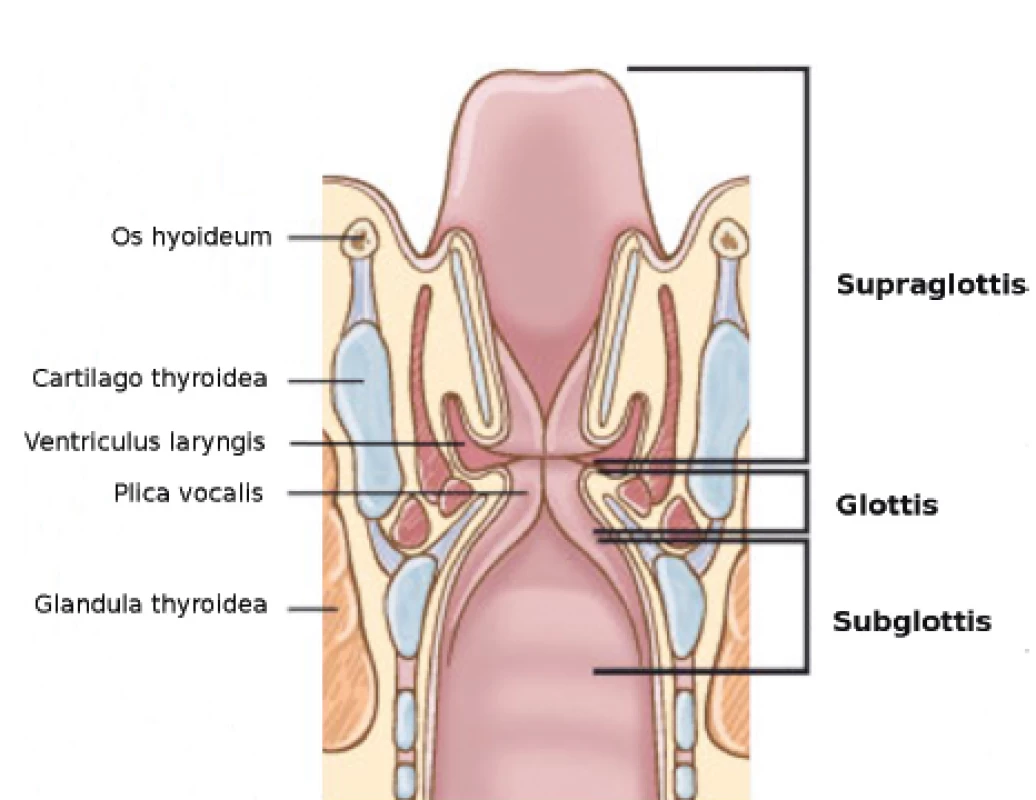
Anatomicky rozdělujeme endolarynx na část supraglotickou (laryngeální plocha epiglottis, aryepiglotické řasy, arytenoidní hrboly a vestibulární řasy), glotickou (rovina procházející nejlaterálnější částí laryngeálního ventrikulu, pravé hlasivkové vazy ohraničené přední a zadní komisurou, spodní hranice arbitrárně 1 cm od spodní plochy pravých hlasivkových vazů), infraglotickou (úsek pod pravými hlasivkovými vazy) (obr. 1). Nejčastěji je postižena oblast glottis, která je nejvíce exponována. Ta tvoří polovinu nádorů hrtanu. Karcinom se zde projeví chrapotem již v časném stadiu. Pro malé lymfatické zásobení této oblasti nalezneme šíření procesu do prelaryngeálních lymfatických uzlin cca v 5 % případů a u nálezů pokročilejších než T1 a T2. Karcinom supraglotický tvoří druhou nejpočetnější skupinu – téměř polovinu karcinomů hrtanu. Bývá méně diferencovaný a s tendencí k lokálně agresivnímu růstu. Stejně jako infraglotický karcinom je z důvodu pozdějšího nástupu klinických příznaků (tab. 2) diagnostikován až v pokročilejších stadiích, tudíž je spjat s horší prognózou. Projevuje se bolestivým polykáním při infekci exofyticky rostoucího karcinomu, hrtanovou dyspnoí, v době diagnózy nalezneme metastázy v mízních uzlinách trigona carotica až v 35 %. Vzácný (3 %) infraglotický karcinom bývá nediferencovaný s neomezeným infiltrativním růstem, projeví se dyspnoí, přerůstá na hlasivku, vzácněji se šíří do průdušnice, metastázuje do peritracheálních a krčních mízních uzlin.
Table 2. Spektrum klinických příznaků karcinomu laryngu 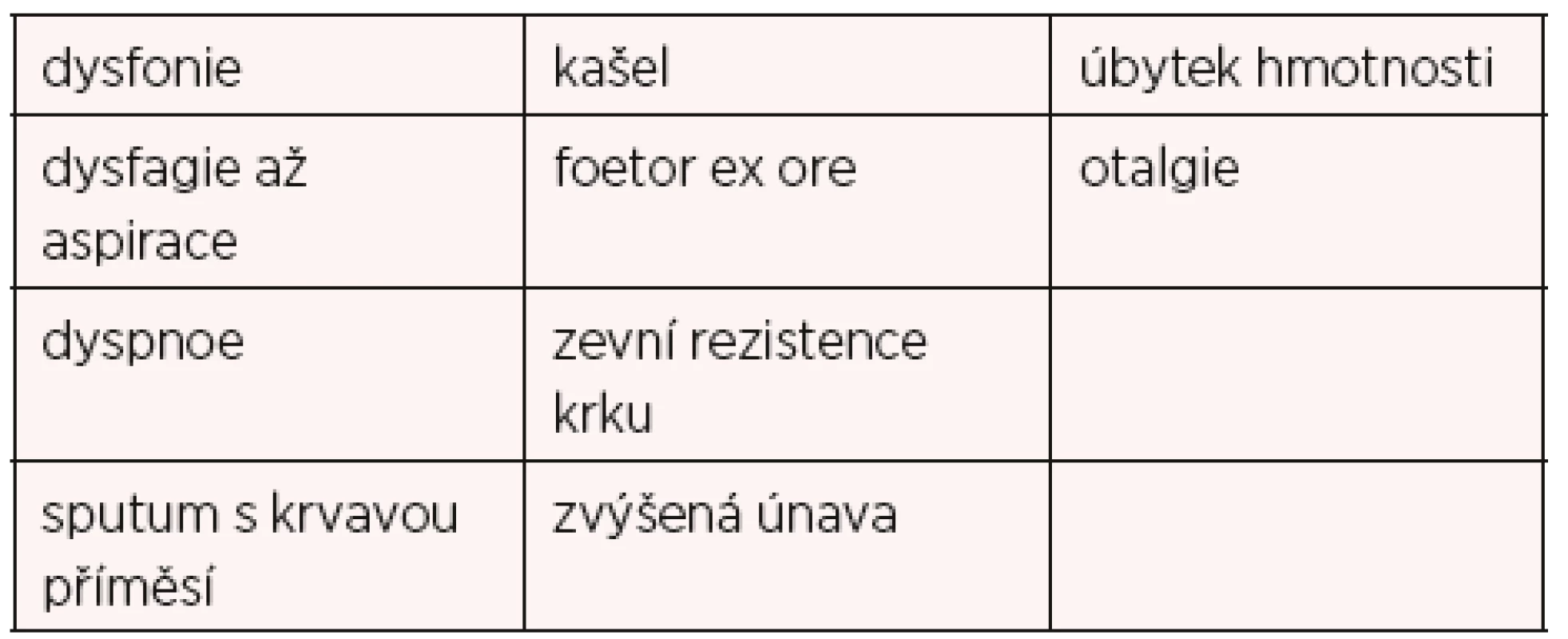
Vzdálené metastázy jsou nalezeny v době diagnózy u cca 5 % karcinomů hrtanu převážně v plicích při současném postižení regionálních mízních uzlin. Sekundárně primární (duplicitní) léze u pacientů s karcinomem hlavy a krku mají vysokou incidenci (2–3 %/rok) (3). Synchronní nebo metachronní karcinom jícnu u pacientů s karcinomem hlavy a krku a opačně karcinomy faryngu u pacientů se spinocelulárním karcinomem jícnu bývají popisovány v rámci tzv. „field of carcinogenesis“ (4). Prolongovaná expozice kancerogenním vlivům způsobující nezávislou transformaci mnoha epiteliálních buněk na odlišných místech vede k vzniku geneticky nezávislých mnohočetných dysplazií a tumorů. Japonský gastroenterolog Nonaka ve své studii prezentuje nález synchronního karcinomu faryngu u pacientů se spinocelulárním karcinomem jícnu v 10 % případů (5).
DIAGNOSTIKA
Nález nádoru hrtanu v časném stadiu má určující vliv nejen na jeho prognózu, ale také na terapeutickou metodu, od níž se odvíjí míra mutilace pacienta, včetně jeho schopnosti polykací, fonační. Klinickému vyšetření hrtanu a hypofaryngu položil základ Manuel Garcia v roce 1855, když použil zubní zrcátko a začal tak vyšetřovat metodou nepřímé laryngoskopie (6). Laryngoskopie přímá byla poprvé popsána Albertem Kirsteinem v roce 1895 (7). Byla rozvíjena až do dnešní podoby, kdy umožňuje odběr vzorku suspektní tkáně k histologickému ověření nálezu. Moderní vyšetřovací postupy využívají rychle se vyvíjející nové endoskopické metody. V této souvislosti mluvíme o takzvané předhistologické diagnostice, kdy na základě podrobného zobrazení slizničních změn v klinickém vyšetření jsme schopni touto tzv. optickou biopsií s vysokou pravděpodobností odhalit přednádorové/časně nádorové změny bez histologického nálezu. Obecně je můžeme rozdělit na horizontální metody (autofluorescence, NBI, zvětšovací a kontaktní mikroskopie) vyšetřující povrch sliznic a vertikální (konfokální endomikroskopie, OCT – optická koherentní tomografie) zkoumající tkáň v jejích vrstvách, tyto zatím spíše experimentálně využívané (8).
Endoskopické vyšetřovací metody
Narrow band imaging (NBI) nebo-li metoda úzkopásmového zobrazení byla vyvinuta v Japonsku a nejprve využívána k zobrazení slizničních lézí v gastroenterologii (9). Její význam spočívá v odhalení patologických slizničních lézí již o rozsahu několika milimetrů. Oproti běžnému endoskopickému vyšetření nevyužívá standardní bílé světlo všech vlnových délek, nýbrž jen vlnové délky v rozmezí 400–430 nm (s maximem 415 nm), resp. 525–555 nm (s maximem 540 nm). Vlastností světla o těchto vlnových délkách je penetrace do povrchových vrstev sliznice, méně do hlubších, je tedy méně rozptylováno. Vzhledem k maximálnímu absorpčnímu spektru odpovídajícímu hemoglobinu jsou zvýrazňovány kapilární kličky (IPCL – intaepithelial papillary capillary loops) v povrchu sliznice, resp. podslizniční cévní pleteně. Ve výsledném obrazu jsou hnědě zobrazeny kapilární kličky v povrchové vrstvě sliznice a azurově podslizniční cévní pleteně. Zvýraznění epitelových změn a slizniční vaskularizace je klíčové pro detekci slizniční patologie. Zvýšené metabolické nároky tkáně postižené prekancerózou či kancerózním procesem samotným jsou spojené nejprve s přestavbou již existujících kapilár (růst, prodlužování, rozšiřování) a následně neoangioinvazí charakterizovanou až ztrátou cévní mikroarchitektury (10). Tyto změny průběhu kapilárních kliček jsou velmi dobře hodnotitelné při použití HDTV (high definition televison) kamery (přináší dostatečné zvětšení a rozlišení) v kombinaci s NBI zobrazením (11). Dle klasifikace Ni et al. definující cévní změny nalezneme obraz typu I–IV v rámci benigních změn, typ Va-c již odpovídá změnám při high-grade dysplaziích, carcinoma in situ, či invazivním karcinomu (10). Specificita a senzitivita vyšetření flexibilním endoskopem v NBI zobrazení u pacientů s dlaždicobuněčným karcinomem hlavy a krku se v literatuře uvádí 91,3 %, resp. 91,6 % (12). Vyšetření může být limitováno sníženou přehledností sliznice při nadměrném slinění, ulpívajícím zahlenění, vysoké hyperkeratóze sliznice. S opatrností je třeba hodnotit nález v terénu postiradiačních změn (kdy okrsek epitelu s nepravidelnými hnědými tečkami postrádá typické ohraničení). S falešně pozitivním nálezem se můžeme setkat u papilomatózy hrtanu, kde je třeba za použití HDTV zobrazení ověřit ztrátu architektury IPCL. Využití NBI zobrazení je velmi efektivní při klinickém vyšetření v ambulantním provozu, výhodou je možnost zpětné analýzy záznamu – a tím hodnocení vývoje léze. Transnazální přístup flexibilním endoskopem při použití lokální anestezie je pro pacienta většinou dostatečně komfortní, je vhodné takto vyšetřit pacienty např. s dysfonií trvající déle než 3 týdny, chronickou faryngitidou, pocitem cizího tělesa v krku. U pacientů dispenzarizovaných po léčbě tumoru v ORL oblasti může vést k časnému odhalení recidiv či perzistence onemocnění. Další možností je například využití rigidních endoskopů peroperačně při zjišťování okrajů léze (obr. 2 a 3).
Image 2. Endoskopické vyšetření v bílém světle – spinocelulární karcinom levé hlasivky 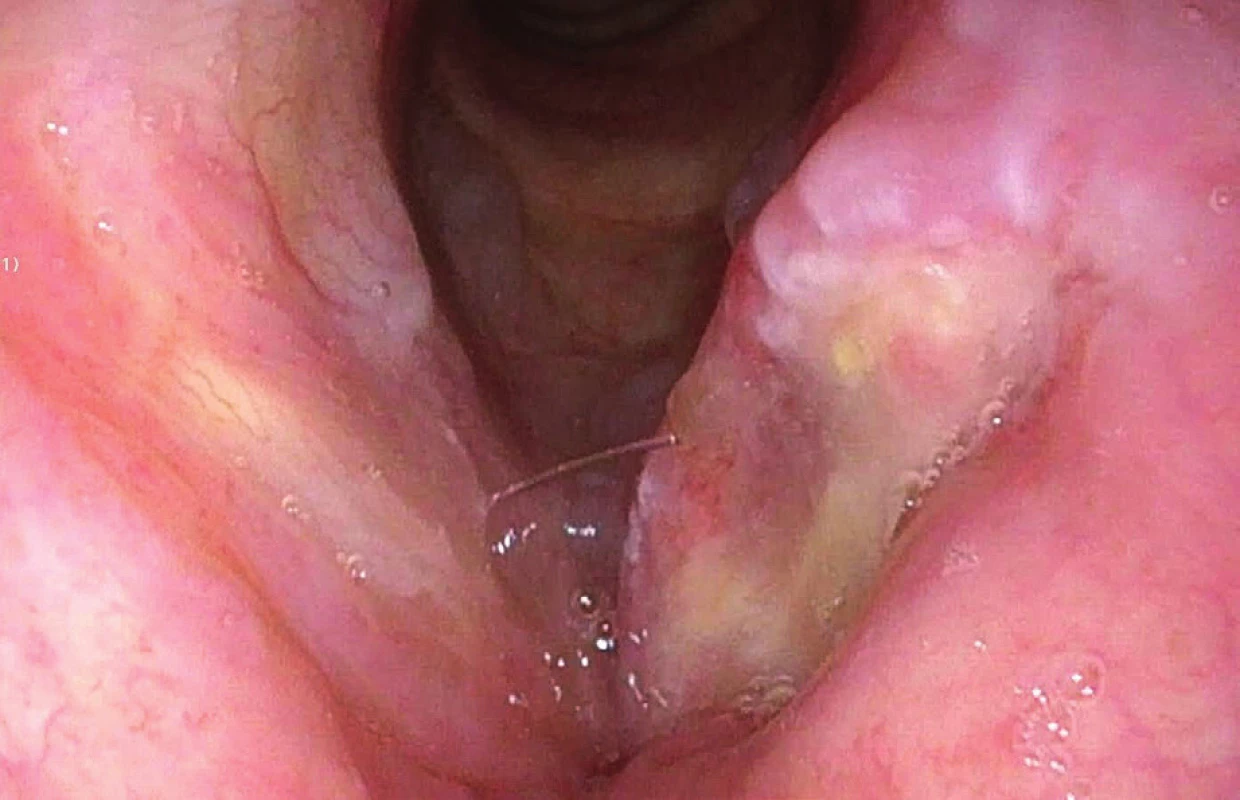
Image 3. Endoskopické vyšetření s NBI – spinocelulární karcinom levé hlasivky, v její střední části patrné patologické změny vaskularizace 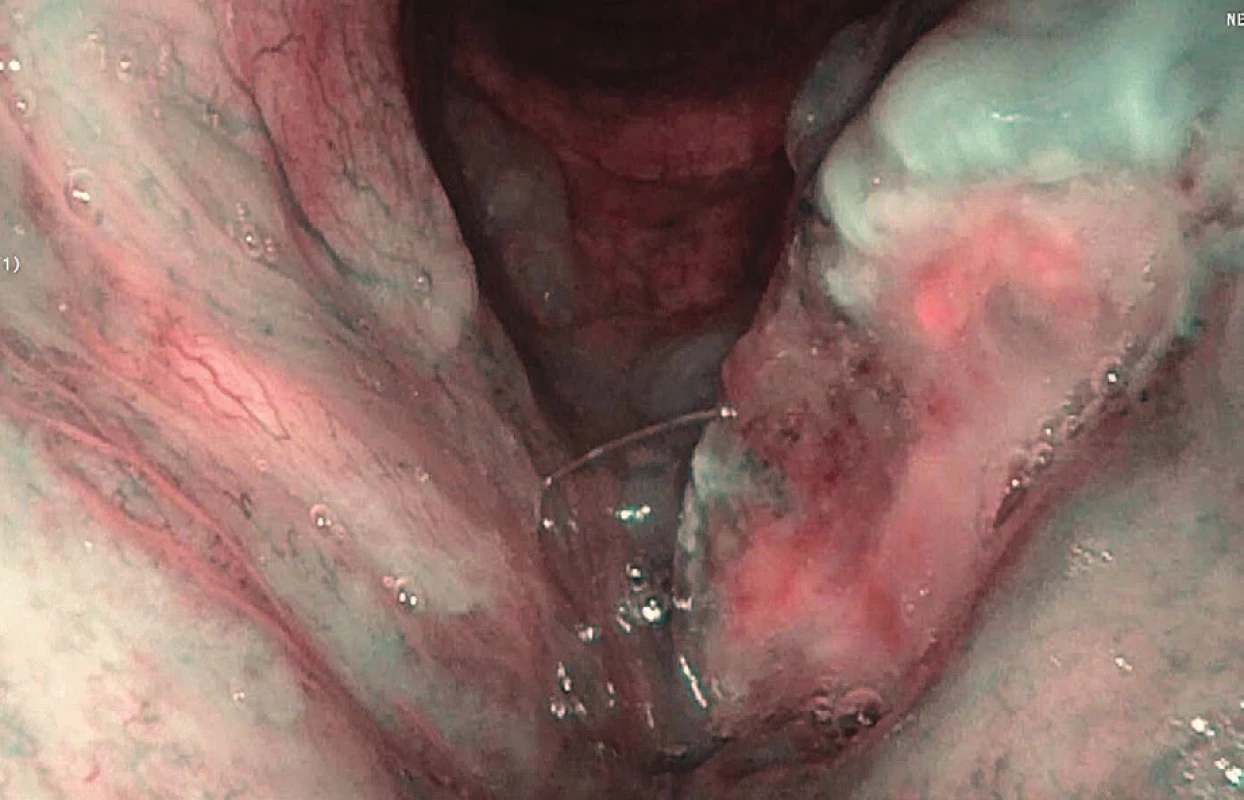
Kombinace kontaktní endoskopie a NBI umožňuje přesné odlišení hranice postižené tkáně, endoskop je v přímém kontaktu se sliznicí a poskytuje 60–150násobné zvětšení zobrazující detaily buněk in vivo (13). Nápadnost nádorové neoangiogeneze může být při použití kontaktní endoskopie podpořena lokálně aplikovanou methylenovou modří zobrazující zvýšenou mitotickou aktivitu nukleových kyselin (obr. 4).
Image 4. Vaskularizace hlasivky v zobrazení kontaktní NBI endoskopie 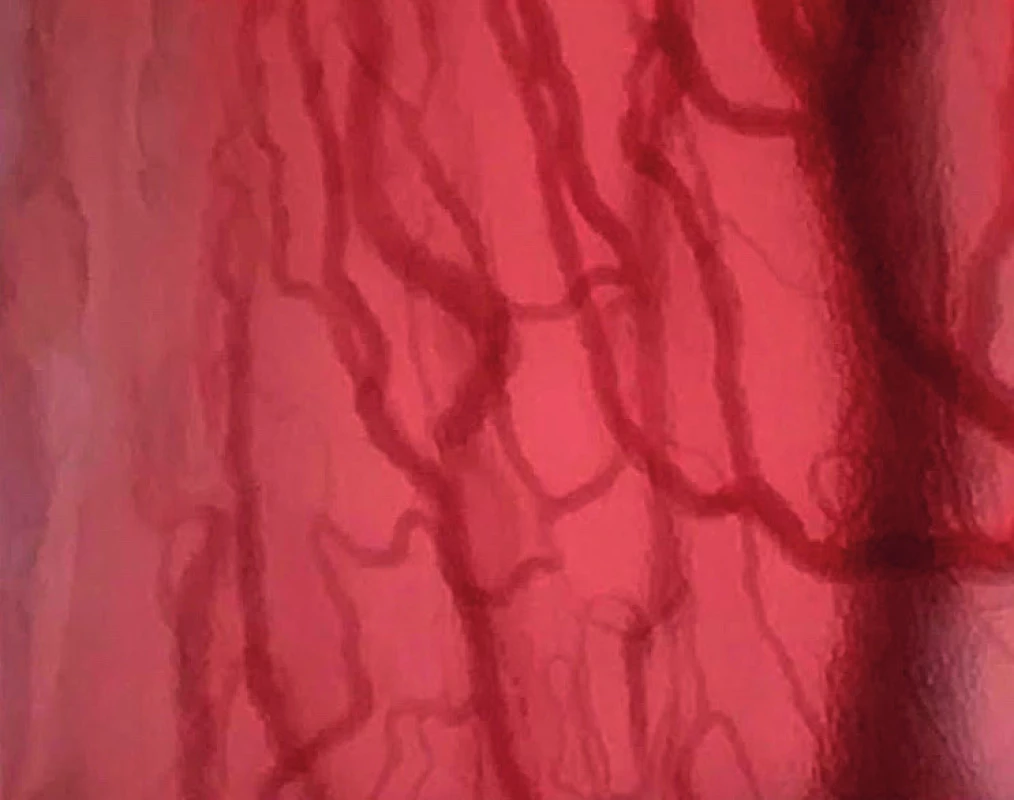
Autofluorescenční endoskopie využívá vlastnosti molekul (tzv. fluoroforů) obsažených v slizničních buňkách emitovat záření, pokud jsou ozářeny světlem o krátké vlnové délce (nejčastěji ultrafialovým). Při jejich ozáření dojde k předání energie a excitaci elektronů těchto molekul na vyšší energetickou hladinu. Následným vyzářením tepla fluorofory klesnou na nižší energetickou hladinu. Tato tzv. autofluorescence je utlumena ve sliznici, která je nádorově změněná. Metoda se využívá v ambulantním režimu i peroperačně při direktní laryngoskopii v celkové anestezii. Její limitací je například omezená výpovědní hodnota v terénu nekrotických, jizevnatých a zánětlivých změn, hyperkeratotických lézí a granulací (14).
Zobrazovací metody
Standardním zobrazovacím vyšetřením, indikovaným u karcinomu hrtanu je CT vyšetření s kontrastní látkou s odpovídající šíří řezu (1–2 mm), které poskytuje informaci o rozsahu tumoru. Velmi užitečnou zobrazovací metodou je PET-CT (pozitronová emisní tomografie-RTG počítačová tomografie), která je kombinací funkčního a morfologického vyšetření (15). Intravenózně podaná fluorodeoxyglukóza (FDG) značená radionuklidem se vychytává v buňkách s vyšší konzumpcí glukózy, jako jsou buňky nádorové. Fotony vyzářené při anihilaci jsou detekovány, obraz je doplněn CT-scany s kontrastní látkou pro bližší morfologické určení a vytváří tak tomografické řezy s mapou metabolicky aktivní tkáně. PET-CT je nejsenzitivnějším vyšetřením k detekci rozsahu primárního tumoru, postižení lymfatických uzlin, detekci vzdálených metastáz či duplicitních tumorů. Využívá se rovněž při hledání primárního tumoru u známého metastatického postižení. Limity vyšetření představuje nespecificita vychytávání radionuklidem značeného analogu glukózy nádorovými buňkami (např. mozková tkáň, ledviny, patrové tonzily se zobrazují metabolicky aktivně i fyziologicky) a rozlišovací schopnost omezená pro léze větší než 0,5 cm. Vyšetření magnetickou rezonancí vypovídá o šíření neoplazie do okolních měkkých tkání, preepiglotického prostoru, invazi skrze thyrohyoidní ligamentum a chrupavčitý skelet hrtanu. Zobrazovací metodou uplatňující se při diagnostice a stagingu karcinomu laryngu je i ultrasonografie krku, která je schopna zobrazit postižení regionálních krčních uzlin.
TERAPIE
Vývoj terapie karcinomu hrtanu započal v roce 1873 první totální laryngektomií německý chirurg Theodor Billroth (7). Počáteční období radikálních chirurgických výkonů zaznamenalo významný vzestup v 20. století s rozvojem celkové anestezie, pooperační péče a chirurgie spádových lymfatických uzlin. Pochopení anatomických poměrů přispělo rozvoji éry parciálních laryngektomií. Po období radikálních a pak částečných chirurgických výkonů následovala etapa hrtan šetřících protokolů (kombinované léčby) s využitím aktinoterapie, jejíž výsledky jsou při použití v časných stadiích karcinomu srovnatelné s chirurgickou terapií.
V dnešní době je základním cílem terapie karcinomu hrtanu jeho odstranění při zachování laryngeálních funkcí. Léčebný postup by měl být ustanoven multioborovým týmem, skládajícím se z onkologa, otorinolaryngologa – chirurga, radiologa, eventuálně maxilofaciálního či plastického chirurga, a to na základě rozsahu, lokalizace, histologického typu nádoru v kombinaci s individuálními podmínkami pacienta (tab. 3 a 4). V časných stadiích tumoru (I, II) se uplatňuje většinou chirurgický larynx šetřící postup, ať už transorální endoskopický, či zevním přístupem. Samotná aktinoterapie přináší srovnatelný výsledek v eliminaci nádoru i funkčních důsledcích, v případě jejího selhání často lze provést záchrannou parciální laryngektomii (16). Pokročilá stadia tumoru (III–IVB) jsou většinou řešena radiochemoterapií, při její neúčinnosti totální laryngektomií. V případě konzervativní terapie pacienti benefitují ze záchovy laryngu, délka přežívání se však neprodlužuje, je také třeba zmínit toxicitu v akutní i pozdní fázi. Primární chirurgická terapie bývá doplněná adjuvantní radio-, eventuálně radiochemoterapií. Moderní záchovné protokoly s neoadjuvantní chemoterapií a následnou RT se neliší v celkovém přežití, jen v záchově laryngu (až u 63 % pacientů) (6), který nemusí být plně funkční a možná lokální recidiva může být obtížněji diagnostikovatelná. Léčba stadia IVC (metastazující/recidivující karcinom) paliativní chemoterapií má za cíl zmírnění progrese nádoru se snížením jeho příznaků.
Table 3. Klasifikace tumoru laryngu – primární tumor (postižení endolaryngu v krajině supraglotické, glotické, infraglotické) 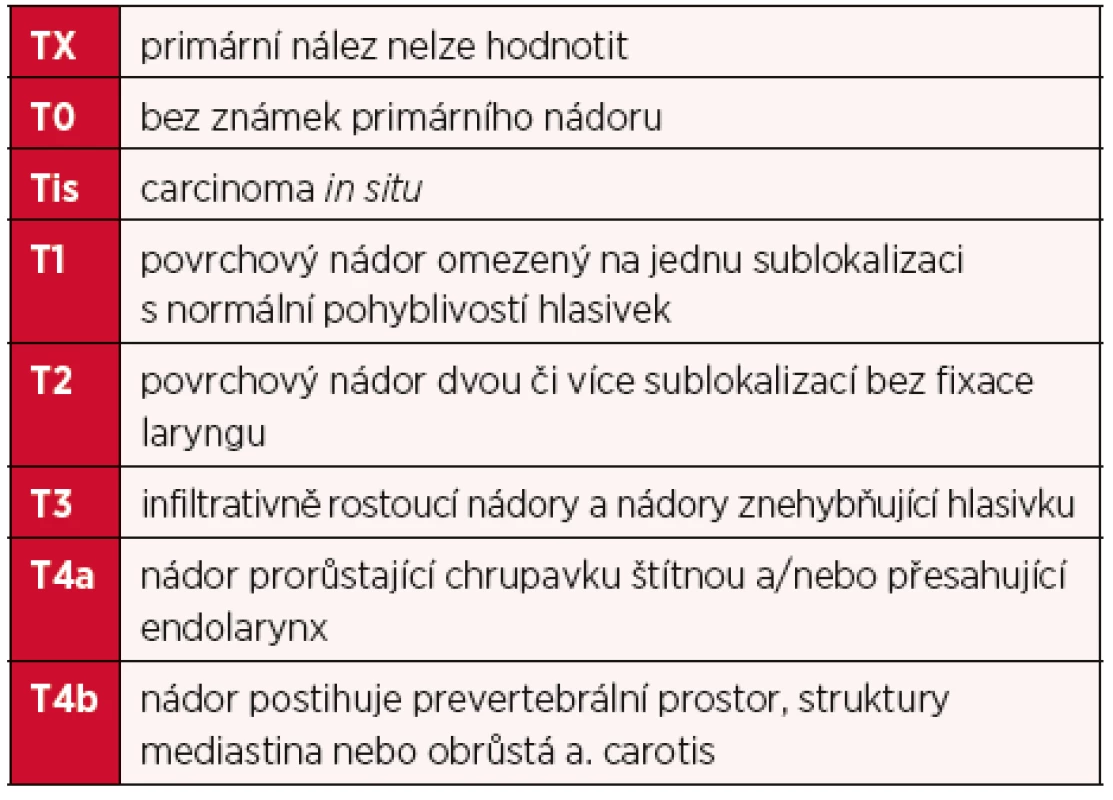
Table 4. Karcinom laryngu TNM klasifikace 8. vydání, rozdělení do stadií 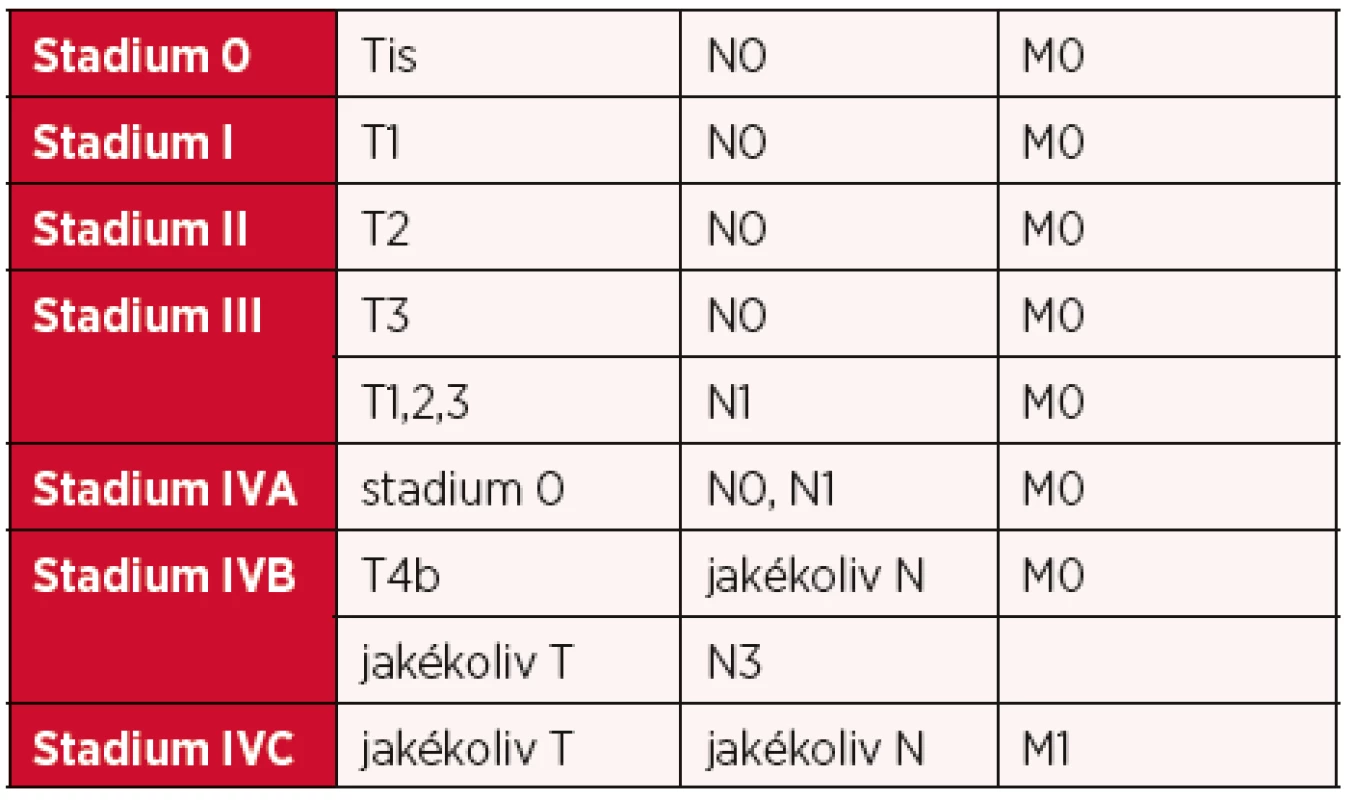
Nejnovějšími trendy v chirurgické terapii je využití CO2 či KPT laseru z transorálního přístupu a technicky náročné robotické chirurgie. Onkologická terapie moderněji používá biologickou léčbu blokátory EGFR, která je méně toxická než chemoterapie, vyšší účinnost se ale neprokázala.
ZÁVĚR
Prognóza karcinomu hrtanu se velmi liší dle stadia, ve kterém je diagnostikována. U nádoru malého rozsahu (TI) v glotické oblasti se uvádí pětileté přežití 80–90 %. Pacienti s nádory postihujícími supraglottis, resp. subglotis v pokročilejším stadiu (TIII) dosahují pětiletého přežití v 53 %, resp. 47 %. Dispenzarizace pacientů je nezbytná z důvodu sekundárně primárních nádorů, recidiv či pozdních metastáz.
Konflikt zájmů: žádný.
MUDr. Barbora Maxová
Thomayerova nemocnice, ORL oddělení
Vídeňská 800, 140 59 Praha 4
e-mail: maxova.ba@gmail.com
Sources
1. Masarykův onkologický ústav. Rakovina hlavy a krku [online]. Dostupné z: https://www.mou.cz/c32-nadory-hrtanu/di47 [cit. 2019-09-02].
2. Hybášek I. Ušní nosní a krční lékařství. Praha: Galén-Karolinum 1999.
3. Jeřábek L. Incidence duplicitních zhoubných nádorů v ORL oblasti a jejich možná etiopatogeneze. Otorinolaryng a Foniat 2001; 50(1): 5–9.
4. van Oijen MG, Slootweg PJ. Oral field cancerization: carcinogen-induced independent events or micrometastatic deposits? Cancer Epidemiol Biomarkers Prev 2000; 9(3): 249–256.
5. Nonaka S, Saito Y, Oda I, et al. Narrow-band imaging endoscopy with magnification is useful for detecting metachronous superficial pharyngeal cancer in patients with esophageal squamous cell carcinoma. J Gastroenterol Hepatol 2010; 25(2): 264–269.
6. Johnson JT. Malignant tumors of the larynx [online]. Dostupné z: https://emedicine.medscape.com/article/848592-overview#showall [cit. 2019-08-30].
7. Čoček A. Vývoj koncepce léčby karcinomu hrtanu [online]. Dostupné z: https://zdravi.euro.cz/clanek/postgradualni-medicina/vyvoj-koncepce-lecby-karcinomu-hrtanu-369033 [cit. 2019-08-30].
8. Lukeš P, Lukešová E, Zábrodský M, a kol. Endoskopické optické zobrazovací metody v diagnostice nádorů hrtanu. Čas. Lék. čes. 2017; 156(4): 192–195.
9. Sano Y, Kobayashi M, Hamamoto Y. New diagnostic method based on color imaging using narrow band imaging (NBI) system for gastrointestinal tract. Gastrointest Endosc 2001; 53(5): AB125.
10. Ni XG, He S, Xu ZG, et al. Endoscopic diagnosis of laryngeal cancer and precancerous lesions by narrow band imaging. J Laryngol Otol 2011; 125(3): 288–296.
11. Piazza C, Cocco D, Del Bon F, et al. Narrow band imaging and high definition television in the endoscopic evaluation of upper aero-digestive tract cancer. Acta Otorhinolaryngol Ital 2011; 31(2): 70–75.
12. Watanabe A, Taniguchi M, Tsujie H, et al. The value of narrow band imaging for early detection of laryngeal cancer. Eur Arch Otorhinolaryngol 2009; 266(7): 1017–1023.
13. Carriero E, Galli J, Fadda G, et al. Preliminary experiences with contact endoscopy of the larynx. Eur Arch Otorhinolaryngol 2000; 257(2): 68–71.
14. Malzahn K, Dreyer T, Glanz H, Arens C. Autofluorescence endoscopy in the diagnosis of early laryngeal cancer and its precursor lesions. Laryngoscope 2002; 112(3): 488–493.
15. Tichý L. Vyšetřovací metoda – PET/CT. Med. pro Praxi 2009; 6(1): 46–49.
16. Pála M. Léčba karcinomu laryngu. Onkologie 2016; 10(3): 138–141.
Labels
General practitioner for children and adolescents General practitioner for adults
Article was published inGeneral Practitioner

2019 Issue 5-
All articles in this issue
- Krátké testy kognitivních funkcí do ordinace praktického lékaře
- Podiatrie, problematika zarůstajícího nehtu a její řešení – metoda Arkady
- Diagnostika a terapie karcinomu laryngu
- Nealkoholové ztukovatění jater u pacientů podstupujících bariatrický výkon v ÚVN Praha
- Sestra s pokročilou praxou v starostlivosti o seniorov
- Dunning-Krugerův efekt a podpora eutanázie
- 61. Purkyňův den v Libochovicích
- 150 let od úmrtí Jana Evangelisty Purkyně (1787–1869)
-
Profesor Dr. Leopold Moll
*2. 3. 1877 Česká Lípa – ✞21. 2. 1933 Vídeň - MUDr. František Kriegel, CSc. (1908–1979) – vzpomínka na lékaře a kontroverzního politika
- Mezinárodní platforma pro strategii v léčbě nádorů žlučníku EURO-CHOLANGIO-NET
- General Practitioner
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Krátké testy kognitivních funkcí do ordinace praktického lékaře
- Diagnostika a terapie karcinomu laryngu
- Podiatrie, problematika zarůstajícího nehtu a její řešení – metoda Arkady
- Nealkoholové ztukovatění jater u pacientů podstupujících bariatrický výkon v ÚVN Praha
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career