-
Medical journals
- Career
Deprese a úzkost těhotných žen
: D. Seifertová 1,2; P. Mohr 1,2; J. Praško 1,3; J. Čermák 1,2
: Psychiatrické centrum, Praha Ředitel: prof. MUDr. Cyril Hoschl, DrSc. 1; Univerzita Karlova, Praha 3. lékařská fakulta Přednosta: prof. MUDr. Cyril Hoschl, DrSc. 2; Fakultní nemocnice Olomouc Psychiatrická klinika Přednosta: doc. MUDr. Ján Praško, CSc. 3
: Prakt. Lék. 2009; 89(9): 508-513
: Therapy
Praktický lékař se ve své ordinaci často setkává s úzkostnými a depresivními příznaky těhotných a kojících žen a rozhoduje se o jejich léčbě. Důležitá je základní orientace v problematice farmakoterapie duševních poruch v těhotenství a laktaci včetně posouzení zisků a rizik. Podstatné je rozhodnutí kdy léčit psychoterapií nebo jinými přístupy, a kdy je naopak nezbytné zahájit léčbu psychofarmaky. V článku jsou uvedeny základní principy farmakoterapie úzkostných a depresivních poruch v těhotenství a laktaci. Zdůrazněna je interdisciplinární spolupráce gynekologa, praktického lékaře, porodníka, neonatologa a genetika.
Klíčová slova:
těhotenství, laktace, úzkostné poruchy, depresivní poruchy, psychofarmaka.Úvod
Praktický lékař ve spolupráci s ošetřujícím gynekologem a později porodníkem se často setkává s objevujícími se psychickými problémy nebo zhoršením stávajících potíží těhotných žen. Těhotenství, porod a poporodní období jsou důležité etapy v životě ženy a celé rodiny. A jakékoliv potíže jsou přijímány s velkou úzkostí a nejistotou. Praktický lékař většinou v prvním kroku řeší, jakého typu jsou potíže, zda somatické, nebo psychické, nebo obojí, zda se jim má věnovat sám, nebo předat léčbu pacientky zcela psychologovi nebo psychiatrovi a jak postupovat ve vzájemné spolupráci s gynekologem.
Pokud pacientka měla psychické potíže, nebo byla přímo léčena psychiatrem, tak je situace jednodušší, protože ambulantní psychiatr by měl léčbu zvládat ve vzájemné spolupráci všech odborníků. Vzájemná spolupráce a informovanost je vždy důležitá, ale v těhotenství nabývá větší závažnosti, protože se jedná nejen o matku, ale i o vývoj dítěte. Ani období šestinedělí nelze zvažovat samostatně, ale vždy v souvislosti s tím, jak probíhalo těhotenství, jaké psychické problémy byly přítomny nebo se objevily a dále jaký byl psychický stav pacientky během porodu a po porodu.
V období po porodu jsou ženy výrazně citlivější, a může docházet k rozvoji deprese, úzkostné nebo i psychotické poruchy. Psychické poruchy mohou nově akutně vzniknout, nebo dojde ke zhoršení až k relapsu onemocnění. Psychický stav žen v tomto období nelze nikdy podceňovat, a musíme počítat se zvýšenou zranitelností vůči psychiatrickým onemocněním v období 3 měsíců po porodu.
Pokud se rozhodneme léčit farmaky těhotnou nebo kojící ženu, je to vždy dilema. Na jedné straně je nutné zvážit rizika, která může podání léků přinést pro plod či kojence a na straně druhé negativní následky neléčené psychické poruchy pro ženu, anebo dítě. Obecně znalosti o účincích léků na plod jsou limitované, nejčastěji pocházejí ze studií na zvířatech, kazuistik, hlášení o nežádoucích účincích, registrů žen vystavených konkrétnímu léku během těhotenství, anebo epidemiologických studií.
K léčbě psychofarmaky gravidních nebo kojících žen přistupujeme v situaci, kdy nefarmakologické, zejména psychoterapeutické postupy, nelze použít, anebo pokud je jejich účinnost limitována závažností psychických symptomů. V takovém případě je třeba zvážit všechna potenciální rizika.
Vysazení medikace je v mnoha případech pro matku spojené s rizikem relapsu nebo zhoršení průběhu a celkového výsledného stavu onemocnění. V případě neléčené duševní poruchy jsou plod a dítě ohroženi, kromě možných přímých vlivů duševní nemoci na vývoj a porodní komplikace, především nedostatečnou péčí v důsledku onemocnění matky, eventuálně jejím sebevražedným jednáním či dokonce infanticidou.
Mezi nejzávažnější rizika pro plod a kojence v důsledku podávání léků patří
- úmrtí plodu,
- kongenitální malformace,
- neonatální toxicita,
- intoxikace a abstinenční symptomy novorozenců.
Dále dlouhodobé neurobehaviorální následky, jako jsou
- defekty a opožděný vývoj centrálního nervového systému,
- kognitivní poruchy,
a konečně poruchy vývoje:
- sedace,
- váhový úbytek,
- dechový útlum kojenců.
Teratogenní efekt léku závisí na míře jeho teratogenního potenciálu, na dávce a na době podávání. Nejkritičtější dobou pro vznik orgánových malformací je prvních 12 týdnů vývoje plodu. Rizika teratogenity jsou nejčastěji určována podle kategorií americké Food and Drug Administration – FDA (tab. 1).
1. Rizika teratogenity některých psychofarmak (podle U.S. Food and Drug Administration 2007) 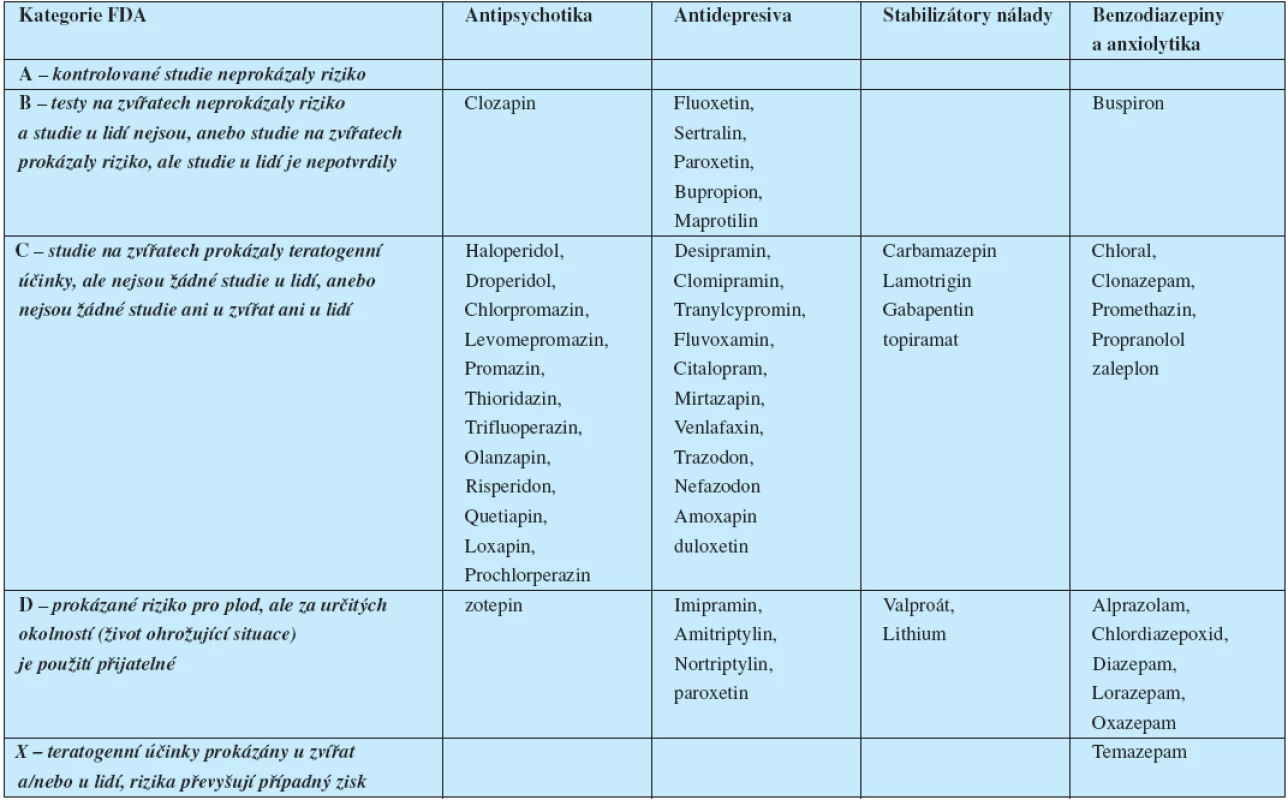
Těhotenství žen léčených psychofarmaky by mělo být vždy plánované, abychom měli možnost upravit farmakoterapii již před koncepcí, ale až polovina těhotenství je neplánovaných. Některé ženy, které užívaly farmaka a otěhotněly, pak žádají o přerušení těhotenství z obav o zdraví a vývoj dítěte. Lékař se pak dostává do náročné situace, protože pacientky většinou požadují jasné doporučení, které není jednoduché. Lékař je zde v přesně definované roli odborníka, který může doporučit optimální terapii a zvážit spolu s pacientkou veškerá rizika. V této situaci je vždy výhodné, pokud má lékař možnost pohovořit současně s partnerem pacientky či s nejbližší rodinou. V klinické praxi se opakovaně osvědčilo, když o možném riziku a doporučení dalšího postupu léčby byla informována jak pacientka, tak její manžel.
Z forenzních důvodů je třeba dostatečné informování pacientky dokumentovat. Je-li farmakoterapie indikovaná, je indikovaná i v těhotenství a indikace musí být jasná. Pokud máme pochyby, zda přípravek nemůže poškodit plod, tak pošleme zprávu gynekologovi a můžeme i konzultovat genetika, případně napíšeme porodníkovi, z jakého poškození plodu máme obavy. Genetik s porodníkem zajistí prenatální diagnostiku plodu. Nikdy nedoporučujeme kvůli farmakoterapii interrupci. To je problém gynekologa a porodníka.
Graviditu u většiny psychicky nemocných žen považujeme za rizikovou pro matku i pro plod. Plánujeme častější kontroly, pátráme po případných prodromech relapsu a pečlivě vážíme všechny benefity a rizika léčby. Údaje o farmakologické léčbě depresivních a úzkostných poruch jsou aktuálně aktualizované (1).
Dalším problematickým obdobím je laktace.
Vzhledem k tomu, že prakticky všechna psychofarmaka přestupují do mateřského mléka, je třeba věnovat pozornost jejich farmakokinetice a zvážit možnost zástavy laktace při pokračující farmakoterapii. Vylučování psychofarmak do mateřského mléka v průběhu dne kolísá, liší se také koncentrace v předním a zadním mléku (vyšší je v zadním). Pokud matka trvá na kojení, pak by se měl lék podávat před nejdelší spánkovou periodou dítěte (tedy večer nakojit a pak užít léky) (2).
Depresivní poruchy
Prevalence depresivní poruchy v graviditě je stejná jako u negravidních žen. Celoživotní riziko onemocnění depresí u žen je uváděno v rozmezí 10–25 %. Relaps depresivní poruchy v graviditě značně zvyšuje riziko poporodních komplikací, nedostatečné péče o dítě či špatné výživy a navíc je prediktorem poporodní deprese. Rizikovými faktory jsou:
- předchozí anamnéza depresivní poruchy,
- mladší věk,
- omezená sociální podpora,
- osamělost a vyšší počet dětí,
- manželské konflikty,
- ambivalentní pocity ohledně gravidity (3).
V naturalistické prospektivní studii souboru 201 žen s anamnézou deprese došlo v těhotenství k relapsu až u 43 % žen (4). Depresivní porucha v graviditě je spojována s nižší porodní hmotností či předčasným porodem a zvyšuje se výskyt dráždivosti u novorozence (5).
V poporodním období se velmi často objevuje zhoršená nálada. Až 50–80 % žen prožívá ve třetím až čtvrtém dni po porodu krátkou epizodu zhoršené nálady, projevující se typicky zvýšenou přecitlivělostí, úzkostností, podrážděností, kolísáním nálady a epizodami pláče. Objevují se pocity strachu a neschopnosti vnímat lásku k novorozenci a z toho vycházející sebeobviňování. Mohou se objevit poruchy spánku.
Tato krátkodobá změna v náladě je způsobená prudkým poklesem hormonů estrogenů a progesteronu. Častěji se objevuje u prvorodiček, adolescentních dívek a žen, které mívají premenstruální tenzi. Příznaky trvající déle než 14 dní mohou znamenat riziko rozvoje vážnější poporodní deprese. Poporodní blues není důvodem k žádné terapii.
Poporodní deprese postihuje 12–16 % žen a u žen s anamnézou deprese až 25 % (6). V etiopatogenezi jsou zvažovány biologické faktory (poruchy cirkadiánních rytmů v období hormonálních změn) a psychosociální faktory (porod a šestinedělí, starost o dítě). Mezi příznaky poporodní deprese převládají pocity
- insuficience,
- nerozhodnosti,
- úzkosti,
- strachu ze samoty,
- bezmoci,
- beznaděje,
- katastrofické obavy z budoucnosti,
- ztráty zájmů,
- poruchy příjmu potravy.
Ženy mají pocit, že dítě asi nechtěly a nedokážou je milovat. Pravidelná schopnost postarat se o dítě klesá. Jako u každé depresivní poruchy i zde se samozřejmě mohou objevit psychotické příznaky. Jde o sebeobviňující se bludy, které mohou být rozšířeny i na dítě, a pak hrozí nebezpečí sebevraždy a až zabití dítěte. Pacientka bývá v silném napětí, může halucinovat a její nálada je zpravidla neodklonitelná. Vždy je třeba pátrat, zda pacientka nemá sebevražedné úvahy.
V případě dlouhodobějšího trvání se objevuje nadměrná únava až vyčerpanost, podrážděnost a sebevýčitky, neschopnost komunikovat s okolím, úporná nespavost, nechutenství a hubnutí. Rizikovými faktory jsou:
- epizoda deprese v anamnéze a depresivní epizoda při minulém porodu,
- nedostatečná sociální podpora,
- negativní životní události,
- nestabilita partnerského stavu, a
- ambivalence týkající se těhotenství.
Z klinické praxe je známá zkušenost, že laické ujišťování ze strany rodiny pacientky, že kvůli dítěti by nebyla schopna sebevražedného jednání, je zcela nesmyslné. Při hodnocení závažnosti musíme vycházet z aktuálního osobního rozhovoru s pacientkou, nikoli z údajů sdělených třetí osobou, a dle toho volit další postup. Obecně platí, že prvotní je zvládnutí závažné symptomatologie matky, i za cenu např. zastavení laktace a medikace vysokými dávkami farmak, nebo i hospitalizace. Vždy je třeba zohlednit závažnost těchto rizikových faktorů:
- závažnost deprese,
- výskyt sebevražedného a sebepoškozujícího jednání aktuálně a v anamnéze,
- stupeň funkčního postižení aktuálně a v anamnéze (schopnost základní péče o sebe, schopnost navštívit lékaře),
- riziko plynoucí z nemoci matky pro plod či dítě (schopnost zajistit výživu, hygienu a bezpečnost),
- diferenciálně diagnosticky vyloučit jinou psychiatrickou diagnózu ( psychóza s počátkem v poporodním období, relaps psychotického onemocnění, bipolární porucha, obsedantně kompulzivní porucha).
Léčba depresivní poruchy v graviditě a po porodu se řídí obecnými zásadami léčby deprese, nicméně má svá specifika. Rozlišujeme léčbu nefarmakologickou a farmakologickou. V prvé řadě uvažujeme o možnosti začít léčbu pomocí psychoterapie.
Psychoterapie depresí v těhotenství a po porodu
V ordinaci praktického lékaře můžeme pacientce nabídnout pouze základní podpůrnou psychoterapii, kde věnujeme pacientce dostatek prostoru a mapujeme a probíráme psychosociální stresory – nedostatečnou sociální podporu, absenci partnera nebo konfliktní partnerský život a přidružené choroby. V případě závažnější deprese doporučujeme pracovníka specializovaného v psychoterapii nebo zvolíme léčbu farmakologickou (7).
Farmakoterapie depresivní poruchy v těhotenství a laktaci
Antidepresivum by mělo mít dokumentovanou bezpečnost užití v těhotenství (u léků déle užívaných je k dispozici více informací). Při dávkování léku je třeba zohlednit vztah mezi účinností a plazmatickou koncentrací léku, zvýšeným hepatálním metabolismem v těhotenství a změnou distribučního objemu. Rizikové období pro nasazení léku je počátek těhotenství a první trimestr. Při volbě antidepresiva volíme lék s nízkým rizikem teratogenity, nízkým počtem metabolitů, krátkým poločasem vylučování a nízkým výskytem nežádoucích účinků.
Zvýšená rizika teratogenity nebyla původně prokázána ani pro tricyklická antidepresiva (TCA), ani pro selektivní inhibitory vychytávání serotoninu (SSRI).
Především skupina SSRI se považovala za relativně bezpečnou při podávání v těhotenství. Data z rozsáhlých populačních studií s desetitisíci porody sice ukázala na možnou souvislost s některými typy vrozených vad, jako jsou
- vady septa a omfalokéla (sertralin),
- defekt pravé komory (paroxetin),
- anencefalie,
- kraniosytóza (SSRI jako skupina).
Absolutní riziko těchto vad je však nízké.
Studie z Kanady u 120 000 porodů ukazuje, že kombinace SSRI s benzodiazepiny zvyšuje riziko vrozených srdečních onemocnění, zatímco monoterapie SSRI zvyšuje incidenci vrozených vad septa (8).
Zajímavé je, že délka antidepresivní terapie v průběhu prvního trimestru nesouvisí s výskytem malformací (9). Na základě epidemiologických studií a údajů registru výrobce se ukazuje, že užívání paroxetinu v prvním trimestru zvyšuje oproti ostatním antidepresivům riziko všech malformací 2,2 krát (na 4 % oproti 3 % v populaci). Riziko malformací se objevuje jen při dávce vyšší než 25 mg paroxetinu (10). Ostatní sledovaná antidepresiva (citalopram, fluoxetin, sertralin) riziko nezvyšovala (11). Na základě publikovaných údajů nová antidepresiva (venlafaxin, mirtazapin, bupropion, trazadon, nefazodon) nezpůsobují zvýšený výskyt malformací (12).
Pokud jde o neonatální komplikace, antidepresiva jsou obecně spojována s častějšími potraty, mají za následek nižší gestační věk a předčasné porody (13). SSRI mohou způsobovat nižší porodní hmotnost a respirační tíseň (14).
Většina neonatálních symptomů je přechodných, zhoršují se však kombinacemi léků (především s benzodiazepiny). Poporodní komplikace pravděpodobně nezávisejí na době expozice (časná nebo pozdní fáze těhotenství), ale na její délce – čím je delší, tím je vyšší riziko (15). Přechodné neonatální komplikace odpovídají syndromu z vysazení až v 30 %. Bylo také popsáno až 6x zvýšené riziko plicní hypertenze u novorozenců po expozici SSRI ve třetím trimestru (16).
Většina studií neprokázala neurobehaviorální toxicitu TCA a SSRI s výjimkou jedné studie v malém souboru dětí, kdy bylo nižší skóre Apgarové a pomalejší psychomotorický vývoj u dětí matek léčených SSRI.
Antidepresiva rovněž přestupují do mateřského mléka, údaje o jejich toxickém působení jsou kazuistické a naopak v některých studiích nebyly popsány nežádoucí účinky u kojenců. Dostupné údaje ukazují, že nejnižší riziko mají kojenci, jejichž matky užívají imipramin, nortriptylin, sertralin a fluvoxamin, vyšší je při užívání paroxetinu a nejvyšší u citalopramu, fluoxetinu a duloxetinu (18).
Alternativou farmakoterapie může být třezalka, repetitivní transkraniální stimulace (18), fototerapie, elektrokonvulzivní léčba (19) a psychoterapie.
Principy pro léčbu antidepresivy v graviditě a laktaci (2)
- Preferujeme nefarmakologické terapeutické intervence, zejména psychoterapii. Bezpečnou alternativou jsou také elektrokonvulze nebo repetitivní transkraniální magnetická stimulace.
- Nízké riziko teratogenity vykazují tricyklická antidepresiva, některá SSRI (fluoxetin) a na základě dostupných údajů i novější antidepresiva (venalafaxin, mirtazapin, bupropion)
- Preferujeme monoterapii, při nejnižším možném dávkování. Vyšší dávky paroxetinu jsou spojeny se vznikem malformací, vyšší dávky venlafaxinu mohou vést k hypertenzi.
- Podávání SSRI matce po 20. týdnu gravidity může zvýšit riziko perzistentní plicní hypertenze u novorozence.
- K prevenci abstinenčního syndromu u novorozenců se doporučuje, je-li to možné, vysazení antidepresiv jeden až dva týdny před plánovaným termínem porodu
- Při podávání antidepresiv doporučujeme zvážit kojení. Nízké koncentrace v mateřském mléku jsou zjištěny u imipraminu, nortriptylinu, sertralinu a fluvoxaminu, vyšší koncentrace jsou u citalopramu a fluoxetinu.
Úzkostné poruchy
Samotná gravidita se může pro ženy stát zdrojem významné úzkosti a často bývá spojena s prožíváním úzkostných stavů a nepohody. Chtěné těhotenství bývá pokládáno za radostnou událost, a lidé tradičně věří, že je spojeno s klidem, vnitřním vyrovnáním, které vede k dozrávání ženy a ke zvýšení sebevědomí. U nejistých a úzkostných žen rodina očekává zlepšení, protože doufá, že narození dítěte znamená nalezení smyslu života a seberealizace. Skutečností ale je, že značná část těhotných žen a nových maminek bývá v některých obdobích více úzkostná a hodně přemýšlí o nastávající zodpovědnosti. Objevuje se větší únavnost a pocity celkové slabosti, starosti a obavy, náladovost a podrážděnost, problémy s koncentrací, vegetativní příznaky úzkosti. Většinou jsou tyto projevy pokládány za celkem normální, ale mohou být i prvními příznaky rozvíjející se úzkostné poruchy. Řada úzkostných poruch se v těhotenství zhoršuje, nebo objevuje poprvé.
Závažná úzkostná porucha v těhotenství nebo v poporodním období může ohrožovat matku, dítě i celou rodinu. Pokud jde o přímý a nepřímý dopad úzkosti matky v průběhu gravidity na vývoj a chování plodu, pak výsledky studií zůstávají nejednoznačné. Zejména původní předpoklady, že vysoká míra úzkosti matky zodpovídá za nižší porodní hmotnost či předčasný porod, nebyly jednoznačně potvrzeny. Plod a později kojený novorozenec mohou být ovlivněny i řadou dalších faktorů, které souvisí z úzkostnou poruchou druhotně:
- častější abúzus alkoholu a drog (souvisí s častějšími malformacemi a poškozením dítěte),
- špatná životospráva včetně kouření,
- rozvrat partnerského vztahu a zhoršení péče o novorozeně (20).
Biologickým podkladem úzkostných poruch v graviditě a poporodním období jsou pravděpodobně hormonální změny v organismu ženy a dysfunkce serotonergního systému. Významnou roli hrají sociální a psychologické faktory a anamnéza životních událostí. Rizikové jsou anamnéza ztráty dítěte nebo narození postiženého dítěte, anamnéza psychické poruchy včetně poruch spánku, stres spojený s těhotenstvím, somatické potíže nebo choroby v těhotenství, sociální a partnerské nejistoty. Při rizikovém těhotenství, a zejména když musí být žena hospitalizována, narůstá incidence duševních poruch až dvojnásobně.
Klinické příznaky úzkostných poruch v těhotenství a poporodním období se významněji neliší od běžných příznaků celého spektra úzkostných poruch. Během těhotenství se výrazně objevují obavy z toho, jak budoucí matka zvládne porod a péči o dítě. S tím je pak spojené sebepodceňování a zvýraznění nejistot. Navíc se objevuje strach z porodu a porodních bolestí, mateřská separační úzkost, fobické vyhýbání se dítěti.
Těhotenství a období po porodu představují riziková období pro počátek obsedantně kompulzivní poruchy. Průběh panické poruchy v graviditě bývá proměnlivý, se zlepšením i zhoršením. Posttraumatická stresová porucha s plně vyjádřenou symptomatikou se může objevit jako následek nejen komplikovaného, ale i zdánlivě neproblematického porodu, po spontánním potratu, popřípadě porodu mrtvého plodu.
V ambulanci Psychiatrického centra pro gravidní a kojící pacientky se nejčastěji objevují úzkostné poruchy (2). Poruchy spánku jsou častou stížností těhotných žen (až 88 %). V posledních fázích gravidity bývá relativně často popisována spánková apnoe. Poruchy spánku přetrvávají i po porodu a bývají i horší, zejména diky intenzivní péči o dítě. V souvislosti s poruchami spánku je pak větší riziko relapsu psychického onemocnění.
Léčba úzkostných poruch v těhotenství a v šestinedělí
V léčbě úzkostných poruch zvažujeme anamnézu psychických obtíží a jejich závažnost a preferenci pacientky. Většina žen se bojí užívat v těhotenství jakékoliv léky, a proto musí být lékař dobře informován o variantách léčby.
Jednou z možností léčby úzkostných poruch v tomto období je psychoterapie. V ordinaci praktického lékaře je nejdůležitější podpůrná psychoterapie. Specializovanější psychoterapie by měli provádět kvalifikovaní pracovníci. Specializovaná kognitivně behaviorální terapie (KBT) úzkostných poruch v těhotenství po porodu se v zásadě neliší od KBT úzkostných poruch, zohledňuje však specifickou situaci a častěji spolupracuje s partnerem a rodinou. Při zahájení léčby je terapeutický proces zaměřený na posílení motivace pacientky ke spolupráci, zvýšení naděje na změnu, vytvoření léčebného kontraktu, konstruktivního terapeutického vztahu.
Při práci s partnerem nebo rodinou je pak důležité vytvořit kontrakt o sociální podpoře. Na cílech se musí terapeut s pacientkou shodnout, musí být jasné a dosažitelné. V řešení životních problémů se zaměřuje na problémy pacientky a její rodiny (20).
Farmakoterapie úzkostných poruch
Ve farmakoterapii úzkostných poruch se stále často používají benzodiazepiny, i když pro dlouhodobější léčbu jsou vhodnější antidepresiva, především SSRI. Pro farmakoterapii antidepresivy platí i u úzkostných poruch stejná pravidla jako při léčbě deprese.
Benzodiazepiny a jiná anxiolytika
Stejně jako všechna ostatní psychofarmaka i benzodiazepiny přestupují přes placentu do krevního oběhu plodu. Pokud jde o teratogenní účinky, na základě výsledků starších studií se předpokládalo, že expozice benzodiazepinům v prvním trimestru těhotenství je spojená se zvýšeným výskytem rozštěpu rtu a patra. Novější práce však tyto údaje zpochybňují, a závěry jsou ve většině případů přinejmenším rozporuplné.
V rozsáhlé metaanalýze bylo potvrzeno zvýšené riziko výskytu rozštěpu po expozici benzodiazepinům v průběhu prvního trimestru (21). Další metaanalýza jiných autorů nenašla významnou souvislost mezi léčbou benzodiazepiny a výskytem malformací (22). A ve studiích, které měly kontrolní soubory, byl výskyt velkých malformací i rozštěpů statisticky častější u žen, které užívaly benzodiazepiny.
Vyšší počet vrozených malformací bývá také vysvětlován současným užíváním alkoholu a drog. Novější populační studie ze Švédska prokázala u souboru 1 979 dětí matek, které v těhotenství užívaly benzodiazepiny nebo benzodiazepinová hypnotika, zvýšené riziko předčasného porodu a nízké porodní hmotnosti ve srovnání s kontrolním souborem (23).
Nejvíce údajů o teratogenním působení benzodiazepinů existuje o diazepamu a alprazolamu, naopak žádné malformace nebyly hlášeny po lorazepamu (který v současné době není bohužel v ČR dostupný). Vrozené defekty byly také popsány u 3 porodů z 19 u žen, které byly léčeny clonazepamem (24).
Betablokátory nejsou považovány za teratogeny, ale mohou způsobit bradykardii plodu, a proto je vhodné je vysadit 1–2 týdny před plánovaným porodem. Zvířecí studie neprokázaly žádné abnormity při užívání zopiclonu, a vzhledem k dosavadním pozitivním zkušenostem s jeho užíváním u těhotných žen jej lze použít v graviditě. O zolpidemu a zaleplonu není dosud k dispozici dostatek informací.
Na základě studií na zvířatech se předpokládá, že benzodiazepiny by mohly mít neurobehaviorální toxicitu, nálezy jsou však nejednoznačné (25). V poporodním období a během laktace je třeba mít na paměti, že benzodiazepiny se vylučují do mateřského mléka, a proto by se jim měly kojící matky vyhnout.
Mezi hlavní vedlejší projevy podávání anxiolytik u novorozenců patří sedace a závislost s abstinenčními symptomy. Opakované podávání dlouhodobě působících benzodiazepinů může způsobit navíc i poruchy krmení a váhový úbytek kojence. Vzhledem k tomu, že prvních 3–5 dní po porodu se benzodiazepiny nekonjugují s kyselinou glukuronovou, udává se rovněž zvýšení rizika vzniku novorozenecké žloutenky (26).
U novorozenců závislých na benzodiazepinech (i při terapii nízkými dávkami) byl popsán „floppy infant“ syndrom. Tento syndrom se objevuje zejména při vyšších dávkách (více než 30 mg diazepamových ekvivalentů denně) a při terapii dlouhodobě působícími benzodiazepiny, např. nitrazepamem. V době porodu se může syndrom objevit i u novorozenců, u kterých vznikla závislost v důsledku terapie matky nízkými dávkami benzodiazepinů v době gravidity.
Mezi abstinenční příznaky patří:
- hypertonus,
- hyperreflexie,
- neklid,
- podrážděnost,
- křeče,
- porucha spánkového rytmu,
- neutěšitelný pláč,
- třes končetin,
- bradykardie,
- cyanóza,
- žvýkací pohyby, a
- roztažení břicha.
Tyto příznaky se mohou objevit krátce po porodu až do 3 týdnů a mohou trvat i několik měsíců.
Nežádoucí účinky nebyly zaznamenány po podání oxazepamu, lorazepamu a temazepamu. Na základě studií sledujících jeho vylučování u zvířat by neměl být podáván buspiron. Chloral sice rovněž může vyvolat sedaci, nicméně riziko je malé a pediatři jeho podávání při kojení doporučují.
Z hypnotik se zopiclon vylučuje v až 50 % mateřské dávky, proto je pravidelné užívání kontraindikováno. Nicméně jednorázová dávka 7,5 mg zopiclonu je pravděpodobně bezpečná, neboť nedochází k jeho akumulaci. Také zaleplon se vylučuje do mateřského mléka. Zolpidem je málo lipofilní a rychle se začíná vylučovat a tak se nachází v mateřském mléce jen v zanedbatelném množství (2).
Principy pro léčbu anxiolytiky a hypnotiky v graviditě a laktaci (2)
- Farmakoterapii se pokud možno vyhýbáme, preferujeme nefarmakologické intervence, psychoterapii, zejména kognitivně behaviorální terapii – KBT.
- Ve farmakoterapii specifických úzkostných poruch, jako jsou panická porucha nebo obsedantně kompulzivní porucha, jsou v těhotenství i laktaci léky volby antidepresiva (SSRI).
- Benzodiazepiny lze podávat po časově omezenou dobu v počátečních akutních stádiích onemocnění v nejnižší účinné dávce. Indikací k jednorázovému podání mohou být stavy extrémní úzkosti a agitovanosti. Nedoporučujeme podávat benzodiazepiny v prvním trimestru těhotenství. vzhledem k zvýšenému riziku kongenitálních malformací.
- Pokud jsou benzodiazepiny v těhotenství nezbytné, pak by měly dostat přednost krátkodobě působící (oxazepam, alprazolam lorazepam,) před dlouhodobě působícími benzodiazepiny (diazepam, clonazepam). V preventivní terapii je výhodnější lorazepam oproti alprazolamu (působí dlouhodoběji, nemá aktivní metabolity a zdá se, že nevyvolává u novorozenců náhlý a tak závažný abstinenční syndrom). V současnosti není lorazepam v ČR dostupný. Z dalších benzodiazepinů s krátkým poločasem lze doporučit podání oxazepamu.
- Pokud to závažnost symptomů těhotné ženy dovoluje, pak jako prevence abstinenčních syndromů novorozence by se měla dávka benzodiazepinů snižovat a postupně vysadit do dvou týdnů před plánovaným porodem. Vysazení musí být pozvolné a je třeba pamatovat na riziko relapsu onemocnění.
- Pokud jde o léčbu nespavosti v těhotenství, dosavadní limitované údaje o zopiclonu potvrzují nálezy ze studií na zvířatech, které neprokázaly jeho teratogenitu.
- V období laktace jsou rovněž postupem volby nefarmakologické intervence, jako např. KBT, relaxační techniky, snížení stresu prostředí a úprava spánkové deprivace.
- Při rozhodování, zda kojit po dobu nutné farmakoterapie, je třeba vzít v úvahu věk a zdraví dítěte, nezbytné je informovat pacientku a jejího partnera o možných rizikách.
- Pokud matka na kojení trvá, pak jsou preferovány krátkodobě působící benzodiazepiny, jako je např. oxazepam. Preferujeme vždy monoterapii. Při laktaci jsou malé jednorázové dávky benzodiazepinů pravděpodobně spojeny s nízkým rizikem, zejména je-li kojenec monitorován pro ospalost.
- Pokud jde o léčbu nespavosti v těhotenství, dosavadní limitované údaje o zopiclonu potvrzují nálezy ze studií na zvířatech, které neprokázaly jeho teratogenitu.
- Pro nespavost doporučují pediatři při kojení zolpidem. Nízká dávka před usnutím a nekojit po několik následujících hodin může minimalizovat potenciální účinky na kojence.
Závěr
Období těhotenství, porodu a poporodní období je náročné pro matku i okolí a je třeba psychickým příznakům věnovat velkou pozornost. Především období po porodu a v šestinedělí je pro matku náročné a může dojít díky její zvýšené citlivosti a zranitelnosti k nenadálým komplikacím. Praktický lékař, který má v současnosti roli rodinného lékaře, má ve své péči nemocné s psychiatrickými poruchami a také ženy, které otěhotní, a teprve během těhotenství se objevují nejrůznější psychické obtíže. Praktický lékař je v první linii léčby a je proto důležitá základní orientace v možnostech léčby nejběžnějších psychických poruch.
Největší opatrnost je třeba věnovat informovanosti pacientky a její rodiny, a především si uvědomit, že duševní porucha ani léčba psychofarmaky nejsou indikací k přerušení těhotenství. Při závažných poruchách je nezbytná mezioborová spolupráce, a v současnosti máme možnost genetické konzultace a cílené prenatální diagnostiky. V Psychiatrickém centru Praha máme poradnu pro psychicky nemocné těhotné pacientky. V článku jsme nastínili problematiku a zájemcům o detailnější znalosti doporučujeme kapitoly v monografiích Postupy v léčbě psychických poruch (2) a Konsiliární psychiatrie (27).
Podpořeno výzkumným záměrem MZČR MZ0PCP 2005
MUDr. Dagmar Seifertová, CSc.
Psychiatrické centrum Praha
Ústavní 91
181 03 Praha 8 - Bohnice
E-mail: seifertova@pcp.lf3.cuni.cz
Sources
1. Mohr, P. Psychofarmaka v ordinaci praktického lékař podávaná v těhotenství a v laktaci. Prakt. Lék. 2007. 87. s. 11-16.
2. Mohr, P., Praško, J., Bareš, M. a kol. Psychické poruchy v graviditě a laktaci. In: Seifertová D., Praško J., Horáček J., Hoschl C. Postupy v léčbě psychických poruch. Academia Medica Pragensis a Medical Tribune, 2008, s. 483-493.
3. Bareš, M. Antidepresiva v léčbě depresivní poruchy v těhotenství a po porodu. Psychiatrie 2002, suppl. 2, s. 6–11.
4. Cohen, L.S., Altshuler, L.L., Harlow, B.L. et al. Relapse of major depression during pregnancy in women who maintain or discontinue antidepressant treatment. JAMA 2006, 295, p. 499–507.
5. MacGabe, J.H., Martinsson, L., Lichtenstein, P. et al. Averse pregnancy outcomes in mothers with affective psychosis. Bipolar. Disord. 2007, 9, p. 305–309.
6. Gotlib, I.H., Whiffen, V.E., Mount, H. et al. Prevalence rates and demografic charcteristics associated with depression in pregnancy and the postpartum. J. Consult. Clin. Psychol. 1989, 57, p. 269–274.
7. Praško, J. Psychoterapie poporodních depresí. Psychiatrie 2002, 6 (suppl. 2), s. 39-44.
8. Oberlander, T.F., Warburton, W., Misri, S. et al. Major congenital malformation following prenatal exposure to serotonin reuptake inhibitors and benzodiazepines using population-based linked health data. Birth Defects Res. B. Dev. Reprod. Toxicol. 2008, 83, p. 68–76.
9. Ramos, E., St-André, M., Rey, E. et al. Duration of antidepressant use during pregnancy and risk of major congenital malformations. Br. J. Psychiatry 2008, 192, p. 344–350.
10. Bérard, A., Ramos, E., Rey, E. et al. First trimester exposure to paroxetine and risk of cardiac malformations in infants: the importace of dosage. Birth Defects Res. B. Dev. Reprod. Toxicol. 2007, 80, p. 18–27.
11. Colem J.A., Ephross, S.A., Cosmatos, I.S., Walker, A.M. Paroxetine in the first trimester and the prevalence of congenital malformations. Pharmacoepidemiol. Drug Saf. 2007, 16, p. 1075 až 1085.
12. Cole, J.A., Modell, J.G., Haight, B.R. et al. Bupropion in pregnancy and the prevalence of congenital malformations. Pharmacoepidemiol. Drug Saf. 2007, 16, p. 474-484.
13. Suri, R., Altshuler, L.L., Hellemann, G. et al. Effects of antenatal depression and antidepressant treatment on gestational age at birth and risk of preterm birth. Am. J. Psychiatry 2007, 164, p. 1206-1213.
14. Oberlander, T.F., Warburton, W., Misri, S. et al. Neonatal outcomes after prenatal exposure to selective serotonin reuptake inhibitor antidepressants and maternal depression using population-based linked health data. Arch. Gen. Psychiatry 2006, 63, p. 898-906.
15. Oberlander, T.F., Warburton, W., Misri, S. et al. Effects of timing and duration of gestational exposure to serotonin reuptake inhibitor antidepressants. Population based study. Br. J. Psychiatry 2008, 192, p. 338–343.
16. Chambers, C.D., Hernandez-Diaz, S. Van Marten, L.J. et al. Selective serotonin-reuptake inhibitors and risk of persistent pulmonary hypertension of newborn. NEJM 2006, 354, p. 379-387.
17. Halberg, P., Sjoblom, V. The use of serotonin-reuptake inhibitors during pregnancy and breast-feeding: a review and clinical aspects. J. Clin. Psychopharmacol. 2005, 25, p. 59-73.
18. Klirova, M., Novak, T., Kopeček, M. et al. Repetitive transcranial magnetic stimulation (rTMS) in major depressive episode during pregnancy. Neuroendocrinol. Lett. 2008, 29, p. 69-70.
19. Seifertová, D. Elektrokonvulze v těhotenství. Psychiatrie 2002, suppl 2, s. 82-83.
20. Praško, J., Kosová, J., Herman, E. Psychoterapie úzkostných poruch v těhotenství a poporodním období. Psychiatrie 2002, suppl. 2, s. 47-57.
21. Altshuler, L., Cohen, L., Szuba, M.P. et al. Pharmacologic management of psychiatric illness during pregnancy: dilemmas and guidelines. Am. J. Psychiatry 1996, 153, p. 592-606.
22. Dolovich, L.R., Addis, A., Vaillancourt, J.M. et al. Benzodiazepine use in pregnancy and major malformations or oral cleft: meta-anylysis of cohort and case-control studies. BMJ 1998, 317, p. 839-843.
23. Wikner, B.N., Stiller, C.O., Bergman, U. et al. Use of benzodiazepines and benzodiazepine receptor agonists during pregnancy : neonatal outcome and congenital malformations. Pharmacoepidemiol. Drug Saf. 2007, 16, p. 1203-1210.
24. American Academy of Pediatrics, Committe on Drugs. Use of psychoactive medication during pregnancy and possible effects on the fetus and newborn. Pediatrics 2000; 105, p. 880-887.
25. Cohen, L.S., Rosenbaum, J.F. Psychotropic drug use in pregnancy: weighing the risks. J. Clin. Psychiatry 1998, 59 (suppl. 2), p. 18-28.
26. Arnon, J., Schechtman, S., Ornoy, A. The use of psychiatric drugs in pregnancy and lactation. J. Psychiatry Relat. Sci. 2000, 37, p. 205-222.
27. Seifertová, D., Čepický, P., Strunzová, V. a kol. Diagnostika a léčba psychických poruch v gynekologii, při těhotenství a laktaci. In: Konsiliární psychiatrie. Praha: Galén, Medical Tribune, 2007, s. 368-377.
Labels
General practitioner for children and adolescents General practitioner for adults
Article was published inGeneral Practitioner

2009 Issue 9-
All articles in this issue
- Burn out syndrome and assessment doctors
- Depression and anxiety in pregnant women
- Concept of discipline General Practice
- Previously expressed wishes or about human freedom and dignity
- Echocardiography and anticoagulation treatment of patients with cardioembolic stroke
- Dementia in a general practitioner‘s office
- Deliberate self-harm – a serious symptom and dangerous social phenomenon
- A comparison of the lifestyles of young healthy women with different smoking behaviours
- General Practitioner
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Depression and anxiety in pregnant women
- Deliberate self-harm – a serious symptom and dangerous social phenomenon
- Dementia in a general practitioner‘s office
- Echocardiography and anticoagulation treatment of patients with cardioembolic stroke
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

