-
Medical journals
- Career
Využití NBI v diagnostice a sledování pacientů s Barrettovým jícnem
Authors: J. Gregar 1; V. Procházka 1; P. Lužná 2; J. Ehrmann jr. 2,3
Authors‘ workplace: I. interní klinika gastro-enterologická a hepatologická, FN Olomouc , Ústav histologie a embryologie, LF UP Olomouc , Ústav klinické a molekulární patologie, LF UP Olomouc 1
Published in: Gastroent Hepatol 2012; 66(3): 165-169
Category: Digestive Endoscopy: Original Article
Overview
Cílem studie bylo vyhodnotit přesnost NBI (Narrow Band Imaging) endoskopie a zjistit schopnost NBI metody předpovědět dysplastické změny u pacientů s Barrettovým jícnem (BJ). Jednak obecně, jednak v predikci low-grade dysplazie (low-grade intraepiteliální neoplazie, LG) a high-grade dysplazie (high-grade intraepiteliální neoplazie, HG).
Materiál a metody:
Naše studie byla provedena na skupině 82 pacientů s diagnózou Barrettova jícnu. U těchto pacientů jsme srovnávali výsledky endoskopického vyšetření v NBI modu s histopatologickým nálezem. Všechny vzorky byly zhodnoceny dvěma zkušenými patology.Výsledky:
U 27 pacientů byl na základě NBI endoskopie podezřelý nález dysplazie, přičemž u 24 pacientů (88,9 %) byl tento nález histopatologicky potvrzen. U tří pacientů (11,1 %) byl histopatologický nález negativní. Na druhou stranu jsme zjistili vysoký podíl falešně negativních výsledků. Dysplazie byla histopatologicky určena u 40 pacientů (34 pacientů LG, 6 pacientů HG) z celkového počtu 82. Ze 34 pacientů s LG dysplazií (histopatologicky určenou) bylo pouze 18 (52,9 %) pozitivních v NBI endoskopickém nálezu, 16 pacientů (47,1 %) bylo negativních. Všichni pacienti s HG dysplazií potvrzenou histopatologicky byli v NBI endoskopii pozitivní.Závěr:
Pozitivní predikce dysplastických změn u Barrettova jícnu při NBI endoskopii byla 88,9 %. Proto se ukazuje, že NBI je velmi užitečná vyšetřovací metoda pro pacienty s Barrettovým jícnem.Klíčová slova:
Barrettův jícen – NBI (Narrow Band Imaging) – histologie – low-grade dysplazie (low-grade intraepiteliální neoplazie) – high-grade dysplazie (high-grade intraepiteliální neoplazie)Diagnóza Barrettova jícnu (BJ) je známa více než 50 let. Zprvu se Norman Barrett domníval, že jde o vrozený stav [1]. Dnes víme, že změny typické pro BJ jsou získané, jde o komplikaci refluxní choroby jícnu. Zájem o problematiku BJ v posledním desetiletí vzrostl. To je dáno především tím, že incidence adenokarcinomu jícnu se zvýšila za posledních 40 let čtyřnásobně [2]. Dalším důvodem zvýšeného zájmu je zdokonalení endoskopického zobrazení a možnost pozorování stále časnějších slizničních změn a patologií. BJ je náhrada dlaždicobuněčného epitelu jícnu epitelem cylindrickým, který má alespoň v některých úsecích charakter intestinální metaplazie [3]. Vzhledem k možnosti přechodu v dysplazii a následně v adenokarcinom je BJ prekancerózou. Dispenzarizace pacientů s tímto postižením je šancí k odhalení vysokého stupně dysplazie a časné formy adenokarcinomu.
Prevalence BJ je v celé populaci odhadována kolem 1 % [4]. U pacientů s refluxní chorobou jícnu je prevalence BJ odhadována až na 12 % [4], podrobněji však není zdokumentována. V 75 % jsou postiženi muži a průměrný věk pacientů je kolem 50 let. Asi 0,3–2,9 % pacientů s BJ dospěje do adenokarcinomu jícnu [5,7,10,12]. Pětileté přežívání pacientů s adenokarcinomem jícnu je méně než 14 % [2]. BJ zvyšuje riziko adenokarcinomu jícnu 30–200×, přičemž riziko adenokarcinomu se zvyšuje se stupněm dysplazie [2,6,10,11].
Současná doporučení odborných společností většiny zemí nevedou k většímu záchytu pacientů s vysokým stupněm dysplazie nebo časnou formou adenokarcinomu a jsou nazývány „hit and miss system“ [8]. Význam nově zavedených endoskopických technologií pro diagnostiku a dispenzarizaci není dosud zhodnocen. Z hlediska experimentálního je BJ ideálním modelem pro studium kancerogeneze [9]. Využitím nových endoskopických metod, např. NBI, zpřesníme diagnostiku BJ i odběr biopsií a můžeme předvídat histologické změny v reálném čase [8,10]. To by mohlo přinést změny stávajících dispenzárních programů, a zlepšit tak prognózu pacientů.
Cíl práce
Cílem práce bylo zhodnotit schopnost predikce histologických změn na podkladě NBI endoskopického vyšetření u pacientů se známou diagnózou BJ.
Materiál a metodika
Na II. interní klinice FN Olomouc byla od roku 2005 vytvořena databáze celkem 106 pacientů s BJ (v roce 2005 retrospektivně vyhledáno ze zdravotní dokumentace a od roku 2005 také doplňováno o nově diagnostikované pacienty). Z této databáze 106 pacientů souhlasilo s dalším prospektivním sledováním dle protokolu projektu 82 pacientů. K hodnocení jsme nezařadili ty pacienty, kteří měli diagnózu BJ stanovenou nově a zatím neměli alespoň první endoskopickou kontrolu. Všech 82 pacientů zařazených do hodnoceného souboru bylo sledováno alespoň jeden rok a tito jsou i nadále prospektivně sledováni na II. interní klinice FN Olomouc. Charakteristika hodnoceného souboru viz tab. 1. Průměrný věk celého souboru je 61,8 let. Nejmladší pacient měl 19 let a nejstarší pacient 86 let. V souboru je 54 (65,85 %) mužů a 28 (34,15 %) žen. Průměrná délka BJ s použitím tzv. Pražské CM klasifikace byla C1,6 M 3,0 – po zaokrouhlení na jednotky běžně používané jde o C2M3.
Table 1. Charakteristika souboru pacientů. Tab. 1. Characteristics of the patient cohort. 
Endoskopická vyšetření byla provedena v souladu s doporučením České gastroenterologické společnosti. Všichni pacienti podepsali informovaný souhlas s endoskopickým vyšetřením horního zažívacího traktu a s odběrem biologického materiálu při endoskopii. K endoskopickému vyšetření byl používán přístroj Olympus GIF Q 260FZ s originálním 4mm capem (pro režim zoom). Přístroj nabízí možnost NBI sledování, zoomu a disponuje modalitou AFI (autofluorescence). Endoskopické nálezy hodnotili dva endoskopisté, jeden s praxí 25 let, druhý s praxí 5 let. BJ byl klasifikován s použitím tzv. Pražské CM klasifikace, která je dnes celosvětově uznávaným a doporučovaným standardem.
K hodnocení suspektních histologických změn při endoskopickém vyšetření bylo využito modality zobrazení pomocí technologie NBI se zoomováním, která je na našem pracovišti k dispozici více než 5 let. Klasifikace předpokládaných histologických změn byla hodnocena dle tzv. pitt patterns a vascular patterns – tedy změn slizniční architektury a změn vaskulární/kapilární sítě. K jednotnému hodnocení endoskopického nálezu v NBI zoom modu jsme použili modifikovanou klasifikaci dle Singha [8]. Klasifikace využívá 4 charakteristické obrazy:
- A – round pits – známka intestinální metaplazie bez dysplazie
- B – villous pits – známka intestinální metaplazie bez dysplazie
- C – absent pits s pravidelnou strukturou cévek – známka intestinální metaplazie bez dysplazie
- D – distorted pits s nepravidelnou strukturou cévek – známka dysplazie
Typy A, B a C jsou suspektní pro histologický nález bez dysplazie. Typ D je známkou možné dysplazie.
Bioptické vzorky byly odebírány jedním druhem endoskopických kleští od dvou různých výrobců (s bodcem, systém swing jaw s výklopnými branžemi). Prvně byla bioptována ložiska suspektních změn v NBI obraze, poté jsme pokračovali v protokolárním odběru biopsií dle doporučení České gastroenterologické společnosti (odběry z jednotlivých kvadrantů, po 1–2cm až nad makroskopicky patrné změny typické pro BJ). Při odběru materiálu k histologickému vyšetření jsme nezaznamenali žádnou komplikaci. Z endoskopií byl pořizován DVD záznam na DVD rekordér a také fotodokumentace na paměťovou kartu (xD, ve formátu jpeg). Lokální anestetikum (xylocain) ke znecitlivění hrdla jsme používali jen na přání pacienta. Analgosedaci či celkovou anestezii jsme k endoskopickému vyšetření využili jen u dvou pacientů (oba měli gastroskopie prováděny v analgosedaci pro intoleranci již dříve). Ostatní vyšetření proběhla bez anestezie. U všech vyšetření byl pacientem podepsán informovaný souhlas a o všech vyšetřeních je řádný záznam v nemocničním informačním systému FN Olomouc. Histologické vyšetření probíhalo standardním postupem, jen jsme u všech histologických vzorků použili tzv. „druhé čtení“ – každý vzorek byl hodnocen nezávisle dvěma zkušenými patology. Léčba pacientů probíhala v souladu s doporučením a současnými poznatky – pacienti byli léčeni inhibitory protonové pumpy (omeprazol, loseprazol, pantoprazol) a eventuelně i v kombinaci s prokinetikem (metoclopramid, itoprid).
Výsledky
Celkový počet hodnocených pacientů byl 82. Histologická analýza: 40 pacientů (48,8 %) z celkového počtu mělo histologický nález dysplazie (z toho 6 pacientů HG a 34 pacientů LG). Zbylých 42 pacientů (51,2 %) mělo nález BJ s intestinální metaplazií. Z 34 pacientů s histologickým nálezem LG dysplazie byl endoskopický nález pozitivní v 18 případech (52,9 %), v 16 případech (47,1 %) byl endoskopický nález negativní. Endoskopická analýza: Pozitivní endoskopický nález (predikovaná dysplazie) byl zjištěn u 27 pacientů, z toho byl u 24 pacientů (88,9 %) pozitivní také histologický nález a ve 3 případech (11,1 %) byl histologický nález negativní. Pozitivní prediktivní hodnota NBI endoskopie pro dysplastické změny je 88,9 %. Predikce dysplazie na základě NBI endoskopie byla u všech šesti pacientů s histologicky verifikovanou HG dysplazií. V resekátu sliznice u jednoho pacienta s histologicky verifikovanou HG dysplazií byl zachycen karcinom. I tento pacient měl pozitivní NBI endoskopické vyšetření.
Podrobnější rozbor 82 pacientů – parametry metody endoskopie NBI při porovnání výsledků vyšetření s histologickým nálezem ukazují následující tab. 2 a 3.
Table 2. Porovnání výsledků endoskopie a histologie. Tab. 2. Comparison of endoscopy and histology results. 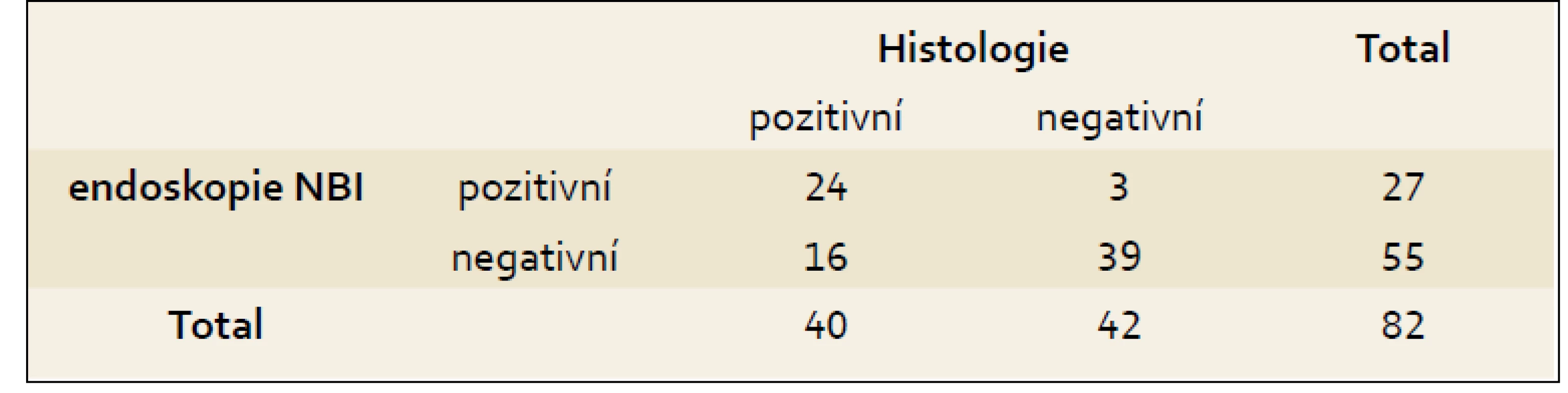
Table 3. Výsledky. Tab. 3. Results. 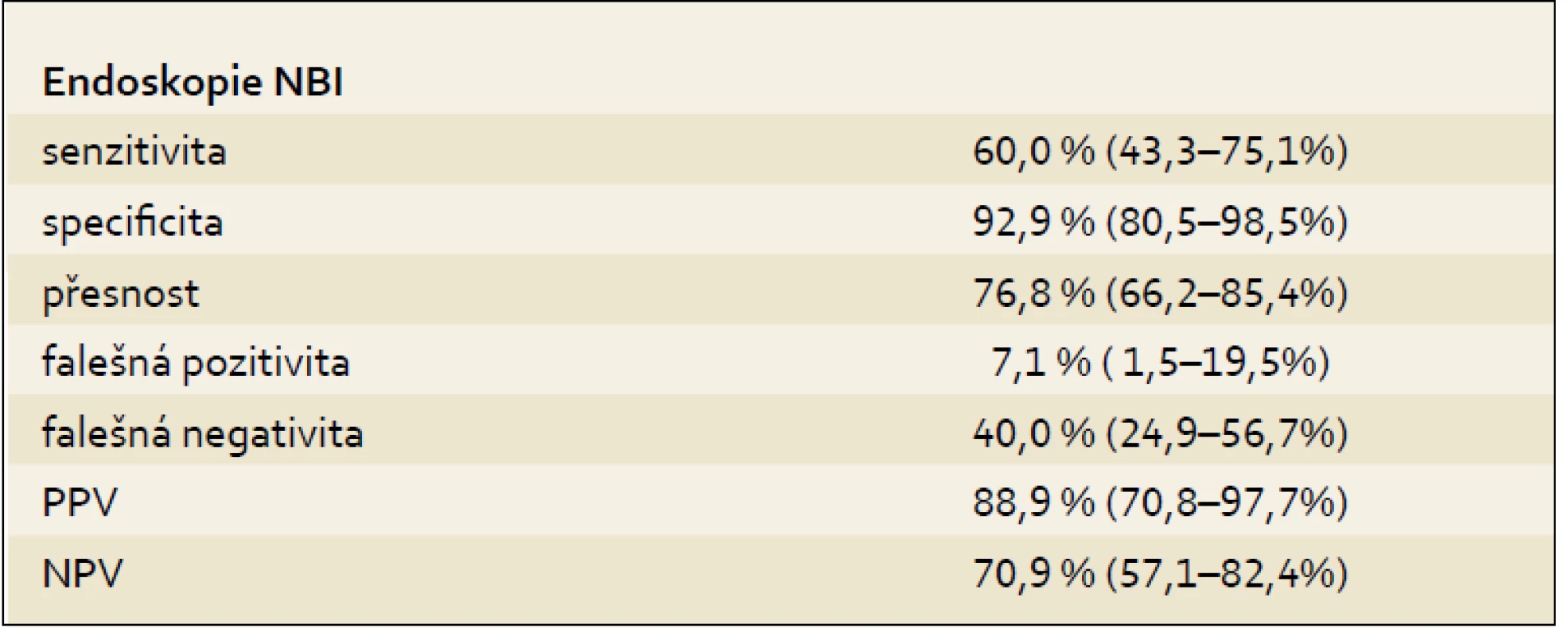
(95% CI) 95% interval spolehlivosti Diskuze
Využití NBI endoskopie v dispenzarizaci pacientů s BJ se jeví jako velmi přínosné. Nejde jen o primární diagnostiku BJ, který je často makroskopicky odlišitelný od fyziologického nálezu v jícnu již endoskopií klasickou, ale spíše o kontroly u pacientů s již známou diagnózou. Endoskopie s NBI pomáhá ve zhodnocení makroskopických změn, pomůže odhalit dysplastické změny a lépe zacílit biopsii. Použití NBI nenahrazuje zavedená doporučení pro odběry biopsií, ale může pomoci při odebrání cílené biopsie s přesnějšími závěry a větší výtěžností. Další bioptické odběry by už měly být odebrány dle doporučení v kvadrantech.
Zkvalitnění rozlišovací schopnosti endoskopů a možnosti speciálních technologií filtrace světla, které umožňují přesnější pozorování slizničních změn a cílený odběr biopsií, jsou velkým přínosem pro sledování pacientů s prekancerózou obecně [8,10]. Prakticky lze použít NBI firmy Olympus, I-scan firmy Pentax nebo F.I.C.E firmy Fuji. V našem případě jsme využili NBI firmy Olympus. Všechny uvedené endoskopické modality (Olympus, Pentax a Fuji) poskytují velmi podobné podmínky pro pozorování suspektních slizničních změn (osobní zkušenosti autorů). Při použití kombinace NBI a zoom endoskopie se dokonce hovoří o histologii v reálném čase, kdy endoskopující lékař, bez závislosti na svých zkušenostech, je s vysokou korelací schopen odhadnout budoucí histologický nález patologa [8].
Otázkou je, zda má smysl sledovat poměrně heterogenní skupinu pacientů s BJ, když riziko vzniku adenokarcinomu je 0,5–2,0 % [2,12]. Recentní studie a práce publikované na světových kongresech a sympoziích ale naznačují, že prevalence BJ je zřejmě vyšší, než se dosud předpokládalo. Alarmující je i fakt o stále se zvyšující incidenci adenokarcinomu jícnu [2,11,12]. Z praktického hlediska je důležité, že až 25 % pacientů s BJ má v době stanovení diagnózy již LG dysplazii [2]. Pacienti s LG dysplazií jsou skupinou s určitým maligním potenciálem a s možností tento potenciál ovlivnit. Z tohoto hlediska má NBI velký význam a přináší novou diagnostickou hodnotu. Pacienti s HG dysplazií jsou vysoce rizikoví (incidence adenokarcinomu je u nich odhadována až na 22 % během jednoho roku trvání BJ) a NBI zde také hraje důležitou roli. U méně než 10 % pacientů s nově diagnostikovaným adenokarcinomem jícnu víme o předchozí diagnóze BJ [7]. Z klinického hlediska naše práce zatím nedává jasné závěry pro BJ s HG dysplazií nebo adenokarcinomem jícnu, a to pro malé množství takových pacientů v našem souboru neumožňující statistické zpracování.
Relativně vysoký věk našeho souboru si vysvětlujeme tím, že takřka polovina souboru je z retrospektivní části databáze pacientů s BJ. Dle literatury jsou věkové průměry podobných souborů kolem 50–55 let. Průměrný věk našeho souboru je 61,8 let. Z pohledu podobných souborů v české populaci je ale průměrný věk našeho souboru srovnatelný [13,14]. V našem souboru máme relativně dost vysoký podíl pacientů s dysplazií, 48,8 %. Naše práce ale není demografickou studií a zařadili jsme i pacienty, kteří k nám byli odesláni z jiných pracovišť.
Dalším aspektem je vlastní histologické vyšetření. V hodnocení dysplastických změn neexistuje absolutní shoda ani mezi patology. Právě shoda při vyhodnocení histologického nálezu low-grade dysplazie (low-grade intraepiteliální neoplazie) u BJ není vysoká. Pro patologa bývá problémem přesně odlišit low-grade dysplazii (low-grade intraepiteliální neoplazii) od reparačních změn, navíc často v terénu postiženém zánětem. Na základě našich výsledků je však možné navrhnout úpravu a doplnění současně platných doporučení ČGS pro sledování pacientů s BJ právě o využití technologie NBI: při endoskopickém vyšetření v NBI modu nejprve odběr bioptických vzorků z ložisek podezřelých z dysplastických změn a teprve potom kvadrantové biopsie
Závěry
Podařilo se nám vytvořit obsáhlý soubor pacientů s BJ, který je statisticky hodnotitelný – v evidenci máme 106 pacientů, do zpracování a vyhodnocení bylo zařazeno 82 pacientů. Na našem pracovišti se nám u pacientů s BJ podařilo zavést NBI endoskopii do rutinní praxe, a nabídnout tak pacientům kvalitnější vyšetření. Ověřili jsme možnost predikce očekávaných histologických změn při endoskopickém vyšetřování s použitím NBI a zoomu. Endoskopista je v 88,9 % schopen predikovat přítomnost dysplastických změn (LG nebo HG dysplazie). To je z klinického hlediska velmi důležité – NBI tedy nabízí hlavně zpřesnění místa odběru biopsie a omezení falešné negativity.
Stále ale existuje určitá skupina pacientů, u kterých při endoskopickém vyšetření nenacházíme změny typické pro možné dysplastické změny, a přesto je histologicky dysplazie potvrzena – naštěstí v našem souboru šlo vždy o LG dysplazii (tedy dysplazii s nižším maligním potenciálem). V neposlední řadě existuje i skupina pacientů s pozitivním endoskopickým nálezem, ale histologické změny odpovídající dysplazii nejsou nalezeny – endoskopická falešná pozitivita. NBI endoskopii s možností zoomu vidíme jako velmi přínosnou v možnosti predikce dysplazie u pacientů s BJ.
Práce byla podpořena granty IGA NS10279-3 (Ministerstvo zdravotnictví České republiky) a Vnitřní grant LF UP Olomouc, č. 91110121 a SM 6198959216 (Ministerstvo školství, mládeže a tělovýchovy České republiky).
Autoři děkují kolektivu pracovníků II. interní kliniky FN Olomouc za asistenci při endoskopických vyšetřeních a kolektivu pracovníků Ústavu klinické a molekulární patologie za zhotovení histologických preparátů.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Doručeno: 7. 2. 2012
Přijato: 10. 3. 2012
MUDr. Jan Gregar
II. interní klinika – gastro-enterologická a hepatologická, FN Olomouc
I. P. Pavlova 6, 775 20 Olomouc
Jan.Gregar@fnol.cz
Sources
1. Barrett NR. Chronic peptic ulcer of the oesophagus lined by columnar epithelium. Surgery 1957; 41(6): 881–894.
2. Devesa SS, Blot WJ, Fraumeni JF Jr. Changing patterns in the incidence of esophageal and gastric carcinoma in the United States. Cancer 1998; 83(10): 2049–2053.
3. Guidelines České gastroenterologické společnosti. http://www.cgs-cls.cz/zc/img//Cgs-cls/refluxni_choroba_jicnu.doc.
4. Lukáš K. Barrettův jícen z pohledu gastroenterologa. Novinky z gastroenterologie 2003; 1 : 3–6.
5. Shaheen NJ, Crosby MA, Bozynski EM et al. Is there publication bias in the reporting of cancer risk of Barrett's esophagus? Gastroenterology 2000; 119(2): 333–338.
6. Jankowski J, Provenzale D, Moayyedi P. Oesophageal adenocarcinoma arising from Barrett´s metaplasma has regional variations in the West. Gastroenterology 2002; 122(2): 588–590.
7. Pera M, Manterola C, Vidal O et al. Epidemiology of esophageal adenocarcinoma. J Surg Oncol 2005; 92(3): 151–159.
8. Singh R, Anagnostopoulos GK, Fortun PJ. Narrow-band imaging with magnification in Barrett's esophagus: validation of a simplified grading system of mucosal morphology patterns against histology. Endoscopy 2008; 40(6): 457–463.
9. Kment M. Barrettův jícen – ideální studijní model kancerogeneze? Čes a Slov Gastroent a Hepatol 2007; 61(1): 47–54.
10. Sharma P, Bansal A, Mathur S. The utility of a novel narrow band imaging endoscopy system in patients with Barrett esophagus. Gastrointest Endosc 2006; 64(2): 167–175.
11. Al Tashi M et al. Barrettův jícen. Výskyt a komplikace onemocnění v období 1994–2003. Čes a Slov Gastroent a Hepatol 2005; 59(2): 62–65.
12. Enzinger PC, Mayer RJ. Esophageal cancer. N Engl J Med 2003; 349 : 2241–2252.
13. Martínek J et al. Low incidence of adenocarcinoma and high-grade intraepithelial neoplasia in patients with Barrett´s esophagus: a prospective cohort study. Endoscopy 2008; 40(9): 711–716.
14. Stefanová et al. Přínos autofluorescence v diagnostice lehké intraepiteliální neoplazie u pacientů s Barrettovým jícnem. Gastroent a Hepatol 2011; 65(5): 249–254.
Labels
Paediatric gastroenterology Gastroenterology and hepatology Surgery
Article was published inGastroenterology and Hepatology
2012 Issue 3-
All articles in this issue
- Jak kvalitní je Vaše kolonoskopie?
- Endosonografie v diagnostice choledocholitiázy
- Využití NBI v diagnostice a sledování pacientů s Barrettovým jícnem
- Endoskopický trénink na neživém zvířecím modelu zlepšuje endoskopické dovednosti
- Snížení dyskomfortu spojeného s kolonoskopií použitím kombinace vodní imerze a insuflace oxidu uhličitého
- Endosonograficky navigovaná alkoholová ablácia cystickej neoplázie pankreasu
- Pozitivita imunoglobulinu IgG4 v krevním séru u osob s karcinomem slinivky břišní
- Korelace indikace k resekci pankreatu s následným histopatologickým nálezem
- Antibiotická profylaxe u akutní pankreatitidy
- Očekávané počty nádorů jater, žlučníku a pankreatu ve světě
- Primární sklerozující cholangoitida u pacientů s idiopatickými střevnímí záněty
- Standardní diagnostický a terapeutický postup u chronické infekce virem hepatitidy C (HCV)
- Highlights of the 34th Czech and Slovak endoscopic days
- Zpráva o DDW 2012
- Ostrava Live Endoscopy
- Prof. MUDr. Julius Špičák, CSc., šedesátníkem
- Prim. MUDr. Karel Lukáš, CSc., sedmdesátiletý
- Moviprep® – moderní příprava střeva před vyšetřením
- Gastroenterology and Hepatology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Moviprep® – moderní příprava střeva před vyšetřením
- Antibiotická profylaxe u akutní pankreatitidy
- Primární sklerozující cholangoitida u pacientů s idiopatickými střevnímí záněty
- Snížení dyskomfortu spojeného s kolonoskopií použitím kombinace vodní imerze a insuflace oxidu uhličitého
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

