-
Medical journals
- Career
Prognostické faktory a načasovanie endoskopie u akútneho nevarikózneho krvácania z horného gastrointestinálneho traktu
Authors: T. Koller 1; J. Sekáč 2; M. Huorka 1; M. Nagyová 1; T. Hlavatý 1; J. Payer 1
Authors‘ workplace: V. interná klinika, LF UK a UN Bratislava 1; II. chirurgická klinika, LF UK a UN Bratislava 2
Published in: Gastroent Hepatol 2011; 65(5): 286-293
Category: Digestive Endoscopy: Original Article
Overview
Účel a ciele:
Poznanie príčin, endoskopického nálezu a klinického priebehu akútneho nevarikózneho krvácania z horného GIT, stanovenie miery opakovaného krvácania, chirurgického riešenia a mortality do 40 dní. Následne identifikácia nezávislých prognostických faktorov a významu načasovania endoskopického výkonu.Metódy:
Prospektívne sme sledovali všetkých pacientov s akútnym nevarikóznym krvácaním z horného GIT počas 2 rokov, pacienti s krvácaním z varixov a s krvácaním z dolného GIT boli vylúčení. Zaznamenali sme anamnézu, hemodynamické premenné, zdroj a stupeň krvácajúcej lézie, počet transfúzií, čas od prijatia po endoskopiu, mieru opakovaného krvácania, chirurgickej liečby a mortality.Výsledky:
Zo 163 pacientov v priemernom veku 65,14 rokov bolo 42,9 % žien, peptické lézie žalúdka a duodéna boli zdrojom v 78,5 % prípadov, aktívne krvácanie malo 19 % pacientov, endoskopickú liečbu sme aplikovali u 49,1 % pacientov. Recidívu krvácania sme pozorovali u 5,5 % a chirurgickú liečbu podstúpilo 4,3 % pacientov, úmrtnosť bola 12,9 %. V multivariantnej analýze boli nezávislými prediktormi úmrtia klinické Rockallovo skóre > 3 (OR = 12,54; p = 0,0014) s 90,5% senzitivitou a 97,8% negatívnou prediktívnou hodnotou, užívanie steroidov alebo SSRI (OR = 5,14; p = 0,045) a najnižšia zaznamenaná koncentrácia hemoglobínu (OR = 2,96; p = 0,031). Endoskopia do 6 hodín od prijatia identifikovala rizikovejšie lézie a častejšie viedla k endoskopickej liečbe, avšak rozdiely v počte transfúzií, v miere recidívy krvácania, chirurgických výkonov a úmrtia sme v našom súbore nezistili.Záver:
Najsilnejším nezávislým prognostickým faktorom bolo Rockallovo skóre viac ako 3 a títo pacienti vyžadujú neodkladnú starostlivosť. Endoskopia do 6 hodín u podskupiny pacientov viedla k častejšej aplikácii endoskopickej liečby bez zisteného vplyvu na klinický priebeh.Klúčové slová:
krvácanie – gastrointestinálny – prognóza – endoskopiaAkútne krvácanie z horného gastrointestinálneho traktu (GIT) je relatívne častým syndrómom s výskytom 40–170 prípadov na 100 000 obyvateľov. Je zaťažený významnou mortalitou, ktorá sa vo vyspelých krajinách pohybuje od 5–14 %. Ešte závažnejšia je prognóza pacientov, u ktorých došlo ku akútnemu krvácaniu počas prebiehajúcej hospitalizácie, kedy je mortalita až dvojnásobná [1]. Incidencia akútneho krvácania nie je na ústupe, čo sa dá vysvetliť starnutím populácie, polymorbiditou a zvyšujúcou sa preskripciou liekov toxických na gastrointestinálny trakt [2]. Naopak, s príchodom stále dokonalejších hemostatických metód sa zvyšuje miera úspešnosti endoskopickej liečby a úmerne sa znižuje potreba chirurgickej intervencie [3]. Uvedené faktory však nie sú jediné, ktoré rozhodujú o prognóze pacientov s akútnym krvácaním. V momente príchodu do nemocnice už často došlo ku kritickej strate krvi s následnými sekundárnymi komplikáciami a samotné vyvolávajúce krvácanie často spontánne ustúpi. O prognóze pacienta preto viac rozhoduje celkový stav pacienta pri prijatí a pridružené choroby, ako samotné promptné ošetrenie krvácajúcej lézie. Aj z týchto dôvodov nie je mortalita akútneho krvácania z horného GIT výrazne odlišná od minulosti [3]. V každodennej klinickej praxi sú preto okrem klinického vyšetrenia veľmi užitočné aj prognostické modely, ktoré dokážu orientačne zaradiť pacientov do rizikových skupín a tým uľahčiť klinické rozhodovanie. Aj samotné načasovanie endoskopického výkonu niekedy závisí nielen od organizačných opatrení nemocnice, ale predovšetkým od celkového stavu pacienta a jeho schopnosti tento výkon podstúpiť. Analýza klinického priebehu akútneho nevarikózneho krvácania z horného GIT bola predmetom nedávnej práce českých autorov [2], ale slovenské údaje nám zatiaľ chýbali. Použiteľnosť prognostických modelov v našej populácii tiež nebola zatiaľ úplne preskúmaná. Problematika načasovania endoskopického výkonu bola predmetom širších diskusií a súčasný konsenzus akceptuje 24-hodinový interval od prijatia po endoskopiu [4]. V súčasnosti sa výskum zameriava na presnejšiu identifikáciu skupín pacientov, ktorí by mohli mať prospech z ešte skoršej endoskopie.
Ciele
Cieľom našej práce bolo analyzovať klinický priebeh akútneho nevarikózneho krvácania do horného GIT.
- Zistiť najčastejšie zdroje krvácania a ich endoskopický nález podľa Forrestovej klasifikácie.
- Zistiť mieru nutnosti chirurgického výkonu, mieru opakovaného krvácania po endoskopickom ošetrení a mieru mortality.
- Identifikovať nezávislé prognostické faktory, ktoré by dokázali už v iniciálnych štádiách predpovedať riziko úmrtia na akútne krvácanie.
- Zistiť význam skorého načasovania endoskopického výkonu do 6 hodín od prijatia do nemocnice.
Pacienti a metódy
Súbor pacientov bol zozbieraný prospektívne v období od februára 2006 do januára 2008 zo všetkých po sebe nasledujúcich hospitalizovaných pacientov, u ktorých bolo vykonané endoskopické vyšetrenie pre akútne krvácanie z horného GIT prejavujúce sa čerstvou hematemézou a/alebo melénou, prípadne enterorágiou, ktorej zdroj sa našiel v hornom GIT. Pacienti boli odoslaní z chirurgickej alebo internej kliniky, kliniky intenzívnej medicíny alebo centrálneho príjmu. Všetci pacienti absolvovali prípravu na vyšetrenie podľa štandardných postupov vrátane intravenóznej antisekrečnej liečby pred výkonom. Po vykonaní endoskopického vyšetrenia bol endoskopistom vypracovaný nález, ktorý bol štruktúrovaný podľa pripraveného formulára. U každého pacienta sme zaznamenali štandardnú anamnézu vrátanie užívaných liekov, klinické vyšetrenie, hemodynamické parametre, v endoskopickom protokole zdroj krvácania, stupeň lézie podľa Forrestovej klasifikácie, podanie endoskopickej liečby. Počas následného obdobia bol zaznamenaný výsledok testu na H. pylori, počet podaných transfúzií, dĺžku hospitalizácie, prípadné opätovné krvácanie, operačné riešenie a úmrtie do 40 dní získané z dostupnej zdravotnej dokumentácie v písomnej alebo elektronickej podobe. Opätovné krvácanie bolo definované ako nová epizóda hematemézy a/alebo hypotenzie a/alebo poklesu hemoglobínu o viac ako 20 g/l. Všetci pacienti mali naplánovanú kontrolnú endoskopiu o mesiac od akútneho krvácania, kedy bol opäť overený status H. pylori a overené hojenie krvácajúcej lézie s odberom vzoriek na histologické vyšetrenie.
Zo súboru boli vylúčení pacienti s krvácaním z pažerákových varixov, pacienti s akútnym krvácaním, ktorí endoskopické vyšetrenie nepodstúpili, pacienti s enterorágiou, pokiaľ sa zdroj v hornom GIT nezistil a pacienti odoslaní na plánovanú endoskopiu, aj keď sa pri endoskopii našla krvácajúca lézia.
U každého pacienta sme pri prijatí vypočítali klinické Rockallovo skóre [5] zahrňujúce vek, tlak krvi, pulz a prítomnosť komorbidity, teda pridružených chorôb srdca, ciev, obličiek a pečene podľa tab. 1 a Glasgow--Blatchfordovo (GB) skóre [6], ktoré obsahuje údaje o koncentrácii hemoglobínu, urey, krvnom tlaku a pulze, prítomnosti melény a synkopy a prípadnom zlyhávaní pečene alebo srdca. Po skončení sledovania sme stanovili ich senzitivitu, špecificitu a pozitívnu a negatívnu prediktívnu hodnotu vo vzťahu k úmrtiu do 40 dní od prijatia do nemocnice. U každého pacienta prijatého do nemocnice sme stanovili čas od vzniku príznakov po prijatie do nemocnice a čas od prijatia do nemocnice po endoskopické vyšetrenie. 10 pacientov už bolo hospitalizovaných počas vzniku krvácania. Počas sledovaného obdobia pre nedostatok personálu nebola na našom pracovisku dostupná urgentná 24-hodinová endoskopia. Pacienti, ktorí boli prijatí počas pracovnej doby (36 pacientov), mali endoskopiu do 6 hodín od prijatia. Ostatní mali endoskopické vyšetrenie počas nasledujúceho pracovného dňa.
Table 1. Klinické Rockallovo skóre, súčet bodov v jednotlivých v stĺpcoch pre vek, tlak krvi/pulz, komorbiditu. Tab. 1. Clinical Rockall score, total of points for age, blood pressure/pulse and comorbidity. 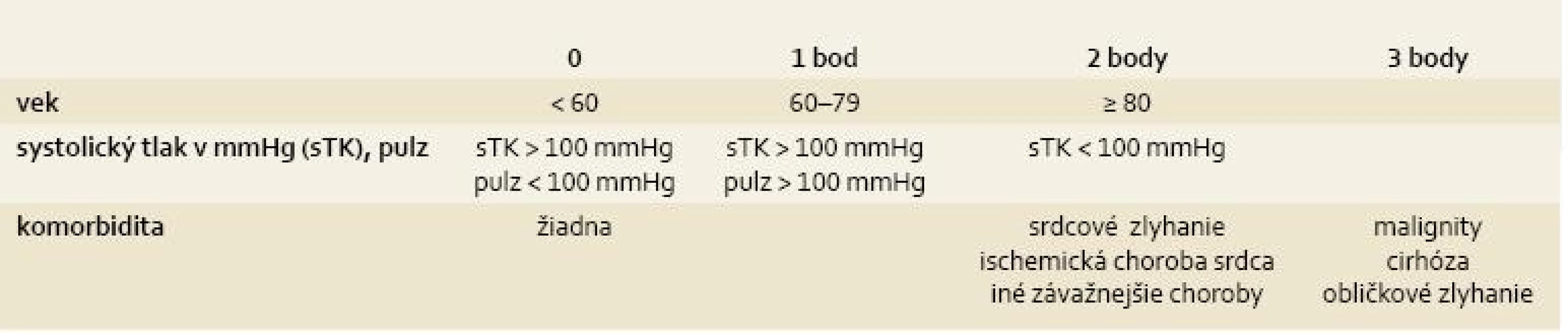
Na štatistické spracovanie súboru sme použili program MyStat 12, pre každú premennú sme stanovili štandardnú odchýlku, pre porovnanie spojitých číselných premenných s normálnou distribúciou sme použili T-test, pre porovnanie kategorických premenných test chi kvadrát. Na stanovenie ROC krivky sme použili úmrtie ako klasifikačnú premennú a Rockallovo a GB skóre ako nezávislé premenné. Pri multivariantnej logistickej analýze sme za závislú premennú považovali prítomnosť úmrtia do 40 dní, premenné asociované s úmrtím boli uvedené medzi nezávislými premennými. Za signifikantný rozdiel sme považovali pravdepodobnosť zamietnutia nulovej hypotézy menšiu ako 0,05. Zbieranie dát bolo schválené lokálnou etickou komisiou.
Výsledky
Počas sledovaného obdobia bolo na našom pracovisku vykonaných 3 186 endoskopií horného GIT. Po vylúčení pacientov definovaných vyššie sme identifikovali 163 pacientov s akútnym nevarikóznym krvácaním z horného GIT. V tab. 2 je uvedená prehľadná štatistika súboru pacientov. Zastúpenie lokalizácie jednotlivých zdrojov krvácania je uvedené v grafe 1. Lokalizácia krvácania v kardii bola najčastejšie spôsobená trhlinami sliznice pri Mallory-Weissovom syndróme, lézie žalúdka a duodéna boli vo veľkej väčšine peptické, len u 5 pacientov sme zistili krvácajúcu artériu pri Dieulafoy lézii. U 10 pacientov v súbore sa zdroj krvácania pri endoskopii nenašiel. Endoskopický nález bol zhodnotený podľa Forrestovej klasifikácie krvácajúcich lézií a zastúpenie jednotlivých stupňov je uvedené v grafe 2. Endoskopická liečba bola vo veľkej väčšine prípadov vo forme sólo opichu riedeným adrenalínom. Len traja pacienti mali aplikovaný hemoklip. Aj napriek výsledku veľkých štúdií v západnej literatúre sa jednalo o endoskopickú liečbu, ktorá bola v tom čase na našom pracovisku dostupná ako jediná. V kontexte urgentného krvácania bolo vyšetrených 78 pacientov na prítomnosť infekcie H. pylori kombináciou ureázového testu a mikroskopického vyšetrenia a z nich bolo pozitívnych 50 %.
Table 2. Prehľadná štatistika súboru 163 pacientov s akútnym nevarikóznym krvácaním do horného GIT. Tab. 2. Summary statistics of 163 patients with acute non-variceal upper-GI bleeding. 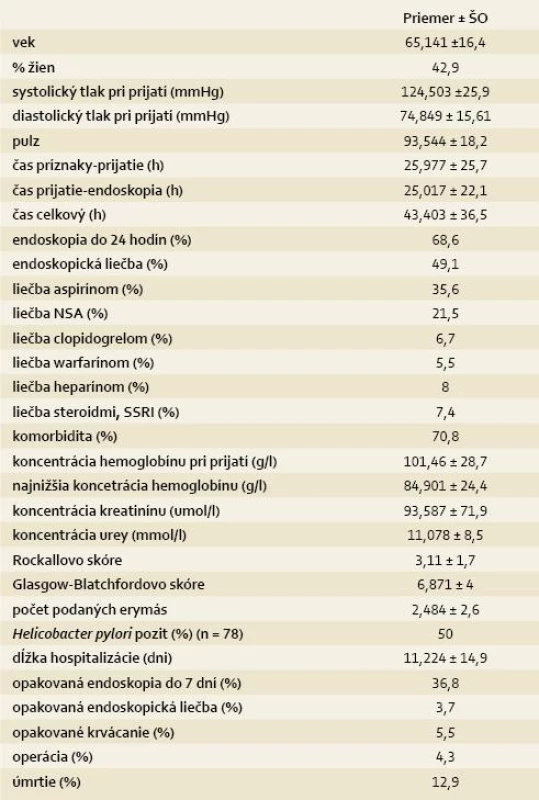
ŠO – štandardná odchýlka Graph 1. Lokalizácia zdroju krvácania u 163 pacientov s akútnym nevarikóznym krvácaním z horného GIT. Graph 1. Anatomical origin of bleeding among 163 patients with acute non- variceal upper-GI bleeding. 
Graph 2. Zastúpenie stupňov krvácajúcich lézií podľa Forresta v súbore 163 pacientov s akútnym nevarikóznym krvácaním do horného GIT (%). Graph 2. Relative incidence of Forrest bleeding lesions grades among 163 patients with acute non-variceal upper-GI bleeding (%). 
Počas sledovaného obdobia 40 dní po urgentnej endoskopii sme recidívu krvácania zaznamenali u 9 (5,5 %) pacientov, z indikácie akútneho krvácania bolo operovaných 7 (4,3 %) pacientov, a úmrtie sme pozorovali u 21 (12,9 %) pacientov.
Porovnaním skupín pacientov podľa prežitia 40 dní od akútnej epizódy krvácania sme zistili, že pacienti, ktorí prežili, mali signifikantne nižšie klinické Rockallovo skóre (2,92 vs 4,43; p < 0,001), menej často užívali kortikosteroidy alebo inhibítory spätného vychytávania serotonínu (SSRI) (5,6 vs 19 %; p = 0,028), mali vyššiu najnižšie dosiahnutú koncentráciu hemoglobínu (86,8 vs 71,7 g/l; p = 0,008) a mali trend k menej častému výskytu závažnejších endoskopických lézií podľa Forrestovej klasifikácie (1, 2a, 2b) (54,3 vs 76,2 %; p = 0,099). Multivariantná analýza uvedených rizikových faktorov úmrtia je uvedená v tab. 3. Do modelu sme dodali aj užívanie nesteroidových antiflogistík (NSA), ale ich užívanie nemalo na úmrtnosť žiadny vplyv. Miery mortality podľa hodnoty klinického Rockallovho skóre a podľa Forrestovej klasifikácie endoskopického nálezu sú zobrazené v grafe 3. Pomocou ROC krivky sme vypočítali senzitivitu, špecificitu, pozitívnu a negatívnu prediktívnu hodnotu pre skórovacie modely podľa Rockalla a GB, ktoré sú uvedené v tab. 4.
Table 3. Multivariantná logistická regresia rizikových faktorov úmrtia u 163 pacientov s akútnym nevarikóznym krvácaním do horného GIT. Tab. 3. Multivariate logistic regression for risk factors of death among 163 patients with acute non-variceal upper-GI bleeding. 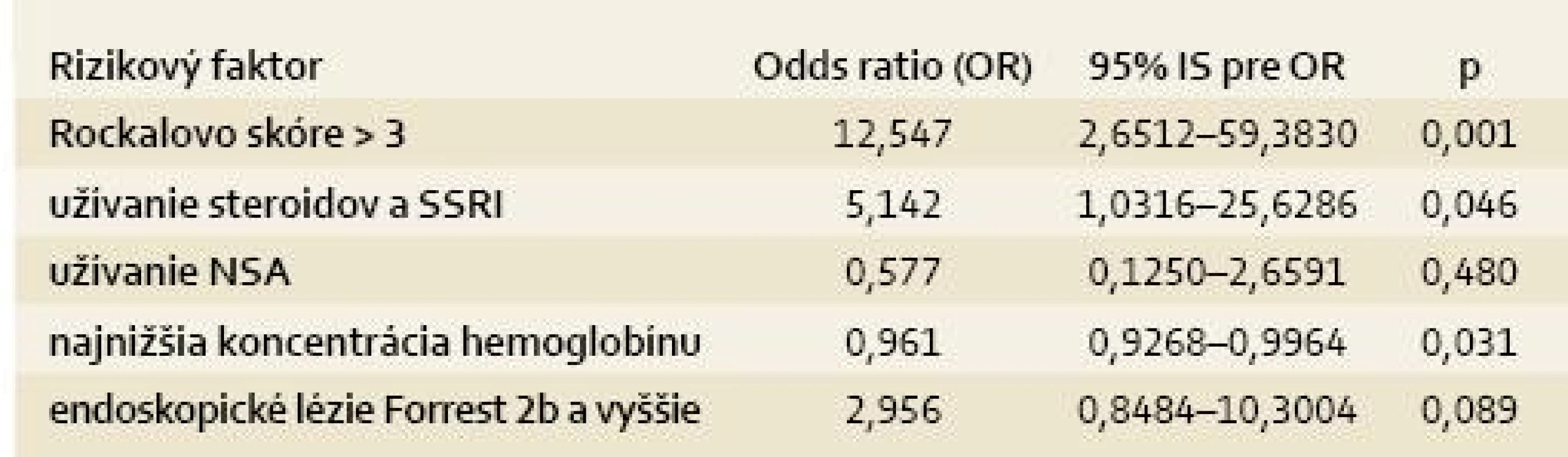
p < 0,0001; 87,84 % pacientov správne klasifikovaných v tomto modeli Table 4. Prediktívna hodnota skórovacích modelov na mieru úmrtia u 163 pacientov s akútnym nevarikóznym krvácaním do horného GIT. Tab. 4. Scoring models predictive values for the mortality rate in 163 patients with acute non-variceal upper-GI bleeding. 
PPH – pozitívna prediktívna hodnota, NPH – negatívna prediktívna hodnota, AUC – Area Under Curve Graph 3. Miera mortality pacientov podľa Rockallovho skóre a endoskopického nálezu podľa Forrestovej klasifikácie u pacientov s akútnym nevarikóznym krvácaním z horného GIT. Graph 3. Mortality rate according to the clinical Rockall score and the Forrest grade of endoscopic lesions among patients with acute non-variceal upper-GI bleeding. 
Nakoniec sme sa zaoberali analýzou časových intervalov od prijatia po endoskopické vyšetrenie. Priemerný časový interval od prijatia do nemocnice po endoskopické vyšetrenie bol u 153 pacientov v našom súbore 25,01. Do 6 hodín od prijatia absolvovalo urgentnú endoskopiu 36 (22 %) pacientov, ostatní pacienti absolvovali endoskopiu v najbližší pracovný deň bez výnimky. Pacienti s endoskopiou do 6 hodín mali signifikantne častejšie prítomné lézie 1, 2a alebo 2b podľa Forresta (graf 4), a následne signifikantne častejšie aplikovanú endoskopickú liečbu (72,2 vs 41 %; p = 0,002). Rozdiely v počte podaných transfúzií sme nezistili. Porovnanie klinického priebehu oboch skupín pacientov je uvedené v tab. 5.
Table 4. Prediktívna hodnota skórovacích modelov na mieru úmrtia u 163 pacientov s akútnym nevarikóznym krvácaním do horného GIT. Tab. 4. Scoring models predictive values for the mortality rate in 163 patients with acute non-variceal upper-GI bleeding. 
PPH – pozitívna prediktívna hodnota, NPH – negatívna prediktívna hodnota, AUC – Area Under Curve Table 6. Načasovanie endoskopického vyšetrenia a jeho vplyv na klinický priebeh. Tab. 5. Timing of endoscopy and its impact on the clinical outcome. 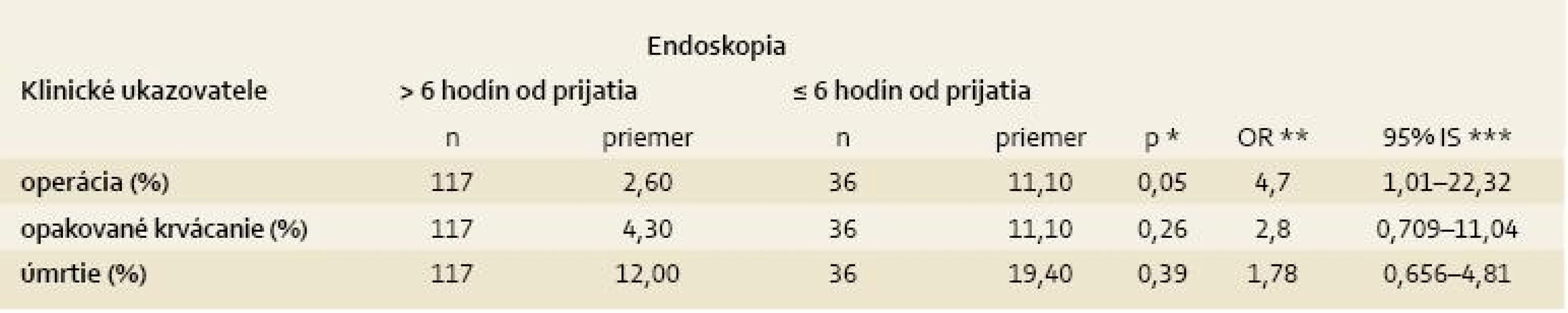
* test chi kvadrát, **odds ratio pri jednoduchej logistickej regresii, *** 95% interval spoľahlivosti pre OR Graph 4. Porovnanie zastúpenia stupňov krvácajúcich lézií podľa Forresta v závislosti od načasovania endoskopie (chi kvadrát; p = 0,0003). Graph 4. Comparison of representation of endoscopic Forrest bleeding lesions grade depending on the timing of endoscopy (chi square; p = 0.0003). 
Diskusia
Akútne krvácanie z horného GIT je stále aktuálny medicínsky problém a vzhľadom na aktuálne trendy ním aj zostane. Je zaťažený signifikantnou mortalitou a na jeho manažment sa vynakladajú nezanedbateľné náklady [7]. Obmedzené personálne a finančné zdroje v zdravotníctve vyžadujú racionálnu organizáciu starostlivosti, ktorej výsledkom by mala byť čo najvyššia efektívnosť v záchrane životov pacientov za primerané náklady. Na dosiahnutie tohto cieľa je preto potrebné aj poznanie priebehu akútneho nevarikózneho krvácania do horného GIT a jeho prognostických faktorov v našich podmienkach.
V našom súbore 163 pacientov s akútnym krvácaním do horného GIT sa jednalo o súbor na hranici geriatrického veku. Najčastejším zdrojom krvácania boli peptické vredy alebo erózie žalúdka a duodéna, ktoré predstavovali 78,5 % všetkých pacientov. Vysoké zastúpenie malo v rizikových faktoroch krvácania užívanie aspirínu (35,6 %) a nesteroidových antiflogistík (21,5 %), ale aj pozitivita H. pylori. Aktívne krvácajúce lézie sme pozorovali u 19 % pacientov, naopak čistú alebo hematínovú spodinu, prípadne negatívny nález až u 39,2 % pacientov. Tieto údaje sú v kontexte predchádzajúcich analýz v našich krajinách aj v zahraničí [1,2,4].
Klinický priebeh krvácania bol u 5,5 % pacientov charakterizovaný recidívou akútneho krvácania. V porovnaní s literatúrou sa táto miera môže javiť ako nízka [8]. My si ju vysvetľujeme vysokým výskytom endoskopického nálezu s čistou alebo hematínovou spodinou, čoho priamym dôsledkom bola nízka miera podanej endoskopickej liečby. Táto skutočnosť môže súvisieť aj s pomerne dlhým intervalom od prijatia po endoskopiu, ktorý bude diskutovaný nižšie. Druhým dôvodom môžu byť aj rozdielne definície opakovaného krvácania. Miera chirurgického riešenia akútneho krvácania je v súčasnosti trvalo udávaná pod 5 % a náš súbor sa v tomto ohľade nijako neodlišuje. Miera mortality taktiež spadá do rozpätia bežne citovaného v literatúre [2,8–10]. Je o niečo vyššia ako mortalita udávaná v klinických štúdiách a veľkých databázach. Mohlo by to byť spôsobené viacerými faktormi v manažmente, ako napríklad nedostupnosťou skorej endoskopie, ale aj podanou len sólo endoskopickou liečbou opichom. Niektoré observačné štúdie však udávajú aj vyššiu mortalitu [11].
Poznanie prognostických faktorov akútneho krvácania je dôležitým predpokladom pre efektívny manažment. Prognostické modely, ako klinické Rockallovo skóre alebo GB skóre, sú v klinickej praxi používané už v mnohých krajinách [1,12]. Klinické Rockallovo skóre bolo vyvinuté na identifikáciu pacientov s vyšším rizikom úmrtia na akútne krvácanie ešte pred realizáciou endoskopického vyšetrenia. V našom súbore mali pacienti s vyšším Rockallovým skóre, s vyšším stupňom endoskopických lézií podľa Forresta, užívatelia steroidov alebo SSRI a anemickí pacienti signifikantne vyššiu úmrtnosť. Multivariantná analýza všetkých spomenutých faktorov asociovaných s mortalitou ukázala klinické Rockallovo skóre > 3 ako najsilnejší nezávislý prediktor mortality. V našom súbore sa ako najvýhodnejší ukázal prah viac ako 3 body, ktorý mal pomerne nízku špecificitu, ale výbornú senzitivitu a negatívnu prediktívnu hodnotu. Dokázal identifikovať 45,2 % pacientov s nízkym rizikom úmrtia (do 5 %), u ktorých by bolo možné aplikovať v manažmente odlišný a menej urgentný postup. Naopak 44,8 % pacientov so skóre viac ako 3 malo mieru mortality na úrovni cca 25 %. V našom súbore sme pozorovali nulovú mortalitu u pacientov s klinickým Rockallovým skóre 0–2. Práca na porovnateľnom počte pacientov udáva tiež skóre 1–3 ako bezpečné [13]. Niektoré odporúčania sú však striktnejšie a považujú za relatívne bezpečné len klinické Rockallovo skóre do 1 [12]. To však výrazne redukuje počet tzv. nízkorizikových pacientov. Z týchto dôvodov bolo vyvinuté Glasgow-Blatchfordovo (GB) skóre. Jeho cieľom bolo identifikovať pacientov s nízkym rizikom intervencií v zmysle podania transfúzií, endoskopickej liečby alebo chirurgickej liečby, ktorí by mohli byť riešení ambulantnou cestou [6]. Tento skórovací model sa ukazuje v mnohých prácach ako presnejší vo výbere nízkorizikových pacientov [14,15]. V našom súbore malo GB skóre 0–1 len 21 (12,8 %) pacientov a z nich malo aspoň jednu intervenciu (transfúziu, endoskopickú liečbu alebo chirurgický výkon) až 10 pacientov, takže táto vlastnosť GB skóre sa na našom súbore nepotvrdila. Dávame to do súvisu s tým, že v našom súbore sa už jednalo o vopred vybraných a už hospitalizovaných pacientov s akútnym krvácaním. Prediktívna hodnota GB skóre aj vo vzťahu k mortalite sa v našom súbore ukázala ako menej preukázateľná v porovnaní s klinickým Rockallovým skóre.
Ďalšie nezávislé rizikové faktory úmrtia v našej multivariantnej analýze, ako užívanie steroidov a SSRI a nízka koncentrácia hemoglobínu sú v literatúre už známe. Čo sa týka užívania nesteroidových antireumatík, tak ich užívanie v tomto modeli nemalo vplyv na mortalitu.
Načasovanie endoskopie je predmetom diskusií už veľa rokov. Už takmer pred polstoročím prof. Mařatka presadzoval tzv. „aktívny diagnostický postup“, čo znamenalo vykonať včasnú gastroskopiu, pokiaľ je možné, ešte počas krvácania [16]. Zároveň však platí zásada, že lege artis je endoskopia vykonaná až po stabilizácii pacienta, aby sa nestala pre pacienta neúmerne zaťažujúcou a rizikovou [17]. Súčasné odporučenia veľkých gastroenterologických a endoskopických spoločností sa zhodujú v tom, že endoskopické vyšetrenie u akútneho nevarikózneho krvácania by malo byť vykonané do 24 hod [1,2,8,12]. Tento interval sa nazýva tzv. skorou endoskopiou. V našom súbore bol však priemerný čas od prijatia po endoskopiu 25,01 hod a endoskopické vyšetrenie do 24 hod malo len 68,6 % pacientov. Je to však len o málo menej, ako udávajú veľké zahraničné databázy ako RUGBE 76 % [8] a Medicare 71,5 % [18]. Preto možno konštatovať, že až u dvoch tretín pacientov bol interval skorej endoskopie do 24 hod dodržaný.
Ešte skoršia realizácia endoskopie ako do 24 hod, teda endoskopia čo najskôr od prijatia nie je zatiaľ ešte v literatúre presne časovo ohraničená, ale dala by sa nazvať tzv. veľmi skorou endoskopiou. Počas zbierania údajov nebola na našom pracovisku dostupná endoskopia počas 24 hod. Z týchto dôvodov sme mali unikátnu a neopakovateľnú možnosť porovnať skupinu pacientov s endoskopiou vykonanou ešte počas pracovnej doby, teda do 6 hod od prijatia (priemer 2,5 hod), so skupinou pacientov s endoskopiou najbližší pracovný deň (priemer 31,9 hod). Aj v skupine s endoskopiou v najbližší pracovný deň malo endoskopiu do 24 hod 59 % pacientov. V našom súbore sme nezistili, že by endoskopia do 6 hod mala lepšiu prognózu alebo kratšiu hospitalizáciu, či nižší počet transfúzií oproti endoskopii v najbližší pracovný deň. V literatúre sa veľmi skorej endoskopii pripisuje význam najmä u vysokorizikových pacientov, teda tých s vyšším Rockallovým skóre a pacientov s červeným aspirátom v sonde. V novších prácach je už udávaný aj rozdiel v mortalite, ale interval veľmi skorej endoskopie bol až 13 hod od prijatia [19]. Ďalšími dôležitými faktormi však môžu byť aj kvalifikovanosť a expertíza endoskopisty, ako aj samotná technika a modality hemostázy, ktoré môžu mať ešte väčší význam, ako čas od prijatia po endoskopiu [3].
Limitáciou nášho súboru v tomto zistení by mohol byť relatívne nízky počet pacientov s endoskopiou vykonanou do 6 hod (36 pacientov), ktorý neumožnil ďalšiu validnú analýzu podskupín. Druhou limitáciou mohol byť klinický úsudok. Pri nedostupnosti 24 hod endoskopie mohol viesť k urýchleniu endoskopie ešte počas pracovnej doby u niektorých vysokorizikových pacientov oproti klinicky nízkorizikovým pacientom. Z tejto limitácie mohla vyplynúť aj hranične signifikantne vyššia miera chirurgickej liečby (11,1 vs 2,6 %; p = 0,05) u pacientov s endoskopiou do 6 hod. Táto limitácia však nie je podľa nášho názoru až tak zásadná, pretože sa týkala len tých vysokorizikových pacientov, ktorí boli prijatí počas pracovnej doby. Vysokorizikoví pacienti prijatí mimo pracovnej doby nemali ani na základe klinického úsudku endoskopické vyšetrenie urýchlené. Navyše, ako už bolo hore uvedené, až 59 % pacientov v skupine s endoskopiou v najbližší pracovný deň, malo endoskopiu do 24 hod. Naše zistenia sú však aj napriek limitáciám v zhode so súčasnými odporúčaniami väčšiny spoločností, ktoré veľmi skorú endoskopiu plošne neodporúčajú. Treba však zdôrazniť, že našim zámerom bolo preskúmať možný význam veľmi skorej endoskopie a nie spochybňovanie skorej endoskopie definovanej do 24 hod od prijatia pacienta, ktorej výhody sú overené a odporúča ju väčšina autorít v tejto oblasti [4,12,17].
Logickým sa ukazuje naše pozorovanie, že endoskopia do 6 hod identifikovala viac rizikovejších lézií s vyššou mierou endoskopickej liečby. Vysvetlením môže byť vysoká efektivita podávanej konzervatívnej antisekrečnej liečby inhibítorom protónovej pumpy, o ktorej je známe, že vedie ku zníženiu rizikovosti krvácajúcej lézie [4]. To však neplatí absolútne, čoho dôkazom je aj naše pozorovanie, že aktívne krvácanie Forrest 1 sme zaznamenali až u každého šiesteho pacienta po priemerne 31,9 hod od prijatia napriek plnej antisekrečnej liečbe. Uvedené poukazuje na komplexnosť problému a naozaj nenahraditeľné miesto endoskopického vyšetrenia v manažmente týchto pacientov. Krvácanie z lézií je pravdepodobne intermitentné a počas konzervatívnej liečby sa často spontánne upraví. Fyziologická hemostáza a efekt liečby sú však zrejme v dynamickej rovnováhe s fibrinolýzou a agresívnymi faktormi vyvolávajúcimi krvácajúce lézie, čo podčiarkuje dôležitosť starostlivého monitorovania pacienta a nízky prah pre skoršiu indikáciu endoskopie.
Pomerne vysoká miera opakovanej endoskopie v našom súbore je vysvetliteľná skôr používanými zvyklosťami nemocnice, ako aj nemožnosťou 24 hod endoskopie v období nášho prospektívneho sledovania.
Záverom by sa dalo konštatovať, že akútne nevarikózne krvácanie z horného GIT je najčastejšie spôsobené peptickými léziami žalúdka alebo dvanástnika. Aj v našich podmienkach je závažným syndrómom, ktorý je zaťažený signifikantnou mortalitou. Medzi najspoľahlivejšie a nezávislé prognostické faktory patrilo klinické Rockallovo skóre, ktoré je možné stanoviť ešte pred endoskopickým vyšetrením. Malo by nám uľahčiť rozhodnutie o spôsobe manažmentu a načasovaní endoskopie. Skóre do 2 nebolo zaťažené mortalitou, skóre nad 3 bolo rizikové. Pacienti s Rockallovým skóre viac ako 3 by mali byť prioritne riešení vrátane endoskopického vyšetrenia a urgentnej hospitalizácie. Endoskopické vyšetrenie do 6 hod od prijatia umožnilo identifikovať viac vysokorizikových lézií a častejšie viedlo k endoskopickému ošetreniu. S určitou rezervou vzhľadom na limitácie sa však dá konštatovať, že miera opakovaného krvácania, chirurgickej liečby a úmrtia nebola ovplyvnená. U pacientov s Rockallovým skóre do 3 by preto bolo možné odloženie endoskopie na ráno nasledujúceho pracovného dňa, aj bez ovplyvnenia mortality. Interval skorej endoskopie do 24 hod od prijatia by však mal byť podľa možností zachovaný. K týmto záverom by však mal byť vždy nadradený klinický úsudok založený na dôkladnom prvotnom vyšetrení, efektívnej liečbe a kontinuálnom sledovaní pacienta.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for biomedical papers.Doručeno/Submitted: 5. 8. 2011
Přijato/Accepted: 28. 8. 2011
MUDr. Tomáš Koller, PhD.
V. interná klinika LFUK a UN Bratislava
Ružinovská 6, 826 06 Bratislava
koller.tomas@gmail.com
Sources
1. Hearnshaw SA, Logan RF, Lowe D et al. Acute upper gastrointestinal bleeding in the UK: patient characteristics, diagnoses and outcomes in the 2007 UK audit. Gut 2011; Jun. 10 epub.
2. Dítě P, Novotný I, Kroupa R et al. Akutní nevarikózní krvácení do horní části trávicího traktu, Čes a Slov Gastroent a Hepatol 2007; 61(1): 6–10.
3. Parente F, Anderloni A, Bargiggia S et al. Outcome of non-variceal acute upper gastrointestinal bleeding in relation to the time of endoscopy and the experience of the endoscopist: a two-year survey. World J Gastroenterol 2005; 11(45): 7122–7130.
4. Barkun AN, Bardou M, Kuipers EJ et al. International consensus recommendations on the management of patients with nonvariceal upper gastrointestinal bleeding. Ann Intern Med 2010; 152(2): 101–113.
5. Rockall TA. Risk scoring in acute upper gastrointestinal haemorrhage. Dig Liver Dis 2006; 38(1): 10–11.
6. Blatchford O, Murray WR, Blatchford M. A risk score to predict need for treatment for upper-gastrointestinal haemorrhage. Lancet 2000; 356(9238): 1318–1321.
7. Alkhatib AA, Abubakr SM, Elkhatib FA. An estimate of hospitalization cost for elderly patients with acute upper gastrointestinal bleeding in the USA. Dig Dis Sci 2009; 54(3): 695.
8. Barkun A, Sabbah S, Enns R et al. The Canadian Registry on Nonvariceal Upper Gastrointestinal Bleeding and Endoscopy (RUGBE): Endoscopic hemostasis and proton pump inhibition are associated with improved outcomes in a real-life setting. Am J Gastroenterol 2004; 99(7): 1238–1246.
9. Morales Uribe CH, Sierra Sierra S, Hernández AM et al. Upper gastrointestinal bleeding: risk factors for mortality in two urban centres in Latin America. Rev Esp Enferm Dig 2011; 103(1): 20–24.
10. González-González JA, Vázquez-Elizondo G, García-Compeán Da et al. Predictors of in-hospital mortality in patients with non-variceal upper gastrointestinal bleeding. Rev Esp Enferm Dig 2011; 103(4): 196–203.
11. Fein F, Weber A, Koch S et al. The prognosis of patients having received optimal therapy for nonvariceal upper gastrointestinal bleeding might be worse in daily practice than in randomized clinical trials. Eur J Gastroenterol Hepatol 2010; 22(3): 361–367.
12. Scottish Intercollegiate Guidelines Network, Management of acute upper and lower gastrointestinal bleeding, A national clinical guideline: Elliott House Edinburgh 2008 : 5–9.
13. Tham TC, James C, Kelly M. Predicting outcome of acute non-variceal upper gastrointestinal haemorrhage without endoscopy using the clinical Rockall Score. Postgrad Med J 2006; 82(973): 757–759.
14. Stanley AJ, Dalton HR, Blatchford O et al. Multicentre comparison of the Glasgow Blatchford and Rockall scores in the prediction of clinical end-points after upper gastrointestinal haemorrhage. Aliment Pharmacol Ther 2011; 34(4): 470–475.
15. Romagnuolo J, Barkun AN, Enns R et al. Simple clinical predictors may obviate urgent endoscopy in selected patients with nonvariceal upper gastrointestinal tract bleeding. Arch Intern Med 2007; 167(3): 265–270.
16. Mařatka Z. Krvácení z trávicí trubice. In: Praktická Gastroenterologie. Státní zdravotnické nakladatelství 1968 : 491–493.
17. Dítě P. Akutni nevarikózní krvácení do horní částí trávicího ústrojí. In: Akutní stavy v Gastroenterologii. Praha: Galén 2005 : 9–19.
18. Cooper GS, Kou TD, Wong RC. Use and impact of early endoscopy in elderly patients with peptic ulcer hemorrhage: a population-based analysis. Gastrointest Endosc 2009; 70(2): 229–235.
19. Lim LG, Ho KY, Chan YH et al. Urgent endoscopy is associated with lower mortality in high-risk but not low-risk nonvariceal upper gastrointestinal bleeding. Endoscopy 2011; 43(4): 300–306.
Labels
Paediatric gastroenterology Gastroenterology and hepatology Surgery
Article was published inGastroenterology and Hepatology
2011 Issue 5-
All articles in this issue
- Natural Orifice Transluminal Endoscopic Surgery (NOTES) – současný stav, vlastní zkušenosti
- Eozinofilní ezofagitida
- Radiofrekvenční ablace v gastrointestinálním traktu – aktuální stav ve světě a v ČR
- Prognostické faktory a načasovanie endoskopie u akútneho nevarikózneho krvácania z horného gastrointestinálneho traktu
- Spontánní retroperitoneální perforace vzestupného tračníku a trombóza portálního řečiště u pacienta s ulcerózní kolitidou
- Za profesorkou MUDr. Dagmar Hauftovou, CSc.(2. 6. 1927–18. 7. 2011)
- Globální problémy s financováním zdravotní péče
- Biologická léčba IBD 2011
- Tento štát nie je pre lekárov
- Společnost gastrointestinální onkologie vás zve na I. národní kongres o kolorektálním karcinomu
- Bude naše cesta bez vizí?
- Vítejte na palubě
- Přínos autofluorescence v diagnostice lehké intraepiteliální neoplazie u pacientů s Barrettovým jícnem
- Dvojí tvář rakoviny jícnu – epidemiologie a etiologie
- Gastroenterology and Hepatology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Eozinofilní ezofagitida
- Dvojí tvář rakoviny jícnu – epidemiologie a etiologie
- Radiofrekvenční ablace v gastrointestinálním traktu – aktuální stav ve světě a v ČR
- Prognostické faktory a načasovanie endoskopie u akútneho nevarikózneho krvácania z horného gastrointestinálneho traktu
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

