-
Medical journals
- Career
Využití nízkoteplotního plazmatu v mikrobiologii a medicíně
Authors: J. Julák 1; V. Scholtz 2
Authors‘ workplace: Ústav imunologie a mikrobiologie, 1. lékařská fakulta Univerzity Karlovy, Praha 1; Ústav fyziky a měřicí techniky, Fakulta chemicko-inženýrská VŠCHT, Praha 2
Published in: Epidemiol. Mikrobiol. Imunol. 69, 2020, č. 1, s. 29-37
Category: Review Article
Overview
Přehled poskytuje základní informace o nízkoteplotním plazmatu, jeho vlastnostech a metodách jeho přípravy. Uvádí příklady jeho použití při inaktivaci bakterií včetně biofilmů, hub a prionů. Uvedeny jsou i související aplikace v humánní medicíně, jmenovitě při hojení ran, v protinádorové terapii, v dentální medicíně a terapii dermatomykóz.
Klíčová slova:
biofilm – dermatomykózy – elektrické výboje – Fungi – inaktivace mikroorganismů – hojení ran
ÚVOD
Fyzika a její metody získaly své pevné místo v medicíně již od dob Konráda Roentgena a Marie Curie-Skłodowske, v mikrobiologii se začaly uplatňovat jen o něco později. Z fyzikálních metod by měl tento přehled poskytnout základní informace a poslední pokroky v použití fyzikálního jevu zvaného nízkoteplotní plazma, který se v různých „emerging methods“ rozsáhle uplatňuje v posledních zhruba deseti letech. Dále uvedený přehled je jen subjektivním výběrem odkazů na zajímavé pokusy a úspěchy v tomto oboru; úplný přehled je znemožněn jeho rozsahem a komplexností obsahu. Úplnější a podrobnější informace mohou poskytnout četné monografie, z novějších např. práce Shintaniho H. a Sakuda A. [1] nebo Metelmanna H. R. et al. [2], z nichž zvláště posledně jmenovaná je ve velkém rozsahu zpracována s německou důkladností. Problematice se věnuje též několik desítek specializovaných časopisů, za všechny je možno jako typický jmenovat Clinical Plasma Medicine (Elsevier, ISSN: 2212-8166). Zájemce o podrobnější informace je proto nutné odkázat na tyto a dále citované zdroje.
PLAZMA
Plazma bylo jako tzv. čtvrté skupenství hmoty objeveno Crookesem již v roce 1879, ale pojmenováno Langmuirem až v roce 1929. Sestává z částečně až úplně ionizovaných atomů a z nich odštěpených volných elektronů, vykazujících tzv. kolektivní chování. Plazma tvoří značnou část vesmíru, neboť jsou z něj „postaveny“ hvězdy včetně Slunce; na Zemi se pak vyskytuje např. v blescích nebo v přístrojích zvaných tokamak. Toto plazma se nazývá vysokoteplotní, jeho teplota dosahuje řádově tisíců kelvinů, a je proto pro aplikaci na živou hmotu nevhodné. Naproti tomu existuje tzv. nízkoteplotní plazma (NTP, non-thermal, též low-temperature či cold plasma), sestávající z vysoce energetických elektronů a nízkoenergetických iontů; v důsledku malé hmotnosti elektronů je jeho teplota jen mírně vyšší než teplota okolí, typicky nepřesahuje 40 °C. Ionty i elektrony jsou ovšem vysoce reaktivní a jejich interakcí s okolním plynem či s kapalinami proto v plazmatu dochází k řadě neobvyklých chemických reakcí a tvorbě řady vysoce reaktivních částic povahy iontů, radikálů a částic s neobvyklou elektronovou konfigurací. Jedná se tzv. ROS (reactive oxygen species) a RNS (reactive nitrogen species) [3], přehled těchto částic uvádí tabulka 1, převzatá z práce Liua D. X. et al. [4]. Většinou jsou velmi nestálé se střední dobou života v řádu zlomků sekundy, vyskytují se ovšem i částice stálé, zejména ozon, peroxid vodíku či oxidy a kyseliny dusíku. Složení a zastoupení těchto částic je velmi závislé na experimentálních podmínkách, zejména na parametrech vzniku plazmatu a složení okolního plynu. Obecně jsou ovšem tyto částice zodpovědné za interakce plazmatu s živou hmotou včetně inaktivace mikroorganismů. Při ní se pravděpodobně rovněž uplatňuje ultrafialové záření produkované v různé míře elektrickými výboji. Mechanismy inaktivace mikroorganismů přehledně popsali Liao et al. [5]: jako základní uvádějí poškození nukleových kyselin UV zářením, peroxidaci lipidů, změny struktury proteinů a indukci apoptózy. Uplatňují se rovněž mechanická poškození buněk, zejména elektrostatická disrupce a elektroporace.
Table 1. Částice vyskytující se v plazmatu a na rozhraní plyn – kapalina
Table 1. Particles found in plasma and at the gas-liquid interface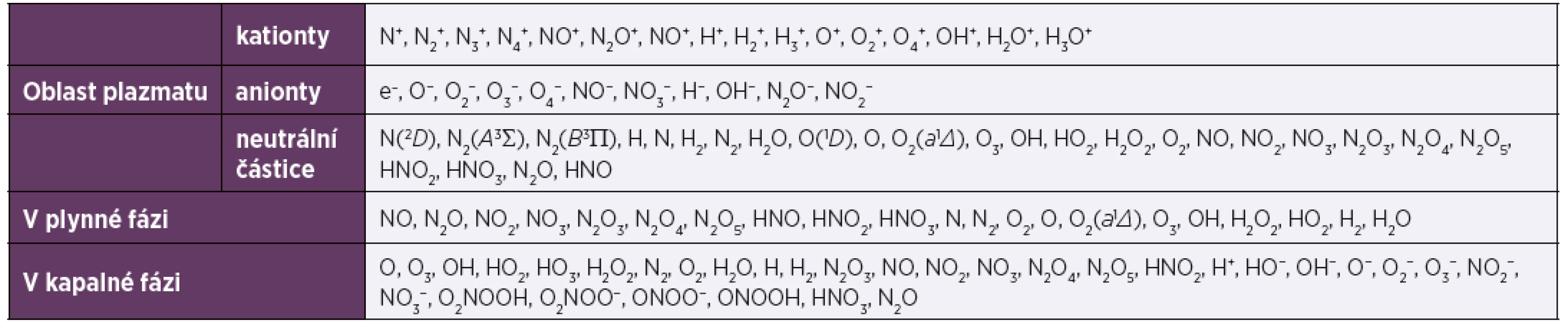
Upraveno podle Liu et al. (2016) [4]
Adapted from Liu et al. (2016) [4].Zajímavým efektem je, že voda a vodné roztoky exponované plazmatem si uchovávají svou mikrobicidní aktivitu po dlouhou dobu až několika měsíců. Aktivita této plazmatem aktivované vody (PAW) je způsobena přetrváváním stálých mikrobicidních částic, zejména peroxidu vodíku, dusíkatých kyselin, pravděpodobně i ozonu apod. Podrobněji o vlastnostech PAW píší např. Laurita R. et al. [6], Julák J. et al. [7], Hozák P. et al. [8], Thirumdas R. et al. [9].
PŘÍPRAVA PLAZMATU
Nízkoteplotní plazma se zpravidla připravuje elektrickými výboji v různém uspořádání, nejběžnější z nich jsou stručně popsána níže a schematicky znázorněna na obrázku 1, podrobnější popis uvádějí např. Ehlbeck J. et al. [10], Šimončicová J. et al. [11].
Image 1. Zdroje plazmatu
Fig. 1. Plasma sources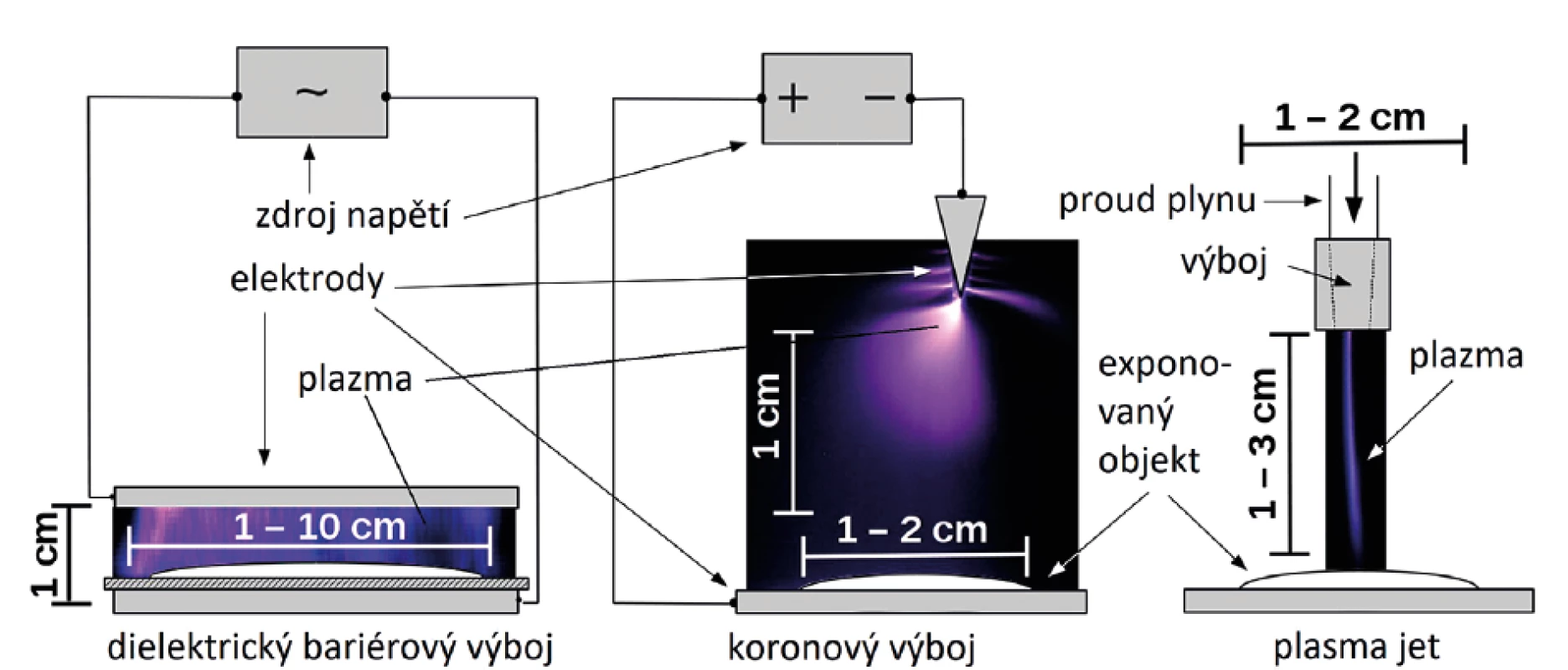
Korónové výboje vznikají vložením stejnosměrného napětí několika kV na ostrý hrot nebo břit. Tiché výboje tohoto typu byly známy již v dávné historii jako světélka na koncích lodních stěžňů a ráhen, zvaná oheň sv. Eliáše. Podle polarity napětí a jeho intenzity má vznikající korona různé podoby, zvané transient spark, pulseless glow, interrupted channel atd., uvedené v práci Khuna J. et al. [12]. Zvláštním uspořádáním hrotových elektrod vzniká tzv. kometární výboj ve tvaru plamene, připomínající plasma jet [13, 14].
Plasma jet (též plasma needle, plasma torch nebo plasma pen), je často používaný zdroj plazmatu, vznikajícího působením vysokofrekvenčního elektrického napětí na proud plynu, obvykle Ar, He nebo vzduchu. Podobně jako korónové výboje zasahuje jen poměrně malou cílovou plochu. Úvodní přehled uvádí práce Laroussiho M. et al. [15], podrobnější popis vlastností studie Nishimeho T. M. C. et al. [16].
Dielektrický bariérový výboj (DBD) vzniká po vložení střídavého napětí na dvě plošné elektrody oddělené nevodivým dielektrikem. Výhodou je větší exponovaná plocha, nevýhodou malá vzdálenost několika milimetrů mezi elektrodami.
Klouzavý výboj (gliding arc) vzniká mezi dvěma divergentními elektrodami; má zpravidla vyšší teplotu a v biologických aplikacích se proto uplatňuje jen zřídka.
Mikrovlnné výboje vznikají působením elektromagnetických frekvencí v řádu stovek GHz; typicky se používají v uzavřených skříních připomínajících mikrovlnné trouby. Otevřený mikrovlnný zdroj generující plazma připomínající plasma jet v atmosféře argonu popsali Nowakowska H. et al. [17].
Instrumentaci pro přípravu NTP vyrábí a dodává řada výrobců, z nichž někteří jsou uvedeni v tabulce 2. Asi nejstarší jsou mikrovlnné skříňové sterilizátory (Sterrad, PE-200), v nichž jsou vložené předměty sterilizovány při laboratorní teplotě výbojem v atmosféře přidaného sterilizačního činidla (peroxidu vodíku). Nadějný systém Plazlyte, používající jako přídavné činidlo peroxoctovou kyselinu, nedoporučila k používání Food and Drug Administration, USA. Nejpoužívanější jsou v současnosti pravděpodobně přístroje na bázi plasma jetu.
Table 2. Příklady komerčních zdrojů NTP
Table 2. Examples of commercial sources of non-thermal plasmas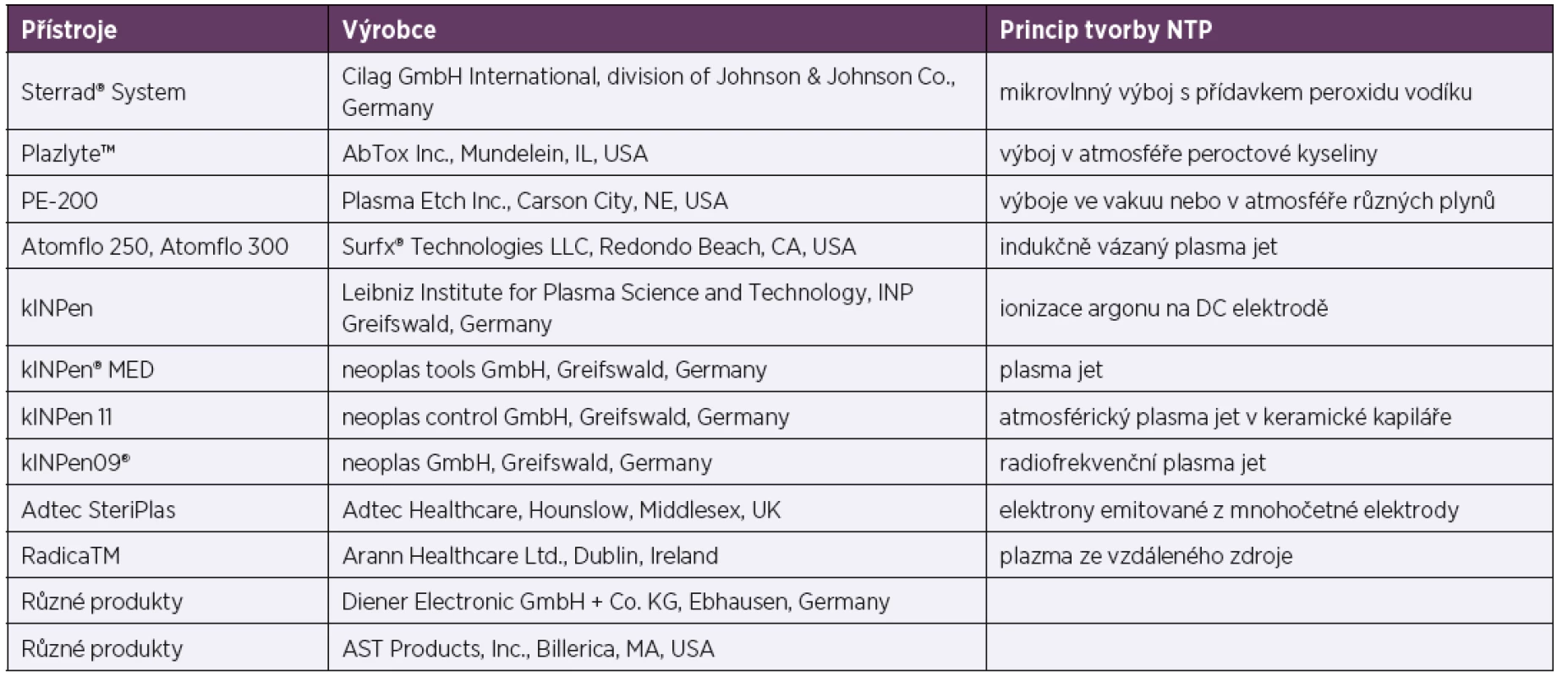
MIKROBIOLOGICKÉ APLIKACE PLAZMATU
V tomto oboru se převážná většina zájmu a relevantních publikací soustřeďuje na inaktivaci bakterií, resp. s ní spojenou dezinfekci až sterilizaci různých materiálů. Pravděpodobně prvním pokusem [18] byla zjištěna urychlená smrt stafylokoků po expozici plazmatem z dnes již kuriózního zdroje (polonium 210 a tritium s vloženým napětím 300 V). V dalších pokusech [19] již byly použity elektrodové systémy s vysokým napětím, umožňující sterilizaci vodných suspenzí Saccharomyces cerevisiae a Bacillus natto. Obsáhlé poznatky v této oblasti shrnula řada přehledných článků, např. Moisana M. et al. [20], Moreaua M. et al. [21], Morenta R. et al. [22], Bourkeové P. et al. [23]; v tomto odstavci jsou zmiňovány studie používající planktonické formy bakterií. Velký počet jednotlivých studií je značně metodicky roztříštěný: inaktivace bakterií byla sledována v suspenzích i na různých površích, nejčastěji agarových půdách; byly používány různé zdroje plazmatu, nejčastěji korónové výboje, dielektrické bariérové výboje a plasma jet; výrazně se lišily i jednotlivé experimentální parametry zdrojových výbojů. Výsledky je přesto možno považovat za zhruba srovnatelné, jejich společným závěrem je, že bakterie jsou plazmatem inaktivovány v závislosti na použité metodice expozicemi v řádu desítek sekund až několika málo minut. Rychlost a účinnost inaktivace se přitom jen málo liší mezi různými bakteriálními druhy [24]; obecně bývají grampozitivní bakterie citlivější než gramnegativní. Příkladem vlivu experimentálního uspořádání může být poněkud rozdílná účinnost korónového výboje v konfiguracích point-to-point a point-to-plane [25]; vliv různých elektrických parametrů výboje ilustrují výsledky studie Scholtze V. et al. [26]: účinnost inaktivace mikrobů se obecně zvyšuje se zvyšujícím se vloženým napětím, samozřejmě i s prodlužující se dobou expozice.
Posledně zmiňovaná studie též ilustruje rozdílnou citlivost prokaryontních a eukaryontních organismů: zatímco bakterie bývají inaktivovány během několika desítek sekund, inaktivace kvasinek vyžaduje expozice v řádu minut. Také v případě kvasinek se projevuje závislost účinnosti inaktivace na experimentálním uspořádání [27]: pro inaktivaci Candida albicans na agarové půdě stačí při použití kvasihomogenního DBD výboje doba expozice kratší než cca 6 minut, potřebných pro inhibici filamentárním DBD výbojem. Při expozici vodné suspenze je ovšem pro inaktivaci téže kandidy nutná expozice po dobu 30 minut [24].
Bakteriální spory jsou na působní plazmatu ještě rezistentnější, jak zmiňuje studie Scholtze V. et al. [24], podrobněji uvádějí práce Boudama M. K. et al. [28], Dobrynina D. et al. [29], Yanga B. et al. [30], Jouberta V. et al. [31], Hojnika N. et al. [32] a shrnuje je přehled Puligundly P. a Moka C. [33]. Pro jejich inaktivaci byla vyzkoušena řada zdrojů plazmatu, jak nízkotlakých (kapacitně vázané a mikrovlnné plazma), tak i zdrojů pracujících za atmosférického tlaku (DBD, korónové výboje, radiofrekvenční plasma jety). Jejich účinnost bývá uváděna jako vyhovující, významného snížení počtu spor bývá dosaženo obvykle během několika minut, jejich kompletní eliminace však vyžaduje expozici v řádu desítek (30–40) minut. Optimální metodika dosud chybí, nejúčinnější se zdají být mikrovlnné výboje při sníženém tlaku; účinnost je ovšem ovlivněna i dalšími parametry, jako složením pracovního plynu, relativní vlhkostí apod.
Bakterie ve formě biofilmu jsou oproti planktonickým obecně méně citlivé na vnější vlivy včetně vyšší rezistence na dezinfekční činidla a antibiotika. V jedné z úvodních studií působení plazmatu na biofilm [34] bylo dosaženo úplné inaktivace biofilmu Chromobacterium violaceum až po desetiminutové expozici plazmatem produkovaným reaktorem Atomflo 250. Řadu pozdějších studií shrnují přehledy [35, 36]. Z jejich závěrů plyne, že plazma je potenciálně významné pro odstraňování biofilmů na různých površích včetně ústní dutiny nebo potravin, její použití je bezpečné pro pacienty i operátora. Nicméně je třeba pamatovat na to, že i při zdánlivě úplném odstranění biofilmu může i jediná přežívající buňka způsobit vývoj nového kompletního biofilmu, zvláště v případech komplexních konsorcií několika různých mikrobů. Některé metody jsou také nákladnější než metody klasické, nicméně je jejich další rozvoj předpokladem minimalizace jejich ceny. Galié et al. [37] uvádějí v přehledu metod likvidace a prevence různých biofilmů plazma jako významnou možnost odstraňování potravinářsky významných patogenů Bacillus cereus, E. coli, Listeria monocytogenes, Salmonella enterica a Staphylococcus aureus. Kromě inaktivace narostlých biofilmů je možno plazmatem docílit přinejmenším částečné prevence jejich opětovného vzniku na slitinách používaných pro výrobu implantátů [38]. Na rozdíl od planktonických forem se pro inaktivaci biofilmu ukázalo jako neúčinné působení plazmatem aktivované vody PAW [8]. Přehled metod inaktivace biofilmů významných v humánní medicíně shrnuje přehled Juláka J. et al. [39]: Široký okruh problematiky interakcí plazmatu s biofilmem je zde rozdělen na studie týkající se obecných aspektů těchto interakcí, na dosud popsaná použití při sterilizaci povrchů různých materiálů používaných v lékařství a na využití plazmatu ve stomatologii. Jsou uvedeny i některé možnosti prevence vývoje biofilmů, jakož i přehled používané instrumentace a jejich výrobců.
Mikroorganismy z říše Fungi včetně plísní a jejich spor jsou k působení plazmatu velmi odolné, jejich citlivost je srovnatelná s bakteriálními sporami. Za tuto odolnost vděčí stavbě své stěny, která je u různých druhů různá, vždy však obsahuje v různém zastoupení chitin [40]. Jejich inaktivace je nicméně možná, jak prokázali Akishev et al. [41] na druzích Aspergillus sp. and Candida spp. rostoucích na povrchu agarového média. Jednotlivé druhy se ovšem svou citlivostí k plazmatu značně liší: zatímco poměrně dobře citlivé kvasinky jsou inaktivovány během několika málo minut, pro plísně exponované na agaru i v suspenzi nalezli Soušková et al. [42, 43, 44] značné rozdíly v citlivosti. Tak např. Cladosporium sphaerospermum, Penicilium crustosum, Trichophyton rubrum a Trichophyton interdigitale byly zcela inaktivovány během 15–25 minut, zatímco Aspergillus oryzae, Arthroderma benhamiae nebo Microsporum gypseum byly i po půlhodině inhibovány jen částečně. Intermediární citlivost pak byla zjištěna pro Alternaria sp. a Byssochlamys nivea. Účinnost inaktivace je přitom závislá na experimentálních podmínkách, např. na povaze použitého výboje [45]. Vyhovující účinnost naštěstí vykazují běžní původci lidských dermatomykóz, jmenovitě Trichophyton rubrum, Trichophyton interdigitale, Microsporum canis a Candida albicans [46], což dává dobré předpoklady pro léčbu těchto onemocnění.
Do oboru mikrobiologie patří též priony, infekční agens tvořená bílkovinou bez nukleových kyselin. Jsou významné jako původci stoprocentně smrtelných a neléčitelných spongiformních encefalopatií, jsou navíc vysoce rezistentní k chemickým i fyzikálním sterilizačním procesům. Některé z nich odolávají i autoklávovaní; podle Rogez-Kreuzeho C. et al. [47] mohou být stoprocentně inaktivovány při laboratorní teplotě peroxidem vodíku ionizovaným v systému Sterrad typu NX (viz tab. 2). Jejich inaktivace je alespoň v laboratorním měřítku možná též jednoduchým korónovým výbojem [48, 49], nebo složitějším vysokofrekvenčním systémem flowing-afterglow [50].
MEDICÍNSKÉ APLIKACE PLAZMATU
Plazma již bylo aplikováno v nejrůznějších oborech lidské činnosti, včetně průmyslu, k úpravám povrchů, v technologii nanočástic apod. Použití v biotechnologiích shrnuje přehled Scholtze V. et al. [51], v potravinářském průmyslu pak přehledy Shawa A. et al. [52], Pankaja S. K. et al. [53], Chizoby Ekezie F. G. et al. [54]. Použití plazmatu ke konzervaci archiválií ověřil Pietrzaka et al. [55]. Využití k čištění odpadních vod uvádí ve své práci Patange A. et al. [56]. Některá raná použití v medicíně shrnuly přehledy Fridmana G. et al. [57], Konga M. G. et al. [58], Isbaryho G. et al. [59], jejich význam je vzhledem k rychlému rozvoji tohoto oboru již spíše jen historický. Přehled Cheruthazhekatty S. et al. [60] shrnul možnosti plazmatické modifikace plastů, kovových slitin, porézních membrán a tkání používaných v medicíně. Ošetření plazmatem je zde prezentováno jako unikátní metoda funkcionalizace povrchů umělých biomateriálů, používaných k výrobě implantátů a podpůrných matric. Takto modifikované povrchy pak podporují adhezi a proliferaci buněk tvořících náhradní tkáně, nebo na ně mohou být vázány pomalu a dlouhodobě uvolňované léčivé antimikrobiální preparáty. Perspektivy využití plazmatu v budoucnosti odhaduje futuristická esej [61], zaměřená hlavně na průmyslové aplikace v technologii skla a optiky, plastů a textilu, v biotechnologiích včetně zemědělských a potravinářských aplikacích a na jejich ekonomický význam. Nicméně je zde předpovídána i významná role plazmatu v medicíně.
Hojení ran
Většina zde uvedených medicínských aplikací spoléhá na inaktivaci mikrobiálních patogenů. Stručný úvod do rozsáhlého souboru těchto aplikací poskytuje přehled [62]. Pro obor „plasma medicine“ jsou v něm jedním ze zakladatelů a vůdčích osobností plazmatické medicíny takto vymezeny základní oblasti působení:
- sterilizace, dezinfekce a dekontaminace;
- zlepšené hojení ran aplikací plazmatu;
- plazma ve stomatologii;
- nádorové aplikace neboli plazmatická onkologie;
- plazmatická farmakologie;
- plazmatické ošetření implantátů pro biokompatibilitu.
V tomto přehledu jsou kromě srozumitelně popsaných principů instrumentace používané pro generování plazmatu uvedeny také některé komerční přístroje schválené pro rutinní používání v tomto oboru; jedná se např. o Rhytec Portrait®, pracující na bázi plasma jetu a schválený US FDA pro použití v dermatologii již v roce 2008. Schválena jsou rovněž zařízení zvaná Bovie J-Plasma®, Canady Helios Cold Plasma a skalpel Hybrid PlasmaTM. V Německu jsou ve třídě IIa certifikovány plasma jety kINPen® a PlasmaDerm® (CINOGY GmbH).
Z terapeutických efektů plazmatu v humánní medicíně je často uváděno zlepšené a zrychlené hojení ran; příčinou tohoto efektu je jednak zrychlená koagulace krve, jakož i inaktivace infikujících a chronické záněty vyvolávajících mikrobů [63]. V této studii bylo rovněž prokázáno, že reaktivní částice produkované plazmatem nemají v koncentracích toxických pro bakterie žádný nepříznivý účinek na životaschopnost a pohyblivost lidských fibroblastů.
Zkrácení doby krvácení ran uvádějí jako jedni z prvních Kuo et al. [64]: na modelu prasat poraněných na kýtě a na ušní žíle zjistili, že aplikace plazmatu ze zdroje typu plasma torch zkracuje dobu krvácení; v závislosti na typu poranění a způsobu aplikace např. ze 190 sekund na 18 sekund nebo z více než 4 minut na 13 sekund.
Další pokroky v tomto oboru shrnuly přehledy Lloyda G. et al. [65], Kuoa S. P. et al. [66], Gweona B. et al. [67], Xionga Z. [68]. Jsou v nich podrobně popsány např. endoskopické elektrochirurgické techniky kontroly aktivního krvácení a koagulace cévních abnormalit, techniky plazmatické ablace, excise a incize systémem Arthrocare CoblationTM, nebo kosmetické odstraňování vrásek systémem Rhytec. V práci Kuo S. P. [66] jsou kromě jinde uvedených principů účinků plazmatu popsány i efekty jeho účinných složek na angiogenezi, kterou pravděpodobně podporují podobným způsobem jako růstové faktory a cytokiny; podrobně jsou zde popsány i další mechanismy účinků plazmatu na buňky a jejich komponenty. Studie Xiong Z. [68] pak je zajímavá podrobnou obrazovou dokumentací působení plazmatu na různá povrchová poranění a léze a průběhu jejich hojení.
Z novějších aplikací plazmatu v tomto oboru je možno zmínit práce Arndta S. et al. [69], Darmawatiho S. et al. [70]. V první z nich jsou podrobně porovnány účinky dvou principiálně odlišných komerčních zařízení. Bylo zjištěno, že jejich působení na buňky je dobře srovnatelné co do exprese kolagenu, indukce cytokinů a růstových faktorů a aktivace imunitních buněk, a tedy i v celkovém příznivém efektu na hojení ran. Rozdíly se projevily jen v ovlivnění proliferace a migrace buněk, mohly však být způsobeny jen rozdílnými experimentálními podmínkami. Druhá výše zmíněná studie podrobně rozpracovává vliv experimentálních podmínek, uvádí možné mechanismy působení a názornými obrázky dokumentuje průběh hojení ran.
Hojení ran je možno také urychlit předběžnou úpravou povrchu obvazových materiálů plazmatem [71]. Těmito úpravami jsou možné nejen ovlivnění povrchových vlastností obvazů (povrchovou energii a propustnost pro vzduch), ale i vazba bioaktivních molekul, jako mikroRNA nebo antimikrobiálních peptidů, podporujících následnou adhezi a proliferaci kmenových buněk.
Možnosti léčby infekčních komplikací v ortopedii shrnul Nguyen et al. [82].
Onkologické aplikace
Novější a poněkud překvapivé jsou aplikace plazmatu v protinádorové terapii. První zmínky o jeho využití v tomto oboru se objevily cca před 10 lety a atraktivita problematiky vedla ke vzniku mnoha nadějných, i když vzhledem k rozsáhlosti problematiky nepříliš dobře porovnatelných studií. Z nich zde budou pro ilustraci uvedeny odkazy na následující, které považujeme za seriózní a reprezentativní. Práce Schlegela J. et al. [72] je přehledem počátečních pokusů publikovaných v tomto oboru. Zavádí termín „plasma oncology“ a uvádí citace na 45 odkazů zabývajících se modelovými pokusy na zvířatech i pokusy o terapii lidských pacientů. Široké spektrum diagnóz zahrnuje fibroblastomy, glioblastomy, neuroblastomy, hepatocelulární karcinomy, melanomy, nádory cervixu, tlustého střeva, ovarií, pankreatu, jakož i případy leukémie. Použitými zdroji plazmatu jsou nejčastěji plasma jet, méně často i DBD. Přehled Songa K. et al. [73] uvádí podobné spektrum nádorových diagnóz, rozšířené o kolorektální a plicní karcinomy. Velká citlivost nádorových buněk na plazma je přičítána zvýšené intracelulární koncentraci reaktivních kyslíkatých částic (ROS), jako mechanismus účinku je uváděna selektivní apoptóza nádorových buněk zprostředkovaná kaspasou-3. Jak uvádí přehled Yana D. et al. [74], zůstává ovšem detailní mechanismus účinku plazmatu na nádorové buňky nejasný. Jako významná je zde navrhována role akvaporinů v transmembránové difuzi peroxidu vodíku, které jsou v nádorových buňkách propustnější než ve zdravých, umožňují tak rychlejší pronikání účinného H2O2 do nádorových buněk a jejich apoptózu a nekrózu. Kromě výše zmíněných zde jsou popisovány účinky plazmatu na buňky nádorů nazofaryngu, ezofágu, prostaty, močového měchýře, štítné žlázy a slinných žláz. Studie Cheruthazhekatty S. et al. [75] přináší některé novější údaje o účincích plazmatu na nádorové buňky a o mechanismech těchto účinků. Plazma je zde doporučováno jako náhrada u malignit rezistentních ke konvenčním chemoterapiím, případně ke kombinacím s nimi, např. s terapií termozolomidem nebo nanočásticemi zlata. Podle Millerové V. et al. [76] je možno plazma použít nejen k lokální aplikaci způsobující smrt nádorových buněk, ale i ke stimulaci systémové odpovědi zpracováním části nádoru, jenž pak způsobí eliminaci všech nádorů obsahujících buňky téhož původu. Díky paměťovému efektu je deklarováno celoživotní působení takto upravených buněk. Článek Keidara M. et al. [77] uvádí některé novější zkušenosti v tomto oboru, jako jeho přínos je možno zmínit důraz na „samoorganizaci“ plazmatu a na význam experimentálních podmínek použitých zdrojů, zejména budicího napětí, pro jeho účinnost. V pojednání Bekeschuse S. et al. je zdůrazněn význam ROS a RNS produkovaných plazmatem pro usnadnění imunogenního zabíjení nádorových buněk a potenciaci protinádorové imunity. Přehled Pasqual-Melové G. et al. [79] se soustřeďuje na případy maligního melanomu a uvádí výsledky klinických studií jeho léčby. Z nich vyplývá, že jako poměrně účinné se jeví kombinace plazmatu se současnou aplikací ionizujícího záření, imunoterapie, nanočástic, elektrochemoterapie, fotodynamické terapie a chemoterapie.
Tento rozvíjející se obor aplikací plazmatu bývá zpravidla označován jako nadějný, praktická uplatnění však obvykle nachází spíše v experimentu než v rutinní praxi. Dobrou zprávou je, že terapie nádorů plazmatem má minimální vedlejší účinky, neboť nepoškozuje zdravé tkáně [80]. Protinádorové účinky vykazuje též plazmatem aktivovaná voda (PAW) [81].
Stomatologické aplikace
Časté a v literatuře hojně zastoupené jsou aplikace plazmatu v dentální, resp. obecně orální medicíně. Plazma je zde zpravidla používáno k inaktivaci ústní mikroflóry, která je zvláště na zubech přítomna ve formě odolných biofilmů. Prvními pokusy v tomto oboru byly téměř současně uveřejněné studie, které ukazují, jak může dané téma tzv. „viset ve vzduchu“ [83, 84]. Za použití plasma jetu jako zdroje plazmatu bylo dosaženo již po minutové expozici inhibice kariogenního Streptococcus mutans na agarovém médiu. Expozice téhož streptokoka ve formě biofilmu kultivovaného bez přídavku sacharózy poskytla podobné výsledky, ovšem biofilm kultivovaný s přídavkem 0,15 % sacharózy se podařilo jen omezit, a to i po opakovaných expozicích plazmatem. Potvrzuje to jak předpokládanou větší rezistenci biofilmu, tak i význam sacharózy pro jeho restituci.
Pozdější pokroky v dekontaminaci, ale i při modifikacích zubních implantátů, pokrývání nebo čištění povrhu zubů apod. shrnují přehledy Pasqual-Melové G. et al. [85], Azada A. [86], Gherardiho M. et al. [87]. Plyne z nich, že rozsáhlý soubor popisovaných aplikací, shrnutý pod pojem „plasma dentistry“, je možno rozdělit do dvou kategorií definovaných jako ošetřování povrchů a přímé aplikace. První kategorie zahrnuje metody modifikace povrchu zubních implantátů modifikující jejich adhezivní vlastnosti, podporující polymerizaci, pokrývání povrchů a jejich čištění. Přímé aplikace pak zahrnují různé mikrobicidní aktivity, zejména povrchové dekontaminace a čištění zubních kanálků. Výhodou všech těchto aplikací je, že na rozdíl od jiných metod, např. laseru, jsou šetrné k živým tkáním a nijak je nepoškozují. Jejich účinek je přitom srovnatelný s běžně používaným desinficiens chlorhexidindiglukonátem.
Jako velmi lákavá se jeví možnost čištění a dezinfekce zubních kanálků a kariózních dutin od endodontického biofilmu; pravděpodobně první pokusy v tomto oboru popsali Sladek et al. [88]. Uvádějí 99% redukci kariogenního Streptococcus mutans po aplikaci plazmatu ze zdroje plasma jet po dobu 1,5 minuty. Podobné výsledky popisují i pozdější studie, např. práce, kde jsou doloženy názornou obrazovou dokumentací [89]. Kromě řady dalších aplikací byl také navržen poněkud kuriózní speciální tříelektrodový systém pro bělení zubů [90].
Dermatologické aplikace
Některé rané aplikace plazmatu v dermatologii shrnul přehled [91], uvádějící léčbu atopické dermatitidy, impetiga, folikulitidy a dalších bakteriálních infekcí. Plazma se uplatňuje i v kosmetické medicíně [92], kde již bylo použito k odstraňování jizev, strií, akné, dyskeratózy, bradavic, mateřských znamének (névů), fibromů a dalších kožních lézí. Je zde uvedeno též úspěšné použití při blefaroplastice očních víček. Je uváděno jen několik kontraindikací těchto kosmetických výkonů, zejména těhotenství a některá systémová onemocnění. Obecně jsou dermatologické aplikace umožněny neškodností plazmatu pro zdravou pokožku [93], kterou je tímto způsobem možno dezinfikovat a během 5–10 minut expozice jí zbavit rezidentní mikroflóry. Problematika bezpečnosti při humánních aplikacích plazmatu je podrobně pojednána a dokumentována ve studii Isbaryho G. et al. [94].
Aplikace plazmatu umožňuje terapii některých povrchových plísňových onemocnění, jak bylo ověřeno pokusy na zvířecích modelech [95, 96]. Na klinickém případu dermatomykózy (tinea corporis, ringworm) se pak prokázala eliminace původce onemocnění Trichophyton interdigitale, jakož i významné zkrácení projevů subjektivních i objektivních příznaků [97, 98]. Také při léčbě plísňových onemocnění nehtů (onychomykóze, tinea unguium) se ve většině případů projevily příznivé účinky aplikace plazmatu, které mohou být podpořeny i dalšími terapeutickými metodami. Aplikace plazmatu byla úspěšná i v případech neúspěšné léčby jen klasickými lokálními i systémovými preparáty [99, 100]. Tato předběžná sdělení uvádějí výsledky získané jen na malém počtu pacientů, v současnosti probíhají rozsáhlejší klinické studie nejen u nás, ale i v zahraničí; podrobnosti o nich je možno nalézt na odkazech [101, 102, 103]. Vzhledem k odolnosti původců onemocnění jsou ovšem v těchto případech nutné opakované expozice plazmatem po dobu několika týdnů.
Poděkování
Vypracování tohoto přehledu bylo podpořeno výzkumným programem Univerzity Karlovy Progres Q25.
Do redakce došlo dne 1. 6. 2019.
doc. RNDr. Jaroslav Julák, CSc.
Ústav imunologie a mikrobiologie 1. LF UK
Studničkova 2028
128 00 Praha-Nové Město
e-mail: Jaroslav.julak@lf1.cuni.cz
Sources
1. Shintani H, Sakudo A (Eds). Gas Plasma Sterilization in Microbiology: Theory, Applications, Pitfalls and New Perspectives. Poole: Caister Academic Press; 2016. Dostupné na www: https://dx.doi.org/10.21775/9781910190258.
2. Metelmann HR, von Woedtke T, Weltmann KD (Eds). Comprehensive clinical plasma medicine: Cold physical plasma for medical applications. Cham: Springer; 2019. Dostupné na www: https://dx.doi.org/10.1007/978-3-319-67627-2 .
3. Graves DB. The emerging role of reactive oxygen and nitrogen species in redox biology and some implications for plasma applications to medicine and biology. J Phys D: App. Phys, 2012;45 : 263001. Dostupné na www: https:// iopscience.iop.org/article/10.1088/0022-3727/45/26/263001.
4. Liu DX, Liu ZC, Chen C, et al. Aqueous reactive species induced by a surface air discharge: Heterogeneous mass transfer and liquid chemistry pathways. Sci Rep, 2016;6 : 23737. Dostupné na www: http://dx.doi.org/10.1038/srep23737.
5. Liao X, Liu D, Xiang Q, et al. Inactivation mechanisms of non-thermal plasma on microbes: A review. Food Control, 2017;75 : 83–91. Dostupné na www: http://dx.doi.org/10.1016/j.foodcont.2016.12.021 .
6. Laurita R, Barbieri D, Gherardi M, et al. Chemical analysis of reactive species and antimicrobial activity of water treated by nanosecond pulsed DBD air plasma. Clin Plasma Med, 3 : 53–6. Dostupné na www: http://dx.doi.org/10.1016/j.cpme.2015.10.001.
7. Julák J, Hujacová A, Scholtz V, et al. Contribution to the chemistry of plasma activated water. Plasma Phys Rep, 2018;44 : 125–136. Dostupné na www: https://link.springer.com/article/10.1134/S1063780X18010075.
8. Hozák P, Scholtz V, Khun J, et al. Further contribution to the chemistry of plasma activated water: Influence on bacteria in planktonic and biofilm form. Plasma Phys Rep, 2018;44 : 799–804. Dostupné na www: https://link.springer.com/article/10.1134/S1063780X18090040.
9. Thirumdas R, Kothakota A, Annapure U, et al. Plasma activated water (PAW): Chemistry, physico-chemical properties, applications in food and agriculture. Trends Food Sci Technol, 2018;77 : 21–31. Dostupný na www: https://doi.org/10.1016/j.tifs.2018.05.007 .
10. Ehlbeck J, Schnabel U, Polak M, et al. Low temperature atmospheric pressure plasma sources for microbial decontamination. J Phys D:Appl Phys, 2011;44 : 013002. Dostupné na www: http://dx.doi.org/10.1088/0022-3727/44/1/013002.
11. Šimončicová J, Kryštofová S, Medvecká V, et al. Technical applications of plasma treatments: current state and perspectives. Appl Microbiol Biotechnol, 2019;13 : 5117–5129. Dostupné na www: https://doi.org/10.1007/s00253-019-09877-x .
12. Khun J, Scholtz V, Hozák P, et al. Various DC driven point-to-plain discharges as non-thermal plasma sources and their bactericidal effects. Plasma Sources Sci Technol, 2018;27 : 065002. Dostupné na www: https://doi.org/10.1088/1361-6595/aabdd0 .
13. Scholtz V, Julák J. The “cometary” discharge, a possible new type of DC electric discharge in air at atmospheric pressure, and its bactericidal properties. J Phys: Conf Ser, 2010;223:012005. Dostupné na www: https://iopscience.iop.org/article/10.1088/1742-6596/223/1/012005 .
14. Scholtz V, Kvasničková E, Julák J. Microbial inactivation by electric discharge with metallic grid. Acta Phys Polon A, 2013;A124 : 62–65. Dostupné na www: http://dx.doi.org/10.12693/APhysPolA.124.62 .
15. Laroussi M, Akan T. Arc-free atmospheric pressure cold plasma jets: A review. Plasma Proces Polym, 2007; 4 : 777–788. Dostupné na www: https://doi.org/10.1002/ppap.200700066.
16. Nishime TMC, Borges AC, Koga-Ito CY, et al. Non-thermal atmospheric pressure plasma jet applied to inactivation of different microorganisms. Surf Coat Technol, 2017;312 : 19–24. Dostupné na www: http://dx.doi.org/10.1016/j.surfcoat.2016.07.076.
17. Nowakowska H, Czylkowski D, Hrycak B, et al. Characterization of a novel microwave plasma sheet source operated at atmospheric pressure. Plasma Sources Sci Technol, 2018;27 : 085008. Dostupné na www: https://doi.org/10.1088/1361-6595/aad402 .
18. Krueger AP, Smith RF, Go IG. The action of air ions on bacteria. I. Protective and lethal effect on suspensions of staphylococci in droplets. J Gen Physiol, 1957;41 : 359–381. Dostupné na www: 10.1085/jgp.41.2.359 .
19. Mizuno A, Hori Y. Destruction of living cells by pulsed high-voltage application. IEEE Trans Ind Appl, 1988;24 : 387–394. Dostupné na www: http://dx.doi.org/10.1109/28.2886.
20. Moisan M, Barbeau J, Moreau S, et al. Low-temperature steriliza-tion using gas plasmas: a review of the experiments and an analysis of the inactivation mechanisms. Int J Pharm, 2001;226 : 1–21. Dostupné na www: http://dx.doi.org/10.1016/S0378-5173(01)00752-9.
21. Moreau M, Orange N, Feuilloley MGJ. Non-thermal plasma technologies: New tools for biodecontamination. Biotechnol Adv, 2008;26 : 610–617. Dostupné na www: http://dx.doi.org/10.1016/j.biotechadv.2008.08.001 .
22. Morent R, De Geyter N. Inactivation of bacteria by non-thermal plasmas. In: Reza Fazel-Rezai (Ed.) Biomedical Engineering – Frontiers and Challenges. InTechOpen, 2011 : 25–54. Dostupné na www: http://dx.doi.org/10.5772/18610 .
23. Bourke P, Ziuzina D, Han L, et al. Microbiological interactions with cold plasma. J Appl Microbiol, 2017;123 : 308–324. Dostupné na www: https://doi.org/10.1111/jam.13429.
24. Scholtz V, Julák J, Kříha V. The microbicidal effect of low-temperature plasma generated by corona discharge: Comparison of various microorganisms on an agar surface or in aqueous suspension. Plasma Proces and Polym, 2010;7 : 237–243. Dostupné na www: http://dx.doi.org/10.1002/ppap.200900072.
25. Scholtz V, Julák J, Štěpánková B. Comparison of point-to plane and point-to point corona discharge for the decontamination or sterilization of surfaces and liquids. Plasma Med, 2011;1 : 21–25. Dostupný na www: http://www.dl.begellhouse.com/journals/5a5b4a3d419387fb,6239f734065d8e3d,27305c4e2624a95a.html.
26. Scholtz V, Kommová L, Julák J. The influence of parameters of stabilized corona discharges on its germicidal effects. Acta Phys Polon A, 2011;A119 : 803–806. Dostupné na www: http://przyrbwn.icm.edu.pl/APP/PDF/119/a119z6p12.pdf.
27. Sláma J, Kříha V, Julák J, et al. Comparison of dielectric barrier discharge modes fungicidal effect on Candida albicans growth. Probl Atom Sci Technol, 2013;83 : 237–239. Dostupné na www: http://vant.kipt.kharkov.ua/ARTICLE/VANT_2013_1/article_2013_1_237.pdf.
28. Boudam MK, Moisan M, Saoudi B, et al. Bacterial spore inactivation by atmospheric-pressure plasmas in the presence or absence of UV photons as obtained with the same gas mixture. J Phys D: Appl Phys, 2006;39 : 3494–3507. Dostupné na www: https://doi.org/10.1088/0022-3727/39/16/s07.
29. Dobrynin D, Fridman G, Mukhin YV, et al. Cold plasma inactivation of Bacillus cereus and Bacillus anthracis (anthrax) spores. IEEE Trans Plasma Sci, 2010;38 : 1878–1884. Dostupné na www: https://ieeexplore.ieee.org/document/5437219.
30. Yang B, Chen J, Yu Q, et al. Inactivation of Bacillus spores using a low-temperature atmospheric plasma brush. IEEE Trans Plasma Sci, 2010;99 : 1–8. Dostupné na www: https://www.semanticscholar.org/paper/Inactivation-of-Bacillus-Spores-Using-a-Atmospheric-Yang-Chen/8df1be3a7d492f098a92b9397b61af5ab1f9f559.
31. Joubert V, Cheype C, Bonnet J, et al. Inactivation of Bacillus subtilis var. niger of both spore and vegetative forms by means of corona discharges applied in water. Water Res, 2013;47 : 1381–1389. Dostupné na www: http://dx.doi.org/10.1016/j.watres.2012.12.011.
32. Hojnik N, Modic M, Ni Y, et al. Effective fungal spore inactivation with an environmentally friendly approach based on atmospheric pres-sure air plasma. Environ Sci Technol, 2019;53 : 1893−1904. Dostupné na www: https://doi.org/10.1021/acs.est.8b05386 .
33. Puligundla P, Mok C. Inactivation of spores by nonthermal plasmas. World J Microbiol Biotechnol, 2018;34 : 143. Dostupné na www: https://doi.org/10.1007/s11274-018-2527-3.
34. Abramzon N, Joaquin JC, Bray J, et al. Biofilm destruction by RF high-pressure cold plasma jet. IEEE Trans Plasma Sci, 2006;34 : 1304–1309. Dostupné na www: http://dx.doi.org/10.1109/TPS.2006.877515.
35. Brelles-Mariño G. Challenges in biofilm inactivation: The use of cold plasma as a new approach. J Bioproces Biotech, 2012;2 : 1000e107. Dostupné na www: http://dx.doi.org/10.4172/2155-9821.1000e107.
36. Brelles-Mariño G. Gas-discharge plasma: Biofilm inactivation. In.: Leon Shohet J (Ed.). Encyclopedia of Plasma Technology, First Edition. Boca Raton: CRC Press; 2016. Dostupné na www: https://doi.org/10.1201/9781351204958.
37. Galié S, García-Gutiérrez C, Miguélez EM, et al. Biofilms in the foodindustry: Health aspects and control methods. Front Microbiol, 2018;9 : 898. Dostupné na www: http://dx.doi.org/10.3389/fmicb.2018.00898.
38. Vaňková E, Válková M, Kašparová P, et al. Prevention of biofilm redevelopment on Ti6Al4V alloy by cometary discharge with metallic grid. Contrib Plasma Phys, 2019;59 : 166–172. Dostupné na www: http://dx.doi.org/10.1002/ctpp.201800044.
39. Julák J, Scholtz V, Vaňková E. Medically important biofilms and non-thermal plasma. World J Microbiol Biotechnol, 2018;34 : 178. Dostupné na www: https://doi.org/10.1007/s11274-018-2560-2.
40. Latgé J-P. The cell wall: a carbohydrate armour for the fungal cell. Mol Microbiol, 2007;66 : 279–290. Dostupné na www: https://doi.org/10.1111/j.1365-2958.2007.05872.x .
41. Akishev Y, Grushin M, Karalnik V, et al. Atmospheric-pressure, nonthermal plasma sterilization of microorganisms in liquids and on surfaces. Pure Appl Chem, 2008;80 : 1953–1969. Dostupné na www: http://dx.doi.org/10.1351/pac200880091953.
42. Soušková H, Scholtz V, Julák J, et al. The survival of micromycetes and yeasts under the low-temperature plasma generated in electrical discharge. Folia microbiol, 2011;56 : 77–79. Dostupné na www: http://dx.doi.org/10.1007/s12223-011-0005-5.
43. Soušková H, Scholtz V, Julák J, et al. The fungal spores survival under the low-temperature plasma. In: Hensel K, Machala Z, Akishev Y (Eds). Plasma for Bio-Decontamination, Medicine and Food Security. Dordrecht: Springer; 2012. s. 57–66. Dostupné na www: http://dx.doi.org/10.1007/978-94-007-2852-3.
44. Scholtz V, Soušková H, Hubka V, et al. Inactivation of human pathogenic dermatophytes by non-thermal plasma. J Microbiol Meth, 2015;119 : 53–58. Dostupné na www: http://dx.doi.org/10.1016/j.mimet.2015.09.017.
45. Julák J, Soušková H, Scholtz V, et al. Comparison of fungicidal pro-perties of non-thermal plasma produced by corona discharge and dielectric barrier discharge. Folia microbiol, 2018;63 : 63–68. Dostupné na www: http://alerts.springer.com/re?l=D0In697yhI6gzce7pIh.
46. Daeschlein G, Scholz S, von Woedtke T, et al. In vitro killing of clinical fungal strains by low-temperature atmospheric-pressure plasma jet. IEEE Trans Plasma Sci, 2011;39 : 815–821. Dostupné na www: http://dx.doi.org/10.1109/TPS.2010.2063441.
47. Rogez-Kreuz C, Yousfi R, Soufflet C, et al. Inactivation of animal and human prions by hydrogen peroxide gas plasma sterilization. Infect Control Hosp Epidemiol, 2009;30 : 769–777. Dostupné na www: https://doi.org/10.1086/598342.
48. Julák J, Janoušková O, Scholtz V, et al. Inactivation of prions using electrical DC discharges at atmospheric pressure and ambient temperature. Plasma Proces Polym, 2011;8 : 316–323. Dostupné na www: https://doi.org/10.1002/ppap.201000100.
49. Janoušková O, Julák J, Scholtz V, et al. Inactivation of Rml pions using gas plasma generated by negative corona discharge at ambient temperature. Prion, 2011;5 : 131–131.
50. Elmoualij B, Thellin O, Gofflot S, et al. Decontamination of prions by the flowing afterglow of a reduced-pressure N2–O2 cold plasma. Plasma Proces Polym, 2012;9 : 612–618. Dostupné na www: http://dx.doi.org/10.1002/ppap.201100194.
51. Scholtz V, Pazlarová J, Soušková H, et al. Nonthermal plasma – the tool for decontamination and disinfection. Biotech Adv, 2015;33 : 1108–1119. Dostupné na www: http://dx.doi.org/10.1016/j.biotechadv.2015.01.002.
52. Shaw A, Shama G, Iza F. Emerging applications of low temperature gas plasmas in the food industry. Biointerphases, 2015;10 : 029402. Dostupné na www: http://dx.doi.org/10.1116/1.4914029.
53. Pankaj SK, Keener KM. Cold plasma: background, applications and current trends. Cur Opinion Food Sci, 2017;6 : 49–52. Dostupné na www: http://dx.doi.org/10.1016/j.cofs.2017.07.008.
54. Chizoba Ekezie FG, Sun DW, Cheng JH. A review on recent advances in cold plasma technology for the food industry: Current applications and future trends. Trends Food Sci Technol, 2017;69 : 46–58. Dostupné na www: http://dx.doi.org/10.1016/j.tifs.2017.08.007.
55. Pietrzaka K, Otlewska A, Danielewicz D, et al. Disinfection of archival documents using thyme essential oil, silver nanoparticles misting and low temperature plasma. J Cult Herit, 2017;24 : 69–77. Dostupné na www: http://dx.doi.org/10.1016/j.culher.2016.10.011.
56. Patange A, Boehm D, Giltrap M, et al. Assessment of the disinfection capacity and eco-toxicological impact of atmospheric cold plasma for treatment of food industry effluents. Sci Total Environ, 2018;631/632 : 298–307. Dostupné na www: http://dx.doi.org/10.1016/j.scitotenv.2018.02.269.
57. Fridman G, Friedman G, Gutso A, et al. Applied plasma medicine. Plasma Proces Polym, 2008;5 : 503–33. Dostupné na www: http://dx.doi.org/10.1002/ppap.200700154.
58. Kong MG, Kroesen G, Morfill G, et al. Plasma medicine: an introductory review. New J Phys, 2009;11 : 115012. Dostupné na www: http://dx.doi.org/10.1088/1367-2630/11/11/115012.
59. Isbary G, Shimizu T, Li YF, et al. Cold atmospheric plasma devices for medical issues. Expert Rev Med Dev, 2013;10 : 367–77. Dostupné na www: http://dx.doi.org/10.1586/erd.13.4.
60. Cheruthazhekatt S, Černák M, Slavíček P, et al. Gas plasmas and plasma modified materials in medicine. J Appl Biomed, 2010;8 : 55–66. Dostupné na www: http://dx.doi.org/10.2478/v10136-009-0013-9.
61. Weltmann K-D, Kolb JF, Holub M, et al. The future for plasma science and technology. Plasma Proces and Polym, 2018;e1800118. Dostupné na www: https://doi.org/10.1002/ppap.201800118.
62. Laroussi M. Plasma medicine: A brief introduction. Plasma, 2018;1 : 5. Dostupné na www: https://doi.org/10.3390/plasma1010005.
63. Nosenko T, Shimizu T, Morfill GE. Designing plasmas for chronic wound disinfection. New J Phys, 2009;11 : 115013. Dostupné na www: http://dx.doi.org/10.1088/1367-2630/11/11/115013.
64. Kuo SP, Chen CY, Lin C S, et al. Wound bleeding control by low temperature air plasma. IEEE Trans Plasma Sci, 2010;38 : 1908–1914. Dostupné na www: http://dx.doi.org/10.1109/TPS.2010.2047028.
65. Lloyd G, Friedman G, Jafr S, et al. Gas plasma: Medical uses and developments in wound care. Plasma Proces Polym, 2010;7 : 194–211. Dostupné na www: http://dx.doi.org/10.1002/ppap.200900097.
66. Haertel B, von Woedtke T, Weltmann KD, et al. Non-thermal atmospheric-pressure plasma: possible application in wound healing. Biomol Therap, 2014;22 : 477–490. Dostupné na www: http://dx.doi.org/10.4062/biomolther.2014.105.
67. Gweon B, Kim K, Choe W, et al. Therapeutic uses of atmospheric pressure plasma: Cancer and wound. In: Jo H, Jun HW, Shin J, Lee S (Eds). Biomedical Engineering: Frontier Research and Converging Technologies. Biosystems & Biorobotics, vol 9. Cham: Springer; 2016. s. 357–385. Dostupné na www: http://dx.doi.org/10.1007/978-3-319-21813-7.
68. Xiong Z. Cold atmospheric pressure plasmas (CAPs) for skin wound healing. In: Yusuf Tutar (Ed.). Plasma medicine – concepts and clinical application. Rijeka: IntechOpen; 2018. s. 121–140. Dostupné na www: http://dx.doi.org/10.5772/intechopen.76093.
69. Arndt S, Schmidt A, Karrer S, et al. Comparing two different plasma devices kINPen and Adtec SteriPlas regarding their molecular and cellular effects on wound healing. Clin Plasma Med, 2018;9 : 24–33. Dostupné na www: https://dx.doi.org/10.1016/j.cpme.2018.01.002.
70. Darmawati S, Rohmani A, Nurani LH, et al. When plasma jet is effective for chronic wound bacteria inactivation, is it also effective for wound healing? Clin Plasma Med, 219;14 : 100085. Dostupné na www: https://dx.doi.org/10.1016/j.cpme.2019.100085.
71. Eswaramoorthy N, McKenzie DR. Plasma treatments of dressings for wound healing: a review. Biophys Rev, 2017;9 : 895–917. Dostupné na www: http://dx.doi.org/10.1007/s12551-017-0327-x.
72. Schlegel J, Köritzer J, Boxhammer V. Plasma in cancer treatment. Clin Plasma Med, 2013;1 : 2–7. Dostupné na www: http://dx.doi.org/10.1016/j.cpme.2013.08.001.
73. Song K, Li G, Ma Y. A review on the selective apoptotic effect of nonthermal atmospheric-pressure plasma on cancer cells. Plasma Med, 2014;4 : 193–209. Dostupné na www: http://dx.doi.org/10.1615/PlasmaMed.2015012629.
74. Yan D, Talbot AN, Sherman H, et al. Toward understanding the selective anticancer capacity of cold atmospheric plasma – a model based on aquaporins (Review). Biointerphases, 2015;10 : 040801. Dostupné na www: http://dx.doi.org/10.1116/1.4938020.
75. Hirst AM, Frame FM, Arya M, et al. Low temperature plasmas as emerging cancer therapeutics: the state of play and thoughts for the future. Tumour Biol, 2016;37 : 7021–7031. Dostupné na www: http://dx.doi.org/10.1007/s13277-016-4911-7.
76. Miller V, Lin A, Fridman A. Why target immune cells for plasma treatment of cancer. Plasma Chem Plasma Proc, 2016;36 : 259–268. Dostupné na www: http://dx.doi.org/10.1007/s11090-015-9676-z.
77. Keidar M, Yan D, Beilis II, et al. Plasmas for treating cancer: opportunities for adaptive and self-adaptive approaches. Trends Biotechnol, 2017;36 : 586–593. Dostupné na www: http://dx.doi.org/10.1016/j.tibtech.2017.06.013.
78. Bekeschus S, Clemen R, Metelmann HR. Potentiating anti-tumor immunity with physical plasma. Clin Plasma Med, 2018;12 : 17–22. Dostupné na www: https://dx.doi.org/10.1016/j.cpme.2018.10.001.
79. Pasqual-Melo G, Gandhirajan RK, Stoffels I, et al. Targeting malignant melanoma with physical plasmas. Clin Plasma Med, 2018;10 : 1–8. Dostupné na www: https://doi.org/10.1016/j.cpme.2018.03.001.
80. Schuster M, Rutkowski R, Hauschild A, et al. Side effects in cold plasma treatment of advanced oral cancer – clinical data and biological interpretation. Clin Plasma Med, 2018;10 : 9–15. Dostupné na www: https://doi.org/10.1016/j.cpme.2018.04.001.
81. Boehm D, Curtin J, Cullen PJ, et al. Hydrogen peroxide and beyond – the potential of high-voltage plasma-activated liquids against cancerous cells. Anti-cancer Agents Med Chem, 2017;17:1–9. Dostupné na www: http://dx.doi.org/10.2174/1871520617666170801110517.
82. Nguyen L, Lu P, Boehm D, Bourke P, et al. Cold atmospheric plasma is a viable solution for treating orthopedic infection: a review. Biol Chem, 2018;400 : 77–86. Dostupné na www: https://doi.org/10.1515/hsz-2018-0235.
83. Goree J, Liu B, Drake D, et al. Killing of S. mutans bacteria using a plasma needle at atmospheric pressure. IEEE Trans Plasma Sci, 2006;34 : 1317–1324. Dostupné na www: http://dx.doi.org/10.1109/TPS.2006.878431.
84. Sladek REJ, Filoche SK, Sissons CH, et al. Treatment of Streptococcus mutans biofilms with a nonthermal atmospheric plasma. Lett Appled Microbiol, 2007;45 : 318–323. Dostupné na www: https://doi.org/10.1111/j.1472-765X.2007.02194.x.
85. Cha S, Park YS. Plasma in dentistry. Clin Plasma Med, 2014;2 : 4–10. Dostupné na www: http://dx.doi.org/10.1016/j.cpme.2014.04.002.
86. Azad A. Dental applications of cold atmospheric plasma. Int J Contemp Med Res, 2017;4 : 1304–1305. Dostupné na www: https://www.researchgate.net/publication/325848621_Dental_Applications_of_Cold_Atmospheric_Plasma.
87. Gherardi M, Tonini R, Colombo V. Plasma in dentistry: Brief history and current status. Trends Biotechnol, 2017;36 : 583–585. Dostupné na www: http://dx.doi.org/10.1016/j.tibtech.2017.06.009.
88. Sladek REJ, Stoffels E, Walraven R, et al. Plasma treatment of dental cavities: a feasibility study. IEEE Trans Plasma Sci, 200432 : 1540–1543. Dostupné na www: https://ieeexplore.ieee.org/document/1341519.
89. Schaudinn C, Jaramillo D, Freire MO, et al. Evaluation of a nonthermal plasma needle to eliminate ex vivo biofilms in root canals of extracted human teeth. Int Endodont J, 2013;46 : 930–937. Dostupné na www: http://dx.doi.org/10.1111/iej.12083.
90. Lee HW, Nam SH, Mohamed AAH, et al. Atmospheric pressure plasma jet composed of three electrodes: Application to tooth bleaching. Plasma Proces Polym, 2010;7 : 274–280. Dostupné na www: http://dx.doi.org/10.1002/ppap.200900083.
91. Heinlin J, Morfill G, Landthaler M, et al. Plasma medicine: possible applications in dermatology. J German Soc Dermatol, 2010;8 : 968–976. Dostupné na www: http://dx.doi.org/10.1111/j.1610-0387.2010.07495.x.
92. King M. Focus on Plasma: The application of plasma devices in aesthetic medicine. PMFA News, 2017;4 : 5. Dostupné na www: https://www.thepmfajournal.com/features/post/focus-on-plasma-the-application-of-plasma-devices-in-aesthetic-medicine.
93. Julák J, Scholtz V. Decontamination of human skin by low-temperature plasma produced by cometary discharge. Clin Plasma Med, 2013;1 : 31–34. Dostupné na www: http://dx.doi.org/10.1016/j.cpme.2013.09.002.
94. Isbary G, Köritzer J, Mitra A, et al. Ex vivo human skin experiments for the evaluation of safety of new cold atmospheric plasma devices. Clin Plasma Med, 2013;1 : 36–44. Dostupné na www: http://dx.doi.org/10.1016/j.cpme.2012.10.001.
95. Julák J, Soušková H, Živná H, et al. Možnosti využití nízkoteplotního plazmatu v léčbě plísňových onemocnění. Veterinární lékař, 2016;14 : 199–204. Dostupné na www: http://www.tigis.cz/images/stories/Veterinarni_Lekar/2016/42016/VL_clanek_Julak_4_2016.pdf .
96. Scholtz V, Soušková H, Švarcová M, et al. Inactivation of dermatophyte infection by nonthermal plasma on animal model. Med Mycol, 2017;55 : 422–428. Dostupné na www: https://doi.org/10.1093/mmy/myw094.
97. Švarcová M, Julák J, Hubka V, et al. Treatment of a superficial mycosis by low-temperature plasma: Case report. Prague Med Rep, 2014;115 : 73–78. Dostupné na www: http://pmr.cuni.cz/file/5683/PMR2014A0008.pdf .
98. Scholtz V, Soušková H, Švarcová M, et al. Inactivation of dermatophytes by non-thermal plasma in vitro and a case report. Dermatophyte workshop Utrecht, Utrecht, 2016. Dostupné na www: http://www.isham.org/members/Dermatophyte/lectures/Sunday/18_Svarcova-Inactivation-plasma.pdf .
99. Lux J, Dobiáš R, Scholtz V, et al. Effectiveness of onychomycosis therapy using non-thermal plasma: Preliminary results. ASM Microbe, Atlanta, USA, 2018. Dostupné na www: https://www.researchgate.net/publication/328578143_Effectiveness_of_Onychomycosis_Therapy_Using_Non_-Thermal_Plasma_Preliminary_Results.
100. Lux J, Dobiáš R, Scholtz V, et al. Možnosti terapie onychomykózy nízkoteplotním plazmatem – kazuistiky. Čs dermatol, 2018;93 : 266–271. Dostupné na www: https://www.prolekare.cz/casopisy/cesko-slovenska-dermatologie/2018-6-12/moznosti-terapie-onychomykozy-nizkoteplotnim-plazmatem-107987.
101. Pilot Study to Evaluate Plasma Treatment of Onychomycosis. US National Library of Medicine, NCT01819051. Dostupné na www: https://clinicaltrials.gov/ct2/show/NCT01819051.
102. Evaluating the Safety, Tolerability and Preliminary Efficacy of Plasma in Improving the Appearance of Onychomycosis. US National Library of Medicine, NCT02724384. Dostupné na www: https://clinicaltrials.gov/ct2/showNCT02724384?recrs=ab&cond=Onychomycosis&cntry1=NA%3AUS&draw=1&rank=10.
103. Early Feasibility Study to Evaluate the Efficacy of the RenewalNail™ Plasma Treatment System in Patients With Onychomycosis (Fungal Nail). US National Library of Medicine, NCT03216200. Dostupné na www: https://clinicaltrials.gov/ct2/show/3216200?recrs=ab&cond=Onychomycosis&cntry1=NA%3AUS&draw=1&rank=3.
Labels
Hygiene and epidemiology Medical virology Clinical microbiology
Article was published inEpidemiology, Microbiology, Immunology

2020 Issue 1-
All articles in this issue
- Tvorba biofilmu močovými patogénmi izolovanými z chronických a rekurentných infekcií močových ciest a vplyv biofilmu na in vitro účinok gentamicínu a kolistínu
- Možnosti terapeutického ovlivnění stafylokokových infekcí prostřednictvím bakteriofágů a vybrané metody testování citlivosti stafylokoků in vitro
- Klonální charakterizace kmenů Streptococcus pneumoniae metodami MLST a MLVA – může metoda MLVA charakterizaci zkvalitnit?
- Využití nízkoteplotního plazmatu v mikrobiologii a medicíně
- Biologická agens bioterorismu – připravenost je nezbytná
- První potvrzený záchyt kmene Staphylococcus argenteus v České republice
- Vzpomínka na MUDr. Martinu Havlíčkovou, CSc.
- Zemřel doc. MUDr. Zdeněk Ježek, DrSc., Rytíř českého lékařského stavu
- Preexpoziční profylaxe jako novinka v prevenci HIV infekce: zkušenosti HIV centra Ústřední vojenské nemocnice Praha
- Epidemiology, Microbiology, Immunology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Možnosti terapeutického ovlivnění stafylokokových infekcí prostřednictvím bakteriofágů a vybrané metody testování citlivosti stafylokoků in vitro
- Biologická agens bioterorismu – připravenost je nezbytná
- První potvrzený záchyt kmene Staphylococcus argenteus v České republice
- Preexpoziční profylaxe jako novinka v prevenci HIV infekce: zkušenosti HIV centra Ústřední vojenské nemocnice Praha
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

