-
Medical journals
- Career
Invazivní pneumokokové onemocnění v České republice v letech 2000–2006
Authors: J. Motlová; Č. Beneš; P. Křížová
Authors‘ workplace: Státní zdravotní ústav, Praha
Published in: Epidemiol. Mikrobiol. Imunol. 57, 2008, č. 1, s. 14-21
Overview
Cíl práce:
Zhodnocení nemocnosti invazivního pneumokokového onemocnění v České republice a analýza pokrytí sérotypů působících invazivní onemocnění pneumokokovými vakcínami.Metodika:
Z období 1997-2006 je analyzována nemocnost a smrtnost hlášené pneumokokové meningitidy (EPIDAT). Dále jsou analyzována data NRL pro streptokoky a enterokoky z období 2000-2006. Nemocnost invazivního pneumokokového onemocnění byla počítána z populace spádových oblastí spolupracujících laboratoří. Typizace pneumokoků byla prováděna v NRL. Bylo určováno procento sérotypů zahrnutých v pneumokokových vakcínách u pneumokoků izolovaných z invazivních onemocnění v období 2000-2006.Výsledky:
Nemocnost invazivního pneumokokového onemocnění se pohybovala v rozmezí 2,30–4,28/100 000 obyvatel. Specifická věková nemocnost invazivního pneumokokového onemocnění dosahovala v letech 2000-2006 nejvyšších hodnot v nejmladších věkových skupinách: 0-11 měsíců 15,75/100 000 a 1-4 roky 8,22/100 000, věková skupina nad 65 roků věku byla na třetím místě (7,3/100 000). Celková smrtnost pneumokokové meningitidy v období 1997-2006 byla 13,7 %. Nejvyšší věkově specifická smrtnost byla zaznamenána u pacientů 65 a více roků věku (24 %). V nejmladších věkových skupinách (0-11 m a 1-4 r) je pokrytí sérotypů konjugovanými vakcínami vyšší než u dospělé populace (40-64 r a nad 65 roků). Ve věkové skupině 0-11 m je pokrytí sérotypů 7-valentní konjugovanou vakcínou 66 %, 10-valentní konjugovanou vakcínou 76 %, 13-valentní konjugovanou vakcínou 82 %. Ve věkové skupině 1-4 r je pokrytí sérotypů 7-valentní konjugovanou vakcínou 65,1 %, 10-valentní konjugovanou vakcínou 76,4 %, 13-valentní konjugovanou vakcínou 85,8 %.Závěr:
Nemocnost invazivního pneumokokového onemocnění v České republice v letech 2000-2006 zjištěná na základě laboratorních dat je srovnatelná s hodnotami uváděnými v Evropě. Nejvyšší nemocnost byla zjištěna v nejnižších věkových skupinách. Distribuce sérotypů působících invazivní pneumokokové onemocnění je odlišná v dětské a dospělé populaci. Pokrytí sérotypů konjugovanými pneumokokovými vakcínami je v dětských věkových skupinách vyšší (66–65 %) než v dospělé a starší populaci (34–65 %). Je žádoucí zahájit celorepublikový program surveillance invazivních pneumokokových onemocnění. Rovněž je žádoucí zařadit pneumokokovou konjugovanou vakcínu do očkovacího schématu dětí.Klíčová slova:
invazivní pneumokokové onemocnění – incidence – pokrytí sérotypů vakcínami – vakcinační strategie.V posledních letech byla v řadě zemí registrována pneumokoková konjugovaná vakcína a v některých zemích již byla zařazena do rutinní vakcinace [10, 16, 19]. Podkladem k rozhodnutí o zařazení pneumokokové vakcíny do rutinní vakcinace má být analýza nemocnosti a smrtnosti invazivního pneumokokového onemocnění. Z tohoto důvodu byla v některých zemích zavedena surveillance invazivních pneumokokových onemocnění, která umožňuje kromě přesného stanovení vakcinační strategie i analýzu efektivity zavedené vakcinace [1–4, 6, 8, 9, 11, 12, 17, 18, 20-24].
V České republice jsou rutinním hlásícím systémem EPIDAT sledovány pouze pneumokokové meningitidy. Ostatní klinické projevy invazivního pneumokokového onemocnění zůstávají v EPIDATu nehlášeny. Celorepublikový program surveillance invazivních pneumokokových onemocnění je zaváděn v roce 2008. Vzhledem k tomu, že celosvětový trend zavádění konjugované pneumokokové vakcíny do rutinní vakcinace je doporučen i Světovou zdravotnickou organizací [26], byla v České republice vyvinuta snaha o získání přesnějších údajů o výskytu invazivního pneumokokového onemocnění, než jaké v současnosti poskytuje EPIDAT.
Retrospektivně byla analyzována laboratorní databáze invazivních pneumokokových onemocnění Národní referenční laboratoře (NRL) pro streptokoky a enterokoky. Sdělení prezentuje srovnání s daty EPIDAT a uvádí pokrytí sérotypů pneumokoků z invazivních onemocnění pneumokokovými vakcínami.
Materiál a metodika
EPIDAT – pneumokoková meningitida
Z období 1997-2006 je analyzována nemocnost a smrtnost - celková a věkově specifická.
Laboratorní data NRL – invazivní pneumokokové onemocnění
Jsou analyzována data z období 2000-2006. Nemocnost byla počítána z populace spádových oblastí 51 laboratoří, které do NRL posílaly všechny izoláty z invazivních pneumokokových onemocnění. Identifikace pneumokoků byla prováděna standardními metodami ve spolupracujících laboratořích a ověřována v NRL. Typizace pneumokoků byla prováděna v NRL Quellung metodou typově specifickými pneumokokovými antiséry (Statens Serum Institut, Kodaň).
Definice invazivního pneumokokového onemocnění
V souladu s definicí ECDC je invazivní pneumokokové onemocnění podmíněno laboratorním průkazem S. pneumoniae z krve, likvoru nebo jiného materiálu, který je za normálních okolností sterilní. Laboratorní průkaz je prováděn kultivací, latexovou aglutinací a metodou PCR (Polymerase Chain Reaction).
Pokrytí sérotypů pneumokokovými vakcínami
Bylo určováno procento sérotypů zahrnutých v pneumokokových vakcínách (již dostupných či vyvíjených) u pneumokoků izolovaných z invazivních onemocnění v období 2000-2006.
7-valentní konjugovaná vakcína (PCV-7) obsahuje sérotypy 4, 6B, 9V, 14, 18C, 19F a 23F. 9-valentní konjugovaná vakcína (PCV-9) obsahuje navíc sérotypy 1 a 5. 10-valentní konjugovaná vakcína (PCV-10) obsahuje navíc sérotyp 3. 11-valentní konjugovaná vakcína (PCV-11) obsahuje navíc sérotyp 7F.13-valentní konjugovaná vakcína (PCV-13) obsahuje navíc sérotypy 6A a 19A. 23-valentní polysacharidová vakcína (PPV-23) obsahuje navíc sérotypy 2, 8, 9N, 10A, 11A, 12F, 15B, 17F, 20, 22F a 33F, neobsahuje sérotyp 6A.
Výsledky
Nemocnost invazivního pneumokokového onemocnění se pohybovala v rozmezí 2,30–4,28/100 000 obyvatel – tabulka 1. Srovnání věkově specifické nemocnosti pneumokokové meningitidy ukazuje, že rozdíly mezi pasivním hlášením (EPIDAT) a daty NRL nejsou významné (tabulka 1, graf 1). Pokud však srovnáme věkovou nemocnost pneumokokové meningitidy v hlášení EPIDAT a věkovou nemocnost invazivního pneumokokového onemocnění v datech NRL (graf 2) je patrné, že v pasivním hlášení dochází k podhlášení ve věkových skupinách nad 40 roků. Specifická věková nemocnost invazivního pneumokokového onemocnění dosahovala v letech 2000-2006 nejvyšších hodnot v nejmladších věkových skupinách: 0-11 měsíců 15,75/100 000 a 1-4 roky 8,22/100 000 (graf 3). Věková skupina nad 65 roků věku byla na třetím místě (7,3/100 000). Celková nemocnost invazivního pneumokokového onemocnění vykazovala za sledované období 2000-2006 stabilní trend – graf 4.
Table 1. Pneumokoková meningitida a invazivní pneumokokové onemocnění Česká republika, 1997-2006, nemocnost na 100 000 (EPIDAT, data NRL) Table 1. Pneumococcal meningitis and invasive pneumococcal disease in the Czech Republic, 1997-2006, incidence per 100 000 population (EPIDAT, NRL data) 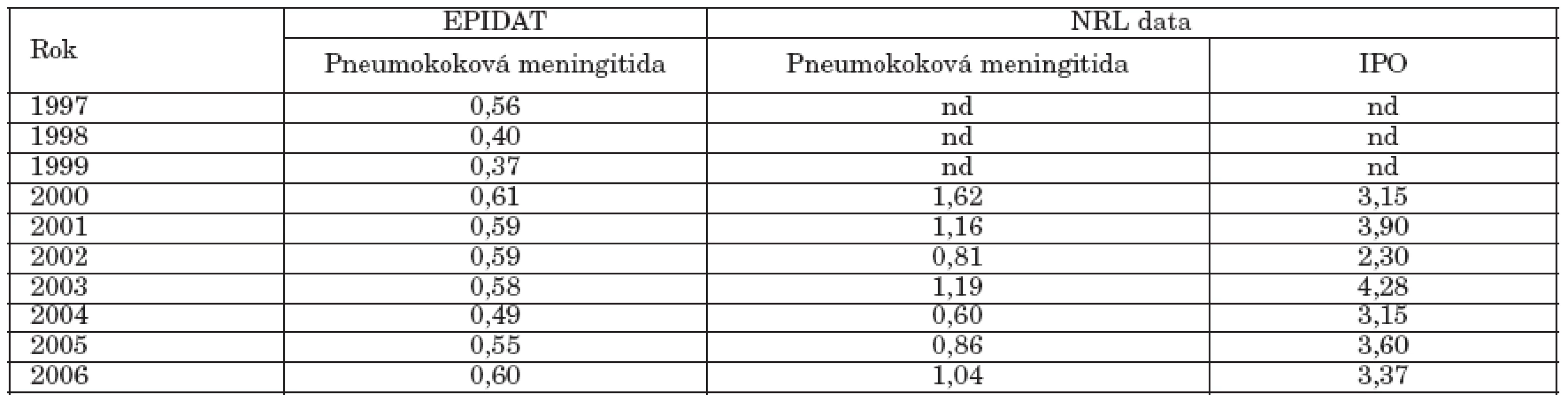
nd = nedostupná data IPO = invazivní pneumokokové onemocnění nd = data not available IPO = invasive pneumococcal disease Graph 1. Pneumokoková meningitida, věkově specifická nemocnost - srovnání dat NRL a EPIDAT, Česká republika, 2000-2006 Figure 1. Pneumococcal meningitis, age-specific incidence – comparison of the NRL and EPIDAT data, Czech Republic, 2000- 2006 
Graph 2. Věkově specifická nemocnost: EPIDAT (pneumokoková meningitida), data NRL (invazivní pneumokokové onemocnění), Česká republika, 2000-2006 Figure 2. Age-specific incidence: EPIDAT (pneumococcal meningitis), NRL data (invasive pneumococcal disease), Czech Republic, 2000-2006 
Graph 3. Invazivní pneumokokové onemocnění - věkově specifická nemocnost, Česká republika, 2000-2006, data NRL Figure 3. Invasive pneumococcal disease, age-specific incidence, Czech Republic, 2000-2006, NRL data 
Graph 4. Invazivní pneumokokové onemocnění - celková nemocnost, Česká republika, 2000-2006, data NRL Figure 4. Invasive pneumococcal disease, total incidence, Czech Republic, 2000-2006, NRL data 
Podklady k hodnocení smrtnosti jsou dostupné pouze pro pneumokokovou meningitidu v hlášení EPIDAT. Celková smrtnost v období 1997-2006 byla 13,7 %. Nejvyšší věkově specifická smrtnost byla zaznamenána u pacientů 65 a více roků věku (24 %) – graf 5. V nejmladších věkových skupinách byla smrtnost relativně nízká (2,3 % u pacientů pod 1 rok věku a 4,7 % u 1-4 letých. Ve věkových skupinách 5-9 roků a 10-14 roků nebylo zaznamenáno žádné úmrtí. Od 15 let věku smrtnost v jednotlivých věkových skupinách postupně vzrůstala.
Graph 5. Věkově specifická smrtnost pneumokokové meningitidy, Česká republika, 1997-2006, EPIDAT Figure 5. Age-specific fatality rate of pneumococcal meningitis, Czech Republic, 1997-2006, EPIDAT 
Distribuci sérotypů působících invazivní pneumokokové onemocnění v České republice v letech 2000-2006 zachycuje tabulka 2. Nejčastěji zjištěné sérotypy ve všech věkových skupinách byly: 3 (12,3 %), 4 (9 %), 14 (7,7 %), 8 (6,7 %) a 19F (6,1 %). Tabulka rovněž dokumentuje rozdílnou distribuci sérotypů ve čtyřech věkových skupinách s nejvyšší incidencí invazivního pneumokokového onemocnění. Ve věkové skupině 0-11 m byly zjištěny dva nejčastější sérotypy 6B (24 %) a 19F (16 %), ve věkové skupině 1-4 r byly tři nejčastější sérotypy 14 (13,2 %), 6B (12,3 %) a 23F (11,3 %), ve věkové skupině 65 a více roků byly čtyři nejčastější sérotypy 3 (15 %), 4 a 9N (oba 8,2 %) a 14 (7,1 %), ve věkové skupině 40-64 roků tři nejčastější sérotypy 3 (14,2 %), 8 (10,4 %) a 4 (10,2 %). Rozdílná distribuce sérotypů v jednotlivých věkových skupinách se promítá i do rozdílného pokrytí sérotypů pneumokokovými vakcínami, které je zachyceno v tabulce 2 a na grafu 6. Ve dvou nejmladších věkových skupinách (0-11 m a 1-4 r) je pokrytí sérotypů 7-valentní konjugovanou vakcínou nad 60 % (66 % a 65,1 %), 9-valentní konjugovanou vakcínou nad 70 % (74 % a 72,6 %), 10-valentní konjugovanou vakcínou 76 % a 76,4 %, 11-valentní konjugovanou vakcínou 82 % a 76,4 %, 13-valentní konjugovanou vakcínou 82 % a 85,8 %, 23-valentní polysacharidovou vakcínou 92 % a 95,3 %. (Pokrytí sérotypů 23-valentní polysacharidovou vakcínou ve věkové skupině 0-11 m je uváděnou pouze teoreticky, protože v této věkové skupině není polysacharidová vakcína účinná.) Ve starších věkových skupinách (65 a více r a 40-64 r) je pokrytí sérotypů 7-valentní konjugovanou vakcínou pod 40 % (39,3 % a 34,4 %), 9-valentní konjugovanou vakcínou 42,9 % a 38,2 %, 10-valentní konjugovanou vakcínou 57,9 % a 52,4 %, 11-valentní konjugovanou vakcínou 60,4 % a 56,7 %, 13-valentní konjugovanou vakcínou 65 % a 62,2 %, 23-valentní polysacharidovou vakcínou 90,4 % a 89,2 %. Ve všech věkových skupinách je pokrytí sérotypů 7-valentní konjugovanou vakcínou 41,5 %, 9-valentní konjugovanou vakcínou 47,1 %, 11-valentní konjugovanou vakcínou 62,8 %, 13-valentní konjugovanou vakcínou 67,9 %, 23-valentní polysacharidovou vakcínou 90,6 %.
Table 2. Sérotypy S. pneumoniae působící invazivní pneumokokové onemocnění v České republice, 2000-2006 (data NRL) Table 2. S. pneumoniae serotypes causing invasive pneumococcal disease in the Czech Republic, 2000-2006 (NRL data) 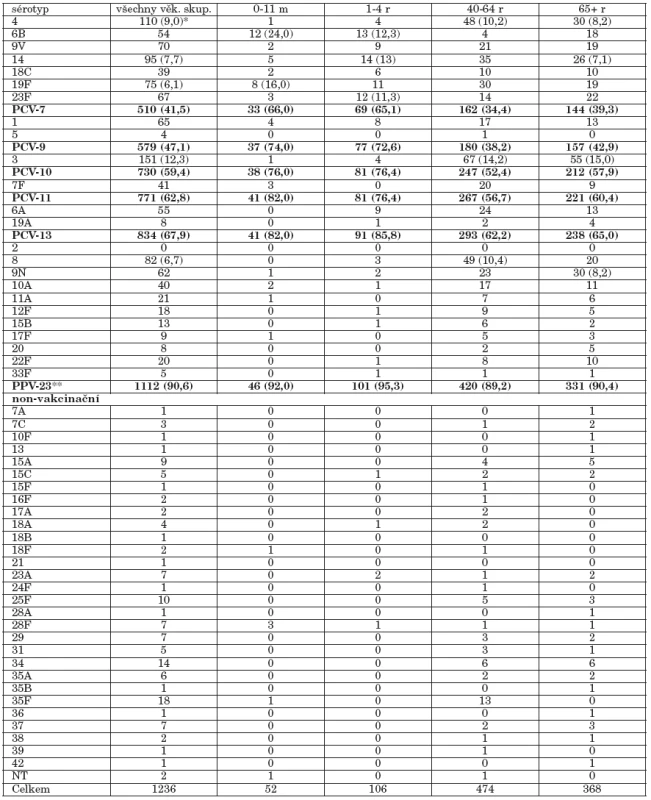
*, v závorkách je procento sérotypů v jednotlivých věkových kategoriích počítané z typovaných izolátů u nejfrekventnějších sérotypů a pro PCV-7, PCV-9, PCV-10, PCV-11, PCV-13 a PPV-23; NT, netypovatelný; PCV-7, 7-valentní pneumokoková konjugovaná vakcína; PCV-9, 9- valentní pneumokoková konjugovaná vakcína; PCV-10, 10- valentní pneumokoková konjugovaná vakcína; PCV-11, 11- valentní pneumokoková konjugovaná vakcína; PCV-13, 13- valentní pneumokoková konjugovaná vakcína; PPV-23, 23- valentní pneumokoková polysacharidová vakcína; **vakcína neobsahuje sérotyp 6A *, in brackets, the percentages of serotypes in different age groups calculated from the numbers of typed isolates for the most frequent serotypes and PCV-7, PCV-9, PCV-10, PCV-11, PCV-13 and PPV-23; NT, nontypeable; PCV-7, 7-valent pneumococcal conjugate vaccine; PCV-9, 9-valent pneumococcal conjugate vaccine; PCV-10, 10-valent pneumococcal conjugate vaccine; PCV- 11, 11-valent pneumococcal conjugate vaccine; PCV-13, 13-valent pneumococcal conjugate vaccine; PPV-23, 23- valent pneumococcal polysaccharide vaccine; **vaccine does not contain serotype 6A Graph 6. Pokrytí sérotypů působících invazivní pneumokokové onemocnění pneumokokovými vakcínami, Česká republika, 2000-2006, data NRL Figure 6. Coverage of causative serotypes by pneumococcal vaccines, Czech Republic, 2000-2006, NRL data 
Diskuse
V řadě evropských zemí je prováděna surveillance invazivních pneumokokových onemocnění a pneumokoková konjugovaná vakcína byla zařazena do očkovacího schématu dětí [1, 2, 3, 4, 6, 8, 9, 10, 11, 12, 16-24].
Srovnání incidence invazivních pneumokokových onemocnění v jednotlivých zemích je však ztíženo odlišnou metodikou jejich sledování (pasivní hlášení, aktivní surveillance, laboratory-based data) a odlišným definováním onemocnění (case definice). Incidence invazivních pneumokokových onemocnění se tedy v Evropě pohybuje v širokém rozsahu: 5,8/100 000 (Holandsko), 6,3/100 000 (Itálie), 7,6/100 000 (Švýcarsko), 8,9/100 000 (Německo), 14,5/100 000 (UK), 24,2/100 000 (Finsko), 42/100 000 (Izrael). Je doporučeno dodržovat ECDC definici invazivního pneumokokového onemocnění: laboratorně potvrzená etiologie (kultivací, latexovou aglutinací, PCR). Bylo prokázáno, že při pasivním hlášení invazivního pneumokokového onemocnění dochází k jeho podhlášení [23] a pouze kvalitně prováděná surveillance poskytuje validní informace, které mohou být podkladem ke stanovení odpovídající vakcinační strategie a dávají předpoklady pro zhodnocení účinnosti vakcinace.
Několikaleté zkušenosti se zavedením plošné vakcinace dětí pneumokokovou konjugovanou vakcínou ukazují, že dochází k nepřímému efektu vakcinace, tj. snížení nemocnosti i v neočkovaných dospělých věkových skupinách díky snížené cirkulaci pneumokoků v populaci vlivem vakcinace [5, 7, 15].
V České republice není invazivní pneumokokové onemocnění dosud hlášeno. V hlásícím systému EPIDAT je hlášena pouze pneumokoková meningitida. Celorepublikový program surveillance je zaváděn v roce 2008 a jeho význam spočívá zejména v rozšíření sledovaných klinických obrazů, tj. sledování všech závažných onemocnění s průkazem pneumokoků z materiálů sterilních za normální situace. Pro získání validních dat však bude nezbytné zvýšit u závažných onemocnění provádění hemokultivací a PCR diagnostiky. Žádáme mikrobiology o zasílání izolátů S. pneumoniae z původně sterilního klinického materiálu a ze sekčního materiálu do NRL pro streptokoky a enterokoky k typizaci.
Pokrytí sérotypů pneumokokovými vakcínami v České republice ukázalo u konjugovaných vakcín rozdíl mezi dětskou a dospělou populací: dětská populace vykazuje vyšší pokrytí. Toto zjištění je příznivé se zřetelem ke skutečnosti, že při vývoji pneumokokových konjugovaných vakcín nebyla distribuce sérotypů v České republice výrobcům vakcín známa. Vzestup pokrytí sérotypů u vícevalentních vakcín je v dětské populaci pomalejší než v dospělé a starší populaci. První informace o pokrytí sérotypů u pneumokoků izolovaných v České republice byly publikovány za období 1995-2003 [13, 14]. Jsou zaznamenány mírné rozdíly v pokrytí sérotypů vzhledem k tomu, že do analýz byly zahrnuty i kmeny izolované z dolních cest dýchacích a sputa. Detailní informace o konjugovaných pneumokokových vakcínách poskytuje přehledný článek Prymuly [19, www.sabin.org/pace].
V souladu s mezinárodními doporučeními [26, www.sabin.org/pace ] je žádoucí zařadit pneumokokovou konjugovanou vakcínu do očkovacího schématu dětí.
Závěr
Nemocnost invazivního pneumokokového onemocnění v České republice v letech 2000-2006 zjištěná na základě laboratorních dat je srovnatelná s hodnotami uváděnými v Evropě. Nejvyšší nemocnost byla zjištěna v nejnižších věkových skupinách. Distribuce sérotypů působících invazivní pneumokokové onemocnění je odlišná v dětské a dospělé populaci. Pokrytí sérotypů konjugovanými pneumokokovými vakcínami je v dětských věkových skupinách vyšší (66–85 %) než v dospělé a starší populaci (34–65 %). Je žádoucí zařadit pneumokokovou konjugovanou vakcínu do očkovacího schématu dětí.
Poděkování
Práce byla podpořena projektem IGA MZ ČR reg. č. NR/8770-3-2006.
Do redakce došlo 30. 7. 2007
RNDr. Jitka Motlová, CSc.
NRL pro streptokoky a enterokoky
SZÚ
Šrobárova 48
100 42 Praha 10
e-mail: motlova@szu.cz
Sources
1. Bossen Konradsen, H., Staum Kaltoft, M. Invasive pneumococcal infections in Denmark from 1995 to 1999: Epidemiology, serotypes, and resistance. Clin Diagn Lab Immunol 2002, 9, 358-365.
2. Dagan, R., Englehard, D., Piccard, E. Epidemiology of invasive childhood pneumococcal infections in Israel. JAMA 1992, 268, 3328-3332.
3. D’Ancona F. et al. Incidence of vaccine preventable pneumococcal invasive infections and blood culture practices in Italy. Vaccine 2005, 23, 2494-2500.
4. Escola, J. et al. Epidemiology of invasive pneumococcal infections in children in Finland. JAMA 1992, 268, 3323-3327.
5. Hammitt, L.L. et al. Indirect effect of conjugate vaccine on adult carriage of Streptococcus pneumoniae: An explanation of trends in invasive pneumococcal disease. J Infec Dis 2006, 193, 1487-1494.
6. Hausdorff, W.P. Invasive pneumococcal disease in children: Geographic and temporal variations in incidence and serotype distribution. Eur J Pediatr 2002, 161, 135-139.
7. Isaacman, D.J. et al. Indirect effects associated with widespread vaccination of infants with heptavalent pneumococcal conjugate vaccine (PCV7, Prevnar). Vaccine 2007, 25, 2420-2427.
8. Ispahani P. et al. Twenty year surveillance of invasive pneumococcal disease in Nottingham: Serogroups responsible and implications for immunisation. Arch Dis Child 2004, 89, 757-762.
9. Kaltoft, M.S., Zeuthen, N., Konradsen, H.B. Epidemiology of invasive pneumococcal infections in children aged 0-6 years in Denmark: A 19-year nationwide surveillance study. Acta Paediatr 2000, 435, 3-10.
10. Lopalco, P. Editorial team. Use of 7-valent pneumococcal conjugate vaccine in EU. Euro Surveill 2006, 11(12):E061207.3. Available from: http://www. eurosurveillance.org/ew/2006/061207.asp#3.
11. McIntosh, E.D.G., Fritzell, B., Fletcher, M.A. Burden of paediatric invasive pneumococcal disease in Europe, 2005. Epidemiol Infect 2006, 7, 1-13.
12. Miller E. et al. Epidemiology of invasive and other pneumococcal disease in children in England and Wales 1996-1998. Acta Paediatr 2000, 89, 11-16.
13. Motlová, J. Distribuce sérotypů Streptococcus pneumoniae v České republice, duben 1995-prosinec 1998. Klin mikrobiol inf lék 1999, 2-3, 60-64.
14. Motlová, J. Distribuce sérotypů a séroskupin Streptococcus pneumoniae u pacientů s invazivními pneumokokovými onemocněními v České republice v letech 1996-2003: podklady pro vakcinační strategii. Epidemiol Mikrobiol Imunol 2005, 1, 3-10.
15. O’Brien, K.L., Dagan, R. The potential indirect effect of conjugate pneumococcal vaccines. Vaccine 2003, 21, 1815-1825.
16. Pebody, R.G. Pneumococcal vaccination policy in Europe. Euro Surveill 2005, 10, 174-178.
17. Pebody, R.G. et al. Pneumococcal disease surveillance in Europe. Euro Surveill 2006, 11, 171-178.
18. Pedersen, M.K. Systemic pneumococcal disease in Norway 1995-2001: Capsular types and antimicrobial resistance. Epidemiol Infect 2004, 132, 167-175.
19. Prymula, R. Současný pohled na konjugované pneumokokové vakcíny. Klin mikrobiol inf lék 2006, 3, 98-102.
20. Serrano, I., Ramirez, M., Melo-Cristino, J. Invasive Streptococcus pneumoniae from Portugal: Implications for vaccination and antimicrobial therapy. Clin Microbiol Infect 2004, 10, 652-656.
21. Spanjaard, L. et al. Epidemiology of meningitis and bacteremia due to Streptococcus pneumoniae in the Netherlands. Acta Paediatr Suppl 2000, 89, 22-26.
22. Venetz, I., Schopfer, K., Muhlemann, K. Paediatric invasive pneumococcal disease in Switzerland, 1985-1994. Int J Epidemiol 1998, 27, 1101-1104.
23. Vergison, A. et al. Epidemiologic features of invasive pneumococcal disease in Belgian children: Passive surveillance is not enough. Pediatrics 2006, 118, 801-809.
24. Von Kries, R. et al. Proportion of invasive pneumococcal infections in German children preventable by pneumococcal conjugate vaccines. Clin Infect Dis 2000, 31, 482-487.
25. Von Kries, R. et al. Prediction of the potential benefit of different pneumococcal conjugate vaccines on invasive pneumococcal disease in German children. Pediatr Infect Dis J 2002, 21, 1017-1023.
26. WHO position paper: Pneumococcal conjugate vaccine for childhood immunization. Weekly Epidemiological Record 2007, 82, 93-104.
Labels
Hygiene and epidemiology Medical virology Clinical microbiology
Article was published inEpidemiology, Microbiology, Immunology

2008 Issue 1-
All articles in this issue
- Průkaz životaschopných, metabolicky aktivních kvasinkových buněk pomocí kolorimetrického média
- Séroprevalencia Toxoplasma gondii u gravidných žien na Slovensku
- Invazivní pneumokokové onemocnění v České republice v letech 2000–2006
- Problematika vulvovaginálního dyskomfortu z hlediska mezioborové spolupráce
- Epidemiology, Microbiology, Immunology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Séroprevalencia Toxoplasma gondii u gravidných žien na Slovensku
- Problematika vulvovaginálního dyskomfortu z hlediska mezioborové spolupráce
- Průkaz životaschopných, metabolicky aktivních kvasinkových buněk pomocí kolorimetrického média
- Invazivní pneumokokové onemocnění v České republice v letech 2000–2006
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

