-
Medical journals
- Career
Úvod do problematiky urogenitálních píštělí: incidence, etiologie, klasifikace, symptomatologie a diagnostika
Authors: Antonín Prouza 1; Lyudmila Vyacheslavovna Tikhonova 2
Authors‘ workplace: Bristol Urological Institute, Southmead Hospital, Bristol, United Kingdom 1; Urology Clinic, JSC European Medical Center, Moscow, Russia 2
Published in: Ces Urol 2020; 24(4): 261-276
Category: Review article
Overview
Prouza A, Tikhonova VL. Úvod do problematiky urogenitálních píštělí: incidence, etiologie, klasifikace, symptomatologie a diagnostika.
Předmětem tohoto textu je přehledně přiblížit čtenáři téma urogenitálních píštělí. Zatímco v rozvojových zemích představují nejčastější příčinu vzniku píštěle poranění vzniklá v důsledku protrahovaného porodu, jsou ve vyspělých státech tyto komplikace naštěstí relativně vzácné. Zde vzniká urogenitální píštěl obvykle jako následek nerozpoznaného iatrogenního poranění močových cest během operačního výkonu; typicky hysterektomie. Radioterapie pánevní oblasti či zánětlivé onemocnění pánve představují některé z méně běžných příčin rozvoje píštělí. Zcela charakteristickým příznakem je kontinuální denní i noční nekontrolovatelný únik moči, který v přítomnosti rizikových faktorů souvisejících s možnou formací píštěle nutí lékaře pomyslet na tuto poměrně vzácnou diagnózu. Důsledně odebraná anamnéza, zevrubné urogynekologické fyzikální vyšetření a barvivový test představují první diagnostické kroky, které jsou často schopné píštěl spolehlivě odhalit. Ze zobrazovacích vyšetření rutinně využíváme retrográdní a mikční cystouretrografii a kontrastní CT močových cest, které vyloučí souběžné poranění močovodů. Uretrocystoskopie v indikovaných případech doplněná biopsií suspektních lézí je nedílnou součástí předoperační diagnostiky. S ohledem na rozsah následujícího sdělení se autoři nezabývají léčbou a managementem píštělí, které budou předmětem budoucího přehledového článku.
Klíčová slova:
urogenitální – píštěl – vezikovaginální – porodnický – iatrogenní
ÚVOD
Problematika urogenitálních píštělí je poměrně rozsáhlá a v řadě ohledů tak může i zkušeným lékařům působit jak diagnostické, tak terapeutické rozpaky. Právě z tohoto důvodu působí poměrně překvapivě absence jednotných doporučení, která by tuto tématiku detailně a systematicky zpracovaly1 . Toto je i limitem následujícího sdělení, které se navíc pro nedostatek kvalitně vedených studií opírá z velké části o průřezové a retrospektivní studie, soubory kazuistik, názory expertů a odborných panelů. Jednotlivá data tak musí být pečlivě interpretována.
<hr>
1 V době publikace tohoto přehledového článku jsou k dispozici doporučení EAU (Evropské urologické asociace) ve formě krátkého addenda guidelines pro inkontinenci moči, zatímco ICS (Mezinárodní společnost pro kontinenci) je v poslední fázi vývoje obsáhlého dokumentu terminologie urogenitálních píštělí.
<hr>
Píštěl představuje patologickou komunikaci mezi dvěma a vzácně i více orgány. V případě urogenitálních fistulí tak v užším slova smyslu hovoříme o abnormálním spojení mezi přilehlými orgány močového traktu a pohlavního ústrojí ženy. Charakteristiky takové píštěle s jejími příznaky pak nejlépe dokumentuje anatomická klasifikace, tak jak bude uvedeno dále v textu. Většina urogenitálních píštělí se vyvine jako následek porodních poranění a komplikací u žen v rozvojových zemích světa (1, 2). S tímto tvrzením ostře kontrastuje skutečnost, že až 90 % píštělí ve vyspělých zemích vzniká iatrogenně, nejčastěji jako následek pánevní operace (3, 4).
PORODNICKÉ PÍŠTĚLE
Incidence, etiologie a patogeneze
Svým počtem jsou porodní poranění způsobená komplikovaným a nepostupujícím porodem nejčastější příčinou vzniku urogenitálních píštělí v rozvojových zemích světa. Skutečná prevalence porodnických píštělí však není známa a její odhady mají obecně tendenci situaci značně podhodnocovat. Relativně reálnou se nicméně jeví incidence často citovaná Světovou zdravotnickou organizací, dle které na světě ročně nově přibude mezi 50 000 – 100 000 nových případů. Odhadem tak touto chorobou trpí celosvětově kolem tří milionů žen (5).
Existují četné epidemiologické studie pocházející převážně ze států rovníkové Afriky, které se podrobně věnují analýze rizikových faktorů souvisejících se vznikem porodnických píštělí. Typická pacientka je obvykle velmi mladá prvorodička (42 % mladší 20 let), bez formálního vzdělání pocházející z velmi chudých socioekonomických poměrů rurálních oblastí zemí Třetího světa, která nemá žádný či jen velmi omezený přístup k nezbytné zdravotní péči (6). Většina porodů je vedených doma, bez asistence porodníka či kvalifikovaného dohledu a bez časného přístupu k potencionálně život zachraňujícímu urgentnímu výkonu, jako je akutní císařský řez. Následky tak bývají katastrofální jak pro matku, tak pro často mrtvě rozené dítě.
Mezi některé ze zjištěných rizikových antropometrických rysů patří obecně nižší postava postižených žen, často pod 150 cm (7) a zúžený příčný průměr pánve mezi sedacími hrboly (8). Naopak přímá souvislost s genitálními mutilacemi se prokázat nepodařila.
Mechanismus rozvoje píštěle souvisí s protrahovaným tlakem hlavičky plodu během nepostupujícího porodu na měkké tkáně matky uskřinuté mezi kostěné struktury porodního kanálu a hlavou plodu, které vedou k rozvoji lokální ischemické nekrózy a následné formaci urogenitální píštěle. Polohu píštěle charakterizuje úroveň, při které došlo k zástavě progrese porodu. Na rozdíl od iatrogenních píštělí, které vznikají často jako následek pouze diskrétních poranění, bývají porodnické píštěle výrazně rozsáhlejší a závažnější a mohou způsobit kompletní devastaci nejen pohlavního a močového traktu matky, ale i konečníku, svalů a nervů perinea a přilehlých kostěných struktur. V anglickém písemnictví se pro tento stav vžil termín „obstructed labor injury complex“, pro který česká literatura nemá v současnosti adekvátní ekvivalent. Popisuje primárně komplexní poranění, která vznikla jako přímý následek protrahovaného porodu, tak sekundární stavy, které vznikají jako pozdější konsekvence v souvislosti s únikem moči a komplikovaným hojením.
Vedle rozvoje uretrovaginální, vezikovaginální či ureterovaginální píštěle může vleklý porod způsobit poranění pochvy vedoucí až k její nekróze, nebo defektu rektovaginálního septa s formací rektovaginální píštěle, jejichž problematika je mimo rámec tohoto textu. Dalším závažným následkem je částečná či dokonce až kompletní destrukce nebo denervace levátoru a tedy celé diaphragma pelvis.
Sekundární potíže mají obzvláště výrazný psychologicko‑sociální přesah. Již tak často nízký společenský status ženy v těchto zemích vede k její kompletní izolaci a stigmatizaci. Vysoká míra rozvodovosti (9), nemožnost sociální interakce a prohlubující se chudoba vedou nevyhnutelně k rozvoji duševních poruch až se suicidálními intencemi.
IATROGENNÍ PÍŠTĚLE
Incidence, etiologie a patogeneze
Iatrogenní poranění močových cest během pánevní operace naopak představuje suverénně nejběžnější příčinu rozvoje urogenitálních píštělí žen žijících ve vyspělých zemích světa. Z dat ze Spojených států vyplývá, že urogenitální píštěle vznikají nejpravděpodobněji jako následek gynekologických operací (10) vedených z benigní indikace (80 %), výrazně méně často jako důsledek porodních poranění či komplikací (10 %), pánevních operací pro malignitu (5 %) a radioterapie malé pánve (5 %).
Hysterektomie je tedy hlavní rizikový faktor pro rozvoj píštěle močových cest v moderním světě (11). Celonárodní finská studie z roku 1998 zkoumala na vzorku více než 62 000 pacientek incidenci peroperačních poranění močového traktu v průběhu hysterektomie a jejich vliv na následné zformování vezikovaginální píštěle. Dospěla k závěru, že iatrogenní léze močového traktu je vzácnou, o to však závažnější komplikací s hlášenou incidencí poranění močového měchýře 1,3 na 1 000 hysterektomií. Průměrná incidence vzniku následné vezikovaginální píštěle byla 0,8 na 1 000 hysterektomií; riziko je vyšší po laparoskopické hysterektomii 2,2 na 1 000 a abdominální hysterektomii 1 na 1 000, na ‑ opak nejbezpečnější z hlediska formace píštěle je vaginálně vedená hysterektomie s frekvencí 0,2 na 1 000 výkonů (12).
Mezi predisponující faktory rozvoje píštělí dolních cest močových zahrnujeme intraoperační poranění měchýře zasahující do trigona či hrdla měchýře, peroperační krevní ztrátu přes 1 000 ml a/nebo hysterektomii prováděnou pro objemnou dělohu (13). Všechny ostatní stavy, které mohou vést ke změně obvyklých anatomických poměrů a horší intraoperační orientaci v malé pánvi, jsou rovněž spojovány s vyšším rizikem poranění močového měchýře a/nebo močovodů a predisponují tak ke vzniku píštěle. Mezi ně řadíme předchozí pánevní operační výkony včetně císařského řezu, radioterapii malé pánve, pánevní adheze, endometriózu, PID (pánevní zánětlivé onemocnění) v anamnéze apod. (14).
Možný mechanismus vzniku urogenitální píštěle po hysterektomii je velmi pestrý. Od fokální ischemie způsobené nešetrnou preparací a disekcí většinou zadní stěny močového měchýře, přes lokální termické poranění při neopatrné elektrokauterizaci působící koagulační nekrózu a rozpad tkáně v místě inzultu, po intraoperačně nerozpoznané přímé poranění s bezprostřední extravazací moči (15). Poranění stěny měchýře včetně postižení močovodu ligaturou či nevhodně umístěnou suturou z nevstřebatelného materiálu způsobí lokální zánětlivou reakci s vysokým rizikem následné formace píštěle. Ke vzniku píštěle může dojít i přes okamžitý pokus o reparaci defektu v první době. Symptomy se objevují často do deseti dnů od výkonu.
Radioterapie malé pánve indikovaná pro karcinom cervixu či jinou pánevní malignitu zastupuje další významnou příčinu rozvoje urogenitální píštěle. Ta může vzniknout buď bezprostředně po ozařování či dokonce v jeho průběhu jako přímý důsledek nekrózy a rozpadu tkáně tumoru, nicméně ani formace píštěle s několikaletým odstupem není vzácností (16). Vzniká jako následek dlouhodobých poruch mikrocirkulace a perfuze zapříčiněné změnami souvisejícími s endarteritis obliterans a rozvojem lokální ischemie.
Poranění měchýře a převážně močové trubice jsou rovněž známými komplikacemi anti‑inkontinenčních operací a chirurgických korekcí prolapsů pánevních orgánů, obzvláště při použití syntetických materiálů ve formě slingů či meshů (17).
KLASIFIKACE A DĚLENÍ UROGENITÁLNÍCH PÍŠTĚLÍ
Jak je z předchozích odstavců patrné, představují urogenitální píštěle velmi různorodou skupinu patologických stavů, které se mohou lišit svými anatomicko‑morfologickými charakteristikami a rysy, funkčními vlastnostmi, průvodními symptomy a v neposlední řadě také způsobem svého rozvoje a vzniku. Odpovídající organizace a kategorizace všech těchto aspektů nám umožňuje navrhnout ideální diagnostický a terapeutický plán a zároveň jimi adresovat individuální představy nemocné.
Základní klasifikace vychází z prostého anatomického popisu polohy píštěle s ohledem na postižené orgány (Obr. 1). Vezikovaginální píštěle jsou nejčastější a tvoří více než 50 % všech píštělí. Až ve 12 % případů se vyskytují současně s ureterovaginálními píštělemi, a proto vždy obligátně doplňujeme vyšetření horních močových cest. Vzhledem ke svému anatomickému průběhu (a vztahu k cervixu během hysterektomie) je poraněním více ohrožen levý močovod. Velmi vzácně jako následek císařského řezu, který je veden dolním segmentem dělohy, pozorujeme rozvoj vezikouterinní nebo vezikocervikální píštěle. Ty tvoří kolem 1–9 % všech píštělí (18). Uretrovaginální píštěle souvisí v 70 % případů s předchozím operačním řešením stresové inkontinence pomocí syntetického slingu (19).
Image 1. Ilustrace polohy urogenitálních píštělí na sagitálním řezu ženské pánve (odshora – vezikouterinní, vezikovaginální, uretrovaginální píštěl)
Fig. 1. Sagital view of female pelvis with highlighted fistula tracts (top to bottom – vesicouterine, vesicovaginal, urethrovaginal fistula)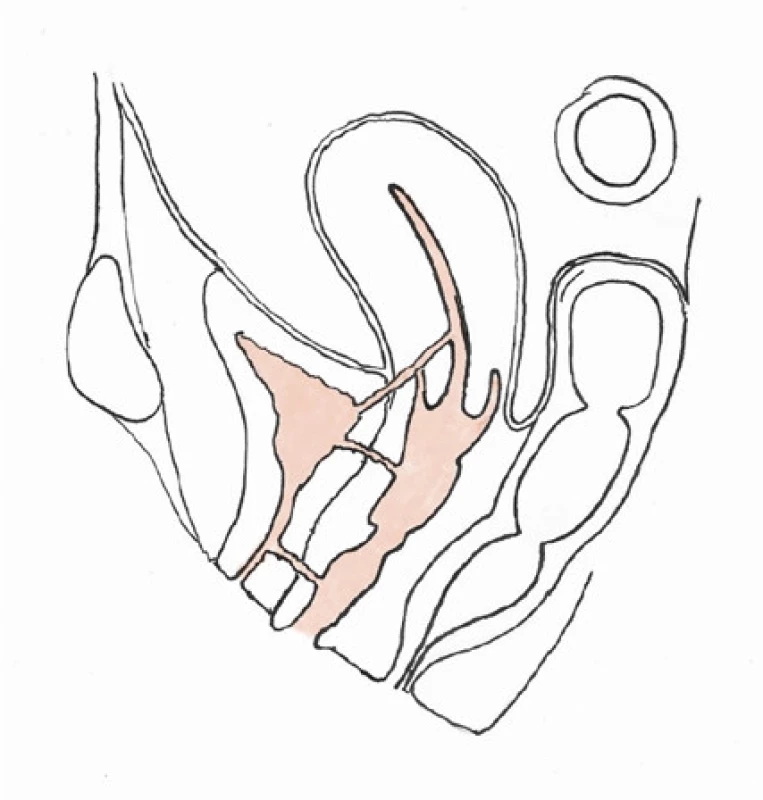
Anatomické dělení urogenitálních píštělí (tučně zvýrazněné nejčastější typy)
1. Vezikální (postihující močový měchýř):
a) veziko‑vaginální
b) veziko‑uterinní
c) veziko‑cervikální
2. Ureterální (postihující močovod):
a) uretero‑vaginální
b) uretero‑uterinní
3. Uretrální (postihující močovou trubici):
a) uretro‑vaginální
4. Komplexní (postihující kombinaci výše zmíněných)
Příčin vzniku píštělí močových cest může být mnoho a zahrnují jak velmi vzácné vrozené vady, tak podstatně častěji vznikají jako následek chorob a stavů získaných v průběhu života ženy. Dle očekávané nové ICS klasifikace rozlišujeme dvě velké skupiny píštělí definované podle skutečnosti, zda jejich rozvoj přímo souvisí s průběhem porodu či nikoliv.
Související s porodem
Porodnická píštěl – vzniká v důsledku protrahovaného porodu a s tím spojených komplikací
Iatrogenní píštěl související s porodem – vzniká v důsledku iatrogenního poranění během císařského řezu, extrakčních metod plodu či jiné instrumentace
Smíšená porodnická a iatrogenní píštěl – vzniká v důsledku císařského řezu vedeného pro nepostupující porod
Nesouvisející s porodem
Kongenitální píštěl – představuje vrozené píštěle v důsledku hypospadie, ektopického ureteru, či dalších vzácných vrozených vývojových vad
Iatrogenní píštěl nesouvisející s porodem – vzniká v důsledku pánevní operace, nejčastěji hysterektomie
Traumatická píštěl – vzniká v důsledku úrazu, kupříkladu fraktury pánve, bodných poranění perinea, sexuálního násilí, mutilací genitálu, inzercí cizích těles do pochvy
Inflamatorní/zánětlivá píštěl – vzniká v důsledku lokální zánětlivé reakce, typicky při endometrióze
Infekční píštěl – vzniká v důsledku lokální infekce či abscesu, příkladem je tuberkulóza či schistosomiáza
Maligní píštěl – vzniká v přímém důsledku rozpadu tumoru či jako následek jeho léčby
Snaha o exaktní morfologický popis píštělí s ohledem na jejich velikost, počet, vztah ke klíčovým strukturám močového měchýře a močové trubice, míru jizvení a další okolnosti vede ke snížení subjektivního vlivu pozorování. Tím umožňuje hodnotit dlouhodobé výsledky i rizika a jejich srovnání napříč institucemi.
Velmi simplifikovaná verze takové klasifikace vezikovaginálních a uretrovaginálních píštělí rozlišuje mezi jednoduchými a komplexními píštělemi. Mezi komplexní uretrovaginální píštěle řadíme píštěle vzniklé jako následek ozařování a/nebo postihující proximální uretru včetně hrdla močového měchýře. Komplexní vezikovaginální píštěle definuje buď předchozí radioterapie či malignita pánve, zkrácená délka pochvy, či velikost píštěle nad 3 cm postihující trigonum. Všechny ostatní případy, které nesplňují tato kritéria, označujeme jako jednoduché píštěle.
KLASIFIKACE DLE GOHOVÉ
V roce 2004 publikovala Judith Gohová nový komplexní klasifikační systém urogenitálních píštělí, ve kterém stanovila meatus uretry jako referenční bod, ke kterému vztahuje anatomicko‑patologický popis píštěle (20). Tím vznikla první standardizovaná a objektivní forma hlášení urogenitálních píštělí, která zůstává do dnešní doby nepřekonána. Základem této klasifikace je rozdělení urogenitálních píštělí do čtyř skupin podle vzdálenosti od zevního meatu uretry. Tyto typy jsou dále definovány velikostí píštěle, rozsahem a stupněm přidruženého jizvení, délkou pochvy a tzv. speciálními znaky (Tab. 1).
Table 1. Klasifikace urogenitálních píštělí dle Gohové
Tab. 1. Goh's classification of urogenital fistula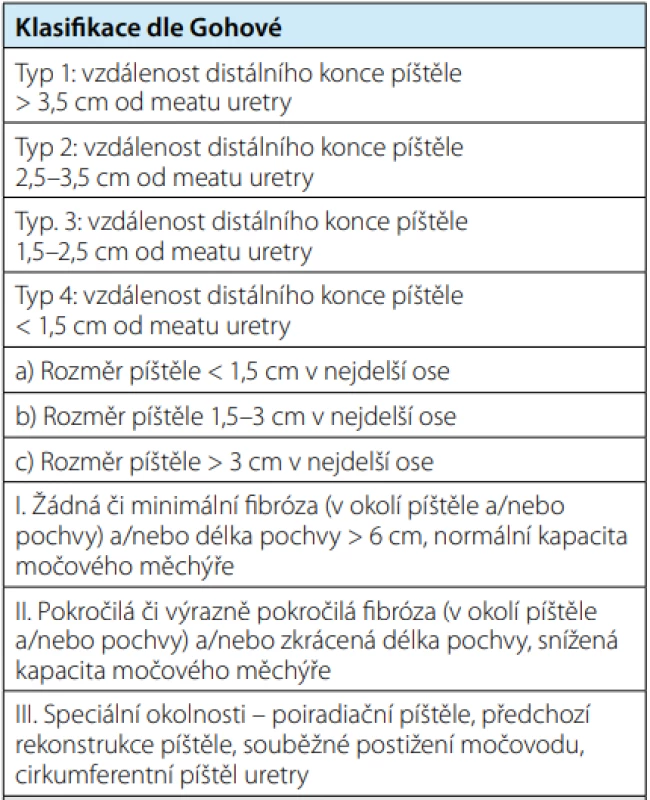
Jako příklad uveďme malou pooperační 5mm píštěl zadní stěny močového měchýře s minimálními známkami jizvení perivezikálních tkání a pochvy. Tu bychom klasifikovali jako vezikovaginální píštěl typu „1ai“. Naopak píštěl trigona a proximální uretry o průměru 35 mm, která vznikla jako následek ozařování pro karcinom cervixu, odpovídá typu „3ciii“, předpokládáme-li její polohu cca 2 cm od zevního meatu. VYŠETŘENÍ A DIAGNOSTIKA UROGENITÁLNÍCH PÍŠTĚLÍ
Základem úspěšné diagnostiky urogenitálních píštělí je vysoká prvotní míra suspekce ošetřujícího lékaře, která se opírá o bazální odběr anamnézy a provedení fyzikálního vyšetření u nemocné. Již tyto úvodní kroky mohou potvrdit lékařovu pracovní diagnózu. Velmi často je však nezbytné doplnit některá z paraklinických vyšetření k detailnějšímu pochopení anatomických a funkčních vlastností píštěle a obzvláště pak zároveň vyloučit možné poranění horních cest močových (Schéma 1). Diferenciální diagnóza urogenitálních fistulí je velmi bohatá a zahrnuje množství urologických a gynekologických patologických stavů, které je svými příznaky mohou blízce napodobovat (Tab. 2).
Table 2. Diferenciální diagnostika kontinuálních úniků moči
Tab. 2. Differential diagnosis of continuous urine leakage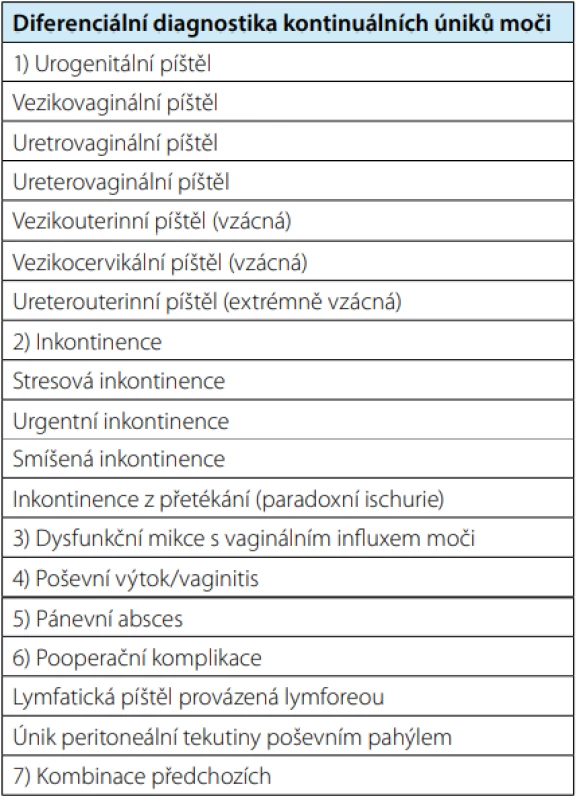
Schéma 1. Vyšetřovací algoritmus při suspekci na urogenitální píštěl (zjednodušeně)
Flowchart 1. Simplified algorithm of the diagnostic work-up for urogenital fistulae
ANAMNÉZA
Správně a detailně odebraná anamnéza představuje první klíč k úspěchu v managementu urogenitálních píštělí. Zvláštní důraz klademe vedle obligátní osobní anamnézy na informace související s předchozími operačními výkony. Podrobně posuzujeme charakter předchozích operací, u pánevních a břišních zákroků rutinně vyžadujeme kopie operačních protokolů, které mohou napovědět více o případném mechanismu poranění.
V rámci porodnické anamnézy dokumentujeme nejen počet těhotenství a porodů, ale i samotný průběh a způsob vedení jednotlivých porodů. Zajímáme se o možné porodní komplikace související s překotným či častěji nepostupujícím porodem v rámci jednotlivých dob porodních.
Informujeme se o případném gynekologickém stonání v předchorobí, jako jsou endometrióza, abnormální děložní krvácení a proběhlé gynekologické záněty, dotazujeme se na přítomnost intrauterinních tělísek či používání pesarů.
Podrobná onkologická anamnéza se soustředí na případné gynekologické, urologické či kolorektální malignity a s nimi související způsoby a metody léčby. Výsledek histologického rozboru, staging onemocnění a již zmíněný operační či ozařovací protokol jsou nedílnou součástí anamnézy pacientky.
SYMPTOMY
Nejběžnějším projevem urogenitální píštěle je únik moči. Klasicky se jedná o kontinuální celodenní nekontrolovatelný únik moči bez suchého intervalu a bez jasné vazby na konkrétní provokační manévry. Obzvláště přítomnost nočních úniků, kdy se žena ráno probudí promočena, je pro přítomnost urogenitálních píštělí zcela typická (21). Ženy nejsou zpravidla schopné přesně určit cestu, kterou k úniku moči dochází; jedná se však o velmi důležitý a varovný poznatek, projeví‑li žena obavu či podezření, že moč uniká pochvou (22). Malé či méně běžné typy píštělí se mohou projevovat i atypickými pozičními úniky vázanými na určité manévry (kupř. vertikalizace ze sedu, pohlavní styk či kašel), anebo jsou podmíněné konkrétní náplní močového měchýře a mají tak spíše intermitentní charakter. Cílenými dotazy na charakter, barvu, objem a zápach tekutiny se snažíme definovat typ tekutiny.
Makroskopická hematurie, jímací (urgence, frekvence, dysurie apod.) i evakuační (přerušovaný proud moči, iniciální hesitance, termi ‑ nální dribbling apod.) symptomy dolních cest močových a recidivující infekty močových cest jsou rovněž možnými méně častými symptomy a projevy urogenitálních píštělí. Relativně běžné jsou stesky související s lokálním únikem moči, jmenovitě na pronikavý zápach po moči, iritaci kůže hráze a kvasinkové infekce perinea a pochvy.
Raritní vezikouterinní píštěle se mohou projevovat amenoreou a cyklickou makroskopickou hematurií, tzv. menourií. Jako „Youssefův syndrom“ popisujeme kombinaci dvou výše zmíněných symptomů se spontánními aborty v prvním trimestru těhotenství a absencí inkontinence (23). Ureterovaginální píštěle se mohou projevovat velmi nespecificky, jako bolest pánve a břicha, nadýmání, porucha střevní pasáže, nauzea a teplota.
Časová souvislost mezi rozvojem prvních příznaků a potencionálním vyvolávajícím inzultem může vyšetřujícímu lékaři poskytnout velmi cenné informace o možném mechanismu poranění. Bezprostřední pooperační únik moči naznačuje nerozpoznané přímé poranění močových cest či selhání její okamžité intraoperační korekce. S latencí, typicky počátkem druhého pooperačního týdne, se projevují poranění močových cest způsobená ať již termickým vlivem elektrokoagulace či nepřímo ischemickými změnami způsobenými svorkami a podvazy. Souvislost vzniku píštěle v iradiačním terénu nemusí být zprvu patrná a může k ní dojít i s více než několikaletým zpožděním (24).
FYZIKÁLNÍ VYŠETŘENÍ
Důkladně provedené celkové fyzikální vyšetření představuje základní krok ve vyšetřovacím algoritmu pacientky s podezřením na urogenitální píštěl. Pečlivé vyšetření břicha včetně operačních jizev je nezbytností u žen, které recentně absolvovaly chirurgický či gynekologický zákrok a u nichž vznikla suspekce na přítomnost píštěle.
Vyšetření pánve zahajujeme aspekcí perinea, které může odhalit známky iritace kůže charak ‑ teru inkontinenční dermatitidy dané dlouhodobým kontaktem kyselé moči s kožním krytem hráze (25). Detailní vyšetření pochvy za použití spekula a adekvátního osvětlení může přímo prokázat patologickou komunikaci mezi močovým měchýřem, či močovou trubicí a pochvou (Obr. 2). Zatímco velké vezikovaginální a většina uretrovaginálních píštělí jsou většinou snadno hmatné a/nebo dokonce i patrné, malé či složitě přístupné píštěle jsou často při fyzikálním vyšetření velmi obtížně identifikovatelné. V takovém případě si při vaginálním vyšetření můžeme vypomoci souběžným tlakem na podbřišek, resp. plný močový měchýř pacientky či nemocnou požádáme o provedení valsalvova manévru. Ne vždy se však tímto postupem podaří potíže reprodukovat.
Image 2. Demonstrace uretrovaginální píštěle sondou zavedenou do meatu uretry; v pochvě dochází k hromadění moči – tzv. pooling (publikováno se svolením prof. Kasyana)
Fig. 2. Surgical probe introduced in the urethral meatus demonstrates clear urethrovaginal fistula; also notice vaginal pooling of urine (courtesy of prof. Kasyan)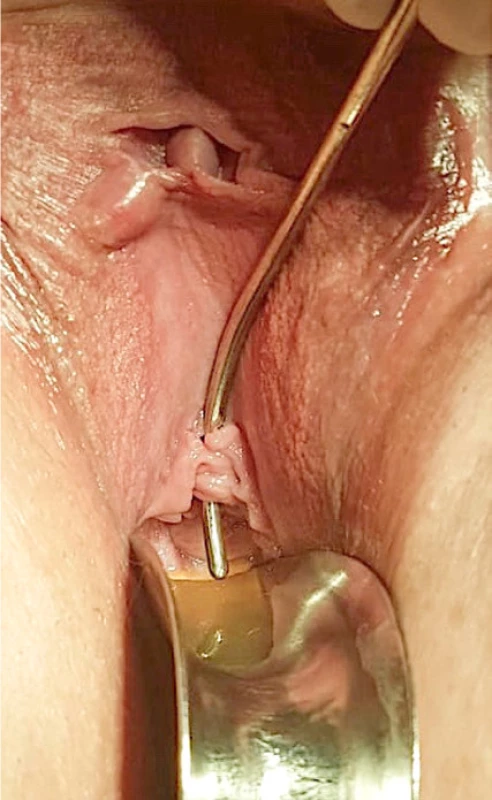
Nepřímým důkazem urogenitální píštěle bývá přítomnost hromadění tekutiny v pochvě, tzv. pooling. Vždy bychom se měli snažit o její odběr a odeslat vzorek k laboratorní analýze a stanovení hladiny urey a kreatininu, která určí původ tekutiny. Hodnoty mnohonásobně překračující hladinu sérového kreatininu jsou typické pro moč. Každé pánevní vyšetření by mělo být zakončeno bimanuální palpací. Při diskomfortu pacientky v průběhu vyšetření jej lze provést za celkové anestezie, v takovém případě často s doplněním cystoskopie či některého z pomocných kontrastních či barvivových testů (viz dále). U všech pacientek se známkami vaginální atrofie je doporučováno zahájit bez prodlení topickou hormonální terapii estrogenem, která i vzhledem k potencionálnímu operačnímu řešení usnadní manipulaci s tkáněmi a následné hojení.
TESTY S BARVIVY
Testy využívající lokální či celkové podání barviv se pro své jednoduché provedení, snadnou interpretaci a bezprostřední výsledky těší v diagnostice urogenitálních píštělí značné oblibě. Nicméně i přes tuto skutečnost není autorům známa studie s dostatečně velkým počtem pacientek, která by hodnotila specificitu a senzitivitu těchto vyšetření. Absolutní 100% senzitivitu na vzorku 12 pacientek publikoval v roce 2000 německý kolektiv autorů po podání methylenové modři do močového měchýře (26).
Provedení testu je zahájeno katetrizací a vyprázdněním močového měchýře s následnou pomalou instilací ředěné methylenové modři či indigokarmínu ve fyziologickém roztoku do objemu 300ml. Současně prováděné vaginální vyšetření často snadno prokáže přítomnost píštěle. Pokud se píštěl takto identifikovat nepodaří, lze test modifikovat tamponádou pochvy třemi zdravotnickými tampony či sterilními čtverci, případně obyčejným dámským menstruačním tamponem a pacientku vyzveme k chůzi a fyzické aktivitě. Neexistuje jasně definovaný postup testu, který se tak může lišit dle zvyklostí konkrétního pracoviště; proto někdy pro usnadnění můžeme využít standardizovaný protokol hodinového vložkového testu2 . Přítomnost zbarvení tamponu hodnotíme jako pozitivní výsledek testu; zatímco zabarvení apikálního tamponu nasvědčuje přítomnosti vezikovaginální píštěle, prostřední či distální je sugestivní pro uretrovaginální píštěl či stresovou inkontinenci (27). Nezbarvený avšak vlhký tampon by nás vždy měl přinutit pomyslet na možnou ureterovaginální píštěl (Obr. 3). V takovém případě přistupujeme k tzv. modifikovanému dvojitému barvivovému testu, kdy současně podáme per os pacientce 200mg phenazopyridinu (pyridium). Vyprázdníme obsah močového měchýře, a jakmile pozorujeme oranžově zbarvenou moč, celý výše zmíněný postup s instilací modři do močového měchýře a vaginální tamponádou zopakujeme. Pacientku opět vyzveme k fyzické činnosti. Oranžové zbarvení tamponu prokazuje ureterovaginální píštěl, modré vezikovaginální či uretrovaginální píštěl. Jejich kombinace prokazuje přítomnost vícečetné či komplexní píštěle (Schéma 2). Nejen v takovém případě je naprosto zásadní vyšetřit podrobněji horní močové cesty, nejčastěji za pomoci kontrastního CT urotraktu se speciálním akcentem na pozdní vylučovací fázi.
Image 3. Schématické znázornění testu s barvivy. Na horním obrázku je zřejmé modré zbarvení apikálního tamponu při vezikovaginální píštěli. Uprostřed oranžové zbarvení tamponu u pacientky s ureterovaginální píštělí po systémovém podání phenazopyridinu. Spodní obrázek demonstruje modré zabarvení distálního tamponu při stresové inkontinenci či uretrovaginální píštěli
Fig. 3. 3 swab test with dye. Top picture demonstrates blue staining of the proximal swab through the vesicovaginal fistula. Middle picture depicts orange staining of the proximal swab via the ureterovaginal fistula. Bottom picture shows staining of the distal swab in a patient with stress incontinence or urethrovaginal fistula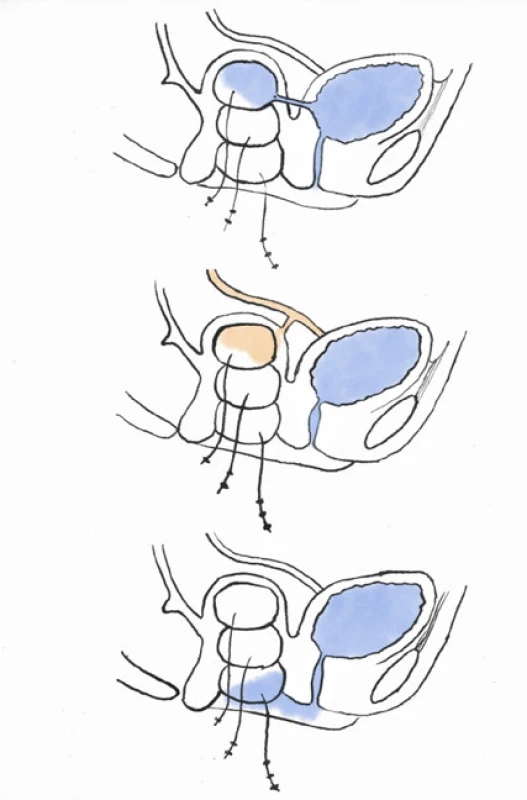
Schéma 2. Provedení a interpretace barvivového testu
Flowchart 2. How to perform and interpret dye tests
<hr>
2 Chůze po rovině, do a ze schodů (30 min.), vertikalizace ze sedu (10×), silný kašel (10×), běh na místě (1 min.), zvednutí drobného předmětu ze země (5×) a mytí rukou pod tekoucí vodou (1 min.).
<hr>
ZOBRAZOVACÍ VYŠETŘOVACÍ METODY
V současné době neexistuje jednotný konsensus stran výběru optimální zobrazovací modality v rámci diagnostiky urogenitálních píštělí. Její volba je z velké míry odvislá od geopolitických a ekonomických charakteristik konkrétního státu a organizace tamnější zdravotní péče. Při nízké dostupnosti sofistikovaných zobrazovacích metod, jako jsou počítačová tomografie či magnetická rezonance, ve venkovských oblastech některých rozvojových zemí je většinou upřednostňována některá z mini‑invazivních skiaskopických kontrastních metod.
Retrográdní cystografie v kombinaci s mikční uretrocystografií představuje pro svou relativní technickou, časovou i finanční nenáročnost často první zobrazovací vyšetření dolních cest močových u pacientek s podezřením na píštěl. Extravazace kontrastní látky z močového měchýře je vysoce specifická pro diagnózu vezikovaginální, vezikouterinní či vezikocervikální píštěle (Obr. 4 a, b). Bohužel ne vždy se touto metodou daří adekvátní a plnohodnotné zobrazení celého průběhu krátké ženské uretry a tak i případné uretrovaginální píštěle. V takové situaci je nutné, aby bylo pracoviště vybaveno jedním ze speciálních typů dvoubalonkových katétrů navržených ke kontrastnímu zobrazení ženské uretry. Trattnerův katétr disponuje dvěma obturačními balonky, menší distální o kapacitě 5 ml je uložen v hrdle močového měchýře, zatímco větší proximální s kapacitou až 20 ml utěsňuje meatus uretry. Katétr má pouze jeden boční otvor mezi oběma balonky, který využíváme k instilaci kontrastní látky a zobrazení uretry. Druhý podobný typ katétru, tzv. Davisův katétr má identický design s tou výjimkou, že jeho meatální balonek lze volně posouvat, a tím tak jeho polohu uzpůsobit délce uretry.
Image 4. a, b. Předozadní a laterální projekce cystografie prokazuje únik kontrastní látky do pochvy (šipky)
Fig. 4 a, b. Anteroposterior and lateral view of the urinary bladder during cystography demonstrates urine leak and vesicovaginal fistula (arrows)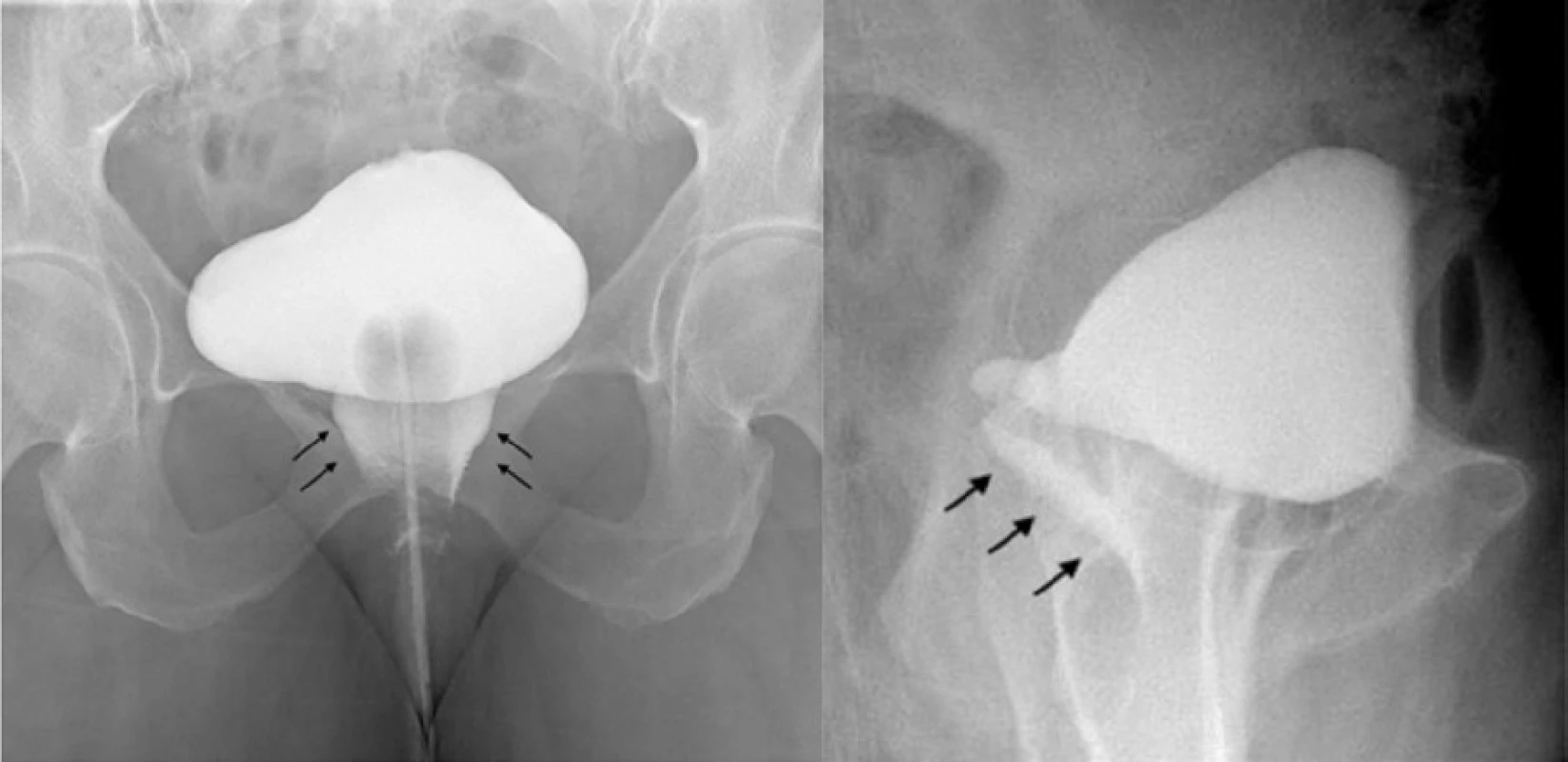
Sofistikovanou alternativou rutinní cystografie je provedení CT cystogramu, který poskytne dokonalý přehled o stavu dolních cest močových a vztahu případné urogenitální píštěle s ostatními strukturami. Nicméně až 12 % všech vezikovaginálních píštělí se může vyskytovat současně s píštělemi ureterovaginálními a tyto mohou být při těchto vyšetřeních snadno opomenuty, což může vést k mylným úvahám v rámci předoperačního plánování a následně tak ke katastrofálním pooperačním komplikacím (28). Z toho důvodu je vždy nutné u suspekcí na urogenitální píštěl zároveň vyšetřit i horní močové cesty a v takovém případě provést vícefázové kontrastní CT ledvin a jasně specifikovat požadavek na doplnění vylučovací fáze snímkování. V zemích, kde CT vyšetření není běžně dostupné, jej lze nahradit provedením intravenózní vylučovací urografie. U pacientek, u kterých trvá důvodné podezření na možné postižení ureterů, které se nepodaří prokázat jedním ze zmíněných vyšetření, lze doplnit rozšířené vyšetření horních močových cest během cystoskopie, tak jak je uvedeno v příslušné kapitole tohoto článku.
Ultrasonografie močových cest nenachází v diagnostice urogenitálních fistulí rutinní uplatnění, ač existují data o vysoké senzitivitě transvaginálního provedení s dopplerovským zobrazením při diagnostice vezikovaginálních fistulí (26).
MRI bychom jako doplňující zobrazovací modalitu měli zvažovat u pacientek s anamnézou pánevní malignity a podezřením na urogenitální píštěl. Magnetická rezonance dokáže velmi citlivě identifikovat případnou rekurenci zhoubného onemocnění a ve svých T2-vážených obrazech se případná píštěl zobrazí jako patologická tekutinová komunikace o vysoké intenzitě (29, 30) (Obr. 5).
Image 5. MRI pánve v sagitální projekci přehledně prokazuje přítomnost vezikovaginální píštěle a moči v pochvě (šipky)
Fig. 5. Sagittal view of pelvic MRI demonstrating vesicovaginal fistula and the presence of urine in the vagina (arrows)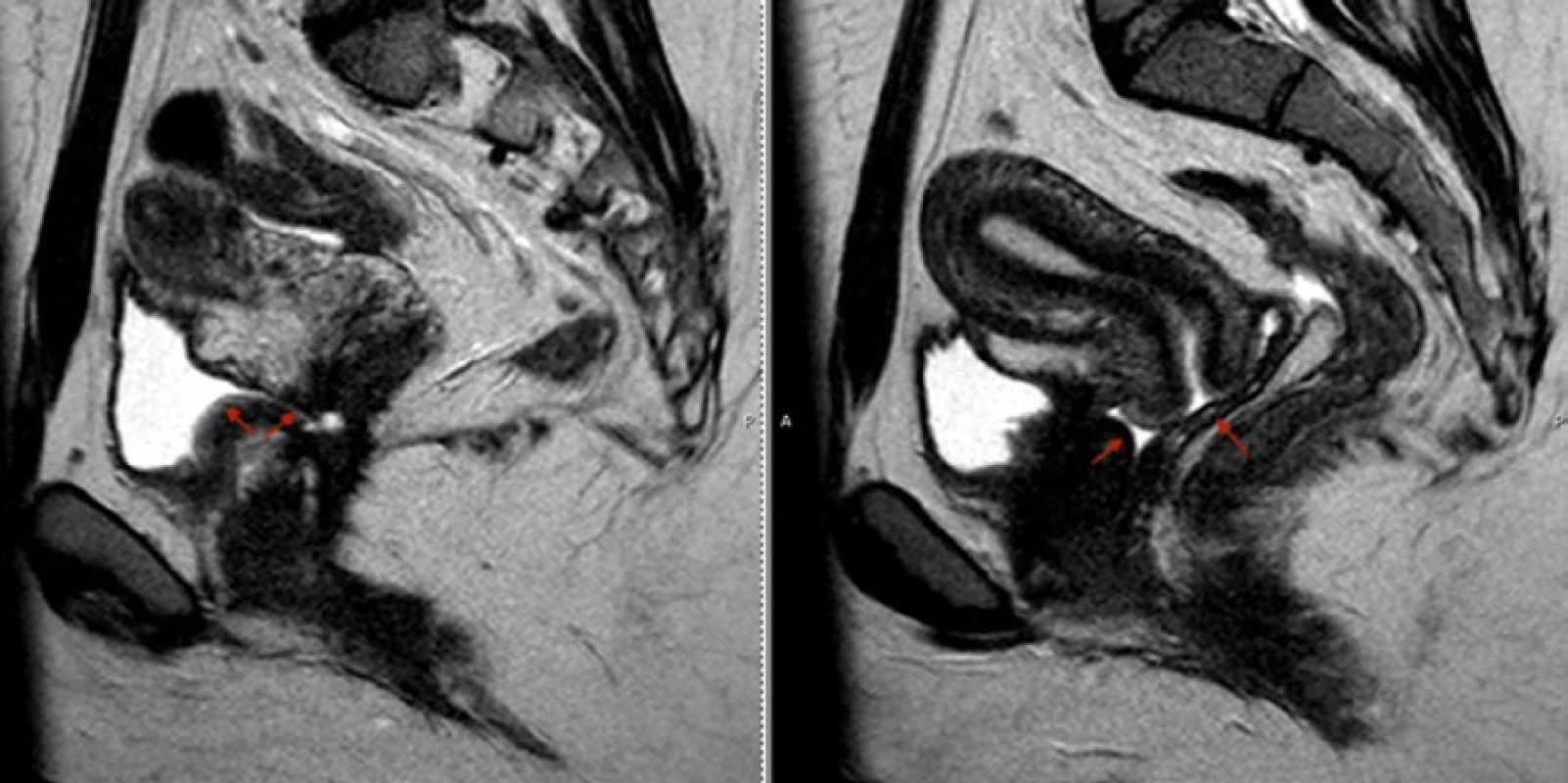
U pacientek s vysokým indexem podezření na vzácnou vezikouterinní píštěl, u kterých CT nepotvrdilo její přítomnost, lze doplnit hysterogram (31).
ENDOSKOPICKÁ VYŠETŘENÍ
Cystoskopie představuje jeden ze základních nástrojů diagnostiky a měla by být provedena u všech pacientek s podezřením na urogenitální píštěl. Na základě dat ze dvou malých skupin pacientek lze cystoskopii považovat za velmi senzitivní test, kterým se podaří prokázat 92–93 % vezikovaginálních a uretrovaginálních fistulí (32). Zralé píštěle lze většinou snadno identifikovat pro své hladké epitelizované okraje a nálevkovitý tvar (Obr. 6 a). Výrazně obtížněji se lokalizuje poloha a průběh čerstvých píštělí, které se nacházejí často v nepřehledném edematózním terénu a většinou bývá úspěšná až sondáž suspektních erytematózních, bulózních či granulomatózních okrsků sliznice za pomocí vodícího drátu či 5Fr ureterálního katétru (Obr. 6b). V případech, kde nemůžeme vyloučit postižení horních močových cest, lze cystoskopii doplnit o současnou ureteroskopii s retrográdní ureteropyelografií. Pochopitelně toto vyšetření pro již významný diskomfort provádíme za svodné či celkové anestezie pacientky. Užitečné je provést souběžně vaginální vyšetření či vaginoskopii, obzvláště v případech, kdy nejsme schopni adekvátně vizualizovat vrchol pochvy a přesvědčivě identifikovat vaginální ústí traktu píštěle (33). Již výše zmíněná sondáž píštěle nám výrazně usnadní určení její polohy. U pacientek s anamnézou gynekologické malignity či radioterapie pánevní oblasti je naprosto zásadní před případným operačním řešením provést dostatečnou a reprezentativní biopsii píštěle k vyloučení lokální rekurence či sekundární malignity.
Image 6. a, b. a) Typický nálevkovitý vzhled píštěle během cystoskopie (černá šipka), stent zavedený do levého ureteru (červená šipka); b) sondáž píštěle ureterálním katétrem usnadňuje manipulaci a orientaci v průběhu výkonu (černá šipka), stent zavedený do levého ureteru (červená šipka)
Fig. 6 a, b. a) Typical funnel-shaped appearance of the fistula during cystoscopy (black arrow), stent inserted in the left ureteric orifice (right arrow); b) ureteral catheter inserted in the fistula to aid manipulation and navigation during surgery (black arrow), stent inserted in the left ureteric orifice (right arrow)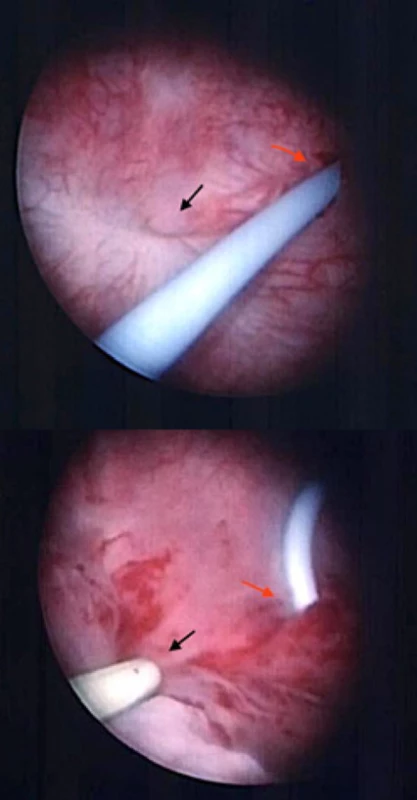
URODYNAMICKÉ VYŠETŘENÍ
Urodynamika obecně nepatří do rutinního diagnostického repertoáru urogenitálních píštělí žen, nicméně u pacientek, které trpí konkomitantními obtěžujícími symptomy dolních cest močových, může poskytnout obzvláště při svém provedení ve formě videourodynamiky vedle funkčních poznatků i cenné informace o morfologii dolních cest močových. Z naší zkušenosti se 5–10 % všech urogenitálních píštělí podaří diagnostikovat právě jako vedlejší nález videourodynamického vyšetření indikovaného původně pro symptomy stresové či urgentní inkontinence. Při svém správném provedení dokáže videourodynamika spolehlivě identifikovat příčinu úniku moči; rozliší stresový, urgentní či smíšený typ inkontinence od méně častých příčin úniků moči, jako je dysfunkční mikce provázená vaginálním influxem moči, divertikl uretry a právě urogenitální píštěl.
Vstupní videourodynamika zhodnotí výchozí funkční vlastnosti močového měchýře a sfinkterového aparátu a může významně ovlivnit a usnadnit předoperační plánování.
Běžným urodynamickým nálezem tak může být u pacientek se souběžnými jímacími symptomy hyperaktivita detruzoru či vzácněji u pacientek po předchozí radioterapii porucha compliance doprovázená sníženou kapacitou močového měchýře (34). Znalost těchto abnormalit může usnadnit rozhodování o jednodobé augmentační cystoplastice či aplikaci botulinumtoxinu do stěny močového měchýře během rekonstrukce píštěle. Méně často se můžeme setkat u těchto pacientek zároveň s dominantní evakuační a postevakuační symptomatologií způsobenou subvezikální obstrukcí, hypoaktivitou detruzoru či jejich kombinací. Management těchto poruch je diametrálně odlišný a nepochybně opravňuje standardní předoperační provedení (video)urodynamického vyšetření. Urodynamická diagnostika subvezikální obstrukce a hypoaktivity detruzoru u žen se do roku 2017 opírala převážně o klinický úsudek vyšetřujícího lékaře. Toto dilema zčásti vyřešila publikace nově vyvinutého nomogramu podle Solomon‑Greenwellové (35), který stratifikuje pacientky podle pravděpodobnosti obstrukce dolních cest močových.
Až 15 % pacientek se známou urogenitální fistulí trpí současně příznaky stresové inkontinence urodynamicky charakterizované hypermobilitou uretry, intrinsickou insuficiencí svěrače či jejich kombinací. Znalost těchto poruch v předoperačním období může vést po adekvátní konzultaci s pacientkou k rozhodnutí o jejich souběžném operačním řešení.
Samotné provedení vyšetření může být technicky značně komplikované, obzvláště u žen s klinicky významnou píštělí, neboť s instilací tekutiny při cystometrii dochází k jejímu průběžnému úniku z močového měchýře, nejčastěji do pochvy. Jednou z variant, jak tomuto zabránit, je pečlivá tamponáda pochvy sterilními čtverci či longetou. Druhým možným krokem je úprava polohy pacientky během plnící fáze z polohy vsedě či vestoje do polohy na zádech. Pokud i tato opatření selhávají, lze se pokusit se souhlasem pacientky o šetrnou sondáž píštěle Foley katétrem (kalibru 8 Ch) a její dočasné utěsnění nafouknutým balonkem katétru při jeho mírné trakci. Únik instilační kapaliny může arteficiálně zvýšit maximální cystometrickou kapacitu měchýře, s čímž je nutno při interpretaci urodynamických záznamů kalkulovat.
ZÁVĚR
Urogenitální píštěle představují v našich podmínkách relativně vzácnou příčinu úniku moči žen. Základem úspěchu je v první řadě pomyslet v rámci širší diferenciálně diagnostické rozvahy na její možnou přítomnost; obzvláště u pacientek s anamnézou nedávné hysterektomie či radioterapie malé pánve. Mezi charakteristické příznaky patří stížnost na nově vzniklý nekontrolovatelný únik moči (nejen) během spánku a pocit konstantního vlhka. Pečlivě provedené fyzikální vyšetření, které lze doplnit o některou z variant barvivého testu, nezřídka prokáže přítomnost píštěle. Kontrastní rentgenová vyšetření včetně cystouretrografie a CT močových cest však představují pro svou vysokou senzitivitu a specificitu stále zlatý standard mezi dostupnými zobrazovacími metodami. Cystoskopie s biopsií suspektních lézí je obligátní u pacientek s anamnézou pánevní malignity či ozařování.
Hlavní stanovisko: Autoři se v následujícím článku podrobně věnují problematice urogenitálních píštělí se speciálním zaměřením na jejich rozdílnou etiologii v rozvojových a vyspělých státech světa. Diskutována je rovněž incidence, bohatá symptomatologie, klasifikace píštělí a úloha dostupných vyšetření v rámci jejich diagnostiky.
Major statement: The authors present their overview of the wide topic of urogenital fistulae with special regard to the diverse etiology in the developed and developing countries. The incidence, symptoms, classification and various diagnostic modalities are also discussed in great detail.
Střet zájmů: Žádný.
Prohlášení o podpoře: Nezávislý článek
Došlo: 21. 7. 2020
Přijato: 15. 9. 2020
Kontaktní adresa:
MUDr. Antonín Prouza
Bristol Urological Institute Southmead Hospital,
Bristol, BS10 5NB, UK
Sources
1. Hilton P. Urogenital fistula in the UK: a personal case series managed over 25 years. Br J Urol Int 2011; 110(1): 102–110.
2. Hilton P, Ward A. Epidemiological and surgical aspects of urogenital fistulae: a review of 25 years‘ experience in southeast Nigeria. Int Urogynecol J Pelvic Floor Dysfunct 1998; 9(4): 189–194.
3. Petrie E. Urologic trauma in gynaecological surgery: diagnosis and management. Curr. Op Obstet Gynecol 1999; 11 : 495–498.
4. Aronson MP, Bose TM. Urinary Tract Injury in Pelvic Surgery, Clinical Obstetrics and Gynecology. June 2002; 45(2): 428–438. 5. Wall LL. Obstetric vesicovaginal fistula as an international public – health problem. Lancet 2006; 368(9542): 1201–1209.
6. Holme A, Breen M, MacArthur C. Obstetric fistulae: a study of women managed at the Monze Mission Hospital, Zambia. BJOG: An International Journal of Obstetrics & Gynaecology 2007; 114 : 1010–1017.
7. Wall LL, Karshima JA, Kirschner C, Arrowsmith SD. The obstetric vesicovaginal fistula: characteristics of 899 patients from Jos, Nigeria. Am J Obstet Gynecol 2004; 190(4): 1011–1019.
8. Browning A, Lewis A, Whiteside S. Predicting women at risk for developing obstetric fistula: a fistula index? An observational study comparison of two cohorts. BJOG 2014; 121(5): 604–609.
9. Kelly J, Kwast BE. Epidemiologic study of vesicovaginal fistulas in ethiopia. Int Urogynecol J 1993; (4): 278–281.
10. Symmonds RE. Incontinence: vesical and urethral fistulas. Clin Obstet Gynecol 1984; 27(2): 499–514.
11. Marks P, Kluth LA, Lang IJ, Fisch M. Vesikovaginale Fisteln: Diagnostik und operatives Management. Der Urologe 2020; 59 : 432–441.
12. Härkki‑Sirén P, Sjöberg J, Tiitinen A. Urinary tract injuries after hysterectomy. Obstet Gynecol 1998; 92(1): 113–118.
13. Duong TH, Gellasch TL, Adam RA. Risk factors for the development of vesicovaginal fistula after incidental cystotomy at the time of a benign hysterectomy. Am J Obstet Gynecol 2009; 201(5): 512.e1–512.e5124.
14. Walters MD, Karram MM. Lower urinary tract fistulas. In MM Karram, American Urological Association, Education and Research Inc. Linthicum MD; ed 2007 : 445–460.
15. Khamzin A, Pacík D. Píštěle mezi uropoetickým a genitálním systémem ženy z pohledu urologa. Praktická gynekologie 2004; 6 : 36–40.
16. Rajaian S, Pragatheeswarane M, Panda A. Vesicovaginal fistula: Review and recent trends. Indian J Urol 2019; 35 : 250–258.
17. Pushkar DY, Dyakov VV, Kosko JW, Kasyan GR. Management of urethrovaginal fistulas. Eur Urol 2006; 50(5): 1000–1005.
18. Porcaro AB, Zicari M, Zecchini Antoniolli S, et al. Vesicouterine fistulas following cesarean section: report on a case, review and update of the literature. Int Urol Nephrol 2002; 34(3): 335–344.
19. Nitti VW, Rosenblum N, Brucker BM. Vaginal Surgery for the Urologist. Female Pelvic Surgery Video Atlas Series Elsevier 2012; 167–182.
20. Goh JT. A new classification for female genital tract fistula. Aust N Z J Obstet Gynaecol 2004; 44(6): 502–504.
21. Záleský M, Zachoval R, Vik V, et al. Urologické konsekvence gynekologických operací. Urol List 2008; 6(1): 78–84.
22. Hillary CJ, Osman NI, Hilton P, Chapple CR. The Aetiology, Treatment, and Outcome of Urogenital Fistulae Managed in Well - and Low‑resourced Countries: A Systematic Review European Urology 2016; 70(3): 478–492.
23. Bhattacharjee S, Kohli UA, Sood A, Tripathy S, Gupta M. Vesicouterine fistula: Youssef’s syndrome. Med J Armed Forces India 2015; 71(Suppl 1): S175–S177.
24. Moore KN, Gold MA, McMeekin DS, Zorn KK. Vesicovaginal fistula formation in patients with Stage IVA cervical carcinoma. Gynecol Oncol 2007; 106(3): 498–501.
25. Gray M, Beeckman D, Bliss DZ, et al. Incontinence‑associated dermatitis: a comprehensive review and update. J Wound Ostomy Continence Nurs 2012; 39(1): 61–74.
26. Volkmer BG, Kuefer R, Nesslauer T, Loeffler M, Gottfried HW. Colour Doppler ultrasound in vesico ‑ vaginal fistulas. Ultrasound Med Biol 2000; 26(5): 771–775.
27. Margolis T, Mercer LJ. Vesicovaginal fistula. Obstet Gynecol Surv 1994; 49(12): 840–847.
28. Kumar A, Goyal NK, Das SK, et al. Our experience with genitourinary fistulae. Urol Int 2009; 82(4): 404–410.
29. Tonolini M. Elucidating vaginal fistulas on CT and MRI. Insights Imaging 2019; 10(1): 123.
30. Yu NC, Raman SS, Patel M, Barbaric Z. Fistulas of the genitourinary tract: a radiologic review. Radiographics 2004; 24(5): 1331–1352.
31. Tancer ML. Vesicouterine fistula – a review. Obstet Gynecol Surv 1986; 41(12): 743–753.
32. Hanif MS, Saeed K, Sheikh MA. Surgical management of genitourinary fistula. J Pak Med Assoc 2005; 55(7): 280–284.
33. Andreoni C, Bruschini H, Truzzi JC, Simonetti R, Srougi M. Combined vaginoscopy‑cystoscopy: a novel simultaneous approach improving vesicovaginal fistula evaluation. J Urol 2003; 170(6 Pt 1): 2330–2332.
34. Hilton P. Urodynamic findings in patients with urogenital fistulae. Br J Urol 1998; 81(4): 539–542.
35. Solomon E, Yasmin H, Duffy M, et al. Developing and validating a new nomogram for diagnosing bladder outlet obstruction in women. Neurourol Urodyn 2018; 37(1): 368–378.
Labels
Paediatric urologist Nephrology Urology
Article was published inCzech Urology
2020 Issue 4-
All articles in this issue
- Editorial
- Pravostranná robotická reimplantace močovodu s Boariho lalokovou plastikou
- Možnosti využití ligandů prostatického specifického membránového antigenu (PSMA) v diagnostice a léčbě karcinomu prostaty
- Úvod do problematiky urogenitálních píštělí: incidence, etiologie, klasifikace, symptomatologie a diagnostika
- Výskyt a výsledky operačního řešení lokálních recidiv zhoubných nádorů ledvin
- Atypická hladkosvalová neoplazie prostaty nejistého maligního potenciálu – leiomyom/leiomyosarkom prostaty
- Raritní případ gigantických kondylomat (Buschke-Löwenstein) v urologické prax
- Postradiační hemoragická cystitida – terapeutické možnosti se zaměřením na hyperbarickou oxygenoterapii
- Fraktura penisu – diagnostika a léčba
- Komentář k práci Schraml J, Broul M, Hlavička M, Bočan M. Šetření hrdla močového měchýře při RARP
- Vzpomínka na doc. MUDr. et MgA. Ivana Kawaciuka, CSc.
- Ohlédnutí za 66. výroční konferencí České urologickém společnosti
- Zpráva o proběhlé akci 8. český video‑seminář, Tipy a triky v urologické operativě 2020
- Výsledky soutěže ČUS o nejlepší vědeckou publikaci za rok 2019
- Czech Urology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Fraktura penisu – diagnostika a léčba
- Úvod do problematiky urogenitálních píštělí: incidence, etiologie, klasifikace, symptomatologie a diagnostika
- Postradiační hemoragická cystitida – terapeutické možnosti se zaměřením na hyperbarickou oxygenoterapii
- Pravostranná robotická reimplantace močovodu s Boariho lalokovou plastikou
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

