-
Medical journals
- Career
Hranice možností záchovného výkonu u tumorů ledviny – desetinásobná resekce solitární ledviny
Authors: Petr Macek 1,2; Libor Zámečník 2; Tomáš Hanuš 2
Authors‘ workplace: Department of Urology, Institut Montsouris, Université Paris Descartes, Paris, France 1; Urologická klinika 1. LF UK a VFN v Praze 2
Published in: Ces Urol 2019; 23(3): 243-249
Category: Case report
Overview
Výskyt vícečetných nádorů ledvin je málo častý, ale nemusí vždy automaticky znamenat odstranění celé ledviny. Prezentujeme případ 60letého muže se solitární ledvinou vpravo (vlevo po nefrektomii pro nádor), u nějž bylo na CT zjištěno celkem deset oblastí (některé ale obsahovaly více ložisek) se solidním ložiskem ledviny. Po rozsáhlé diskuzi o dostupných možnostech a následně rizicích chirurgického řešení byla provedena otevřená 10násobná resekce ledviny. Největší tumor resekován na počátku v 17 min. studené ischemie a ostatní následně bez ischemie. Výkon trval 250 minut, bez perioperačních komplikací. V pooperačním období se neobjevily žádné chirurgické komplikace. Došlo ale k významnému zhoršení funkce ledviny, která si vyžádala nefrologickou farmakologickou intervenci pro hyperkalemii a metabolickou acidózu, dialýza však nebyla potřebná. Histologicky zjištěno 13 ložisek světlobuněčného karcinomu ledviny G3 velikosti od 5 do 35 mm. Kontrolní CT jeden rok od operace prokázalo jedno nejisté ložisko, které bude sledováno. Funkce ledviny je stabilní s kreatininemií do 200 μmol/l.
Klíčová slova:
Mnohočetný nádor ledviny – vícenásobná resekce ledviny – individuální řešení
ÚVOD
V incidenci maligních tumorů ledvin patří České republice nelichotivé světové prvenství (1). V průběhu posledních let incidence na 100 000 obyvatel stále pomalu narůstá, přičemž v roce 2016 dosáhla 30,31 případů (2). S přibývajícím množstvím různých zobrazovacích vyšetření se proporcionálně zvýšilo množství pacientů s nádory klinické kategorie T1 (2). Oboustranné nádory jsou možné, byť nejsou příliš časté (1–2 %) (3, 4). Vícečetné postižení je udáváno v rozmezí od 4 do 25 % (5). Základem léčby solidních nádorů ledvin je chirurgické odstranění orgánu (nefrektomie) nebo záchovný výkon s odstraněním nádoru (resekce ledviny). V závislosti na celé řadě faktorů, jako jsou například celkový stav a komorbidity pacienta, renální funkce či přání pacienta apod., je možné v řadě případů využít i nechirurgických metod s tepelnou ablací nebo sledování vývoje ložiska zobrazovacími metodami (6). Při výskytu mnohočetného nádorového postižení ledviny (tj. dvě a více ložisek) je nutné vždy hodnotit a řešit situaci individuálně.
KAZUISTIKA
Prezentujeme případ 60letého muže, který se dostavil na pravidelnou kontrolu pět let po radikální nefrektomii vlevo. Provedené CT vyšetření odhalilo vícečetnou recidivu v pravé solitární ledvině. Primární hodnocení radiologa popsalo čtyři ložiska velikosti – nejmenší 11 mm a největší 39 mm. Revize snímkové dokumentace nicméně odhalila celkem deset oblastí s jistou nebo pravděpodobnou solidní sytící se lézí. Zajímavostí také je, že s ohledem na velikost 39 mm u největšího z nádorů byla podrobena revizi také snímková dokumentace z doby 12 měsíců předcházejících poslednímu vyšetření (tj. čtyři roky od radikální nefrektomie vlevo), protože vývoj byl vcelku netypický. Původní popis (datovaný 12 měsíců zpět) konstatoval absenci recidivy lokální i vzdálené, přesto revize těchto snímků potvrdila přítomnost nejméně tří jistých solidních ložisek, přičemž největší mělo v dané době 27 mm, tj. v průběhu roku došlo k nárůstu o 12 mm.
V době nálezu byl muž aktivním kuřákem 20 cigaret denně (po dobu 30 let), bez trvalé medikace, performance status 0, aktivně pracující, BMI 27,7 (váha 100 kg při výšce 190 cm). V anamnéze měl provedenou laparoskopickou radikální nefrektomii vpravo pro tumor ledviny před pěti lety. Histologicky se jednalo o světlobuněčný karcinom o velikosti 50 mm, grade 3 s přítomnou vaskulární i lymfatickou invazí, negativní resekčním okrajem a absencí uzlinových či vzdálených metastáz dle zobrazovacích vyšetření (= pT1b G3 V1 L1 R0 N0 M0). Interní vyšetření nicméně diagnostikovalo hypertenzi a byla zahájena její léčba. Laboratorní vyšetření neodhalilo odchylky v krevním obraze, jaterních funkcích a koagulačních parametrech, pouze hladina kreatininu byla iniciálně 122 μmol/l a před vlastní operací pak na hodnotě 102. Stagingové CT vyšetření břicha a hrudníku neodhalilo, mimo ložisek solitární pravé ledviny, žádnou vzdálenou recidivu.
Situace s přítomností deseti postižených oblastí pravé solitární ledviny (tři oblasti obsahovaly dvě ložiska vedle sebe, velikosti od 5 do 39 mm) vedla k diskuzi o možnostech řešení. Největší ložisko bylo uloženo mediálně při hilu v kontaktu s kaudálními segmentálními cévami, RENAL skóre 9ah. Všechna ostatní ložiska o velikosti 5 až 20 mm měla skóre nižší (v rozsahu od 4 do 6) a byla uložena v korové části parenchymu jak ventrálně, tak dorzálně, a rozmístěna po celé ledvině (obrázky 1–10). Jako primární se nabízela možnost radikální nefrektomie, která by situaci nepochybně řešila efektivně, ale s nutností okamžitého zahájení dialýzy. Diskutovány byly proto i jiné možnosti, které by umožnily pacientovi vyhnout se značnému zhoršení kvality života. Vzhledem k příznivému uložení naprosté většiny ložisek vznikla shoda na operačním řešení se záměrem provedení mnohočetné resekce solitární ledviny. Pacient byl srozuměn s možností okamžité radikální nefrektomie, s výrazně vyšší pravděpodobností lokálních peri - i pooperačních komplikací a také riziku trvalé dialyzační léčby i přes možný technický úspěch.
Image 1. Největší solidní ložisko velikosti 39 mm předoperačně, bylo odstraněno jako první, uvedené ložisko bylo jako jediné resekováno ve studené ischemii
Fig. 1. The largest solid lesion, size of 39mm, preoperatively. It was removed as the first one. This one only was resected in cold ischemia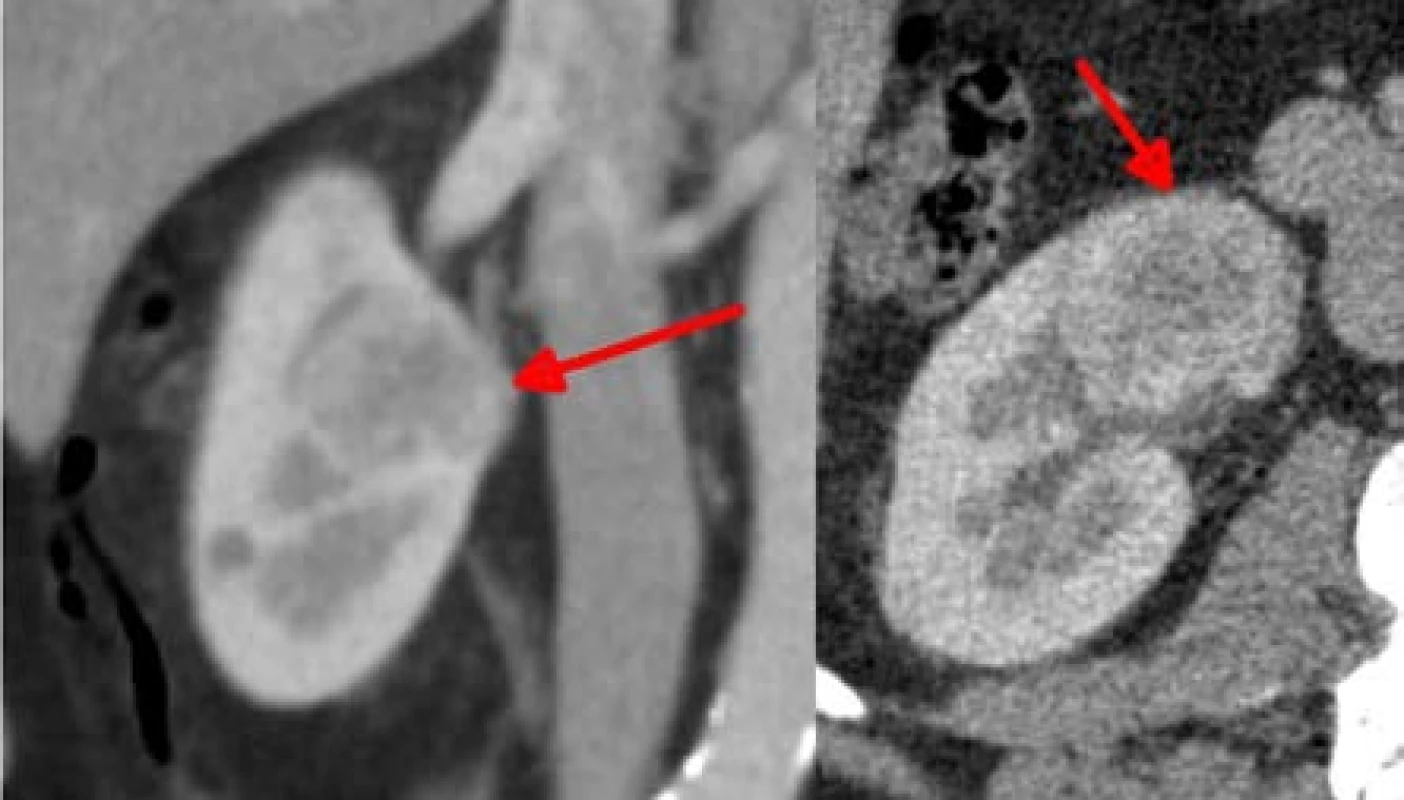
Image 2. Dvě ložiska velikosti 14 a 7 mm, která byla resekována současně, jako druhé v pořadí, bez ischemie
Fig. 2. Two lesions of 14 and 7mm, which were removed togerther as the second resection site, without ischemia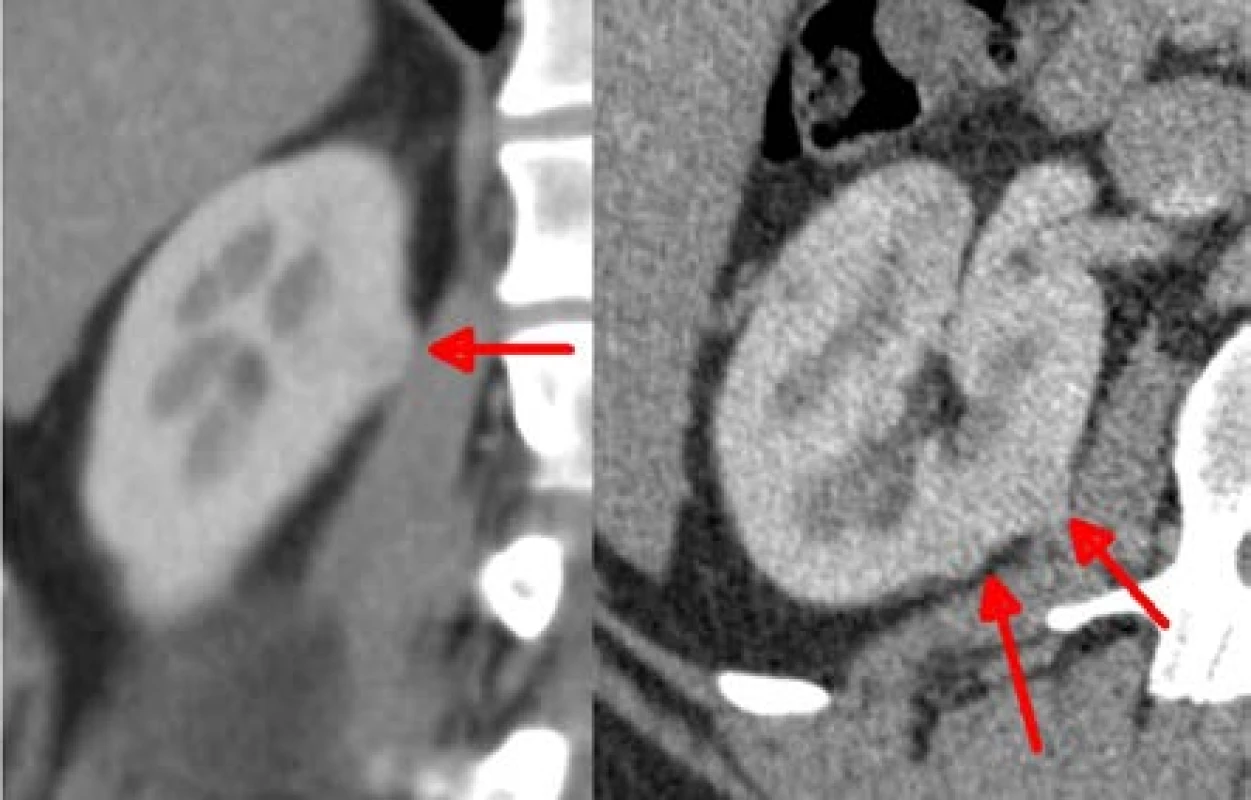
Image 3. Nejmenší ložisko velikosti 5 mm, odstraněno jako třetí, bez ischemie
Fig. 3. The smallest lesion of 5 mm. It was removed as the third one, without ischemia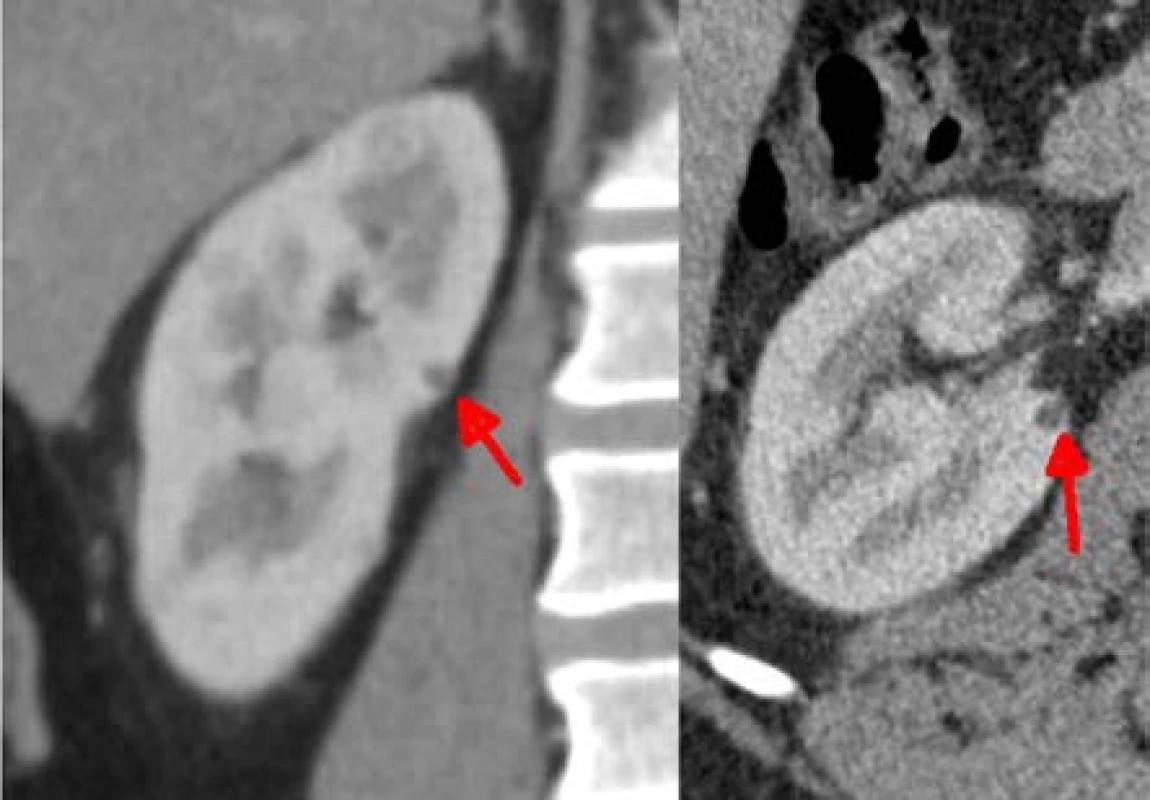
Image 4. Ložisko velikosti 7 mm, odstraněné jako čtvrté, bez ischemie
Fig. 4. Lesion of 7mm removed as the fourth one, without ischemia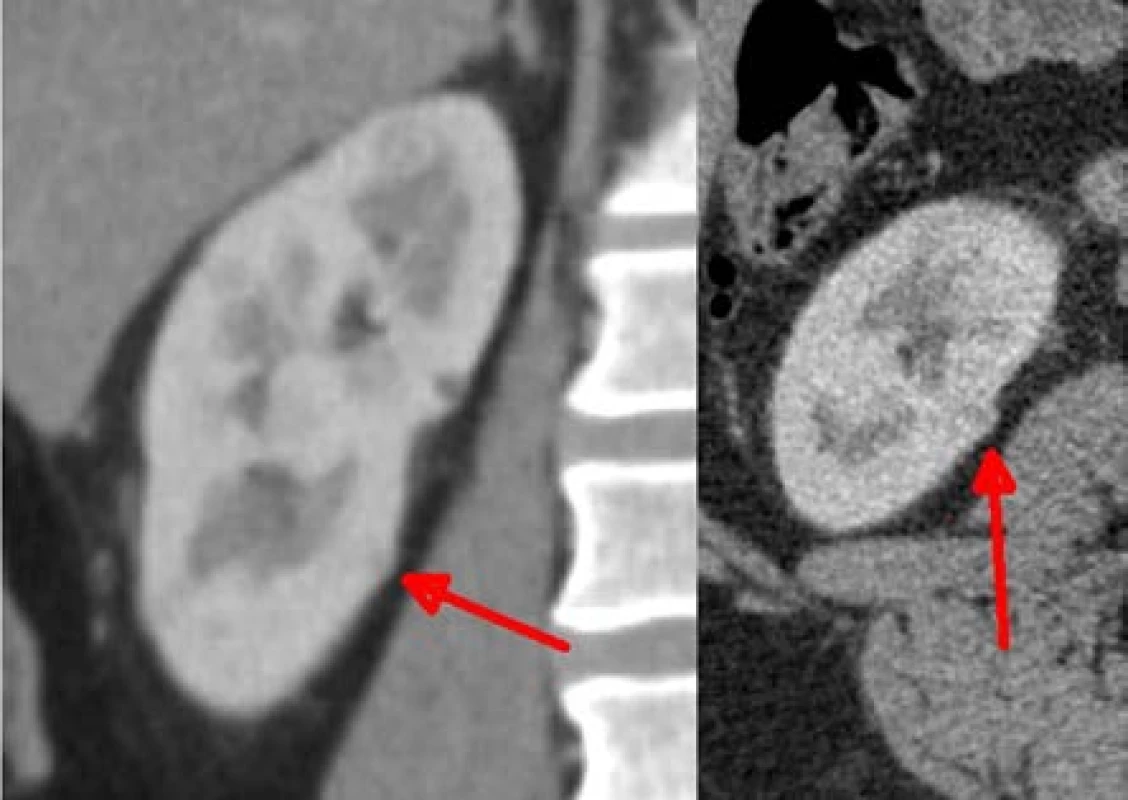
Image 5. Ložisko velikosti 15 mm na konvexitě dolního pólu, odstraněné jako páté, bez ischemie
Fig. 5. Lesion of 15mm on the convexity of a lower pole, which was removed as the fifth one, without ischemia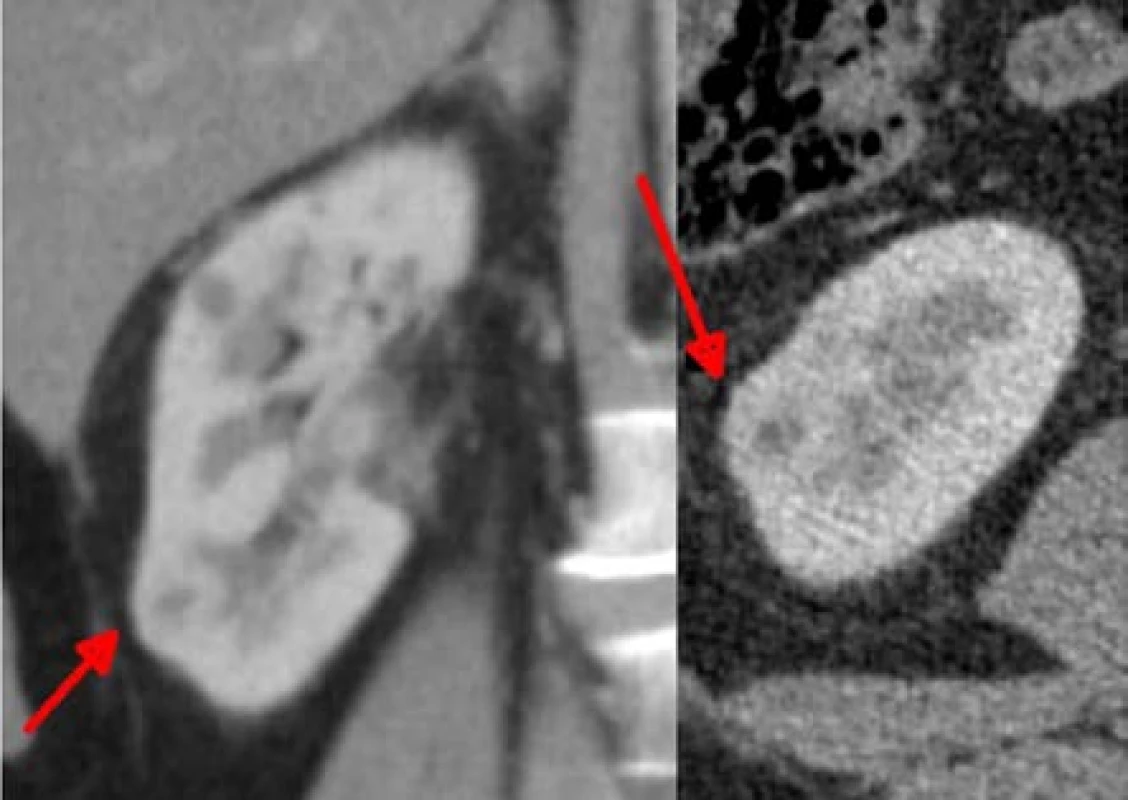
Table 1. Menší ložisko konvexity dolního pólu o velikosti 8 mm, odstraněno jako šesté, bez ischemie
Fig. 6. Smaller lesion of 8mm located on the lower pole convexity, it was resected as the sixth one, without ischemia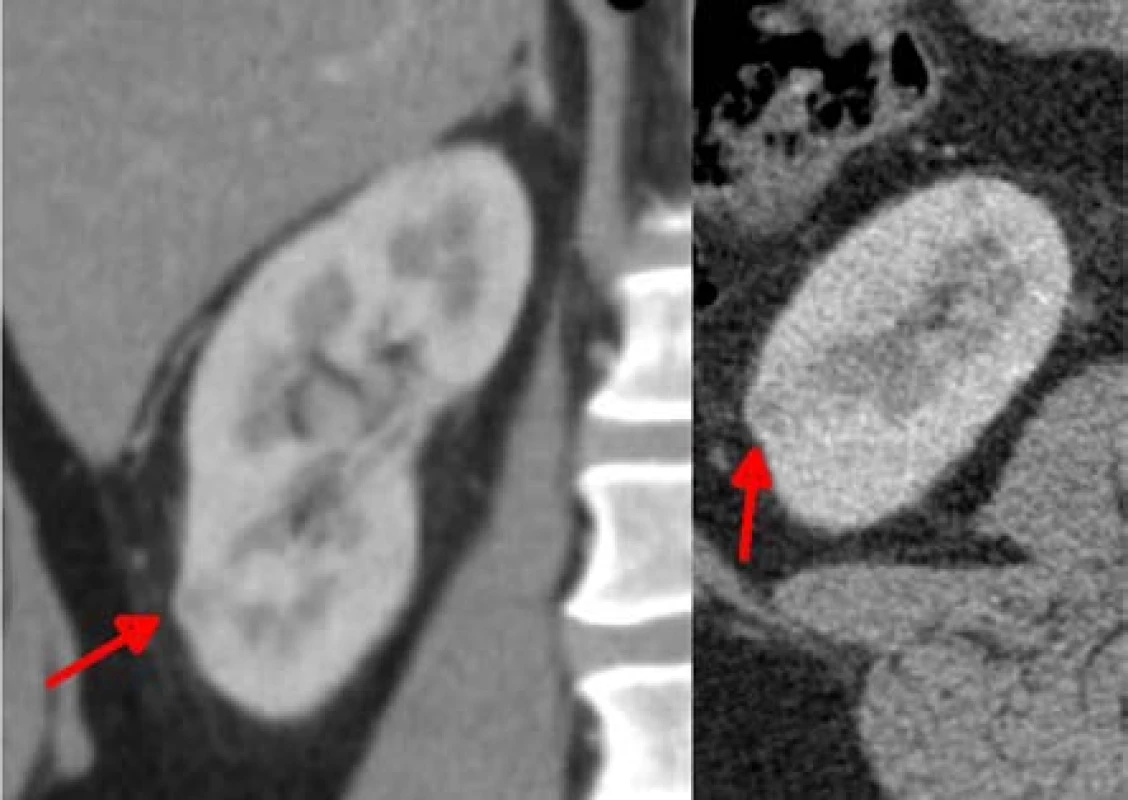
Image 6. Ložisko velikosti 8 mm na ventrální ploše dolního pólu, odstraněné jako sedmá oblast, bez ischemie
Fig. 7. Smaller lesion of 8mm located on the lower pole convexity, it was resected as the sixth one, without ischemia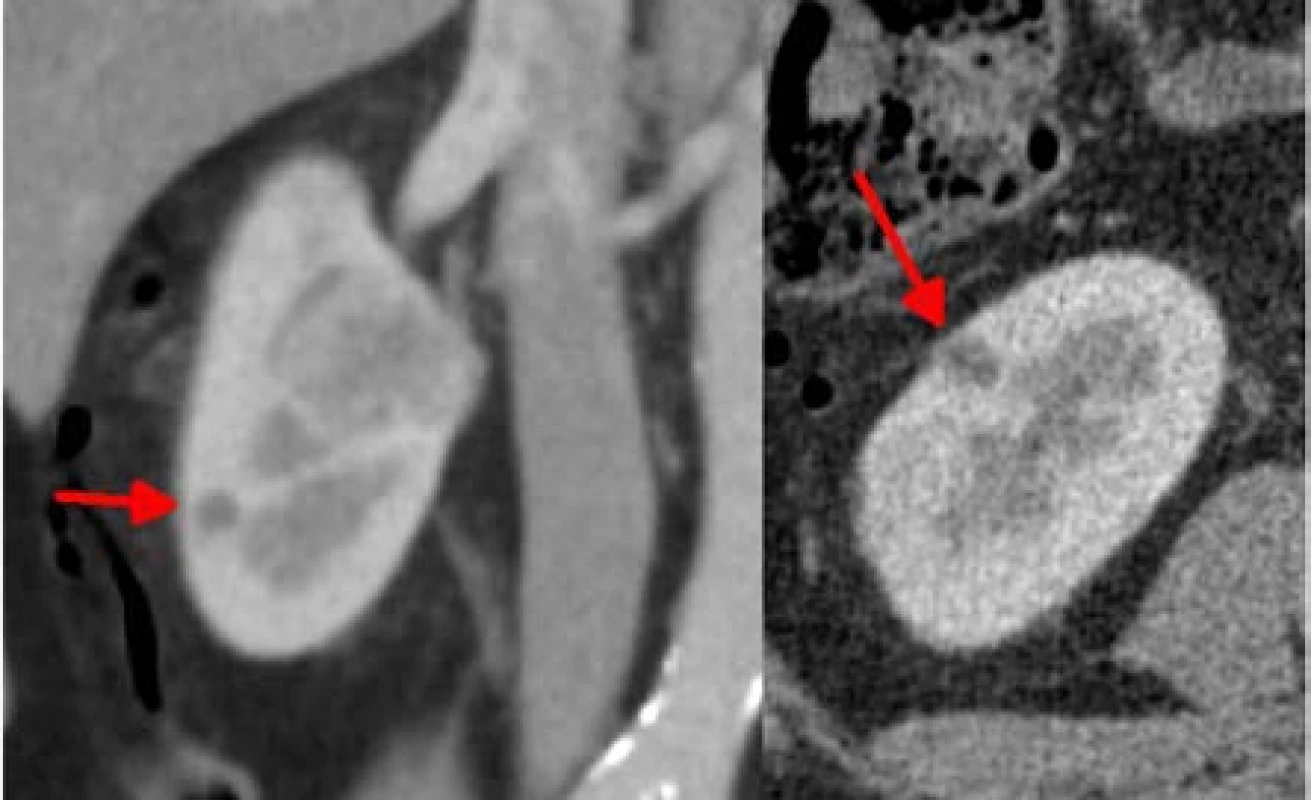
Table 2. Ložisko velikosti 10 m na ventrální ploše střední části ledviny, perioperačně zde bylo patrné ještě jedno drobné satelitní ložisko velikosti 5 mm a odstraněno současně v jednom vzorku jako osmé v pořadí, bez ischemie
Fig. 8. Lesion 10mm in size on the ventral aspect of the mid part of the kidney. Perioperatively, there was visible also another small 5mm satelite lesion. They were removed together as one specimen, as the eigth one in the row, without ischemia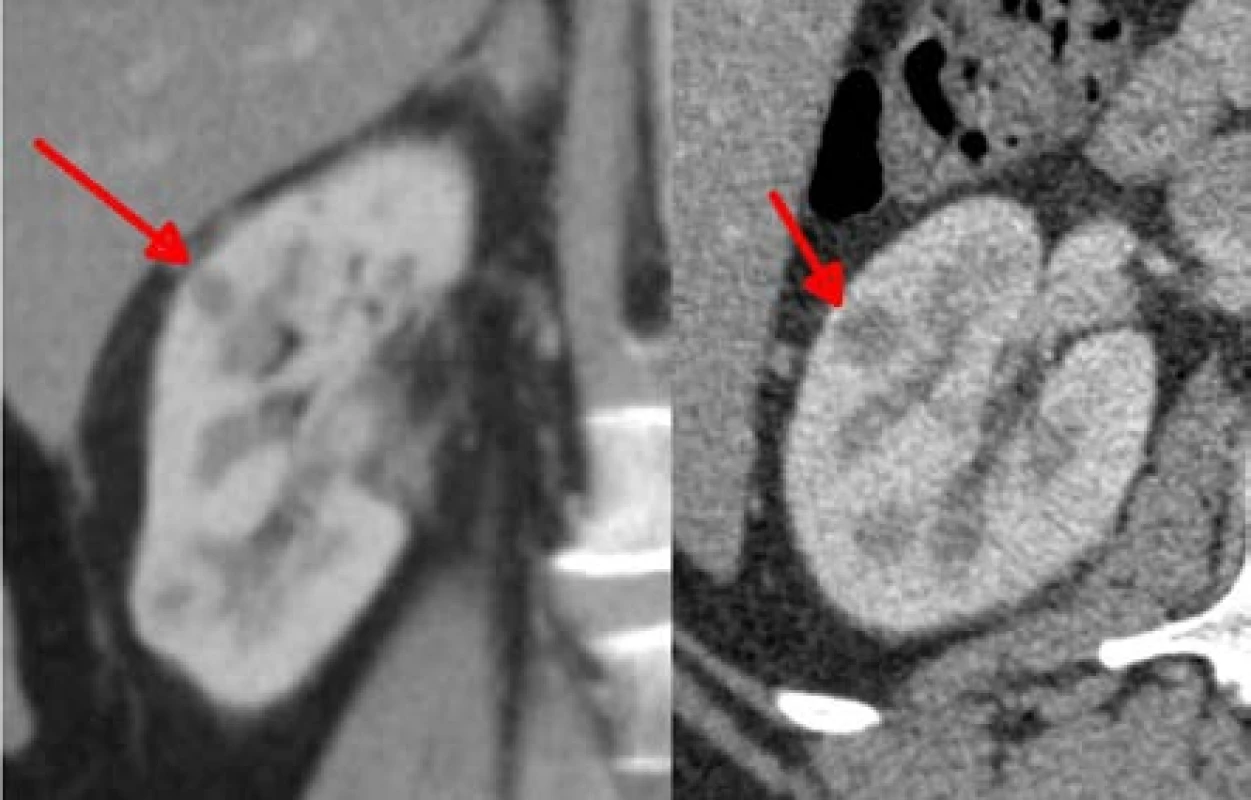
Table 3. Ložisko velikosti 11 mm na konvexitě horního pólu, které bylo odstraněno současně s dalším drobným solidním ložiskem, oblast odstraněna in toto jako devátá v pořadí, bez ischemie
Fig. 9. Lesion 11mm in size on the upper pole convexity, which was resected together with another small solid lesion. This was the ninth region, no ischemia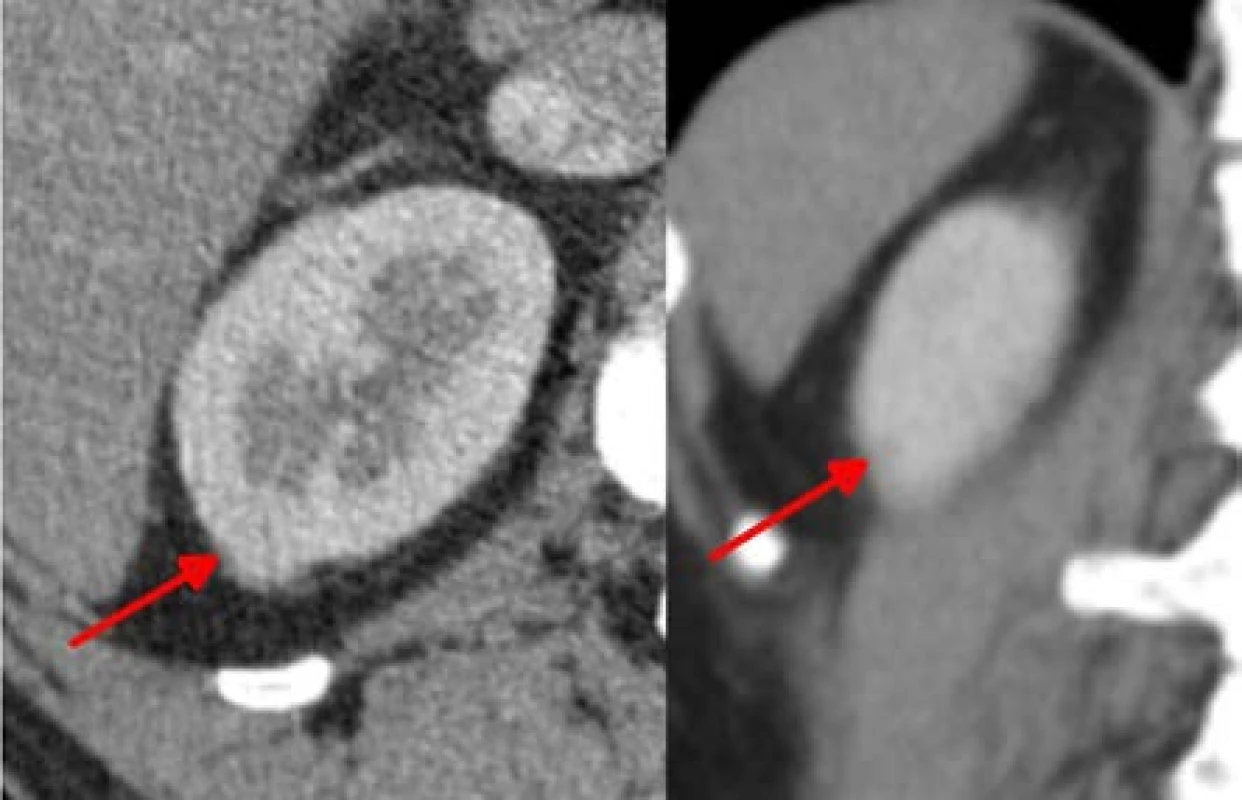
Image 7. Ložisko velikosti 9 mm na horním pólu, které bylo odstraněno jako poslední, také bez ischemie
Fig. 10. Nine millimeter lesion on the upper pole, removed as the last one, also no ischemia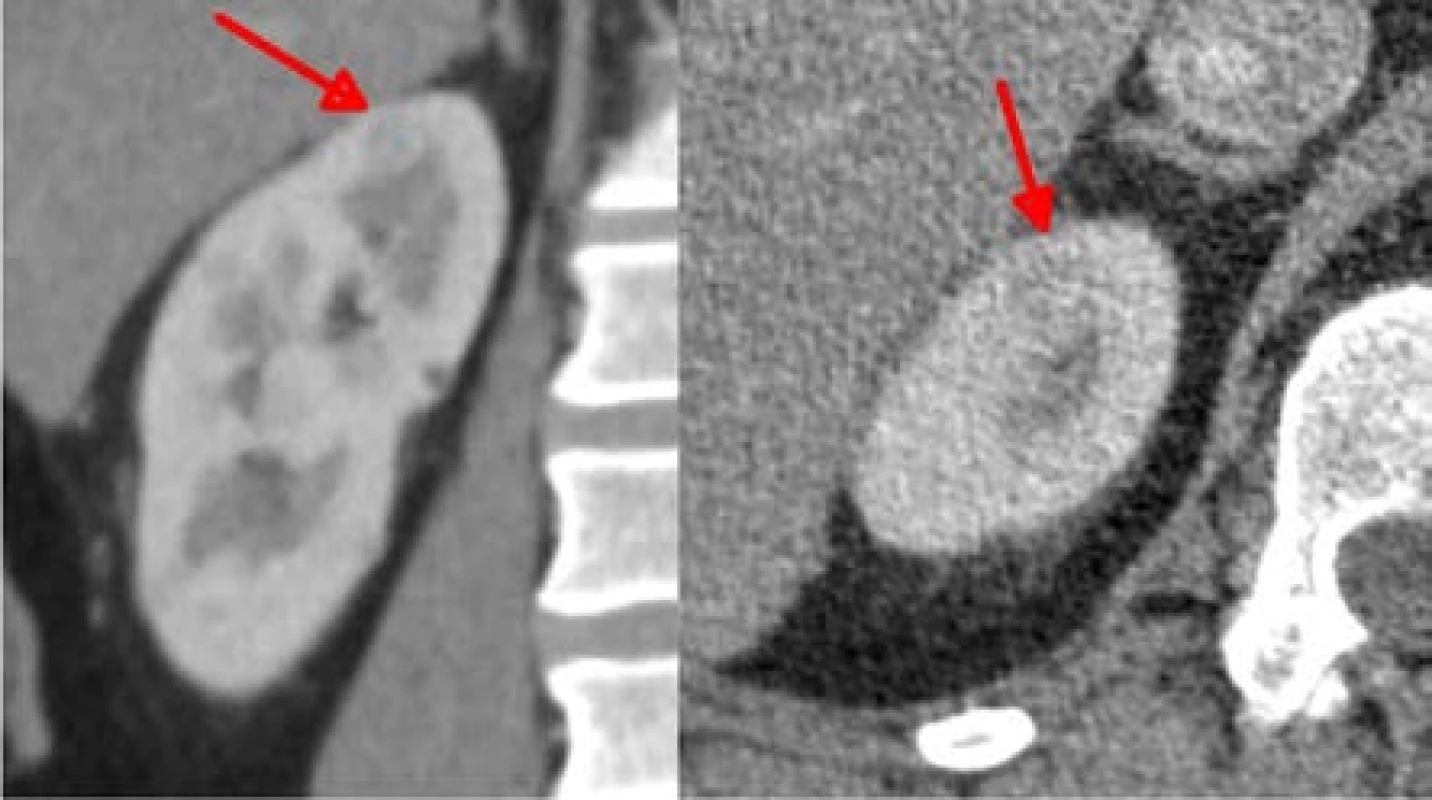
Operace byla provedena otevřeným transperitoneálním přístupem (mj. i pro možnost případné nefrektomie, pokud by peroperační nález nebyl onkologicky dobře řešitelný) ze subkostální incize. Po obvyklé mobilizaci celé ledviny s odstraněním tuku byl připraven turniket kolem hlavních hilových cév a samostatného svazku akcesorní tepny, která byla v kontaktu s největším nádorovým ložiskem, které bylo mediálně a ventrálně při hilu. Výkon byl zahájen intervencí na tomto ložisku, protože jeho technický úspěch či neúspěch rozhodoval o zbývající části výkonu. Odstranění největšího tumoru bylo provedeno ve studené ischemii s ledovou tříští, resekce nůžkami, dutý systém byl odsunut bez otevření (pánvička i dolní kalichy byly v kontaktu s tumorem, ale bez známek infiltrace) a stejně tak se podařilo zachovat akcesorní svazek pro dolní pól. Sutura defektu byla provedena stehem V-LocTM 90 3/0. Délka studené ischemie byla 17 minut. Následně byly systematicky resekovány všechny identifikované oblasti s postupem od dolního pólu kraniálním směrem, přičemž tři oblasti obsahovaly ložiska dvě. Všechny uvedené zbývající resekce byly bez ischemie, s případnou manuální kompresí přilehlého parenchymu dle potřeby. Resekce byla provedena nůžkami nebo elektroskalpem a sutura vždy v jedné vrstvě buď V-LocTM 90 3/0 nebo u menších ložisek VicrylTM 2/0 či 3/0. Perioperační sonografie nebyla potřebná. Hemostatický materiál použit nebyl. Na konci výkonu byla ledvina vrácena do původní polohy, provedena sutura tukového pouzdra a retroperitonealizace ledviny obnovením polohy tračníku. Délka výkonu byla 250 minut, krevní ztráta 600 ml.
V pooperačním období následovala mobilizace od druhého pooperačního dne, obnova pasáže bez komplikací a hojení per primam intentionem. Pooperační funkce ledviny se postupně zhoršovala až do osmého pooperačního dne, kdy dosáhla minima a kreatinin vystoupil až na 575 μmol/l. Byla přítomna také hyperkalemie 5,8 mmol/l a metabolická acidóza s BE-8,7. Po nefrologické konzultaci byl upraven dietní režim, zahájena léčba bikarbonátem a změněna antihypertenzní medikace z ACE inhibitoru na kalciový blokátor. Dále již docházelo k postupnému zlepšování a v době dimise 14. pooperační den byl kreatinin 277 μmol/l a kalemie 5,3 mmol/l.
Histologické vyšetření prokázalo v deseti místech 13 nádorů (tři místa obsahovala dvě ložiska) světlobuněčného renálního karcinomu pT1a(m) G2-3, velikosti od 5 do 35 mm. Ve třech resekátech byl popsán fokálně pozitivní okraj. Na kontrole šest týdnů po výkonu byl již kreatinin 209 μmol/l. Pacient je dále sledován nefrologem, přičemž jeho kreatininémie kolísá v rozmezí 166–199 μmol/l. CT hrudníku a břicha 12 měsíců po výkonu nepopsalo jasnou recidivu, nicméně jedno místo na ledvině je hodnoceno jako nejasné vzhledem k pooperační deformaci ledviny. Nález bude dále sledován zobrazovacími metodami. Pacientovi bylo doporučeno genetické vyšetření, které neabsolvoval.
DISKUZE
Řešení solidních ložisek ledvin prodělalo významný vývoj. Na počátku byla nefrektomie standardním výkonem bez ohledu na velikost ložiska. Záchovné výkony sice byly raritně prováděny, ale až vývoj modernějších šicích a hemostatických materiálů a také rozšíření znalostí o funkci ledviny a nárůst zkušeností vedly k rozšíření ledvinu šetřících výkonů. Zpočátku se širokým resekčním okrajem, později i minimálním až po „prosté“ enukleace či následně také méně invazivní metody založené na ablaci různými formami energie a až po sledování v řadě případů. Cílem je snaha o zachování co největšího množství funkčních nefronů k minimalizaci rizika dialyzační léčby v krátkodobém horizontu a ke snížení možných vlivů na celkové přežití (7). Vždy je nutné pečlivě vyvážit funkční přínos a onkologickou bezpečnost. Bilateralita a/ nebo multifokalita renálních nádorů může být přítomna i sporadicky, nicméně častěji se vyskytuje u osob s hereditárními syndromy (4). Multifokalita se klinicky udává do zhruba 11 %, ale při patologickém hodnocení jsou drobné satelitní tumory nacházeny až v 25 % (5).
Právě tato skupina (nejčastěji jsou zastoupeni pacienti s von Hippel-Lindauovým syndromem) dominuje v souborech popisujících řešení vícečetných lézí záchovným výkonem a/nebo tepelně ablační metodou. Na druhou stranu není vždy nutné intervenovat okamžitě při detekci ložiska minimální velikosti, protože opakované výkony na ledvině jsou spojeny s větším rizikem komplikací. Řada lézí je tak sledována a k aktivnímu řešení je přistupováno poté, kdy největší ložisko dosáhne velikosti 3 cm (4). V minulosti byl jednoznačně dominující otevřený přístup, nicméně s rozvojem minimálně invazivních metod (MI) je možné řadu případů řešit takto (8, 9, 10). Vzhledem ke komplexnosti výkonu je u MI technik preferován roboticky-asistovaný přístup (9, 10). Mimo obvyklých benefitů MI na rekonvalescenci může být teoretickou výhodou i menší množství intraabdominálních srůstů (4). Použití MI techniky by nemělo být na úkor snahy zachovat onkologickou bezpečnost. Práce referující výsledky vícečetných resekcí ledviny nejsou v uvádění pozitivních okrajů konzistentní, přesto lze v řadě případů dosáhnout výsledků srovnatelných s resekcemi solitárních ložisek (9, 11, 12). Vlastní technika resekce odlišná není. Je však značně maximalizovaná snaha o co nejvýraznější zkrácení (nebo absenci) teplé ischemie různými metodami. Mezi ně patří jednotlivě nebo v kombinaci segmentální uzávěr tepenných větví, manuální komprese přilehlého parenchymu nebo časné ukončení ischemie podle průběhu výkonu apod. (8, 10, 13, 14, 15, 16, 17). Je však obvyklé, že výkony pro mnohočetné léze jsou delší, jsou spojeny s vyšší krevní ztrátou (více míst a snaha o operaci bez ischemie nebo jen v krátké ischemii) a také jsou následně doprovázeny vyšším výskytem komplikací (krvácení, močové píštěle, transfuze nebo výrazné funkční zhoršení s dočasnou dialyzační léčbou). Čím je resekovaných ložisek více, tím je riziko komplikací vyšší (10, 12, 14).
Literární údaje o vícečetných nádorech uvádějí, že záchovným výkonem bylo řešeno až 52 ložisek jedné ledviny v jedné době, přičemž délka některých výkonů dosáhla až devíti hodin (10). Jde nepochybně o extrémní situace, do nichž se obvykle nedostaneme. I u vícečetného postižení je však správné alespoň uvažovat o možnosti záchovného nebo kombinovaného výkonu (s tepelně ablačními metodami), pokud to dovolí velikost a uložení nádorů. Plánování řešení může být spojeno i s bioptickou verifikací jednoho či více ložisek. To může být výhodné u ložisek atypických např. s rizikem lymfomového postižení, které je obvykle řešeno ne-chirurgicky a na zobrazovací vyšetřeních mívá odlišný vzhled (18). Je ale popsáno, že mnohočetná solidní ložiska mají nezřídka odlišný charakter (19). Z toho vyplývá, že skutečný přínos biopsie jediného ložiska bude při rozhodování o řešení mnohočetných lézích jen omezeně přínosný.
ZÁVĚR
Nádory ledvin tvoří značně heterogenní skupinu a je správné, pokud je jejich řešení plánováno individuálně pro každého pacienta. I u vícečetných nádorů lze v případě příznivého uložení provést záchovný výkon mnohočetnou resekcí. Při diskuzi s pacienty je nutné dobře komunikovat vyšší riziko komplikací, pozitivních okrajů a do budoucna možnost doplňkových či opakovaných výkonů. To platí zejména pro pacienty s hereditárními syndromy. Je také nezbytné racionálně přistoupit ke sledování zobrazovacími metodami, protože opakované vyšetření může vést k významné kumulaci radiační zátěže. Je na místě, aby řešení mnohočetných tumorů prováděla referenční pracoviště s odpovídající zkušeností. Obrazová dokumentace: Obrázky 1–10 demonstrují předoperační nález na CT vyšetření. Každý obrázek obsahuje koronární projekci (levá strana dvojobrázku) a axiální projekci (pravá strana dvojobrázku) k lepší orientaci. Některé obrázky demonstrují dvě ložiska současně vzhledem k jejich blízkosti a/nebo protože byla resekována současně (v jednom resekátu). U každého ložiska jsou uvedeny předoperační rozměry. Jako první bylo resekováno největší ložisko (zde označené číslem).
Došlo: 30. 5. 2019
Přijato: 21. 6. 2019
Kontaktní adresa:
MUDr. Petr Macek, Ph.D., FEBU
Departement of Urologie
Institut Mutualiste Montsouris
42 Boulevard Jourdan
75014 Paris, France
e-mail: macekp@gentlemail.com
Střet zájmů: Žádný.
Prohlášení o podpoře: Autor prohlašuje, že zpracování článku nebylo podpořeno farmaceutickou firmou.
Sources
1. Richter I, Dvořák J. Úvod do problematiky léčby zhoubných nádorů ledvin. Klin Onkol 2018; 31(2): 110–116.
2. Dušek L, Mužík J, Kubásek M, et al. Epidemiologie zhoubných nádorů v České republice [online]. Masarykova univerzita [2005] [cit. 2019-5-26]. Dostupný z WWW: http://www.svod.cz. Verze 7.0 [2007], ISSN 1802-8861.
3. Hurtová M, Louda M, Romžová M, et al. Bilaterální karcinom ledviny řešený jednodobou operací, nefrektomií a resekcí ledviny. Ces Urol 2012; 16(2): 117–120
4. Metwalli AR, Llinehan WM. Nephron‑sparing surgery for multifocal and hereditary renal tumors. Curr Opin Urol: 2014; 24(5): 466–473.
5. Linehan WM, Walther MM, Zbar B. The genetic basis of cancer of the kidney. J Urol 2003; 170(6): 2163–2172.
6. Macek P. Novinky v chirurgické léčbě nádorů ledvin. Onkologie 2017; 11(1): 14–18.
7. Sun M, Trinh QD, Bianchi M, et al. A non‑cancer‑related survival benefit is associated with partial nephrectomy. Eur Urol 2012; 61(4): 725–731.
8. Steinberg AP, Kilciler M, Abreu SC, et al. Laparoscopic nephron‑sparing surgery for two or more ipsilateral renal tumors. Urology 2004; 64(2): 255–258.
9. Calaway AC, Gupta GN, Bhandar A, et al. Robot‑assisted renal tumor enucleo‑resection in patients with a solitary kidney. Can J Urol 2015; 22(4): 7907–7913.
10. Hankins RA, Walton‑Diaz A, Truong H, et al. Renal functional outcomes after robotic multiplex partial nephrectomy: the National Cancer Institute experience with robotic partial nephrectomy for 3 or more tumors in a single kidney. Int Urol Nephrol 2016; 48(11): 1817–1821.
11. Gupta GN, Peterson J, Thakore KN, et al. Oncological outcomes of partial nephrectomy for multifocal renal cell carcinoma greater than 4 cm. J Urol 2010; 184(1): 59–63.
12. Maurice MJ, Ramirez D, Nelson RJ, et al. Multiple Tumor Excisions in Ipsilateral Kidney Increase Complications After Partial Nephrectomy. J Endourol 2016; 30(11): 1200–1206.
13. Curcio L, Salama B, Pinto DL, et al. Laparoscopic partial nephrectomy for multiple (four) tumors. Int Braz J Urol 2017; 43(video #3): 567.
14. Fadahunsi AT, Sanford T, Linehan WM, et al. Feasibility and outcomes of partial nephrectomy for resection of at least 20 tumors in a single renal unit. J Urol 2011; 185(1): 49–53.
15. Kahn AE, Shumate AM, Ball CT, et al. Pre‑operative factors that predict trifecta and pentafecta in robotic assisted partial nephrectomy. J Robot Surg 2019; doi: 10.1007/s11701-019-00958-7.
16. Swavely NR, Anele UA, Porpiglia F, et al. Optimization of renal function preservation during robotic partial nephrectomy. Ther Adv Urol 2019; 11: doi: 10.1177/1756287218815819.
17. Tan M, Xu Y, Xu D, et al. Laparoscopic Partial Nephrectomy With Sequential Precise Tumor‑specific Segmental Renal Artery Clamping for Multiple Ipsilateral Renal Tumors: A New Treatment Approach and Initial Experience. Urology 2017; 108 : 102–107.
18. Sheth S, Ali S, Fishman E. Imaging of renal lymphoma: patterns of disease with pathologic correlation. Radiographics 2006; 26(4): 1151–1168.
19. Simhan J, Canter DJ, Sterious SN, et al. Pathological concordance and surgical outcomes of sporadic synchronous unilateral multifocal renal masses treated with partial nephrectomy. J Urol 2013; 189(1): 43–47.
Labels
Paediatric urologist Nephrology Urology
Article was published inCzech Urology
2019 Issue 3-
All articles in this issue
- Editorial
- Prevence tromboembolických komplikací v urologii
- PSA a jeho izoformy jako moderní markery karcinomu prostaty
- Urologické komplikácie po transplantácii obličky
- Laparoskopická resekce ledviny – komplexní hodnocení perioperačních výsledků jednoho centra
- Wunderlichův syndrom – soubor pacientů s netraumatickým spontánním krvácením do retroperitonea
- Uroteliální karcinom ledvinné pánvičky vpravo a distálního močovodu vlevo
- Hranice možností záchovného výkonu u tumorů ledviny – desetinásobná resekce solitární ledviny
- Bilaterální tumor ledvin jako náhodný nález při ultrazvukovém vyšetření u 82letého pacienta s močovou retencí
- Centrálně lokalizovaná cystická renální léze nejasné biologické povahy
- 3rd Ostrava Urological-Neurological Symposium
- Report on the 7th Annual Video Seminar „Tips and tricks in urological surgery”
- Report from the 26th annual meeting of Slovak urological society
- Czech Urology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- PSA a jeho izoformy jako moderní markery karcinomu prostaty
- Urologické komplikácie po transplantácii obličky
- Wunderlichův syndrom – soubor pacientů s netraumatickým spontánním krvácením do retroperitonea
- Uroteliální karcinom ledvinné pánvičky vpravo a distálního močovodu vlevo
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

