-
Medical journals
- Career
Využití extraanatomického stentu (EAS) u pacientů s pokročilým maligním onemocněním
Authors: David Němec; Jan Krhut; David Míka; Ondřej Havránek
Authors‘ workplace: Urologické oddělení FN, Ostrava
Published in: Ces Urol 2012; 16(4): 241-246
Category: Original article
Overview
Cíl:
Častou komplikací u pacientů s maligním onemocněním je ureterální obstrukce. Řešením je zavedení ureterálního stentu, nefrostomická drenáž nebo otevřená chirurgická intervence. Extraanatomické stenty (EAS) jsou alternativou derivace moči u pacientů s pokročilým maligním onemocněním s krátkou životní prognózou. Cílem práce je ověřit efektivitu derivace moči pomocí EAS a vyhodnotit kvalitu života (QoL – Quality of Life).Metoda:
Soubor zahrnuje jedenáct pacientů (osm mužů a tři ženy), průměrný věk 64,5 let (38–80 let). Jde o pět pacientů s generalizovaným karcinomem močového měchýře, tři pacienty s lokálně pokročilým karcinomem prostaty, jednu pacientku s lokálně pokročilým karcinomem děložního čípku a dva pacienty s uzlinovým syndromem při generalizovaném karcinomu tlustého střeva. V devíti případech byla volena metoda s vyústěním EAS do urostomického sáčku, ve dvou případech jsme použili EAS k oboustrannému nefrovezikálnímu bypassu. Kvalitu života jsme hodnotili pomocí dotazníku King’s Health Questionnaire (KHQ) před založením EAS a 4 týdny po založení. Výsledky jsou zpracovány pomocí Wilcoxonova testu na hladině významnosti 0,05.Výsledky:
Průměrná doba sledování pacientů je 40 týdnů (8–55 týdnů). Kvalita života po založení EAS se statisticky signifikantně zvýšila ve všech sledovaných parametrech. K vyřešení hydronefrózy došlo v deseti případech a zlepšení u jednoho pacienta. Předoperační hladina sérového kreatininu (186,6 ± 64,67 µmol/l) po operaci významně poklesla (106 ± 24,49 µmol/l).Závěr:
EAS je slibnou alternativou v řešení ureterální obstrukce u maligního onemocnění v terminálním stádiu. Metoda není technicky náročná a poskytuje velmi dobré funkční výsledky spolu se signifikantním zvýšením kvality života pacientů.Klíčová slova:
extra-anatomický stent, kvalita života, nefrostomie, ureterální obstrukce.ÚVOD
Častou komplikací u pacientů s maligním onemocněním je extramurální ureterální obstrukce. Složitou problematiku řešení ureterální obstrukce potvrzuje množství endoskopických a chirurgických metod používaných k řešení tohoto problému (1). Řešením volby je zavedení ureterálního stentu a nefrostomická drenáž s nutností opakované výměny, nebo otevřená chirurgická intervence (2). Zavedení stentu představuje nejjednodušší formu drenáže močových cest. Již od roku 1967, kdy Zimskind et al. (3) poprvé popsali zavedení stentu, se tato procedura stala nepostradatelným nástrojem v každodenní praxi urologů. Velkým problémem u vnitřní drenáže ureteru stentem je poměrně vysoké riziko tvorby inkrustaci s následným obtížným řešením (4). Otevřená chirurgická intervence bývá vzhledem k celkovému stavu onkologicky nemocného pacienta a práci v ozářeném či již operovaném terénu značně problematická, v některých případech nemožná. Velmi často je ureterální obstrukce oboustranná. V případě, že zavedení ureterálního stentu není možné, nebo není efektivní, je jedinou možností nefrostomická drenáž. Nefrostomie (mnohdy oboustranná) výrazně snižuje kvalitu života pacienta. Hledáme alternativy derivace moči v paliativní léčbě onkologicky nemocného. Cílem práce je ověřit efektivitu derivace moči pomocí extraanatomického stentu (EAS) a vyhodnotit kvalitu života (QoL – Quality of Life).
MATERIÁL A METODY
Náš soubor zahrnuje jedenáct pacientů (osm mužů a tři ženy), průměrný věk 64,5 let (38–80 let). U všech pacientů byla prokázána oboustranná ureterální obstrukce s alterací renálních funkcí. Jde o pět pacientů s generalizovaným karcinomem močového měchýře, tři pacienty s lokálně pokročilým karcinomem prostaty, jednu pacientku s lokálně pokročilým karcinomem děložního čípku a dva pacienty s uzlinovým syndromem při generalizovaném karcinomu tlustého střeva.
Využití extraanatomických stentů je možné dvěma způsoby. Prvním je nefrovezikální bypass, druhým je nefrokutánní bypass (vyústění EAS do urostomického sáčku). Založení EAS lze provést v krátké celkové či svodné anestezii. Používáme set extraanatomického stentu firmy Rüsch Ch 12 (obr. 1, 2). Set obsahuje dvě punkční jehly, drátěný vodič, dilatátory, dva stenty s kovovou jehlou k tunelizaci podkožím a kovovou spojovací část.
Image 1. Schéma extraanatomického stentu A – oboustranný nefrokutánní bypass; B – oboustranný nefrovezikální bypass Fig. 1. Scheme of extra-anatomic stent A – bilateral nephocutaneous bypass; B – bilateral nephrovesical bypass 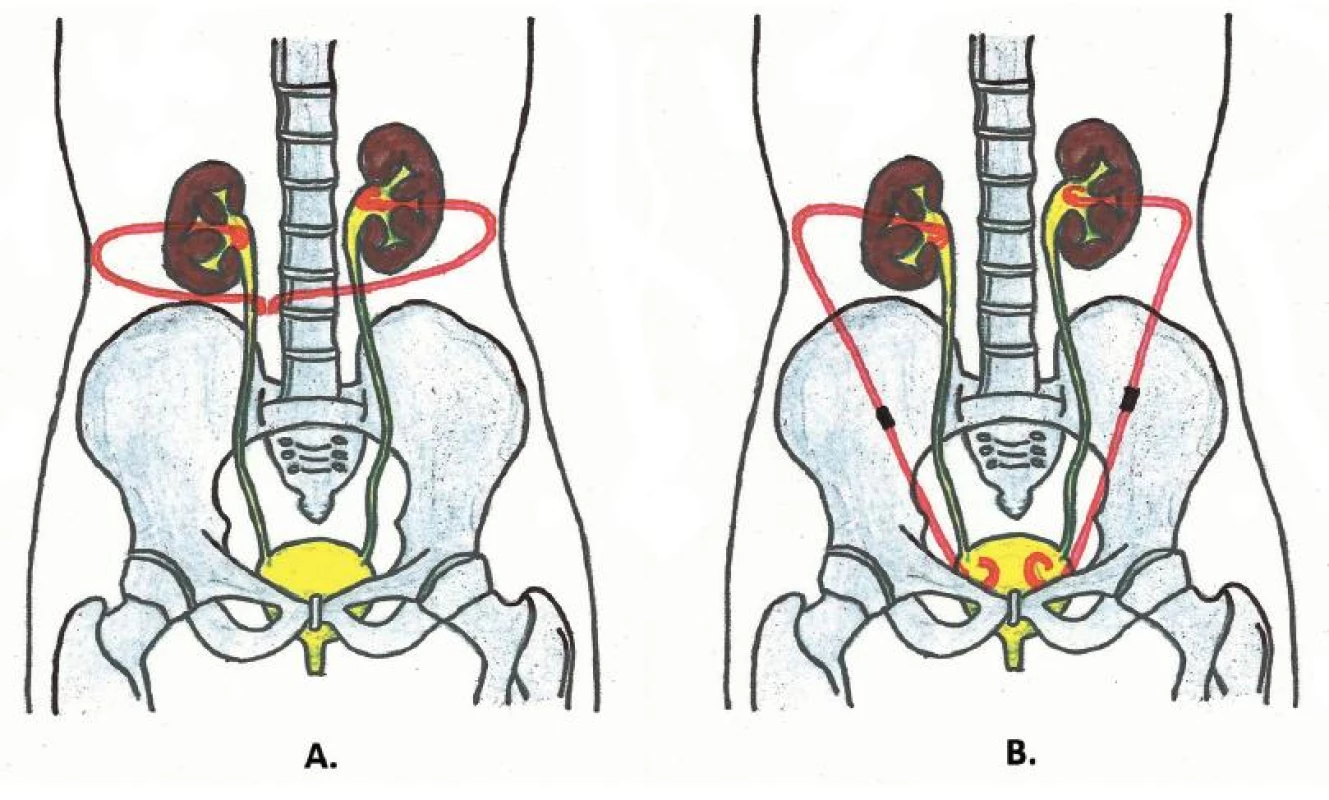
Image 2. Extraanatomický stent Fig. 2. Extra-anatomic stent 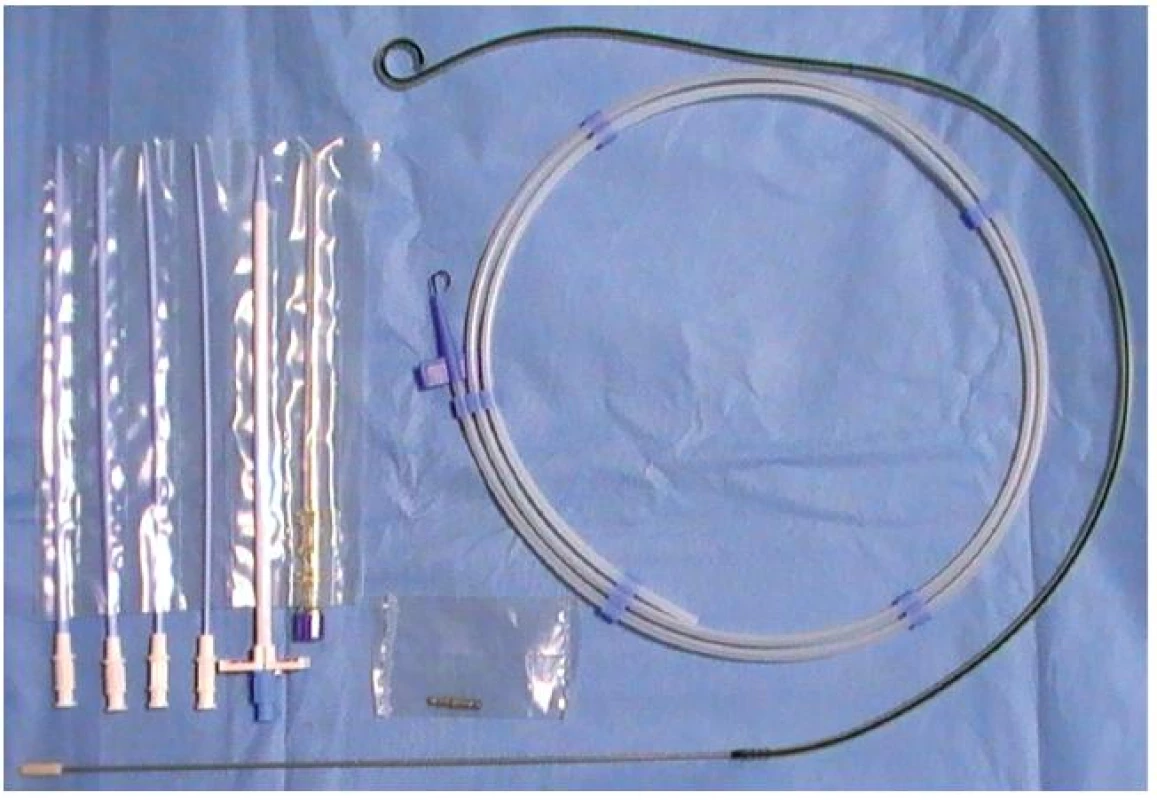
Principem je zavedení EAS do kalichopánvičkového systému (KPS) ledviny perkutánní punkcí. Tunelizace stentu podkožím se provádí pomocí kovové jehly, jež je součástí distálního konce stentu. Následuje napojení na druhou část bypassu zavedeného suprapubickou punkcí do močového měchýře, který je také tunelizován podkožím k místu spojení v mezogastriu. Ke spojení se využívá kovová spojovací část. Při metodě s vyústěním do urostomického sáčku (nefrokutánní bypass) vyvedeme stenty v pravém mezogastriu a fixujeme ke kůži nevstřebatelnými stehy. Následuje nalepení urostomického sáčku.
Založení EAS je možno provést jako primární derivační operaci, nebo sekundárně při již zavedené nefrostomické drenáži. Primárním založením výrazně snižujeme riziko infekce. Jako prevenci před uroinfekty podáváme před a týden po implantaci EAS antibiotika. Po založení nefrovezikálního bypassu zavádíme permanentní katétr na 48 hodin v rámci prevence perivezikálního urinomu.
V našem souboru byla v devíti případech volena metoda s vyústěním do urostomického sáčku, ve dvou případech jsme použili EAS k nefrovezikálnímu bypassu. Rozhodujícím kritériem při výběru možnosti byla funkční kapacita močového měchýře. Za dostatečnou kapacitu považujeme 300 ml a více. Kvalitu života jsme hodnotili pomocí dotazníku King’s Health Questionnaire (KHQ) (5) před založením EAS a 4 týdny po založení. Výsledky jsou zpracovány pomocí Wilcoxonova testu na hladině významnosti 0,05 (tab. 1). V rámci dispenzarizace jsou prováděny pravidelné kontroly renálních parametrů a ultrazvuková kontrola.
Table 1. Vyhodnocení dotazníku King’s Health Questionnaire (KHQ) Table 1. King‘s Health Questionnaire (KHQ) evaluation 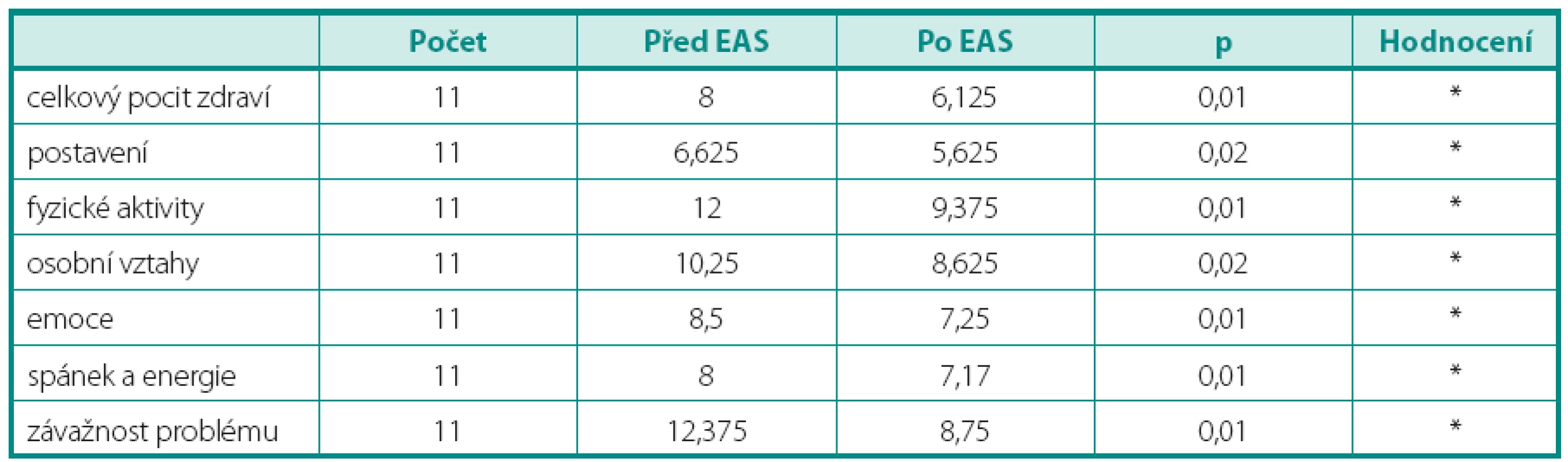
*rozdíl statisticky významný VÝSLEDKY
Průměrná doba sledování pacientů v souboru je 40 týdnů (8–55 týdnů). Kvalita života po založení EAS se statisticky signifikantně zvýšila ve všech sledovaných parametrech dotazníku kvality života (graf 1). K vyřešení hydronefrózy došlo v deseti případech a zlepšení u jednoho pacienta. Předoperační hladina sérového kreatininu (186,6 ± 64,67 µmol/l) významně poklesla po operaci (106 ± 24,49 µmol/l). Průměrný operační čas byl 70 minut u oboustranného nefrovezikálního bypassu a 40 minut u nefrokutánního bypassu.
Graph 1. Vyhodnocení dotazníku King’s Health Questionnaire (KHQ) Graph 1. King‘s Health Questionnaire (KHQ) evaluation 
Komplikace byly hodnoceny pomocí Clavien-Dindo klasifikace chirurgických komplikací (6). Nebyly zaznamenány žádné život ohrožující komplikace. V jednom případě byla nutná relokace částečně dislokovaného EAS do KPS ledviny (IIIa), dvakrát byla nutná následná léčba uroinfektu (II) a v jednom případě jsme museli řešit sekundární hojení rány s nutností založení nového extraanatomického stentu (IIIb). Dva pacienti již zemřeli v důsledku progrese základního onemocnění (3 a 4 měsíce po založení EAS).
DISKUSE
Extraanatomické stenty (EAS) jsou alternativou v symptomatické léčbě subrenální obstrukce u pacientů s pokročilým maligním onemocněním a krátkou životní prognózou.
Není to metoda nová, její princip byl popsán již Lingamem před téměř 20 lety, zatím však nedoznala většího rozšíření (7). Podle dostupných literárních pramenů je to však metoda velmi efektivní a neprávem opomíjená (8).
Metoda není technicky náročná a provedená laboratorní a paraklinická vyšetření potvrzují efektivní drenáž moči po založení EAS. Vyřešení hydronefrózy a reparace renálních funkcí po založení EAS je ve všech parametrech srovnatelná s drenáží perkutánní nefrostomií (9).
Prací hodnotících přínos metody pro zlepšení kvality života je málo a přímé srovnání s našimi výsledky je jen velmi obtížné, protože většina jiných autorů používá k hodnocení kvality života vizuálně analogovou škálu (10). Naše práce jako první užívá k hodnocení kvality života standardizovaný validovaný dotazník. Obecně lze však říci, že zlepšení kvality života pacientů v terminálním stádiu nádorového onemocnění je hlavní výhodou EAS. Zlepšují mobilitu pacientů, prodlužují dobu jejich soběstačnosti a jsou podstatně jednodušší z hlediska ošetřování než klasické nefrostomie. Z našich výsledků je patrný i pozitivní vliv na celkové vnímání nemoci.
Limitací využití nefrovezikálního bypassu je funkční kapacita močového měchýře, která bývá u těchto pacientů často velmi malá. Za minimální funkční kapacitu močového měchýře, která umožňuje využít nefrovezikální bypass, považujeme 200 ml. U pacientů s nižší kapacitou je subjektivně lépe vnímána derivace moči nefrokutánní, kdy odpadá zejména pro pacienty velmi únavná nykturie. Dalším faktorem, který je nutné brát v úvahu během rozhodování o typu bypassu, je lokální nález v močovém měchýři. Při primárních nádorech močového měchýře, nebo sekundárním prorůstání malignit z okolí, volíme raději nefrokutánní bypass z obavy před hematurií z lokálního dráždění a možnou obturací v případě eventuálního nefrovezikálního bypassu. Absolutní kontraindikací využití EAS je porucha hemokoagulace a neschopnost podstoupit zákrok v celkové či spinální anestezii.
V našem souboru jsme nezaznamenali žádné život ohrožující komplikace. Rovněž jsme nemuseli řešit nejčastěji uváděnou komplikaci – obturaci stentu při inkrustacích. Někteří autoři doporučují k prevenci inkrustací užívat stenty s větším průsvitem, většinou 15–17 Ch (11). Na základě našich výsledků se domníváme, že u pacientů s krátkou očekávanou délkou přežití je běžně užívaný průsvit 12 Ch dostatečný. Nutností je zajistit u pacientů adekvátní diurézu, v úvahu připadá i acidifikace moči.
Cena setu pro EAS je asi trojnásobná ve srovnáním s cenou klasického nefrostomického setu. Při ekonomické rozvaze však musíme brát v úvahu nutnost pravidelných relativně častých výměn a vyšší riziko uroinfektu u pacientů s nefrostomií. Benefit pro pacienta z hlediska zlepšení kvality života při použití EAS je vyčíslitelný jen obtížně.
Na základě našich iniciálních zkušeností se domníváme, že EAS může představovat atraktivní alternativu derivace moči v indikované skupině pacientů.
ZÁVĚR
Extraanatomický stent je jednoduchá, minimálně invazivní a vysoce účinná léčba pro pacienty se subrenální obstrukcí při maligním onemocnění v terminálním stádiu. Metoda není technicky náročná a poskytuje velmi dobré funkční výsledky spolu se signifikantním zvýšením kvality života pacientů.
Došlo: 14. 9. 2012.
Přijato: 19. 10. 2012.
Kontaktní adresa
MUDr. David Němec
Urologické oddělení FN
17. listopadu 1790, 708 00 Ostrava-Poruba
e-mail: nemec.david@seznam.cz
Střet zájmů: žádný.
Sources
1. Dvořáček J. Ureterální obstrukce. In Dvořáček J, Babjuk M, et al. Onkourologie. Praha: Galén 2005; 403–404.
2. Babjuk M. Derivace moči u nemocných s nádory močového měchýře. In Dvořáček J, Babjuk M, et al. Onkourologie. Praha: Galén 2005; 183–196.
3. Zimskind PD, Fetter TR, Wilkerson JL. Clinical use of long term indwelling silicone rubber ureteral splints inserted cystoscopically. J Urol 1967; 97 : 840–844.
4. Kočovská P, Eret V, Toufarová P, Chudáček Z, Hora M. Možnosti endoskopického řešení dlouhodobě ponechaných inkrustovaných uretrálních stentů. Ces Urol 2012; 16(2): 101–107.
5. KHQ – http://www.nice.org.uk/nicemedia/live/10996/30291/30291.doc
6. Dindo D, Demartines N, Clavien PA. Classification of Surgical Complications, A new proposal with evaluation in a Cohort of 6336 patients and results of a survey. Ann Surg 2004; 240(2): 205–213.
7. Lingam K, Paterson PJ, Lingam MK, Buckley JF, Forrester A. Subcutaneous urinary diversion: an alternative to percutaneous nephrostomy. J Urol 1994; 152 : 70–72.
8. Nissenkorn I, Gdor Y. Nephrovesical subcutaneous stent: an alternative to permanent nephrostomy. J Urol 2000; 163(2): 528–530.
9. Belej K, Záťura F, Hluší P. Možnost úpravy funkce ledvin po odstranění obstrukce. Ces Urol 2001; 2 : 33–37.
10. Schmidbauer J, Kratzik C, Klinger HC, Remzi M, Lackner J, Marberger M. Nephrovesical subcutaneous ureteric bypass: long-term results in patients with advanced metastatic disease-improvement of renal function and quality of life. Eur Urol 2006; 50(5): 1073–1078.
11. Andonian S, Zorn KC, Paraskevas S, Anidjar M. Artificial ureters in renal transplantation. Urology 2005; 66 : 1109.
Labels
Paediatric urologist Nephrology Urology
Article was published inCzech Urology

2012 Issue 4-
All articles in this issue
- Zobrazení karcinomu prostaty metodami nukleární medicíny
- Využití molekulární genetiky v diferenciální diagnostice nádorů ledvin
- Srovnání laparoskopické a retropubické radikální prostatektomie – zkušenosti z jednoho centra
- Prognóza pacientů s T1G3 uroteliálním karcinomem močového měchýře léčených vakcínou BCG – retrospektivní analýza
- Využití extraanatomického stentu (EAS) u pacientů s pokročilým maligním onemocněním
- Liposarkom retroperitonea v lokalizaci dolního polu ledviny
- Myoglobinurie jako projev rabdomyolýzy po extrémní fyzické zátěži
- 12th Central European Meeting
- Czech Urology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Myoglobinurie jako projev rabdomyolýzy po extrémní fyzické zátěži
- Zobrazení karcinomu prostaty metodami nukleární medicíny
- Prognóza pacientů s T1G3 uroteliálním karcinomem močového měchýře léčených vakcínou BCG – retrospektivní analýza
- Liposarkom retroperitonea v lokalizaci dolního polu ledviny
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

