-
Medical journals
- Career
Evoluce operační techniky laparoskopické resekce nádorů ledvin
Authors: Milan Hora 1; Viktor Eret 1; Petr Stránský 1; Tomáš Ürge 1; Jiří Klečka jr. 1; Ondřej Hes 2; Zdeněk Chudáček 3; Jiří Ferda 4
Authors‘ workplace: Urologická klinika LF UK a FN Plzeň 1; Šiklův patologicko-anatomický ústav LF UK a FN Plzeň 2; Radiodiagnostické oddělení LF UK a FN Plzeň 3; Radiodiagnostická klinika LF UK a FN Plzeň 4
Published in: Ces Urol 2010; 14(1): 24-31
Category: Original article
Overview
Cíl:
Na vlastním souboru laparoskopických resekcí (LR) tumorů ledvin dokumentovat technický vývoj metodiky.Materiál a metodika:
Metodiku LR provádíme od 9/2004. Do 6/2009 jsme provedli 73 LR. Během let jsme metodiku modifikovali na základě získávání vlastních zkušeností a na základě průběžného studia recentní odborné literatury.Výsledky:
První výkony jsme prováděli u malých extrarenálních tumorů, klampovali jsme hilus malou endosvorkou en bloc a resekční plochu šili pomocí zdlouhavého intrakroporálního uzlení. Metodiku jsme průběžně modifikovali. V plánování operace preferujeme multidetektorové CT včetně dvoufázové CT angiografie. Mezi nejpodstatnější změny v metodologii vlastní LR v našem souboru lze zařadit klampování pouze renální artérie, u komplexních hilů klampování en bloc extrakorporální cévní svorkou, možnost ošetření spodiny resekce argonovým koagulátorem, sutura dotahovaná pomocí uzamykatelných klipů (na spodině vstřebatelnými PDS klipy, na renorafii většími nevstřebatelnými Hem-o-lok® klipy) a využití trombinového lepidla ve vybraných případech. S rostoucími zkušenostmi jsme schopni nezanedbatelnou část tumorů řešit bez klampování hilových cév.Závěr:
Postupné zdokonalování operační techniky u LR umožňuje ošetřit touto metodikou větší procentu tumorů ledvin a zlepšují se i operační výsledky. Přesto je LR stále určena jen pro přísně vybrané případy a otevřená resekce zůstává zlatým standardem.Klíčová slova:
nádor ledviny, laparoskopie, nefrektomie, resekce ledviny.Úvod
Nádory ledvin jsou důležitou součástí práce českých urologů. Incidence nádorů ledvin je stále vysoká, nejvyšší na celém světě. V roce 2006 to bylo 32,9 (18,2) případů na 100 000 mužů (žen) (1). Dále se zvyšuje zastoupení stádia I (nádory T1N0M0), což jsou nádory potenciálně vhodné k resekčním výkonům. Doba radikálních nefrektomií u většiny nádorů je nahrazena u velkého procenta nádorů operacemi záchovnými, prováděnými standardně otevřeně. Objevují se však nové metodiky – laparoskopická resekce, které se budeme věnovat podrobněji, ablační termální metodiky (radiofrekvence a kryoablace) aplikované perkutánně či laparoskopicky a další spíše již experimentální metodiky. Nesmíme zapomínat i na možnost aktivního sledování.
Uplynulo více než 10 let od prezentace první větší série laparoskopické resekce (LR) nádorů ledvin (2). Výskyt komplikací byl vysoký, ale se získáváním zkušeností a se zdokonalováním operační techniky a využíváním stále dalších a dalších technických vymožeností se výskyt komplikací začal razantně snižovat. Technika LR se neustále vyvíjí, i když ne skokem, ale malými drobnými postupnými krůčky. Relativně dobré výsledky dosahují a publikují tzv. laparoskopická „centres of excellence” (vysokoobjemová centra specializující se na laparoskopii mj. i na LR). Příkladem je skupina Gilla a Kaouka z Cleveland Clinic v americkém Ohiu, která provedla už přes 1000 LR. Postupy těchto center pomalu přejímají urologové do běžné rutinní praxe. Dřívější indikace k LR byly malé exofytické tumory dobře přístupné pro laparoskopické nástroje. Zmíněná „centres of excellence“ rozšiřují díky pokroku v operační technice a zdokonalování operační techniky indikace na komplexnější tumory – tumory na horního polu (3), centrální (4) a hilové tumory (5, 6), tumory T1b, T2 i výše (7, 8) a další neobvyklé případy (předchozí chirurgie ledvin, mnohočetné nádory, zavzetí nadledviny do tumoru, konkomitantní patologie renální artérie, obezita) a dokonce solitární ledvina (9). Nově popisovaná vylepšení LR se snažíme dle možností postupně zavádět i do naší klinické praxe a svoje zkušenosti shrnujeme v článku.
Image 1. Graf ukazuje, jaká část chirurgicky řešených nádorů ledvin na Urologické klinice LF UK a FN Plzeň byla řešena laparoskopickou resekcí (světle modrá křivka) a dalšími metodami Fig. 1. The graph shows spectrum of methods of surgical treatment of kidney tumours at Department of Urology Plzeň, CZ. A light blue curve shows the laparoscopic resections 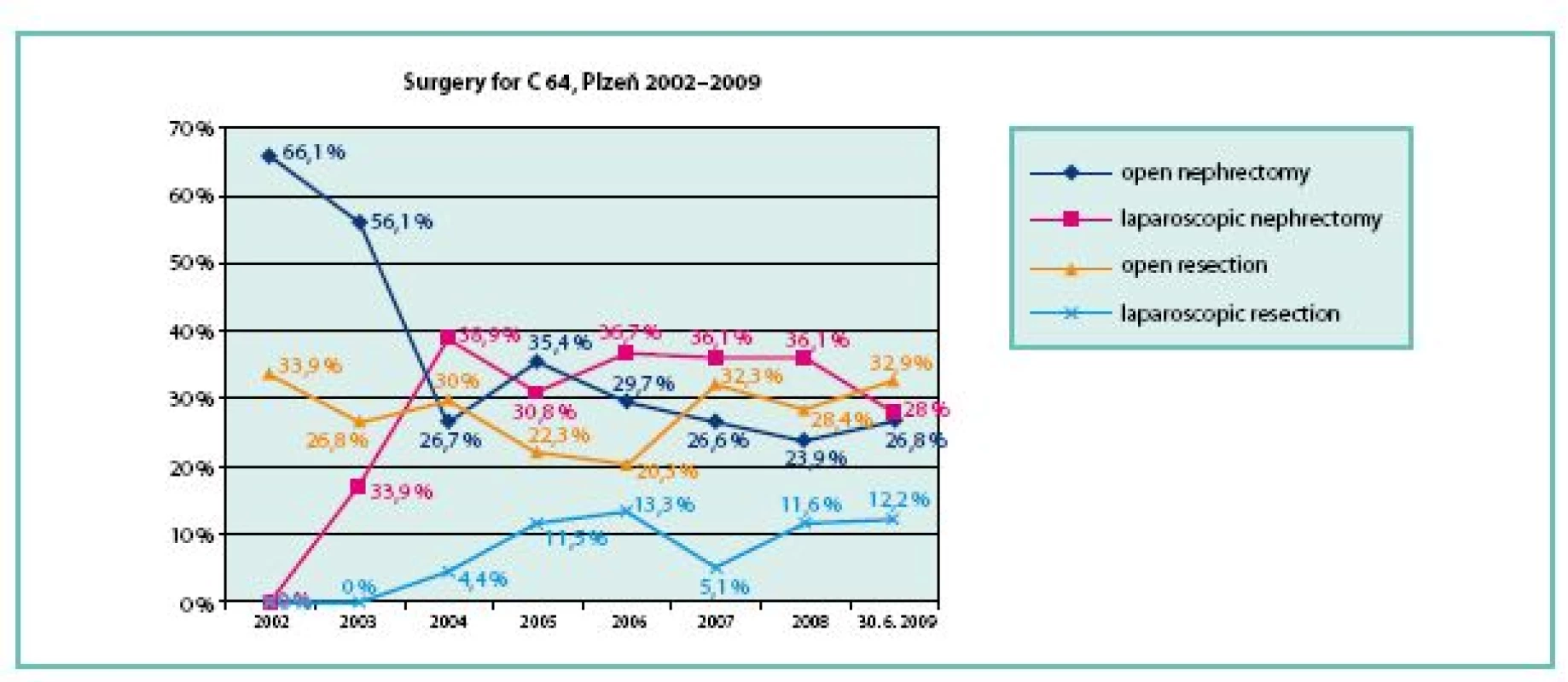
Image 2. Malá endosvorka užívaná ke klampování renální artérie s uzavíracím tlakem 450 g Fig. 2. Photo of the small endoscopic clamp for clamping of the renal artery with closing pressure 450 g 
Image 3. Cévní svorky zaváděné přes stěnu břišní (buď přímo, či přes flexibilní trokar). Umožňují klampovat hilus en bloc se snadným ovládáním. Fig. 3. The big clamp for clamping of renal hilum en bloc. Clamp is introduced in abdominal cavity straight or through flexible trocar 
Image 4. Aplikátor pro trombinové lepidlo FloSeal<sup>®</sup> Fig. 4. The applicator for thrombin sealant FloSeal<sup>®</sup> 
Image 5. A, B. CT a fotografie z laparoskopie ukazují extrarenálně rostoucí papilární renální karcinom, který byl řešen bez kampování renálních cév Fig. 5A, B. CT and peroperative photo show extrarenally growing papillary renal cell carcinoma, which was treated without camping of renal vessels 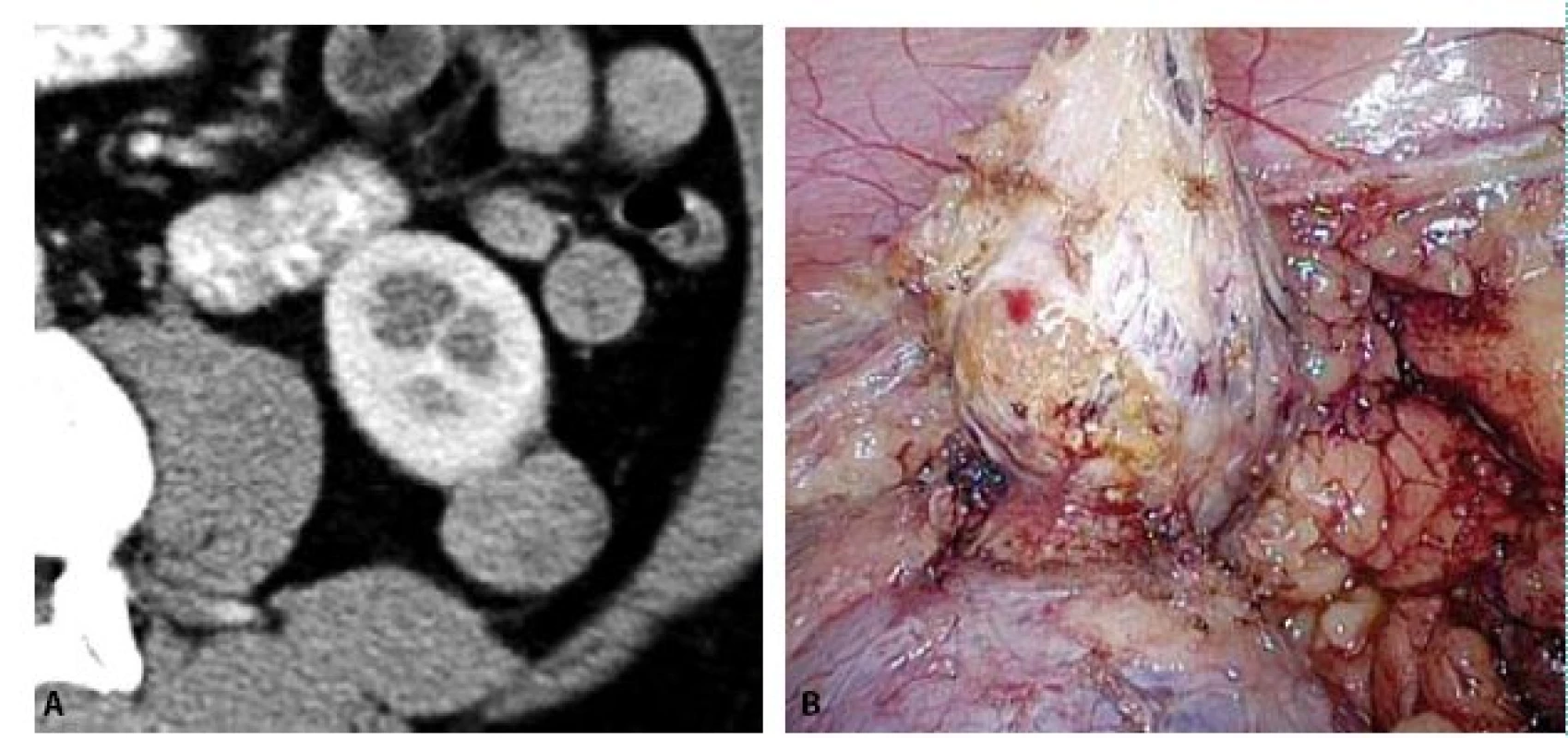
Vlastní výsledky
Od roku 2004 do června 2009 jsme provedli 73 LR. Nedávno jsme naše výsledky – prvních 62 LR včetně srovnání prvních 31 výkonů s druhou polovinou a srovnání LR se skupinou otevřených resekcí – publikovali (10, 11). Proto zde uvádíme jen základní data. Průměrný věk pacientů byl 61,9 ± 12,3 (25,6–83,0) let. Průměrná velikost tumoru byla 26 ± 11 (11–50) mm. Průměrný čas operace byl 110 ± 29 (50 až 180) minut. Průměrná doba klampování hilových cév byla 17,4 ± 9,6 (0–40) minut. Ve 34 případech byla klampována jen artérie (z toho 12× jen některá z jejich větví), 22× klampován hilus en bloc (většinou endosvorkami, 7× dlouhými cévními svorkami zavedenými před stěnu břišní buď přímo, či flexibilním portem). V osmi případech byla dvěma endosvorkami klampována selektivně tepna i žíla. V devíti případech byla provedena resekce bez klampování hilových cév. Průměrná krevní ztráta byla 184 ± 292 (0–1500) ml. Od 25. případu jsme používali místo intrakorporálního uzlení vstřebatelné PDS klipy (materiál polydioxanon, Absolok®, v literatuře označován jako LaproTy či Lahodny), od 63. případu Hem-olok ® Weck klipy s následným dotažením až po jejich nasazení na steh. Od 63. případu máme k dispozici argonový koagulátor, do té doby jsme používali koagulační lžičku s přístrojem nastaveným na modus spray. Trombinové lepidlo FloSeal® jsme mohli užívat od 25. případu (dříve nebyl v České republice k dispozici laparoskopický aplikátor) a celkem jsme jej aplikovali 10×. Tkanou celulózu (Surgicel®) používáme ve většině případů, i když ne jako polštářek, přes nějž jsou prováděny stehy (provedli jsme 2×), ale pouze jej přikládáme na resekční plochu po ukončení sutury. Při resekci bez klampování hilu často používáme techniku s jemným bipolárním disektorem, který za postupného pálení pomalu uzavíráme a vlastně jím řežeme ledvinný parenchym.
Diskuse
V rámci předoperačních vyšetření jednoznačně preferujme provedení multidetektorového spirálního CT, které umožňuje dvoufázovou CT angiografii (12). Důležité je, aby se podařilo radiologovi zachytit v jedné fázi zobrazenou artérii i vénu zároveň. To umožní udělat si obrázek o cévním zásobení, což je nesmírně důležité při klampování renálních cév (13).
Stále není jednoznačně určen ideální přístup při LR tumorů ledvin. Samozřejmě lze při LR užít oba obecně známé přístupy – transperitoneální či retroperitoneální. V literatuře lze nalézt řadu důvodů proč užívat ten či onen přístup. Většina pracovišť preferuje přístup laparoskopický a retroperitoneoskopický si ponechává pro dorzálně uložené tumory. Některá pracoviště ale i dorzálně uložené tumory řeší transperitoneálně, přičemž si ledvinu celou uvolní a překlopí. Náš přístup je ale dle možností vždy transperitoneální. Je tam více prostoru, což je zejména pro suturu důležité. U dorzálně uložených tumorů užíváme buď zmíněnou technikou překlopení, či častěji dáváme přednost přístupu otevřenému. Také tumory horního pólu ledviny indikujeme spíše k otevřené resekci.
K rychlému a bezkrevnému otevření zadního peritonea, Gerotovy fascie a uvolnění ledviny včetně hilových cév lze z moderních přístrojů užít harmonický skalpel či Ligasure® s nástrojem Advance®. Jako první preparujeme vždy nádor, abychom si ověřili, že se jedná o tumor. Několikrát se stalo, že se jednalo pouze o zkalenou cystu; zde samozřejmě stačí jen ablace a preparace cév by byla nadbytečná. Při preparaci cév používáme nejčastěji jednoduchou metodiku – háček s koagulačním proudem. Tkáň kolem cév se podebere a za kombinace jemného tahu a koagulace se bezkrevně přeruší.
Řada pracovišť k verifikaci tumoru užívá peroperační sonografii. U nás indikujeme vždy alespoň částečně extrarenálně uložené tumory, velmi dobře vizuálně patrné, takže potřebu peroperační sonografie necítíme. Peroperační sonografii užíváme pouze u intrarenálně uložených tumorů, které ale řešíme výhradně otevřenou resekcí. Někteří autoři si označují pomocí sonografu i linii resekce, ale nespatřujeme v tom výhodu.
Následuje zaklampování renálních cév. Metody jsou v zásadě dvě: pomocí intrakorporálních či extrakorporálních cévních svorek. Janetschek (5) dává před intrakorporálními svorkami přednost gumovým turniketům značeným barevně (červeně a modře na artérii, resp. na žílu). Je-li to technicky možné a tumor nezasahuje příliš hluboko, klampujeme pomocí intrakorporální cévní svorky pouze artérii či jen její větev (14). Hemostáza bývá dostatečná, lehce se zkrátí doba ischémie o dobu potřebnou k uzavírání a uvolňování žily a hlavně se sníží nebezpečí poranění žíly, která je díky své tenké stěně náchylná na trauma. Je-li vhodné klampovat i žílu, dáváme přednost klampování opět selektivně pomocí dvou intrakorporálních svorek. U intrakorporálních svorek používáme novější zdokonalenou sadu od firmy Aesculap se zdokonaleným aplikátorem. Není-li to technicky možné, poté se dle aktuální situace rozhodujeme pro intrakorporální či extrakorporální klampování en bloc. Extrakorporální svorku užíváme obecně zejména u širších komplexnějších hilů a tam, kde se nám nedaří dostatečně vypreparovat tkáň kolem hilových cév. Extrakorporální svorku zavádíme většinou přímo přes stěnu břišní, jen výjimečně pomocí speciálního flexibilního trokáru. Manitol ani furosemid při resekci ledviny nepoužíváme, neboť jsme v literatuře nenašli žádný důkaz o efektivitě těchto preparátů ke snížení následků ischémie. Je popsána možnost klampování vlastního parenchymu ledvinu pomocí velkých svorek (15), sami jsme tuto variantu nikdy nevyužili.
Bylo popsáno několik metod ke chlazení ledviny během resekce. Buď obalení ledviny do ledové tříště, nebo laváž ledviny chladným roztokem katétrem zavedeným z třísla do renální artérie, laváž dutého systému chladným roztokem uretrálním katétrem zavedeným endoskopicky, přičemž roztok odtéká do ureteru zavedeným zavaděčem pro flexibilní ureteroskopii (16). Autoři těchto metod je doporučují zejména u komplexních tumorů, tedy u složitých resekcí. V recentní literatuře ale žádná pracoviště metodiky nezmiňuje. Sami u komplexních tumorů dáváme přednost otevřené resekci, takže necítíme potřebu zvládnout metodiky chlazení.
Po provedení resekce lze ošetřit spodinu koagulací z důvodů onkologických a z důvodů hemostázy. Dříve jsme užívali koagulační „lžičku s modem spray, čímž jsme omezovali adherenci tkáně. Od loňského roku užíváme argonový koagulátor, který koaguluje spodinu bezkontaktně a u něhož nedochází k adherenci tkáně s jejím následným odtržením. Koagulaci rozhodně nepoužíváme standardně. Indikujeme ji, je-li linie resekce těsně u nádoru (zde z onkologických důvodů) anebo u parenchymu, předpokládáme - li, že nebude možná dokonalá sutura. Nepoužíváme ji, když jsou na spodině resekce velké cévy či otevřený dutý systém.
Následuje sutura resekce vstřebatelným materiálem polyglactinem. Dřívější technika sutury byla pomocí intrakorporálního uzlení. Steh byl nasazen a zauzlen. Dříve jsme používali jednotlivé stehy. Později jsme používali pokračující steh, který jsme zauzlili znovu na závěr. Dalším vývojem bylo využití na začátku a na konci sutury vstřebatelných PDS klipů místo uzlení. Vstřebatelné PDS klipy lze bez obav užít i k sutuře dutého systému. V další fázi jsme užívali PDS klipy i k průběžnému zajištění sutury – steh protažený parenchymem a dotažený byl následně zajištěn PDS klipem. Od podzimu 2008 užíváme techniku, která byla popsána v roce 2007 (17) a byla zpopularizována urology provádějící resekce pomocí robotického systému da Vinci. Stehy jsou zajišťovány jak v místě vpichu (zde se dotahují klipy sami), tak v místě vypíchnutí stehu Hemo - Lok® Weck klipy. V místě vypíchnutí jehly je na steh naložen Weck klip a ten je grasperem dotažen po vláknu (nataženým jehelcem) kolmo k parenchymu pomocí zmíněného grasperu. Benway et al. (18) užívají jednotlivé stehy, které lze ještě později dotáhnout, a navíc Weck klipy zajišťují ještě s PDS klipy. Rutinně užíváme suturu ve dvou vrstvách. V první vrstvě se provede sutura cév spodiny s eventuálním uzavřením otevřeného dutého systému a ve druhé vrstvě k sobě stáhneme okraje resekované ledviny. Hodně autorů před druhou vrstvou rutinně aplikuje trombinové lepidlo FloSeal® a přikládá smotanou tkanou celulózu Surgicel ®. Využití lepidel při resekcích ledvin jsme nedávno publikovali v přehledném článku (19) i ve videomonografii (20). Sami ale většinou provádíme rovnou suturu bez lepidel či celulózy. Je to rychlejší a levnější. Variantu s lepidlem a celulózou ponecháváme jen u defektů, kde předpokládáme, že okraje ledviny nebude možné k sobě dobře adaptovat. I technika sutury má ale své varianty. Lze provést i ošetření pouze spodiny resekce u centrálních tumorů (zašití dutého systému a obšití cév, na parenchym se poté aplikuje trombinové lepidlo Flo - Seal® a po kompresi 3 minut přes Surgicel se uvolní hilové cévy (4). Metodikou se zkrátí čas resekce. Nedávno byla popsána další metodika sutury vedoucí ke zkrácení doby ischémie (21). Provede se při zaklampovaném hilu pouze sutura první vrstvy, jíž jsou ošetřeny všechny větší cévy, poté se uvolní hilové cévy a sutura okrajů resekovaného parenchymu se provádí již na perfundované ledvině.
Během let byla snaha využít aplikace tepelné ablace, zejména ve formě radiofrekvence na spodinu tumoru, což umožní následnou resekci tumoru bez klampování hilových cév. I v případě pozitivních okrajů, a tedy inkompletní resekce, lze předpokládat, že reziduální tumor byl ošetřen radiofrekvencí (22). Výhoda techniky spočívá v tom, že není nutné klampovat hilus a není nutná intrakorporální sutura. U tumorů jdoucích až k dutému systému bychom se ale obávali vzniku urinózní píštěle (23, 24), takže lze zvažovat spíše periferní tumory exofytické tumory, kde je pro zkušeného laparoskopistu standardní provedení LR poměrně jednoduché. Technika zatím nenašla širšího uplatnění a sami s ní nemáme žádné zkušenosti.
Po ukončení výkonu provádíme rekonstrukci obalů ledviny. Buď pomocí pokračujícího polyglaktinového stehu, který je kotven vstřebatelnými PDS klipy, nebo rychlejší metodou, kdy se obaly ledviny k sobě přiblíží a secvaknou se s Hem-o-lok® Weck klipy velikosti L, které jsou schopné mezi své čelisti zavzít i Gerotovu fascii, tukové pouzdro i peritoneum. Drén zavádíme laterálním portem. Tuhý Redonův drén s tvarovou pamětí je nevhodný, neboť se v dutině břišní ve většině případů stočí mezi kličky střevní a přestane plnit svoji úlohu. Bylo by nutné užívat speciální Redonovy drény s měkkým plochým koncem. Sami dáváme přednost měkkému páskovému kapilárnímu drénu, který odvádí sekret a krev pouhým vzlínáním.
Recentně se objevují články o provedení laparoskopické resekce z přístupu jedním portem (25). Tyto techniky snižují sice invazivitu, ale snížení invazivity je oproti portům 5 mm diskutabilní a výkon se stává technicky výrazně obtížnější. Do rutinní praxe zatím nelze doporučit. Diskuse se vedou nyní o robotické resekci. Robot usnadňuje přístup i k tumorům horního pólu ledviny a sutura je jednodušší, doba výuky (angl. learning curve) je kratší, nevýhodou je samozřejmě cena výkonu a delikátní operace s hilovými cévami (nasazení a sejmutí cévních svorek musí provádět asistent nikoliv operatér) (26–28). Diskuse na toto téma jistě bude delší dobu pokračovat, nicméně lze předpokládat, že roboticky asistovaná LR bude nadále expandovat.
Práce byla podpořena výzkumným záměrem MSM 0021620819.
Došlo: 7. 7. 2009.
Přijato: 30. 7. 2009.
Kontaktní adresa
doc. MUDr. Milan Hora, Ph.D.
Urologická klinika LF UK a FN Plzeň
E. Beneše 13,
305 99 Plzeň
e-mail: horam@fnplzen.cz
Sources
1. Novotvary ČR. Praha: ÚZIS 2009; 256.
2. McDougall EM, Elbahnasy AM, Clayman RV. Laparoscopic wedge resection and partial nephrectomy – the Washington University experience and review of the literature. J Soc Laparoendosc Surg 1998; 2 : 15–23.
3. Zorn KC, Gong EM, Mendiola FP, Mikhail AA, Orvieto MA, Gofrit ON, Steinberg GD, Shalhav AL. Operative Outcomes of Upper Pole Laparoscopic Partial Nephrectomy: Comparison of Lower Pole Laparoscopic and Upper Pole Open Partial Nephrectomy. Urology 2007; 70 : 28–34.
4. Weight CJ, Lane BR, Gill IS. Laparoscopic partial nephrectomy for selected central tumours: omitting the bolster. BJU Int 2007; 100 : 375–378.
5. Lattouf J-B, Beri A, D’Ambros OFJ, Grüll M, Leeb K, Janetschek G. Laparoscopic Partial Nephrectomy for Hilar Tumors: Technique and Results. Eur Urol 2008; 54 : 409–418.
6. Richstone L, Montan S, Ost M, Reggio E, Permpongkosol S, Kavoussi LR. Laparoscopic Partial Nephrectomy for Hilar Tumors: Evaluation of Short-Term Oncologic Outcome. Urology 2008; 71 : 36–40.
7. Simmons MN, Chung I, Gill IS. Perioperative efficacy of laparoscopic partial nephrectomy for tumors larger than 4 cm. Eur Urol 2009; 55 : 199–208.
8. Ukimura O, Haber GP, Remer EM, et al. Laparoscopic partial nephrectomy for incidental stage pT2 or worse tumors. Urology 2006; 68 : 976–982.
9. Turna B, Aron M, Gill IS. Expanding Indications for Laparoscopic Partial Nephrectomy. Urology 2008; 72 : 481–487.
10. Hora M, Ürge T, Eret V, Stránský P, Klečka J jr, Hes O, Ferda J, Chudáček Z, Michal M. Laparoskopická resekce nádorů ledvin, Edukační sborník. XXXIII. brněnské onkologické dny 2009; 303–304.
11. Hora M, Eret V, Ürge T, Stránský P, Klečka J jr, Hes O, Michal M, Chudáček Z, Ferda J. Results of laparoscopic resection of kidney tumour in everyday clinical practice. Central European Journal of Urology 2009; 62(3): 160–166.
12. Ferda J, Hora M, Hes O, Ferdová E, Kreuzberg B. Assessment of the kidney tumor vascular supply by two-phase MDCT-angiography. Eur J Radiol 2007; 62 : 295–301.
13. Hora M, Ferda J, Kreuzberg B, Klečka J, Hes O, Chudáček Z. Využití dvoufázové CT-angiografie při chirurgické léčbě nádorů ledvin. Čes Urol 2005; 9 : 14–19.
14. Gong EM, Zorn KC, Orvieto MA, Lucioni A, Msezane LP, Shalhav AL. Artery - Only Occlusion May Provide Superior Renal Preservation During Laparoscopic Partial Nephrectomy. Urology 2008; 72 : 843–846.
15. Verhoest G, Manunta A, Bensalah K, Vincendeau S, Rioux-Leclercq N, Guille F, Patard JJ. Laparoscopic Partial Nephrectomy with Clamping of the Renal Parenchyma: Initial Experience. Eur Urol 2007; 52 : 1340–1346.
16. Hora M, Klečka J, Ürge T, Ferda J, Hes O, Eret V. Laparoskopická resekce tumorů ledvin. Čes Urol 2006; 10 : 32–39.
17. Canales BK, Lunch AC, Fernandes E, Anderson JK, Ramani AP. Novel Technique of Knotless Hemostatic Renal Parenchymal Suture Repair During Laparoscopic Partial Nephrectomy. Urology 2007; 70 : 358–359.
18. Benway BM, Wang AJ, Cabello JM, Bhayani SM. Robotic partial nephrectomy with sliding–clip renorrhaphy: Technique and outcomes. Eur Urol 2009; 55 : 592 – 599.
19. Hora M, Eret V, Ürge T, Klečka J. Možnosti využití tkáňových lepidel při ledvinu šetřících výkonech u tumorů ledvin. Čes Urol 2007; 11 : 147–153.
20. Hora M, Eret V, Klečka J, Stránský P, Ürge T, Hes O, Chudáček Z, Ferda J. Využití tkáňových lepidel při resekcích ledvin. Praha: Galén 2008; DVD – 6 videí a článek 7 s.
21. Baumert H, Ballaro A, Shah N, Mansouri D, Zafar N, Molinie V, Neal D. Reducing Warm Ischaemia Time During Laparoscopic Partial Nephrectomy: A Prospective Comparison of Two Renal Closure Techniques. Eur Urol 2007; 52 : 1164–1169.
22. Zeltser IS, Moonat S, Park S, Anderson JK, Cadeddu JA. Intermediate-term prospective results of radiofrequency-assisted laparoscopic partial nephrectomy: a non-ischaemic coagulative technique. BJU Int 2007; 101 : 36–38.
23. Eret V, Hora M, Sýkora R, Hes O, Ürge T, Klečka J, Matějovič M. GreenLight (532 nm) laser partial nephrectomy followed by the suture of the collecting system without renal hilar clamping in a porcine model. Urology 2009; 73 : 1115–1118.
24. Zeltser IS, Gusta A, Bensalah K, Kabbani W, Jenkins A, Part S, Perle MS, Cadeddu J. Focal radiofrequency coagulation-assisted laparoscopic partial nephrectomy: a novel nonischemic technique. J Endourol 2008; 22 : 1269–1273.
25. Aron M, Canes D, Desai MM, Haber GP, Kaouk JH, Gill IS. Transumbilical single-port laparoscopic partial nephrectomy. BJU Int 2008; 103 : 516–521.
26. Aron M, Kleniv P, Kaouk JH, Nguyen MM, Desai MM, Gill IS. Robotic and laparoscopic partial nephrectomy: a matched-pair comparison from a high-volume Centre. BJU Int 2008; 102 : 86–92.
27. Deane LA, Lee HJ, Box GN, Melamud O, Yee DS, Abraham JB, Finley DS, Borin JFM, McDougall EM, Clayman RV, Ornstein DK. Robotic versus standard laparoscopic partial/wedge nephrectomy: a comparison of intraoperative and perioperative results from a single institution. J Endourol 2008; 22 : 947–952.
28. Wang AJ, Bhyani SB. Robotic partial nephrectomy versus laparoscopic partial nephrectomy for renal cell carcinoma: single-surgeon analysis of > 100 consecutive procedures. Urology 2009; 73 : 306–310.
Labels
Paediatric urologist Nephrology Urology
Article was published inCzech Urology

2010 Issue 1-
All articles in this issue
- Incidence, diagnostika a léčba karcinomu prostaty u HIV pozitivních pacientů
- Evoluce operační techniky laparoskopické resekce nádorů ledvin
- Laparoskopická nefropexe – technika pomocí tří nevstřebatelných stehů
- Exprese DD3PCA3 (Differential Display Code 3) mRNA ve tkáni prostaty u pacientů s karcinomem prostaty a benigní hyperplazií prostaty
- Agresivní karcinom prostaty u pacientů s nízkým PSA
- Anatomické aspekty chirurgické konverze pohlaví u pacientek s male-to-female transsexualismem – výsledky hodnocené tři měsíce po výkonu
- Pheochromocytoma and paraganglioma syndromes: going on 2010
- Czech Urology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Agresivní karcinom prostaty u pacientů s nízkým PSA
- Anatomické aspekty chirurgické konverze pohlaví u pacientek s male-to-female transsexualismem – výsledky hodnocené tři měsíce po výkonu
- Laparoskopická nefropexe – technika pomocí tří nevstřebatelných stehů
- Incidence, diagnostika a léčba karcinomu prostaty u HIV pozitivních pacientů
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

