-
Medical journals
- Career
Kryptorchizmus – potreba včasnej diagnostiky a liečby
Authors: M. Michalisko; M. Vidiščák; E. Dobríková; J. Novotný; R. Koreň; E. Murár
Authors‘ workplace: Klinika detskej chirurgie SZU, Detská fakultná nemocnica s poliklinikou, Banská Bystrica prednosta prof. MUDr. M. Vidiščák, PhD., FEBPS
Published in: Čes-slov Pediat 2014; 69 (1): 29-38.
Category: Reviews
Overview
Kryptorchizmus je najčastejšia vrodená chyba mužských pohlavných orgánov znamenajúca neprítomnosť semenníkov v skróte. Pri narodení má približne 5 % donosených novorodencov nezostúpený semenník, vo veku 12 mesiacov je to už len 1 %. Keďže v 6. mesiaci dochádza k znižovaniu počtu zárodočných buniek a spontánny zostup po tomto období je vzácny, liečba kryptorchizmu už môže začať v tomto období a mala by byť ukončená do veku 18 mesiacov. Pri hmatnom semenníku je indikovaná operačná liečba – orchidopexia z inguinálneho prístupu, pri nehmatnom semenníku je indikovaná diagnostická laparoskopia – pri náleze nízko uloženého intraabdominálneho semenníka je možná jednodobá orchidopexia bez prerušenia testikulárnych ciev, pri vysoko uloženom intraabdominálnom semenníku sa pokračuje jednodobou alebo dvojdobou orchidopexiou s prerušením testikulárnych ciev.
V súčasnosti získava v liečbe kryptorchizmu význam adjuvantná hormonálna liečba k operačnej liečbe, ktorá môže zlepšiť fertilitu. Hormonálna liečba je však stále kontroverzná a aj napriek pozitívnemu vplyvu na fertilitu má mnoho odporcov a zatiaľ nie je štandardnou liečbou kryptorchizmu.Kľúčové slová:
kryptorchizmus, dôsledky kryptorchizmu, liečba kryptorchizmuÚvod
Termín kryptorchizmus je gréckeho pôvodu, „kryptos“ znamená skrytý a „orchis“ znamená semenník. Retencia znamená zastavenie zostupu semenníka v jeho normálnej dráhe. Termín kryptorchizmus je širší, pretože zahrňuje aj ektopiu semenníka a anorchiu [1]. Nezostúpený semenník sa vyskytuje u 3,4–5,8 % donosených novorodencov, k spontánnemu zostupu dochádza v prvých šiestich mesiacoch života – v tomto období má retinovaný semenník ešte približne 0,8 % donosených a 10 % nedonosených chlapcov. Medzi nedonosenými chlapcami je incidencia výrazne vyššia – 9 až 30 % nedonosených chlapcov má nezostúpený semenník. Novorodenci s pôrodnou hmotnosťou nižšou ako 900 g majú takmer 100% incidenciu nezostúpeného semenníka, táto incidencia klesá pri stúpajúcej pôrodnej hmotnosti. Niektorí autori uvádzajú zvýšenú prevalenciu nezostúpeného semenníka u prepubertálnych chlapcov (až 7 %), čo môže byť spôsobené vzostupom semenníkov, predtým nerozpoznaným nezostúpeným semenníkom pri vysokej skrotálnej alebo inguinálnej polohe a retraktilným semenníkom, u ktorého došlo k neskoršiemu vzostupu [2]. V 72 % je retencia inguinálna, v 20 % preskrotálna a v 8 % abdominálna [1]. Nezostúpené semenníky sa častejšie vyskytujú pri hypospádiách, zníženej virilizácii a iných endokrinných poruchách [3].
Výskyt anomálií horných močových ciest nie je zvýšený. Pri kombinácii hypospádie a retencie s hmatnými semenníkmi je asi 15% riziko a pri nehmatných semenníkoch 50%, že sa jedná o poruchu vývoja pohlavia. S retenciou semenníkov môžu byť spojené viaceré ťažké vrodené chyby ako napríklad chromozomálne aberácie a defekty brušnej steny (omfalokéla, gastroschíza, prune-belly syndróm) [1].
Zostup semenníkov a vývoj zarodočných buniek
Zostup semenníkov začína približne v 10. týždni tehotenstva, krátko po začatí sexuálnej diferenciácie. Počas prvej fázy zostupu, ktorá prebieha v 10.–15. týždni gestácie, dochádza u mužského pohlavia k zhrubnutiu kaudálneho konca genito-inguinálneho ligamenta (gubernakula). Kaudálny koniec gubernakula upevňuje semenník v blízkosti inguinálnej oblasti počas rastu brušnej dutiny embrya, čím zabraňuje vzdialeniu sa semenníka z inguinálnej oblasti. Dochádza tak k relatívnemu zostupu semenníka v porovnaní s ováriom u ženského pohlavia. V druhej fáze zostupu, medzi 25.–35. týždňom gestácie, dochádza k migrácii kaudálnej časti gubernakula z inguinálneho kanála do skróta, čím gubernakulum sťahuje semenník do skróta [4].
Vývoj zárodočných buniek a endokrinnej činnosti semenníkov začína počas 7. gastačného týždňa a pokračuje do dospelosti. Konečným zmenám dozrievania v puberte predchádzajú štyri stupne dozrievania zárodočných buniek (dva prenatálne a dva postnatálne). V prvom stupni dochádza k diferenciácii primordiálnych zárodočných buniek na gonocyty. Pôsobením hCG dochádza k vývoju fetálnych Leydigových buniek, ich proliferácii a k sekrécii testosterónu. V druhom stupni dochádza k diferenciácii gonocytov na fetálne spermatogónie. Počas tohto obdobia, približne v 13. gestačnom týždni, dosahujú vrchol hladiny hCG, testosterónu a počet Leydigových fetálnych buniek.
Tretí stupeň dozrievania prebieha postnatálne, približne v druhom mesiaci po narodení. Vzostup hladín LH a FSH stimuluje proliferáciu fetálnych Leydigových buniek, čo spôsobí vzostup hladiny testosterónu. Dochádza k apoptóze väčšiny zárodočných buniek, kým menší počet zárodočných buniek sa transformuje na dospelé tmavé spermatogónie – adult dark (Ad) spermatogónie. Transformácia a apoptóza zárodočných buniek je ukončená v šiestom mesiaci života. Štvrtý stupeň dozrievania prebieha v 5. roku života. Pôsobením testosterónu dochádza k zvýšeniu počtu Ad spermatogónií a ich transformácii na primárne spermatocyty. Semenník následne pretrváva v pokojovom štádiu, až kým v puberte začnú prebiehať záverečné kroky spermatogenézy.
Konečné dozrievanie zárodočných buniek v puberte závisí od dostatočného ukončenia dvoch prepubertálnych stupňov. V puberte dochádza k vzostupu hladín LH a FSH, ktoré stimulujú množenie a dozrievanie neaktívnych juvenilných Leydigových buniek na dospelé Leydigové bunky. Tie následne produkujú vysoké hladiny testosterónu, ktoré spúšťajú záverečné kroky maturácie spermatocytov na spermie. Spermatogenéza je dokončená v 13.–15. roku života [2]. Súčasne prebieha vývoj Sertoliho buniek. Fetálne Sertoliho bunky sa vyvíjajú v 7. gestačnom týždni, po narodení sa transformujú na Sa a Sb podtypy a Sc podtypy v období puberty. Celkový počet Sertoliho buniek sa rovnomerne znižuje od narodenia po pubertu.
Porucha vývoja zárodočných buniek u pacientov s kryptorchizmom je výsledkom zlyhania dvoch dôležitých krokov dozrievania buniek po narodení. Najskôr dochádza k oneskoreniu prvej postnatálnej transformácie, čo sa prejavuje pretrvávaním prítomnosti gonocytov aj po 6. mesiaci a znížením počtu Ad spermatogónií. Prítomné spermatogónie sú prevažne fetálne a majú bizarný tvar jadier, čím je ovplyvnená kvalita a kvantita spermatogónií. Následne dochádza k zlyhaniu druhého kroku transformácie Ad spermatogónií na primárne spermatocyty. Počet Leydigovych buniek je výrazne znížený, dochádza tak k poklesu normálneho zvýšeného vyplavenia testosterónu, ktoré je prítomné vo veku 2–3 mesiacov. Taktiež je porušená transformácia Sertoliho buniek, dochádza k skorej strate fetálnych Sertoliho buniek a v puberte iba k čiastočnej transformácii Sa na Sc. Tieto zmeny spôsobujú zníženú fertilitu a obnovenie normálneho vývoja zárodočných buniek po včasnej orchidopexii stále nemusí mať za následok normálny spermiogram [5].
Klasifikácia
Pacienti s kryptorchizmom sa delia na pacientov s hmatným semenníkom (retinovaným, ektopickým a retraktilným) a na pacientov s nehmatným semenníkom (intraabdominálna retencia, prípadne ektopia a anorchia). Ďalšiu skupinu tvoria pacienti so vzostúpeným semenníkom. Nezostúpený (retinovaný) semenník je taký, ktorý sa zastaví v dráhe svojho fyziologického zostupu. Podľa polohy sa delí na supraskrotálny, inguinuálny a abdominálny [1]. Objemovo je menší, často je prítomné aj hypoplastické skrótum a má histologické známky kryptorchizmu [3]. Ektopický semenník je taký, ktorý odbočí z dráhy svojho fyziologického zostupu. Môže byť uložený laterálne od vonkajšieho anulu, v oblasti perinea, pri koreni penisu, v druhej polovici skróta, femorálne alebo intraabdominálne. Pri retraktilnom semenníku sa nejedná o retenciu. Semenník je vyťahovaný zvýšenou aktivitou musculus cremaster mimo skrótum. Možno ho stiahnúť do skróta, kde zostáva až do doby, kým nie je ťahom svalov vytiahnutý nahor [1]. Retraktilný semenník je potrebné kontrolovať raz ročne počas detstva, keďže môže nastať jeho vzostup [6]. Polyorchizmus je stav, keď dôjde k rozdeleniu základu semenníka a následnej duplikácii na jednej strane. Skrížená dystopia je stav, pri ktorom nachádzame na jednej strane dva semenníky, z ktorých každý má svoje vlastné cievne zásobenie, pričom na druhej strane semenník chýba [7]. Od retinovaného semenníka je dôležité odlíšiť retraktilný semenník, ktorý nevyžaduje liečbu, ektopický semenník, inkarcerovanú inguinálnu herniu, inguinálnu lymfadenopatiu a hydrokélu spermatického povrazca [7, 8].
Približne 15–20 % nezostúpených semenníkov je nehmatných. Ak semenník chýba, jedná sa buď o primárnu anorchiu pre poruchu vývoja, alebo o sekundárnu anorchiu, ktorá vzniká na podklade poruchy krvného zásobenia pred pôrodom, napr. torzia testis [3]. Vzostúpený semenník je taký, ktorý sa nachádzal v skróte, zmenil svoju polohu a je trvalo uložený mimo skrótum, buď primárne alebo sekundárne [9]. Primárne k tomu dochádza pri poruche proporciálnej elongácie spermatického povrazca, keď je semenník progresívne retrahovaný zo skróta pri raste. Častejšie však dochádza k iatrogénnemu sekundárnemu vzostupu semenníka, keď je funikulus prichytený k fascii jazvou po operácii v slabine a následne je rastom vytiahnutý zo skróta [3]. Liečba vzostúpeného semenníka je potrebná, pretože dochádza k histologickým zmenám a k zmenám hodnôt spermiogramu vplyvom zvýšenej teploty v inguinálnom kanáli [9].
Table 1. Klasifikácia nezostúpených semenníkov. 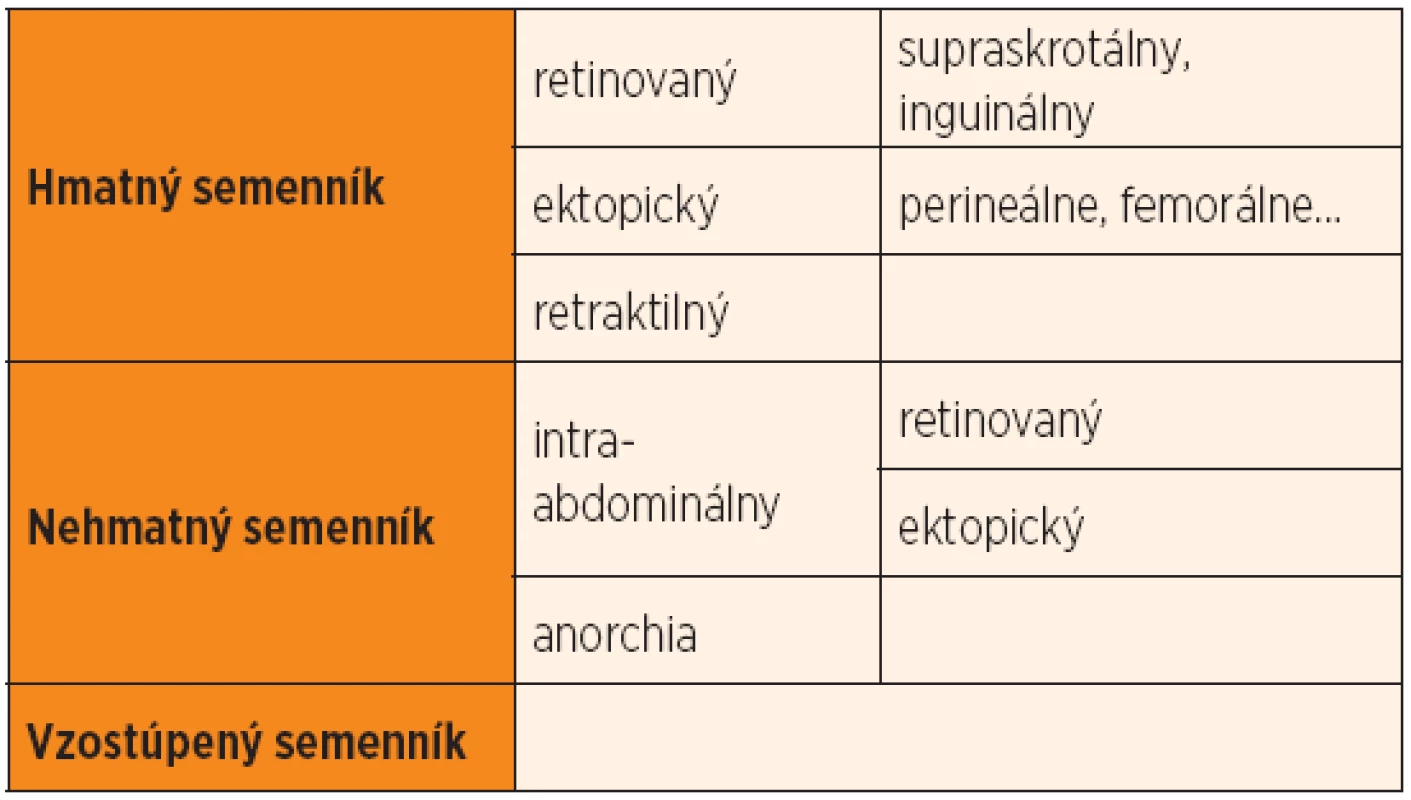
Diagnostika
V anamnéze pacienta s kryptorchizmom zisťujeme prípadný predčasný pôrod, expozíciu alebo užívanie exogénnych hormónov (estrogénov) matkou, predošlú operáciu v oblasti inguíny, rodinnú anamnézu kryptorchizmu, prípadne iných vrodených anomálií, predčasnú pubertu, neplodnosť a konsangvinitu. Je dôležité vedieť, či semenníky boli hmatné v skróte pri narodení alebo počas prvého roka života. Retrakcia semenníka je najčastejšia medzi 4.–6. rokom života pre silný kremasterový reflex [2]. Môže dôjsť k vzostupu pôvodne retraktilného semenníka mimo skrótum, čím sa stane retinovaným.
Pre správnu diagnózu nezostúpeného semenníka je rozhodujúce fyzikálne vyšetrenie – vyšetrujeme v pokoji, teplými rukami. Vyšetrujeme celý genitál, pátrame po hypospádii, hypoplázii skróta a penisu [1]. Vyšetrenie sa robí v ľahu bimanuálnou palpáciou, semenník sa snažíme jemne vytlačiť z podbruška kaudálnym smerom v smere inguinálneho kanála proti prstom druhej ruky. Tiež je potrebné skontrolovať miesta možnej ektopie. Ďalej vyšetrujeme pacienta v tureckom sede s miernym predklonom, pri ktorom pacient najlepšie povolí brušné svaly, čím môžeme zrušiť sťah svalu musculus cremaster. Jemnou manipuláciou sa snažíme semenník stiahnuť do skróta. Ak tam zostane, nejedná sa o nezostúpený semenník, ale o retraktilný semenník [10]. Na oslabenie sťahu musculus cremaster je potrebné nechať semenník stiahnutý v skróte na minútu – ak pri uvoľnení semenníka dôjde k jeho vytiahnutiu do preskrotálnej polohy, jedná sa o nezostúpený semenník, ak zostane v miešku, jedná sa o retraktilný semenník [2]. Lokalizáciu je potrebné zaznamenávať aj z dôvodu detekcie vzostúpeného semenníka, keďže vzostúpený semenník je najčastejšou príčinou neskorej diagnostiky kryptorchizmu. V prípade obojstranne nehmatného semenníka alebo jednostranného kryptorchizmu spojeného s hypospádiou je potrebné komplexné endokrinologické a genetické vyšetrenie, pretože tieto stavy poukazujú na poruchu sexuálnej diferenciácie [9].
Pri diagnostike nehmatných nezostúpených semenníkov je zlatým štandardom laparoskopia, počas ktorej môžeme určiť lokalizáciu a anatómiu semenníka, nadsemenníka, semenovodu a testikulárnych ciev. USG, CT a magnetická rezonancia nemajú dostatočnú senzitivitu a špecificitu, aby mohli byť považované za štandard diagnostiky [3, 9].
Dôsledky kryptorchizmu
Vplyv na fertilitu
Paternita u pacientov s liečeným jednostranným nezostúpeným semenníkom je takmer rovnaká ako v bežnej populácii, aj keď sú prítomné zmeny v spermiograme. Infertilita sa u týchto pacientov vyskytuje v 10 %, kým v bežnej populácii v 6 % [9]. Muži s obojstranným nezostúpeným semenníkom majú šesťnásobne vyššie riziko neplodnosti v porovnaní s mužmi s jednostranným nezostúpeným semenníkom a bežnou populáciou. Incidencia azospermie u mužov s jednostranným nezostúpeným semenníkom je 13 % bez ohľadu na to, či sa stav liečil alebo nie. U mužov s obojstranným nezostúpeným semenníkom, ktorí neboli liečení, sa vyvinula azospermia v 98 %. Riziko azospermie však klesá u tých, ktorí sa liečili medikamentózne, na 32 % a u tých, ktorí podstúpili orchidopexiu v detstve, na 46 %. Približne 10 % neplodných mužov má v anamnéze nezostúpený semenník alebo orchidopexiu [11].
Riziko vzniku nádorov semenníkov
Nádory semenníkov tvoria 1 % všetkých malignít, ale patria medzi najčastejšie nádory u mladých mužov [12]. Incidencia týchto tumorov sa zvyšuje, u mužov vo veku 15–40 rokov sú najčastejšou formou rakoviny. Relatívne riziko vzniku nádoru semenníkov u pacientov s nezostúpeným semenníkom je 5-krát vyššie ako u bežnej populácie [13]. Približne 10 % týchto nádorov je v pôvodne nezostúpených semenníkoch. Riziko je vyššie, čím je vyššia retencia semenníka – pri intraabdominálnej retencii je päťnásobne vyššie ako pri inguinálnej [1]. U pacientov, ktorým bola vykonaná orchidopexia do veku 6 rokov, je riziko vzniku nádoru semenníkov dvojnásobné ako u bežnej populácie, ak bola orchidopexia vykonaná vo veku nad 13 rokov, riziko je viac ako päťnásobné [14]. U pacientov s jednostranným nezostúpeným semenníkom je riziko nádoru v kontralaterálnom semenníku zvýšené, nie však do takej miery ako v nezostupenom semenníku [13].
Rutinná biopsia nezostupeného semenníka za účelom diagnostiky nádoru, prípadne prekancerózy nie je potrebná. U detí sa však doporučuje pravidelné vyšetrenie lekárom u všetkých pacientov s anamnézou kryptorchizmu, dospelých s anamnézou nezostúpeného semenníka je potrebné naučiť samovyšetreniu semenníkov, aby sa včas mohla zachytiť akákoľvek abnormalita [9]. Súčasný trend vykonávať orchidopexiu u pacientov v nižších vekových skupinách môže znížiť riziko vzniku nádorov semenníkov [13, 14].
Riziko torzie semenníka
Aj keď je iba málo dostatočných dôkazov, incidencia torzie je vyššia u nezostúpených semenníkov ako u normálne lokalizovaných skrotálnych semenníkov. Torzia nezostúpeného semenníka sa vyskytuje často pri testikulárnych tumoroch, pravdepodobne z dôvodu zvýšenej hmotnosti a zmeny normálneho tvaru postihnutého semenníka. Torzia semenníka sa môže prezentovať akútnym bruchom, preto je dôležité pri fyzikálnom vyšetrovaní pacienta s akútnym bruchom vyšetrovať aj semenníky [15].
Liečba
Hlavnými dôvodmi liečby kryptorchizmu sú zvýšená neplodnosť u pacientov s kryptorchizmom, zvýšené riziko malignity, torzie, poranenia semenníka a psychologické stigmy ako dôsledok prázdneho skróta. Stiahnutie semenníka do skróta je dôležité najmä preto, aby bol semenník lepšie prístupný pohmatu, čo môže včas odhaliť akékoľvek podozrenie na malignitu. Nepriaznivé dlhodobé následky kryptorchizmu sa vyskytujú aj napriek úspešnej liečbe [2]. Liečba nezostúpeného semenníka sa môže začať už po 6. mesiaci života, pretože spontánny zostup po tomto období je vzácny [3, 9, 10]. Pre vývoj histologických zmien by liečba mala byť ukončená najneskôr do 2. roku života, najlepšie však do veku 12–15 mesiacov. Znižovanie počtu zárodočných buniek začína už po 6. mesiaci života. V 1. roku života neboli zistené významné rozdiely v množstve spermatogónií v nezostúpených semenníkoch v porovnaní s normálnymi semenníkmi, postupne sú však rozdiely viditeľnejšie a v 2. roku života dochádza k úplnej strate zárodočných buniek u 38 % pacientov s kryptorchizmom. Histologický nález týkajúci sa počtu zárodočných buniek je pri skoršej operácii preto priaznivejší. Pre fertilitu má dôležitý význam stupeň maturácie gonocytov na Ad spermatogónie [8]. Nižšia teplota v skróte je dôležitá pre zachovanie spermatogónií a pre spermatogenézu, dokonca je spájaná s nižšou incidenciou neoplázie [3, 16].
Liečba závisí od toho, či je semenník hmatný alebo nehmatný – pri hmatnom semenníku je zlatým štandardom orchidopexia, pri nehmatnom semenníku diagnostická laparoskopia – pri náleze nízko uloženého intraabdominálneho semenníka je možná jednodobá orchidopexia bez prerušenia testikulárnych ciev, pri vysoko uloženom intrabdominálnom semenníku sa pokračuje jednodobou alebo dvojdobou orchidopexiou s prerušením testikulárnych ciev. Pri obojstrannom nehmatnom semenníku je dôležité genetické vyšetrenie a stimulačný hCG test. Injekčne sa podá jedná dávka hCG (100 IU/kg) – čo pri prítomnosti semenníkov vedie k zvýšeniu hladiny testosterónu v sére o 4–5 dní [2, 10]. Úspešnosť hormonálnej liečby (dosiahnutie skrotálnej lokalizácie bez známok atrofie) sa udáva v rozmedzí 8–60 %. Takéto vysoké rozdiely v úspešnosti hormonálnej liečby sú pripisované faktu, že niektorí autori zahrňujú do štúdií aj retraktilné semenníky. Z troch meta-analýz dostupných štúdií sa úspešnosť hormonálnej liečby udáva v 20 %, pri dlhodobom sledovaní však klesá na 15 % pre výskyt sekundárneho vzostupu semenníkov. V porovnaní s hormonálnou liečbou je úspešnosť primárnej chirurgickej liečby 95% [6]. Hormonálna liečba má veľmi obmedzené indikácie, získava však význam ako adjuvantná či neoadjuvantná liečba k operačnej liečbe [10]. Zdá sa, že podávanie hormonálnej liečby pri kryptorchizme je neúčinné v pôsobení na zostup semenníkov a môže indukovať ireverzibilné zmeny na semenníkoch, ako adjuvantná liečba LH-RH po orchidopexii však môže zlepšiť maturáciu zárodočných buniek a zvýšiť ich počet [5].
Hormonálna liečba
V hormonálnej liečbe sa používa ľudský choriový gonadotropín (hCG) alebo analógy gonadotropin-releasing hormónu (LH-RH). Čím je semenník uložený nižšie, tým je hormonálna liečba úspešnejšia. Nehmatný semenník sa po hormonálnej liečbe môže stať hmatným, ale aj tak môže vyžadovať ďalšiu operačnú liečbu. Semenník môže po určitej dobe po úspešnej hormonálnej liečbe vystúpiť do pôvodnej polohy, preto je potrebné pacientov liečených hormonálnou liečbou dlhodobo sledovať. Hormonálna liečba je kontraindikovaná pri predchádzajúcej operácii v inguinálnom kanáli, pri ektopickom semenníku a pri retencii s inguinálnou herniou [7, 10]. V roku 1930 bol hCG v liečbe použitý prvýkrát, používa sa vo forme intramuskulárnych injekcií a má podobný účinok na stimuláciu testosterónu ako LH [2, 5, 10]. Úspešnosť zostupu do skróta sa uvádza v rozmedzí 25–55 % v nekontrolovaných štúdiách, v randomizovaných je však iba 6–21 %.
Medzi nežiaduce účinky liečby hCG patria hyperpigmentácia genitálií, zvýšené pubické ochlpenie, rast penisu a zvýšená náchylnosť k erekciám – tieto príznaky sú však reverzibilné a po skončení liečby ustúpia [2, 10]. Lisá uvádza úspešný zostup semenníkov po aplikácii hCG 500–1000 j jedenkrát týždenne po dobu 3–6 týždňov u 68 % detí do veku 1,5 roka, u starších v 40 % [17]. Je však potrebné vyhnúť sa dávke vyššej ako 15 000 IU, keďže môže dôjsť k predčasnému uzáveru rastových štrbín, a tým k spomaleniu somatického rastu [2]. hCG taktiež zvyšuje apoptózu spermatogónií v ľudských semenníkoch [18]. Analógy LH-RH sa používajú od roku 1974 vo forme intranazálneho spreja. LH-RH stimuluje tvorbu LH v hypofýze, ktorý následne zvýši tvorbu testosterónu v Leydigových bunkách. Taktiež zvyšuje produkciu FSH v hypofýze, a tým stimuluje Sertoliho bunky. Štúdie biopsií semenníkov po liečbe LH-RH v posledných rokoch dokázali, že liečba LH-RH zvyšuje počet spermatogónií v seminiformnom kanáliku. Úspešnosť liečby s analógom LH-RH je v nekontrolovaných štúdiách v rozsahu 13–78 %, v kontrolovaných dosiahla hodnotu 6–38 % [2]. Medzi nežiaduce účinky liečby LH-RH patria virilizačné účinky a zvýšená excitabilita, virilizačné účinky sú v porovnaní s hCG nižšie [10].
Neoadjuvantná hormonálna liečba
Schwentner a kol. skúmali histopatologický index fertility u 42 pacientov v randomizovanej štúdii, kde bola pacientom podávaná neoadjuvantná liečba LH-RH vo forme nosového spreja v dávke 1,2 mg po dobu 4 týždňov, následne bola u pacientov vykonaná orchidopexia, kontrolná skupina pacientov podstúpila iba orchidopexiu. U oboch skupín bola počas operácie vykonaná biopsia. Dospeli k záveru, že index fertility bol u skupiny liečenej LH-RH signifikantne vyšší v porovnaní so skupinou bez hormonálnej stimulácie. Maximum aktívneho zárodočného tkaniva sa dosiahne pri liečbe kryptorchizmu pred skončením prvého roku života [19].
Adjuvantná hormonálna liečba
Liečbu analógom LH-RH po operácii podporuje dôkaz zníženého počtu Ad spermatogónií v seminiformných kanálikoch zo vzoriek semenníkov získaných biopsiou pri orchidopexii. Ak v biopsii operovaných semenníkov neboli Ad spermatogónie prítomné, pacienti mali abnormálny spermiogram aj napriek skorej orchidopexii. Transformácia gonocytov na Ad spermatogónie sa tak javí ako kľúčová pre mužskú plodnosť. Hlavnou príčinou abnormálneho spermiogramu sú poruchy v transformácii gonocytov na Ad spermatogónie počas mini-puberty – obdobia vyplavovania gonadotropínov a testosterónu v ranom detstve. Pri jednostrannom nezostúpenom semenníku vykazuje kontralaterálny zostúpený semenník určité histologické poruchy, čo podporuje tvrdenie, že pri kryptorchizme sa jedná o endokrinopatiu. Liečba LH-RH zmierňuje atrofiu Leydigových buniek a stimuluje ich prekurzorové bunky k dozrievaniu.
Hadziselimovic a kol. podávali pacientom s jednostranným kryptorchizmom po orchidopexii LH-RH analóg s cieľom upraviť zmeny v transformácii gonocytov počas mini-puberty. V štúdii s 30 pacientmi s kryptorchizmom, ktorým bola vykonaná peroperačná biopsia (Ad spermatogónie neboli prítomné u žiadneho pacienta), analyzovali po puberte spermiogram. Pätnástim pacientom podávali pooperačne analóg LH-RH – Buserelin v dávke 10 μg formou nosového spreja obdeň po dobu 6 mesiacov, ďalším 15 pooperačná liečba nebola podávaná. Všetci pacienti, ktorým nebol Buserelin podávaný, boli ťažko oligospermickí, 20 % z nich bolo azospermických. Naproti tomu 86 % pacientov, ktorým bol Buserelin podávaný, mali normálny spermiogram. Týmto prvýkrát poukázali, že neplodnosť pri kryptorchizme môže byť úspešne upravená liečbou analógom LH-RH. Parametre spermiogramu sa normalizovali po liečbe u väčšiny pacientov, ktorí by boli neplodní, ak by neboli hormonálne liečení. Takmer polovica pacientov s kryptorchizmom nemá v semenníku počas orchidopexie Ad spermatogónie. Práve títo pacienti sú kandidátmi pre hormonálnu liečbu. Histológia semenníka závisí od polohy, kde je retinovaný – všeobecne platí, že čím je bližšie k skrótu, tým je histológia priaznivejšia. Keďže nie všetci pacienti s jednostranným kryptorchizmom patria do skupiny, ktorá je z hľadiska fertility riziková, u niektorých postačuje čisto chirurgická liečba bez potreby adjuvantnej hormonálnej liečby. Biopsia semenníka je preto jedinou diagnostickou procedúrou, ktorá môže určiť pacientov, ktorí budú profitovať z hormonálnej adjuvantnej liečby. Autori preto navrhujú rutinnú biopsiu semenníka počas orchidopexie [20].
Niektorí autori však hormonálnu liečbu neodporúčajú, keďže má potenciálne nevýhody – cena, nízke percento zostupu semenníkov, potenciálne oneskorenie chirurgickej liečby a potenciálne nežiaduce účinky ako akcelerácia sekundárnych sexuálnych znakov a apoptóza zarodočných buniek. Poukazujú, že aj keď je pri jednostrannom semenníku fertilita znížená, paternita je rovnaká ako u bežnej populácie [21, 22]. U pacientov s anamnézou obojstranného nezostúpeného semenníka je paternita znížená a doposiaľ nebol dokázaný benefit hormonálnej liečby pri obojstrannom kryptorchizme [22].
Chirurgická liečba
Chirurgická liečba hmatného nezostúpeného semenníka zahŕňa orchidofunikulolýzu a orchidopexiu prevažne inguinálnym prístupom. Úspešnosť operácie (dosiahnutie skrotálnej pozície bez známok atrofie semenníka) závisí od predoperačnej lokalizácie nezostúpeného semenníka. Pri intraabdominálnom semenníku je to 74 %, ak je semenník v oblasti vnútorného anulu 82 %, v inguinálnom kanáli 87 %, ak je distálne od vonkajšieho anulu, dosahuje až 92 % [23]. Operácia sa vykonáva šikmým rezom v hypogastriu na strane nezostúpeného semenníka. Vykoná sa funikulolýza, t.j. uvoľnenie semenníka a funiculus spermaticus až do retroperitoneálneho priestoru, pričom je dôležité preťatie vláken m. cremaster. Izoluje sa processus vaginalis peritonei, prípadne herniový vak a po naložení opichovej ligatúry sa processus vaginalis peritonei resp. herniový vak resekuje. V podkoží príslušného hemiskróta sa vytvorí ukazovákom kanál a pod tunica dartos sa vytvorí kapsa, do ktorej sa cez obaly stiahne semenník. Zúžený priechod cez obaly bráni retrakcii semenníka. Následne sa semenník fixuje stehom do priestoru medzi kožu a tunica dartos. Predpokladom úspechu chirurgického postupu je uloženie semenníka do skróta bez napätia funikulu [7, 10].
Moderný spôsob diagnostiky a liečby pacientov s nehmatným semenníkom predstavuje laparoskopia. V súčasnosti neexistuje žiadna pomocná zobrazovacia metóda schopná so 100% senzitivitou odhaliť anorchiu alebo vysoko intraabdominálne uložený semenník [24]. Pri vysoko uloženom intraabdominálnom semenníku sa vykonáva operácia podľa Fowlera-Stephensa. Fowlerova-Stephensova orchidopexia sa používa vtedy, ak sú testikulárne cievy krátke na to, aby mohol byť semenník uložený do skróta, ak je semenovod dostatočne dlhý a ak sú cievy semenovodu dostatočné pre zásobenie semenníka. V prvej fáze, ktorá sa vykonáva laparoskopicky, sa prerušia testikulárne cievy, po ich prerušení je krvné zásobenie semenníka závislé na kolaterálnej cirkulácii z arteria ductus deferentis – vetvy arteria umbilicalis a z arteria cremasterica – vetvy arteria epigastrica inferior [25, 26]. Dvojfázová Fowlerova-Stephensova orchidopexia dovoľuje maximálny vývoj kolaterálnej cirkulácie v porovnaní s okamžitou mobilizáciou semenníka pri jednofázovej operácii, pri ktorej je zvýšené riziko vazospazmu arterie ductus deferens, čo vedie k atrofii operovaného semenníka [27]. Druhá fáza operácie sa vykonáva o 6–9 mesiacov po prerušení testikulárnych ciev. Pokračuje sa klasickou orchidopexiou, ktorá sa môže kombinovať s laparoskopiou, pri ktorej je možné uvoľniť semenník s bezpečnou ochranou kolaterálnych ciev [25]. Úspešnosť (dosiahnutie skrotálnej polohy bez známok atrofie semenníka) je v jednotlivých štúdiách zaoberajúcich sa orchidopexiou pri nehmatnom semenníku rôzna. Docimo pri zhrnutí údajov zo 64 článkov svetovej literatúry zistil, že pri jednofázovej Fowlerovej-Stephensovej operácii je úspešnosť 67 % a pri dvojfázovej 77 % [23].
Záver
Liečba kryptorchizmu môže začať už v 6. mesiaci života, keďže v tomto období dochádza k znižovaniu počtu zárodočných buniek a spontánny zostup semenníka po tomto období je vzácny. Pre vývoj nepriaznivých histologických zmien v nezostúpenom semenníku by mala byť ukončená do veku 18 mesiacov. Aby sa minimalizovali dlhodobé nepriaznivé vplyvy kryptorchizmu – neplodnosť a zvýšené riziko malignity, je potrebné odoslať pacienta s nezostúpeným semenníkom na odborné pracovisko už vo veku 6 mesiacov, kde mu môže byť poskytnutá včasná liečba.
U pacientov s kryptorchizmom je potrebné dlhodobé sledovanie aj po úspešnej liečbe, aby sa prípadná malignita mohla včas zachytiť a liečiť. Dôležité je aj sledovanie druhostranného zostupenného semenníka, v ktorom je taktiež zvýšené riziko vzniku nádoru. Pre zvýšenú incidenciu torzie nezostúpeného semenníka je potrebné poučiť rodičov o okamžitom lekárskom vyšetrení pri náhle vzniknutých bolestiach semenníka alebo brucha.
Došlo: 17. 11. 2012
Přijato. 1. 8. 2013
MUDr. Martin Michalisko
Klinika detskej chirurgie SZU
Detská fakultná nemocnica s poliklinikou
Nám. L. Svobodu 4
974 09 Banská Bystrica
Slovensko
e-mail: michalmart2000@yahoo.com
Sources
1. Zeman L. Retence varlete. In: Šnajdauf J, et al. Dětská chirurgie. 1. vyd. Praha: Galén, 2005 : 272–276. ISBN 80-7262-329-X.
2. Kolon TF. Cryptorchidism. In: Docimo SG, Canning DA, Khoury AE, et al. Clinical Pediatric Urology. 5th ed. Abingdon: Informa Healthcare UK Ltd, 2007 : 1295–1307. ISBN 1841845043.
3. Bianchi A. The undescendent testis. In: Burge DM, Griffiths DM, Steinbrecher HA, Wheeler RA, et al. Paediatric Surgery. 2nd ed. London: Hodder Education, 2005 : 311–319. ISBN 0 340809108.
4. Hutson JM. Cryptorchidism. In: Puri P, Höllwarth M, et al. Pediatric Surgery: Diagnosis and Management. 1st ed. Berlin: Springer-Verlag, 2009 : 919–926. ISBN 978-3-540-69559-2.
5. Ong C, Hasthorpe S, Hutson JM. Germ cell development in the descended and cryptorchid testis and the effects of hormonal manipulation. Pediatr Surg Int 2005; 21 : 240–254.
6. Ritzén EM. Undescended testes: A consensus on management. Eur J Endocrinol 2008; 159 : 87–90.
7. Hušťavová L, Michalka P. Retentio testis. In: Vidiščák M, et al. Novorodenecká chirurgia I. 1. vyd. Krivá: M-service, 2008 : 57–62. ISBN 978-80-969978.
8. Hušťavová L. Hydrocele testis, hydrocele funikuli spermatici. In: Vidiščák M, et al. Novorodenecká chirurgia I. 1. vyd. Krivá: M-service, 2008 : 62–63. ISBN 978-80-969978.
9. Gapany CH, et al. Management of cryptorchidism in children: guidelines. Swiss Med Wkly 2008; 138, č. 33–34 : 492–498.
10. Kočvara R. Kryptorchizmus: kdy načasovat a jakou léčbu provést? Urologicke Listy 2007; 5 (1): 30–33.
11. Chung E, Brock GB. Cryptorchidism and its impact on male fertility: a state of art review of current literature. Can Urol Assoc J 2011; 5 (3): 210–214.
12. Li YX, Coucke PA, Qian TN et al. Seminoma arising in corrected and uncorrected inguinal cryptorchidism: treatment and prognosis in 66 patients. Int J Radiat Oncol Biol Phys 1997; 38 (2): 343–350.
13. Forman D, Pike MC, Davey G, et al. Aetiology of testicular cancer: association with congenital abnormalities, age at puberty, infertility, and exercise. BMJ 1994; 308 : 1393–1399.
14. Pettersson A, Richiardi L, Nordenskjold A, et al. Age at surgery for undescended testis and risk of testicular cancer. N Engl J Med 2007; 356 (18): 1835–1841.
15. Docimo SG, Silver RI, Cromie W. The undescended testicle: Diagnosis and management. Am Fam Physician 2000; 62 (9): 2037–2044.
16. Hušťavová L. Varicocele. In: Vidiščák M, et al. Novorodenecká chirurgia I. 1. vyd. Krivá: M-service, 2008 : 64–65. ISBN 978-80-969978.
17. Lisá L. Nesestouplá varlata. Čes-slov Pediat 1996; 51 : 235–237.
18. Dunkel L, Taskinen S, Hovatta O, et al. Germ cell apoptosis after treatment of cryptorchidism with human chorionic gonadotropin is associated with impaired reproductive function in the adult. J Clin Invest 1997; 100 (9): 2341–2346.
19. Schwentner C, Oswald J, Kreczy A, et al. Neoadjuvant gonadotropin-releasing hormone therapy before surgery may improve the fertility index in undescended testes: a prospective randomized trial. J Urol 2005; 173 (3): 974–977.
20. Hadziselimovic F. Successful treatment of unilateral cryptorchid boys risking infertility with LH-RH analogue. Int Brazilian J Urol 2008; 34 (3): 319–328.
21. Hutson JM. Undescendent testes. In: Stringer M, Oldham KT, Mouriquand PDE, et al. Pediatric Surgery and Urology: Long-term Outcomes. 2nd ed. Cambridge: Cambridge University Press, 2006 : 652–663. ISBN 0-521-83902-5.
22. Ludwikowski B, González R. The controversy regarding the need for hormonal treatment in boys with unilateral cryptorchidism goes on: a review of the literature. Eur J Pediatr 2012, dostupné na internete: http://www.springerlink.c om/content/v7x3575708731085/fulltext.pdf.
23. Docimo SG. The results of surgical therapy for cryptorchidism: a literature review and analysis. J Urol 1995; 154 (3): 1148–1152.
24. Drlík M, Kočvara R. Nehmatné varle u dítěte: začít diagnostickou laparoskopií nebo otevřenou revizí třísla? Česká Urologie 2011; 15 (2): 101–107.
25. Franco I. Management of impalpable testes. In: Najmaldin A, Rothenberg S, Crabbe S, et al. Operative Endoscopy and Endoscopic Surgery in Infants and Children. 1st ed. London: Hodder Arnold, 2005 : 385–390. ISBN 0 340 80725 3.
26. Frank JD, Geahart JP, Snyder HM. Operative Pediatric Urology. 2nd ed. London: Churchill Livingstone, 2002 : 260–270. ISBN 0-443-05358-8.
27. Esposito C, et al. Long-term outcome of laparoscopic Fowler-Stephens orchiopexy in boys with intra-abdominal testis. J Urol 2009; 181 (4): 1851–1856.
Labels
Neonatology Paediatrics General practitioner for children and adolescents
Article was published inCzech-Slovak Pediatrics

2014 Issue 1-
All articles in this issue
- Tranzitorní pseudohypoaldosteronismus – nefro-urologické „puzzle“
- Adipsický diabetes insipidus u pacienta s dysgenézou corpus callosum
- Péče o předčasně narozené dítě: Kdy začíná a kdy končí?
- ICON – souhrn nejnovějších doporučení v managementu průduškového astmatu u dětí
- Kryptorchizmus – potreba včasnej diagnostiky a liečby
- Vědecké důkazy o prospěšnosti výživy mateřským mlékem
- Czech-Slovak Pediatrics
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Kryptorchizmus – potreba včasnej diagnostiky a liečby
- Tranzitorní pseudohypoaldosteronismus – nefro-urologické „puzzle“
- Péče o předčasně narozené dítě: Kdy začíná a kdy končí?
- Adipsický diabetes insipidus u pacienta s dysgenézou corpus callosum
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

