-
Medical journals
- Career
Metody bezkrevní péče v gynekologii a onkogynekologii
Authors: D. Seidlová 1; Vít Weinberger 2
Authors‘ workplace: II. ARO a KARIM, LF MU a FN, Brno 1; Gynekologicko-porodnická klinika, LF MU a FN, Brno 2
Published in: Ceska Gynekol 2014; 79(6): 499-504
Overview
Přehledová práce.
Metody bezkrevní medicíny jsou využívány v řadě chirurgických oborů. Cílem článku je upozornit na možnost využití těchto postupů v gynekologické operativě ke snížení počtu podávaných transfuzí.Klíčová slova:
bezkrevní medicína, gynekologická operativa, krvácení, transfuze, monitorace, operační techniky, hemostatika, hemodiluce, řízená hypotenze, cell-saver, krevní sráženíÚVOD
Každý medicínský zákrok s sebou nese určitou míru rizika a podání krevní transfuze není výjimkou [10, 14, 18, 20, 21, 25]. V současnosti stále více pacientek vyjadřuje obavy z rizika provázejícího podání alogenní transfuze krve a žádají bezkrevný chirurgický přístup [8, 25].
Nežádoucí účinky krevní transfuze lze rozdělit na infekční, neinfekční a imunologické [21, 25, 49]. Z infekčních jsou to virus HIV, hepatitidy B, C, EB virus, lidské T-lymfotropní viry a cytomegalovirus, virus západonilské horečky, parazity způsobená Chagasova choroba a malárie [20, 25, 33, 42]. K neinfekční komplikaci transfuze patří transfuzní chyba, která má incidenci 1 : 12 000 [20, 25, 30, 31]. Dále jsou to syndrom respirační tísně dospělých, hypotermie, hemosideróza, arytmie, hypokalcémie a hypomagnezémie [20, 25, 37]. Závažné imunologické komplikace vyvolávají potransfuzní akutní a opožděnou hemolýzu, horečku, alergické reakce, post-transfuzní purpuru a TRALI syndrom – akutní poškození plic způsobené transfuzí [20, 25, 48].
CÍL
Cílem tohoto článku není odmítnout transfuze v případě a situaci, kdy je podání indikované, ale nabídnout možnosti, jak tomu předejít. Postupy bezkrevní medicíny minimalizují množství podaných transfuzních přípravků individualizovaným přizpůsobením terapie pacientovi. V gynekologii a onkogynekologii jsou jak akutní, tak chronické stavy a onemocnění, které jsou spojeny s krevní ztrátou a rozvojem akutní či chronické anémie. V článku rozebíráme metody, které umožňují potenciálně se vyhnout podání transfuze.
PATOFYZIOLOGIE
Zdravá žena kompenzuje akutní krevní ztrátu do 10 % krevního objemu. Ztráta nad 20–30 % krevního objemu (1500–2000 ml) vede ke snížení srdečního výdeje, dochází k hypoperfuzi méně důležitých orgánů a centralizaci oběhu, další hypovolémie vede k hypotenzi, rozvíjí se šokový stav [23]. Podle studií porovnávajících různé typy hysterektomií krevní ztráta přesahující 1000 ml se objevuje v 1–2 % [21] a 10–15 % pacientek podstupujících abdominální hysterektomii vyžaduje transfuzi [17, 19].
PŘEDOPERAČNÍ POSOUZENÍ ZDRAVOTNÍHO STAVU PACIENTKY
- Anamnéza pacientky
- Příčiny eventuální anéemie
- Přesná gynekologická anamnéza se snahou o rozklíčení poruch menstruačního cyklu, dotazy na atypické krvácení při porodech s nutností transfuze
- Koagulopatie vrozené či získané
- Předchozí podání transfuzí – množství, důvod a případné potransfuzní reakce
- Chronická medikace: zvláště antikoagulancia, antitrombotika, hemostatika
- Abúzus
V případě podezření na závažnou koagulopatii je vhodné hematologické konzilium.
Predikce krvácení
Pokles hladiny fibrinogenu je spojen s vyšším rizikem perioperačního krvácení [4, 12, 20].
Postupy bezkrevní medicíny v gynekologii a onkogynekologii jsou přehledně uvedeny v tabulce 1.
Table 1. Postupy bezkrevní medicíny v gynekologii a onkogynekologii přehledně 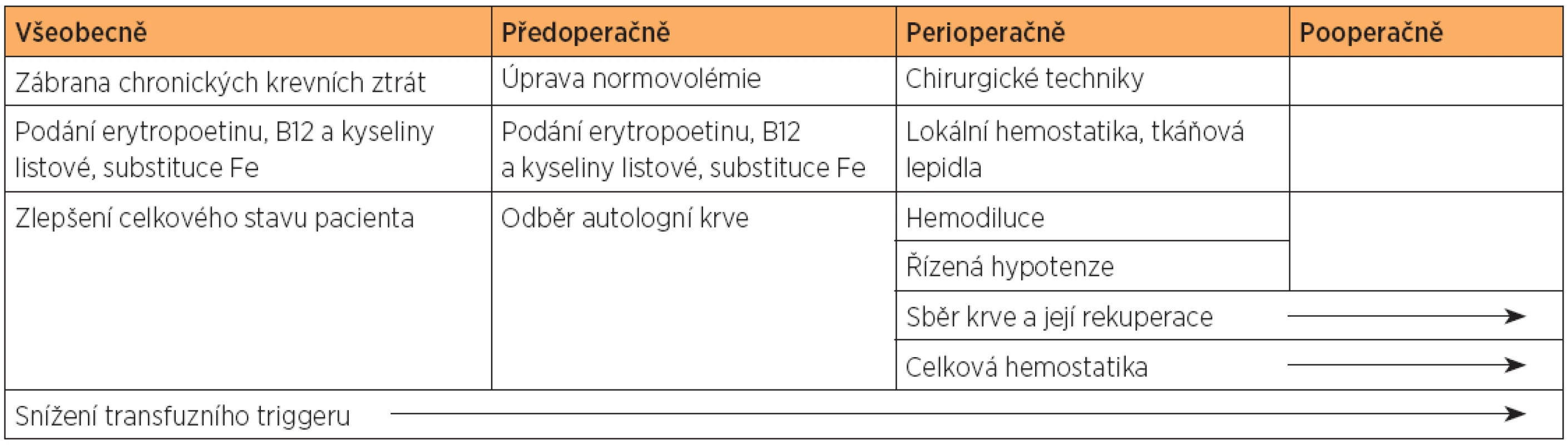
PŘEDOPERAČNÍ MANAGEMENT ANÉMIE
Substituce železa
Sideropenickou anémii léčíme podáváním železa. Do léčby je vhodné přidat kyselinu listovou a vitamin B12, event. i kyselinu askorbovou [16, 20, 38].
Rekombinantní erytropoetin (EPO)
EPO je nejčastěji využíván v onkogynekologii ke korekci anémie při probíhající chemoterapii. Jeho aplikace vede ke snížení počtu podaných transfuzí [10, 15, 20, 33, 38, 47].
Hormonální terapie
U terapie hypermenorey způsobené hormonální dysbalancí či benigním onemocněním dělohy je indikováno podání hormonálních kontraceptiv či zavedení nitroděložního systému s gestagen le-vonorgestrelem, čímž je redukována chronická krevní ztráta a v kombinaci s aplikací železa je dosaženo lepší úpravy krevního obrazu [9].
Autologní transfuze
Je využívána před plánovanou operací s očekávanou větší krevní ztrátou. Několik týdnů před výkonem je opakovaně odebrána pacientce krev. Následná „autotransfuze“ vyloučí většinu výše zmíněných nežádoucích účinků [20, 38].
Selektivní embolizace
Těsně předoperačně je možno provést angiografickou embolizaci uterinních či interních ilických arterií v rámci předcházení excesivní krevní ztráty [13, 19, 20, 48]. Stejně tak je indikováno tuto možnost využít při neošetřitelném krvácení v souvislosti s operačním výkonem [13, 19, 20, 39, 40, 42, 48].
MANAGEMENT ZÁSTAVY KRVÁCENÍ BĚHEM OPERACE
Kooperace celého operačního týmu vede k minimalizaci krevních ztrát a množství případně podaných transfuzí. Operatér používá vhodné operační postupy a anesteziolog volí specializované techniky a medikamenty a je zároveň zodpovědný za adekvátní hrazení krevních ztrát.
CHIRURGICKÉ TECHNIKY A POSTUPY
Redukce krevní ztráty dosáhneme znalostí anatomie, přesnou chirurgickou preparací za využití bezkrevných prostor obklopujících jednotlivé orgány a struktury a časnou zástavou vzniklého krvácení i s případnou aplikací lokálních hemostatik.
Zástava peroperačního krvácení - krok první
Zásadní je komprese krvácejícího místa, obklad horkými rouškami [3, 16, 17]. U laparoskopických výkonů komprimujeme atraumatickým nástrojem, ke stlačení zdroje lze využít i tampony. Při poranění velkých cév v retroperitoneu je většinou nutná konverze na laparotomii.
Identifikace zdroje krvácení
Masivní krvácení vzniká nejčastěji poraněním dolní duté žíly, presakrálních žil, ovariálních cév, ilických cév, parametriálních a paracervikálních varikózních komplexů, při radikálních onkogynekologických výkonech dále poškozením aorty, paravertebrálních cévních spojek a pletení, jater a sleziny. Operování v avaskulárních prostorech (paravezikální, pararektální, vezikovaginální a rektovaginální) umožňuje minimalizovat krevní ztrátu a pohybovat se v relativně bezpečných anatomických lokalitách [3, 16, 17].
Zástava krvácení
K zástavě krvácení cév malého průměru je vhodná elektrokoagulace (monopolární elektrokoagulace je méně vhodná než bipolární), ligatura či klip při přesné identifikaci zdroje. Krvácení z velkých cév v retroperitoneu řešíme primárně kompresí, zaklemováním cévní svorkou a následnou suturou monofilamentním vláknem 4–0 až 6–0 [16, 17, 42].
Ligace arteria ilica interna
Pokud není dosaženo kontroly krvácení, je nutný podvaz a. ilica interna nebo selektivní embolizace. Oboustranný podvaz redukuje průtok krve do malé pánve o polovinu a snižuje pulzní tlak v cévách o 85 %. Oboustranně v retroperitoneu je asi 2 cm od bifurkace na interní ilickou arterii naložena pravoúhlá cévní svorka (pozor na vespod běžící vénu), poté jsou naloženy dvě ligatury za verifikace intaktního průtoku externí ilickou arterií [16, 17, 42]. Při neúspěšné zástavě krvácení po ligaci interních ilických arterií provedení selektivní embolizace distálních cév hluboko v malé pánvi není možné [13, 19, 39].
Tamponáda malé pánve
Vytamponování malé pánve rouškami je variantou volby při selhání těchto postupů. Po maximálně 48 hodinách následuje second-look a definitivní chirurgické uzavření dutiny břišní. Intraperitoneální nebo retroperitoneální krvácení může vést ke zvýšení nitrobřišního tlaku a rozvoji syndromu abdominálního kompartmentu [3, 16, 40, 42].
Lokální hemostatické přípravky
Působí přímo v místě krvácení. U malých ran nebo v obtížně dostupných lokalitách může jejich použití nahradit tradiční chirurgické postupy. V kombinaci s pečlivou chirurgickou technikou a celkovou terapií jsou dobrým doplňkem léčby i závažného krvácení [40, 44]. Jedná se o preparáty na bázi celulózy (Surgicel, Bloodcare, Traumacel), vepřové želatiny (Surgiflo, Spongostan, Gelaspon) a zvířecího kolagenu (Avitene, Gentafleece): slouží jako matrice pro vychytávání trombocytů, bobtnají [32]. Vstřebávání trvá týdny. Fibrinová a trombinová lepidla ovlivňují přímo koagulační pochody v místě poranění. Užívají se samostatně (Tissucol, Periplast, Evicel) nebo v kombinaci především s kolagenovou matrix (FloSeal, TachoSil) [32]. Syntetická lepidla (Omnex, Histoacryl, Glubran) neovlivňují koagulační pochody, jejich hemostatický účinek je dán pevným spojením nebo utěsněním krvácející cévy. Jsou enzymaticky odbouratelná v řádu let [44].
ANESTEZIOLOGICKÝ MANAGEMENT
Anesteziolog je obeznámen s typem operačního výkonu a způsobem jeho provedení, celkovým stavem pacienta; predikuje velikost krevní ztráty, objednává do rezervy transfuzní přípravky a krevní deriváty a volí takové postupy, které vedou ke snížení krevních ztrát [8, 20].
Všeobecné zásady: vhodný typ a dostatečná hloubka anestezie pro daný výkon i pacienta, minimalizace tepelných ztrát, kvalitní žilní vstupy a adekvátní monitorace nejen celkového stavu, ale i hemostázy a homeostázy laboratorně [20, 27]. Zde je třeba se zmínit o zavedení bed-side metody měření viskoelasticity krevního koagula (ROTEM, TEG) do peroperační monitorace. Při použití této metody dochází k výraznému snížení počtu podaných transfuzí [2, 8, 15, 20, 28, 45].
Specializované postupy vhodné pro gynekologickou operativu:
Akutní normovolemická hemodiluce: Principem je odebrání předem definovaného množství krve pacienta bezprostředně před výkonem, ale již v anestezii. Nezbytné je zachování množství cirkulujícího objemu podáním krystaloidních a koloidních náhradních roztoků. Dochází ke snížení hematokritu cirkulující krve. Ztráta erytrocytů je menší, než by tomu bylo v případě ztráty stejného množství krve s vysokou hodnotou hematokritu. Následuje zpětná transfuze odebrané krve na konci operace [8, 20].
Sběr krve a rekuperace: technika je založena na peroperačním odsávání krve do speciálního vaku, krev je antikoagulována, promývána, centrifugována a jako erytrocytární koncentrát navrácena zpět do oběhu operovaného, s výhodou lze její aplikaci prodloužit i na časné pooperační období. Vzhledem ke kontraindikacím (infekce nebo operace zhoubných nádorů) je tato technika vhodná pro velmi malý okruh pacientek (myomatóza dělohy, úrazy, malformace) [8, 20, 26].
Řízená hypotenze: metoda využívaná dlouhodobě především ve spondylochirurgii. Pro gynekologickou operativu se jeví jako vhodná, v literatuře jsou zmíněny pouze sporadické odkazy [22], na našem pracovišti je zatím ve stadiu experimentu. Principem je snížení krevního tlaku na tlak perfuzní (MAP 65-70torr) za kontinuální invazivní monitorace. K dosažení většinou postačuje hluboká anestezie, někdy v kombinaci s kontinuálně podávanými hypotenzivy. Operovaná oblast musí být nejvýše, a je tak méně prokrvena [8, 20, 26, 27, 38].
Medikamentózní ovlivnění krevních ztrát (hemostatika pro celkové podání)
Jedná se o heterogenní skupinu přípravků, které různými mechanismy vstupují do procesu hemostázy. Pro správný výběr daného hemostatika je nutno znát mechanismus jeho účinku.
Látky působící primárně vazokonstrikčně
Vazopresin a desmopresin jsou používány spíše experimentálně jak lokálně, tak celkově. Terlipresin (Remestyp) má vazokonstrikční a protikrvácivý účinek především ve splanchnické oblasti, zvyšuje tonus a motilitu hladkého svalstva. Zintenzivňuje myometriální aktivitu, snižuje průtok krve dělohou, více v kombinaci s oxytocinem a metylergometrinem [20].
Látky působící primárně na trombocyty
Etamsylate (Dicynone) zvyšuje adhezivitu destiček a upravuje kapilární rezistenci [20].
Calcium Ca ovlivňuje výkonnost celého koagulačního systému. Je doporučena substituce – k dosažení hladiny ionizovaného kalcia nad 1,2 mmol/l [20].
Krevní deriváty se získávají z lidské plazmy nebo rekombinantní technologií.
Fibrinogen koagulační faktor I (Fibrinogen, Haemocomplettan) je produkován v játrech. Získává se z krevní plazmy. Hraje v procesu koagulace zásadní roli, bez jeho dostatečné hladiny nelze dosáhnout kontroly krvácení a tvorby kvalitního koagula. Substituce v dávce 4–6 g je doporučována při poklesu fyziologické hladiny 2 g/l [4, 12, 20, 28, 35, 36, 38]. Není-li dostupný, lze jeho podání nahradit aplikací kryoproteinu [20].
Koncentráty koagulačních faktorů (Feiba, Protromplex) získané z lidské plazmy jsou používány k razantnímu zrušení účinku perorálních antikoagulancií u akutních stavů [20, 38].
Faktory VIII a IX jsou používány k substituční léčbě u hemofiliků [20].
Faktor XIII, fibrin stabilizující faktor (Fibrogammin) je enzym, který vytváří křížové vazby mezi molekulami fibrinu, k jeho aktivaci jsou potřebné vápenaté ionty [20].
Rekombinantní faktor VIIa – eptacog alfa – rFVIIa (Novoseven) rekombinantně připravovaný. Podle SPC je indikován u primárních poruch koagulace. Jeho podání v indikaci život ohrožujícího krvácení, i když se jeví jako účinné, je hodnoceno jako rescue therapy [20, 24, 38].
Antifibrinolytika jsou látky zpomalující nebo zastavující fibrinolýzu: neutralizují činnost proteolytických enzymů. Kyselina tranexamová (Exacyl), je lékem volby u život ohrožujícího krvácení [7, 20, 34, 38, 46]. Ve studii Crush II u pacientů s traumaty její podání vedlo k signifikantnímu snížení mortality, krevních ztrát i počtu transfuzí [20, 46]. U operací Ca ovaria došlo ke snižení velikosti krevní ztráty, stejně jako u císařských řezů [7, 11, 20, 34, 38].
Hemostatické přípravky souhrnně uvádí tabulka 2.
Table 2. Hemostatické přípravky 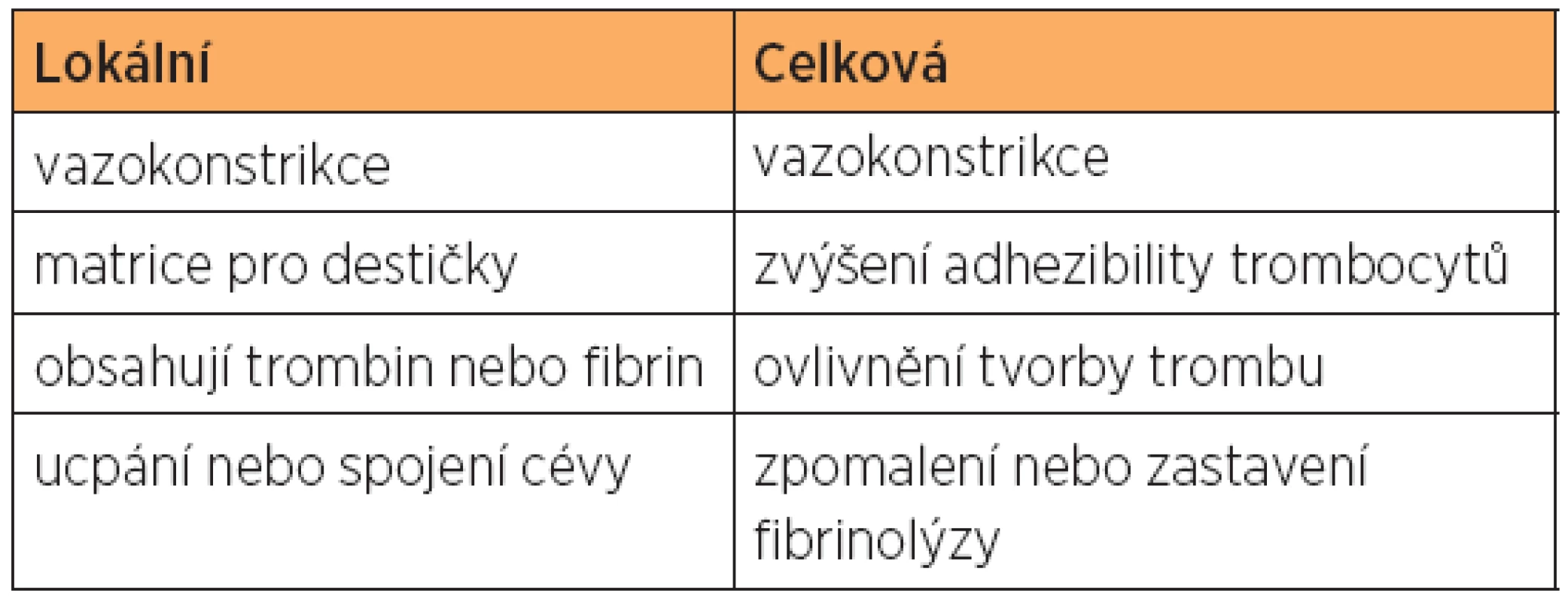
POOPERAČNÍ KRVÁCENÍ
V pooperační péči je nezbytná monitorace velikosti ztrát do drenů a sledování celkového stavu pacientky a laboratorních parametrů. Při použití peroperační rekuperace je vhodné pokračovat s touto metodou i v časném pooperačním období [8, 20]. Pacientka po větší krevní ztrátě provázející operační výkon by měla být hospitalizována na JIP. Při narůstajících ztrátách do drenů či poklesu v krevním obrazu je nutno pátrat po zdroji krvácení a situaci řešit ad hoc. Nedílnou součástí péče je i snaha o minimalizaci množství odebírané krve pro laboratorní účely. V celkové terapii hemostatickými přípravky je samozřejmě vhodné pokračovat i pooperačně [20].
PODÁNÍ TRANSFUZNÍCH PŘÍPRAVKŮ
Ve studii 300 pacientek, odmítajících transfuzi, nebylo zaznamenáno žádné úmrtí při hladině hemoglobinu 70–80 g/l. Při hladině 51–70 g/l byla mortalita 9 %, při 31–50 g/l byla 30 % a při hladině pod 30 g/l byla mortalita 64 % [17, 21].
Dnes již klasická Hebertova práce [18] prokázala prospěšnost restriktivní hemoterapie [14, 18, 20]. Dřívější práh pro podání transfuzí (Hb 100 g/l a Htk 0,33) je dávno minulostí. Transfuzní trigger je u zdravých jedinců většinou uváděn mezi 60–70 g/l, u pacientů kompromitovaných závažnými komorbiditami pak kolem 80 g/l [20, 25, 36]. Je vždy třeba se řídit aktuálním stavem pacienta spolu s hodnotou krevního obrazu a koagulogramem a vzít do úvahy i potřebu tkání na dodávku kyslíku (pH, hladina laktátu) [14, 20, 25, 36]. Pokud indikujeme podání erykoncentrátu, měl by to být přípravek, u kterého byla provedena nejlépe prestorage leukodeplece a jehož stáří je co nejkratší [1, 20, 41, 43]. Princip patient blood management [15, 20, 35, 36] znamená na míru přizpůsobenou hemoterapii pomocí konkrétních transfuzních přípravků a krevních derivátů (erykoncentrátu, trombokoncentrátu a koncentrátu fibrinogenu) nejlépe za využití bed-side monitorace koagula [2, 4, 12, 15, 20, 28, 35, 36, 45].
ZÁVĚR
Optimalizace zdravotního stavu předoperačně, prevence krevních ztrát per - a pooperačně spolu s restriktivní transfuzní terapií je pro pacientky podstupující gynekologický operační výkon přínosná. Pro dosažení tohoto cíle je nutné, aby gynekolog tyto postupy vzal do úvahy již při stanovení termínu operace, zavčas ve spolupráci s praktickým lékařem nastavil optimální terapii, v anesteziologické ambulanci anesteziolog předem zvážil možnosti, které se nabízejí. V průběhu operačního výkonu a pooperačně je pak celý tým veden snahou omezit krevní ztráty na minimum a každou jednotlivou případnou transfuzi indikovat přísně individuálně a nikoli paušálně na základě adekvátní monitorace hemostázy a homeostázy pacientky.
Podpořeno MZ ČR – RVO (FNBr, 65269705).
Autorka je vědeckým sekretářem České společnosti bezkrevní medicíny www.csbm.cz.
MUDr. Dagmar Seidlová, Ph.D.
II. ARO a KARIM
LF MU a FN
Jihlavská 20
625 00 Brno
e-mail: dseidlova@fnbrno.cz
Sources
1. Aubron, C., Bailey, M., McQuilten, Z., et al. Duration of red blood cells storage and outcome in critically ill patients. J crit Care, 2014, 29(3), p. 476–e1.
2. Afshari, A., Wikkelso, A., Brok, J., et al. Thrombelastography (TEG) or thromboelastometry (ROTEM) to monitor haemotherapy versus usual care in patients with massive transfusion. Cochrane Database Syst Rev 2011; 3:CD007871.
3. Balogh, Z., Jones, F., D‘Amours, S., et al. Continuous intra-abdominal pressure measurement technique. Am J Surg, 2004, 188, 6, p. 679–684.
4. Blombäck, B. Fibrinogen and fibrin-proteins with complex roles in hemostasis and thrombosis. Clin Hemorheol Microcirculation, 1996, 16(4), p. 383–477.
5. Capasso, A., Pisano, A. Leukocyte depletion of transfused blood to reduce perioperative mortality. In Reducing mortality in the perioperative perio. Springer International Publishing, 2014, p. 85–92.
6. Carson, JL., Noveck, H., Berlin, JA., Gould, SA. Mortality and morbidity in patients with very low postoperative Hb levels who decline blood transfusion. Transfusion, 2002, 42, 7, p. 812–818.
7. Celebi, N., Celebioglu, B., Selcuk, M., et al. The role of antifibrinolytic agents in gynecologic cancer surgery. Saudi Med J, 2006, 27, p. 637–641.
8. Čundrle, I., Vlach, O., Zimová, I., et al. Eficience jednotlivých metod bezkrevní medicíny. Novinky v anesteziologii, intenzivní medicíně a léčbě bolesti. 2008, s. 124–126.
9. De Aloysio, D., Altieri, P., Pretolani, G., et al. The combined effect of a GnRH analog in premenopause plus postmenopausal estrogen deficiency for the treatment of uterine leiomyomas in perimenopausal women. Gynecol Obstet Invest, 1995, 39, 2, p. 115–119.
10. Dodd, RY. Current safety of the blood supply in the United States. Int J Hematol, 2004, 80, 4, p. 301–305.
11. Ducloy-Bouthors, AS., Jude, B., Duhamel, A., et al. High-dose tranexamic acid reduces blood loss in postpartum haemor-rhage. Crit Care, 2011, 15, R117.
12. Fenger-Eriksen, C., Lindberg-Larsen, M., Christensen, AQ., et al. Fibrinogen concentrate substitution therapy in patients with massive haemorrhage and low plasma fibrinogen concentrations. Brit J Anaesth, 2008, 101(6), p. 769–773.
13. Frati, A., Ducarme, G., Wernet, A., et al. Uterine artery embolization as treatment for life-threatening haemorrhage from a cervical choriocarcinoma: A case report. Eur J Obstet Gynec Reprod Biol, 2008, 141(1), p. 87–88.
14. Glance, LG., Dick, AW., Mukamel, DB., et al. Association bet-ween intraoperative blood transfusion and mortality and morbidity in patients undergoing noncardiac surgery. Anesthesiology, 2011, 114, p. 283–292.
15. Goodnough, LT., Shander, A. Patient blood management. Anesthesiology, 2012, 116(6), p. 1367–1376.
16. Gostout, BS., Cliby, WA., Podratz, KC. Prevention and management of acute intraoperative bleeding. Clin Obstet Gynecol, 2002, 45, 2, p. 481–491.
17. Harrison, WJ. Early complications of abdominal and vaginal hysterectomy. Obstet Gynecol Surv, 1995, 50, 11, p. 795–805.
18. Hébert, PC., Wells, G., Blajchman, MA., et al. A multicenter, randomized, controlled clinical trial of transfusion requirements in critical care. N Engl J Med, 1999, 340(6), p. 409–417.
19. Howard, RJ., Straughn, JM., Huh, WK., Rouse, DJ. Pelvic umbrella pack for refractory obstetric hemorrhage secondary to posterior uterine rupture. Obstet Gynecol, 2002, 100, 5,p. 1061–1063.
20. Kozek-Langenecker, SA., Afshari, A., Albaladejo, P., Santullano, CAA., et al. Management of severe perioperative bleeding: guidelines from the European Society of Anaesthesiology. Eur J Anaesth (EJA), 2013, 30(6), p. 270–382.
21. Linden, JV., Paul, B., Dressler, KP. A report of 104 transfusion errors in New York State. Transfusion, 1992, 32, 7, p. 601–606.
22. Little Jr, DM. „Controlled Hypotension“ in anesthesia and surgery. Anest Analgesia, 1956, 35(4), 284.
23. Longmore, JM. Oxford handbook of clinical medicine. 8. vyd. Oxford : Oxford university press, 2010. ISBN 9780199232178.
24. Martinowitz, U., Michaelson, M. Israeli Multidisciplinary rFVIIa Task Force Guidelines for the use of recombinant activated factor VII (rFVIIa) in uncontrolled bleeding: a report by the Israeli Multidisciplinary rFVIIa Task Force. J Thromb Haemost, 2005, 3, p. 640–648.
25. Nicholls, MD. Transfusion: morbidity and mortality. Anaesth Intensive Care, 1993, 21, 1, s. 15–9.
26. Nuttall, GA., Horlocker, TT., Santrach, PJ., et al. Predictors of blood transfusions in spinal instrumentation and fusion surgery. Spine, 2000, 25(5), p. 596–601.
27. Rajagopalan, S., Mascha, E., Na, J., Sessler, DI. The effects of mild perioperative hypothermia on blood loss and transfusion requirement. Anesthesiology, 2008, 108(1), p. 71–77.
28. Rahe-Meyer, N., Pichlmaier, M., Haverich, A., et al. Bleeding management with fibrinogen concentrate targeting a high-normal plasma fibrinogen level: a pilot study. Br J Anaesth, 2009, 102, p. 785–792.
29. Rayburn, WF., et al. Prevention and management of complications from gynecologic surgery. Obstet Gynec Clinics, 2010, 37, 3, p. 427–436.
30. Santoso, JT., Saunders, BA., Grosshart, K. Massive blood loss and transfusion in obstetrics and gynecology. Obstet Gynecol Surv, 2005, 60, 12, p. 827–837.
31. Santoso, JT., Lin, DW., Miller, DS. Transfusion medicine in obstetrics and gynecology. Obstet Gynecol Surv, 1995, 50, 6, p. 470–481.
32. Schonauer, C., Tessitore, E., Barbagallo, G., et al. The use of local agents: bone wax, gelatin, collagen, oxidized cellulose. Eur Spine J, 2004, 13(1), p. S89–S96.
33. Sesti, F., Ticconi, C., Bonifacio, S., Piccione, E. Preoperative administration of recombinant human erythropoietin in patients undergoing gynecologic surgery. Gynecol Obstet Invest, 2002, 54, 1, p. 1–5.
34. Shakur, H., Roberts, I., et al., CRASH-trial collaborators. Effects of tranexamic acid on death, vascular occlusive events, and blood transfusion in trauma patients with significant hae-morrhage (CRASH-2): randomised, placebo-controlled trial. Lancet, 2010, 376, p. 23–32.
35. Shander, A., Van Aken, H., Colomina, MJ., et al. Patientblood management in Europe. Brit J Anaesth, 2012, 139.
36. Shander, A., Javidroozi, M., Perelman, S., et al. From bloodless surgery to patient blood management. Mount Sinai J Med: J Translat Personalized Med, 2012, 79(1), p. 56–65.
37. Simou, M., Thomakos, N., Zagouri, F., et al. Non-blood medical care in gynecologic oncology: a review and update of blood conservation management schemes. World J Surg Oncol, 2011, 9, p. 142.
38. Slipac, J. Bezkrevní medicína. Praha: Triton, 2008.
39. Smith, DC., Wyatt, JF. Embolization of the hypogastric arteries in the control of massive vaginal hemorrhage. Obstet Gynec Survey, 1977, 32(7), p. 490–494.
40. Spahn, DR., Cerny, V., Coats, TJ.,et al., Task Force for Advanced Bleeding Care in Trauma. Management of bleeding following major trauma: a European guideline. Crit Care, 2012, 11(1), R17.
41. Spinella, PC., et al. Duration of red blood cell storage is associated with increased incidence of deep vein thrombosis and in-hospital mortality in patients with traumatic injuries. Critical Care, 2009, 13:R151 doi:10.1186/cc8050,
42. Tamizian, O., Arulkumaran, S. The surgical management of postpartum haemorrhage. Curr Opin Obstet Gynecol, 2001,13, 2, p. 127–131.
43. Tinmouth, A., Fergusson, D., Yee, IC., Hebert, PC. Clinical consequences of red cell storage in the critically ill. Transfusion, 2006, 46(11), p. 2014–2027.
44. Tomizawa, Y. Clinical benefits and risk analysis of topical hemostats: a review. J Artific Organs, 2005, 8(3), p. 137–142.
45. Weber, CF., Görlinger, K., Meininger, D., et al. Point-of-care testing: a prospective, randomized clinical trial of efficacy in coagulopathic cardiac surgery patients. Anesthesiology, 2012, 117(3), p. 531–547.
46. Williams-Johnson, JA., McDonald, AH., Strachan, GG., Williams, EW. Effects of tranexamic acid on death, vascular occlusive events, and blood transfusion in trauma patients with significant haemorrhage (CRASH-2): a randomised, placebo-controlled trial. West Indian Med J, 2010, 59(6), p. 612–624.
47. Wurnig, C., Schatz, K., Noske, H., et al. Subcutaneous low-dose epoetin beta for the avoidance of transfusion in patients scheduled for elective surgery not eligible for autologous blood donation. Eur Surg Res, 2001, 33, 5–6, p. 303–310.
48. Yamashita, Y., Harada, M., Yamamoto, H., et al. Trans-catheter arterial embolization of obstetric and gynaecological bleeding: efficacy and clinical outcome. Brit J Radiol, 1994, 67(798), p. 530–534.
Labels
Paediatric gynaecology Gynaecology and obstetrics Reproduction medicine
Article was published inCzech Gynaecology

2014 Issue 6-
All articles in this issue
- Staging zhoubného nádoru děložního hrdla (stanovení předoperačního rozsahu onemocnění) – přehled výsledků nejnovějších ultrazvukových studií
- Ultrazvukový staging karcinomu děložního hrdla – návrh standardního postupu
- Zhoubný nádor děložního těla – předoperační odlišení nádorů s nízkým a vysokým rizikem metastázování (přehled výsledků nejnovějších ultrazvukových studií)
- Ultrazvukový staging karcinomu endometria – doporučená metodika vyšetření
- Doporučený diagnostický postup u ženy s ovariální cystou nebo nádorem
- Volba vhodné bioptické metody u primárně inoperabilního nebo recidivujícího zhoubného nádoru a metodika bioptického odběru
- Význam screeningu v onkogynekologii
- Metody bezkrevní péče v gynekologii a onkogynekologii
- Volba zobrazovací metody v onkogynekologii
- Czech Gynaecology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Doporučený diagnostický postup u ženy s ovariální cystou nebo nádorem
- Ultrazvukový staging karcinomu endometria – doporučená metodika vyšetření
- Ultrazvukový staging karcinomu děložního hrdla – návrh standardního postupu
- Zhoubný nádor děložního těla – předoperační odlišení nádorů s nízkým a vysokým rizikem metastázování (přehled výsledků nejnovějších ultrazvukových studií)
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

