-
Medical journals
- Career
Optimalizace vyšetření protilátek proti trombocytům u těhotných a žen po porodu
: Z. Čermáková 1; P. Kovářová 2; A. Malušková 2; M. Paulišková 2; D. Fizková 2
: Lékařská fakulta Ostravské univerzity 1; Krevní centrum FN Ostrava, vedoucí pracoviště MUDr. Z. Čermáková, Ph. D. 2
: Ceska Gynekol 2011; 76(3): 239-242
Cíl studie:
Optimalizovat vyšetření trombocytárních protilátek v rámci imunohematologického vyšetření těhotných žen a žen krátce po porodu.Typ studie:
Retrospektivní analýza.Název a sídlo pracoviště:
Krevní centrum FN Ostrava, Lékařská fakulta OSU.Metodika:
Analýza a vlastní zkušenosti při zavádění testů pro vyšetření trombocytárních protilátek na sledovaném souboru pacientek.Závěr:
Postup vyšetření trombocytárních protilátek nově zaváděných v letech 2008-2009 kombinací základních a speciálních vyšetření se v praxi pracoviště Krevního centra FN Ostrava ukazuje jako optimální pro záchyt neonatální trombocytopenie.Klíčová slova:
trombocytární protilátky, antigeny trombocytů, neonatální aloimunní trombocytopenie.ÚVOD
Neonatální (fetomaternální) aloimunní trombocytopenie (FMAIT, NAITP) se rozvíjí v důsledku inkompatibility v HPA (Human Platelet Antigens) systému antigenů, mezi matkou a plodem, podobně jako u hemolytického onemocnění novorozenců [18]. Incidence NAITP se udává okolo 1 na 1500 porodů [4, 8, 9]. Přestože většinou dochází k aloimunizaci až při porodu, může dojít k manifestaci již v prvním těhotenství [11, 15]. NAITP je nejčastěji vyvoláno přítomností anti-HPA-1a protilátky (v kavkazké populaci 75–95 % případů), zbylých 5–25 % je vyvoláno ostatními anti-HPA, především anti-HPA-5b, -3a, -15. Byly publikovány i případy, kdy NAITP indukovaly specifické anti-HLA protilátky [4, 5, 9, 10, 11, 12, 15, 16, 19]. Trombocytopenie způsobená přítomností těchto protilátek spontánně odeznívá obvykle do 4 týdnů [15]. Nejzávažnější komplikaci představuje intrakraniální krvácení u plodu, které se vyskytuje přibližně 1 na 20 000 porodů (zejména u anti-HPA-1a, -3a pozitivních žen) [5, 9, 10]. V naší populaci jsou přibližně 2 % HPA-1a negativních žen (genotyp HPA-1b/1b), asi u 10 % z nich dochází k aloimunizaci, tj. tvorbě anti-HPA-1a protilátky [10].
SOUBOR PACIENTŮ A METODIKA
V rámci požadavků na imunohematologické vyšetření u žen krátce po porodu nebo během těhotenství jsou v Krevním centru FNO vyšetřovány protilátky proti trombocytům a leukocytům. Ročně je provedeno přibližně 300 vyšetření. V případě pozitivity ve screeningovém testu zachytávajícím protilátky proti trombocytům není možné určit, o jaký typ protilátky jde (aloimunní anti-HLA, anti-HPA, auto-/panreaktivní trombocytární protilátky, eventuálně falešnou pozitivitu). Pro rozlišení a identifikaci aloimunních HLA a HPA protilátek jsou v ČR k dispozici komerční testy – PAK 12 nebo kity MACE (MACE 1 a MACE 2) od firmy GTI (GTI Diagnostics, Brookfield, USA). V Krevním centru FNO jsme v praxi vyzkoušeli oba typy testů.
V roce 2007 bylo testem MACE 1 a MACE2 vyšetřeno 22 vybraných gravidních žen pozitivních ve screeningových testech zachycujících trombocytární protilátky (ELISA – enzym linked immunosorbent assay, DIFT – destičkový imunofluerescenční test) včetně jedné ženy po porodu indikované k vyšetření na základě trombocytopenie u novorozence. ELISA test PAK 12 je využíván rutinně od konce roku 2009. Dosud jím bylo vyšetřeno 28 gravidních nebo žen po porodu, pozitivních ve screeningovém vyšetření zachycujícím trombocytární protilátky (ELISA, DIFT) a 6 žen po porodu indikovaných k vyšetření na základě trombocytopenie u novorozence.
Při sérii analýz jak testem MACE, tak PAK12 byla identifikována anti-HPA-1a protilátka, nejčastější příčina FMAIT (vždy jedenkrát). Vyšetření bylo doplněno genotypizací HPA znaků. V roce 2008 a 2009, před zavedením rutinního testování kitem PAK 12, byla u gravidních s pozitivním DIFT (případně zároveň ELISA či LCT testem) prováděna křížová zkouška (cross-match) mezi trombocyty otce a sérem matky, doplněná genotypizací HPA znaků obou rodičů. Kombinace vyšetření anti-HLA/-HPA protilátek testem PAK 12 s HPA genotypizací matky případně dítěte či otce, která byla zavedena ke konci roku 2009, napomáhá při potvrzení či vyloučení přítomnosti specifických aloimunních HPA protilátek, z nichž anti - HPA-1a a anti HPA-5b jsou nejčastější příčinou neonatální aloimunní trombocytopenie u plodu [1, 9, 14].
Pro screening protilátek byly provedeny tyto testy:
LCT – lymfocytotoxický test (standardizovaný podle National Institutes of Health – NIH, detekce komplement dependentních anti-HLA protilátek), ELISA – enzym linked immuno sorbent assay (zachycuje protilátky proti trombocytům aktivovaným adhezí), DIFT – destičkový imunofluorescenční test (zachycuje všechny protilátky reagující s trombocyty) [20], GAT – granuloaglutinační test (detekuje protilátky proti granulocytům).
K identifikaci protilátek byly testovány kity:
PAK 12 (ELISA technika, GTI Diagnostics, Brookfield, USA) – odlišení HLA protilátek od anti-HPA a/nebo identifikace specifických trombocytárních protilátek (anti-HPA-1,-3,-4a, -5); MACE 1 a MACE 2 (Modified Antigen Capture ELISA, GTI Diagnostics, Brookfield, USA) – odlišení anti-HLA protilátek od anti-HPA anebo identifikace specifických trombocytárních protilátek.
Jako doplňující vyšetření byla provedena HPA-1, -2, -3, -4, -5, -15 genotypizace metodou PCR-SSP (polymerázová řetězová reakce se sekvenčně specifickými primery) kity firmy BAG Health Care (Německo) a křížová zkouška (DIFT cross-match) mezi sérem/plazmou matky a trombocyty otce.
VÝSLEDKY
V roce 2007 bylo testem MACE 1 a MACE 2 vyšetřeno 22 gravidních žen vybraných pro pozitivitu při screeningu v destičkovém imunofluorescenčním testu a/nebo pro pozitivitu v trombocytovém ELISA testu či LCT. MACE 1 a MACE 2 jsou testy technicky a časově náročnější než test PAK12 vzhledem k nutnosti přípravy testovacích trombocytů (součástí kitu jsou lyofilizované trombocyty určené pouze pro pozitivní a negativní kontrolu). MACE 1 je určen pro záchyt HLA protilátek proti antigenům I. třídy a k detekci protilátek proti GPIIa/IIIa, respektive HPA epitopům nacházejícím se na těchto glykoproteinech (tj. HPA-1, HPA-3, HPA-4, HPA-7, HPA.9, HPA-10). MACE 2 je určen pro identifikaci protilátek proti GPIa/IIa (epitop HPA-5), IV a IIb/IX (epitop HPA-2). Pro testování byla připravena suspenze trombocytů od dárců krve (krevní skupina 0), u kterých byla provedena HPA genotypizace (směs trombocytů obsahovala tyto znaky: HPA-1a/a, HPA-2a/a, HPA-3a/b, HPA-4a/a, HPA-5a/a, HPA-15a/b). Výsledky testování kitem MACE 1 a MACE 2 jsou uvedeny v tabulce 1.
1. Souhrn výsledků screeningových testů a identifikačních testů MACE 1 a MACE 2 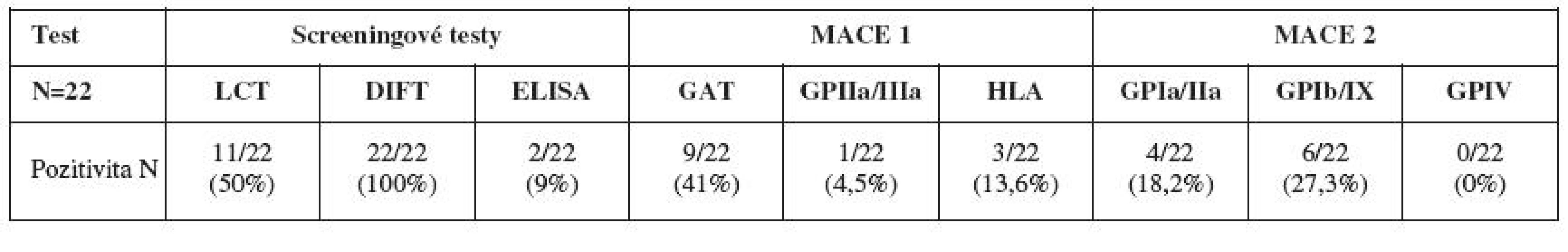
V roce 2008–2010 bylo provedeno celkem 1057 screeningových vyšetření (viz tab. 2). V roce 2008 a 2009 byl u vybraných gravidních či žen po porodu pozitivních v DIFT a/ nebo pozitivních také v ELISA nebo LCT testu, proveden cross-match mezi trombocyty otce a plazmou/sérem matky a zároveň genotypizace HPA znaků matky či obou rodičů. Takto bylo vyšetřeno 9 párů. V 15 případech byla provedena HPA genotypizace pouze u matky (tab. 3). U dvou matek, nositelek genotypu HPA-1b/1b, nebyla přítomnost protilátky anti-HPA-1a testováním kitem PAK 12 respektive křížovou zkouškou ani opakovaným screenigem (DIFT) potvrzena (tab. 3). Výše uvedenou kombinací testování často nebylo možné vyloučit přítomnost protilátek anti-HPA-5b (11krát), tj. druhé nejfrekventovaněji uváděné příčiny FMAIT [12, 13] a také vyloučení anti-HPA-15a/b (8krát). Vzhledem k problematičtější interpretaci a skutečnosti, že náběry pro doplnění vyšetření o HPA genotypizaci rodičů a křížovou zkoušku nebyly často na naše pracoviště dodány, zavedli jsme ke konci roku 2009 rutinní testování specifických protilátek proti trombocytům (anti-HPA) kitem PAK 12 (tab. 3).
2. Screeningová vyšetření u těhotných nebo matek po porodu 
3. Speciální vyšetření u těhotných nebo matek po porodu 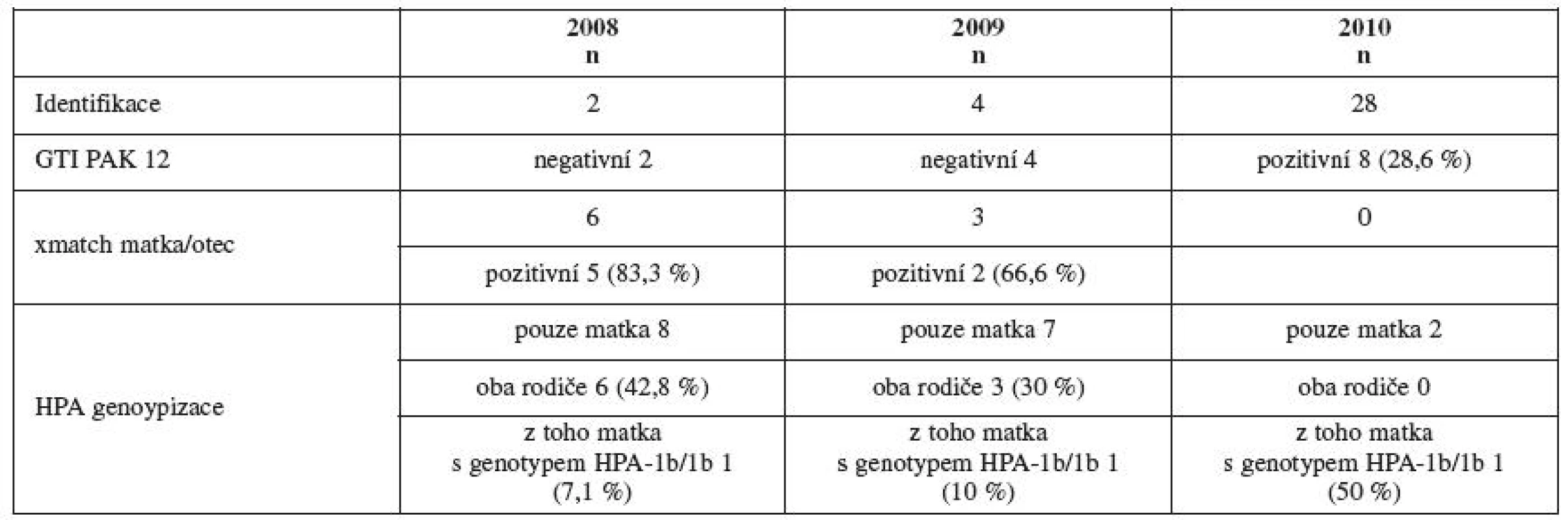
DISKUSE
MACE 1 a MACE 2 test je ve srovnání s PAK 12 finančně, časově i technicky náročnější. Pro identifikaci nejčastějších respektive klinicky nejzávažnějších protilátek z hlediska rozvoje FMAIT se testování pouze kitem MACE 1 (anti-HPA-1a a anti-HPA-3a) jeví jako nedostačující, je nutno použít také kit MACE 2 (identifikace anti-HPA-5b). Proto postup, při kterém na základě pozitivity v DIFT případně současně v ELISA či LCT testu, následuje potvrzení pozitivity testem PAK 12, se v běžné praxi osvědčil lépe. Podle některých studií může hladina specifických trombocytárních protilátek během těhotenství kolísat [2, 11] anebo se mohou vyskytnout časné přechodné protilátky bez klinického významu [21]. Kvůli vyloučení falešně pozitivních (nespecifických) reakcí, které se u tohoto typu testu mohou vyskytnout [13] respektive pro potvrzení přítomnosti specifické protilátky je potřeba vždy provést i HPA genotypizaci matky a otce (před porodem) anebo dítěte (po porodu), eventuálně testování kitem PAK 12 opakovat, a navíc doplnit křížovým testem mezi sérem matky a trombocyty otce. GTI-PAK 12 je široce užívaný spolehlivý screeningový test, který je díky své jednoduchosti vhodný zejména pro menší rutinní laboratoře [6, 17, 22]. Nevýhodou komerčního kitu PAK 12 je, že jím nelze zachytit protilátky proti antigenu HPA-15 respektive protilátky proti antigenům trombocytů s velmi nízkou frekvencí výskytu, které také mohou být klinicky relevantní. Na jejich přítomnost pak můžeme usuzovat pouze z výsledků HPA genotypizace, z opakované pozitivity v DIFT (při LCT testu negativním) a z pozitivní křížové zkoušky mezi trombocyty otce a sérem matky. V takových případech je potřeba zorganizovat vyšetření v (referenční) laboratoři využívající techniky, které detekci těchto protilátek umožňují.
ZÁVĚR
Na národní a mezinárodní úrovni zatím neexistují jednotné guidelines pro postup při identifikaci respektive stanovení protilátek vedoucích k NAITP. Na druhé straně existuje několik in house a komerčních testů k zachycení a identifikaci aloimunních anti-HPA a anti-HLA protilátek majících různou citlivost, specificitu a své výhody či omezení [22]. V Krevním centru FNO jsou imunhematologická vyšetření prováděna u rizikových pacientek na základě požadavku gynekologů a dále při nálezu trombocytopenie u novorozenců. Postup vyšetření, při kterém na základě pozitivity v DIFT a/nebo ELISA a/nebo lymfocytotoxického testu následuje vyšetření kitem PAK 12, v indikovaných případech doplněných o genotypizaci HPA systému anebo křížovou zkoušku mezi trombocyty otce a sérem matky, se v praxi Krevního centra jeví zatím jako dostačující. S přibývajícími praktickými zkušenostmi a přibývajícími komerčními detekčními technikami lze očekávat další úpravy v postupu při potvrzování diagnózy NAITP.
MUDr. Zuzana Čermáková, Ph.D.
Krevní centrum FN Ostrava
17. listopadu 1790
708 52 Ostrava
e-mail: zuzana.cermakova@fno.cz
Sources
1. Ahya, R., Turner, ML., Urbaniak, SJ., SNAIT Study Team. Fetomaternal alloimmune thrombocytopenia. Tranfus Apher Sci, 2001, 25, p. 139-145.
2. Bertrand, G., Martageix, C., Jallu, V., et al. Predictive value of sequential maternal anti-HPA-1a antibody concentrations for the sseverity of fetal alloimmune thrombocytopenia. J Thromb Haemost, 2006, 4, p. 628-637.
3. Blanchette, VS., Chen, L., de Friedberg, ZS. Alloimmunization to the PlA1 platelet antigen: results of a prospective study. Br J Haematol, 1990, 74, p. 209-215.
4. Blanchette, VS., Johnson, J., Rand, M. The management of alloimmune neonatal thrombocytopenia. Bailliére’s Best Pract Res Clin Haematol, 2000, 13, p. 365-390.
5. Davoren, A., Curtis, BR., Aster, RH., McFarland, JG. Human platelet antigen-specific alloantibodies implicated in 1162 cases of neonatal alloimmune thrombocytopenia. Transfusion, 2004, 44, p. 1220-1225.
6. Davoren, A., McFarland, JG., Crowley, J., et al. Antenatal screening for human platelet antigen-1a: result of a prospective study at a large maternity hospital in Ireland. Brit J Obstet Gynaec, 2003, 110, p. 492-496.
7. Dreyfus, M., Kaplan, C., Verdy, E. Frequency of immune thrombocytopenia in newborns: a prospective study. Immune Thrombocytopenia Working Group. Blood, 1997, 89, p. 4402-4406.
8. Durand-Zaleski, I., Schlegel, N., Blum-Boisgard, C. Screening primiparous women and newborns for fetal/neonatal alloimmune thrombocytopenia: a prospective comparison of effectiveness and costs. Immune Thrombocytopenia Working Group. Am J Perinatol, 1996, 13, p. 423-431.
9. Ghevaert, C., Campbell, K., Walton, J., et al. Management and outcome of 200 cases of fetomaternal alloimune thrombocytopenia. Transfusion, 2007, 47, p. 901-910.
10. Kiefel, V., Bassler, D., Kroll, H., et al. Antigen-positive platelet transfusion in neonatal alloimmune thrombocytopenia (NAIT). Blood, 2006, 107, p. 3761-3763.
11. Killie, MK., Husebekk, A., Kjeldsen-Kragh, J., Skogen, B. A prospective study of maternal anti-HPA 1a antibody level as a potential predictor of alloimmune thrombocytopenia in the newborn. Haematol, 93, 6, p. 870-877.
12. Koch, K., Stenzel, A., Bringman, G., et al. Neonatal alloimmune thrombocytopenia (NAIT) in twins caused by maternal HLA antibodies anti-HLA-A2 and anti-HLA-A68. Vox Sanguinis 2010, 99, Suppl. 1, p. 397.
13. Leach, MF., Aubuchon, JP. False reactivity in GTI Pak Plus ELISA kits due to the presence of anti-mouse antibody in patiens samples. Immunohematology 2003, 19, p. 112-116.
14. Mandelbaum, M., Koren, D., Eichelberger, L., et al. Frequencies of maternal platelet alloantibodies and autoantibodies in suspected fetal/neonatal alloimmune thrombocytopenia, with emphasis on human platelet antigen-15 alloimmunization. Vox Sang, 2005, 89, p. 39-43.
15. Mueller-Eckhardt, C., Kiefel, V., Grubert, A., et al. 348 cases of suspected neonatal alloimmune thrombocytopenia. Lancet, 1989, 1, p. 363-366.
16. Moncharmont, P., Dubois, V., Obegi, C., et al. HLA antibodies and neonatal alloimmune thrombocytopenia. Acta Haematol, 2004, 111, p. 215-220.
17. Munizza, M., Nance, S., Keashen-Schnell, MA., et al. Provosion of HPA-1a (PLA1)-negative platelets for neonatal alloimmune thrombocytopenia: screening, testing, and transfusion protocol. Immunohematology, 1999, 15, p. 71-74.
18. Porcelijn, L., van den Akker, ES., Oepkes, D. Fetal thrombocytopenia (Review). Semin Fetal Neonatal Med, 2008, 13, p. 223-230.
19. Saito, S., Ota, M., Komatsu, Y., et al. Serologic analysis of three cases of neonatal alloimmune thrombocytopenia associated with HLA antibodies. Transfusion, 2003, 43, p. 908-917.
20. von dem Borne, AE., Verheugt, FW., Oosterhof, F., et al. A simple immunofluorescence test for the detection of platelet antibodies. Br J Haematol, 1978, 39, p. 195-207.
21. Williamson, LM., Hacket, G., Rennie, J., et al. The natural history of fetomaternal alloimmunization to the platelet-specific antigen HPA-1a (PlA1, Zwa) as determined by antenatal screening. Blood, 1998, 92, p. 2280-2287.
22. Wu, GG., Kaplan, C., Curtis, BR., Pearson, HA. Report on the 14th international society of blood transfusion platelet immunology workshop. Vox Sanguinis, 2010, 99, p. 375-381.
Labels
Paediatric gynaecology Gynaecology and obstetrics Reproduction medicine
Article was published inCzech Gynaecology

2011 Issue 3-
All articles in this issue
- Primary drug resistance/sensitivity in vitro and clininical outcome in ovarian cancer patients
- Predictors of combined hormone contraception choice between Czech and Slovak women
- Prognostic importance of selected molecular genetic immunohistochemical markers and DNA ploidy in endometrial cancer
- Psychosocial factors influencing the perinatal health care satisfaction of parturients
- Spontaneous preterm birth in mother in an artificial sleep on ECMO with severe form of H1N1 infection
-
Guideline gynekologických zhoubných nádorů 2010
Primární chirurgická léčba zhoubných nádorů endometria - Risk-reducing surgery in women at hereditary risk of gynaecological cancer
- Biophysical methods in diagnosis of intrapartal fetal hypoxia
- Advanced maternal age as a sole indication for amniocentesis – analysis of 418 fetal karyotypes
- High resistance of bacterial strains Streptococcus agalactiae to antibiotic therapy in early-onset and late-onset disease in newborns
- Optimization of antibodies examanination against thrombocytes in pregnant and postpartum women
- Hereditary susceptibility to endometrial cancer
- The role of hysterectomy in management of cervical precancer lesions
- Czech Gynaecology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- High resistance of bacterial strains Streptococcus agalactiae to antibiotic therapy in early-onset and late-onset disease in newborns
- Optimization of antibodies examanination against thrombocytes in pregnant and postpartum women
- Biophysical methods in diagnosis of intrapartal fetal hypoxia
- The role of hysterectomy in management of cervical precancer lesions
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

