-
Medical journals
- Career
Ashermanův syndrom I – historie, prevalence, histopatologie, klasifikace, etiologie, symptomatologie a vyšetřovací metody
Authors: L. Hrazdírová; D. Kužel; Z. Žižka
Authors‘ workplace: Gynekologicko-porodnická klinika VFN a 1. LF UK, Praha, přednosta prof. MUDr. A. Martan, DrSc.
Published in: Ceska Gynekol 2010; 75(6): 492-498
Overview
Cíl:
Souhrnně prezentovat aktuální znalosti o Ashermanově syndromu – historické souvislosti, prevalenci, histopatologii, klasifikaci, etiologii, symptomatologii a používané vyšetřovací metody.Typ studie:
Přehled.Název a sídlo pracoviště:
Gynekologicko-porodnická klinika Všeobecné fakultní nemocnice a 1. lékařské fakulty Univerzity Karlovy, Praha.Metodika a výsledky:
V souborném článku jsou prezentovány historické souvislosti definice Ashermanova syndromu. Ashermanův syndrom je způsoben fibrotizací endometria – nejčastějším etiologickým faktorem je trauma v souvislosti s graviditou, v malém procentu mohou adheze vznikat i na netěhotné děloze. Jeho prevalence výskytu závisí na mnoha faktorech – počtu ilegálních a terapeutických potratů, procentu zánětů v souvislosti s graviditou, indikačních kritérií aj. Pouze v případě genitální tbc a schistosomózy vznikají adheze bez nitroděložního traumatu, v jiných případech nebyl samostatný vliv zánětu prokázán. Mezi příznaky Ashermanova syndromu kromě anamnézy nitroděložního výkonu patří nepravidelnosti menstruace (hypomenorea, amenorea), sterilita, infertilita a komplikace těhotenství (např. opakované potraty, poruchy placentace atd.). V průběhu času byly popsány různé klasifikace, které závisí hlavně na zvolené diagnostické metodě. Slibnou diagnostickou metodou je sonohysterografie, ale zlatým standardem vyšetřovacích metod je hysteroskopie, umožňující současně i terapii.Závěr:
Ashermanův syndrom je závažné onemocnění, které významně ovlivňuje možnost ženy otěhotnět a donosit zdravý plod.Klíčová slova:
Ashermanův syndrom, nitroděložní adheze, sterilita, hysteroskopie.ÚVOD
Historie definice posttraumatického děložního syndromu je stará přibližně 100 let.
Rozvoj sekundární amenorey po postpartální kyretáži byl prvně popsán Heinrichem Fritschem již v roce 1894 [13]. V roce 1927 byla publikována studie s 1500 pacientkami, které podstoupily indukovaný potrat, u 20 z nich šlo o obstrukci děložního kanálu [5]. Nejvýznamněji se ale o rozvoj poznatků o posttraumatických nitroděložních adhezí zasloužil Joseph G. Asherman. Od roku 1948 publikoval sérii článků, které popsaly frekvenci, etiologii, symptomy a rentgenové obrazy tohoto syndromu. S postupem času bylo publikováno mnoho dalších studií, což souviselo s rozvojem endoskopické techniky – zaměřovaly se na diagnostiku, terapii a reprodukční výsledky [3, 4].
Asherman sám definoval tento syndrom jako částečný nebo úplný adhezivní proces v dutině děložní nebo v děložním kanále, který se projevuje menstruačními obtížemi, infertilitou nebo opakovanými těhotenskými ztrátami a je v přímé souvislosti s nitroděložním traumatem.
V roce 1995 byla do klasifikace Ashermanova syndromu Evropskou společností pro gynekologickou endoskopii zařazena i tzv. fibróza dutiny děložní. Fibróza může být pouze mírná, povrchová, nebo rozsáhlá a zasahující hluboko do myometria. Nemusí být přítomny nitroděložní adheze. Průkaz fibrózy je vždy založen na histologické verifikaci [43].
Ke stanovení diagnózy Ashermanova syndromu by měly být splněny dvě podmínky:
- Přítomnost jednoho nebo více klinických příznaků (menstruační patologie charakteru amenorey, nebo hypomenorey, těhotenské patologie – infertilita či sterilita, opakované těhotenské ztráty, nebo historie abnormální placentace – zahrnující placentu previa nebo accreta).
- Druhou podmínkou je průkaz intrauterinních adhezí (ideálně diagnostikovaných hysteroskopicky), nebo histologický průkaz intrauterinní fibrózy [49].
PREVALENCE
Prevalenci Ashermanova syndromu je v obecné populaci obtížné hodnotit – liší se v různých studiích podle zvolené vyšetřovací metody a typu populační studie. V roce 1982 Schenker a Margolioth revidovali 90 studií, ve kterých bylo popsáno 2981 případů Ashermanova syndromu v různých zemích. Vyšší incidence byla popsána v Izraeli, Řecku a v Jižní Americe. Autoři zhodnotili geografickou odlišnost přítomnosti adhezí a uzavřeli, že závisí na zkušenosti kliniků, počtu ilegálních a terapeutických potratů v různých částech světa a procentu využití tupé, ostré kyrety a sukční evakuace dutiny děložní po porodu a potratu. Dalším faktorem, který ovlivňuje incidenci, je četnost případů genitální tuberkulózy a puerperální infekce [31, 49]. U vybraných pacientek, které byly doporučeny k hysterosalpingografii je popsáno kolem 1,5 % Ashermanova syndromu [2]. U infertilních pacientek, které byly vyšetřovány sonohysterograficky byla popsána prevalence 0,3 % [40].
U žen s opakovanými těhotenskými ztrátami vyšetřených hysteroskopicky byly intrauterinní adheze diagnostikovány u 7 až 21,8 % [42, 45].
HISTOPATOLOGICKÉ SOUVISLOSTI
Ashermanův sydrom je způsoben fibrotizací endometria – endometriální stroma je nahrazeno fibrózní tkání a žlázky jsou tvořeny neaktivním kubo-kolumnárním epitelem endometriálního typu. Odlišnost mezi funkcionální a bazální vrstvou endometria je ztracena a funkcionální vrstva je nahrazena jednobuněčným epitelem, který není schopen reagovat na hormonální stimulaci a v dutině děložní se tvoří fibrózní synechie. Dále může dojít ke kalcifikaci, a dokonce osifikaci stromatu, žlázky zřídnou a inaktivují se a cysticky se dilatují. Vaskularizace může být hojná, vyskytují se tenkostěnné dilatované cévy, často je však tkáň avaskulární [49].
Adheze mohou zahrnovat různé vrstvy endometria, myometria a pojivové tkáně. Adheze odvozené z každé z těchto tkání se projevují charakteristickým hysteroskopickým obrazem – slizniční adheze vypadají podobně jako okolní endometrium, myofibrózní adheze, se kterými se často setkáváme, jsou charakteristické přítomností tenké vrstvy endometria, která je pokrývá, povrch je pokryt mnoha ústími žlázek. Povrch adhezí z pojivové tkáně a fibrózní adheze postrádají endometriální vrstvení, a kontrastují tak s přilehlým endometriem [2].
Při bioptickém vyšetření celé tlouštky myometria Yaffe prokázal, že děložní stěna u těchto pacientek obsahuje 50–80 % fibrózní tkáně v porovnání s 13–20 % v kontrolní skupině zdravých pacientek [47]. March předpokládal, že fibróza limituje aktivitu myometria a snižuje prostupnost pro pohlavní steroidy, což vede k atrofii. Někdy se může fibróza endometria vyvinout bez zjevných nitroděložních adhezí [20].
Histologicky podobné Ashermanovu syndromu jsou nálezy po transcervikální resekci endometria (TCRE). Po TCRE se k fibróze často přídávají další nálezy – epiteloidy z cizích tělních granulomů, kolekce hemosiderinu a pigmentů a méně často nekrotizující granulomatózní zánět [21, 33].
KLASIFIKACE
Během času bylo vytvořeno několik klasifikací, které jsou založeny na rozdílných diagnostických přístupech.
Základním rozdělením je klasifikace podle lokalizace:
- totální atrézie (obliterace celé děložní dutiny i děložního hrdla),
- korporální adheze,
- cervikoistmické adheze – způsobující blokádu děložního hrdla [2].
V roce 1978 byla vytvořena klasifikace hysterosalpingografického semikvantitativního průkazu intrauterinních adhezí [39].
S příchodem hysteroskopie bylo publikováno několik klasifikací v závislosti na rozsahu adhezí a vizualizaci tubárních ústí.
V roce 1988 American Fertility Society (AFS) publikovala objektivní skórovací systém, ve kterém jsou zohledněny hysteroskopické a hysterosalpingografické nálezy spolu s menstruační anamnézou pacientky [38] (tab. 1).
Table 1. Klasifikace nitroděložních adhezí podle American Fertility Society (AFS, 1988) 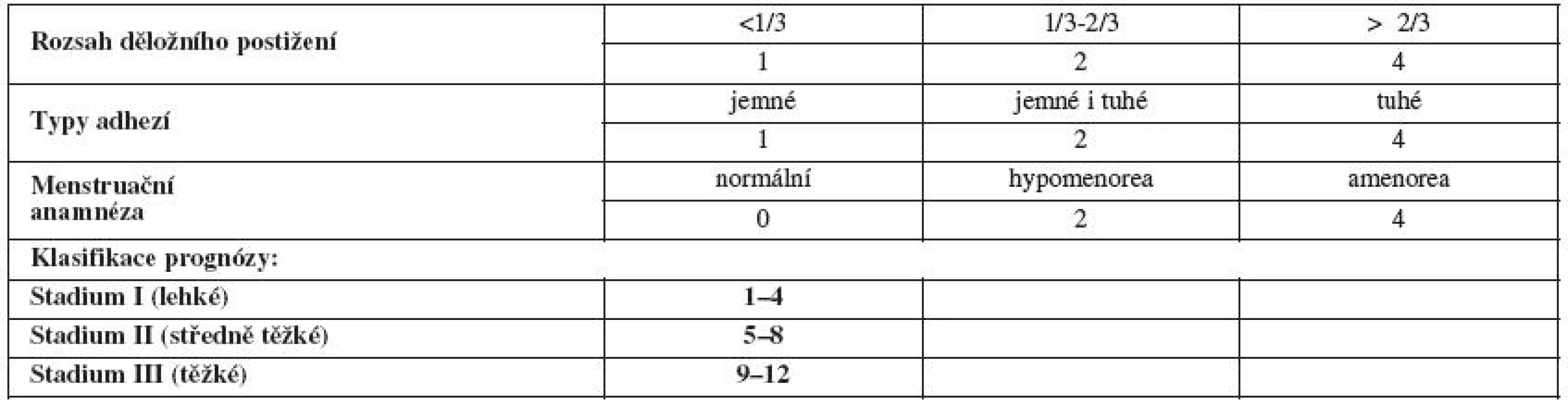
Zdroj: The American Fertility Society classifications of adnexal adhesions distal tubal occlusion, tubal occlusion secondary to tubal ligation, tubal pregnancies, Mullerian anomalies and intrauterine adhesions. Fertil Steril, 1988, 49, p. 944-955. V roce 1989 Evropská společnost pro hysteroskopii (ESH) publikovala klasifikaci intrauterinních adhezí – čistě makroskopický popis dutiny děložní a adhezí, bez vlivu intenzity menstruačního krvácení [43] (tab. 2).
Table 2. Klasifikace adhezí podle European Society for Hysteroscopy (ESH) 1989 
Zdroj: Wamsteker, K., De Block, S. Diagnostic hysteroscopy: technique and documentation. In: Sutton, C., Diamond, M., eds. Endoscopis Surgery for Gynecologists. London, UK, Saunders, 1993, p. 263-276. V roce 1995 vydala Evropská společnost pro gynekologickou endoskopii (ESGE) revidovanou verzi klasifikace intrauterinních adhezí [44], kde již byla zahrnuta i fibróza endometria (tab. 3).
Table 3. Klasifikace nitroděložních adhezí podle European Society for Gynecologic Endoscopy (ESGE, 1995) 
Zdroj: Wamsteker, K., De Block, S. Diagnostic hysteroscopy:technique and documantation. In Sutton, C., Diamond, M., eds. Endoscopic surgery for gynecologists. London: WB Sauders, 1998, p. 511-524. V roce 2000 Nasr publikoval klasifikační systém, který zařazuje i klinické projevy, hysteroskopické nálezy a reprodukční anamnézu, se snahou predikovat reprodukční šance [23] (tab. 4).
Table 4. Hysteroskopicko-klinická klasifikace (Nasr, 2000) 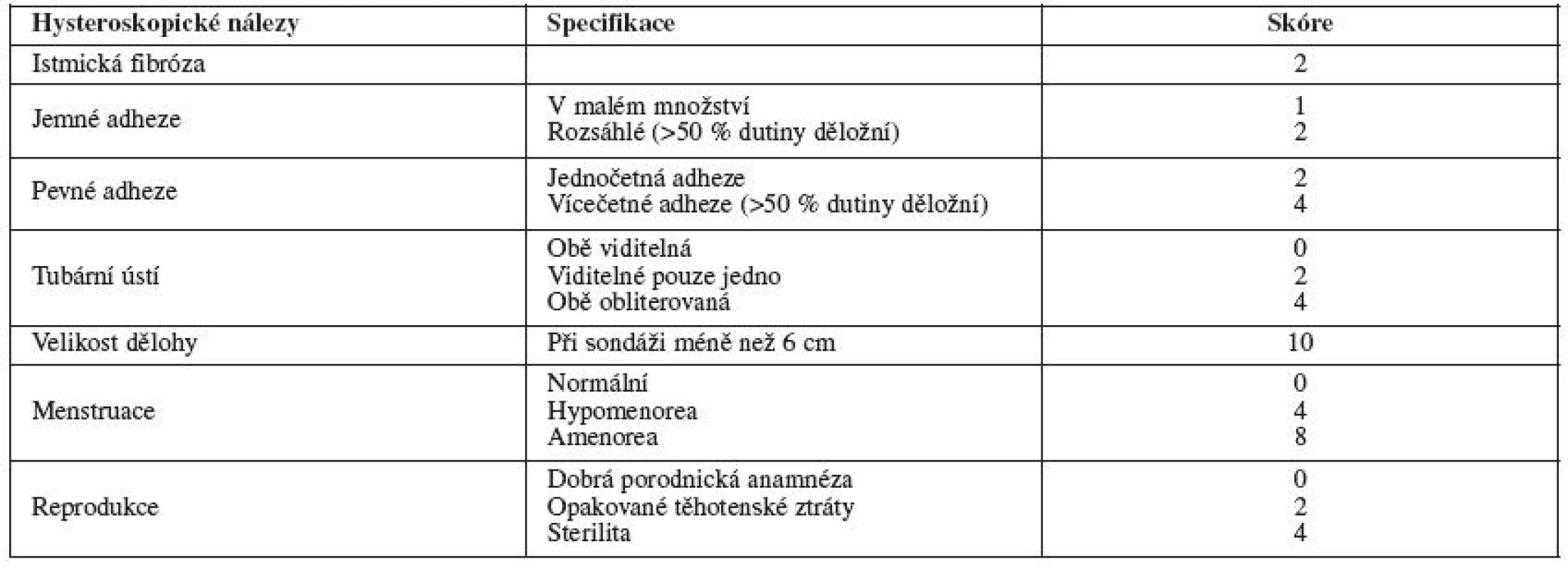
Výsledky: 0-4 body – dobrá prognóza; 5-10 bodů – střední prognóza; 11-22 – špatná prognóza Zdroj: Nasr, AL., Al-Inany, HG., Thabet, SM., et. al. A clinicohysteroscopic scoring systém of intrauterine adhesions. Gynecol Obstet Invest., 2000, 50, p. 178-181. Každá z těchto klasifikací má své výhody i nevýhody, nejčastěji jsou využívány klasifikace AFS a ESGE.
ETIOLOGIE
Trauma těhotné dělohy
Trauma těhotné dělohy je nejčastější příčinou Ashermanova syndromu – intrauterinní výkon v postpartálním období nebo revize po potratu či císařském řezu.
Podle revize Schenkera z 1856 případů Ashermanova syndromu bylo těhotenství hlavním predisponujícím faktorem v 90,8 %, z této skupiny byl Ashermanův syndrom způsoben revizí po spontánním potratu nebo interrupci v 66,7 %, revizí v postpartálním období 21 %, ve 2 % po císařském řezu a v 0,6 % po evakuaci dělohy pro mollu [31, 32].
Jedním z možných etiologických faktorů je nízká hladina estrogenů v období operace – regenerace endometria je závislá na estrogenech, tento fakt však zatím nebyl podpořen studií s dostatečným počtem pacientek [46]. Taskin na rozdíl od Westendorpa žádný rozdíl mezi skupinou estrogensuprimovaných a nesuprimovaných žen neprokázal [37].
Jiným možným vysvětlením mohou být fyziologické změny, které se objevují v těhotné děloze – v období gravidity je pravděpodobně zranitelnější bazální vrstva endometria [49].
V několika studiích byl popsán vznik intrauterinních adhezí po revizi dutiny děložní po spontánním abortu v prvním trimestru – po jednom potratu byla incidence intrauterinních adhezí 16,3 %, po 3 a více abortech to bylo 32 % [11]. Jiná studie prokázala, že není rozdíl v procentu vzniku adhezí po výkonu pro inkompletní abort a pro missed abortion. Tato studie také potvrzuje výrazně vyšší procento IUA u pacientek s opakovanými těhotenskými ztrátami proti ženám po jednom potratu (47,6 % vs. 18,8 % [26].
Po spontánním porodu a prosté manuální lýze bylo riziko vzniku IUA popsáno ve 2 % [14]. Westendorp ve své studii z roku 1998 popisuje skupinu pacientek po revizi dutiny děložní s odstupem delším než 24 hodin po porodu – v této skupině popisuje riziko IUA 40 %, z toho stupně II–IV – ve 30 % [46].
Schenker a March 1996 popisuje i závislost na časování intrauterinního výkonu – vyšší riziko udává při postpartální kyretáži ve 2.,3. a 4. týdnu po porodu [20, 32].
Trauma u netěhotné dělohy
V Schenkerově souboru byly popsány i případy vzniku nitroděložních adhezí po diagnostické kyretáži (1,6 %), abdominální myomektomii (1,3 %), cervikální biopsii, polypektomii (0,5 %), inzerci nitroděložního tělíska (0,2 %) a po radiaci (0,05 %) [31]. Nitroděložní srůsty mohou být způsobeny i různým typem hysteroskopické operativy – v randomizované studii o 95 pacientkách, které podstoupily různé formy hysteroskopické operace byla popsána incidence IUA: po resekci děložního septa v 6,7 %, po resekci jednoho nebo více submukózních myomů byl vznik IUA ve 31,3 a 45,5 % [37]. Yang popsal závislost vzniku IUA nejen na počtu resekovaných myomů, ale i na uložení resekovaných myomů v dutině děložní, při resekci solitárního myomu vznikly IUA u 1,5 % žen, ve skupině pacientek, které měly početné myomy na přiléhajících stranách dutiny děložní byly IUA prokázány v 78 % [48].
Vznik IUA byl popsán i u pacientek po embolizačních metodách pro myomatózu [19], a to ve 14 %. Kazuisticky byl popsán i vznik závažného Ashermanova syndromu po devaskularizační operaci pro těžké postpartální krvácení [25].
Dalším intrauterinním výkonem, po kterém vznikají nitroděložní adheze relativně často, je ablace a termoablace endometria. Po termoablaci endometria balonovou metodou byla formace intrauterinních adhezí popsána ve 36,4 % a fibróza dutiny děložní v 18 % [17].
Infekce
Mechanismus vzniku Ashermanova syndromu samotnou infekční noxou nebyl dosud přesně prokázán. Mnozí se domnívají, že základem každého Ashermanova syndromu je akutní nebo subakutní endometritida [7], v jiných studiích je prezentován opačný názor, který staví na práci Polishuka, jenž studoval 171 žen, které podstoupily císařský řez – 28 z nich mělo prokázanou endometritidu. Hysterosalpingografie, která v odstupu následovala, neukázala signifikantní rozdíl v přítomnosti adhezí mezi skupinou se zánětem a bez něj. Studie byla ukončena se závěrem, že zánět zřejmě není hlavní faktor v patogenezi intrauterinních a cervikálních adhezí [24]. Jiní autoři ale věří, že zánět přispívá k destruktivnímu efektu traumatu, který nakonec vede ke vzniku adhezí, není to však podpořeno statisticky významnou skupinou pacientek [46].
Shaffer se domnívá, že zásadní roli v tvorbě adhezí hrají spolu se zánětem rezidua po předchozí graviditě [30].
Jedinou objektivně prokázánou infekcí, která samostatně, bez jiného vlivu způsobuje IU adheze, je genitální tuberkulóza – poprvé byla tato souvislost popsána v roce 1956. Genitální tuberkulóza často končí úplnou obliterací děložní dutiny a totální destrukcí endometria – které vede k amenoree a sterilitě [49]. V Schenkerově review byla genitální tuberkulóza popsána v 74 případech [31].
Bukulmez prezentuje studii 12 pacientek, u kterých došlo po genitální tbc ke vzniku Ashermanova syndromu – po hysteroskopické adheziolýze došlo k úplné obliteraci u všech pacietek. Autor uzavřel, že pokud je Ashermanův syndrom způsobený tuberkulózou, šance na obnovení fertility jsou minimální (6).
V jedné kazuistice byl také popsán případ Ashermanova syndromu způsobeného schistosomózou [16].
Vrozené vady dělohy
V roce 1985 Stillman a Asarkof publikovali práci, která se zabývala studiem infertilních párů a prokázala signifikantně významné spojení mezi Ashermanovým syndromem a malformacemi mulleriánských duktů, speciálně u uterus septus. Ze 43 pacientek, které měly vrozené vady, u 16 % byl diagnostikován Ashermanův syndrom. Není jisté, zda děložní malformace sama o sobě predisponuje k tvorbě děložních adhezí. Je však pravděpodobnější, že ženy s kongenitální děložní anomálií mají vyšší riziko opakovaných těhotenských ztrát a opakované obtížné revize dělohy zvyšují riziko tvorby adhezí [35].
SYMPTOMATOLOGIE
Mezi symptomy, kterými se Ashermanův syndrom může projevit, patří: nepravidelnosti menstruace, dysmenorea, periodické bolesti, sterilita, opakované těhotenské ztráty a další těhotenské komplikace [49].
Nepravidelnosti menstruace
Do této skupiny patří hypomenorea a amenorea – což jsou nejčastější klinické projevy spojené s Ashermanovým syndromem (u 68 % pacientek podle Shenkera); amenorea může být různého původu v závislosti na uložení adhezivního procesu: 1. obstrukce cervikálního kanálu blokující menstruační krvácení, 2. těžká fibróza endometria, která vede k destrukci bazální vrstvy. Dysmenorea se vyskytuje spíše příležitostně (3,5 % podle Shenkera). Atrézie děložního hrdla nebo části děložní dutiny s endometriem, která nekomunikuje s cervikálním kanálem, se může projevit periodickým dyskomfortem, bolestí, hematometrou a výjimečně a hematosalpingem [31, 49].
Sterilita
Shenker s Margoliothem ve své studii prokázali sterilitu u 43 % žen. Jednou možnou příčinou sterility je okluze tubárních ústí, děložní dutiny nebo cervikálního kanálu způsobené adhezivním procesem. Synechie mohou zabránit průniku spermie nebo oocytu a implantaci embrya [49].
Opakované těhotenské ztráty
Závažné stupně děložních adhezí způsobují obstrukci dutiny děložní a sterilitu. Mírnější stupně intrauterinních adhezí mohou být spojeny s opakovaným těhotenskými ztrátami. K etiologickým faktorům jistě patří zúžení dutiny děložní adhezemi, nedostatek funkční endometriální tkáně nezbytné pro implantaci a rozvoj placenty a v neposlední řadě nedostatečná vaskularizace reziduální endometriální tkáně na podkladě fibrózy endometria [49].
Ostatní těhotenské komplikace
V Schenkerově studii u neléčených žen s Ashermanovým syndromem byla popsána spontánní koncepce u 45,5 %. Spontánním potratem skončilo 40 % z těchto gravidit, 23 % žen porodilo předčasně, 30 % v termínu porodu [31].
Porucha placentace je jednou z nejčastějších a nejzávažnějších těhotenských komplikací. Velmi často končí závažným postpartálním krvácením a hysterektomií. Byl však popsán i případ úspěšné konzervativní terapie [15].
Defektní endometrium a obliterovaná dutina děložní zvyšuje riziko ektopické tubární a cervikální gravidity [9, 12].
Další komplikací je vyšší riziko předčasného porodu (Schenker 23 %) a IUGR. Nitroděložní růstová retardace plodu pravděpodobně souvisí se suboptimální placentací, která snižuje placentární perfuzi v průběhu těhotenství [49].
Jinou možnou komplikací gravidity u pacientek po operační terapii Ashermanova syndromu je ruptura děložní, která souvisí se zeslabenou a zjizvenou děložní stěnou po operaci, obzvláště pokud došlo v průběhu výkonu k perforaci. Byla však popsána ruptura dělohy v průběhu spontánního porodu ve 39. týdnu gestace i po nekomplikované remodelaci dutiny děložní resektoskopem (29).
Obecně jsou těhotenství u pacientek s Ashermanovým syndromem vysoce riziková. Je nezbytné pacientku, hlavně ve třetím trimestru pečlivě sledovat.
VYŠETŘOVACÍ METODY
Hysterosalpingografie
Před obdobím hysteroskopie byla hysterosalpingografie (HSG) první volbou k vyšetření tvaru děložní dutiny. Její výhodou je možnost zobrazit obrysy okludovaných oblastí, vyplnit defekty a zhodnotit oblasti děložních rohů, tubární kontury a průchodnost vejcovodů. V hysterosalpingografickém obraze se nitroděložní adheze jeví jako defekty, které jsou ohraničeny ostrými obrysy. Jsou uloženy centrálně nebo marginálně, mohou být nepravidelné a zahnuté. Častým nálezem je parciální obliterace děložní dutiny s nepravidelnými okraji a jedním nebo oběma okludovanými vejcovody. U závažných adhezí je dutina děložní zkroucená a úzká a obě tubární ústí jsou uzavřená. V případě obliterace dolní části děložní dutiny je nevýhodou HSG, že se dutina děložní neplní vůbec a HSG nám neposkytne validní výsledky. Tenké malé jemné adheze mohou být zobrazeny jako normální nález a také plynové bubliny a sliznice mohou imitovat defekty. Velké množství kontrastního média v dutině děložní může zničit nitroděložní stíny intrauterinních adhezí. Další významnou nevýhodou je i radiační zátěž [1, 49].
Úspěšnost hysterosalpingografie v diagnostice intrauterinních adhezí byla hodnocena v několika studiích. V retrospektivní studii – vyšetřovaných 400 pacientek byla prokázána hysterosalpingografie stejně úspěšná v diagnostice normální a abnormální děložní dutiny jako hysteroskopie, ale původ konkrétních nitroděložních patologií byl popsán až hysteroskopicky [10]. V dalších studiích, které porovnávají hysterosalpingografii s hysteroskopií jako zlatým standardem – je senzitivita HSG popisována od 75 do 81,2 % [8, 34], HSG měla 21,8 falešně pozitivních výsledků a 90 % falešně negativních, celková shoda mezi oběma metodami byla v 73 % [8].
Ultrasonografie
Jde o neinvazivní vyšetření, které dovoluje vizualizaci děložní dutiny. Výhodou je možnost vyšetření děložní dutiny v případě její obliterace, což je limitováno při HSG a hysteroskopii. Je-li obliterována pouze dolní část dělohy, pak průkaz endometria ve fundu je dobrým prognostickým faktorem.
U žen se závažnými adhezemi se mohou projevit následujícími obrazy: obtížně vizualizovatelné endometriální echo, s nepravidelnou sílou nebo jedno a vícečetná přerušení endometriálního povrchu v místech fibrózy. Také se může vyskytovat jedna nebo více cystických oblastí, které přerušují endometrium a reprezentují se kolekcí menstruační krve v místě, kde je funkční vrstva endometria zachována [49].
Fedele v roce 1996 prezentoval studii, ve které vyšetřoval 77 žen s opakovanými aborty, ženy byly transvaginálně ultrazvukem vyšetřovány v pokročilé sekreční fázi endometria a nitroděložní adheze byly identifikovány u 10 z 11 žen [11].
Shalev v roce 2000 prezentoval studii, ve které vyšetřil 74 pacientek, kromě jiných patologií u 10 z nich prokázal intrauterinní adheze – transvaginální ultrazvuk byl proveden v časné a pozdní folikulární fázi a prokázal je u 8 z 10 pacientek [28].
V jiných studiích jsou ale výsledky při diagnostice IUA pomocí TVS relativně špatné. Senzitivita i specificita ultrazvukové diagnostiky nitroděložních adhezí jsou nízké, senzitivita transvaginálního ultrazvuku je 52 % a specificita pouze 11 % [27].
Lo v roce 2008 prezentoval studii, kdy vyšetřoval pacientky s Ashermanovým syndromem a zjistil, že u těchto žen v místě, kde je zachované endometrium (např. v případě synechického hrdla) je toto endometrium signifikantně nižší než u kontrolní skupiny s normálním menstruačním cyklem (3,9 mm vs. 8,5 mm) [18].
Pokrokem ve využití ultrazvuku v gynekologii je sonohysterografie. Kombinuje transvaginální ultrazvuk s intrauterinní instilací fyziologického roztoku. Ukazuje se, že v detekci IU adhezí je srovnatelná s hysterosalpingografií. Při této technice je do dutiny děložní instilováno 20–30 ml fyziologického roztoku katétrem. Podezření na nitroděložní adheze je vysoké, pokud se zobrazí jedno nebo více hypoechogenních oblastí rozdělenými echogennějšími pruhy mezi přední a zadní stěnou děložní. Ve studii 19 pacientek s nitroděložními adhezemi byla prokázána senzitiva hysterosalpingografie a sonohysterografie v diagnostice adhezí, u obou 100%, a senzitivita u transvaginální sonografie byla pouze 52% [27]. V jiné studii na 65 ženách měla stejnou senzitivitu i specificitu sonohysterografie jako hysterosalpingografie, 75 % [34]. Sonohysterograficky je možné provést kompletní ultrazvukové vyšetření dutiny děložní a myometria. Toto všechno je použitelné pouze v případě vyšetření u parciální obstrukce děložní dutiny, protože fyziologický roztok není schopen proniknout do dutiny děložní v případě kompletní obstrukce. Sonohysterografie je metoda užitečná v situacích, kde transvaginální ultrazvuk zobrazuje normální nález, ale klinicky je vysoká suspekce na nitroděložní adheze.
3D ultrasonografické techniky byly použity několika investigátory v detekci nitroděložních adhezí se specificitou 45 % [36]. Jiná studie v případě vyšetření nitroděložních adhezí zobrazila 4 ze 6 případů [22].
Magnetická rezonance
Hlavní výhodou MRI je schopnost zobrazit dutiny děložní nad adhezemi, zobrazit rezidua endometria v horní části děložní dutiny, která mohou ovlivnit další postup v terapii. Naproti tomu MRI neumí zobrazit intrauterinní adheze detailně, adheze produkují signál malé intenzity v T2 obrazech. MRI by měla mít spíše doplňující roli v diagnostice kompletní obliterace děložní dutiny nebo cervikální obstrukce, která nemůže být zobrazena hysteroskopicky [49].
Hysteroskopie
Hysteroskopie v porovnání s radiologickými metodami nejlépe diagnostikuje rozsah a stupeň intrauterinních adhezí a kvalitu endometria, protože zhodnotí celou dutinu děložní. Superficiální slizniční adheze mají stejnou barvu jako okolní endometrium a mohou být jednoduše rozrušeny pohybem hysteroskopu. Fibrózní a myometrální adheze jsou bělavé a pevné a je obtížné je rozrušit. Adheze tuberkulózního původu působí jako síť malých alveol pokrývající děložní stěny, fundus může působit dojmem plástve medu. Endometriální fibróza vypadá v hysteroskopu jako bílé záplaty (49).
Není-li možné provést hysteroskopii dostatečně kvůli obliteraci dutiny děložní, je vhodné využít kombinace a provést hysteroskopickou adheziolýzu pod ultrasonografickou kontrolou. K rozlišení fibrózy a normální endometriální vrstvy lze použít metylenovou modř. Když je metylenová modř injikována přes vstupní kanál hysteroskopu – endometrium se zabarví dobře, oblast pojivové tkáně a myometrium se nezbarvují (41). Od používání methylenové modři se ale postupně odkláníme pro častější závažné alergické reakce, proto fibrózu verifikujeme histologicky.
Tato práce je podpořena grantem IGA 10576--3/2009.
MUDr. Lucie Hrazdirová
Gynekologicko-porodnická klinika VFN
Apolinářská 18
128 00 Praha 2
e-mail: lucie.hra@seznam.cz
Sources
1. Alborzi, S., Dehbashi, S., Khodaee, R. Sonohysterosalpingographic screeninig for infertile patiens. Int J Gynecol Obst, 2003, 82, p. 57-62.
2. Al-Inany, H. Intrauterine adhesions. An update. Acta Obstet Gynecol Scand, 2001, 80, p. 986-993.
3. Asherman, JG. Amenorrhoea traumatica (atretica). J Obstet Gynacol Br Emp, 1948, 55, s. 23-30.
4. Asherman, JG. Traumatic intrauterine adhesions. J Obstet Gynaecol Br Emp, 1948, 57, p. 892-896.
5. Bass, B. Ueber die Verwachsungen in der cervix uterinach curettagen. Zentralbl Gynaecol, 1927, 51, p. 223.
6. Bukulmez, O., Yarali, H., Gurgan, T. Total corporal synechiae due to tuberculosis carry a very poor prognosis following hysteroscopic synechialysis. Hum Reprod, 1999, 14(8), p. 1960‑1961.
7. Czernobilsky, B. Endometritis and infertility. Fertil Steril, 1978, 30(2), p. 119-130.
8. Dalfó, AR., Úbeda, B., Úbeda, A., et al. Diagnostic value of hysterosalpingography in the detection of intrauterine abnormalities. AJR, 2004, 183, p. 1405-1409.
9. Dicker, D., Feldberg, D., Samuel, N., et al. Etiology of cervical pregnancy. Association with abortion, pelvic patology, IUDs and Asherman syndrome. J Reprod Med, 1985, 30, p. 25-27.
10. Fayez, JA., Mutie, G., Schneider, PJ. The diagnostic value of hysterosalpingography and hysteroscopy in infertility investigation. Am J Obstet Gynecol, 1987, 156, p. 558-560.
11. Fedele, L., Bianco, S., Dorta, M., et al. Intrauterine adhesions: Detection with transvaginal US. Radiology, 1996, 199, p. 757-759.
11. Fiedler, S., Margolioth, EJ., Kafka, I., et al. Incidence of post-abortion intra-uterine adhesions evaluated by hysteroscopy – a prospective study. Hum Reprod, 1993, 8, 3, p. 442-444.
12. Forssman, L. Posttraumatic intrauterine synechiae and pregnancy. Obstet Gynecol, 1965, 26, p. 710-713.
13. Fritsch, H. Ein Fall von vollingen Schwund der Gebaumutterholde nach Auskratzung. Zentralbl Gynaekol, 1894, 18, s. 1337-1342.
14. Golan, A., Raziel, A., Pansky, M., et al. Manual removal of the placenta - its role in intrauterine adhesion formativ. Int J Fertil Menopausal Stud, 1996, 41(5), p. 450-451.
15. Khopkar, U., Williams, RM., Selinger, M. Morbid adhesion of the placenta after hysteroscopic lysis of intrauterine adhesions. Fertil Steril, 2006, 86, 5, p. 1513e1-e3.
16. Krolikowski, A., Janowski, K., Larsen, JV. Asherman syndrome caused by schistosomiasis. Obstet Gynecol, 1995, 85, p. 898-899.
17. Leung, PL., Tam, WH, Yuen, PM. Hysteroscopic appearance of the endometrial cavity following thermal ballon endometrial ablativ. Fertil Steril, 2003, 79, 5, p. 1226-1228.
18. Lo, ST., Ramsay, P., Person, R. Endometrial thickness measured by ultrasound scan in women with uterine outlet obstruction due to intrauterine or upper cervical adhesions. Hum Reprod, 2008, 23, 2, p. 306-309.
19. Mara, M., Fučíkova, Z., Kuzel, D., et al. Hysteroscopy after uterine fibroid embolisation in women of fertile age. J Obstet Gynaecol Res, 2007, 33(3), p. 316-324.
20. March, CM. Intrauterine adhesions. Obstet Gynecol Clin North Am, 1995, 22(3), p. 491-505.
21. McCulloch, TA., Wagner, B., Duffy, S., et al. The patology of hysterectomy specimen following trans-cervical resection of the endometrium. Histopathology, 1995, 27, p. 541-547.
22. Makris, N., Kalmantis, K., Skartados, N., et al. Tree dimensional hysterosonography versus hysteroscopy for the detection of intracavitary uterine abnormalities. Int J Gynecol Obstet, 2007, 1, p. 6-9.
23. Nasr, AL., Al-Inany, HG., Thabet, SM., et al. A clinicohysteroscopic scoring system of intrauterine adhesions. Gynecol Obstet Invest, 2000, 50, p. 178-181.
24. Polishuk, WZ., Anteby, SO., Weinstein, D. Puerperal endometritis and intrauterine adhesions. Int Surg, 1975, 60, p. 418-420.
25. Roman, H., Sentilhes, L., Cingotti, M., et al. Uterine devascularisation and subsequent major intrauterine synechiae and ovarian silure. Fertil Steril, 2005, 83, p. 755-757.
26. Romer, T. Post-abortion-hysteroscopy – a method for early diagnosis od congenital and acquired intrauterine cause sof abortion. Eur J Obstet Gynecol Reprod Biol, 1994, 57, 3, p. 171-173.
27. Salle, B., Gaucherand, P., de Saint Hilaire, P., et al. Transvaginal sonohysterographic evaluation of intrauterine adhesions. J Clin Ultrasound, 1999, 27(3), p. 131-134.
28. Shalev, J., Meizner, I., Bar-Hava, I., et al. Predictive value of transvaginal sonography performed before routine diagnostic hysteroscopy for evalution of infertility. Fertil Steril, 2000, 73, 2, p. 412-417.
29. Shiau, C., Hsieh, C., Chiang, C., et al. Intrapartum spontaneus uterine rupture following uncomplicated resectoskopic treatment of Asherman syndrome. Chang Gung Med J, 2005, 28, 5, p. 123-126.
30. Schaffer, W. Role of uterine adhesions in the cause of multiple pregnancy losos. Clin Obstet Gynecol, 1986, 29, p. 912-924.
31. Schenker, JG., Margolioth, EJ. Intrauterine adhesions: an updated appraisal. Fertil Steril, 1982, 37, p. 593-610.
32. Schenker, JG. Etiology of and therapeutic approach to synechia uteri. Eur J Obstet Gynecol Reprod Biol, 1996, 65, p. 109-113.
33. Silvernagel, SW., Harsbarger, KE., Shevlin, DW. Postoperative granulomas of the endometrium: histological features after endometrial ablativ. Ann Diagn Pathol, 1997, 1, p. 82-90.
34. Soares, SR., Barbosa dos Reis, MM., Camargos, AF. Diagnostic accuracy of sonohysterography, transvaginal sonography and hysterosalpingography in patiens with uterine cavity diseases. Fertil Steril, 1995, 63, p. 410-413.
35. Stillman, RJ., Asakof, N. Association between Mullerian duct malformations and Asherman syndrome in infetile women. Obstet Gynecol, 1985, 65, p. 673-677.
36. Sylvestre, C., Child, TJ., Tulandi, T., et al. A prospective study to evaluate the efficacy of two - and free-dimensional sonohysterography in women with intrauterine laesions. Fertil Steril, 2003, 79, p. 1222-1225.
37. Taskin, O., Sadik, S., Onoglu, A., et al. Role of endometrial suppression on the frequency of intrauterine adhesions after resectoskopic surgery. J Am Assoc Gynecol Laparosc, 2000, 7, p. 351-354.
38. The American Fertility Society classifications of adnexal adhesions distal tubal occlusion, tubal occlusion secondary to tubal ligation, tubal pregnancies, Mullerian anomalies and intrauterine adhesions. Fertil Steril, 1988, 49, p. 944-955.
39. Toaff, R., Ballas, S. Traumatic hypomenorrhea-amenorrhea (Ashermans syndrome). Fertil Steril, 1978, 30, p. 379-387.
40. Tur-Kaspa, I., Gal, M., Hatman, M., et al. A prospective evaluation of uterine abnormalities by saline infusion sonohysterography in 1009 women with infertility or abnormal uterine bleeding. Fertil Steril, 2006, 86, p. 1731-1735.
41. Valle, RF., Sciarra, JJ. Intrauterine adhesions: hysteroscopic diagnosis, clasification, tratment and reproductive outcome. Am J Obstet Gynecol, 1988, 158, p. 1459-1470.
42. Ventolini, G., Zhang, M., Gruber, J. Hysteroscopy in the evaluation of patiens with recurent pregnanacy loss: a cohort study in a primary care. Surg Endosc, 2004, 18, p. 1782-1784.
43. Wamsteker, K., De Block, S. Diagnostic hysteroscopy: technique and documentation. In Sutton, C., Diamond, M., eds. Endoscopis surgery for gynecologists. London: W.B. Saunders, 1993, p. 263‑276.
44. Wamsteker, K., De Block, S. Diagnostic hysteroscopy:technique and documantation. In Sutton, C., Diamond, M, eds. Endoscopic surgery for gynecologists. London: W.B. Saunders, 1998, p. 511-524.
45. Weiss, A., Shalev, E., Romano, S. Hysteroscopy may by justified after two miscarriages. Hum Reprod, 2005, 20, p. 2628-2631.
46. Westendorp, IC., Ankum, WM., Mol, BW., et al. Prevalence od Ashermans syndrome after secondary removal od placetal remnants or repeat curettage for incomplete abortion. Hum Reprod, 1998, 13(12), p. 3347-3350.
47. Yaffe, H., Ron, M., Polishuk, WZ. Amenorrhoea, hypomenorrhoea and uterine fibrosis. Am J Obstet Gynecol, 1978, 130, p. 599-601.
48. Yang, J., Chen, M., Wu, M., et al. Office hysteroscopic early lysis of intrauterine adhesion after transcervical resection of multiple apposing submucous myomas. Fertil Steril, 2008, 89, 5, p. 1254-1259.
49. Yu, D., Wong, Y., Cheong, Y., et al. Asherman syndrome - one century later. Fertil Steril, 2008, 89(4), p. 759-779.
Labels
Paediatric gynaecology Gynaecology and obstetrics Reproduction medicine
Article was published inCzech Gynaecology

2010 Issue 6-
All articles in this issue
- Ashermanův syndrom I – historie, prevalence, histopatologie, klasifikace, etiologie, symptomatologie a vyšetřovací metody
- Ashermanův syndrom II – terapie, asistenční metody, prevence readhezí, komplikace a výsledky léčby
- Hysteroskopie v ambulantním režimu v podmínkách gynekologické ordinace
- Gynekologická robotická chirurgie a naše první zkušenosti
- Operační metody sterilizace u žen
- Nový pohled na problematiku vulvodynie
- Výchova gynekologických operatérov
- Česká verze dotazníku EORTC QLQ - CX24 pro pacientky s karcinomem děložního hrdla
- Sekundární malignity ženského genitálu
- Hodnotenie funkčného stavu panvového dna metódou EMG-Biofeedback podľa Perfect schémy u pacientiek po abdominálnej a vaginálnej hysterektómii
- Jak dále v diagnostice kvasinek u gynekologických pacientek?
- Prevence invaze maligních buněk při gynekologických operacích nádorů
- Postižení parametrií u pacientek s časným stadiem cervikálního karcinomu s velikostí nádoru do 2 cm: mýtus, nebo realita?
- Metastázy extramamárních solidních tumorů do mléčné žlázy – skutečný diagnostický problém
- Využití nalbuphinu v porodnické analgezii
- Czech Gynaecology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Nový pohled na problematiku vulvodynie
- Operační metody sterilizace u žen
- Ashermanův syndrom II – terapie, asistenční metody, prevence readhezí, komplikace a výsledky léčby
- Využití nalbuphinu v porodnické analgezii
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

