-
Medical journals
- Career
Možnosti využití hyaluronátu sodného ve farmacii a medicíně
: Veronika Pechová; Jan Gajdziok
: Čes. slov. Farm., 2017; 66, 154-159
: Review Articles
Hyaluronát sodný představuje moderní biomateriál pro široké využití ve farmacii a medicíně. Jedná se o tělu vlastní glykosaminoglykan, který se vyskytuje především v mezibuněčné hmotě, synoviální tekutině, kloubní chrupavce, pokožce a očním sklivci. Funguje jako signální molekula imunologických dějů, ovlivňuje mobilitu a adhezi buněk, hojení ran a má také významné antioxidační vlastnosti. Praktické využití proto nachází v řadě oborů medicíny při potřebě doplnění do tkání v případě jeho nedostatku, nebo v rámci prevence i léčby vybraných onemocnění. Díky svým hydratačním, regeneračním a ochranným účinkům se využívá rovněž v kosmetice.
Klíčová slova:
hyaluronát sodný • kyselina hyaluronová • hyaluronan • deriváty hyaluronátu sodného • lékové formy • medicínské využitíÚvod a základní vlastnosti hyaluronátu sodného
Hyaluronát sodný (sodná sůl kyseliny hyaluronové, hyaluronan, HS) je glykosaminoglykan (GAG) složený z disacharidových podjednotek kyseliny D-glukuronové a N-acetyl-D-glukosaminu1). Kyselina hyaluronová (HA) se při fyziologickém pH vykytuje ve formě sodné soli, tzv. hyaluronanu2). Jedná se o jediný GAG, jehož monomerní jednotka neobsahuje zbytek kyseliny sírové ani není jinak modifikována3). Strukturu monomerní jednotky HA znázorňuje obrázek 1. Jedná se o aniontový biopolymer, který se nachází ve většině tělních tekutin a tkáních savců s největším zastoupením v mezibuněčné hmotě a v měkkých pojivových tkáních4, 5). HS je vytvářen řadou buněk, přičemž nejvýznamněji se na jeho syntéze podílejí především fibroblasty, keratinocyty a chondrocyty. V lidském těle o hmotnosti 70 kg je obsaženo přibližně 15 g HS6). Funkční skupiny činí HS natolik hydrofilním, že je schopen vázat až 1000krát více vody, než by vyplývalo z jeho struktury3).
1. Monomerní jednotka kyseliny hyaluronové <sup>4)</sup> 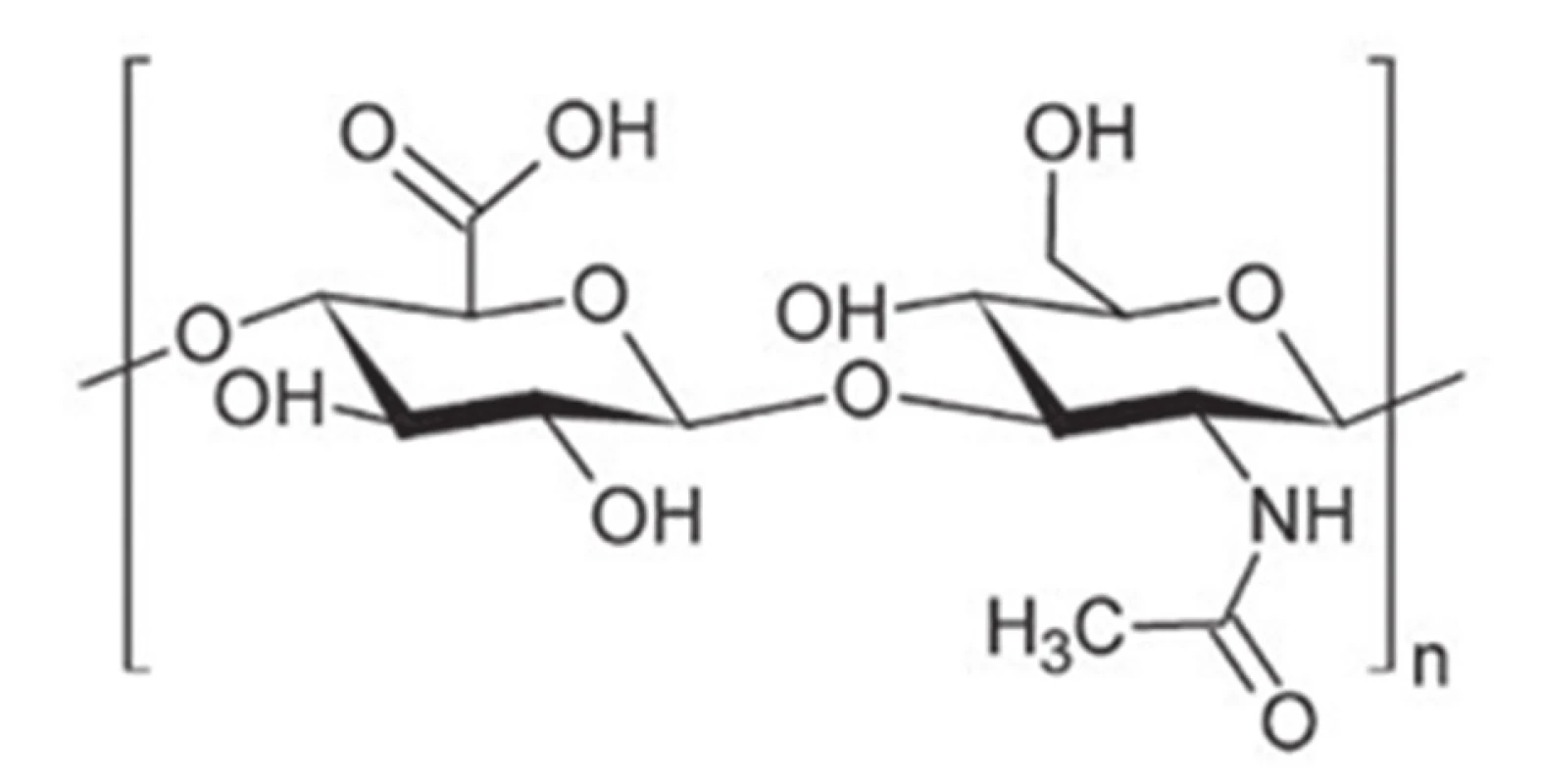
Izolovaný HS je ve formě bílého nebo téměř bílého velmi hygroskopického prášku, který je v závislosti na typu HS mírně nebo dobře rozpustný ve vodě1). Typickou vlastností HS v hydratovaném stavu je jeho viskoelasticita, která se může měnit v závislosti na smykovém namáhání a oscilačním pohybu. Viskozita 1% roztoku HA o relativní molekulové hmotnosti (Mr) 3–4 MDa je asi 500 000krát vyšší než viskozita vody. Hodnota viskozity však může poklesnout až 1000krát, pokud je roztok HA protlačen tenkou jehlou. Důsledkem rychlého pohybu tedy viskozita klesá a současně se zvyšuje elasticita roztoku, čímž se omezí vnitřní tření a umožní se obnovení původního stavu způsobeného deformací7). HS představuje ideální biologický lubrikant, protože snižuje pracovní zátěž během rychlých pohybů. Viskozita i elasticita roztoku je ovlivněna jak molární hmotností použitého HS, tak také jeho koncentrací, což jsou důležité faktory podmiňující jeho medicínské využití3).
HS je zapojen do řady klíčových procesů, které probíhají v organismu, jako je např. buněčná signalizace, hojení ran a regenerace tkání s omezením nadměrného jizvení5). HS má nezastupitelnou úlohu v embryogenezi a následně v rámci celého nitroděložního vývoje plodu6). Mezi další důležité fyziologické funkce HS se mimo jiné řadí podíl na udržování osmotického tlaku, zabezpečení hydratace tkání a rohové vrstvy kůže, lubrikace chrupavek a prevence poškození tkání oxidačním stresem vychytáváním volných radikálů8, 9).
Biologický poločas HS je zpravidla velmi krátký (např. 0,5–1 den v kloubech; 1–2 hodiny v přední komoře oční; avšak 20–70 dní ve sklivci). Proto musí být nastolena rovnováha mezi místní syntézou HS prostřednictvím enzymu hyaluronan-syntasy v příslušných tkáních a degradací HS prostřednictvím hyaluronidas. Rozklad HS částečně probíhá přímo v tkáních a dále v místních lymfatických uzlinách a v játrech3).
Výroba hyaluronátu sodného
V roce 1934 byla HA poprvé izolovaná ze sklivce kravského oka. Její název byl odvozen z řeckého označení pro sklo/sklovitý „hyalos/hyaloid“ a názvu „uronat“ označující uronovou kyselinu10, 11). Následně byla HA získávána ze synoviální tekutiny, pupeční šňůry nebo kůže12). Tradiční způsob výroby představuje extrakci HS z kohoutích hřebínků1), která je založena na enzymatickém štěpení s následnou separací a purifikací produktu12). V současnosti se HS získává především fermentací z grampozitivních bakterií rodu Streptococcus sp.1, 4) Například firma Contipro a. s. (Dolní Dobrouč, CZ) vyrábí HS biotechnologickým postupem fermentací z bakteriálního kmene Streptococcus equi susp. zooepidemicus13).
Modifikace a deriváty hyaluronátu sodného
HS se využívá v lineární přírodní formě, nebo jako chemicky modifikovaný HS. Modifikací lineárního řetězce se připravují buď deriváty HS, nebo trojrozměrné zesíťované formy HS vytvořením kovalentních vazeb mezi jednotlivými lineárními řetězci14). Schématické znázornění možných forem HS je uvedeno na obrázku 2.
2. Formy HS – a) lineární forma, b) chemicky modifikovaný HS, c) zesíťovaný HS <sup>14)</sup> 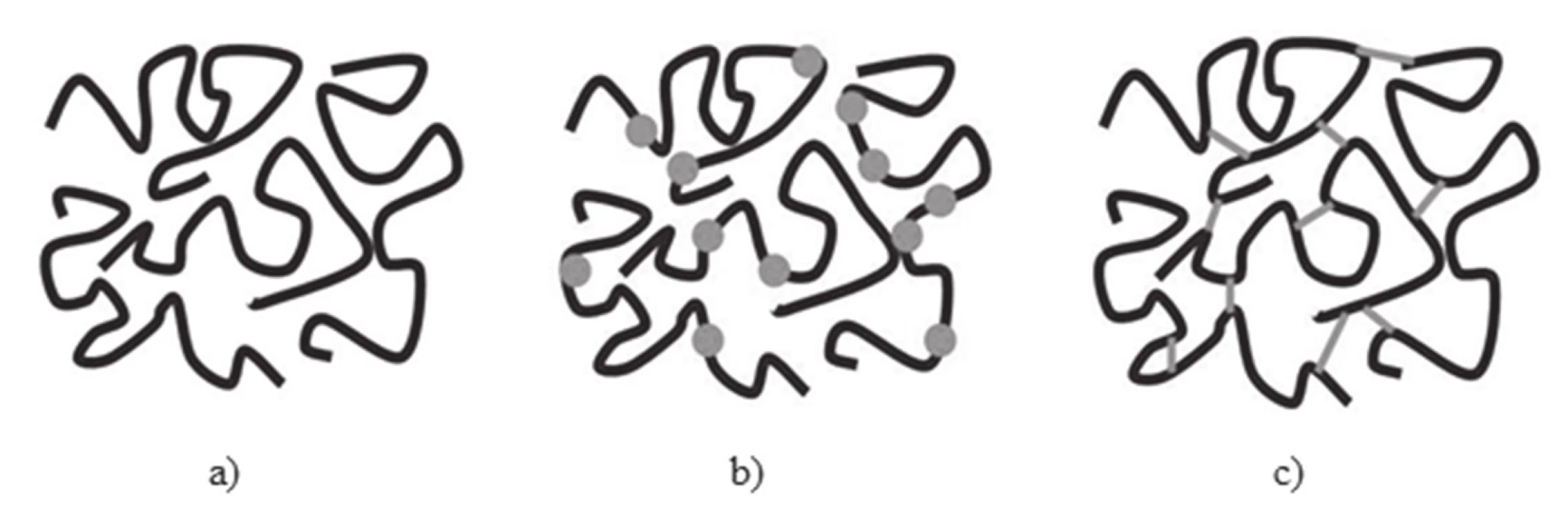
Vedle řady fyziologických funkcí se přírodní HS pro své výhodné viskoelastické a reologické vlastnosti využívá především v oftalmologii, ortopedii nebo např. při hojení ran. Navázáním funkčních skupin prostřednictvím chemické modifikace přírodního HS lze rozšířit možnosti medicinálního využití HS změnou jeho vlastností. Deriváty HS, označované také jako hylany, jsou rozsáhlou skupinou různých variant chemických modifikací nativního HS15). Hlavním důvodem pro přípravu derivátů HS je především zabránění rychlému rozkladu nativního HS v organismu. Například esterifikací karboxylové skupiny dochází ke zvýšení hydrofobního charakteru molekuly, čímž se prodlouží biologický poločas esterifikovaného HS. Estery jsou nejběžnější deriváty HS s hlavním využitím ve tkáňovém inženýrství. Zesíťované formy vynikají především větší mechanickou odolností a své využití proto nacházejí např. ve formě intraartikulárních injekcí v terapii osteoartrózy, v tkáňovém inženýrství nebo jako výplně vrásek v estetické medicíně14).
Praktické využití hyaluronátu sodného ve farmacii a medicíně
HS se ve velké míře využívá pro výrobu léčiv, zdravotnických prostředků a kosmetických přípravků4), kde se uplatňují jeho výhodné vlastnosti, a to především biokompatibilita, biodegradovatelnost a nepůsobení imunitní odpovědi po podání do organismu16). Klinicky se HS používá jako diagnostický marker pro řadu chorobných stavů, včetně rakoviny, revmatoidní artritidy, jaterních chorob a také jako časný marker pro hrozící rejekci transplantovaného orgánu5). V případě rakovinného bujení je prokázáno nejméně 14 typů karcinomu, u kterých byla zjištěna zvýšená koncentrace HS, a to jak přímo v buňkách samotných, tak i v mezibuněčném stromatu. Pro své vynikající viskoelastické vlastnosti se HS využívá v oční chirurgii, při artroskopických operacích a v terapii osteoartrózy, jako výplň vrásek v plastické chirurgii, při terapii močové inkontinence, při endoskopických operacích k prevenci jizvení, k intravezikální instilaci při cystitidách a v očních či nosních kapkách6).
Oční podání hyaluronátu sodného
HS je viskoelastickým a mukoadhezivním polymerem, který je přirozenou součástí lidského oka17). V humánní medicíně byl HS poprvé využit v padesátých letech 20. století jako náhrada sklivce při operaci oka. Roztok HS ve formě intraokulární injekce se využívá v oční chirurgii i v současnosti, a to k udržení tvaru oka, především pak v chirurgii katarakty k udržování hloubky přední komory oční11). Pro intraokulární chirurgické výkony je na trhu dostupná řada viskochirurgických pomůcek (angl. ophthalmic viscosurgical devices, OVD), především viskoelastických roztoků, které se liší svými fyzikálně-chemickými a reologickými vlastnostmi (tab. 1). Jedná se o speciální roztoky užívané při operacích k ochraně rohovkového endotelu, ke stabilizaci tkáně během zákroku, k vyrovnání tlaku v předním a zadním segmentu oka nebo pro vytvoření dostatečného prostoru pro manipulaci v přední komoře oční během operace. Hlavními atributy viskoelastického materiálu jsou mj. viskozita, kohezivita nebo elasticita. OVD se dělí podle Mr a hodnoty klidové viskozity na kohezivní (vysoká Mr, vyšší viskozita) a disperzivní (nízká Mr, nižší viskozita)18, 19).
1. Příklady lékových a aplikačních forem s obsahem HS <sup>34, 35, 37, 41-45, 53–59)</sup> 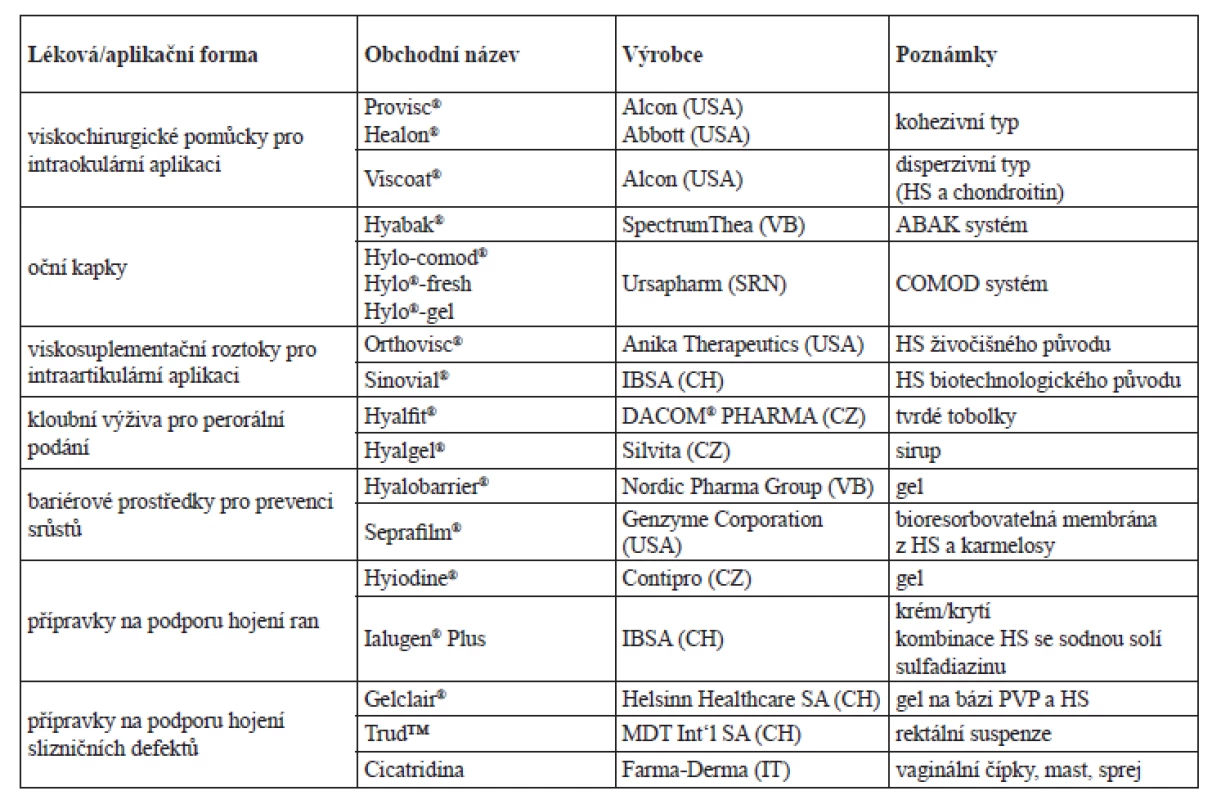
HS nachází široké využití jako oční lubrikant ve formě očních kapek v symptomatické léčbě syndromu suchého oka20). Konzervativní způsob léčby spočívá v substituci nedostatečného přirozeného slzného filmu formou očních kapek (tzv. umělé slzy)21) nebo formou mastí, gelů a očních sprejů na bázi lipozomů22). Po aplikaci očních kapek s obsahem HS se na rohovce vytváří hydrogelová vrstva, která nahrazuje přirozený slzný film a současně může urychlit hojení endotelu rohovky (např. po poranění nebo po operaci oka)17). Oční kapky s obsahem HS (případně též s obsahem karbomeru nebo xyloglukanu) jsou charakteristické vyšší viskozitou, a proto se využívají převážně u těžších forem syndromu suchého oka. Povidon, polyvinylalkohol nebo karmelosa sodná sůl se z důvodu nižší viskozity očních kapek doporučují u lehčích forem syndromu suchého oka21). Příklady očních kapek s obsahem HS jsou uvedeny v tabulce 1. Především u těžších forem syndromu suchého oka představuje optimální řešení podání sterilních jednorázových preparátů v jednodávkovém obalu nebo jiné aplikační formy bez konzervačních přísad22). Výhodným řešením je využití speciálních vícedávkových obalů, konkrétně systému COMOD® a systému ABAK® 23), které se často využívají jako primární obal u očních kapek s obsahem HS (tab. 1). Oba systémy umožňují uchovávat větší množství tekuté formy po otevření sterilní, aniž by do nich byly přidány konzervační látky. Základem systému COMOD® (COntinous MOnoDose system) je tzv. „airless pump“. Jedná se o dávkovací mechanismus se dvěma ventily, které zabraňují průniku vzduchu a kapaliny do nádobky. Do sterilního roztoku se tak nemohou dostat nežádoucí mikroorganismy z prostředí. Stlačením dna lahvičky dojde k vykápnutí přesně odměřeného množství očních kapek. Ventily a ostatní části nádobky, které jsou v kontaktu s roztokem, jsou navíc postříbřené, což znemožňuje množení bakterií24). Speciální obal se systémem ABAK® obsahuje antibakteriální filtr z nylonového vlákna o tloušťce 0,2 μm, přes který se před odebráním každé dávky oční kapky přefiltrují25).
Intraartikulární podání hyaluronátu sodného a kloubní výživa
Hlavní složkou synoviální tekutiny je HS, jehož koncentrace a Mr je v kloubech postižených osteoartrózou oproti normálnímu stavu pozměněna, s čímž souvisí nižší viskozita a elasticita synoviální tekutiny v kloubech postižených artrózou oproti kloubům zdravým26, 27). Viskosuplementace představuje léčebný postup, kdy formou intraartikulární injekce je do prostoru kloubního pouzdra aplikován roztok s obsahem vysokomolekulárního HS. Jedná se o terapeutický přístup využívaný u pacientů s osteoartrózou za účelem zlepšení reologických parametrů v kloubech postižených artrózou3). Přípravky s obsahem HS mají účinky jak přímé (lubrikace, hydratace, neutralizace volných radikálů, zakrytí nociceptorů), tak také nepřímé, zprostředkované aktivací receptoru CD44 (protizánětlivé působení, indukce syntézy endogenního HS a proteoglykanů). Injekce je přitom možné aplikovat do všech kloubů, nejlépe však do kloubů nosných28). HS byl poprvé aplikován v sedmdesátých letech 20. století do poraněných kloubů závodních koní s osteoartrózou v kombinaci s metylprednisolon acetátem. U této kombinace se zaznamenaly klinicky lepší výsledky než v případě samotného podávání steroidů26, 29). Na trhu existuje řada přípravků pro viskosuplementaci (viz tab. 1), které se mezi sebou liší Mr, původem (HS živočišného nebo biotechnologického původu) a chemickými modifikacemi použitého HS. Dělí se na přípravky s nízkou Mr (< 700 kDa), se střední Mr (800–1500 kDa) a na preparáty s vysokou Mr (> 1500 kDa). S nárůstem Mr se prodlužuje nitrokloubní poločas a délka působení HS28). Obecně platí, že přípravky s nižší Mr mají rychlejší nástup účinku, jejich degradace v kloubu je však také rychlejší (cca 10 hodin). Přípravky s vysokou Mr přetrvávají v kloubu až 40 hodin a léčebný účinek trvá i řadu měsíců30). Stabilizace chemických vazeb zesíťováním HS vede u vysokomolekulárních přípravků k vysoké viskozitě, což může indukovat jejich imunogenicitu. Naopak nízkomolekulární přípravky představují nejčastěji pouze fragmenty přirozeného HS a jejich podávání bývá provázeno minimálním výskytem imunologických či alergických reakcí28).
Na trhu rovněž existují preparáty s obsahem HS určené pro perorální podání v různých lékových formách, např. tobolky, tablety, gely a sirupy. Využívají se pro podporu kloubní regenerace, při prevenci osteoporózy, případně také pro zlepšení kvality kůže a podporu růstu a kvality vlasů31). Absorpce HA po perorálním podání a její distribuce do pojivových tkání byla experimentálně potvrzena u laboratorních zvířat (potkan, pes) zobrazením HA značené radionuklidem 99mtechnecium (99mTc-HA) v kloubech, kostech a kůži laboratorních zvířat32). Příklady doplňků stravy s obsahem HS jsou uvedeny v tabulce 1.
Hyaluronát sodný v chirurgických oborech
HS jakožto vysoce hydrofilní látka se využívá v chirurgii tělních dutin za účelem minimalizace tvorby srůstů11). Srůsty (adheze) jsou abnormální spojení mezi tkáněmi a orgány, které mohou být vrozené nebo získané. Získané srůsty jsou jednou z nejčastějších pozdních komplikací břišní a pánevní chirurgie. Srůsty mohou zapříčinit řadu zdravotních komplikací, např. střevní neprůchodnost nebo neplodnost33). Prevence vzniku adhezí spočívá především v precizní operační technice a šetrném nakládání s tkáněmi. Nejlepším peroperačním ošetřením rizikových míst se jeví profylaktická aplikace sterilního vysoce viskózního gelu s obsahem HA (Hyalobarrier gel®), který je na trhu dostupný ve dvou formách pro laparotomické a pro endoskopické výkony. Při aplikaci by měla být zachována integrita gelu tak, aby nanášená vrstva gelu kryla oblast operovaného ložiska a překrývala také okolní zdravou tkáň. Své využití nachází především v gynekologii a porodnictví34, 35). V klinické praxi se k prevenci vzniku srůstů dále využívají fyzikální separátory a bariéry. Hlavním požadavkem na funkci bariéry je schopnost účinného oddělení traumatizované peritoneální plochy během kritického období vývoje adhezí (3–5 dnů po operaci)36). Aplikace dostupných bariérových prostředků s sebou nese i určitá rizika, jako je prodloužení operačního času a přítomnost cizího tělesa v dutině břišní34). Zástupcem bariérových prostředků je např. Seprafilm®. Jedná se o sterilní, bioresorbovatelnou, průsvitnou membránu složenou z modifikovaného HS a karmelosy. Používá se jako fyzikální bariéra za účelem prevence vzniku adhezí s ověřeným účinkem na zvířecích modelech i v randomizovaných klinických studiích37).
Hyaluronát sodný při hojení ran
Největší podíl HS přítomného v lidském těle se nachází v kůži. Mezi hlavní funkce HS v kůži se řadí např. schopnost zadržovat vodu ve tkáni a měnit objem vázané vody v kůži, ovlivnění stlačitelnosti kůže, vliv na proliferaci a diferenciaci buněk a pozitivní ovlivnění reparačních procesů. Množství HS v kůži se mění během hojení ran, při nemocech i během stárnutí kůže38). HS představuje výhodný výchozí biomateriál k získání vhodných struktur pro regeneraci tkání39).
Proces hojení ran je dynamický proces, charakteristický obnovou jednotlivých složek matrix, přičemž HS plní v tomto procesu řadu funkcí. Především se jedná o podporu tvorby granulační tkáně navázáním HS na příslušné receptory, usnadnění migrace buněk do hojící se tkáně, facilitace dělení buněk a angiogeneze a také ochrana buněk proti účinku volných radikálů. HS rovněž omezuje tvorbu jizev40). Pro hydrataci hlubokých ran a kožních defektů se využívá přípravek Hyiodine®. Jedná se o sterilní antiadhezivní a atraumatický zdravotnický prostředek ve formě gelu, který zajišťuje příznivé prostředí pro hojení rány. Jeho lubrikační vlastnosti jsou ideální pro zabránění adheze obvazu k ráně. Obsah jodového komplexu v produktu chrání HS před degradací bakteriálními enzymy a současně poskytuje antimikrobiální ochranu rány. Vysoké efektivity je dosaženo především při hojení diabetických ran, dutin a píštělí41). Přípravek Ialugen® Plus s obsahem HS a stříbrné soli sulfadiazinu s antibakteriálními účinky, dostupný v lékové formě krému nebo impregnovaného obvazu, je určen k profylaxi a léčbě infikovaných kožních lézí, konkrétně ran, odřenin a popálenin42).
Hyaluronát sodný v lokální terapii sliznic
HS se rovněž využívá pro lokální léčbu zánětlivých onemocnění sliznice gastrointestinálního traktu. Bolestivé léze sliznice dutiny ústní jsou charakteristické pro orální mukositidy, které velmi často doprovázejí chemoterapii a radioterapii, postihují pacienty s HIV nebo jsou projevem aftózní stomatitidy. Pro topickou léčbu orálních mukositid je určený bariérový gel na bázi polyvinylpyrolidonu a HS Gelclair®. Gelclair® vytváří ochranný film, který pomáhá mírnit bolest a zklidňuje poškození ústní sliznice43, 44).
HS je důležitou součástí střevní sliznice, kde přispívá k její hydrataci a udržení integrity. K narušení fyziologických funkcí střevní sliznice dochází u ulcerózní kolitidy (UC), která se řadí mezi chronická zánětlivá onemocnění postihující sliznici tlustého střeva. UC je mimo jiné podmíněna úbytkem HS v subepiteliální bazální vrstvě. HS má na sliznici tlustého střeva antifibrotický a také imunomodulační efekt. Na českém trhu je nově k dispozici HS ve formě rektální suspenze Trud™, která je určena k doplňkové léčbě nemocných s lehkou a středně těžkou formou UC45, 46). Jedná se o směs složenou z HS o vysoké Mr (1800 kDa), která ulpívá na povrchu epitelové výstelky střeva a zvyšuje viskozitu i tloušťku slizničního hlenu. Druhou komponentou je nízkomolekulární HS (350 kDa), který po lokální aplikaci difunduje do mezibuněčného prostoru, kde potlačením adheze leukocytů brání jejich průniku do kapilárního řečiště, čímž potlačuje aktivitu zánětlivého procesu46).
Při pobytu v suchém, klimatizovaném prostředí a vlivem větru a slunečního záření může vznikat pocit suché nosní sliznice. Přídavek HS do složení nosních kapek nebo spreje působí zvlhčení nosní sliznice tvorbou stabilního zvlhčujícího filmu. Kombinace dekongescentu nosní sliznice s HS je obsažena např. ve složení nosního spreje Olynth HA42, 47).
Pro urychlení hojení a podporu reepitelizace po destrukčních a ablačních zákrocích na děložním čípku, po porodu, po dalších gynekologických operacích a také po přeléčeném zánětlivém a mykotickém onemocnění se využívají přípravky s obsahem HS ve formě vaginálních čípků, případně také v masti nebo ve spreji (Cicatridina). Lokální přípravky s obsahem HS rovněž mohou zlepšit suchost vaginální sliznice v postmenopauze, v době kojení, po chemoterapii a radioterapii35).
Intravezikální instilace sterilního roztoku HA a chondroitinsulfátu sodného (Ialuril®) vede k významnému snížení výskytu recidivujících symptomatických uroifekcí a menšímu podílu multirezistentních patogenů při chronické kolonizaci sliznic dolních močových cest48). V urologii lze využít aplikaci HS do oblasti uretry k dočasnému zlepšení potíží se stresovou inkontinencí moči49).
Hyaluronát sodný v kosmetice
Stárnutí kůže představuje multifaktoriální proces, kdy jedním z faktorů je úbytek HS v epidermis. Nižší obsah HS v rohové vrstvě kůže vede ke ztrátě hydratace a pružnosti kůže a k rozvoji vrásek. Zároveň se v průběhu stárnutí snižuje velikost molekul HS v kůži50). Obnovení elasticity a zjemnění textury kůže je možné řešit přidáním HS do kosmetických prostředků. HS může být formulován v různých kosmetických přípravcích, jako jsou krémy, pleťové vody, séra, šampony, kondicionéry, koupelové oleje, rtěnky či balzámy na rty. Kosmetické prostředky s obsahem HS rovněž mohou chránit pokožku před škodlivými účinky UV záření vzhledem k omezení peroxidace lipidů v kůži v důsledku snížené tvorby volných radikálů51).
Pro omlazení kůže se v současné době rovněž využívá metoda mezoterapie. Jedná se o mnohonásobnou aplikaci mikroinjekcí s obsahem bioaktivních látek do kůže za účelem zvýšení míry hydratace a obnovení optimálního fyziologického prostředí pro fibroblasty. Intradermální aplikace sterilního roztoku HS zlepšuje hydrataci, pevnost a viskoelastické vlastnosti kůže52).
Střet zájmů: žádný.
doc. PharmDr. Jan Gajdziok, Ph.D.
V. Pechová
Ústav technologie léků, Farmaceutická fakulta
Veterinární a farmaceutická univerzita
Palackého třída 1946/1, 612 42 Brno
e-mail: gajdziokj@vfu.cz
Sources
1. Ministerstvo zdravotnictví ČR. Český lékopis 2009. 1. vydání. Praha: Grada Publishing 2009.
2. Balazs E. A., Laurent T. C., Jeanloz R. W. Nomenclature of hyaluronic acid. Biochem. J. 1986; 235, 903.
3. Schiller J., Volpi N., Hrabárová E., Šoltés L. Hyaluronic acid: A natural biopolymer. In: Kalia S., Avérous L. (eds.) Biopolymers: Biomedical and environmental applications. Hoboken: John Wiley and Sons 2011.
4. Sosnik A., das Neves J., Sarmento B. Mucoadhesive polymers in the design of nanodrug delivery systems for administration by non-parenteral routes: A review. Prog. Polym. Sci. 2014; 39, 2030–2075.
5. Volpi N., Schiller J., Stern R., Soltés L. Role, metabolism, chemical modifications and applications of hyaluronan. Curr. Med. Chem. 2009; 16, 1718–1745.
6. Slíva J., Minárik J. Hyaluronát – nejen pasivní pozorovatel, nýbrž aktivní modulátor imunitních reakcí. New EU Magazine of Medicine. 2009; 1–2, 75–79.
7. Fraser J. R., Laurent T. C., Laurent U. B. Hyaluronan: its nature, distribution, functions and turnover. J. Intern. Med. 1997; 242, 27–33.
8. Laurent T. C., Laurent U. B. G., Fraser J. R. E. The structure and function of hyaluronan: An overview. Immunol. Cell Biol. 1996; 74, A1–A7.
9. Hašová M., Crhák T., Safránková B., Dvořáková J., Muthný T., Velebný V., Kubala L. Hyaluronan minimizes effects of UV irradiation on human keratinocytes. Arch. Dermatol. Res. 2011; 303, 277–284.
10. Meyer K., Palmer J. W. The polysaccharide of the vitreous humor. J. Biol. Chem. 1934; 107, 629–634.
11. Necas J., Bartosikova L, Brauner P., Kolar J. Hyaluronic acid (hyaluronan): a review. Vet. Med. 2008; 53, 397–411.
12. Long F. D., Adams R. G., DeVore D. P. Preparation of hyaluronic acid from eggshell membrane. US Patent No. 6946551; 2005.
13. Contipro. Hyaluronic acid. https://www.contipro.com/images/ProductLists/Hyaluronic-Acid_Contipro.pdf (29. 6. 2017).
14. Schiraldi Ch., La Gatta A., de Rosa M. Biotechnological Production and Application of Hyaluronan. In: Elnashar M. eds. Biopolymers. Rijeka: Intech 2010.
15. Larsen N. E., Balazs E. A. Drug delivery systems using hyaluronan and its derivatives. Adv. Drug Delivery Rev. 1991; 7, 279–293.
16. Šedová P., Buffa R., Kettou S., Huerta-Angeles G., Hermannová M., Leierová V., Šmejkalová D., Moravcová M., Velebný V. Preparation of hyaluronan polyaldehyde-a precursor of biopolymer conjugates. Carbohydr. Res. 2013; 371, 8–15.
17. Uhart M., Pirot F., Boillon A., Senaux E., Tall L., Diouf E., Burillon C., Padois K., Falson F., Leboucher G., Pivot C. Assessment of sodium hyaluronate gel as vehicle for intracameral delivery of cefuroxime in endophthalmitis prophylaxis. Int. J. Pharm. 2010; 398, 14–20.
18. Kuchynka P. Oční lékařství. 2., přepracované a doplněné vydání. Praha: Grada Publishing 2016.
19. Arshinoff S. A. Dispersive-cohesive viscoelastic soft shell technique. J. Cataract. Refract. Surg. 1999; 25, 167–173.
20. Nepp J., Schauersberger J., Schild G., Jandrasits K., Haslinger-Akramian J., Derbolav A., Wedrich A. The clinical use of viscoelastic artificial tears and sodium chloride in dry-eye syndrome. Biomaterials. 2001; 22, 3305–3310.
21. Varcholová D. Současné možnosti v substituční terapii syndromu suchého oka. Remedia 2006; 5, 2006, 503–508.
22. Odehnal M., Ferrová K., Malec J. Léčba suchého oka – Poruchy slzných žláz, slzného filmu a využití umělých slz v praxi. Praktické lékárenství 2010; 6, 149–152.
23. Messmer E. M. Konservierungsmittel in der Ophthalmologie. Ophthalmologie 2012; 109, 1064–1070.
24. Ursapharm. COMOD®-systém. http://ursapharm.cz/cz/vyroba-systemy/comod-system/ (29. 6. 2017).
25. Théa. ABAK Pure technology in a bottle. http://www.laboratoires-thea.com/medias/abak_brochure_eng.pdf (29. 6. 2017).
26. Engström-Laurent A. Hyaluronan in joint disease (Minisymposium: Hyaluronan). J. Intern. Med. 1997; 242, 57–60.
27. Akmal M., Singh A., Anand A., Kesani A., Aslam N., Goodship A., Bentley G. The effects of hyaluronic acid on articular chondrocytes. J. Bone Jt. Surg. Br. Vol. 2005; 87, 1143–1149.
28. Trč T. Současný stav viskosuplementace v léčbě osteoartrózy. Farmakoterapie 2012; 8, 608–611.
29. Butler J., Rydell N. W., Balazs E. A. Hyaluronic acid in synovial fluid. VI. Effect of intra-articular injection of hyaluronic acid on the clinical symptoms of arthritis in track horses. Acta Vet. Scand. 1970; 11, 139–155.
30. Frei R. Viskosuplementace v léčbě osteoartrózy. Farmakoterapie v praxi (ortopedie, revmatologie) 2014; 5, 3–6.
31. Contipro. Nutrihyl®. http://www.aktivnizvire.cz/hyaluronan-pro-klouby (29. 6. 2017).
32. Balogh L., Polyak A., Mathe D., Kiraly R., Thuroczy J., Terez M., Janoki G., Ting Y., Bucci L. R., Schauss A. G. Absorption, uptake and tissue affinity of high-molecular-weight hyaluronan after oral administration in rats and dogs. J. Agric. Food Chem. 2008; 56, 10582–10593.
33. Sahbaz A., Aynioglu O., Isik H., Ozmen U., Cengil O., Gun B. D., Gungorduk K. Bromelain: A natural proteolytic for intra-abdominal adhesion prevention. Int. J. Surg. 2015; 14, 7–11.
34. Matěna O. Antiadhezivní prostředky v laparoskopické operativě. Prakt. Gyn. 2013; 17, 237–240.
35. Křižan V., Pánková S., Hudeček R. Význam hyaluronátu v gynekologii a porodnictví. Prakt. Gyn. 2012; 16, 7–12.
36. Pánková S., Hudeček R., Račanská E. Peroperační prevence adhezí v gynekologii. Prakt. Gyn. 2009; 13, 70–75.
37. Huang H., Deng M., Jin H., Dirsch O., Dahmen U. Preventing intra-abdominal adhesions with a sodium hyaluronate carboxymethylcellulose membrane enabled visualization of hepatic microcirculation. Int. J. Surg. 2013; 11, 935–943.
38. Juhlin L. Hyaluronan in skin. J. Intern. Med. 1997; 242, 61–66.
39. Borzacchiello A., Russo L., Malle B. M., Schwach-Abdellaoui K., Ambrosio, L. Hyaluronic acid based hydrogels for regenerative medicine applications. BioMed Research International 2015; 2015, 1–12.
40. Dicker K. T., Gurski L. A., Pradhan-Bhatt S., Witt R. L., Farach-Carson M. C., Jia X. Hyaluronan: A simple polysaccharide with diverse biological functions. Acta Biomater. 2014; 10, 1558–1570.
41. Hyiodine®. Příručka k aplikaci. https://www.hyiodine.cz/images/Brochures/hyodine_%20prirucka_k_aplikaci.pdf (29. 6. 2017).
42. SÚKL. Databáze léků. http://www.sukl.cz/modules/medication/search.php (29. 6. 2017).
43. Buchsel P. C. Polyvinylpyrrolidone-sodium hyaluronate gel (Gelclair): a bioadherent oral gel for the treatment of oral mucositis and other painful oral lesions. Expert Opin. Drug Metab. Toxicol. 2008; 4, 1449–1454.
44. Gelclair®. Bioadherent oral rinse gel for effective relief of pain associated with oral mucositis. http://www.gelclair.com/ (29. 6. 2017).
45. Trud™. A new treatment for ulcerative colitis. http://www.treatwithtrud.com/-EN - (29. 6. 2017).
46. Bortlík M. Hyaluronát sodný: nová cesta v léčbě ulcerózní kolitidy? Gastroent. Hepatol. 2014; 68, 468–469.
47. Hysan® Care sprej. Návod k použití. http://www.nosnipece.cz/sites/default/files/PB%20HYSAN%20Pfl%20CZ_SK%2090.1656.pdf (29. 6. 2017).
48. Rejchrt M., Havlová K., Kříž J. Prevence recidivujících uroinfekcí intravezikální instilací kyseliny hyaluronové a chondroitinsulfátu u pacientů po míšním poranění. Urol. praxi 2015; 16, 43.
49. Romžová M. Možné příčiny vzniku inkontinence a jejich řešení. Urol. praxi 2014; 15, 221–226.
50. Papakonstantinou E., Roth M., Karakiulakis G. Hyaluronic acid: A key molecule in skin aging. Dermatoendocrinol. 2012; 4, 253–258.
51. Trommer H., Wartewig S., Bötcher R., Pöppl A., Hoentsch J., Ozegowski J. H., Neubert R. H. The effects of hyaluronan and its fragments on lipid models exposed to UV irradiation. Int. J. Pharm. 2003; 254, 223–234.
52. Baspeyras M., Rouvrais C., Liégard L., Delalleau A., Letellier S., Bacle I., Courrech L., Murat P., Mengeaud V., Schmitt A. M. Clinical and biometrological efficacy of a hyaluronic acid-based mesotherapy product: A randomised controlled study. Arch. Dermatol. Res. 2013; 305, 673–682.
53. Dick H. B., Schwenn O. Viscoelastics in Ophthalmic Surgery. 1. vydání. Berlín: Springer 2000.
54. Hyabak®. Preservative-free Sodium Hyaluronate dry eye drops. http://www.thea-pharmaceuticals.co.uk/products/hyabak (29. 6. 2017).
55. Ursapharm. Hylo® Eye Care. http://ursapharm.cz/cz/produkty/zdravotnicke-prostredky/hylo-eye-care/ (29. 6. 2017).
56. Drug Reference Encyclopedia. Orthovisc. http://www.theodora.com/drugs/orthovisc_injection_depuy_mitek.html (29. 7. 2016).
57. Sinovial®. Návod k použití. http://www.ibi.cz/download/Sinovial_navod_k_pouziti.pdf (29. 7. 2016).
58. Dacom® Pharma. Hyalfit®. https://www.dacom.cz/klouby-a-kosti/0-hyalfit-kolagen-kyselina-hyaluronova-kapsle.html (29. 6. 2017).
59. Silvita. Hyalgel. http://www.hyalgel.cz/hyalgel/eshop/1-1-Hyalgel (29. 6. 2017).
Labels
Addictology Clinical biochemistry Paediatric clinical oncology Paediatric psychiatry Diabetology Endocrinology Pharmacy Clinical pharmacology Intensive Care Medicine Internal medicine General practitioner for children and adolescents General practitioner for adults Psychiatry Toxicology Pharmaceutical assistant
Article was published inCzech and Slovak Pharmacy

2017 Issue 4-
All articles in this issue
- Cholinesterase activity assays and their use in the diagnosis of various pathological states including poisoning by neurotoxic agents
- Possibilities of using sodium hyaluronate in pharmaceutical and medical fields
- Specifics of some calcium salts in intravenous therapy of hypocalcemia and their further use
- Synergistic effect of azole antimycotics (clotrimazole and fluconazole) and natural substances
- Simplicia and medical containers from the Jesuit pharmacy in Telč
- Czech and Slovak Pharmacy
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Possibilities of using sodium hyaluronate in pharmaceutical and medical fields
- Specifics of some calcium salts in intravenous therapy of hypocalcemia and their further use
- Synergistic effect of azole antimycotics (clotrimazole and fluconazole) and natural substances
- Cholinesterase activity assays and their use in the diagnosis of various pathological states including poisoning by neurotoxic agents
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

