-
Medical journals
- Career
Efektivní separace tkáňových vrstev dárcovské rohovky pro DMEK injekcí tekutiny mezi Descemetskou membránu a rohovkové stroma: Výsledky prvního souboru operací
Authors: P. Stodůlka 1,2; M. Horáčková 1; M. Šramka 1,3; M. Slovák 1
Authors‘ workplace: Gemini oční klinika, Zlín, Česká republika 1; Oftalmologická klinika, 3. lékařské fakulty, Univerzita Karlova v Praze 2; Katedra teorie obvodů, Fakulta elektrotechnická, České vysoké učení technické v Praze 3
Published in: Čes. a slov. Oftal., 75, 2019, No. 1, p. 32-37
Category: Original Article
doi: https://doi.org/10.31348/2019/1/4Overview
Cíl: Klinické výsledky zadní lamelární transplantace Descemetské membrány s endotelem (DMEK) novou metodou oddělení dárcovské Descemetské membrány (DM) hydroseparací v 6 měsíční sledovací době.
Materiály a metody: Retrospektivní studie jednoho centra a chirurga u 16 očí po sobě jdoucích pacientů, kteří podstoupili DMEK anebo DMEK kombinovaný s operací katarakty se separací membrány dárce kapalinou. K oddělení DM dárcovské rohovky byl použit Ringerův roztok vstříknutý pod tlakem mezi DM a rohovkové stroma pomocí tupé jehly. Hustota buněk endotelu, korigovaná a nekorigovaná zraková ostrost (CDVA, UDVA) a topografie rohovky K2, K1 se vyhodnotila před a šest měsíců po transplantaci.
Výsledky: DM s endotelem pro DMEK se úspěšně a bez roztržení oddělila z rohovky dárce ve všech případech a u všech pacientů došlo k její adhezi k rohovce příjemce. Celkově se korigovaná zraková ostrost do dálky CDVA zlepšila signifikantně (p < 0,0001) z 0,69 logMAR (0,45–0,92, 95% CI) na 0,1 logMAR (0,04–0,15). Nekorigovaná zraková ostrost do dálky UDVA byla horší u pacientů po kombinované operaci katarakty a DMEK po šesti měsících 0,38 logMAR (0,18–0,43) v porovnání s 0,3 logMAR (0,14–0,61) u pacientů po DMEK. U rohovkového astigmatismu došlo k signifikantnímu zlepšení K2-K1 (p = 0,0137) z předoperačního průměru všech očí 2,89 D (0,19–0,43) na 0,98 D (0,48–1,48) za 6 měsíců po operaci.
Závěr: Hydroseparace je efektivní a rychlou metodou oddělení dárcovského štěpu pro DMEK. DMEK pomocí hydroseparace štepu dárce zlepšuje zrakovou ostrost a produkuje pouze malou hodnotu astigmatismu šest měsíců po operaci. Další klinické studie jsou potřeba k potvrzení úspěšnosti této metody a v případě kombinované operace s kataraktou k optimalizaci kalkulace optické mohutnosti nitroočních čoček.
Klíčová slova:
DMEK – transplantace rohovky – endotel – Descemetská membrána – hydroseparace
Úvod
Zadní lamelární keratoplastika Descemetské membrány s endotelem (DMEK), kdy je transplantována pouze tenká Descemetská membrána (DM) s vrstvou endotelu se stává stále více populární pro chirurgické řešení Fuchsovy dystrofie a bulózní keratopatie [8] a je u těchto indikací považována za metodu volby. Separace DMEK štěpu je obyčejně provedena opatrným seškrábnutím a sloupnutím DM z dárcovské rohovky [1,6]. Tento proces je časové náročný, vyžaduje vysokou zručnost a přináší nemalé riziko protržení membrány [2,8,15]. Nedávno se objevily nové metody, u kterých dochází k oddělení DM pomocí vzduchu/tekutiny injikované mezi DM a rohovkové stroma [9,13,14,16]. Přímo kapalinové oddělení pomocí jehly zasunuté mezi DM a rohovkové stroma je rychlý a jednoduchý způsob, který minimalizuje riziko roztržení membrány [11,16]. Navíc v průběhu oddělení pomocí kapaliny je možné současně obarvit pouze DM na straně rohovkového stromatu a tím minimalizovat chemické působení trypanovou modří na citlivé endotelové buňky [19]. Oddělená DM je transplantována a její adheze k příjemcově rohovce je podporována vzduchovou bublinou v přední komoře.
Tato studie se zabývá oddělením DMEK štěpu injektáží kapaliny (hydroseparace) mezi DM a rohovkové stroma s Duovou vrstvou [3]. Cílem je poskytnout první klinické výsledky této nové techniky provedené u dvou skupin pacientů - DMEK a kombinovaného zákroku DMEK s operací katarakty.
Materiály a metody
Souhlas a etická komise: Souhlas s provedením zákroku byl obdržen od všech pacientů před zákrokem a etická komise udělila svolení k retrospektivní analýze anonymizovaných dat.
Dárcovská tkáň: Dárcovské rohovky byly obdrženy z tkáňové banky Národního centra tkání a buněk (Brno, Česká republika) a Fakultní nemocnice Královské Vinohrady (Praha, Česká republika).
Design studie: Retrospektivní analýza DMEK a kombinované operace katarakty s DMEK na sérii konsekutivních operací pacientů operovaných v jednom centru v období od listopadu 2014 do února 2016. Separace i transplantace membrány byly provedeny jedním chirurgem (PS) na oční klinice Gemini (Zlín, Česká republika) v průběhu jedné návštěvy. Zastoupení pohlaví pacientů bylo šest mužů a devět žen ve věku 67 ± 7,7 let (průměr ± směrodatná odchylka). U osmi případů se jednalo pouze o DMEK a u osmi o kombinovaný výkon DMEK s operací katarakty.
Příprava membrány pro DMEK: Dárcovská rohovka se vyjme, opláchne Ringerovým roztokem a upevní na podtlakovém držáku. Nemusí se použít umělá přední komora. Polotupou špátlí zavedenou pod DM zevně od trabekula se vytvoří tunel (Obrázek 1) tak, že se špátle posouvá vpřed a zároveň mírně nadzvedává DM. Potom se do tohoto tunelu zavede kanyla s plochým koncem (např. cat. number 585155, BVI Beaver-Visitec International, Waltham, MA, USA), upevněná na stříkačce naplněné Ringerovým roztokem (Obrázek 2). Nemusí se používat špičatá jehla, protože kanyla se zavádí přímo mezi DM a rohovkové stroma. Ústí kanyly může zůstat na straně, anebo se může zavést blíže ke středu rohovky. Pozice ústí kanyly nebude mít vliv na velikost bubliny, protože ta vzniká mezi rohovkovým stromatem a DM vrstvou, a ne v DM vrstvě jako takové. Důležité je, aby tunel byl dostatečně dlouhý a těsný, aby většina vstřikované tekutiny proudila do prostoru mezi DM a rohovkové stroma. Kanyla je při injektáži udržována ve stejné pozici, anebo je opatrně posouvána pod DM směrem do středu rohovky. Používá se Ringerův roztok, který vytvoří prostor pod DM před jehlou. Při určitém tlaku tekutiny dojde k oddělení DM od rohovkového stromatu s Duovou vrstvou (Obrázek 3) a vytvoří se velká konvexní bublina [19]. Následující videa demonstrují techniku metody a provedení operace: https://youtu.be/Mr5DynQT1Ow a https://youtu.be/2GRNiIiCrWs. Kapalina pod membránou je odsáta stejnou kanylou, kterou byla vstříknuta a DMEK štěp je připraven k trepanaci na požadovaný průměr. Rohovka se umístí do konkávního držáku endotelovou stranou vzhůru a poté je vyříznuta trepanem o průměru 8,5 až 9,0 mm. Hydroseparovaná DM s endotelem se lehce sejme vázací pinzetou a umístí do misky s Ringerovým roztokem. Membrána má tendenci se srolovat endotelovou stranou vně. Po obarvení trypanovou modří je připravena k transplantaci.
Image 1. Otvor vytvořený pod DM před oddělením pomocí kapalinové bubliny 
Image 2. Jehla je zavedena do otvoru pod DM tak, aby se oddělila DM od rohovkového stroma a Dua vrstvy 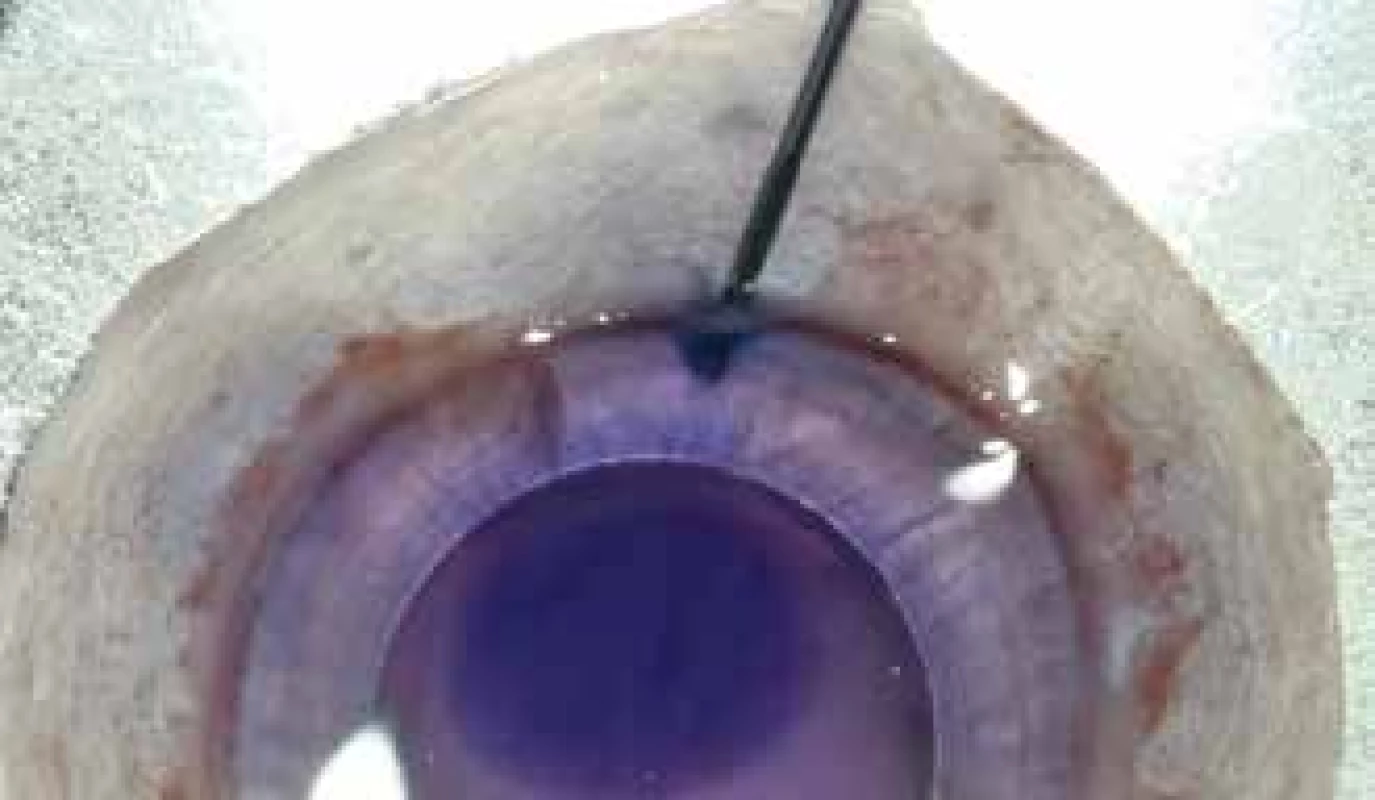
Image 3. Konvexní DM separace bublinkou kapaliny. Vzduchová bublinka a trypanová modř k obarvení DM 
Operace katarakty s implantací nitrooční čočky: V některých případech byl DMEK kombinován s operací katarakty. Operace katarakty se provedla 2,2 mm širokým řezem přístrojem Stellaris PC (Bausch and Lomb, Bridgewater, NJ, USA). Při operaci nebyl nitroočně použit žádný viskomateriál (OVD). Jak kontinuální cirkulární kapsulorhexe (CCC), tak implantace umělé nitrooční čočky byly provedeny při stabilizaci oka irigační kanylou zavedenou pomocnou rohovkovou incizí. Do čočkového vaku byla implantována monofokální hydrofilní nitrooční čočka.
Transplantace DM: DM příjemce je odstraněna seškrábnutím pod infuzí vzduchu do přední komory pod tlakem 40 mmHg. DMEK štěp je zaveden do přední komory hlavní incizí 2,2 mm rovnou skleněnou pipetou (DORC International BV, Holandsko) a rozbalen endotelem dolů pokud možno bezkontaktní metodou. Přední komora je částečně naplněna bublinou vzduchu tak, aby při poloze obličejem nahoru bublina přitlačovala štěp k rohovkovému stromatu.
Pooperační péče: Po operaci byly předepsány kombinované protizánětlivé a antibiotické kapky (Tobradex, Alcon) a pacienti dostali instrukce držet hlavu obličejem vzhůru po dobu tří dnů do vstřebání vzduchové bubliny a byli pozváni na kontrolu týden po zákroku. Předněsegmentová optická koherenční tomografie (AC-OCT) přístrojem Casia SS-1000 (Tomey, Japonsko) byla provedena k zobrazení přilnutí DM. Pokud nedošlo k úplnému přichycení DM, zopakovalo se zavedení vzduchové bubliny do přední oční komory.
Vyhodnocení: Vyhodnocovala se průměrná hustota buněk centrálního endotelu spekulárním mikroskopem EM-3000 (Tomey, Japan) na oku příjemce v počtu buněk na mm2. Nekorigovaná a korigovaná zraková ostrost na dálku (UDVA, CDVA) v logMAR, subjektivní refrakce (SR) převedená na sférický ekvivalent, subjektivní astigmatismus (SA) a rohovkový astigmatismus vyjádřený jako rozdíl K2-K1 měřené Tonoref II (Nidek ltd, Japan) před transplantací, v prvním týdnu, prvním, třetím a šestém měsíci po operaci. Pro zjednodušení jsou data prezentována pouze před transplantací a šest měsíců po operaci.
Statistické metody: Pokud není uvedeno jinak, všechny hodnoty jsou uvedeny jako průměr a 95% interval spolehlivosti. Jelikož analyzovaná data nejsou z normálního-Gaussova rozdělení, použil se neparametrický Wilcoxonův test pro vyhodnocení dat před operací a 6 měsíců po. Počet buněk endotelu a UDVA v šestém měsíci byly porovnány pomocí Mann-Whitney testu.
Výsledky
U všech 16 očí bylo na operačním sále těsně před transplantací provedeno oddělení DMEK štěpu hydroseparací až k periferii. Zde jsou 6 měsíční výsledky: Celkově došlo k signifikantnímu zlepšení UDVA (p=0,0012) z průměrné předoperační zrakové ostrosti 0,85 logMAR (95% CI, 0,64-1,05) na průměrných 0,31 logMAR (0,19-0,43). CDVA se také zlepšila signifikantně (p<0,0001) z 0,69 logMAR (0,45-0,92) na 0,1 logMAR (0,04-0,15), ke zlepšení došlo u všech pacientů a 15/16 pacientů dosáhlo minimální zrakové ostrosti 0,3 logMAR (Graf 1 a 2). UDVA byla horší u kombinovaných kataraktových případů v porovnání s čistým DMEK, v průměru 0,38 logMAR (0,18–0,43) v porovnání s 0,3 logMAR (0,14 – 0,61), nicméně toto nebylo signifikantní (p=0,7786, Mann-Whitney). Průměrná subjektivní refrakce na dálku a subjektivní astigmatismus se nezměnily signifikantně ani u jedné skupiny. Keratometrie K1 a K2 nemohly být změřeny u 3 z 16 pacientů před transplantací. Celkově došlo k signifikantnímu zmenšení rohovkového astigmatismu K2-K1 (p=0,0137) z 2,89 D (0,19-0,43) na 0,98 D (0,48–1,48) u všech změřených očí se průměrné zakřivení rohovky signifikantně snížilo (p=0,0234) ze 44,9 D (43,63–46,22) předoperačně na 44,35 D (42,86–45,83) (Tabulka 1.).
Graf 1, 2. Korigovaná a nekorigovaná zraková ostrost (CDVA a UDVA) u obou skupin šest měsíců po transplantaci 
Table 1. Subjektivní refrakce, subjektivní astigmatismus a topografie rohovky 6 měsíců po transplantaci u DMEK a DMEK kombinovaných s kataraktou 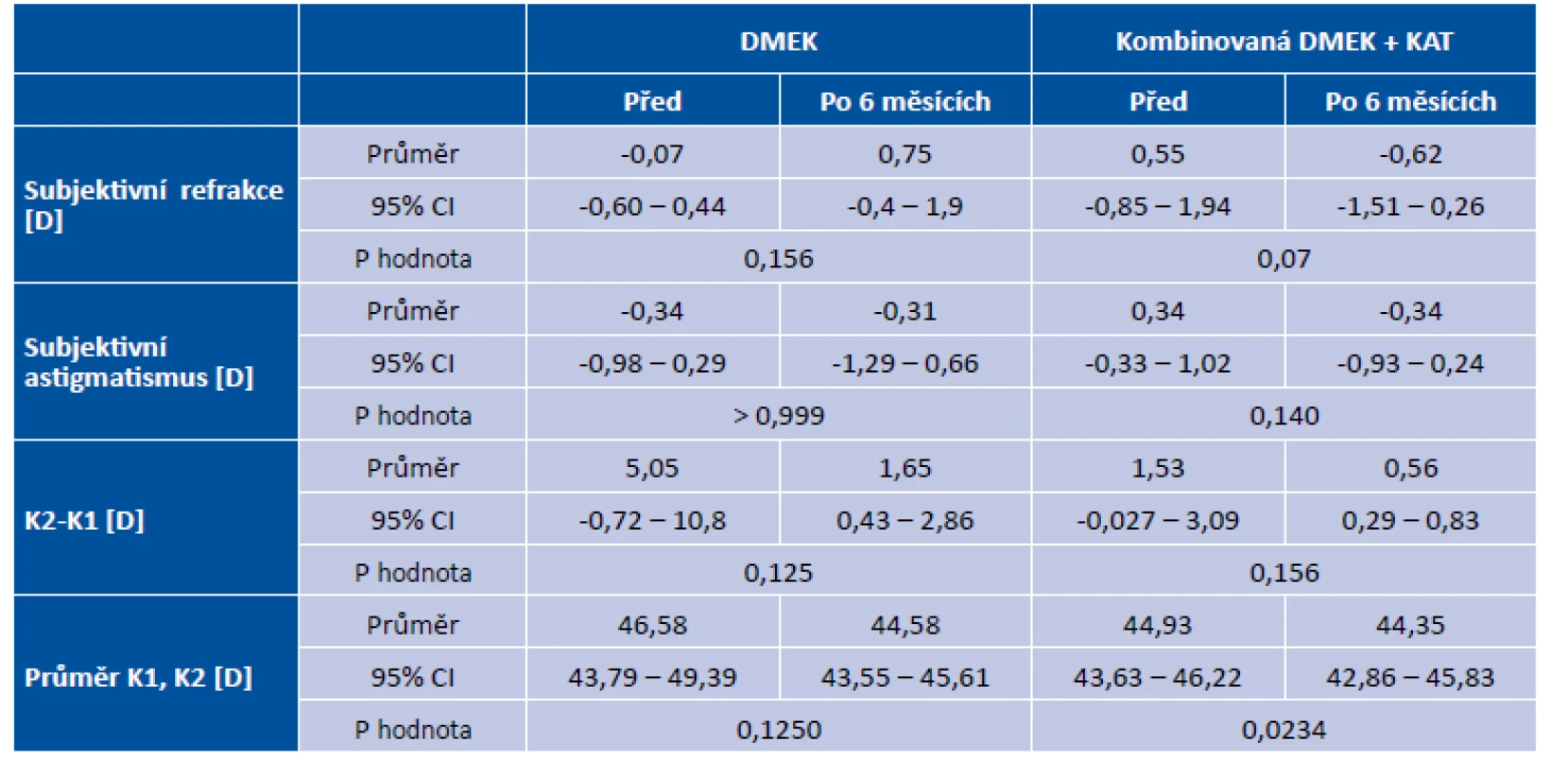
Průměrná hustota buněk endotelu poskytnutá tkáňovou bankou byla u dárcovské rohovky 2826 buněk/mm2 (95 % CI, 2670-2983). Šest měsíců po transplantaci činila průměrná hustota endotelových buněk u všech očí 1336 (95% CI, 1111-1561) buněk/mm2. U DMEK operací byla 1230 (95 % CI, 997 1463) buněk/mm2 a u kombinovaných operací byla 1483 (925-2042) buněk/mm2. Rozdíl mezi těmito dvěma skupinami nebyl statisticky signifikantní (p=0,4318, Mann-Whitney).
Na týdenní kontrole nebyla transplantovaná membrána zcela přiložena u 8/16 očí. K přiložení membrány vedla opakovaná aplikace bubliny vzduchu do přední komory. Dolní část membrány přilnula lépe u (5/8) případů než vrchní část. Žádné další komplikace se neobjevily.
Diskuse
Metoda separace membrány dárcovské rohovky pro DMEK injekcí kapaliny mezi DM a rohovkové stroma zkracuje čas přípravy a snižuje riziko roztržení membrány [11,16]. Tato metoda má teoretický potenciál pro celkově vyšší počet buněk endotelu po operaci z důvodu menší mechanické manipulace na straně endotelu v porovnání s klasickou metodou škrábaní. Zde prezentujeme prvních šest měsíců klinických výsledků u této nové metody DMEK operace pomocí separace kapalinou, která je vstříknuta přímo mezi DM a rohovkové stroma a tlakem oddělí tyto dvě vrstvy.
Protože rohovkové stroma zůstane nedotčené, membrána se může odloupnout společně s okolní tkání, upevnit na podstavec a vyříznout trepanem. Tímto zůstane zbytek dárcovské tkáně nepoškozený a může se použít např. pro hlubokou přední lamelární keratoplastiku (DALK) podobně jako popsal Groeneveld-van Beck [4], což je další výhodou popsaného postupu.
Námi sledovaný úbytek počtu endotelových buněk je sice značný, ale hodnoty hustoty buněk endotelu šest měsíců po transplantaci v této studii se v podstatě neliší od předchozích výsledků jiných multicentrických studií [8,10]. Na XXVI. výročním sjezdu České oftalmologické společnosti v sekci Rohovka II bylo diskutováno, že průměrná hustota buněk endotelu udávaná tkáňovými bankami je spíše vyšší, než jaké se běžně vyskytují v praxi [16]. Absolutní pooperační úbytek je tak závislý na měření udávané tkáňovými bankami. Udávaná hodnota hustoty buněk endotelu může být nižší z důvodu rozdílu v měřící metodě in-vivo a ex-vivo [20], nepřesného označení mrtvých buněk [6,22], ale může být také závislá na délce skladování zejména u mladších dárců [15]. V budoucnosti by bylo vhodné zaměřit se na metodiku měření endotelových buněk před operací tak, aby bylo možné provést pooperační vyhodnocení úbytku přesněji.
15 ze 16 očí dosáhlo minimální korigované zrakové ostrosti do dálky CDVA deklarované pro řízení (0,3 logMAR) po šesti měsících. Nekorigovaná zraková ostrost UDVA byla horší u případů s kombinovanou kataraktou, protože průměrná SR byla myopická. Vzhledem k tomu, že předchozí studie DMEK vykazovaly hyperopickou SR při kalkulaci na emetropii [5,17], byla optická mohutnost nitrooční čočky zvýšena oproti kalkulaci, což zapříčinilo myopickou výslednou SR. Další optimalizace výpočtu nitroočních čoček u kombinovaných případů bude předmětem dalších studií.
Nejčastější pooperační komplikací je neúplné přilnutí implantované DM. Četnost, kdy se musela zavést vzduchová bublinka znovu je různorodá a udává se mezi 9-82 % [13]. V naší studii se musela bublinka zavést znovu u 50 % očí a následně došlo k úplnému kompletnímu zhojení u všech očí. V případech, kde nedošlo k úplnému přilnutí v dolní části rohovky, máme podezření, že to mohlo být způsobeno nedodržením pooperačního režimu polohování hlavy, kdy došlo k posunutí bublinky do vrchní části předního segmentu oka. Vyvíjíme proto přístroj, který bude sledovat polohu hlavy pacienta po operaci a pomáhat dodržovat pooperační režim.
Tato práce poskytuje první klinické výsledky u DMEK a kombinované DMEK s operací katarakty, kdy byla dárcovská membrána připravena injektáží kapaliny mezi DM a rohovkové stroma. Tato metoda je efektivní, rychlá a s minimální manipulací na straně buněk endotelu. DMEK zlepšuje zrakovou ostrost a produkuje pouze malou hodnotu astigmatismu šest měsíců po operaci. Další klinické studie jsou potřeba k potvrzení této úspěšnosti a k další optimalizaci výpočtu v případě kombinované operace s kataraktou.
Prohlášení: První autor je konzultantem pro Bausch and Lomb. Autoři práce prohlašují, že vznik i téma odborného sdělení a jeho zveřejnění není ve střetu zájmů a není podpořeno žádnou farmaceutickou firmou.
Pavel Stodůlka, prim. MUDr., Ph.D., FEBOS-CR
Gemini oční klinika,
U Gemini 360, 760 01 Zlín,
Česká republika
e-mail: stodulka@lasik.cz
Do redakce doručeno dne: 20. 7. 2018
Do tisku přijato dne: 4. 2. 2019
Sources
1. Altaan, S.L., Gupta, A., Sidney, L.E., et al.: Endothelial cell loss following tissue harvesting by pneumodissection for endothelial keratoplasty: An ex vivo study. Br. J. Ophthalmol., 99(5); 2015 : 710–3.
2. Droutsas, K., Giallouros, E., Melles, G.R.J., et al.: Descemet Membrane Endothelial Keratoplasty. Cornea, 32; 2013 : 1075–1079.
3. Dua, H.S., Faraj, L.A., Said, D.G., et al.: Human Corneal Anatomy Redefined. Ophthalmology, 120; 2013 : 1778–1785.
4. Groeneveld-van Beek, E.A., Lie, J.T., van der Wees, J., et al.: Standardized ‘no-touch’ donor tissue preparation for DALK and DMEK: harvesting undamaged anterior and posterior transplants from the same donor cornea. Acta Ophthalmol., 91; 2013 : 145–150.
5. Ham, L., Dapena, I., Moutsouris, K., et al.: Refractive change and stability after Descemet membrane endothelial keratoplasty. J. Cataract Refract. Surg., 37; 2011 : 1455–1464.
6. Jirsova, K.: Chapter 3 and Chapter 4. Light and Specular Microscopy of the Cornea. Springer International Publishing; Book. 2017:
7. Lie, J.T., Birbal, R., Ham, L., et al.: Donor tissue preparation for Descemet membrane endothelial keratoplasty. J. Cataract Refract. Surg., 34; 2008 : 1578–1583.
8. Melles, G.R.J., Ong, T.S., Ververs, B., et al.: Descemet Membrane Endothelial Keratoplasty (DMEK). Cornea, 25; 2006 : 987–990.
9. Monnereau, C., Quilendrino, R., Dapena, I., et al.: Multicenter Study of Descemet Membrane Endothelial Keratoplasty. JAMA Ophthalmol., 132; 2014 : 1192.
10. Muraine, M., Gueudry, J., He, Z., et al.: Novel Technique for the Preparation of Corneal Grafts for Descemet Membrane Endothelial Keratoplasty. Am. J. Ophthalmol., 156; 2013 : 851–859.
11. Oellerich, S., Baydoun, L., Peraza-Nieves, J., et al.: Multicenter Study of 6-Month Clinical Outcomes After Descemet Membrane Endothelial Keratoplasty. Cornea, 36; 2017 : 1467–1476.
12. Parekh, M., Borroni, D., Ruzza, A., et al.: A comparative study on different Descemet membrane endothelial keratoplasty graft preparation techniques. Acta Ophthalmol., 2018, DOI: 10.1111/aos.13746.
13. Parekh, M., Leon, P., Ruzza, A., et al.: Graft detachment and rebubbling rate in Descemet membrane endothelial keratoplasty. Surv. Ophthalmol., 63; 2018 : 245–250.
14. Parekh, M., Ruzza, A., Salvalaio, G., et al.: Descemet Membrane Endothelial Keratoplasty Tissue Preparation From Donor Corneas Using a Standardized Submerged Hydro-separation Method. Am. J. Ophthalmol., 158; 2014 : 277–285.
15. Rodríguez-Calvo de Mora, M., Groeneveld-van Beek, E.A., Frank, L.E., et al.: Association Between Graft Storage Time and Donor Age With Endothelial Cell Density and Graft Adherence After Descemet Membrane Endothelial Keratoplasty. JAMA Ophthalmol., 134; 2016 : 91.
16. Diskuze v sekci Rohovka II. na XXVI. Výroční Sjezd České Oftalmologické Společnosti ČLS JEP v Praze 13.-15.9.2018. BOS org s.r.o. ISBN 978-80-87562-80-2
17. Salvalaio, G., Parekh, M., Ruzza, A., et al.: DMEK lenticule preparation from donor corneas using a novel ‘SubHyS’ technique followed by anterior corneal dissection. Br. J. Ophthalmol., 98; 2014 : 1120–1125.
18. Satué, M., Rodríguez-Calvo-de-Mora, M., Naveiras, M., et al.: La estandarización en el trasplante endotelial de membrana de Descemet: resultados de las primeras 450 cirugías. Arch. Soc. Esp. Oftalmol., 90; 2015 : 356–364.
19. Szurman, P., Januschowski, K., Rickmann, A., et al.: Novel liquid bubble dissection technique for DMEK lenticule preparation. Graefe’s Arch. Clin. Exp. Ophthalmol., 254; 2016 : 1819–1823.
20. Thuret, G., Deb-Joardar, N., Manissolle, C., et al.: Assessment of the human corneal endothelium: In vivo Topcon SP2000P specular microscope versus ex vivo sambacornea eye bank analyser. Br. J. Ophthalmol. 91; 2007 : 256-266.
21. van Dijk, K., Ham, L., Tse, W.H.W., et al.: Near complete visual recovery and refractive stability in modern corneal transplantation: Descemet membrane endothelial keratoplasty (DMEK). Contact Lens Anterior Eye, 36; 2013 : 13–21.
22. Wilhelmus, K.R., Stulting, R.D., Sugar, J., et al.: Primary corneal graft failure. A national reporting system. Medical Advisory Board of the Eye Bank Association of America. Arch. Ophthalmol. (Chicago, Ill. 1960), 113; 1995 : 1497–502.
Labels
Ophthalmology
Article was published inCzech and Slovak Ophthalmology

2019 Issue 1-
All articles in this issue
- Využití shear waves elastografie k diagnostice změn okohybných svalů u pacientů s endokrinní orbitopatií
- Léčba idiopatické choroidální neovaskulární membrány ranibizumabem – naše zkušenosti
- Postradiačná makulopatia u pacientov s malígnym melanómom corpus ciliare a chorioidey po stereotaktickej rádiochirurgii
- Efektivní separace tkáňových vrstev dárcovské rohovky pro DMEK injekcí tekutiny mezi Descemetskou membránu a rohovkové stroma: Výsledky prvního souboru operací
- Primární orbitální teratom
- Pozdní pooperační syndrom distenze pouzdra
- Czech and Slovak Ophthalmology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Pozdní pooperační syndrom distenze pouzdra
- Primární orbitální teratom
- Léčba idiopatické choroidální neovaskulární membrány ranibizumabem – naše zkušenosti
- Postradiačná makulopatia u pacientov s malígnym melanómom corpus ciliare a chorioidey po stereotaktickej rádiochirurgii
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

