-
Medical journals
- Career
Hodnocení očního povrchu u pacientů léčených analogy prostaglandinů s ohledem na obsaženou konzervační látku
Authors: E. Mlčáková 1; P. Mlčák 1; M. Karhanová 1; K. Langová 2; K. Marešová 1
Authors‘ workplace: Oční klinika Lékařské fakulty Univerzity Palackého v Olomouci a Fakultní nemocnice, Olomouc, přednosta prof. MUDr. Jiří Řehák, CSc., FEBO 1; Ústav lékařské biofyziky Lékařské fakulty Univerzity Palackého, Olomouc, přednosta prof. RNDr. Hana Kolářová, CSc. 2
Published in: Čes. a slov. Oftal., 72, 2016, No. 4, p. 120-127
Category: Original Article
Overview
Cíl:
Cílem studie bylo zhodnotit stav očního povrchu u pacientů léčených analogy prostaglandinů s ohledem na obsaženou konzervační látku.Metodika:
Do observační studie bylo zařazeno 60 pacientů léčených monoterapií analogy prostaglandinů pro glaukom nebo oční hypertenzi. Kontrolní skupinu tvořilo 20 pacientů se suspektním glaukomem nebo oční hypertenzí bez lokální či celkové antiglaukomatózní léčby. U všech pacientů byla zaznamenána demografická data, osobní a oční anamnéza. Pacienti vyplnili dotazník složený z českého překladu Ocular surface disease index© (OSDI). Na sledovaných očích byla v rámci očního vyšetření zhodnocena úroveň hyperémie spojivky dle Efrona, odečten break up time (BUT) a stanoven stupeň barvení spojivky a rohovky podle Oxfordské klasifikace. Léčení pacienti byli rozděleni podle použité konzervační látky v léčivém přípravku na 3 skupiny: bez konzervačních látek (18 pacientů), s konzervační látkou polykvadium-chlorid (17 pacientů) a s konzervační látkou benzalkonium-chlorid (BAK) (25 pacientů).Výsledky:
V kontrolní skupině byla statisticky významně nižší úroveň barvení spojivky a rohovky fluoresceinem ve srovnání s pacienty ve skupinách bez konzervačních látek (p = 0,001), polykvadium-chlorid (p = 0,007) a BAK (p = 0,002). Ve skupině bez konzervačních látek byly statisticky významně nižší hodnoty hyperémie spojivky ve srovnání s pacienty ve skupině polykvadium-chlorid (p = 0,011). Mezi ostatními skupinami významné rozdíly prokázány nebyly. Rozdíl mezi skupinami ve výsledné hodnotě OSDI ani BUT nebyl statisticky významný.Závěr:
Naše studie potvrdila, že stav očního povrchu u pacientů na monoterapii analogy prostaglandinů je horší než u neléčených jedinců. Statisticky významné rozdíly mezi léčenými pacienty v závislosti na obsažené konzervační látce však prokázány nebyly.Klíčová slova:
analoga prostaglandinů, benzalkonium-chlorid, glaukom, konzervační látky, ocular surface diseaseÚVOD
Ocular surface disease (OSD) je multifaktoriální onemocnění očního povrchu spojené s nepříjemnými očními pocity, zrakovými obtížemi, nestabilitou slzného filmu a poškozením očního povrchu. Jednou z vnějších příčin dysfunkce slzného filmu je dlouhodobé užívání kapek s konzervačními látkami (2, 31), k němuž dochází především při léčbě glaukomu.
Glaukom je chronická ireverzibilní neuropatie zrakového nervu spojená s progresivní ztrátou retinálních gangliových buněk vedoucí k charakteristickým morfologickým změnám na terči zrakového nervu a ve vrstvě nervových vláken a k defektům v zorném poli (11, 24, 35).
Jediný v současné době jednoznačně léčebně ovlivnitelný rizikový faktor vzniku a progrese glaukomu je nitrooční tlak. Léky první volby se pro svou dobrou účinnost, snášenlivost, bezpečnost a jednoduchost dávkování stala analoga prostaglandinů (11, 35). Nitrooční tlak snižují zvýšením odtoku nitrooční tekutiny cestou uveosklerální a v menší míře i trabekulární. Mechanismus účinku je založen na regulaci matrix-metaloproteináz a remodelaci extracelulární matrix, což má za následek změnu permeability tkání (38). Aktuálně jsou na českém trhu dostupné přípravky obsahující latanoprost, travoprost, bimatoprost a tafluprost (9). Mezi jejich nejčastější vedlejší účinky patří hyperémie spojivky, změny řas, zvýšená pigmentace duhovky a kůže periokulárně. U řas dochází k nárůstu jejich počtu, délky a tloušťky, což může být někdy žádoucí z kosmetických důvodů, nikoli však při jednostranné léčbě. Tyto změny se vyskytují častěji při léčbě bimatoprostem a travoprostem (1). Zvýšená pigmentace kůže je reverzibilní na rozdíl od pigmentace duhovky, která je trvalá. Dosud nebyly nalezeny podstatné rozdíly v jejím výskytu při léčbě jednotlivými analogy prostaglandinů (1). Otázka hyperémie spojivky bude diskutována níže. Mezi méně časté lokální vedlejší účinky analog prostaglandinů řadíme cysty duhovky, cystoidní makulární edém, přední uveitidu či reaktivaci herpetické keratitidy. Systémové nežádoucí účinky jsou extrémně vzácné (1).
Cílem léčby glaukomu je jednak předejít jeho progresi, jednak zabránit snižování kvality života, čehož lze dosáhnout mimo jiné minimalizováním očního diskomfortu při chronické lokální léčbě (8, 31, 40). Proto je nezbytné ke každému pacientovi přistupovat individuálně a léčbu volit dle jeho potřeb (34). Bezpečnost léčby u glaukomu by měla být na prvním místě (21). Většina vedlejších účinků lokální léčby u pacientů s glaukomem je způsobena spíše konzervačními látkami než aktivní substancí (2, 37).
Konzervační látky se do očních kapek přidávají za účelem zachování sterility roztoku. V oftalmologii je nejrozšířenější konzervační látkou benzalkonium-chlorid (BAK) (2, 26, 27, 29). Jedná se o ve vodě dobře rozpustnou nitrogenní kationickou povrchově aktivní látku patřící mezi kvartérní amoniové soli. Rozpouští bakteriální stěny a cytoplazmatické membrány. Konzervační látky, zvláště BAK, mají nežádoucí účinky na povrchové tkáně oka a jejich dlouhodobé užívání způsobuje subklinický zánět spojivky, úbytek pohárkových buněk, fibrózní proliferaci v substancia propria spojivky a Tenonově membráně (2, 37), což následně potencuje pooperační jizvení a může vést až k selhání filtrační operace (2). BAK ovlivňuje slzný film jak svým detergentním působením na lipidovou vrstvu, tak svou toxicitou vůči pohárkovým buňkám produkujícím mucin. Oba tyto mechanismy vedou k nestabilitě slzného filmu a jeho zvýšené evaporaci. BAK také indukuje apoptózu buněk trabekula, a pokud dojde k jeho absorpci nosní sliznicí, může u vnímavých jedinců způsobit bronchokonstrikci (2). Rossi et al. (31) však uvádí, že krátkodobá expozice BAK není spojena se změnami očního povrchu.
Toxicita BAK závisí na dávce (2), při léčbě glaukomu je tedy snahou snížit počet aplikovaných kapek s BAK, a to použitím fixní kombinace, přípravku bez BAK či zcela bez konzervačních látek (11, 30).
Je obtížné docílit, aby konzervační látka nebyla toxická a zároveň měla dostatečný antimikrobiální efekt. Alternativou BAK, dostupnou v České republice, je polykvadium-chlorid. Patří do skupiny polykationických polymerů. Narušuje buněčnou membránu bakteriálních buněk, avšak nepůsobí jako detergent a jeho velká molekula neproniká do savčích buněk (29). Byl vyvinut v 80. letech 20. století jako konzervační látka do roztoků na kontaktní čočky, v současnosti je také součástí antiglaukomatik a umělých slz. Je sice méně toxický než BAK (18, 26), ale také vede k buněčné smrti a uvolňování prozánětlivých cytokinů (26).
Přípravky bez konzervačních látek jsou spojeny s vyššími náklady, často se vyrábí v jednodávkových obalech, které mohou činit potíže při manipulaci, zejména u méně zručných pacientů a pacientů s významným poškozením zraku. Navíc k zachování požadovaných vlastností účinné látky je někdy nutné léčivý přípravek obohatit o speciální příměs. Například aktuálně jediný latanoprost bez konzervačních látek (Monopost®) obsahuje komplex polymerů s funkcemi surfaktantu, který zajišťuje stabilní pH a patřičnou viskozitu roztoku, stabilitu aktivní látky při pokojové teplotě, zabraňuje adsorpci latanoprostu na vnitřní povrch obalu (1) a usnadňuje jeho průnik do oka (33).
Batra et al. (4) prosazují kombinovaný přístup k léčbě glaukomu, který zahrnuje i zvládnutí OSD, což vede ke zlepšení kontroly nitroočního tlaku a snížení potřeby drenážních operací. Oční povrch by měl být u pacientů s glaukomem či oční hypertenzí pravidelně sledován (3, 11, 19, 30, 31). Mezi nejčastěji používané diagnostické testy patří dotazníky, hodnocení stability slzného filmu (break up time (BUT)), barvení očního povrchu (fluoresceinem, lisaminovou zelení nebo bengálskou červení). Kombinace i interpretace těchto testů jsou však nejednotné, chybí všeobecně uznávaný konsenzus pro diagnostiku OSD (19, 20). Labbé et al. (19) vidí perspektivu v zavedení měření osmolarity slzného filmu do diagnostického schématu OSD. U pacientů léčených antiglaukomatiky je zvýšená osmolarita slzného filmu. Byla prokázána její korelace s počtem užívaných přípravků. Tento jev je vysvětlován na základě chemických vlastností konzervačních látek, které působí zejména na lipidovou vrstvu slzného filmu, čímž snižují jeho stabilitu, zvyšují evaporaci a tím i osmolaritu (19).
Cílem naší studie bylo zhodnotit stav očního povrchu u pacientů léčených analogy prostaglandinů s ohledem na obsaženou konzervační látku.
METODIKA
Design studie
Do observační studie byli zařazeni pacienti léčení monoterapií analogy prostaglandinů pro glaukom (primární či sekundární) nebo oční hypertenzi, kteří byli vyšetřeni v glaukomové poradně Oční kliniky Fakultní nemocnice Olomouc od začátku září 2014 do konce února 2015. Kontrolní skupinu tvořili pacienti se suspektním glaukomem nebo oční hypertenzí bez lokální či celkové antiglaukomatózní léčby. V případě opakované návštěvy pacienta během sledovaného období byla pro hodnocení v této studii použita data získaná při jeho první návštěvě. Inkluzní kritéria obsahovala: věk nad 18 let, léčba analogem prostaglandinů v monoterapii, minimální délka aktuální antiglaukomatózní léčby 4 měsíce. Exkluzní kritéria zahrnovala: operace nebo úraz oka méně než rok před prováděným hodnocením, aktivní zánětlivé onemocnění oka, nositel kontaktních čoček, přítomnost systémového onemocnění asociovaného se syndromem suchého oka, aplikace konkomitantní lokální oční léčby s obsahem konzervačních látek v posledních 3 měsících. Studie byla realizována v souladu s Helsinskou deklarací. Všichni pacienti byli podrobně informováni a vyslovili souhlas se zařazením do studie.
Postup
U všech pacientů byla zaznamenána demografická data, osobní a oční anamnéza, včetně délky léčby aktuálním léčivým přípravkem a frekvence aplikace umělých slz. Pacienti vyplnili dotazník složený z českého překladu Ocular surface disease index© (OSDI) (25). Při následujícím klinickém vyšetření byla na sledovaných očích nejprve zhodnocena úroveň hyperémie spojivky dle Efrona (10) a bezprostředně po aplikaci 1 kapky 0,2% roztoku fluoresceinu byl na štěrbinové lampě s použitím modrého kobaltového filtru a zvětšení 16x odečten BUT (jako interval mezi posledním mrknutím a vznikem první tmavé skvrny) a poté stanoven stupeň barvení spojivky a rohovky podle Oxfordské klasifikace (5).
Charakteristika souboru
Ve sledovaném období bylo do studie zařazeno celkem 80 pacientů (156 očí). Z toho 20 pacientů (40 očí) ve věku 20–70 let (medián 61,5 let), 7 mužů a 13 žen, tvořilo kontrolní soubor. 60 pacientů (116 očí) léčených analogem prostaglandinů bylo rozděleno podle použité konzervační látky v léčivém přípravku na 3 skupiny: bez konzervačních látek – 18 pacientů (36 očí) ve věku 22–76 let (medián 60,5 let), 6 mužů a 12 žen; s konzervační látkou polykvadium-chlorid – 17 pacientů (34 očí) ve věku 18–79 let (medián 64,0 let), 6 mužů a 11 žen a s konzervační látkou BAK – 25 pacientů (46 očí) ve věku 23 – 83 let (medián 65,0 let), 12 mužů a 13 žen. Přehled užívaných léčivých přípravků ve skupinách je uveden v tabulce 1. Pokud byla léčba aplikována pouze do jednoho oka a druhé oko bylo bez léčby, byl pacient zařazen do příslušné skupiny podle použité konzervační látky v léčivém přípravku a hodnoceno bylo pouze léčené oko.
Table 1. Přehled užívaných léčivých přípravků 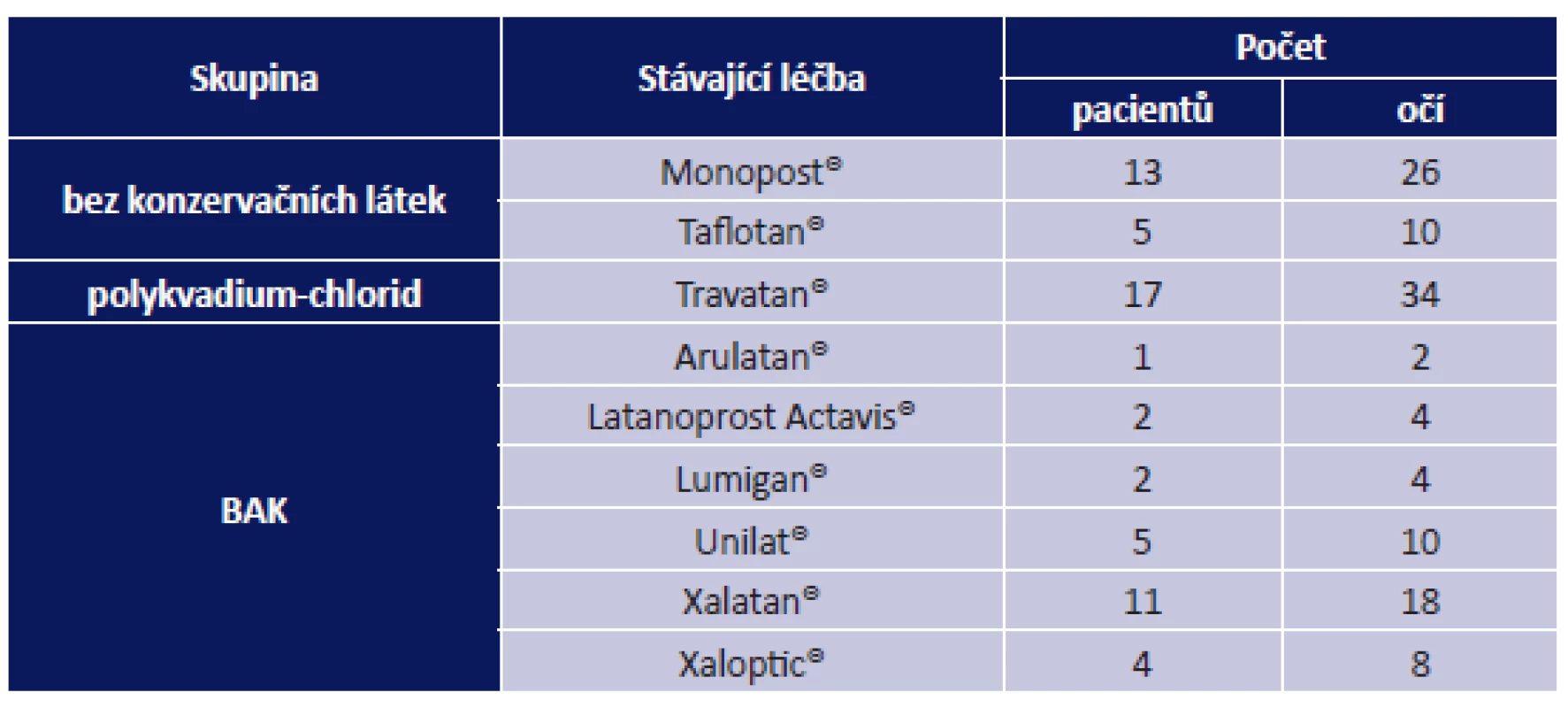
Pozn.: BAK – benzalkonium-chlorid Analýza dat a statistické hodnocení
Data zařazených pacientů byla zaznamenána do formulářů, po provedení výpočtu OSDI převedena do elektronické podoby, podrobena deskriptivní analýze a statisticky zpracována. Ke statistickému zpracování byl použit statistický software IBM SPSS Statistics 22. Data byla popsána pomocí ukazatelů popisné statistiky – průměru, směrodatné odchylky, minimální a maximální hodnoty a mediánu. Vzhledem k velikosti skupin a charakteru dat byl pro porovnání v kvantitativních znacích použit neparametrický Kruskal-Wallisův test. Pro porovnání skupin v kvalitativních znacích byl použit Fisherův přesný test. Všechny statistické testy byly provedeny na hladině signifikance 0,05.
VÝSLEDKY
Rozdíl ve věkovém složení ani v zastoupení jednotlivých pohlaví ve srovnávaných skupinách nebyl statisticky významný (tab. 2, tab. 3). Ve skupině bez konzervačních látek byly statisticky významně nižší hodnoty délky léčby aktuálním přípravkem ve srovnání se skupinou polykvadium-chlorid (p = 0,001) a skupinou BAK (p = 0,004) (viz tab. 3). Mezi skupinami polykvadium-chlorid a BAK významné rozdíly prokázány nebyly (p = 1,000). Normální hodnotu OSDI mělo ve skupině bez konzervačních látek 56 % pacientů, ve skupině polykvadium-chlorid 59 %, ve skupině BAK 72 % a v kontrolní skupině 85 %. Hodnoty svědčící pro těžké OSD byly zastoupeny pouze ve skupině BAK, a to u 8 % pacientů (graf 1). Srovnání zastoupení hodnot BUT v jednotlivých skupinách je znázorněno v grafu 2. Rozdíl mezi skupinami ve výsledné hodnotě OSDI ani BUT nebyl statisticky významný (viz tab. 3, tab. 4). Nejnižší stupeň barvení spojivky a rohovky fluoresceinem byl zaznamenán u 33 % pacientů ve skupině bez konzervačních látek, 44 % ve skupině polykvadium-chlorid, 41 % ve skupině BAK a u 75 % pacientů kontrolní skupiny. Nejvyššího stupně barvení spojivky a rohovky v této studii (Oxford III) dosáhlo 6 % pacientů skupiny polykvadium-chlorid a 7 % pacientů skupiny BAK (graf 3). V kontrolní skupině byla statisticky významně nižší úroveň barvení spojivky a rohovky fluoresceinem ve srovnání s pacienty ve skupinách bez konzervačních látek (p = 0,001), polykvadium-chlorid (p = 0,007) a BAK (p = 0,002). Mezi ostatními skupinami významné rozdíly prokázány nebyly (viz tab. 4). Ve skupině bez konzervačních látek byly statisticky významně nižší hodnoty hyperémie spojivky ve srovnání s pacienty ve skupině polykvadium-chlorid (p = 0,011). Mezi ostatními skupinami významné rozdíly prokázány nebyly (viz tab. 4, graf 4). Umělé slzy nekapalo nebo neznalo 90 % pacientů v kontrolní skupině, 67 % ve skupině bez konzervačních látek, 59 % ve skupině polykvadium-chlorid a 76 % ve skupině BAK (graf 5).
Table 2. Zastoupení pohlaví 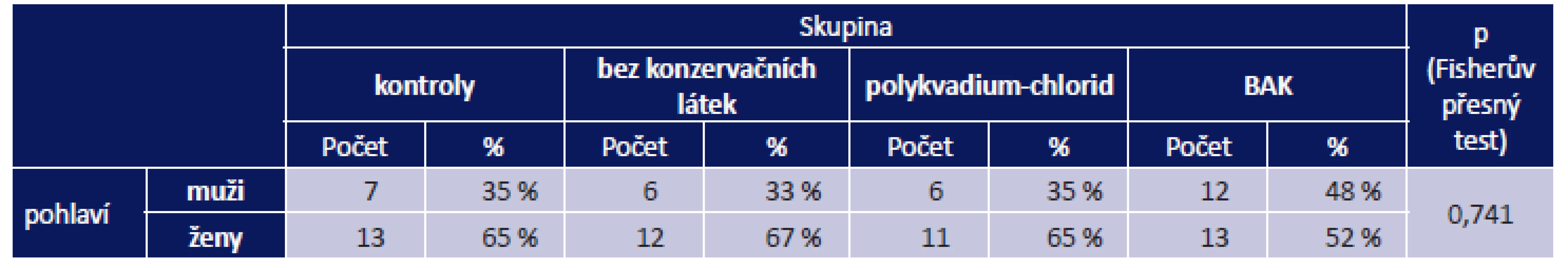
Pozn.: BAK – benzalkonium-chlorid Table 3. Věkové složení skupin, Ocular surface disease index© a délka stávající léčby 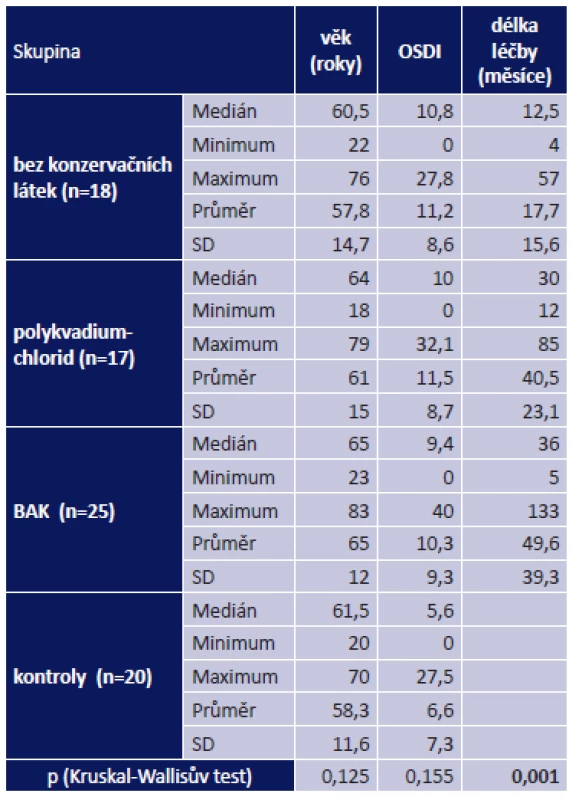
Pozn.: OSDI – Ocular surface disease index©; BAK – benzalkoniumchlorid; SD – směrodatná odchylka Table 4. Výsledky hodnocení očního povrchu 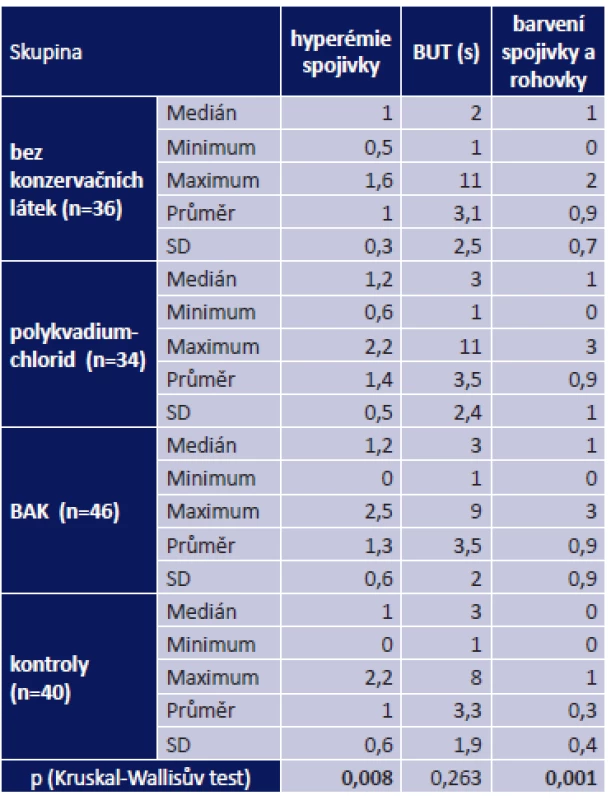
Pozn.: BUT – break up time; BAK – benzalkonium-chlorid, SD – směrodatná odchylka Graph 1. Ocular surface disease index<sup>©</sup> Pozn.: OSD – ocular surface disease 
Graph 3. Barvení spojivky a rohovky fluoresceinem 
Graph 5. Frekvence aplikace umělých slz 
DISKUSE
V mnoha klinických studiích (14, 19, 20, 28, 36) více než polovina pacientů užívajících antiglaukomatózní terapii udávala subjektivní potíže spojené s OSD.
Dle Piselly et al. (28) je třeba minimalizovat vedlejší účinky léčby, což přispěje k nárůstu její efektivity, podpoře compliance a pokračování v léčbě. Lokální léčba by neměla snižovat úspěch případné chirurgické léčby glaukomu. Nenápadné známky oční toxicity jako tečkovitá keratopatie svědčí pro chronické poškození buněk, které může mít dlouhodobé následky. Aplikace konzervačních látek vyvolává v rohovce redukci buněčné proliferace a viability s následným narušením hojení a ohrožením epiteliální bariéry (28).
Výskyt příznaků OSD při léčbě antiglaukomatiky závisí na množství konzervační látky, vzrůstá s počtem aplikovaných kapek a klesá po konverzi na přípravek bez konzervačních látek, což je mimo jiné důkazem reverzibility známek OSD (28).
Uusitalo et al. (39) srovnávali účinnost a snášenlivost tafluprostu bez konzervačních látek s latanoprostem s BAK. Po 3 měsících od výměny latanoprostu za tafluprost byla hodnota nitroočního tlaku stejná a došlo k významné redukci subjektivních potíží (až o 50 %), barvení rohovky a spojivky, hyperémie spojivky a naopak zvýšení hodnoty Schirmerova testu a BUT.
Ve studii (15) zabývající se účinností a snášenlivostí tafluprostu bez konzervačních látek u pacientů původně léčených analogem prostaglandinů s BAK se po 3 měsících od změny léčby signifikantně snížil nitrooční tlak, zlepšili subjektivní potíže a redukovaly objektivní vedlejší účinky. Výskyt střední až těžké hyperémie spojivky poklesl ze 43,2 % na 1,9 %.
Rouland et al. (33) srovnávali účinnost a bezpečnost latanoprostu bez konzervačních látek s latanoprostem s BAK. Po 84 dnech od počátku léčby (zahájené po uplynutí vymývacího intervalu) byla hodnota nitroočního tlaku srovnatelná, zatímco ve skupině bez konzervačních látek byl signifikantně nižší výskyt subjektivních potíží a střední až těžké hyperémie spojivky (21 % versus 29 %), rozdíl v barvení rohovky zaznamenán nebyl.
V multicentrické studii (17) provedené v České republice byla hodnocena účinnost a snášenlivost tafluprostu bez konzervačních látek u pacientů s nově zahájenou léčbou či převedených z jiné antiglaukomatózní terapie na tafluprost. Nejčastějšími důvody pro změnu na tafluprost byly lokální nesnášenlivost stávající léčby (iritace oka a hyperémie spojivky) (67,7 %) a její nedostatečná účinnost (34,6 %). Nitrooční tlak po změně na tafluprost signifikantně poklesl a zlepšila se subjektivní snášenlivost.
Nežádoucí účinky jsou druhým nejčastějším důvodem ke změně léčby po nedostatečné účinnosti (43). Klinické studie (15, 17, 28, 33, 39) dokazují, že výměna přípravku s BAK za preparát bez BAK vede ke zlepšení stavu očního povrchu pacienta.
Cvenkel et al. (8) hodnotili subjektivní a objektivní příznaky OSD u pacientů léčených antiglaukomatiky s konzervačními látkami, kteří měli ve srovnání s kontrolní neléčenou skupinou signifikantně kratší BUT a vyšší stupeň barvení spojivky a rohovky dle Oxfordské klasifikace, což bylo v korelaci s počtem kapek aplikovaných za den.
Rossi et al. (32) sledovali přítomnost OSD u pacientů užívajících antiglaukomatika s konzervačními látkami ve vztahu k počtu kapek aplikovaných za den. S rostoucím počtem aplikovaných kapek za den se sice zvyšovala úroveň hyperémie spojivky a četnost výskytu tečkovitých defektů rohovky, ale rozdíl mezi skupinami nebyl signifikantní stejně jako při srovnání OSDI. V další studii Rossi et al. (31) zaznamenali u pacientů léčených pro glaukom či oční hypertenzi abnormální BUT u 30,5 % očí a tečkovitou keratopatii u 31,7 % očí.
Leung et al. (20) při monitorování OSD u glaukomatiků zjistili, že každá další kapka s BAK za den je spojena s dvakrát vyšší pravděpodobností abnormálního barvení spojivky a rohovky lisaminovou zelení, ovšem závislost mezi počtem kapek s BAK za den a BUT, Schirmerovým testem ani OSDI nebyla významná. Také korelace mezi výsledky OSDI a provedenými klinickými testy k diagnostice OSD byla slabá.
Saade et al. (36) zaznamenali abnormální OSDI u 68 % pacientů léčených antiglaukomatiky, ale pouze u 13 % subjektů v kontrolní neléčené skupině. Abnormální BUT a barvení spojivky a rohovky lisaminovou zelení pozorovali u 68 % léčených a 17 % kontrol. Zavedli index ke kvantifikaci lokální léčby (vypočítaný jako počet kapek aplikovaných za týden násobený délkou léčby v letech), který koreluje s OSDI.
Mathews et al. (23) potvrdili přímou úměrnost mezi množstvím užívaných antiglaukomatik a stupněm barvení rohovky. OSDI považují za slabý nástroj k záchytu OSD u glaukomatiků vzhledem k jeho neschopnosti odlišit potíže způsobené poškozením zorného pole.
Fechtner et al. (13) a Garcia-Feijoo et al. (14) v nezávislých studiích kvantifikovali výskyt OSD u pacientů na terapii antiglaukomatiky pomocí OSDI, které bylo abnormální u 48 %, resp. 59 % probandů. U pacientů léčených méně než 6 let byl OSDI signifikantně nižší než u pacientů léčených více než 6 let (14).
Baudouin et al. (3) identifikovali rizikové faktory pro rozvoj OSD u pacientů léčených antiglaukomatiky. Patří mezi ně věk, délka léčby, počet kapek aplikovaných za den, změna lokální léčby z důvodu intolerance, hodnota nitroočního tlaku a pokročilost glaukomu. OSD prokázali u 51 % pacientů, hyperémii spojivky u 60,3 %, barvení rohovky fluoresceinem u 34,7 % a BUT pod 5 s u 20,9 % pacientů.
Z českých autorů se konzervačním látkám v antiglaukomaticích věnují Výborný et al. (41, 42), kteří kalkulovali denní dávku BAK v očních kapkách s ohledem na velikost kapky, koncentraci BAK a frekvenci aplikace.
V naší studii jsou statisticky významně nižší hodnoty délky léčby aktuálním přípravkem ve skupině bez konzervačních látek ve srovnání se skupinou polykvadium-chlorid a skupinou BAK nejspíše dány relativně nedávným nástupem analog prostaglandinů bez konzervačních látek na český trh. Ve skupinách léčených antiglaukomatiky se ve srovnání s kontrolami vyskytoval častěji abnormální výsledek OSDI, stejně jako ve studii Saade et al. (36). Rozdíl mezi skupinami ve výsledné hodnotě OSDI ani BUT však nebyl statisticky významný, k podobnému závěru dospěli i Rossi et al. (32) a Leung et al. (20).
Absenci rozdílu v subjektivních očních příznacích mezi pacienty na terapii antiglaukomatiky a kontrolami vysvětlují Martone et al. (22). Prokázali, že počet nervových vláken v rohovce je signifikantně nižší u pacientů na lokální antiglaukomatózní léčbě než u zdravých dobrovolníků.
Statisticky významně nižší stupeň barvení spojivky a rohovky v naší kontrolní skupině ve srovnání s léčenými skupinami odpovídá výsledkům studie Cvenkel et al. (8) a Saade et al. (36). Absenci rozdílu v barvení očního povrchu mezi skupinami léčenými analogem prostaglandinů s konzervační látkou i bez ní popisují také Rouland et al. (33).
Ve skupině bez konzervačních látek byly statisticky významně nižší hodnoty hyperémie spojivky ve srovnání s pacienty ve skupině polykvadium-chlorid. Podobných výsledků dosáhli v nezávislých studiích i Uusitalo et al. (39), Hommer et al. (15) a Rouland et al. (33), kteří však srovnávali analog prostaglandinů bez konzervačních látek s analogy prostaglandinů obsahujícími BAK. Hyperémie spojivky závisí na dávce účinné látky (15) a je potencovaná vysokou koncentrací BAK, přesný mechanismus však dosud nebyl objasněn (39). Výsledky metaanalýz (6, 12, 16) ukazují, že výskyt hyperémie spojivky je nižší při léčbě latanoprostem než travoprostem. Na jejich základě se lze domnívat, že vyšší hyperémie spojivky ve skupině polykvadium-chlorid může být způsobena aktivní látkou přípravku, protože travoprost je v České republice jediný dostupný analog prostaglandinů s konzervační látku polykvadium-chlorid. Crichton et al. (7) ale neprokázali signifikantní rozdíl v hyperémii spojivky, BUT ani barvení rohovky mezi pacienty léčenými bimatoprostem, travoprostem či latanoprostem s konzervačními látkami.
Absenci rozdílu ve sledovaných znacích mezi jednotlivými léčenými skupinami si vysvětlujeme tím, že symptomatičtí pacienti většinou byli časně převedeni na šetrnější přípravek. Navíc u problematických pacientů často dochází k relativně rychlé výměně preparátů nebo noncompliance.
Naše studie je limitována velikostí zkoumaného souboru, která je zapříčiněna monocentricitou a relativně přísnými inkluzními kritérii. Vzhledem k velikosti skupin jsme neprovedli vzájemné korelace demografických dat a sledovaných znaků. Také jsme nezohlednili léčbu užívanou před aktuálním přípravkem.
Rozdílné dílčí výsledky studií mohou být vysvětleny nejednotným diagnostickým schématem při posuzování OSD. Existují však i další faktory, které mohou ovlivňovat reprodukovatelnost testů používaných k průkazu OSD. Patří mezi ně přirozené fluktuace během dne, národnostní variabilita, systémová léčba, životní prostředí a další (8).
ZÁVĚR
Glaukom je závažné zrak ohrožující onemocnění. Vedlejší účinky antiglaukomatózní léčby by neměly být přehlíženy, protože mohou mít dopad na kompenzaci glaukomu, výsledek filtrační operace, compliance a zejména kvalitu života pacienta. Jejich eliminace vede nejen ke spokojenosti pacienta a lékaře, ale i ke snížení celkových nákladů na léčbu. Naše studie potvrdila, že stav očního povrchu u pacientů na monoterapii analogy prostaglandinů je horší než u neléčených jedinců, což odpovídá výsledkům zahraničních autorů. Statisticky významné rozdíly mezi léčenými pacienty v závislosti na obsažené konzervační látce však prokázány nebyly. K tomu je třeba dalších studií na větších skupinách pacientů s použitím jednotného hodnocení OSD.
Prezentováno formou posteru na 12. kongresu Evropské glaukomové společnosti v Praze 19. – 22. 6. 2016.
Autoři práce prohlašují, že vznik i téma odborného sdělení a jeho zveřejnění není ve střetu zájmu a není podpořeno žádnou farmaceutickou firmou.
Do redakce doručeno dne 18. 4. 2016
Do tisku přijato dne 26. 7. 2016
MUDr. Eva Mlčáková
Oční klinika LF UP a FN Olomouc
I. P. Pavlova 6
779 00 Olomouc
e-mail: eva.mlcakova@fnol.cz
Sources
1. Alm, A.: Latanoprost in the treatment of glaucoma. Clin Ophthalmol, 8; 2014 : 1967–1985.
2. Baudouin, C., Labbé, A., Liang, H. et al.: Preservatives in eyedrops: the good, the bad and the ugly. Prog Retin Eye Res, 29(4); 2010 : 312–334.
3. Baudouin, C., Renard, JP., Nordmann, JP. et al.: Prevalence and risk factors for ocular surface disease among patients treated over the long term for glaucoma or ocular hypertension. Eur J Ophthalmol, 23(1); 2013 : 47–54.
4. Batra, R., Tailor, R., Mohamed, S.: Ocular surface disease exacerbated glaucoma: optimizing the ocular surface improves intraocular pressure control. J Glaucoma, 23(1); 2014 : 56–60.
5. Bron, AJ., Evans, VE., Smith, JA.: Grading of corneal and conjunctival staining in context of other dry eye tests. Cornea, 22(7); 2003 : 640–650.
6. Cheng, JW., Xi, GL., Wei, RL. et al.: Effects of travoprost in the treatment of open-angle glaucoma or ocular hypertension: a systematic review and meta-analysis. Curr Ther Res Clin Exp, 70(4); 2009 : 335–350.
7. Crichton, ACS., Vold, S., Williams, JM. et al.: Ocular surface tolerability of prostaglandin analogs and prostamides in patients with glaucoma or ocular hypertension. Adv Ther, 30(3); 2013 : 260–270.
8. Cvenkel, B., Štunf, Š., Kirbiš, IS. et al.: Symptoms and signs of ocular surface disease related to topical medication in patients with glaucoma. Clin Ophthalmol, 9; 2015 : 625–631.
9. Databáze léků (online). Praha: Státní ústav pro kontrolu léčiv, 2015 (cit. 2016-06-03). Dostupný z WWW: <http://www.sukl.cz/modules/medication/search.php>.
10. Efron, N.: Grading scales for contact lens complications. In Efron, N. (Ed), Contact lens complications, 3. ed. Edinburgh-Toronto, Elsevier/Saunders, 2012, p. 301-306.
11. European glaucoma society: Terminology and guidelines for glaucoma, 4. ed, Savona, PubliComm, 2014, 195 p.
12. Eyawo, O., Nachega, J., Lefebvre, P. et al.: Efficacy and safety of prostaglandin analogues in patients with predominantly primary open-angle glaucoma or ocular hypertension: a meta-analysis. Clin Ophthalmol, 3; 2009 : 447–456.
13. Fechtner, RD., Godfrey, DG., Budenz, D. et al: Prevalence of ocular surface complaints in patients with glaucoma using topical intraocular pressure-lowering medications. Cornea, 29(6); 2010 : 618–621.
14. Garcia-Feijoo, J., Sampaolesi, JR.: A multicenter evaluation of ocular surface disease prevalence in patients with glaucoma. Clin Ophthalmol, 6; 2012 : 441–446.
15. Hommer, A., Kimmich, F.: Switching patients from preserved prostaglandin-analog monotherapy to preservative-free tafluprost. Clin Ophthalmol, 5; 2011 : 623–631.
16. Honrubia, F., García-Sánchez, J., Polo, V. et al.: Conjunctival hyperemia with use of latanoprost versus other prostaglandin analogues in patients with ocular hypertension or glaucoma: a meta-analysis of randomised clinical trials. Br J Ophthalmol, 93(3); 2009 : 316–321.
17. Karhanová, M., Mlčák, P., Fryšák, Z. et al.: Účinnost a snášenlivost tafluprostu 0,0015% bez konzervačních látek v léčbě glaukomu a oční hypertenze. Čes a Slov Oftal, 68(4); 2012 : 150–155.
18. Labbé, A., Pauly, A., Liang, H. et al.: Comparison of toxicological profiles of benzalkonium chloride and polyquaternium-1: an experimental study. J Ocul Pharmacol Ther, 22(4); 2006 : 267–278.
19. Labbé, A., Terry, O., Brasnu, E. et al.: Tear film osmolarity in patients treated for glaucoma or ocular hypertension. Cornea, 31(9); 2012 : 994–999.
20. Leung, EW., Medeiros, FA., Weinreb, RN.: Prevalence of ocular surface disease in glaucoma patients. J Glaucoma, 17(5); 2008 : 350–355.
21. Liehneová, I.: Farmakoterapie glaukomu. Čes a Slov Oftal, 66(4); 2010 : 155–158.
22. Martone, G., Frezzotti, P., Tosi, GM. et al: An in vivo confocal microscopy analysis of effects of topical antiglaucoma therapy with preservative on corneal innervation and morphology. Am J Ophthalmol, 147; 2009 : 725–35.
23. Mathews, PM., Ramulu, PY., Friedman, DS. et al.: Evaluation of ocular surface disease in patients with glaucoma. Ophthalmology, 120(11); 2013 : 2241–2248.
24. Mlčák, P., Karhanová, M., Marešová, K.: Konzervativní léčba glaukomu. Prakt lékáren, 5(1); 2009 : 22–25.
25. Ocular surface disease index© (OSDI©) (online). Irvine, CA: Allergan, Inc., c2004 (cit. 2014-07-13). Dostupný z WWW: <http://www.thecenterforeyecareandoptical.com/UserFiles/OSDI_questionnare.pdf>.
26. Paimela, T., Ryhänen, T., Kauppinen, A. et al.: The preservative polyquaternium-1 increases cytoxicity and NF-kappaB linked inflammation in human corneal epithelial cells. Mol Vis, 18; 2012 : 1189–1196.
27. Pflugfelder, SC., Baudouin, C.: Challenges in the clinical measurement of ocular surface disease in glaucoma patients. Clin Ophthalmol, 5; 2011 : 1575–1583.
28. Pisella, PJ., Pouliquen, P., Baudouin, C.: Prevalence of ocular symptoms and signs with preserved and preservative free glaucoma medication. Br J Ophthalmol, 86; 2002 : 418–423.
29. Rolando, M., Crider, JY., Kahook, MY.: Ophthalmic preservatives: focus on polyquaternium-1. Expert Opin Drug Deliv, 8(11); 2011 : 1425–1438.
30. Rossi, GCM., Pasinetti, GM., Scudeller, L. et al.: Ocular surface disease and glaucoma: how to evaluate impact on quality of life. J Ocul Pharmacol Ther, 29(4); 2013 : 390–394.
31. Rossi, GCM., Pasinetti, GM., Scudeller, L. et al.: Risk factors to develop ocular surface disease in treated glaucoma or ocular hypertension patients. Eur J Ophthalmol, 23(3); 2013 : 296–302.
32. Rossi, GCM., Tinelli, C., Pasinetti, GM. et al.: Dry eye syndrome – related quality of life in glaucoma patients. Eur J Ophthalmol, 19(4); 2009 : 572–579.
33. Rouland, JF., Traverso, CE., Stalmans, I. et al.: Efficacy and safety of preservative-free latanoprost eyedrops, compared with BAK-preserved latanoprost in patients with ocular hypertension or glaucoma. Br J Ophthalmol, 97; 2013 : 196–200.
34. Růžičková, E.: Farmakoterapie glaukomu. In Rozsíval, P. (Ed), Trendy soudobé oftalmologie, sv. 4. Praha, Galén, 2007, s. 151–174.
35. Růžičková, E.: Glaukom, Praha, Maxdorf, 2006, 95 s.
36. Saade, CE., Lari, HB., Berezina, TL. et al.: Topical glaucoma therapy and ocular surface disease: a prospective, controlled cohort study. Can J Ophthalmol, 50(2); 2015 : 132–136.
37. Šebesta, P.: Konzervativní terapie glaukomu. In Rozsíval, P. (Ed), Glaukom – vybrané kapitoly. Hradec Králové, Nucleus HK, 2008, s. 133–156.
38. Toris, CB., Gabelt, BT., Kaufman, PL.: Update on the mechanism of action of topical prostaglandins for intraocular pressure reduction. Surv Ophthalmol, 53(Suppl 1); 2008: S107–S120.
39. Uusitalo, H., Chen, E., Pfeiffer, N. et al.: Switching from a preserved to a preservative-free prostaglandin preparation in topical glaucoma medication. Acta Ophthalmol, 88; 2010 : 329–336.
40. Výborný, P., Fučík, M., Rozsíval, P.: Glaukom. In Kuchynka, P. (Ed), Oční lékařství. Praha, Grada, 2007, s. 555–607.
41. Výborný, P., Sičáková, S.: Denní dávka benzalkonium chloridu – významné kritérium v léčbě glaukomu. Čes a Slov Oftal, 67(2); 2011 : 63–66.
42. Výborný, P., Sičáková, S., Veselá Flórová, Z.: Konzervační činidla – denní dávka benzalkonium chloridu v léčbě glaukomu z pohledu pacienta. Čes a Slov Oftal, 70(3); 2014 : 95–97.
43. Zimmerman, TJ., Hahn, SR., Gelb, L. et al.: The impact of ocular adverse effects in patients treated with topical prostaglandin analogs: changes in prescription patterns and patient persistence. J Ocul Pharmacol Ther, 25(2); 2009 : 145–152.
Labels
Ophthalmology
Article was published inCzech and Slovak Ophthalmology

2016 Issue 4-
All articles in this issue
- Nová diagnostická zobrazovací metoda – shear waves elastografie
- Historický přehled technik zadní lamelární keratoplastiky
- Hodnocení očního povrchu u pacientů léčených analogy prostaglandinů s ohledem na obsaženou konzervační látku
- Genová terapie dědičných onemocnění SÍTNICE A ZRAKOVÉHO NERVU: současný stav poznání
- HEMANGIOMY ORBITÁLNÍ KRAJINY U DĚTÍ
- MUTÁCIA BRAF A MOŽNOSTI IDENTIFIKÁCIE PROGNOSTICKÝCH MARKEROV METASTÁZOVANIA UVEÁLNEHO MELANÓMU
- Porucha motility bulbu s diplopií jako první příznak tumoru prorůstajícího do orbity z vedlejších dutin nosních
- Czech and Slovak Ophthalmology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Genová terapie dědičných onemocnění SÍTNICE A ZRAKOVÉHO NERVU: současný stav poznání
- Nová diagnostická zobrazovací metoda – shear waves elastografie
- HEMANGIOMY ORBITÁLNÍ KRAJINY U DĚTÍ
- MUTÁCIA BRAF A MOŽNOSTI IDENTIFIKÁCIE PROGNOSTICKÝCH MARKEROV METASTÁZOVANIA UVEÁLNEHO MELANÓMU
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career




