-
Medical journals
- Career
Cytomegalovirová retinitida u HIV negativních pacientů – retrospektivní studie
Authors: A. Beňová; M. Brichová; P. Svozílková; B. Kousal; D. Jeníčková; prof. MUDr. Jarmila Heissigerová, Ph.D., MBA; E. Říhová
Authors‘ workplace: Oční klinika, 1. lékařská fakulta, Univerzity Karlovy nemocnice v Praze a Všeobecná fakultní nemocnice, Praha, přednostka doc. MUDr. Bohdana Kalvodová, CSc.
Published in: Čes. a slov. Oftal., 69, 2013, No. 6, p. 227-234
Category: Original Article
Práce byla prezentována na XXI. výročním sjezdu České oftalmologické společnosti Brně v roce 2013
Overview
Cíl:
Zhodnotit vlastní zkušenosti s diagnostikou a léčbou cytomegalovirové (CMV) retinitidy u imunodeficitních HIV negativních pacientů.Metodika:
Retrospektivní studie a kazuistická sdělení.Výsledky:
V Centru pro diagnostiku a léčbu uveitid 1. LF UK a VFN v Praze jsme v období od června 2003 do června 2012 vyšetřili celkem 1869 pacientů s uveitidou. CMV retinitidu jsme diagnostikovali na základě charakteristického klinického obrazu a anamnézy imunodeficitu u 7 pacientů (1 žena a 6 mužů). U 2 atypických nálezů byla diagnóza potvrzena až detekcí DNA patogenu ve vzorku sklivce (pacientka s non-Hodgkinovým lymfomem) nebo pozitivní sérologií s vyšetřením CMV v leukocytech (indolentní forma CMV retinitidy u pacientky se systémovým lupus erythematodes). V 8 případech se jednalo o fulminantní formu, u 1 pacientky o indolentní formu CMV retinitidy. Průměrný věk pacientů byl 39,1 let (18 až 51 let), poměr mužů k ženám 6 : 3. V 6 z 9 případů jsme zachytili oboustranný nález. Průměrná doba sledování v souboru byla 15,8 měsíců (1 až 48 měsíců). U 5 pacientů došlo k rozvoji CMV retinitidy po transplantaci kostní dřeně. Ve 2 případech byla CMV retinitida komplikací imunodeficitu při terapii systémového onemocnění (ulcerózní kolitida, systémový lupus erythematodes) a 2 pacienti byli léčeni pro lymfom. Zahájení či úpravu terapie (gancyklovir p.o./i.v., foskarnet i.v.) jsme konzultovali a koordinovali se specialisty daných oborů. Po nasazení terapie jsme sledovali celkem 7 nemocných. U 4 očí 3 pacientů (31 %) jsme zaznamenali zlepšení centrální zrakové ostrosti (CZO), u 5 očí 5 pacientů (38 %) její stabilizaci. Zhoršení CZO u 4 očí 3 pacientů (31 %) bylo způsobeno komplikacemi, které nesouvisely s virostatickou léčbou. Všichni sledovaní pacienti, kteří prodělali transplantaci kostní dřeně, zemřeli do 12 měsíců od stanovení diagnózy CMV retinitidy.Závěr:
Záchyt CMV retinitidy pouze u 9 pacientů, tj. 0,48 % všech uveálních pacientů, potvrzuje její vzácný výskyt. Pro diagnózu CMV retinitidy je anamnéza imunodeficitu klíčová. U atypických nálezů je možno v diagnostice využít analýzy nitroočních tekutin či sérologie. Výskyt CMV retinitidy představuje pro pacienty po transplantaci kostní dřeně velmi nepříznivý prognostický faktor a v našem souboru zemřeli všichni tito pacienti do 12 měsíců od stanovení diagnózy CMV retinitidy. Léčba vyžaduje úzkou mezioborovou spolupráci.Klíčová slova:
cytomegalovirus, cytomegalovirová retinitida, gancyklovir, foskarnet, cidofovir, imunodeficitÚVOD
Cytomegalovirová (CMV) retinitida je vzácné, ale závažné virové onemocnění sítnice s typickým obrazem na fundu postiženého oka. Vyskytuje se především u jedinců s imunodeficitem. Nejčastěji jsou to pacienti s manifestním syndromem získané imunodeficience (Acquired Immune Deficiency Syndrome – AIDS), s leukémií, lymfomem, pacienti po orgánových transplantacích, po chemoterapii nebo s celkovou imunosupresivní terapií z různých příčin (1, 2, 3, 4, 8, 11, 12, 14, 16, 17, 18, 21). Poprvé ji popsala H. C. W. Foerster v USA v roce 1959 (7). Do roku 1970 bylo v západních zemích popsáno pouze několik případů CMV retinitidy. V roce 1971 se ji podařilo poprvé prokázat i histologicky. V 70.–80. letech, kdy došlo k nárůstu osob infikovaných virem HIV a rozšířily se možnosti a indikace imunosuprese a chemoterapie, incidence CMV retinitidy výrazně stoupla. Před zavedením vysoce aktivní antiretrovirové terapie (highly active antiretroviral therapy – HAART) v roce 1996 se CMV retinitida vyskytovala u 25–40 % pacientů s AIDS (6, 11, 12, 13) a byla nejčastější oportunní infekcí u těchto nemocných (18). HAART snížila incidenci CMV retinitidy o 55–80 % (1). Nadále však zůstává hlavní příčinou ztráty nebo zhoršení vidění u HIV pozitivních. Incidence CMV retinitidy stoupá u pacientů po orgánových transplantacích (stoupá i počet transplantovaných pacientů) (21). Je vzácná u imunokompetentních jedinců a byla vzácně popsána i u jedinců po intravitreální aplikaci kortikoidů. U imunosuprimovaných pacientů je onemocněním s velmi nepříznivou prognózou (3, 18). Incidence CMV retinitidy je stejná u mužů i žen. Prevalence je ale vyšší u mužů z důvodu vyšší prevalence AIDS (1, 12). K rozvoji CMV retinitidy dochází nejčastěji mezi 20.–50. rokem života (1). Symptomy CMV retinitidy závisí na lokalizaci postižení sítnice. Nejčastěji jsou to plovoucí mušky, pokles vidění různého stupně, výpady v zorném poli (1, 4, 8, 12, 14, 18). Při výskytu drobných nebo periferních lézí může být pacient zcela bez potíží (18). Postižené oko bývá bledé, klidné a nebolestivé.
CMV retinitida je vzácná nekrotizující virová retinitida. Virus způsobuje nekrózu sítnice v celé její tloušťce (3, 18). Onemocnění má typický klinický obraz a je provázeno jen mírnou vitritidou. Retinitida obvykle začíná kolem cév ve střední periferii a rychle se šíří na zadní pól a dále do periferie splýváním stávajících ložisek s novotvořenými (šíří se jako „stepní požár“). Na fundu postiženého oka nacházíme vícečetná dobře ohraničená bělavá ložiska retinální infiltrace a nekrózy geografického tvaru, s různým množstvím krvácení (obraz „kečupu a sýra“, též „pizza-pie“) (18). Mohou být přítomny široké perivaskulární infiltráty, někdy až typu „omrzlých větví“. Velmi vzácně byla popsána i neuritida optického nervu (1, 4, 12, 14, 17, 18). CMV retinitida se vyskytuje ve 2 formách – indolentní (periferní léze granulárního vzhledu, ojedinělé retinální hemoragie; pomalá progrese) (obr. 1) a závažnější fulminantní formě (četné retinální hemoragie a bělavá ložiska retinální nekrózy; rychlá progrese) (obr. 2). Obě tyto formy prezentují „dva konce“ na sebe navazujícího klinického obrazu (1, 12). Zánět bývá bilaterální, stranově asymetrický (3, 18). Ložiska CMV retinitidy se často nejdříve objeví kolem cév na zadním pólu, což je pravděpodobně způsobeno jak hematogenním šířením, tak vasotropní povahou viru (3). Ložiska v periferii jsou zřídka doprovázena krvácením, naopak u ložisek centrálních jsou rozsáhlé hemoragie časté. Aktivní okraj ložiska, kde dochází nadále k replikaci viru, má granulární vzhled (14, 18). Regrese nálezu na fundu při adekvátní léčbě CMV retinitidy je charakterizována resorpcí retinálních hemoragií a jizvením (atrofizací) sítnice s hrubými přesuny pigmentu (12).
Image 1. Indolentní forma CMV retinitidy. Fotografie fundu zachycuje periferní léze granulárního vzhledu s ojedinělými hemoragiemi u 59letého pacienta s lymfomem po transplantaci kostní dřeně, s fulminantní CMV retinitidou a poruchou vizu OL, bez poruchy vizu na OP a, b) 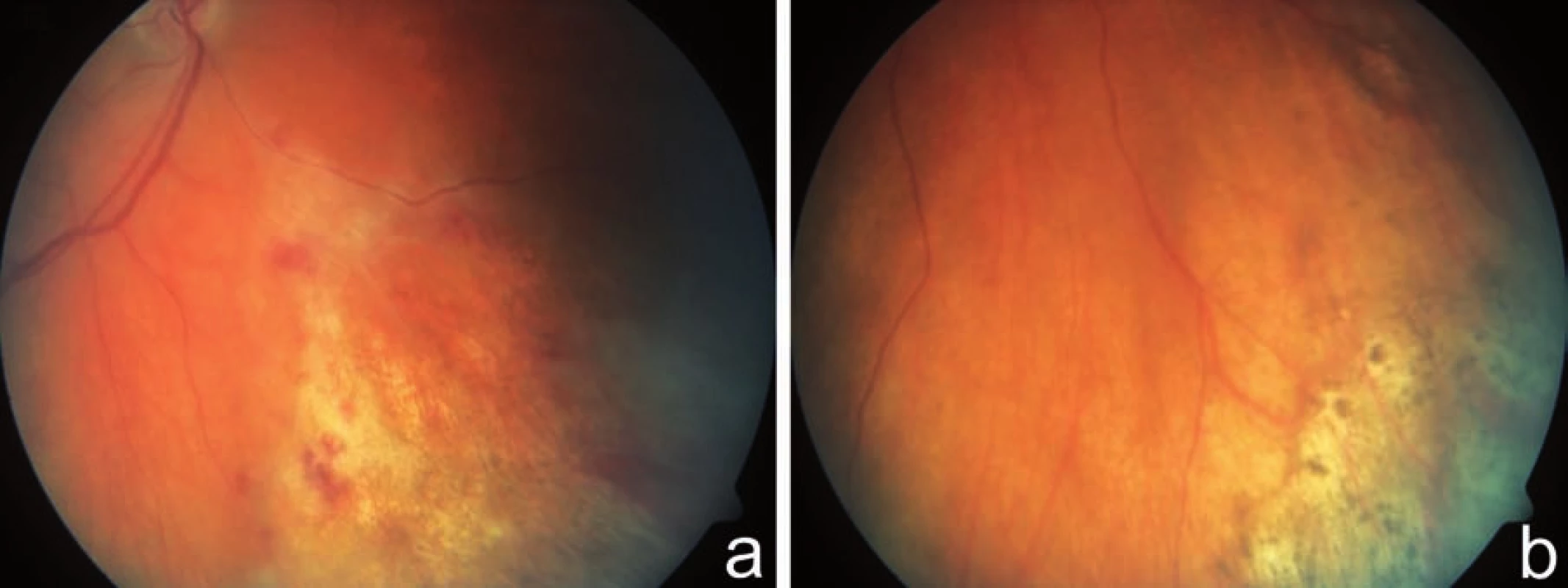
Image 2. Fulminantní forma CMV retinitidy. Fotografie fundu dokumentuje nález bělavých ložisek retinální infiltrace a nekrózy s krvácením (obraz „kečupu a sýra“) u 59letého pacienta po transplantaci kostní dřeně pro lymfom a), u 32letého pacienta po alogenní transplantaci kmenových krvetvorných buněk pro akutní myeloidní leukémii b), u 51letého pacienta s non-Hodgkinovym lymfomem c), u 32letého pacienta po alogenní transplantaci kmenových krvetvorných buněk pro akutní myeloidní leukémii d), u 31letého pacienta po 2 transplantacích kostní dřeně pro akutní myeloidní leukémii e) 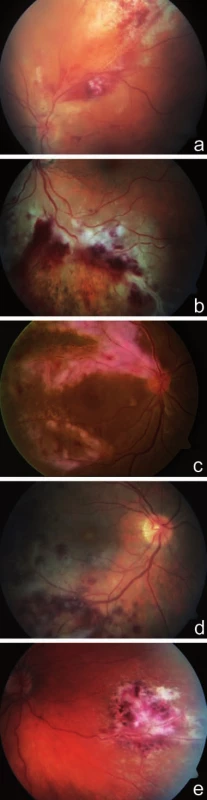
CMV retinitida je relativně pomalu progredující onemocnění, vyžadující týdny až měsíce k postižení celé sítnice (1). Pokles vidění je způsoben buď přímo nekrotizující retinitidou v oblasti zadního pólu oka nebo sekundárním odchlípením sítnice na podkladě trhlin na rozhraní normální a patologicky změněné (nekrotické nebo již atrofické) sítnice (20). Rhegmatogenní amoce je nejčastější komplikací CMV retinitidy (1, 4, 6, 12, 13, 14, 16, 18). Neléčená CMV retinitida vede k progresivní ztrátě vidění až slepotě. U HIV pozitivních pacientů byla CMV retinitida popisována jako „end-stage disease“, která předpovídala dobu přežití pacienta na přibližně 6 týdnů (1, 9). Se zavedením HAART se průměrná doba přežití po stanovení diagnózy CMV retinitidy u HIV pozitivních zvýšila na 6–8 měsíců (9).
Diagnózu CMV retinitidy stanovíme na základě typického klinického obrazu (nálezu na fundu postiženého oka – obraz „kečupu a sýra“) a anamnézy imunodeficitu (18). K potvrzení diagnózy zejména v nejasných případech může pomoci přímá detekce virové DNA pomocí polymerázové řetězové reakce (PCR) a dále sérologie (specifické protilátky IgG, IgA, IgM), stanovení Pp65 antigenu v krvi a detekce viru v moči (1, 22). CMV retinitidu diagnostikuje oftalmolog, ale léčbu vede ošetřující lékař (hematolog, revmatolog) ve spolupráci s oftalmologem.
Cytomegalovirová retinitida obecně špatně reaguje na léčbu (18). Přímým účinkem antivirotik je inhibice DNA polymerázy cytomegaloviru, a tím zabránění jeho další replikace (14). Léčba CMV retinitidy je konzervativní a chirurgická (PPV, endolaser, tamponáda silikonovým olejem v případě odchlípení sítnice (1, 18) nebo intravitreální implantát (Vitrasert, gancyklovir 4,5 mg, Bausch&Lomb, 1996) implantovatelný cestou pars plana obvykle do dolního temporálního kvadrantu). Ke konzervativní léčbě (1, 12, 18) patří systémově podávaná virostatika – gancyklovir i.v. (preparát Cymevene, v ČR dostupný), valgancyklovir p.o. (preparát Valcyte, v ČR dostupný), foskarnet i.v. (preparát Foscavir, v ČR dostupný – mimořádný dovoz), cidofovir i.v. (preparát Vistide, v ČR dostupný – mimořádný dovoz). K nežádoucím účinkům léčby patří výrazná orgánová toxicita (myelosuprese s neutropenií, trombocytopenií – gancyklovir, valgancyklovir; nefrotoxicita – foskarnet, cidofovir). Z toho plyne i limitace této léčby (18). Dalším úskalím léčby je její finanční náročnost, omezená preskripce a nutnost mezioborové spolupráce. Další možností léčby CMV retinitidy je intravitreální aplikace (IVT) antivirotik (1, 14, 18). Lokální léčba ale postrádá protektivní vliv na druhé oko (3). IVT lze aplikovat následující léky (léčba off label): gancyklovir, foskarnet, cidofovir. K léčbě řadíme také laserovou fotokoagulaci, kterou může být ošetřeno malé odchlípení sítnice v periferii. Profylaktické laserové ošetření sítnice druhého oka s CMV retinitidou většinou ale není prevencí možného odchlípení sítnice (1, 6, 18).
Nejčastější komplikací CMV retinitidy je rhegmatogenní odchlípení sítnice (ARR) – výskyt až u 50 % pacientů v průběhu prvního roku od stanovení diagnózy (18). Vzniká sekundárně na podkladě trhlin na rozhraní normální a nekrotické nebo již atrofické sítnice (20). Riziko vzniku ARR stoupá s délkou trvání CMV infekce a s výskytem velkých periferně uložených lézí (3, 18). Možný je vznik cystoidního makulárního edému (CME), epiretinální membrány (ERM) či hemoftalmu. Dále ke komplikacím řadíme vedlejší účinky systémové léčby (selhání ledvin, leukopénie v důsledku myelosuprese) a vznik rezistence na virostatika (1, 18).
METODIKA
Náš soubor tvořilo 9 pacientů (3 ženy a 6 mužů). Všichni pacienti byli HIV negativní. Pacientům jsme podrobně odebrali celkovou i oční anamnézu. V celkové anamnéze, která je u diagnózy CMV retinitidy klíčová, jsme pátrali po imunodeficitu. CZO jsme vyšetřovali na Snellenových optotypech. Přední i zadní segment jsme vyšetřovali na štěrbinové lampě, fotodokumentaci prováděli pomocí funduskamery (FF450 plus IR Fundus Camera, Carl Zeiss Meditec AG, Německo). Z pomocných vyšetření jsme využili perimetr (M-700, Medmont International Pty Ltd., Austrálie), optickou koherenční tomografii se spektrální doménou (SD-OCT, Spectral OCT/SLO, OTI Ophthalmic Technologies, Inc., Kanada) a ultrazvuk (USG, Ultrascan Imaging System, Alcon, USA). Nitrooční tlak jsme měřili aplanačně. Celková léčba základních onemocnění pacientů byla vedena specialistou daného oboru (hematologem/revmatologem). V souboru jsme sledovali věk při stanovení diagnózy, pohlaví a základní onemocnění pacientů, postižení oka/očí, zrakovou ostrost při stanovení diagnózy a při ukončení sledování, délku sledování, léčbu a případné komplikace.
VÝSLEDKY
V našem souboru 9 pacientů (15 očí) bylo celkem 6 mužů (67 %) a 3 ženy (33 %). Průměrný věk pacientů v začátku sledování byl 39,1 let (18–51 let). Nejvyšší incidence výskytu CMV retinitidy v našem souboru byla ve věku 41–50 let; celkem 4 pacienti (45 %). Více byli postiženi muži (67 %) než ženy. Postiženo bylo celkem 15 očí (9 pacientů). Z toho u 6 pacientů (67 %) byl nález oboustranný, u 3 pacientů (33 %) se jednalo o jednostranné postižení.
Table 1. Vlastní soubor pacientů 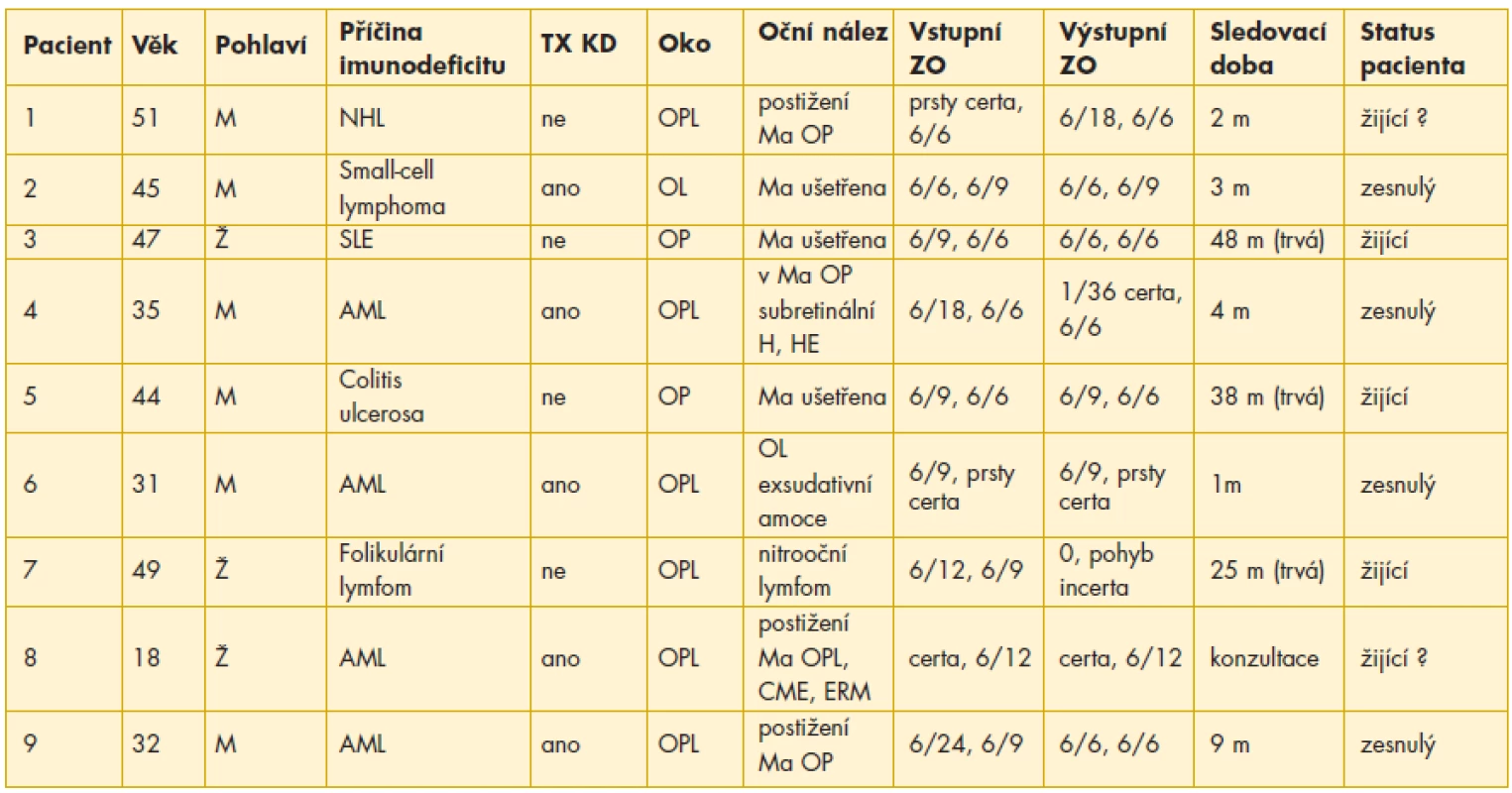
M – muž, Ž – žena, SLE – systémový lupus erythematodes, NHL – non-Hodgkinův lymfom, AML – akutní myeloidní leukémie, TX KD – transplantace kostní dřeně, Ma – makula,H – hemoragie, HE – hemoftalmus, CME – cystoidní makulární edém, ERM – epiretinální membrána, m – měsíce V souboru bylo 5 pacientů (9 očí; 56 %) po transplantaci kostní dřeně (výskyt CMV retinitidy za 5–12 měsíců po transplantaci pro hematologickou malignitu; z toho 80 % tvořili pacienti s akutní myeloidní leukémií – AML), dva pacienti (4 oči; 22 %) s hematologickou malignitou (non–Hodgkinův lymfom – NHL, folikulární lymfom), jeden pacient (1 oko; 11 %) s ulcerózní kolitidou a jeden pacient (1 oko; 11 %) se systémovým lupus erythematodes (SLE), oba s celkovou imunosupresivní léčbou (graf 1).
Graph 1. Základní onemocnění pacientů a příčina imunodeficitu 
Pět pacientů z našeho souboru (56 %) si stěžovalo na poruchu v zorném poli postiženého oka (výpad v zorném poli) a čtyři pacienti (44 %) na nespecifické zhoršení vidění (zamlžení, pokles vidění, plovoucí mušky před okem). U 7 z 15 očí (47 %) byla makula postiženého oka ušetřena, u 8 očí (53 %) jsme zaznamenali postižení makuly (vlastní zánětlivá infiltrace, cystoidní makulární edém, epiretinální membrána, subretinální hemoragie, exsudativní amoce).
Úroveň CZO jsme hodnotili u 8 z 9 pacientů (celkem 13 z 15 očí). Pacientku s oboustranným postižením, kterou jsme pouze konzultovali, jsme v tomto případě nehodnotili. U stanovení diagnózy CMV retinitidy byla nejlepší vstupní CZO 6/6 a nejhorší prsty s jistou světelnou projekcí. Nejlepší výsledná CZO byla 6/6, nejhorší 0 (graf 2). Nejnižší výstupní CZO (amauróza) byla u pacientky s NHL, u které byla diagnóza CMV retinitidy potvrzena až zachycením DNA patogenu ve vzorku sklivce. Druhá nejhorší výstupní CZO (1/36, správná světelná projekce) byla u pacienta, u kterého se stav po zklidnění zánětu zkomplikoval hemoftalmem. U 4 očí 3 pacientů (31 %) jsme po nasazení adekvátní terapie pozorovali zlepšení CZO, u 5 očí 5 pacientů (38 %) její stabilizaci. U 4 očí 3 pacientů (31 %) jsme zaznamenali zhoršení CZO (2 oči u pacientky s NHL, 2 oči dvou pacientů s komplikacemi – hemoftalmus a exsudativní amoce) (graf 3).
Graph 2. Vstupní a výstupní zraková ostrost 
Graph 3. Úroveň zrakové ostrosti při ukončení sledování 
Nasazení či úpravu terapie virostatiky u pacientů v našem souboru jsme koordinovali s ošetřujícími lékaři (hematology resp. revmatology). U 4 pacientů byla před rozvojem CMV retinitidy diagnostikována a léčena systémová CMV infekce – ve 3 případech v časném posttransplantačním období a u 1 pacienta po chemoterapii pro lymfom. U 2 našich pacientů byl k terapii použit gancyklovir i.v. (Cymevene), v 1 případě foskarnet i.v. (Foscavir). U 2 nemocných s předcházející systémovou CMV infekcí byla s rozvojem retinitidy reindukována i.v. léčba gancyklovirem a v 1 případě byl gancyklovir nahrazen foskarnetem. Jeden pacient byl léčen gancyklovirem p.o. (Valcyte). Pacientka s indolentní formou byla jen sledována. Jedna pacientka (2 oči) při zhoršení nálezu i vizu odmítla navrhovanou změnu terapie.
U žádného pacienta z našeho souboru se nevyskytla nejčastěji popisována komplikace CMV retinitidy – sekundární rhegmatogenní amoce sítnice. U 1 pacienta (1 oko z 13 očí; 8 %) jsme popsali exsudativní amoci a u 1 pacienta (1 oko; 8 %) se nález po zklidnění zánětu zkomplikoval hemoftalmem. Jiné oční komplikace jsme v našem souboru nezaznamenali.
Průměrná doba sledování našeho souboru byla 15,8 měsíců. Maximální doba sledování 48 měsíců, minimální 1 měsíc. V jednom případě se jednalo o jednorázové konziliární vyšetření. Po nasazení terapie jsme sledovali 6 nemocných. U 4 očí 3 pacientů bylo léčbou dosaženo zklidnění nálezu a zlepšení vizu, u 5 očí 5 pacientů se nález zklidnil a vizus stabilizoval. Čtyři pacienti z našeho souboru (45 %, všichni po transplantaci kostní dřeně) zemřeli za 1, 4, 5 a 9 měsíců po stanovení diagnózy CMV retinitidy pro komplikace, které nesouvisely s terapií virostatiky.
Kazuistika č. 1
U 45letého muže s diagnózou NHL z malých buněk se CMV retinitida levého oka objevila 12 měsíců po alogenní transplantaci kostní dřeně. Pacient byl odeslán ke konziliárnímu vyšetření na naše pracoviště pro plovoucí mušky a rušivý stín nahoře v periferii zorného pole levého oka. Diagnóza byla stanovena dle typického nálezu na fundu s přihlédnutím k anamnéze imunodeficitu. Sklivec postiženého oka byl jen minimálně zkalen, na fundu jsme v povodí dolních arkád popsali bělavá nekrotická ložiska promíchaná s plošnými hemoragiemi a „omrzlé cévy“. Dolní okraj ložiska granulárního vzhledu odpovídal místu, kde nadále docházelo k replikaci viru (obr. 3a). CZO pravého oka byla 6/6, CZO levého oka 6/9. Při léčbě gancyklovirem i.v. (Cymevene) došlo ke stabilizaci CZO a regresi nálezu na fundu levého oka (obr. 3b). Pacient zemřel po 3 měsících po stanovení diagnózy CMV retinitidy.
Image 3. Klinický nález u pacienta z kazuistiky 1. Obraz fulminantní formy CMV retinitidy typu „kečup a sýr“ a perivaskulární infiltráty typu „omrzlých větví“ u 32letého pacienta po alogenní transplantaci kmenových krvetvorných buněk pro akutní myeloidní leukémii a), regrese nálezu na fundu postiženého oka po 8 týdnech terapie gancyklovir i.v. (Cymevene) s resorpcí retinálních hemoragií a jizvením (atrofizací) sítnice s hrubými přesuny pigmentu b) 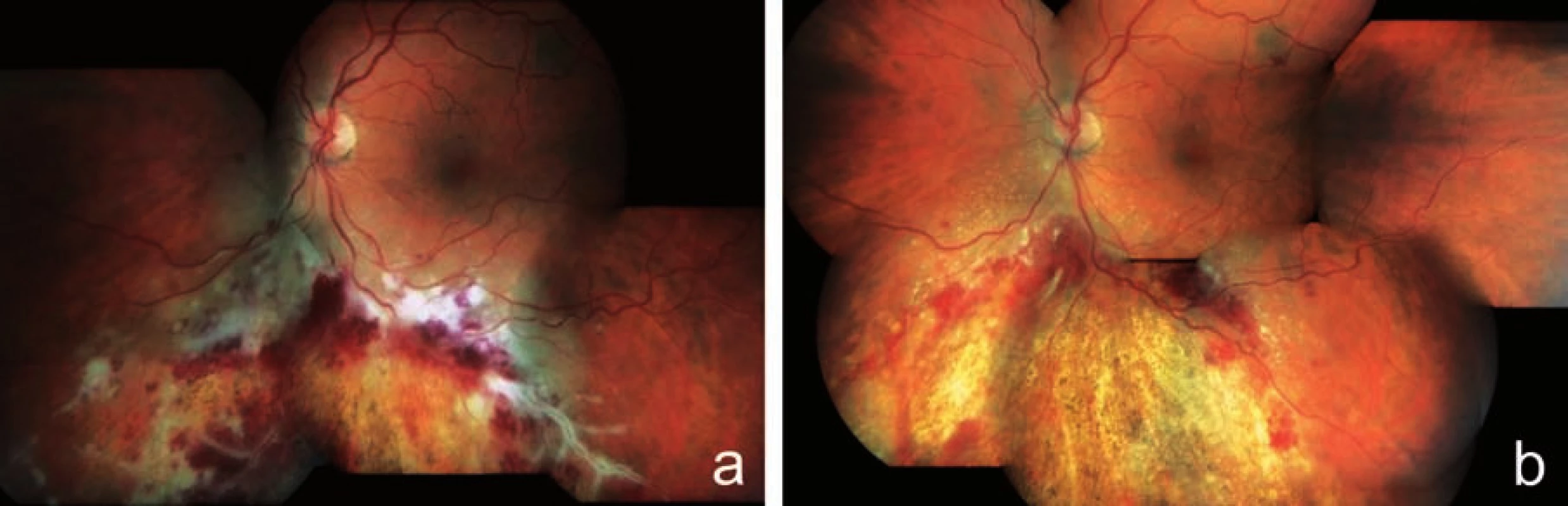
Kazuistika č. 2
44letý pacient s ulcerózní kolitidou na celkové imunosupresi (t.č. Medrol, dříve kombinace Cyklofosfamid + Prednison, léčen od r. 1993) byl k nám odeslán pro 3 týdny trvající zhoršené vidění pravého oka a stín v dolní části zorného pole. Oční potíže byly vázány na vysazení cyklofosfamidu. CZO pravého oka byla 6/9, CZO levého oka 6/6. Sklivec pravého oka byl čirý, na fundu v temporálním horním kvadrantu jsme nalezli rozsáhlé bělavé ložisko s četnými retinálními hemoragiemi, v okolí ložiska cévy s doprovodnými proužky (obr. 4a). Statická počítačová perimetrie zaznamenala výpad v zorném poli dole pod centrem (obr. 4c). U pacienta jsme dle klinického obrazu diagnostikovali CMV retinitidu, nedávno proběhlá CMV infekce byla potvrzena i sérologicky. Při léčbě gancyklovirem i.v. (Cymevene) po dobu 5 týdnů došlo ke stabilizaci CZO a zklidnění nálezu na fundu postiženého oka (obr. 4b). Pacienta nadále sledujeme.
Image 4. Klinický nález u pacienta z kazuistiky 2. Fotografie dokumentuje bělavá již resorbující se ložiska infiltrace a hemoragie s atrofizací sítnice v horním nazálním kvadrantu pravého oka u pacienta na celkové imunosupresi (Medrol + Cyklofosfamid) pro ulcerózní kolitidu a), klidná jizva pro proběhlé CMV retinitidě b), statická automatická perimetrie pravého oka s odpovídajícím výpadem v zorném poli c) 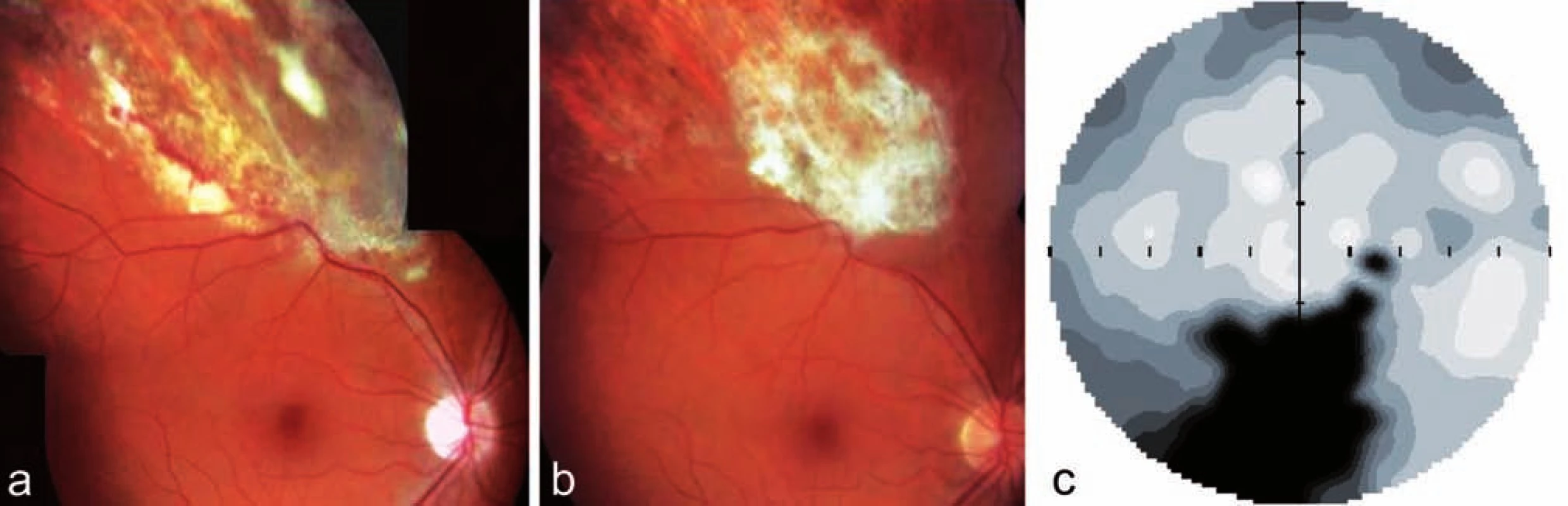
Kazuistika č. 3
U 31letého muže s diagnózou akutní myeloidní leukémie se oboustranná CMV retinitida rozvinula 6 měsíců po transplantaci kostní dřeně. Pacient již byl léčen gancyklovirem i.v. (Cymevene) pro systémovou CMV infekci, která se rozvinula v časném posttransplantačném období. Pacient si stěžoval na náhle vzniklou poruchu vidění levého oka s výpadem temporální poloviny zorného pole. CZO pravého oka byla 6/9, CZO levého oka prsty před okem, správná světelná projekce. Sklivec pravého oka byl čirý, na fundu nazálně od papily a temporálně dole jsme popsali ohraničené oválné bělavé ložisko s centrálními hemoragiemi (obr. 5a, b, c). Fundus levého oka bylo možné jen velmi obtížně diferencovat pro výrazné zastření sklivce. Ultrazvukové vyšetření levého oka potvrdilo exsudativní amoci v dolní polovině. Nález jsme uzavřeli jako bilaterální CMV retinitidu a doporučili pokračovat v terapii gancyklovirem i.v. Pacient zemřel krátce po stanovení diagnózy CMV retinitidy (cca 6 měsíců po transplantaci kostní dřeně).
Image 5. Klinický nález u pacienta z kazuistiky 3. Na fotografii fundu pravého oka u 31letého pacienta po 2 transplantacích kostní dřeně pro akutní myeloidní leukémii je patrné ohraničené bělavé ložisko infiltrované sítnice s hemoragiemi, v bezprostředním okolí ložiska nahoře malá exsudativní amoce sítnice a, b), vertikální scan SD-OCT ložiskem CMV retinitidy dokumentuje destrukci všech vrstev sítnice c) 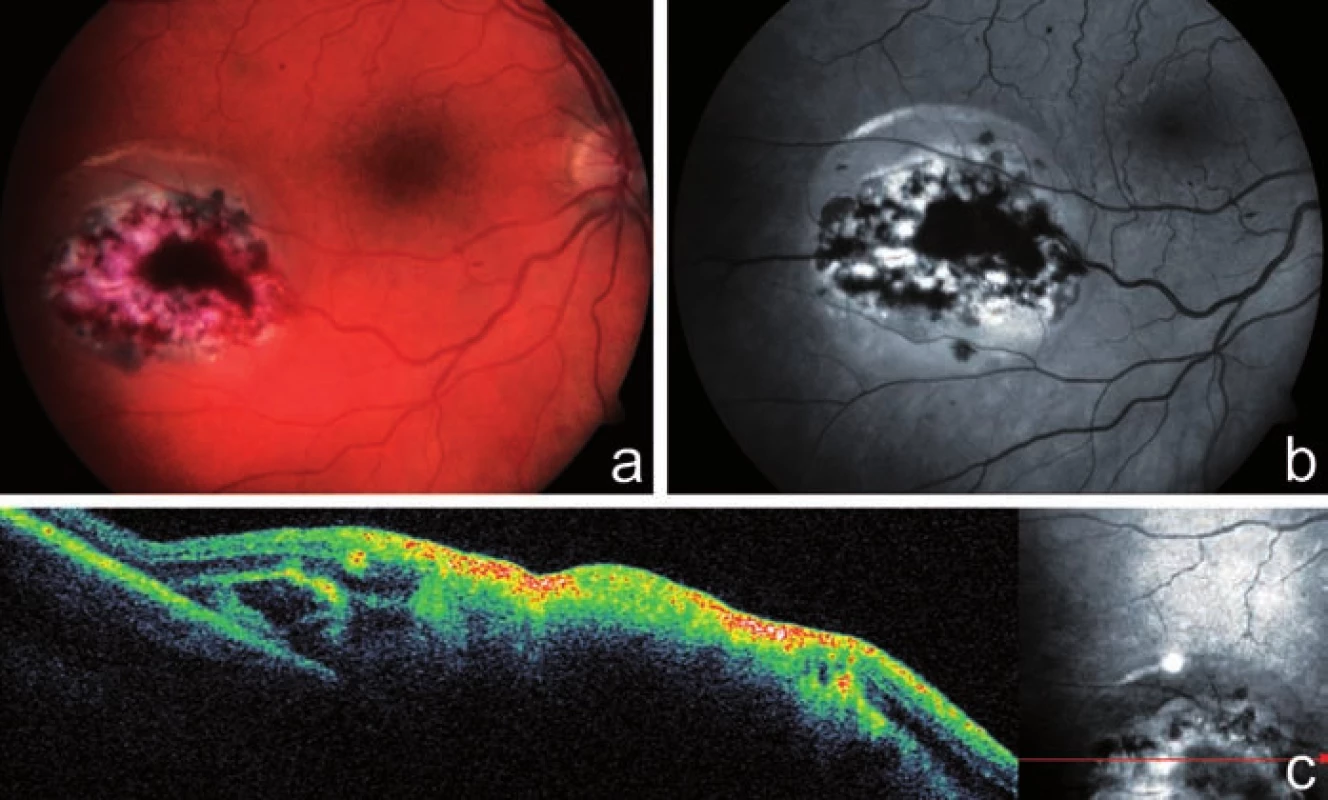
DISKUSE
Do naší retrospektivní studie bylo zařazeno 9 pacientů (3 ženy a 6 mužů). CMV retinitidu jsme diagnostikovali u 8 pacientů, jednu pacientku s již stanovenou diagnózou jsme jen konzultovali. Do souboru byli zařazeni pacienti HIV negativní, u kterých byla CMV retinitida diagnostikována na našem pracovišti v letech 2003–2012 na základě typického klinického obrazu a anamnézy (6 z 8 pacientů). U 2 atypických nálezů jsme diagnózu potvrdili až zachycením DNA patogenu ve vzorku sklivce (pacientka s NHL) a pozitivní sérologií s vyšetřením CMV v leukocytech (indolentní forma CMV retinitidy u pacientky s SLE). V 8 případech se jednalo o fulminantní formu, u 1 pacientky o indolentní formu CMV retinitidy.
Ve studii jsme sledovali incidenci onemocnění v závislosti na věku pacientů při stanovení diagnózy, pohlaví a příčině imunodeficitu (základní onemocnění pacientů). Dále jsme se zaměřili na postižení očí (jednostranné/oboustranné), vstupní a výstupní vizus, délku sledování a výskyt komplikací. Naše výsledky jsou srovnatelné s výsledky několika obdobných retrospektivních studií, které proběhly ve světě (5, 10, 15).
Limitujícím faktorem naší studie by mohla být malá velikost souboru (9 pacientů v průběhu 9 let), ale velikostí je náš soubor srovnatelný se soubory jiných retrospektivních studií: 18 pacientů za 19 let v Marylandu, USA (15); 9 pacientů za 14 let v Minnesotě, USA (5) a 11 pacientů zachycených v průběhu 10 let v Soulu, Korea (10).
V našem souboru jsme sledovali věk pacientů při stanovení diagnózy CMV retinitidy, průměrný věk byl 39,1 let (rozmezí 18 až 51 let). Jiné studie uvádí průměrný věk 43 let (10) a 58 let (5, 15). Poměr muži : ženy byl v našem souboru 6 : 3, v jiných studiích byl 6 : 3 (5), 8 : 3 (10) a 13 : 5 (15). Literatura uvádí výskyt CMV retinitidy mezi 20.–50. rokem života, se stejnou incidencí u mužů i žen (1, 12).
Všichni naši pacienti byli HIV negativní, ale imunokompromitovaní. U 5 pacientů došlo k rozvoji CMV retinitidy po transplantaci kostní dřeně (za 5–12 měsíců). Ve 2 případech byla CMV retinitida komplikací imunodeficitu při terapii systémového onemocnění (ulcerózní kolitida a SLE) a 2 pacienti byli léčeni pro lymfom. U 4 nemocných byla před rozvojem CMV retinitidy diagnostikována a léčena systémová CMV infekce: ve 3 případech v časném posttransplatačním období a u 1 pacienta po chemoterapii pro lymfom. Příčiny imunodeficitu byly obdobné i v ostatních zmiňovaných studiích: transplantace kostní dřeně (nejčastější), orgánové transplantace (srdce, ledviny, játra), autoimunitní onemocnění a lymfoproliferace (5, 10, 15). CMV retinitida se u pacientů v našem i v souborech jiných studií rozvinula v průběhu prvního roku po transplantaci kostní dřeně nebo orgánu (5, 15). U imunosuprimovaných pacientů bývá tento časový interval delší, Kuo a kol. (2004) uvádějí 8,5 až 21 měsíců po nasazení imunosuprese (15).
V 6 z 9 případů jsme zachytili oboustranný nález. V jiných studiích byl oboustranný nález popsán u 12 z 18 pacientů (15) a u 5 z 9 pacientů (5). Boguzsaková (2007) uvádí u CMV retinitidy (ale u HIV pozitivních pacientů) nález oboustranný, stranově asymetrický (3).
Subjektivní stesky našich pacientů se shodovaly se symptomy pacientů z jiných studií (výpad v zorném poli, plovoucí tečky, zhoršené vidění) (5, 10, 15). Eid a kol. (2008) popsali fotofobii (5), která ale k typickým symptomům CMV retinitidy nepatří.
Průměrná doba sledování našeho souboru byla 15,8 měsíců (v rozmezí 1 až 48 měsíců). Ve srovnatelné studii (5) sledovali pacienty v průměru 20 měsíců (v rozmezí 2 až 71 měsíců).
U 4 očí 3 pacientů (31 %) jsme po adekvátní léčbě zaznamenali zlepšení CZO, u 5 očí 5 pacientů (38 %) její stabilizaci. Eid a kol. (2008) udávají zlepšení CZO u 4 očí 4 pacientů (28,5 %) a stabilizaci CZO u 4 očí 4 pacientů (28,5 %) (5). Zhoršení CZO v našem souboru u 4 očí 3 pacientů (31 %) bylo způsobeno komplikacemi (1 pacient – 1 oko s hemoftalmem, 1 pacient – 1 oko s exsudativní amocí) nebo primárním očním onemocněním (oboustranné postižení u pacientky s primárním nitroočním lymfomem, která při zhoršení nálezu i vizu odmítla navrhovanou změnu terapie).
Nejčastější komplikace CMV retinitidy – ARR se v našem souboru nevyskytla. Zahraniční studie ale dokumentují výskyt této komplikace. Eid a kol. (2008) popsali ARR na 1 oku jednoho pacienta (ze 14 očí 9 pacientů) (5). Kuo a kol. (2004) zachytili ARR u 2 očí 2 pacientů (z 30 očí 18 pacientů), a to mezi 1.–7. měsícem od stanovení diagnózy CMV retinitidy. V této studii popsali u dalších 2 očí 2 pacientů ARR již v době diagnózy CMV retinitidy (15). V literatuře se uvádí výskyt ARR jako komplikace až v 50 % případů, nejčastěji v průběhu prvního roku po stanovení diagnózy CMV retinitidy (18).
Čtyři pacienti z našeho souboru (45 %; všichni po transplantaci kostní dřeně) zemřeli za 1, 4, 5 a 9 měsíců po stanovení diagnózy CMV retinitidy. Kuo a kol. (2004) uvádějí úmrtí u 10 z 18 pacientů (56 %) v průběhu doby sledování a průměrnou dobu přežití po stanovení diagnózy CMV retinitidy 11 měsíců (15).
U jedné naší pacientky jsme při snížení dávky virostatik zaznamenali relaps zánětu. Eid a kol. (2008) popsali recidivu CMV retinitidy u 3 očí 2 pacientů (21 %) (5). Kanski (2003) uvádí výskyt relapsu CMV retinitidy až u 50 % pacientů při udržovací léčbě (12).
ZÁVĚR
CMV retinitida je vzácné, zrak ohrožující virové onemocnění sítnice. Původně byla považována za typickou oportunní infekci u pacientů AIDS, ale vyskytuje se i u HIV negativních imunosuprimovaných pacientů. V Centru pro diagnostiku a léčbu uveitid 1. LF UK a VFN v Praze jsme v období od června 2003 do června 2012 vyšetřili celkem 1869 pacientů s uveitidou, z toho 423 pacientů se zadní uveitidou. CMV retinitidu jsme diagnostikovali u 8 pacientů, 1 pacientku s již stanovenou diagnózou jsme jen konzultovali. Záchyt CMV retinitidy pouze u 9 pacientů v průběhu 9 let, tj. 0,48 % všech uveálních pacientů za dané období, potvrzuje její vzácný výskyt. Všichni pacienti z našeho souboru byli HIV negativní, ale měli určitou formu imunodeficitu (po transplantaci kostní dřeně pro hematologickou malignitu, celková imunosuprese). Právě anamnéza imunodeficitu je pro diagnózu CMV retinitidy klíčová. Výskyt CMV retinitidy představuje pro pacienty po transplantaci velmi nepříznivý prognostický faktor a v našem souboru zemřeli všichni do 12 měsíců po stanovení diagnózy CMV retinitidy. Léčba vyžaduje úzkou mezioborovou spolupráci.
Do redakce doručeno dne 11. 12. 2013
Do tisku přijato dne 22. 1. 2013
MUDr. Andrea Beňová
Oční klinika
1. lékařská fakulta, Univerzity Karlovy
v Praze a Všeobecná fakultní nemocnice v Praze
U Nemocnice 2
128 00 Praha 2
e-mail: Andrea.Benova@vfn.cz
Sources
1. Altaweel, M., et al.: CMV retinitis [online]. July 11, 2012 [cit. 2012-08-13]. Dostupné z: http://emedicine.medscape. com/article/1227228-overview.
2. Banker, AS.: Posterior segment manifestations of Human Immunodeficiency Virus/ Acquired Immune Deficiency Syndrome. Indian J Ophthalmol. 2008; 56(5): 377–383.
3. Boguzsaková, J.: Oko a celková onemocnění. In: Kuchynka, P., et al. Oční lékařství. Praha: Grada Publishing, 2007.
4. Cihelková, I., Souček, P.: Atlas makulárních chorob. 1. vyd. Praha: Karolinum, 2005.
5. Eid AJ., Bakri, SJ., Kijipittayarit, S., et al.: Clinical features and outcomes of cytomegalovirus retinitis after transplantation. Transpl Infec Dis. 2008; 10(1): 13-18.
6. Freeman, WR., Friedberg DN., Berry C., et al.: Risk factors for development of rhegmatogenous retinal detachment in patients with cytomegalovirus retinitis. Am J Ophthalmol, 1993; 116(6): 713–720.
7. Foerster, HW. Pathology of granulomatous uveitis. Surv Ophthalmol. 1959; 4(3, Part 2): 283–326.
8. Gupta, AK., Mazumdar, S., Choudhry, S.: Practical approach to ophthalmoscopic retinal diagnosis. 1st edition.New Delhi: Jaypee Brothers Medical Publisher, 2010.
9. Hopkins, J., Gallant, J.: Johns Hopkins HIV guide 2012. 1st edition. Burlington: Jones&Bartlett Publishers, 2012.
10. Chung, H., Kim, K., Kim, J., et al.: Retinal complications in patients with solid organ or bone marrow transplantations. Transplantation, 2007; 83(6): 694-699.
11. Jabs, DA.: Ocular manifestations of HIV infection. Trans Am Ophthalmol Soc, 1995; 93 : 623–683.
12. Kanski, JJ.: Clinical Ophthalmology - a systematic approach. 5th edition. Philadelphia: Butterworth Heinemann, 2003.
13. Kempen, JH., Jabs, DA., Wilson, LA., et al.: Risk of vision loss in patients with cytomegalovirus retinitis and the Acquired Immune Deficiency Syndrome. Arch Ophthalmol. 2003; 121 : 466–476.
14. Kuchynka, P., et al.: Oční lékařství. Praha: Grada Publishing, 2007.
15. Kuo CI., Kempen, HJ., et al.: Clinical characteristics and outcomes of cytomegalovirus retinitis in persons without Human Immunodeficiency Virus infection. Am J Ophthalmol, 2004; 138(3): 338–346.
16. Reynolds, DJ.: Pediatric retina. New York: Springer, 2011.
17. Ryan, JS.: Retina. 3rd edition. Missoury: Mosby, 2001.
18. Říhová, E., et al.: Uveitidy. 1. vyd. Praha: Grada, 2009.
19. Viralzone. Cytomegalovirus [online]. July, 2012 [cit. 2012-08-16]. Dostupné z: http://viralzone.expasy.org/all_by_species/180.
20. Vlková, E., Pitrová, Š., Vlk, F.: Lexikon očního lékařství. 1. vyd. Brno: nakladatelství František Vlk, 2008.
21. Xhaard, A., Robin, M., Scieux, C., et al.: Increased incidence of cytomegalovirus retinitis after allogenic hematopoetic stem cell transplantation. Transplantation. 2007; 83(1): 80–83.
22. Zeicher, LS., Read, SJ.: Handbook of pediatric HIV care. Cambridge: Cambridge University Press, 2006.
Labels
Ophthalmology
Article was published inCzech and Slovak Ophthalmology

2013 Issue 6-
All articles in this issue
- Cytomegalovirová retinitida u HIV negativních pacientů – retrospektivní studie
- Hodnocení klinických výsledků implantace hydrofobně-hydrofilní nitrooční čočky EriFlex 877 FAB
- Strategie léčby vrozené neprůchodnosti slzných cest I. část – konzervativně intervenční postup
- Pars plana vitrektomie pro hemoftalmus na podkladě arteria hyaloidea persistens u tří dětí
- Operační řešení u velmi pokročilých rhegmatogenních amocí
- Ztráta zraku po nekomplikované pars plana vitrektomii
- Czech and Slovak Ophthalmology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Ztráta zraku po nekomplikované pars plana vitrektomii
- Strategie léčby vrozené neprůchodnosti slzných cest I. část – konzervativně intervenční postup
- Cytomegalovirová retinitida u HIV negativních pacientů – retrospektivní studie
- Pars plana vitrektomie pro hemoftalmus na podkladě arteria hyaloidea persistens u tří dětí
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

