-
Medical journals
- Career
Efektivita hluboké sklerektomie s implantací T-Fluxu – dlouhodobé výsledky
Authors: P. Studený 1,2; L. Koliášová 1; D. Siveková 2; J. Vránová 3; P. Kuchynka 2
Authors‘ workplace: Oční oddělení Karlovarské krajské nemocnice a. s., prim. MUDr. Andrej Farkaš 1; Oční klinika FNKV a 3. LF UK, Praha, přednosta prof. MUDr. Pavel Kuchynka, CSc. 2; Ústav lékařské biofyziky a lékařské informatiky, 3. LF UK, Praha, přednosta doc. MUDr. Jozef Rosina, Ph. D. 3
Published in: Čes. a slov. Oftal., 67, 2011, No. 1, p. 7-11
Category: Original Article
Overview
Cíl:
Zhodnotit dlouhodobou efektivitu hluboké sklerektomie s použitím implantátu T-Flux na výši nitroočního tlaku.Metodika:
Retrospektivní nekomparativní analýza pacientů naší glaukomové ambulance, u kterých byla provedena hluboká sklerektomie s implantací T-Fluxu. Pooperačně jsme hodnotili hodnotu nitroočního tlaku, nutnost další antiglaukomatózní terapie, provedení goniopunkturace.Výsledky:
Průměrná předoperační hodnota NOT byla 26,7 (± 0,8) mmHg, 6 měsíců po operaci 17,4 (± 0,8), ve 12. měsíci 16,5 (± 0,7), ve 24. měsíci 16,9 (± 0,9), ve 36. měsíci 17,2 (± 1,0), ve 48. měsíci 18,6 (± 1,1), v 60. měsíci 17,6 (± 1,1) a v 72. měsíci 18,3 (± 1,8). Průměrné předoperační množství antiglaukomové terapie bylo 2,5 (± 0,13) léku, pooperačně pak v 6. měsíci 0,73 (± 0,13), ve 12. měsíci 1,02 (± 0,13), ve 24. měsíci 1,1 (± 0,15), ve 36. měsíci 1,0 (± 0,18), v 48. měsíci 1,22 (± 0,18), v 60. měsíci 1,68 (± 0,2), a v 72. měsíci 1,8 (± 0,3). U 4 pacientů (10 %) byla provedena časná, u 6 (15 %) pozdní Nd:YAG goniopunktura.Závěr:
Hluboká sklerektomie s použitím implantátu T-Flux je relativně bezpečná antiglaukomatózní operace s minimálním množstvím komplikací, vysokou prediktabilitou výsledku a velmi dobrou dlouhodobou efektivitou.Klíčová slova:
hluboká sklerektomie, T-Flux, goniopunkturaPráce byla přednesena na XVIII. výročním sjezdu ČOS, 23. – 25. 9. 2010, Teplice
Úvod
Přes značné pokroky ve farmakologické léčbě glaukomu zůstávají filtrující operace důležitou součástí léčby pacientů se zeleným zákalem. A to především u pacientů refraktilních na farmakologickou léčbu, u pacientů s nízkou compliance nebo u pacientů s alergickými reakcemi na účinné nebo konzervační látky obsažené v antiglaukomových preparátech.
Obecně je možné rozdělit filtrující operace na perforující a neperforující. Trabekulektomie, zástupce perforujících výkonů (u nás v současné době pravděpodobně nejpoužívanější antiglaukomatózní operace) má zpravidla velmi dobrý efekt na zvýšení odtoku komorové vody. Nicméně tato operace je spojena s relativně vysokým počtem peroperačních i pooperačních komplikací – krvácení do přední komory, mělká přední komora, přechodná hypotonie nebo hypertonie bulbu, ablace cévnatky, pooperační iritida, endoftalmitida, indukce katarakty atd. (17). Neperforující techniky mají oproti tomu výrazně nižší výskyt těchto komplikací (6, 7, 11, 14, 20). V oftalmologii jsou neperforujícící filtrující operace známy již řadu let (8, 12, 13). V současné době se mezi nejvíce používané postupy řadí hluboká sklerektomie a viskokanalostomie (4) ad. Nicméně výhradou řady chirurgů zůstává relativně menší účinnost těchto operací, především v delším sledovacím období, vyšší náklady na operaci a delší učební křivka (14). Použití implantátů při hluboké sklerektomii ovšem přibližuje efektivitu operace na úroveň trabekulektomie, při zachování všech výhod neperforujících operací. Neperforující antiglaukomové operace s použitím implantátů byly v literatuře popsány jako efektivní metody ke snížení nitroočního tlaku u pacientů s prostým glaukomem s otevřeným úhlem (10), ale i u jiných typů glaukomu jako je pseudoexfoliativní (5, 15) nebo uveitický (2).
Cílem naší práce bylo retrospektivně zhodnotit dlouhodobý efekt hluboké sklerektomie s implantací T-Fluxu na snížení nitroočního tlaku.
Metodika
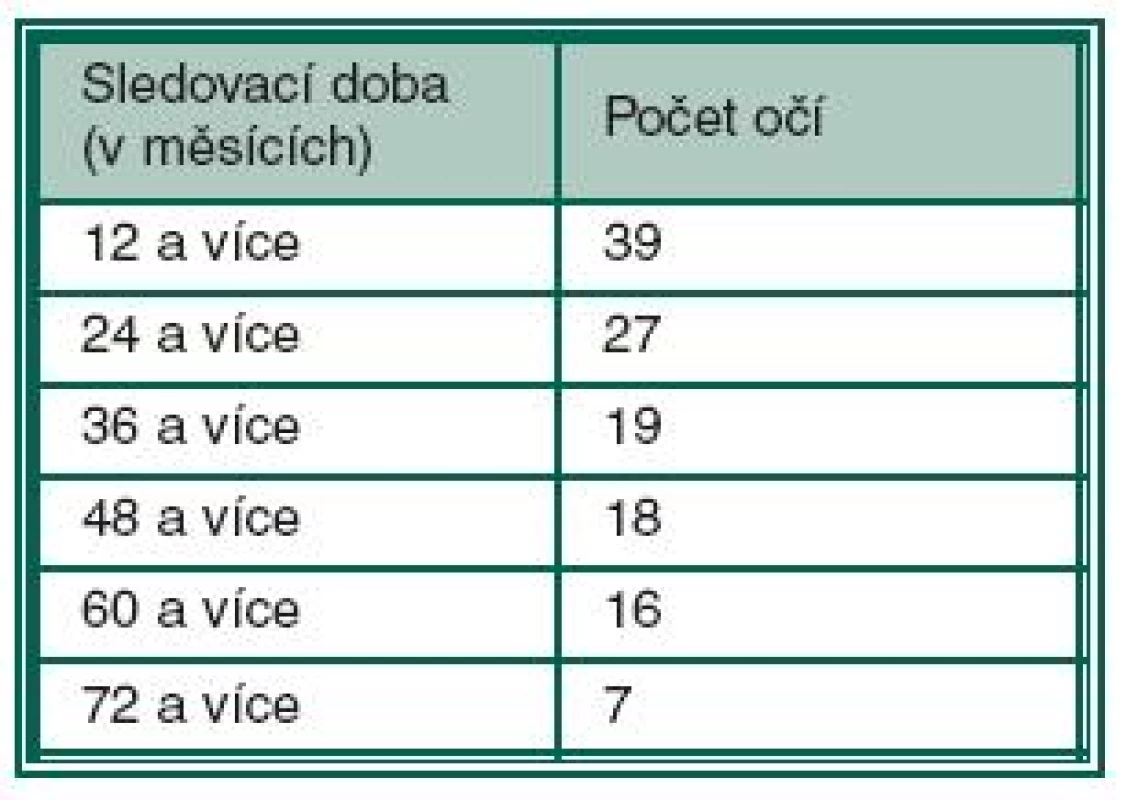
Na našem pracovišti bylo v období 3/2003 až 4/2009 provedeno 210 hlubokých sklerektomií, z toho u 69 operací byl výkon doplněna implantací T-Fluxu. Do retrospektivního hodnocení jsme zařadili všechny pacienty naší glaukomové ambulance, u kterých jsme měli možnost dlouhodobě sledovat výsledky operace. Celkem se jednalo o 40 očí 33 pacientů. U 7 pacientů byla tedy operace provedena oboustranně. Ve 32 případech se jednalo o prostý glaukom s otevřeným úhlem a pacienti neměli jiné oční onemocnění. 3 pacienti měli přítomnu diabetickou retinopatii a 1 pacient prodělal okluzi centrální retinální vény, nicméně ani u jednoho z těchto pacientů nebyly známky neovaskularizace duhovky ani v oblasti komorového úhlu. Dva pacienti prodělali anamnesticky iridocyclitidu, jedenkrát byly přítomny pseudoexfoliace a jedenkrát byla v anamnéze uváděna kontuze bulbu, rovněž bez viditelných gonioskopických změn. Minimální sledovací doba byla 12 měsíců, maximální 84 měsíců, v průměru 49,4 (± 25,3) měsíců (tab. 1).
Operace prováděl jeden chirurg. Operace byla prováděna v podspojivkové anestezii (0,1ml Marcain 0,5% AstraZeneca, Cheschire, Velká Británie) v horním kvadrantu, zhruba u č. 12. Otevření spojivky jsme prováděli incizí ve fornixu. Bulbus jsme stabilizovali v pohledové poloze směrem dolů fixací bulbární spojivky pomocným stehem (Silk 5/0; Chirmax, ČR) na okraje víčkového rozvěrače. Po obnažení skléry jsme stavěli krvácení převážně využitím komprese pomocí tupého skalpelu, pouze v případě masivnějšího krvácení skléry jsme provedli šetrnou diatermokoagulaci. Poté jsme vytvořili sklerální lalok tloušťky zhruba 1/3 až 1/2 celkové tloušťky skléry. Velikost lalůčku byla asi 5x5 mm, s bází při limbu. K řezu byl použit třicetistupňový jednorázový nůž (Ophthalmic Knife 30°, Alcon Surgical, Fort Worth, USA) a po dosažení požadované hloubky byla vytvořena sklerální lamela jednorázovým nožem crescent (Sharpoint Crescent knife, Surgical Specialties Corporation, Reading, USA). Obdobným postupem (30° nůž a crescent) jsme vytnuli hlubokou lamelu velikosti 3,5 x 4 mm, s ponecháním jen tenké vrstvy sklerálních vláken nad cévnatkou. Na limbální straně zasahoval lalok asi 1 mm do oblasti čiré rohovky, prakticky na úroveň Descemetovy membrány. Dosažení správné hloubky preparace bylo indikováno prosakováním komorové tekutiny přes vytvořenou trabekulodescemeteskou membránu (TDM). Vytnutím lamely byl zároveň otevřen Schlemmův kanál, respektive odstraněna jeho zevní stěna. Následně jsme provedli peeling Schlemmova kanálu, kdy jsme pomocí jemné pinzety (Mermoud NPGS Forceps, Huco Vision SA, St.Blaise, Switzerland) odstranili endotel jeho vnitřní stěny. Otevřené okraje kanálu jsme nasondovali cyklospatulí. Pomocí hydrodisekční kanyly jsme do Schlemmova kanálu injikovali malé množství Ringerova roztoku a sledovali jsme průchodnost vodních cévek spojujících Schlemmův kanál se spojivkovými cévami. Průchodnost těchto cév byla indikována odbarvením krevního sloupce v episklerálních vénách. Na TDM jsme položili implantát T-Flux NV (Carl Zeiss Meditec SAS, La Rochelle Cedex, France). Obě jeho ramena jsme zanořili do otevřených ústí Schlemmova kanálu. Novější varianta implantátu je opatřena otvůrkem v centru, který umožňuje jeho fixaci rohovkovým stehem ke spodině. My jsme tuto možnost u žádného pacienta nevyužili, neboť implantát se nám vždy jevil jako dostatečně stabilní díky fixaci ramének v Schlemmově kanálu. Sklerální lalůček kryjící implantát jsme fixovali dvěma neresorbovatelnými stehy Nylon 10/0 (Alcon Surgical, Fort Worth , USA), v obou rozích sklerotomie. Spojivka a Tenonská kapsula byly zašity v jednom kroku pokračujícím resorbovatelným stehem (Vicryl, Ethicon 8/0; Johnson & Johnson, St. Stevens-Woluwe, Belgium).
Pooperačně pacienti aplikovali tobramycin a dexamethasone ve formě kapek (Tobradex gtt, Alcon Couvreur, Puurs, Belgium) pětkrát denně po dobu jednoho týdne a následně třikrát denně po dobu 3 týdnů. Pooperační kontroly byly prováděny 1. a 7. pooperační den, následně po 1 a 3 měsících, a dále pak každé 3 měsíce. Při kontrolách byla sledována hodnota nitroočního tlaku aplanačně pomocí Goldmanova tonometru.
Výsledky a úspěšnost operace jsme hodnotili dle standardů a doporučení World Glaucoma Association WGA (22). Jako úspěšnou jsme operaci hodnotili tehdy, pokud pooperační nitrooční tlak byl nižší nebo roven 21 mmHg a vyšší než 6 mmHg, a zároveň došlo k poklesu tlaku minimálně o 20 % ve srovnání s hodnotou předoperační. Pokud bylo tohoto stavu dosaženo bez nutnosti antiglaukomatózní terapie byl úspěch považován za absolutní, pokud byla k dosažení tohoto výsledku nutná antiglaukomatózní terapie (maximálně ovšem 2 léky) byl úspěch hodnocen jako relativní. Žádný z našich pacientů pooperačně neužíval systémově inhibitory karboanhydrázy. Za selhání operace jsme považovali hodnoty NOT mimo stanované rozmezí (6–21 mmHg) nebo byl pokles tlaku o méně než 20 % ve srovnání s předoperační hodnotou. Jako částečný neúspěch jsme hodnotili pacienty, u kterých bylo překročeno jedno kritérium, tj. pokles méně než o 20 % nebo hodnoty tlaku nad 21 mmHg. Jako úplný neúspěch jsme hodnotili pacienty, u kterých byla překročena obě kriteria, nebo byla nutná další chirurgická intervence. Nd:YAG goniopunkturu, provedenou u některých pacientů v pooperačním období jsme dle doporučení WGA nepovažovali za chirurgickou intervenci a pokud došlo k odpovídajícímu poklesu tlaku, byla operace následně hodnocena jako úspěšná.
Výsledky
Výsledné hodnoty nitroočního tlaku a množství používané terapie v jednotlivých sledovaných obdobích jsou přehledně uvedeny v tabulce (tabulka 2). Průměrná předoperační hodnota NOT byla 26,7 (± 0,8) mmHg, 6 měsíců po operaci 17,4 (± 0,8), ve 12. měsíci 16,5 (± 0,7), ve 24. měsíci 16,9 (± 0,9), ve 36. měsíci 17,2 (± 1,0), ve 48. měsíci 18,6 (± 1,1), v 60. měsíci 17,6 (± 1,1) a v 72. měsíci 18,3 (± 1,8) mmHg (graf 1). Statistická významnost výsledků byla hodnocena Bonferroni testem. V porovnání s předoperační hodnotou nitroočního tlaku došlo ve všech hodnocených obdobích ke statisticky významnému snížení (viz tabulka 3). Přestože s delší sledovací dobou došlo postupně k mírnému nárůstu hodnot NOT, nebyl tento nárůst statisticky významný. Druhou hodnocenou veličinou bylo množství podávané lokální antiglaukomatózní terapie. Předoperační hodnota byla 2,5 (± 0,13) léku, pooperačně pak v 6. měsíci 0,73 (± 0,13), ve 12. měsíci 1,02 (± 0,13), ve 24. měsíci 1,1 ± 0,15), ve 36. měsíci 1,0 (± 0,18), v 48. měsíci 1,22 (± 0,18), v 60. měsíci 1,68 (± 0,2), a v 72. měsíci 1,8 (± 0,3) (graf 2). Dle Bonferroni testu statistické významnosti bylo snížení antiglaukomatózní terapie v pooperačním období ve srovnání s předoperační hodnotou statisticky významné, a to ve všech hodnocených obdobích. Opět došlo postupně k mírnému zvyšování počtu antiglaukomatózní léčby. Statisticky významný rozdíl jsme však zaznamenali pouze při porovnání medikace skupiny v 60. a 72. měsíci v porovnání s množstvím léčby v 6. měsíci (tabulka 4).
Table 2. Průměrné hodnoty NOT a průměrné množství použité terapie v jednotlivých sledovaných obdobích 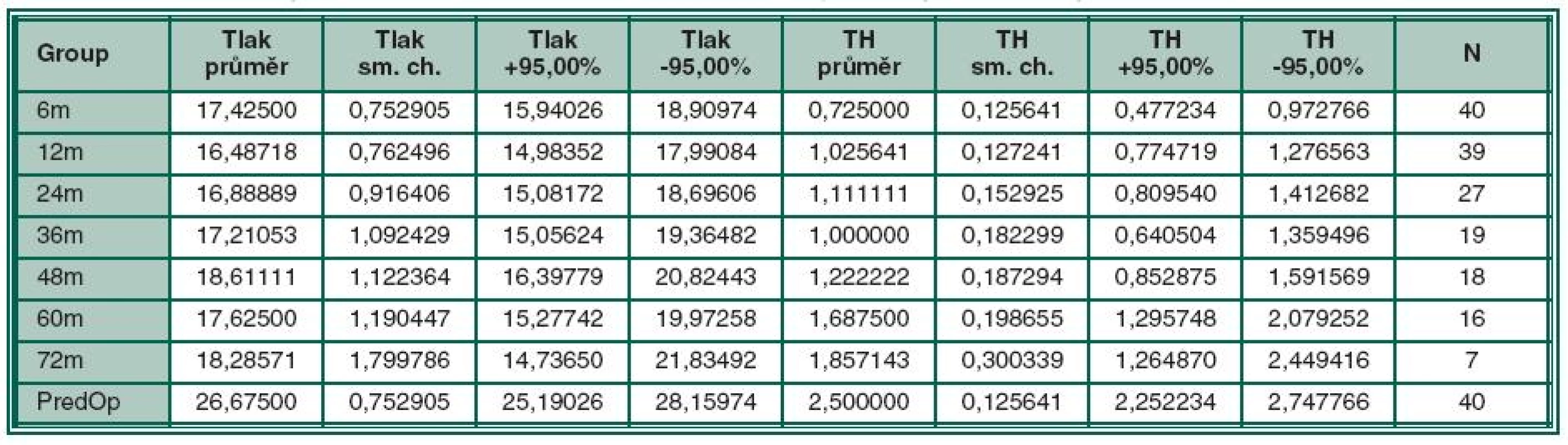
Graph 1. Průměrné hodnoty nitroočního tlaku v jednotlivých sledovaných obdobích 
Table 3. Bonferroni test statistické významnosti – NOT 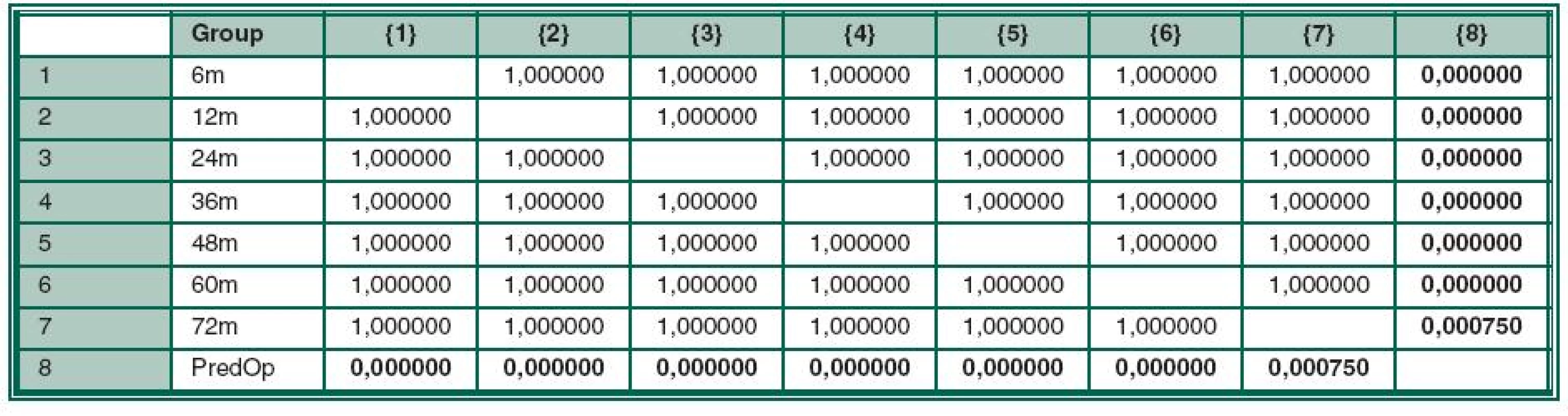
Graph 2. Průměrné hodnoty množství antiglaukomové terapie v jednotlivých sledovaných obdobích 
Table 4. Bonferroni test statistické významnosti – terapie 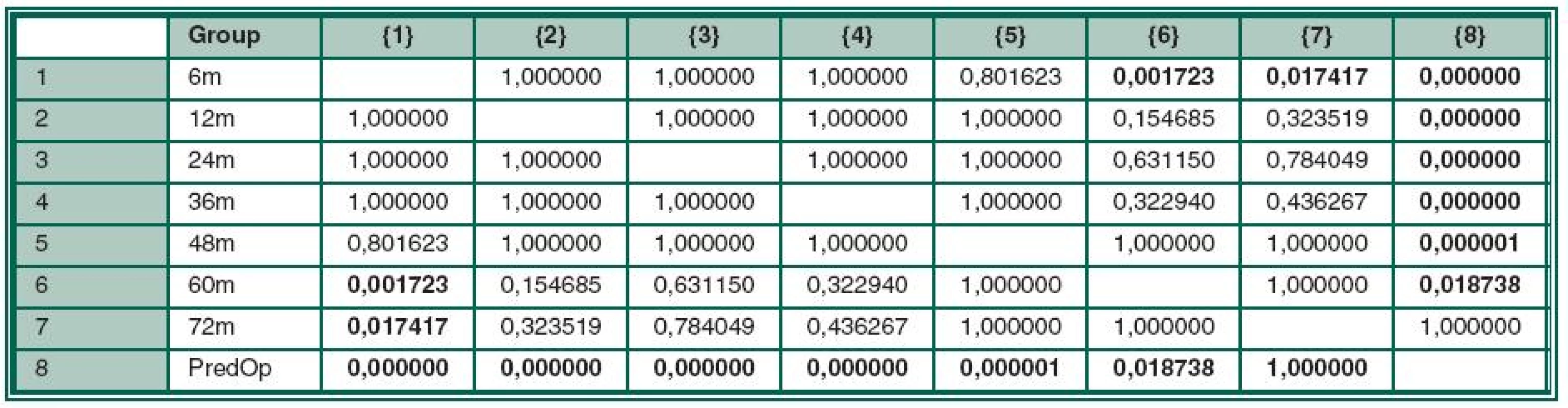
Dále byla hodnocena úspěšnost operace dle stanovených kriterií. V období 6 měsíců po operaci bylo 16 operací hodnoceno jako absolutně úspěšné, 14 jako relativně úspěšné (tzn. dosažení požadovaného snížení NOT v obou kritériích, ale s antiglaukomatózní terapií), 8 operací bylo hodnoceno jako částečně neúspěšné (dosažení pouze jednoho z kritérií poklesu nitroočního tlaku) a 2 operace byly hodnoceny jako úplně neúspěšné (AN). U jednoho z těchto pacientů byla provedena Nd:YAG goniopunktura, došlo k úpravě nitroočního tlaku a v následujících obdobích byl již hodnocen jako relativně úspěšný. U druhého z pacientů bohužel nedošlo k potřebnému snížení tlaku a musela být provedena další antiglaukomatózní operace – trabekulektomie. Tento pacient byl z další statistiky vyřazen. 12 měsíců po operaci bylo 11 operací hodnoceno jako kompletně úspěšné (AÚ), 21 jako relativně úspěšné (RÚ), 7 jako částečně neúspěšné (RN). Ve 24. měsíci jsme hodnotili 5 operací jako AÚ, 15 RÚ, 7 RN. Ve 36. měsíci 3 AÚ, 13 RÚ, 3 RN; v 48. měsíci 1 AÚ, 13 RÚ, 4 RN; v 60. měsíci 1 AÚ 12 RÚ, 3 RN a v 72. měsíci 7 RÚ (graf 3).
Graph 3. Úspěšnost operace v jednotlivých sledovaných obdobích 
Z časných pooperačních komplikací jsme v našem souboru zaznamenali jedenkrát přechodnou hypotenzi a změlčení přední komory (2,5 %), jedenkrát pooperačně vysoký nitrooční tlak (nad 30 mmHg), reagující na léčbu (2,5 %), u dvou pacientů byla patrna hyphaema (5 %) a dvakrát jsme zaznamenali dehiscenci spojivkové rány.
U 4 našich pacientů jsme provedli časnou (10 %) a u 6 pozdní (15 %) Nd:YAG goniopunkturu.
Diskuse
Implantáty používané v současné době jako doplnění neperforujících operací můžeme v zásadě rozdělit na dvě základní skupiny – resorbovatelné a neresorbovatelné. Mezi komerčně dostupné resorbovatelné implantáty řadíme například kolagenový implantát, kyselinu hyaluronovou, zesíťovanou kyselinu hyaluronovou – SK gel (3, 9). Kromě těchto firemně vyráběných implantátů bylo v odborné literatuře popsáno i použití dalších materiálů k udržení prostoru pod sklerálním lalokem – Healon GV (19), chromovaný šicí materiál (23), implantace autologní skléry (18) atd. Jediným komerčně dostupným neresorbovatelným implantátem na našem trhu v současné době je T Flux (1). Hlavním úkolem implantátu u neperforující filtrujících antiglaukomatózních operacích je především udržení volného prostoru pod sklerálním lalokem v místě provedené sklerektomie, eventuelně udržení otevřeného vstupu do Schlemmova kanálu. Další výhodou implantátu u těchto operací je možnost pooperačního provedení Nd:YAG laserové goniopunktury (16). Při tomto zákroku vytvoříme drobné mikroperforace v oblasti trabekulodescemetské membrány, a tak de facto převedeme operaci neperforující na operaci mikroperforující. Vzhledem k tomu, že komplikace při tomto postupu jsou velmi vzácné, je zachována hlavní výhoda neperforujících operací ve srovnání s perforujícími, a tou je relativně nízký výskyt peroperačních a pooperačních komplikací.
Provedení Nd:YAG goniopunktury lze z časového hlediska rozdělit na dvě období – časné: do 3 měsíců a pozdní: nad 3 měsíce. Příčinou časného provedení goniopunktury je zpravidla určitá nedokonalost v operačním postupu, kdy je tloušťka vypreparované TDM příliš velká a komorová tekutina pak neprotéká do oblasti sklerektomie v dostatečném množství. Indikací k provedení goniopunktury v pozdějším období, tj. po uplynutí 3 měsíců, je zpravidla fibróza v oblasti TDM (21). Pozdní provedení goniopunktury je výkonem specifickým právě jen u operace HS s implantací T-Fluxu, neboť v případě použití resorbovatelných implantátů (typu kolagen, SK gel atd.) je goniopunkturace v tomto období již neúčinná. V krátkodobém sledování je efektivita T-Fluxu srovnatelná s dalšími implantáty, např. SK gelem (24), ale hlavní výhodou neresorbovatelného implantátu T-Flux je především permanentně udržovaný otevřený prostor pod sklerální lamelou, do které je možný odtok a následně postupná resorpce komorové tekutiny, udržení otevřeného ústí Schlemmova kanálu a možnost doplnění operace YAG laserovou goniopunkturou, a to v podstatě kdykoliv v pooperačním období. To teoreticky významně zvyšuje efektivitu takto provedené neperforující antiglaukomové operace.
Závěr
Hluboká sklerektomie s implantací T-Fluxu je relativně bezpečná procedura s minimálním množstvím komplikací, s vysokou prediktabilitou výsledku a velmi dobrou dlouhodobou efektivitou. Použití neresorbovatelného implantátu výrazně zvyšuje účinnost operace. Implantát T-Flux je v současné době akceptován zdravotními pojišťovnami jako zvlášť účtovaný materiál (ZUM) a nepředstavuje tak pro zdravotnické zařízení zvýšené náklady na operaci. V podstatě jedinou nevýhodou této operace ve srovnání s klasickou antiglaukomovou operací – trabekulektomií zůstává relativně obtížnější chirurgický postup s delší učební křivkou.
Do redakce doručeno dne 27. 10. 2010
Do tisku přijato dne 10. 2. 2011MUDr. Pavel Studený
Oční klinika FNKV a 3.LF UK Praha
Šrobárova 50
100 00 Praha
studenypavel@seznam.cz
Sources
1. Ates, H., Uretmen, O., Andac, K. et al.: Deep sclerectomy with a nonabsorbable implant (T-Flux): preliminary results. Can J Ophthalmol, 38, 2003; 6 : 482–8.
2. Auer, C., Mermoud, A., Herbort, C.P.: Deep sclerectomy for the management of uncontrolled uveitic glaucoma: preliminary data. Klin Monatsbl Augenheilkd, 221, 2004; 5 : 339–42.
3. Bissig, A., Rivier, D., Zaninetti, M. et al.: Ten years follow-up after deep sclerectomy with collagen implant. J Glaucoma, 17, 2008; 8 : 680–6.
4. David, V.P., Kutty, K.G., Somasundraram, N. et al.: Five-year results of viscocanalostomy. Eur J Ophthalmol, 18, 2008; 3 : 417–22.
5. Drolsum L.: Deep sclerectomy in patiens with capsular glaucoma. Acta Ophthalmol Scand, 81, 2003; 6 : 567–72.
6. Drolsum L.: Conversion from trabeculectomy to deep sclerectomy. Prospective study of the first 44 cases. J Cataract Refract Surg, 29, 2003; 7 : 1378–84.
7. Egrilmez, S., Ates, H., Nalcaci, S. et al.: Surgically induced corneal refractive change following glaucoma surgery: nonpenetrating trabecular surgeries versus trabeculectomy. J Cataract Refract Surg, 30, 2004; 6 : 1232–9.
8. Fyodorov, S.N.: Non-penetrating deep sclerectomy in open-angle glaucoma. Eye Microsurg, 1989 : 52–5.
9. Galassi, F., Giambene, B.: Deep sclerectomy with SkGel implant: 5-years results. J Glaucoma, 17, 2008; 1 : 52–6.
10. Hondur, A., Onol, M., Hasanreisoglu, B.: Nonpenetrating glaucoma surgery: meta-analysis of recent results. J Glaucoma, 17, 2008; 2 : 139–46.
11. Chiou, A.G., Mermoud, A., Jewelewicz, D.A.: Post-operative inflammation following deep sclerectomy with collagen implant versus standard trabeculectomy. Graefes Arch Clin Exp Ophthalmol, 236, 1998; 8 : 593–6..
12. Kozlov, V.I., Bagrov, S.N., Anisimova, S.Y. et al.: Deep sclerectomy with collagen. Eye Microsurg, 3, 1990 : 44–46.
13. Krasnov, M.M.: Externalization of Schlemmęs canal (sinusotomy ) in glaucoma. Br J Ophthalmol, 52, 1968; 2 : 157–61.
14. Mendrinos, E., Mermoud, A., Shaarawy, T.: Nonpenetrating glaucoma surgery. Surv Ophthalmol, 53, 2008; 6 : 592–630.
15. Mendrinos, E., Mansouri, K., Mermoud, A. et al.: Long-term results of deep sclerectomy with collagen implant in Exfoliative glaucoma. J Glaucoma,18, 2009; 5 : 361–7.
16. Mermoud, A., Karlen, M.E., Schnyder, C.C. et al.: Nd:YAG goniopuncture after deep sclerectomy with collagen implant. Ophthalmic Surg Lasers., 30, 1999; 2 : 120–5.
17. Mosaed, S., Dustin, L., Minckler, D.S.: Comparative outcomes between newer and older surgeries for glaucoma.Trans Am Ophthalmol Soc., 107, 2009; 127–33..
18. Mousa, A.S.: Preliminary evaluation of nonpenetrating deep sclerectomy with autologous scleral implant in open-angle glaucoma. Eye 21, 2007; 9 : 1234–8.
19. Ravinet, E., Bovey, E., Mermoud, A.: T-flux implant versus Healon GV in deep sclerectomy. J Glaucoma, 13, 2004; 1 : 46–50.
20. Russo, V., Scott, I.U., Stella, A., et al.: Nonpenetgrating deep sclerectomy with reticulated hyaluronic acid implant versus punch trabeculectomy: a prospective clinical trial. Eur J Ophthalmol, 18, 2008; 5 : 751–7.
21. Shaarawy, T.: Postoperative management of non-penetrating filtering surgery. In: Mermoud, A., Shaarawy, T. (Eds), Non-Penetrating Glaucoma Surgery, London, Martin Dunitz Ltd, 2001, s.132–134.
22. Shaarawy, T.M., Sherwood, M.B., Grehn, F.: Guidelines on Design and Reporting of Glaucoma Surgical Trials. Amsterdam, Kugler Publications, 2009.
23. Wevill, M.T., Meyer, D., Van Aswegen, E.: A pilot study of deep sclerectomy with implantation of chromic suture material as a collagen implant: medium-term results. Eye, 19, 2005; 5 : 549–54.
24. Wiermann, A., Zeits, O., Jochim, E., et al.: A comparison between absorbable and non-resorbable scleral implants in deep sclerectomy (T-Flux and SK-gel). Ophthalmologe, 104, 2007; 5 : 409–14.
Labels
Ophthalmology
Article was published inCzech and Slovak Ophthalmology

2011 Issue 1-
All articles in this issue
- Současné možnosti náhrady vidění nevidomých pacientů pomocí arteficiálních neuroprotéz
- Efektivita hluboké sklerektomie s implantací T-Fluxu – dlouhodobé výsledky
- Výskyt kardiovaskulárních onemocnění u pacientů s pseudoexfoliativním syndromem a pseudoexfoliativním glaukomem
- Elektronický systém pro kontrolu správné polohy hlavy po některých vitreoretinálních operacích
- Návrh systému starostlivosti o zrakovo postihnuté deti v SR
- Katarakta po úraze bleskom
- Czech and Slovak Ophthalmology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Výskyt kardiovaskulárních onemocnění u pacientů s pseudoexfoliativním syndromem a pseudoexfoliativním glaukomem
- Současné možnosti náhrady vidění nevidomých pacientů pomocí arteficiálních neuroprotéz
- Efektivita hluboké sklerektomie s implantací T-Fluxu – dlouhodobé výsledky
- Katarakta po úraze bleskom
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career