-
Medical journals
- Career
Klinické sledovanie účinnosti a bezpečnosti generického produktu UNILAT v terapii glaukómu a vnútroočnej hypertenzie
Authors: P. Strmeň 1; V. Jančuš 2; J. Okkelová 3; M. Tvrdoňová 2
Authors‘ workplace: Klinika Oftalmológie, LFUK, Bratislava, prednosta prof. MUDr. Peter Strmeň, CSc. 1; UNIMED PHARMA, spol. s r. o., Bratislava, Oddelenie výskumu a vývoja, generálny riaditeľ RNDr. Elena Slučiaková 2; UNIMED PHARMA, spol. s r. o., Bratislava, Oddelenie farmakovigilancie, generálny riaditeľ RNDr. Elena Slučiaková 3
Published in: Čes. a slov. Oftal., 66, 2010, No. 6, p. 258-261
Category: Original Article
Overview
Autori predstavujú nové generikum UNILAT od slovenskej farmaceutickej spoločnosti UNIMED PHARMA, s r.o., a hodnotia jeho účinnosť a bezpečnosť v terapii glaukómu a vnútroočnej hypertenzie v rámci III. fázy klinického skúšania. Dizajn klinického skúšania bol založený na otvorenej multicentrickej porovnávacej štúdii, ktorej cieľom bolo preukázať, že generikum UNILAT (latanoprost 50 μg/ml očná roztoková instilácia, Unimed Pharma) je rovnako účinný a bezpečný ako originálny produkt XALATAN (latanoprost 50 μg/ml očná roztoková instilácia, Pfizer). Štúdia sa uskutočnila v 7 súkromných oftalmologických ambulanciách na Slovensku a zúčastnilo sa jej 77 pacientov, ktorí boli sledovaní počas troch mesiacov v období od 5. 2. 2008 do 24. 7. 2008. Primárnym parametrom na preukázanie účinnosti generika UNILAT bol pokles priemernej hodnoty vnútroočného tlaku (VOT) medzi prvou a poslednou kontrolnou návštevou. Sekundárnym sledovaným parametrom bol podiel pacientov, u ktorých bola výsledná nameraná hodnota VOT na konci sledovania menšia ako 21 mmHg. Hodnotenie bezpečnosti generika UNILAT bolo založené na sledovaní frekvencie výskytu nežiaducich účinkov.
Výsledky klinickej štúdie potvrdili terapeutické indikácie generika UNILAT a zároveň preukázali, že je rovnako účinný a bezpečný ako originálny produkt.Kľúčové slová:
UNILAT, účinnosť, bezpečnosť, latanoprost, glaukómÚvod
Glaukóm je multifaktoriálne ochorenie, ktoré je druhou najčastejšou príčinou slepoty. Podľa Svetovej zdravotníckej organizácie (WHO) postihuje až 66,8 milióna ľudí na celom svete. Hlavným rizikovým faktorom je vo väčšine prípadov zvýšený vnútroočný tlak (VOT nad 21 mmHg), ktorý ohrozuje výživu vnútroočných tkanív a postupne vedie k poškodzovaniu papily zrakového nervu a zhoršeniu zrakových funkcií [3].
Liečba glaukómu je zvyčajne celoživotná a uplatňujú sa pri nej konzervatívne aj invazívne postupy. V posledných rokoch dochádza k zmenám vo farmakoterapii, predovšetkým ide o obmedzenie používania starých preparátov v prospech nových antiglaukomatík, ktoré sú menej zaťažené nežiaducimi účinkami a zároveň zvyšujú komfort pacientov z pohľadu dávkovania (1krát denne). Novú perspektívu v liečbe glaukómu priniesli prostaglandíny s výborným účinkom na zníženie vnútroočného tlaku. Naviac, lokálne používanie a receptorová selektivita prostaglandínov je dôvodom nízkeho výskytu nežiaducich reakcií s minimálnou systémovou záťažou. Účinná látka latanoprost je analóg prostaglandínu F2α, ktorý bol cielene syntetizovaný na liečbu glaukómu. Je to selektívny agonista prostaglandínového FP receptora, ktorý znižuje vnútroočný tlak zvýšením odtoku komorového moku. Zníženie VOT u ľudí sa začína asi o 3–4 hodiny po jeho podaní a maximálny účinok sa dosahuje po 8–12 hodinách. Zníženie tlaku pretrváva najmenej počas 24 hodín [4, 6].
Prvým originálnym produktom s účinnou látkou latanoprost bol XALATAN, očná roztoková instilácia od firmy Pfizer, ktorý je na slovenskom trhu od roku 1998. V súčasnosti sa na trh postupne dostávajú generické produkty s obsahom latanoprostu, medzi ktoré patrí UNILAT (obr. 1), očná roztoková instilácia od slovenskej farmaceutickej spoločnosti UNIMED PHARMA, s r.o.
Image 1. Generický produkt UNILAT (latanoprost 50 μg/ml, očná roztoková instilácia, Unimed Pharma) 
Cieľom prezentovanej klinickej štúdie bolo porovnať generický produkt UNILAT s originálnym liekom XALATAN, potvrdiť jeho terapeutické indikácie, a dokázať, že UNILAT je rovnako účinný a bezpečný v liečbe glaukómu a vnútroočnej hypertenzie ako originálny produkt. Štúdia bola povolená krajskými etickými komisiami a bola uskutočnená v súlade s etickými princípmi Helsinskej deklarácie a správnej klinickej praxe.
Materiál a metódy
Do klinického sledovania bolo celkovo zaradených 77 pacientov. Boli to novodiagnostikovaní pacienti s primárnym glaukómom s otvoreným uhlom (PGOU), vnútroočnou hypertenziou a pacienti liečení lokálnymi β-adrenergnými blokátormi a inhibítormi karboanhydrázy (ICA) s následnou vymývacou fázou trvajúcou 4 týždne.
Novodiagnostikovaní pacienti a pacienti po vymývacej fáze s VOT > 21 mmHg boli randomizovaní na liečbu produktmi XALATAN (latanoprost 50 μg/ml očná roztoková instilácia, Pfizer) jedenkrát denne a UNILAT (latanoprost 50 μg/ml očná roztoková instilácia, Unimed Pharma) jedenkrát denne počas 12 týždňov. Obidve skupiny boli paralelne sledované od začiatku terapie po dobu 3 mesiacov. V prípade pacientov podstupujúcich vymývaciu fázu bola táto doba predĺžená o 1 mesiac. V čase vymývacej fázy bola povinná návšteva na 14 deň ± 2 dni a v prípade, ak by skúšajúci považoval nameranú hodnotu VOT za potenciálne nebezpečnú, pacient by bol vyňatý zo štúdie. V prípade tohto sledovania však k takejto situácii nedošlo. Po splnení zaraďujúcich kritérií a podpísaní informovaného súhlasu sa zaznamenali demografické údaje pacienta, osobná a rodinná anamnéza, sprievodná terapia. Pacient absolvoval nasledovné vyšetrenia: zraková ostrosť, zorné pole, vyšetrenie predného segmentu oka štrbinovou lampou vrátane gonioskopie, priamu a nepriamu oftalmoskopiu.
Vyraďujúce kritéria možno zhrnúť do nasledujúcich bodov:
- pacient s lokálnou protiglaukómovou liečbou inou ako β adrenergnými blokátormi a ICA,
- pacient s anamnézou glaukómu s uzatvoreným uhlom,
- pacient v minulosti s výskytom nežiaducich reakcií na protiglaukómovú liečbu a konzervačnú látku benzalkónium chlorid (BAC),
- pacient s vážnym úrazom oka/očí v minulosti,
- pacient, ktorý počas posledných 6 mesiacov absolvoval operáciu oka alebo sa podrobil laserovej trabekuloplastike,
- prítomnosť závažnej formy syndrómu suchého oka,
- prítomnosť zápalovej choroby oka/očí v anamnéze počas posledných troch mesiacov,
- pacient s ťažkou alebo zle kontrolovanou astmou,
- pacient, u ktorého lekár usúdil, že monoterapia je nedostatočná.
Ďalej sa klinického skúšania nemohol zúčastniť pacient, ak mal menej ako 18 rokov, ak sa zúčastňoval iného klinického sledovania alebo ak lekár predpokladal, že existuje zvláštny dôvod, prečo by pacient nemal byť zaradený do sledovania. Ak bola pacientkou žena, nemohla sa zúčastniť klinického sledovania v prípade gravidity a laktácie.
Odporúčané dávkovanie bola 1 kvapka do postihnutého oka/očí jedenkrát denne. Viaceré štúdie dokázali, že optimálny účinok sa dosiahne, ak sa latanoprost podáva večer [1, 7]. Odporúčaná doba podávania bola teda medzi 19.–21. hodinou večer. Meranie hodnoty VOT sa uskutočnilo pred začiatkom terapie v čase vstupnej návštevy a potom v pravidelných intervaloch po týždni (deň 7 ± dni), mesiaci (deň 28 ± 2 dni) a troch mesiacoch (deň 84 ± 2 dni) terapie. VOT bol meraný pomocou Goldmannovho aplanačného tonometra v presne stanovenom čase (8. hodina ráno ± 1 hodina).
Po skončení klinického skúšania sa v obidvoch skupinách porovnala účinnosť a bezpečnosť liečby na základe analýzy primárneho a sekundárneho parametra. Primárnym sledovaným parametrom bol pokles priemernej hodnoty VOT medzi prvou a poslednou kontrolnou návštevou (deň 84 ± 2 dni), pričom na potvrdenie účinnosti bol potrebný pokles VOT minimálne o 5 jednotiek mmHg. Sekundárnym parametrom na potvrdenie účinnosti bol podiel pacientov s výslednou hodnotou VOT < 21 mmHg na konci sledovania.
Bezpečnosť generika UNILAT bola stanovená na základe výskytu nežiaducich reakcií u pacientov.
Výsledky
Na klinickom sledovaní sa podieľalo 7 súkromných očných ambulancií s celkovým počtom 77 pacientov, z ktorých bolo 37 (33 žien, 4 muži) zaradených na liečbu produktom XALATAN. V tejto skupine malo 20 pacientov diagnostikovaný PGOU a 17 vnútroočnú hypertenziu, pričom 12 pacientov muselo absolvovať vymývaciu fázu. Z tejto skupiny bol jeden pacient vyradený po prvom mesiaci sledovania v dôsledku pretrvávajúcej hyperémie spojoviek. Na liečbu produktom UNILAT bolo zaradených 40 pacientov (31 žien a 9 mužov), z ktorých ani jeden nebol vyradený z klinického sledovania. V tejto skupine malo 25 pacientov diagnostikovaný PGOU, 15 vnútroočnú hypertenziu a 11 z nich muselo absolvovať vymývaciu fázu. Medzi pacientmi zo skupiny UNILAT a XALATAN neboli signifikantné rozdiely týkajúce sa veku, anamnézy, zdravotného stavu, respektíve bazálnych hodnôt VOT nameraných na začiatku klinického sledovania.
Po ukončení klinického sledovania nasledovala štatistická analýza získaných dát, pričom v obidvoch skupinách, boli vypočítané základné štatistické charakteristiky (tab. 1).
Table 1. Prehľad priemerných hodnôt VOT a štatistických charakteristík vypočítaných pre sledované súbory 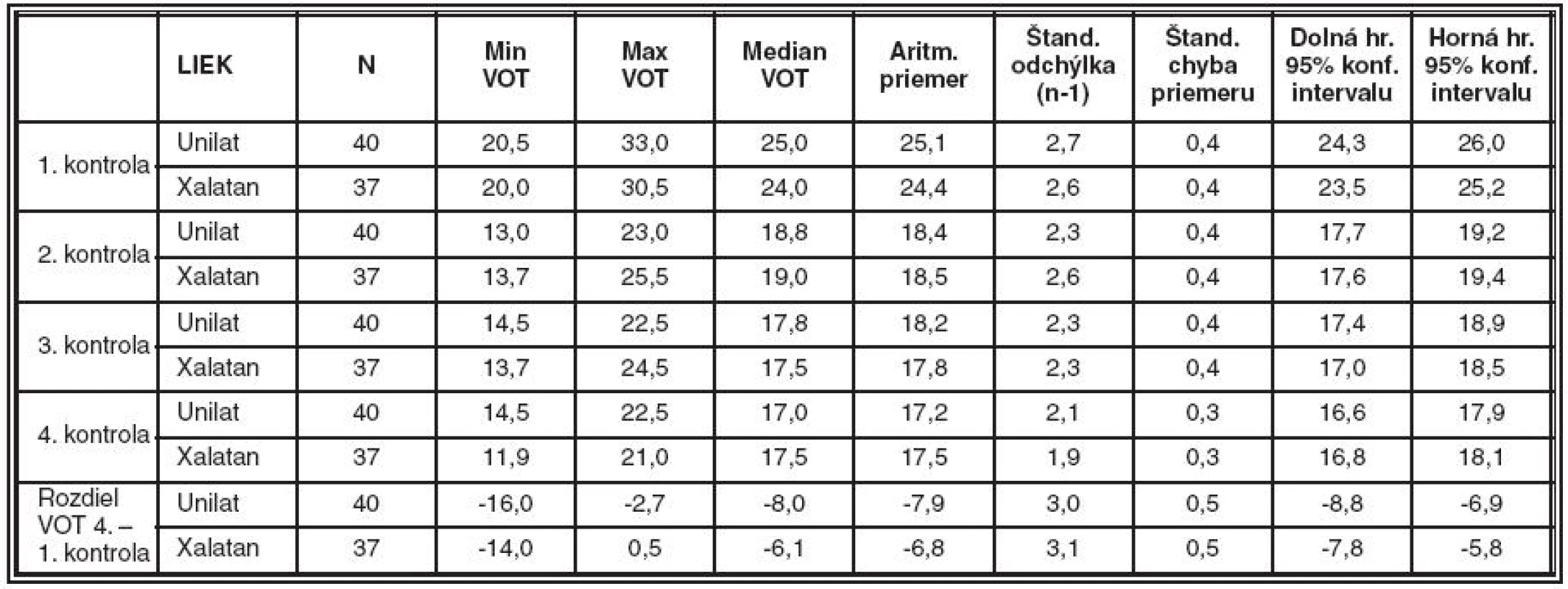
Hodnotenie účinnosti generika UNILAT bolo založené na testovaní non-inferiority podľa smerníc Európskej liekovej agentúry EMA [2, 5], ktorého cieľom je dokázať, že testovaný produkt nie je horší ako originálny o viac ako vopred stanovená hranica (non-inferiority margin Δ). Testovanie non-inferiority teda vychádzalo z výpočtu obojstranného 95% konfidenčného intervalu stredných hodnôt rozdielov VOT v sledovaných súboroch a porovnania jeho hornej hranice s hranicou non-inferiority Δ, ktorá bola podľa štandardných predpisov stanovená na hodnotu 1,5 mmHg. Keďže horná hranica 95% konfidenčného intervalu ležala pod hranicou non-inferiority (Δ = 1,5 mmHg), možno konštatovať, že generikum UNILAT nie je horší ako originálny liek XALATAN (obr. 2).
Image 2. Testovanie non-inferiority: horná hranica 95% konfidenčného intervalu leží pod úrovňou non-inferiority Δ, teda generický produkt UNILAT nie je horší ako originálny produkt XALATAN 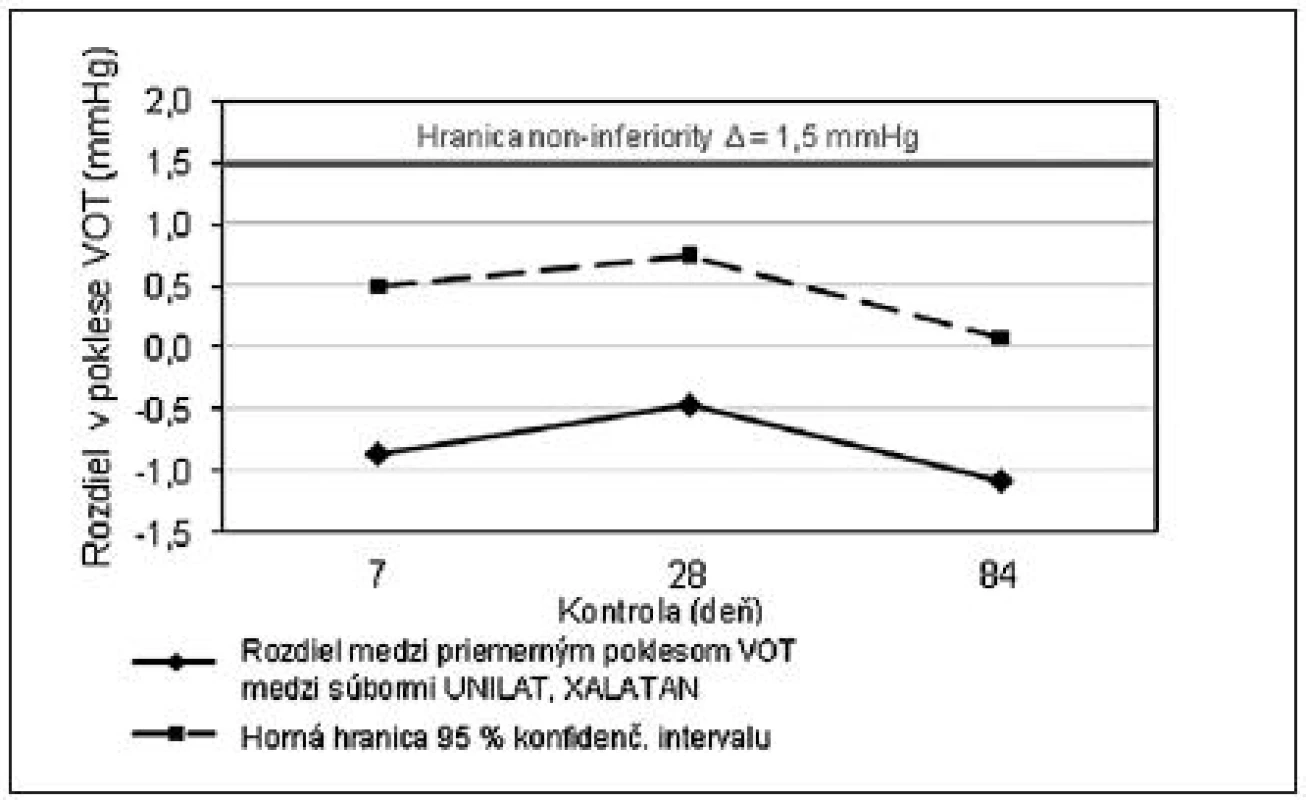
Primárnym sledovaným parametrom v obidvoch súboroch bol pokles VOT na konci sledovania minimálne o 5 jednotiek mmHg. V súbore XALATAN bol priemerný pokles VOT na konci sledovania o 6,8 mmHg a v súbore UNILAT o 7,9 mmHg, čo síce svedčí v prospech UNILATu, ale tento rozdiel nie je štatisticky významný.
Priemerné hodnoty VOT namerané v skupine UNILAT a XALATAN počas jednotlivých kontrol sú znázornené na obr. 3. Priebeh účinku aktívnej substancie latanoprost je u oboch produktov veľmi podobný, charakterizovaný jeho rýchlym nástupom v prvom týždni liečby a potom miernym poklesom VOT až do konca klinického sledovania.
Image 3. Priemerné hodnoty vnútroočného tlaku VOT namerané v sledovaných skupinách (UNILAT, XALATAN) počas jednotlivých kontrol 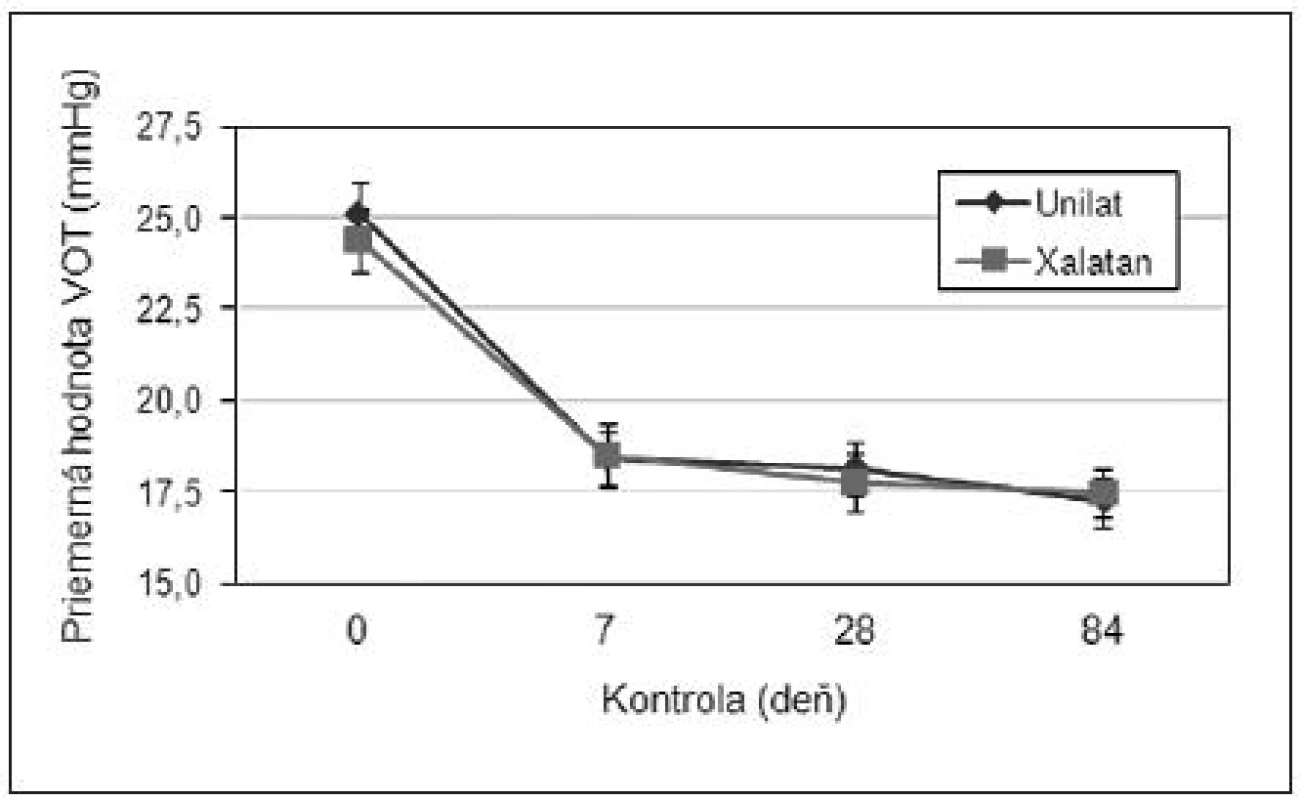
Vyhodnotenie sekundárneho parametra, pokles VOT na konci trojmesačného sledovania pod hodnotu 21mmHg, taktiež nepoukázal na signifikatné rozdiely medzi sledovanými skupinami. V skupine XALATAN bola u 88,9 % pacientov (32 z celkového počtu 36) nameraná hodnota VOT na konci sledovania pod hranicou 21 mmHg, pričom priemerná hodnota VOT na konci sledovania bola 18,1 mmHg. V skupine UNILAT to bolo 90,0 % pacientov (36 z celkového počtu 40) s hodnotou VOT < 21 mmHg na konci sledovania, pričom priemerná hodnota VOT pacientov počas poslednej kontroly bola 17,9 mmHg.
Hodnotenie bezpečnosti generika UNILAT bolo založené na sledovaní frekvencie výskytu nežiaducich účinkov. Najčastejšie hlásenými nežiaducimi účinkami zo skupiny veľmi časté boli: hyperémia, predĺženie a/alebo stmavnutie očných rias, svrbenie, podráždenie očí a pocit cudzieho telieska v oku. Žiadny z týchto nežiaducich účinkov nepovažovali ošetrujúci lekári za závažný a taktiež nebol zaznamenaný signifikantný rozdiel medzi sledovanými skupinami. Prehľad najčastejšie sa vyskytujúcich nežiaducich účinkov počas jednotlivých kontrolných návštev je uvedený v tab. 2.
Table 2. Frekvencia výskytu nežiaducich účinkov v sledovaných skupinách (UNILAT, XALATAN) počas jednotlivých kontrol 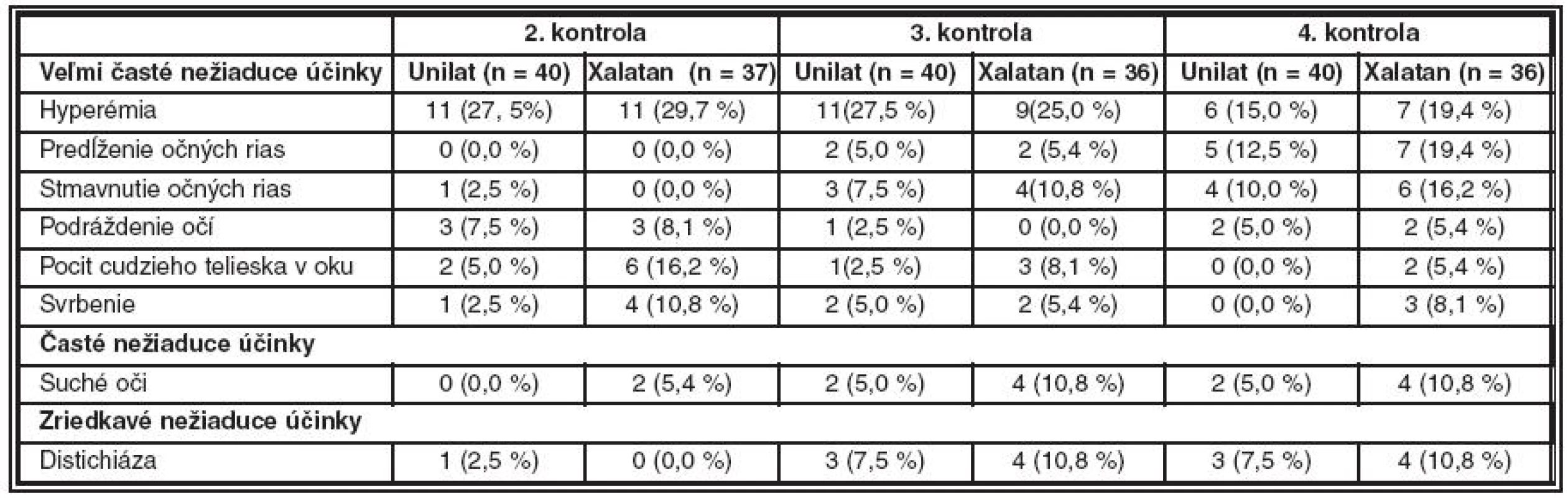
Diskusia
Nový generický produkt UNILAT od slovenskej spoločnosti UNIMED PHARMA, s r.o., sa vyznačuje rovnakým kvalitatívnym i kvantitatívnym obsahom účinnej látky (latanoprost 50 μg/ml) ako originálny liek XALATAN a zároveň aj rovnakým zastúpením pomocných látok (tab. 3).
Table 3. Chemické zloženie generického a originálneho produktu 
Na potvrdenie terapeutických indikácií, účinnosti a bezpečnosti generika UNILAT v liečbe glaukómu a vnútroočnej hypertenzie bola uskutočnená trojmesačná, multicentrická, porovnávacia (non-inferiority) štúdia, ktorej sa zúčastnilo 77 pacientov.
Výsledky klinickej štúdie preukázali, že generikum UNILAT je rovnako účinný a bezpečný ako originálny liek. Medzi sledovanými skupinami neboli pozorované signifikantné rozdiely vo výsledných hodnotách VOT (XALATAN: 18,1 mmHg; UNILAT: 17,9 mmHg), rovnako ako aj v priemernom poklese VOT na konci sledovania (XALATAN: 6,8 mmHg; UNILAT: 7,9 mmHg). Generikum UNILAT bolo pacientmi veľmi dobre tolerované a taktiež neboli preukázané signifikantné rozdiely vo výskyte nežiaducich účinkov medzi sledovanými súbormi.
Medzi najčastejšie hlásené nežiaduce účinky patrili: hyperémia, svrbenie, podráždenie očí, predĺženie a/alebo stmavnutie očných rias, pocit cudzieho telieska v oku, ktoré však ošetrujúci lekári v obidvoch skupinách nepovažovali za závažné.
Na základe týchto skutočností možno skonštatovať, že generikum UNILAT je účinným a bezpečným produktom zo skupiny prostaglandínov vhodným na liečbu glaukómu a vnútroočnej hypertenzie. Keďže liečba týchto ochorení si vo väčšine prípadov vyžaduje dlhodobú, resp. celoživotnú terapiu, generikum UNILAT sa javí ako vhodná voľba jednak z pohľadu nižšej ceny, ale predovšetkým nižším obsahom konzervačnej látky. UNILAT totiž obsahuje o 50 % menej konzervačnej látky ako originálny liek, resp. konkurenčné produkty zo skupiny prostaglandínov.
Záver
Generické liečivá sú dôležitou súčasťou farmaceutického trhu väčšiny vyspelých štátov, ktoré zároveň dbajú na garanciu ich kvality, účinnosti a bezpečnosti. Výhodou generických liekov je to, že obsahujú účinné látky, ktorými sú pacienti liečení už minimálne 10 rokov v podobe originálneho lieku, teda sú overené v praxi. Väčšina výrobcov generík po uplynutí 10ročnej patentovej ochrany originálu prináša na trh kópie s vylepšenými vlastnosťami. Neobsahujú napríklad niektoré pomocné látky, ktoré môžu u pacientov vyvolávať alergické reakcie či iné ťažkosti a podobne, ako je to i v prípade UNILATu, môžu obsahovať menej konzervačných látok. Účelom generík nie je nahradiť či vytlačiť originálne liečivá z farmaceutického trhu, ale spoluvytvárať lepšie konkurenčné prostredie, a tak vyvíjať tlak na nižšie ceny a vyššiu kvalitu liečiv.
PaedDr. Martina Tvrdoňová, PhD.,
UNIMED PHARMA, spol. s r.o. , Bratislava,
Oddelenie výskumu a vývoja,
tel.: +421 908 810 228,
email: tvrdonova@unimedpharma.sk
Sources
1. Alm A., Widengard I., Kjellgren D., et al.: Latanoprost administered once daily caused a maintained reduction of intraocular pressure in glaucoma patients treated concomitantly with timolol. BMC Ophthalmology, 1995, 79 : 12–16.
2. Guideline on the choice of the non-inferiority margin. London, 2005; EMEA/CPMP/EWP/2158/99.
3. http://www.zelenyzakal.sk/zeleny-zakal/glaukom/..
4. Perry C.M., McGavin J.K., Culy Ch.R. et al.: Latanoprost. An Update of its Use in Glaucoma Hypertension. Drugs & aging, 2003, 20 : 597–630.
5. Points to consider on switching between superiority and non-inferiority. London 2000; CPMP/EWP/482/99.
6. Resul B., Stjernschantz J., Kiyo N., et al.: Phenyl-Substituted Prostaglandins: Potent and selective antiglaucoma agents. J Med Chem, 1993, 36 : 243–248.
7. Stjernschantz J., Resul B.: Phenyl substituted prostaglandin analogs for glaucoma treatment. Drugs of the future, 1992, 17 : 691–704.
Labels
Ophthalmology
Article was published inCzech and Slovak Ophthalmology

2010 Issue 6-
All articles in this issue
- Rohovkové aberace vyššího řádu u zdravého oka a jejich změny s věkem
- Klinické sledovanie účinnosti a bezpečnosti generického produktu UNILAT v terapii glaukómu a vnútroočnej hypertenzie
- Hluboká perforující trabekulektomie – až šestileté výsledky
- Kompenzácia zrakového postihnutia u detí prostredníctvom optických pomôcok
- Corneal cross-linking – moderná metóda liečby keratokónusu
- Czech and Slovak Ophthalmology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Rohovkové aberace vyššího řádu u zdravého oka a jejich změny s věkem
- Corneal cross-linking – moderná metóda liečby keratokónusu
- Hluboká perforující trabekulektomie – až šestileté výsledky
- Kompenzácia zrakového postihnutia u detí prostredníctvom optických pomôcok
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

