-
Medical journals
- Career
Lucentis v liečbe vlhkej formy vekom podmienenej degenerácie makuly – dvojročné skúsenosti
Authors: M. Molnárová; V. Lešková; P. Demský; R. Vida; M. Izák
Authors‘ workplace: II. očná klinika SZU FNsP F. D. Roosevelta, Banská Bystrica, prednosta prof. MUDr. Milan Izák, CSc., FEBO
Published in: Čes. a slov. Oftal., 65, 2009, No. 5, p. 182-185
Overview
V súbore 114 pacientov (39 mužov, 75 žien) s priemerným vekom 72,5 rokov (od 52 do 89 rokov) s priemernou dobou sledovania 8 mesiacov sme v retrospektívnej štúdii sledovali efektívnosť a bezpečnosť liečby vlhkej formy vekom podmienenej degenerácie makuly (VPDM) intravitreálnou aplikáciou ranibizumab = Lucentis. Všetci pacienti splnili inklúzne kritériá. Liečba bola ambulantná, robená za prísne sterilných podmienok na operačnej sále ako každá iná vnútroočná operácia.
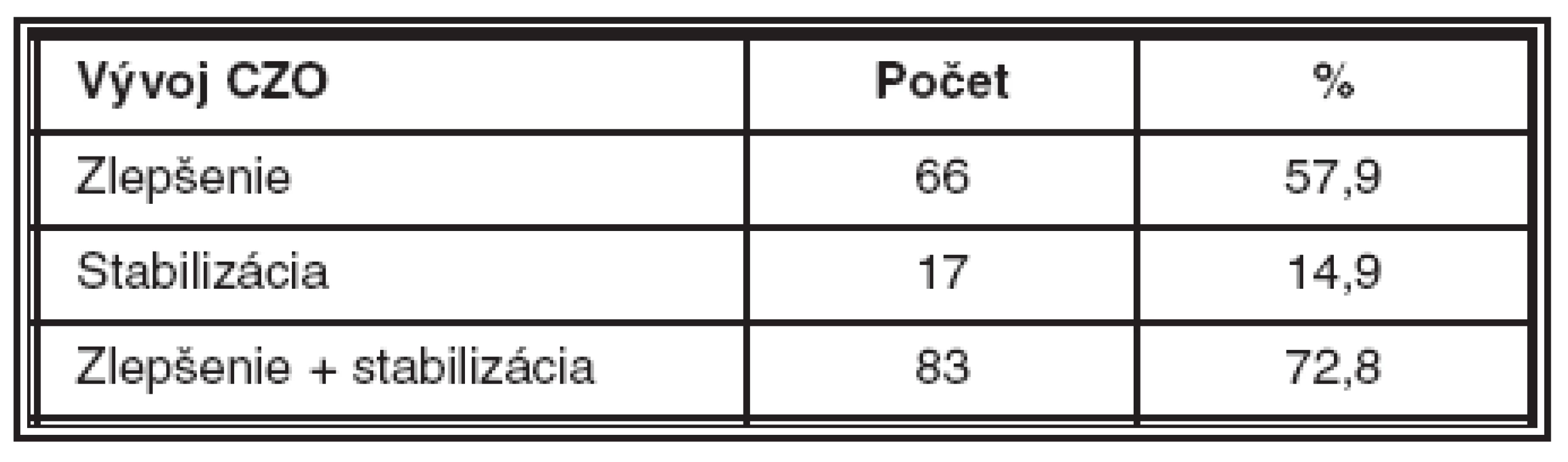
Zlepšenie centrálnej zrakovej ostrosti (CZO) sme za dobu sledovania dosiahli celkom u 66 pacientov (57,9 %), stabilizáciu CZO – pacienti nestratili, ale ani nezískali žiadne písmeno – sme našli u 17 pacientov (14,9 %). U 31 pacientov (27,2 %) došlo k zhoršeniu centrálnej zrakovej ostrosti. Peroperačné komplikácie sme nemali. Z pooperačných komplikácií sme našli 22-krát prechodné zvýšenie VOT, 21-krát sufúziu, 3-krát sme zaznamenali vývoj subretinálnej hemorágie, 1-krát vznikla ruptúra pigmentového epitelu sietnice (PES) a 1-krát sa pridružila predná ischemická optikopatia.Nami dosiahnuté výsledky sú v súlade so štúdiou PRONTO i PIER.
Kľúčové slová:
vlhká forma VPDM, intravitreálna liečba, antiVEGF – LucentisÚVOD
S narastajúcou priemernou dĺžkou života vo svete sa zvyšuje riziko vzniku vekom podmienenej degenerácie makuly (VPDM). Keďže katarakta, ktorá donedávna bola hlavnou príčinou praktickej slepoty, sa vo vyspelých krajinách sveta aktuálne rieši chirurgicky s implantáciou umelej vnútroočnej šošovky, nevedie toto ochorenie už ku vzniku praktickej slepoty. Z tohto dôvodu sa zhruba pred 30 rokmi na prvé miesto príčin praktickej slepoty dostala VPDM (7).
Vekom podmienená degenerácia makuly je multifaktoriálne progredujúce ochorenie, ktoré sa vyvinie pôsobením rizikových faktorov pri genetickej predispozícii pre toto závažné ochorenie. O VPDM sa hovorí ak je centrálna zraková ostrosť (CZO) 20/40 alebo horšia, v objektívnom náleze sú drúzy, subretinálna exsudácia, edém sietnice, krvácanie alebo disciformná jazva, ale tiež strata foveolárneho reflexu a dystrofia pigmentového epitelu sietnice (5).
Antirastové faktory (antiVEGF) predstavujú novú éru v liečbe vlhkej formy VPDM. Vo svete i na Slovensku sa na liečbu vlhkej formy VPDM intravitreálne používajú pegaptanib sodium (Macugen), ranibizumab (Lucentis) a off lebel bevacizumab (Avastin).
MATERIÁL A METODIKA
Prvú intravitreálnu aplikáciu Lucentisu v liečbe vlhkej formy VPDM sme na našej klinike urobili 22. 2. 2007. V retrospektívnej štúdii hodnotíme 114 pacientov so všetkými podtypmi subretinálnej neovaskulárnej membrány (SRNM) pri VPDM liečených intravitreálnou aplikáciou Lucentisu. Priemerný vek sledovaného súboru je 72,5 rokov (od 53 rokov a do 89 rokov). Doba sledovania je od 2 do 24 mesiacov, priemerná doba sledovania je 8 mesiacov.
Table 1. Chrakateristika súboru 
R – roky, M – mesiace Table 2. Typ subretinálnej neovaskulárnej membrány 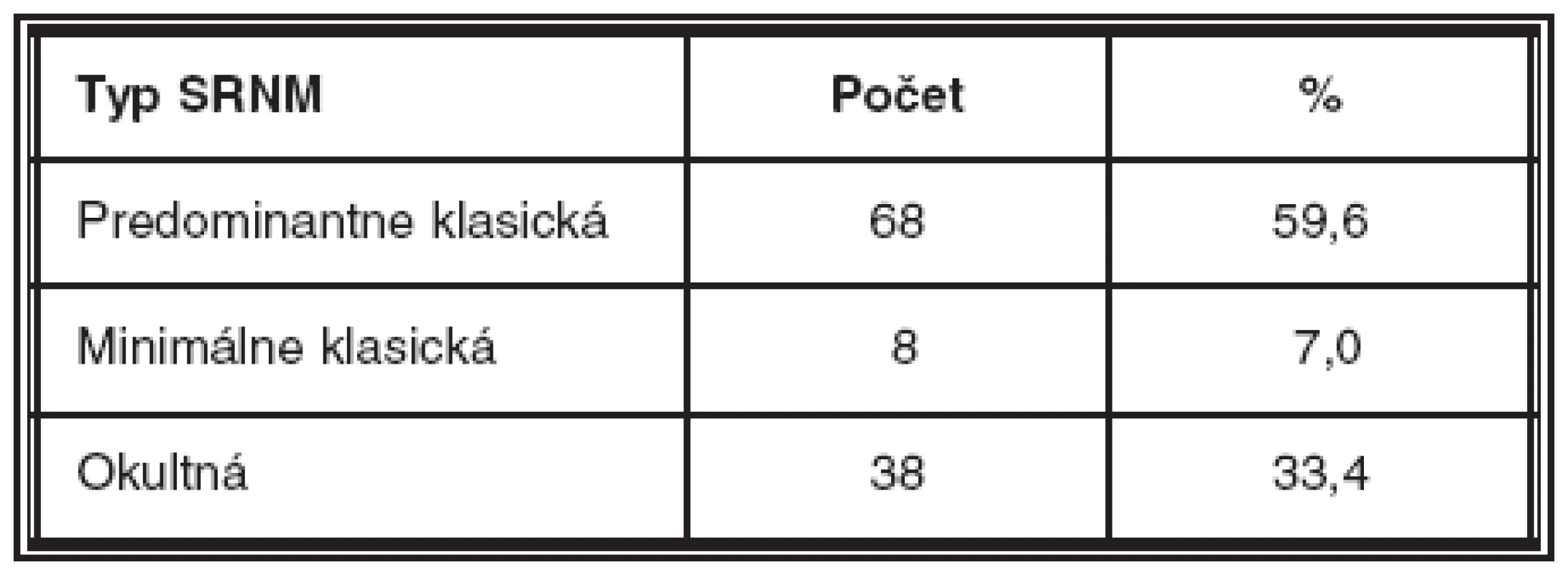
SRNM – subretinálna neovaskulárna membrána U 68 pacientov (59,6 % súboru) sa jednalo o predominantne klasickú subretinálnu neovaskulárnu membránu, u 8 pacientov (7,0 % ) o minimálne klasickú a u 38 pacientov (33,4 %) o okultnú subretinálnu neovaskulárnu membránu pri VPDM dokázanú pomocou. FAG na Heidelbergskom angiografe
Všetci pacienti, u ktorých bola indikovaná liečba vlhkej formy VPDM, splnili inklúzne kritéria: centrálna zraková ostrosť od 20/40 do 20/320, veľkosť lézie maximálne 12 papilárnych diametrov, prítomnosť subretinálnej hemorágie menej ako 50% plochy lézie, prítomnosť subretinálneho fibrózneho tkaniva menej ako 25 % plochy lézie, vek nad 50 rokov, všetky angiografické typy membrán.
Intravitreálna aplikácia Lucentisu bola uskutočňovaná na operačnej sále za sterilných podmienok v topickej anestéze s Benoxi gtt. 3 až 3,5 mm od limbu sme aplikovali 0,5 mg = 50 μl ranibizumabu intravitreálne. Pred a po aplikácii sme sterilne merali vnútroočný tlak.
Do spojovkového vaku boli aplikované 3 dni pred aplikáciou a 5 dní po aplikácii lokálne ATB kvapky Tobrex gtt, Azidamphenicol gtt, Uniflox gtt alebo Gentamycin gtt 5 x denne. U všetkých pacientov sme pred každou aplikáciou, prvý deň po aplikácii a l mesiac po aplikácii vyšetrovali najlepšie korigovanú centrálnu zrakovú ostrosť, vnútroočný tlak bezkontaktnou metódou, biomikroskopiu predného segmentu oka, stereoskopické vyšetrenie fundu Volkovou šošovkou 78 D.
Pred aplikáciou, l mesiac po prvých troch aplikáciách a potom po každej ďalšej aplikácii sme robili FAG a vyšetrenie OCT. Najlepšie korigovanú centrálnu zrakovú ostrosť sme vyšetrovali na ETDRS optotype, VOT sme merali na bezkontaktnom tonometri Canon. FAG sme robili na Heidelbergskom angiografe a na meranie hrúbky sietnice a veľkosti lézie sme používali OCT 3 STRATUS.
Liečbu sme vykonávali podľa štúdie PIER, teda prvé 3 aplikácie boli aplikované 1-krát za 4 týždne a potom 5., 8. a 11. mesiac od začiatku liečby.
Za dobu sledovania sme urobili 476 aplikácií Lucentisu. Tabuľka 3 ukazuje počet pacientov zaradených do retrospektívnej štúdie s počtom aplikácií viac ako 3.
Table 3. Charakteristika súboru podľa počtu aplikácií 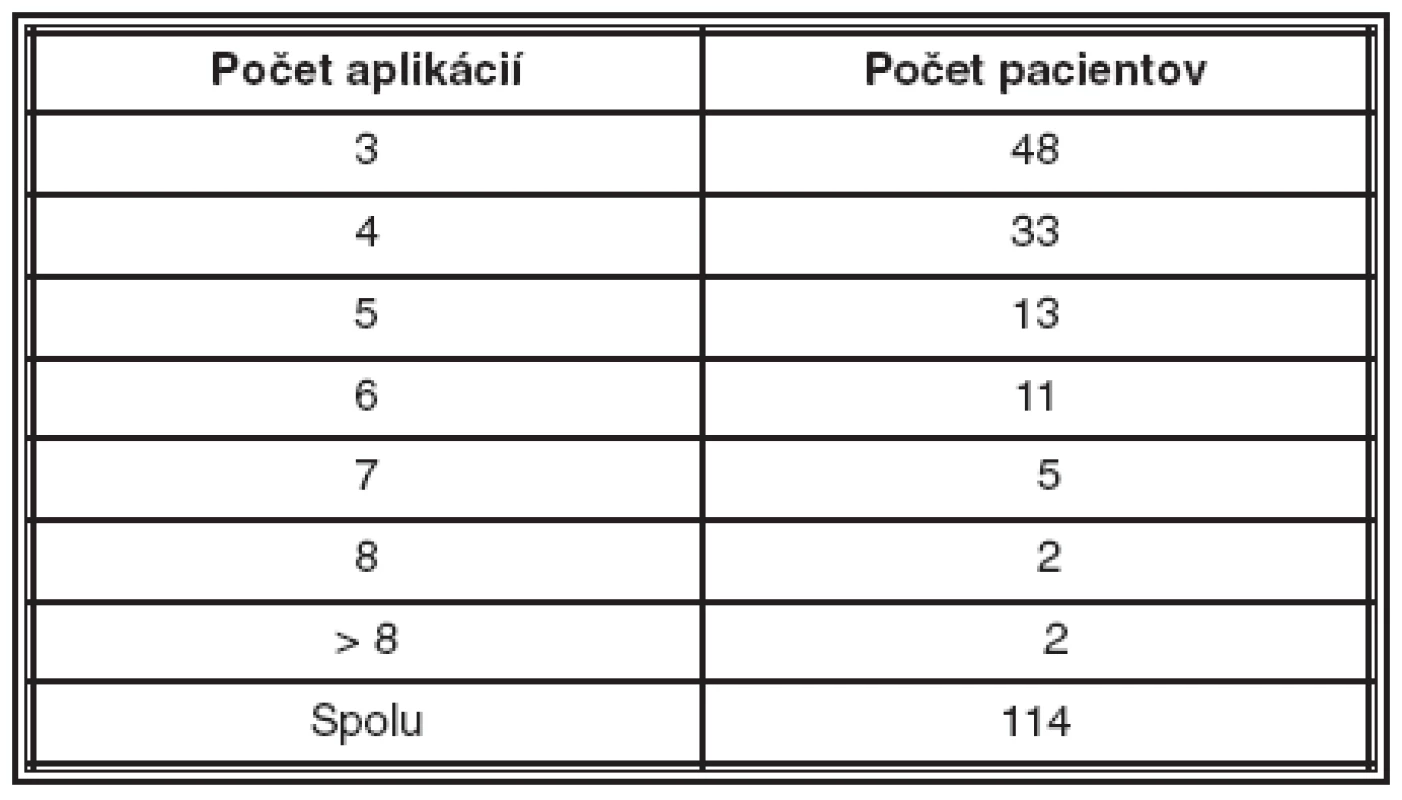
VÝSLEDKY
Retrospektívne sme sledovali efektívnosť a bezpečnosť intravitreálnej liečby vlhkej formy VPDM antiVEGF Lucentisom. V rámci efektívnosti liečby sme sledovali vývoj centrálnej zrakovej ostrosti (CZO) na ETDRS optotype. Hodnotili sme počet písmen, ktoré pacient liečbou získal, alebo stratil. Vývoj hrúbky sietnice sme sledovali pomocou OCT 3 a hodnotili sme zmenu hrúbky sietnice v mikrometroch (μm).
Table 7. Pooperačné komplikácie 
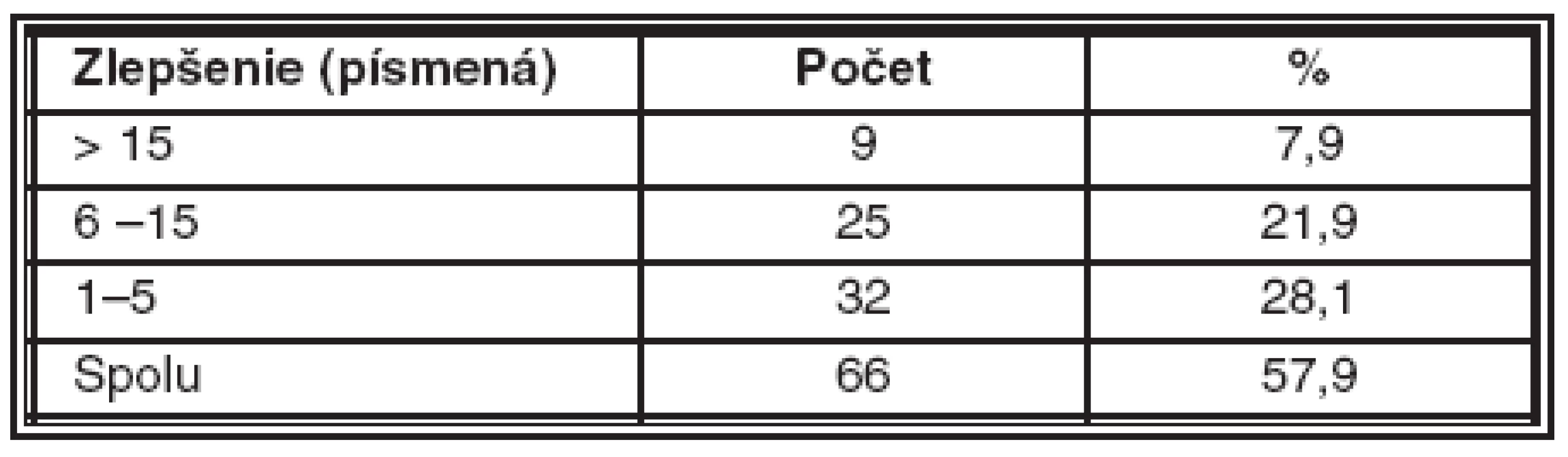
VOT – vnútroočný tlak AION – anterior ischemic opticopathy V sledovanom súbore sme zlepšenie CZO za dobu sledovania dosiahli celkom u 66 pacientov (57,9 %) a to zlepšenie od 1 do 5 písmen ETDRS optotypu u 32 pacientov (28,1 %), od 6 do 15 písmen u 25 pacientov (21,9 %) a o viac ako 15 písmen u 9 pacientov (7,9 %).
Stabilizáciu CZO – pacienti nestratili ale ani nezískali žiadne písmeno – sme našli u 17 pacientov(14,9 %). Zlepšenie a stabilizáciu CZO a nálezu sme za dobu sledovania dosiahli u 83 pacientov (72,8 %).
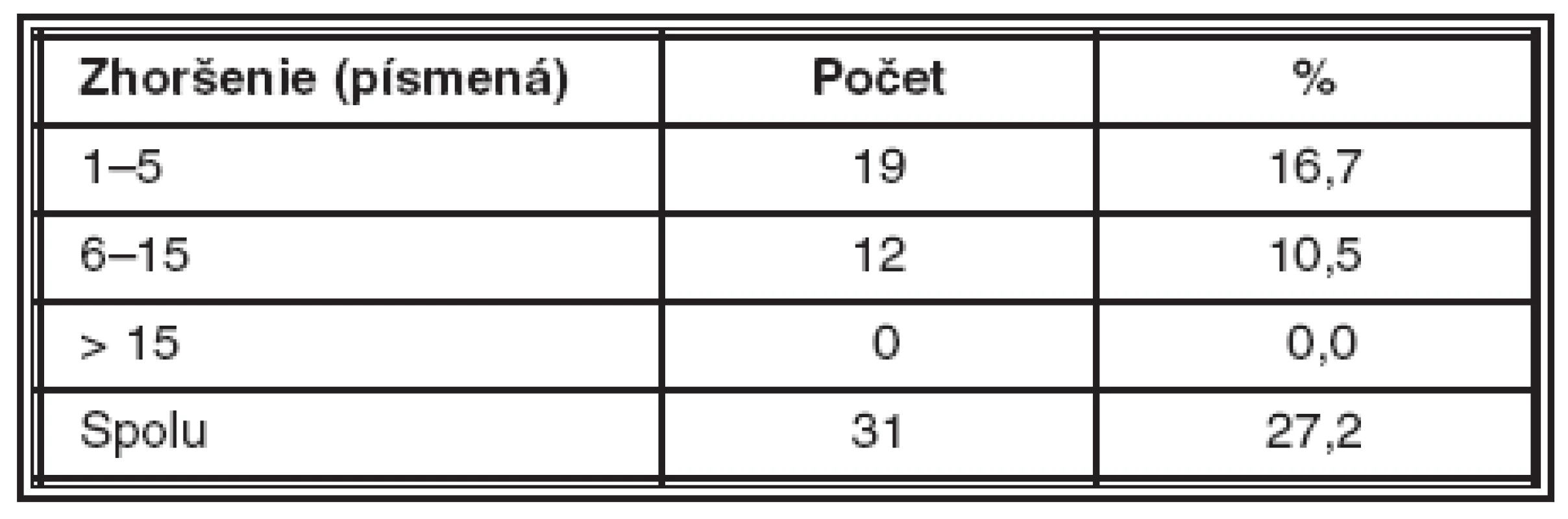
U 31 pacientov za dobu sledovania došlo k zhoršeniu CZO, a to u 19 pacientov (16,7%) o 1 až 5 písmen ETDRS optopypu, u 12 pacientov (10,5 %) o 6 až 15 písmen. Ani u jedného pacienta sme nepozorovali výrazné zhoršenie CZO o viac ako 15 písmen.
Peroperačné komplikácie sme nemali.
Z pooperačných komplikácií sme našli prechodné zvýšenie VOT 22-krát, sufúziu 21-krát, 3-krát vznikla sub - alebo intraretinálna hemorágia, 1-krát ruptúra PES a 1-krát sme konštatovali koincidenciu s prednou ischemickou optikopatiou, 7 pacientov nereagovalo na liečbu a nález pomaly progredoval napriek aplikovanej liečbe.
V súbore sme ďalej sledovali vývoj hrúbky sietnice počas liečby Lucentisom. Zistili sme, že so ziskom počtu písmen (graf 2) sa znižovala hrúbka sietnice (graf 3).
Graph 2. Vývoj centrálnej zrakovej ostrosti 
Graph 3. Vývoj hrúbky sietnice 
V sledovanom súbore pacientov s vlhkou formou VPDM liečených intravitreálnou aplikáciou Lucentisu sme za dobu sledovania konštatovali benefit liečby a to priemerný zisk 4,5 písmen a redukciu hrúbky sietnice priemerne o 95 μm.
DISKUSIA
Molekula VEGF ( vascular endotel growth factor ) je homodimerický glykoproteín prirodzene sa nachádzajúci v sietnici, ktorý udržuje zdravú vaskulatúru. Známe sú VEGF A, VEGF B, VEGF C, VEGF D a PlGF. Kľúčovú rolu v patogenéze vlhkej formy VPDM a zvýšenej permeabilite ciev hrá hlavne VEGF A (2, 3). VEGF sú vylučované rôznymi bunkami sietnice ako odpoveď na hypoxiu. U pacientov s vlhkou formou VPDM bola dokázaná zvýšená hladina VEGF A v sklovci.
Molekula VEGF A je polypeptid. Syntézu všetkých izoforiem VEGF A riadi gén VEGF. Základnými izoformami sú izoformy 121, 145, 165, 183, 189, 206. Za patologickú neoangiogenézu v oku je zodpovedná izoforma 165 (6), kým fyziologickú angiogenézu zaisťuje hlavne izoforma 121. Za fyziologických podmienok je VEGF hlavným faktorom, ktorý zaisťuje a umožňuje reprodukciu ciev choriokapilaris a udržuje prietok krvi, zodpovedá za udržanie fenestrácií endotelu ciev choriokapilaris a má tiež neuroprotektívny efekt (1). Za patologických okolností VEGF vedie k rozvoju patologickej neovaskularizácie v oku, vedie k zvýšeniu permeability ciev a indukuje zápalové mediátory (8).
Antirastové faktory predstavujú novú éru v liečbe vlhkej formy VPDM.
Ranibizumab = Lucentis je v súčasnosti najúčinnejší antirastový faktor, ktorý sa používa v liečbe vlhkej formy VPDM. V Európe bol registrovaný 24. 1. 2007. Na Slovensku bol ranibizumab kategorizovaný 1. 7. 2007. Na našej klinike sme na základe mimoriadneho dovozu s liečbou vlhkej formy VPDM intravitreálnou aplikáciou ranibizumabu začali 22. 2. 2007.
Ranibizumab (Lucentis) je humanizovaný fragment monoklonálnej protilátky proti VEGF vytvorený v bunkách Escherichia coli rekombinantnou DNK technológiou. Bol vyvinutý ako malá molekula o molekulovej hmotnosti 48 kD, čo jej umožňuje rýchly prechod sietnicou, rýchlu systémovú elimináciu a zníženú antigénnu aktivitu. Avastin má v porovnaní s Lucentisom veľkú molekulu o molekulovej hmotnosti 150 kD, neznámy mechanizmus prechodu cez sietnicu a má pomalšiu systémovú elimináciu (4).
Efektívnosť a bezpečnosť liečby bola sledovaná v 3 randomizovaných dvojite zaslepených klinických štúdiách. V štúdii MARINA boli liečení pacienti s minimálne klasickou alebo okultnou subretinálnou neovaskulárnou membránou (CNV) intravitreálnou aplikáciou 0,3mg a 0,5mg ranibizumabu a placebom. V štúdii ANCHOR boli zaradení pacienti s predominantne klasickou CNV. V obidvoch štúdiách u 95 % pacientov došlo k strate menej ako 15 písmen ETDRS optotypu a dokonca u 34 až 40 % pacientov liečených s ranibizumabom došlo ku klinicky signifikantnému zlepšeniu CZO. (1,9). Štúdia PIER sledovala účinnosť ranibizumabu v alternatívnom dávkovaní. Do tejto štúdie boli zaradení pacienti so všetkými typmi CNV. Pacienti boli liečení s 0,3 a 0,5 mg ranibizumabu a placebom a to prvé 3 aplikácie mesačne a potom 3 aplikácie každé 3 mesiace. 90 % pacientov v štúdii PIER si počas 12 mesiacov zachovala CZO.
ZÁVER
V súlade so závermi štúdií MARINA a ANCHOR sme v našom súbore pacientov s vlhkou formou VPDM liečených počas doby sledovania ITV aplikáciou Lucentisu dosiahli výborné výsledky. Ani v jednom prípade nedošlo k výraznej strate CZP o viac ako 15 písmen ETDRS optotypu, čím sme splnili cieľ liečby – stabilizovať centrálnu zrakovú ostrosť ukľudnením a uzavretím presakujúcich subfoveálnych chorioidálnych neovaskularizácií.
Do redakce doručeno dne 12. 3. 2009
Do tisku přijato dne: 1. 9. 2009
MUDr. Mária Molnárová
II. Očná klinika SZU
FNsP F. D. Roosevelta
Nám. L. Svobodu 1
975 17 Banská Bystrica
Slovenská republika
e-mail: m.molnarova@nspbb.sk
Sources
1. Brown, D.M., Kaiser, P.K., Michelsm, M. et al.: Ranibizumab versus verteporfin for neovascular age-related macular degeneration. N. Engl. J. Med., 355, 2006; 1432–1444.
2. Ferrara, N., Gerber, H.P., Le Couter, J.: The biology of endothelial growth factor and its receptors. Nat. Med., 9, 2003; 669–676.
3. Ferrara, N.: Vascular endothelial growth factor: basic science and clinical progress. Endocrine Rev., 25, 2004; 581–611.
4. Ferrara, N., D’Amico, L., Shams, N. et al.: Development of ranibizumab, an anti-vascular endothelial growth factor antigen binding fragment, as therapy for neovascular age-related macular degeneration. Retina, 26, 2006; 859–870.
5. Goldberg, J., Flowerdew, G., Smith, E. et al.: Factors associated with age-related macular degeneration. An analysis of data from the first National and Health and Nutritional Examination Survey. Am. J. Epidemiol., 128, 1988; 700–710.
6. Ishida, S., Usui, T., Yamashiro, K. et al.: VEGF 164-mediated inflammation is required for pathological, but not physiological, ischemia - reduced retinal neovasculariosation. J. Exp. Med., 198, 2003; 483–489.
7. Kolař, P. a kolektív.: Věkem podměnená makulární degenerace. Grada Publishing, 2008; 148.
8. Matsuoka, M., Ogata, N., Otsui, T., et al.: Expression of pigment epithelium derived factor and endothelial growth factor in choroidal neovascular membranes and polypoidal choroidal vasculopathy. Br. J. Ophthalmol., 88, 2004; 809–815.
9. Rosenfeld, P.J., Brown, D.M., Heier, J.S., et al.: Ranibizumab for neovascular age-related macular degeneration. N. Engl. J. Med., 355, 2006; 1419–1431.
10. Shima, D.T., Nishijama, K., Jo, N., et al.: VEGF mediated neuroprotection in ischemic retina. Invest. Ophthalmol Vis. Sci., 45, 2004; E-abstract, 3270.
Labels
Ophthalmology
Article was published inCzech and Slovak Ophthalmology

2009 Issue 5-
All articles in this issue
- Diagnostika akantamébovej keratitídy
- Současné přístupy k léčbě neinfekčních uveitid
- Kontrastní citlivost a aberace vyšších řádů po konvenčním LASIKu
- Změny aberací vyšších řádů a kontrastní citlivosti po standardní fotorefrakční keratektomii
- Lucentis v liečbe vlhkej formy vekom podmienenej degenerácie makuly – dvojročné skúsenosti
- Kombinované cievne oklúzie sietnice
- Porovnání prahové interpolační a celořádkové metody při testování zrakové ostrosti na optotypových tabulích logMÚR ETDRS a Snellen
- Benefit chirurgické léčby idiopatické intrakraniální hypertenze – kazuistické sdělení
- Czech and Slovak Ophthalmology
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Diagnostika akantamébovej keratitídy
- Současné přístupy k léčbě neinfekčních uveitid
- Benefit chirurgické léčby idiopatické intrakraniální hypertenze – kazuistické sdělení
- Kontrastní citlivost a aberace vyšších řádů po konvenčním LASIKu
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career